ZusammensetzungWirkstoffe
Pomalidomidum.
Hilfsstoffe
Mannitol, vorverkleisterte Stärke, Natriumstearylfumarat.
Kapselhülle: Gelatine, Titandioxid, gelbes Eisenoxid (nur bei Hartkapseln 1 mg, 2 mg und 3 mg), Indigocarmin, Erythrosin (nur bei Hartkapseln 2 mg), Brillantblau FCF (nur bei Hartkapseln 4 mg).
Drucktinte: Shellack, schwarzes Eisenoxid, Titandioxid, Simeticon, Propylenglycol, Ammoniak-Lösung.
Eine Hartkapsel enthält max. 0,018 mg (Hartkapseln 1 mg) bzw. max. 0,036 mg (Hartkapseln 2 mg) bzw. max. 0,025 mg (Hartkapseln 3 mg) bzw. max. 0,033 (Hartkapseln 4 mg) Natrium.
Darreichungsform und Wirkstoffmenge pro EinheitHartkapseln zu 1 mg, 2 mg, 3 mg und 4 mg.
Indikationen/AnwendungsmöglichkeitenImnovid in Kombination mit Bortezomib und Dexamethason ist indiziert zur Behandlung von erwachsenen Patienten mit multiplem Myelom (MM), welche mindestens eine vorgängige Therapie, inklusive Lenalidomid, erhielten.
Imnovid in Kombination mit Dexamethason ist indiziert zur Behandlung von rezidiviertem und refraktärem multiplem Myelom bei Patienten, welche mindestens zwei vorgängige Therapien erhielten (inklusive Lenalidomid und Bortezomib) und welche eine Progredienz zur letzten Therapie gezeigt haben.
Dosierung/AnwendungDie Behandlung muss von einem erfahrenen Hämatologen oder Onkologen begonnen und überwacht werden.
Imnovid in Kombination mit Bortezomib und Dexamethason (PVd) bei Patienten mit multiplem Myelom, welche mindestens eine vorgängige Therapie erhalten haben
Die empfohlene Anfangsdosis von Imnovid beträgt 4 mg einmal täglich oral an den Tagen 1-14 der sich wiederholenden 21-tägigen Behandlungszyklen.
Die empfohlene Dosis von Bortezomib beträgt 1,3 mg/m2 und die empfohlene Dosis von Dexamethason beträgt 20 mg/Tag oral einmal täglich, wobei die Anwendung entsprechend dem in Tabelle 1 gezeigten Dosierungsschema erfolgt.
Die Dosierung wird auf der Basis von klinischen Befunden und Laborbefunden fortgesetzt oder modifiziert. Die Behandlung soll bei Fortschreiten der Erkrankung abgebrochen werden.
Tabelle 1: Empfohlenes Dosierungsschema für Imnovid in Kombination mit Bortezomib und Dexamethason

* Für Patienten >75 Jahre siehe Abschnitt "Spezielle Dosierungsanweisungen" .
Imnovid in Kombination mit Dexamethason (Pd) bei Patienten mit rezidiviertem und refraktärem multiplem Myelom, welche mindestens zwei vorgängige Therapien erhalten haben
Die empfohlene Anfangsdosis von Imnovid beträgt 4 mg einmal täglich oral an den Tagen 1-21 der sich wiederholenden 28-tägigen Behandlungszyklen bis zur Progredienz. Die empfohlene Dosis Dexamethason beträgt 40 mg einmal täglich oral an den Tagen 1, 8, 15 und 22 eines jeden 28-Tage-Behandlungszyklus.
Die Dosierung wird auf der Basis von klinischen Befunden und Laborbefunden fortgesetzt oder modifiziert.
Das Dosierungsschema ist in Tabelle 2 gezeigt.
Tabelle 2: Empfohlenes Dosierungsschema für Imnovid in Kombination mit Dexamethason
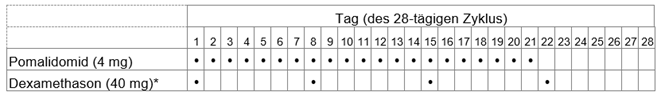
* Für Patienten >75 Jahre siehe Abschnitt "Spezielle Dosierungsanweisungen" .
Dosisanpassung oder -unterbrechung
Hämatotoxizität
Bei einer Thrombozytopenie mit Abfall der Werte auf <25 x 109/l oder bei einer Neutropenie mit Abfall der Werte auf <0,5 x 109/l oder bei einer febrilen Neutropenie (Fieber ≥38,5 °C und ANZ <1,0 x 109/l) sollte die Behandlung mit Pomalidomid unterbrochen werden, gefolgt von wöchentlichen Kontrollen des vollständigen Blutbildes (und im Fall des Absinkens der Neutrophilenzahl zusätzlich G-CSF im Ermessen des behandelnden Arztes). Nach Normalisierung der Thrombozyten/Neutrophilenzahlen sollte die Behandlung mit Pomalidomid in einer Dosierung von 3 mg täglich fortgeführt werden. Bei jedem nachfolgenden Abfall (<25 x 109/l respektive <0,5 × 109/l) sollte die Behandlung mit Pomalidomid unterbrochen werden. Nach Normalisierung der Thrombozyten/Neutrophilenzahlen sollte die Behandlung mit Pomalidomid in einer gegenüber der letzten Dosis um 1 mg reduzierten Dosierung fortgeführt werden.
Imnovid in Kombination mit Bortezomib und Dexamethason (PVd): Um einen neuen Pomalidomid-Zyklus beginnen zu können, muss die Neutrophilenzahl ≥1 × 109/l und die Thrombozytenzahl ≥50 × 109/l sein.
Imnovid in Kombination mit Dexamethason (Pd): Um einen neuen Pomalidomid-Zyklus beginnen zu können, muss die Neutrophilenzahl ≥0,5 × 109/l und die Thrombozytenzahl ≥50 × 109/l sein.
Weitere Toxizitäten 3./4. Grades
Bei anderen Grad 3/4 Toxizitäten, bei denen ein Zusammenhang mit Pomalidomid angenommen wird, ist die Behandlung abzusetzen und nach ärztlichem Ermessen in einer gegenüber der letzten Dosis um 1 mg reduzierten Dosierung wiederaufzunehmen, wenn sich die Toxizität auf ≤ Grad 2 zurückgebildet hat. Wenn die jeweiligen Toxizitäten auch nach Dosisreduktion auf 1 mg auftreten, muss das Arzneimittel abgesetzt werden.
Für Dosisanpassungen aufgrund der Toxizität von Bortezomib wird auf die entsprechende Arzneimittel-Fachinformation verwiesen.
Dosisanpassung bei gleichzeitiger Gabe von CYP1A2-Hemmern
Vermeiden Sie die gleichzeitige Anwendung von Pomalidomid mit starken CYP1A2-Hemmern. Ziehen Sie alternative Behandlungsmethoden in Betracht. Wenn starke CYP1A2-Hemmer (z.B. Ciprofloxacin und Fluvoxamin) gleichzeitig mit Pomalidomid verabreicht werden, muss die Pomalidomid-Dosis um 50% reduziert werden.
Absetzen von Pomalidomid
Bei einem Grad-2- oder Grad-3-Hautausschlag sollte eine Unterbrechung oder das Absetzen der Behandlung mit Pomalidomid erwogen werden.
Bei Angioödem, Anaphylaxie, Grad-4-Hautausschlag, exfoliativem oder bullösem Hautausschlag oder bei Verdacht auf Stevens-Johnson-Syndrom (SJS), toxischer epidermaler Nekrolyse (TEN) oder Arzneimittelexanthem mit Eosinophilie und systemischen Symptomen (DRESS) muss Pomalidomid abgesetzt werden. Wurde die Behandlung wegen derartiger Reaktionen beendet, sollte sie nicht mehr aufgenommen werden.
Spezielle Dosierungsanweisungen
Patienten mit Leberfunktionsstörungen
Für Patienten mit leicht, bis mässig eingeschränkter Leberfunktion (Child-Pugh-Klassen A oder B) beträgt die empfohlene Anfangsdosis 3 mg täglich (Dosisreduktion um 25%). Für Patienten mit stark eingeschränkter Leberfunktion (Child-Pugh Klasse C) beträgt die empfohlene Dosis 2 mg (Dosisreduktion um 50%).
Patienten mit Nierenfunktionsstörungen
Bei Patienten mit mässiger Niereninsuffizienz und Patienten mit schwerer Niereninsuffizienz, die nicht dialysepflichtig sind, ist keine Dosisanpassung von Pomalidomid erforderlich. Bei dialysepflichtigen Patienten mit schwerer Niereninsuffizienz beträgt die empfohlene Anfangsdosis 3 mg täglich (Dosisreduktion um 25%). An Hämodialysetagen sollte Pomalidomid nach der Hämodialyse eingenommen werden.
Ältere Patienten
Für Pomalidomid ist keine Dosierungsanpassung erforderlich.
Imnovid in Kombination mit Bortezomib und Dexamethason (PVd) nach mindestens einer vorgängigen Therapie:
Bei Patienten >75 Jahre beträgt die Dexamethason-Dosis 10 mg einmal täglich an den Tagen 1, 2, 4, 5, 8, 9, 11 und 12 eines 21-tägigen Zyklus für die Zyklen 1-8, und von Zyklus 9 an 10 mg einmal täglich an den Tagen 1, 2, 8 und 9 eines 21-tägigen Zyklus.
Imnovid in Kombination mit Dexamethason (Pd) nach mindestens 2 vorgängigen Therapien:
Bei Patienten >75 Jahre beträgt die Anfangsdosis von Dexamethason 20 mg einmal täglich an den Tagen 1, 8, 15 und 22 eines jeden 28-Tage-Zyklus.
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit bei Kindern und Jugendlichen ist nicht erwiesen.
Art der Anwendung
Imnovid sollte jeden Tag etwa zur gleichen Tageszeit oral eingenommen werden. Die Kapseln sollen nicht geöffnet, zerbrochen oder zerkaut werden. Die Imnovid-Kapseln sollen unabhängig von einer Mahlzeit vorzugsweise mit etwas Wasser unzerkaut eingenommen werden. Wenn der Patient die Einnahme von Imnovid an einem Tag vergessen hat, sollte er die nächste Kapsel zur gewohnten Zeit am nächsten Tag einnehmen. Patienten sollen die Zahl der eingenommenen Kapseln nicht erhöhen, um die vergessene Dosis Imnovid vom Vortag nachzuholen.
Zur Anwendung anderer Arzneimittel in Kombination mit Pomalidomid wird auf die entsprechende Fachinformation für das jeweilige Arzneimittel verwiesen.
KontraindikationenÜberempfindlichkeit gegenüber Pomalidomid oder einem der Hilfsstoffe oder Thalidomid und Lenalidomid.
Schwangerschaft.
Gebärfähige Frauen, ausser wenn alle Bedingungen des Schwangerschaftsverhütungsprogramms erfüllt sind.
Zur Anwendung anderer Arzneimittel in Kombination mit Pomalidomid wird auf die entsprechende Fachinformation für das jeweilige Arzneimittel verwiesen.
Warnhinweise und VorsichtsmassnahmenPomalidomid ist ein Thalidomidanalog. Thalidomid hat bekanntlich reproduktionstoxische Wirkungen beim Menschen, die zu schweren lebensbedrohlichen Geburtsfehlern führen. Pomalidomid hat sich sowohl bei Ratten als auch bei Kaninchen als reproduktionstoxisch erwiesen, wenn es in der Phase gegeben wird, in der die wichtigen Organe angelegt werden (siehe "Präklinische Daten" ). Wird Pomalidomid während der Schwangerschaft eingenommen, ist auch beim Menschen mit einer reproduktionstoxischen Wirkung zu rechnen.
Schwangerschaftsverhütungsprogramm
Programm bei Patientinnen
Die Bedingungen des Schwangerschaftsverhütungsprogramms müssen bei allen Patientinnen erfüllt sein, ausser wenn die Patientin erwiesenermassen nicht schwanger werden kann.
Kriterien zur Abklärung des Schwangerschaftspotentials
Eine Patientin oder Partnerin eines männlichen Patienten wird als gebärfähig klassifiziert, ausser sie erfüllt mindestens eine der folgenden Bedingungen:
-Alter ≥50 Jahre und spontan amenorrhoisch während ≥1 Jahr*
-Bestätigtes vorzeitiges Ovarialversagen
-Vorhergehende beidseitige Salpingo-Oophorektomie, Tubensterilisation oder Hysterektomie
-XY-Genotyp, Turner Syndrom, Uterus-Aplasie
* Eine Amenorrhoe nach Krebstherapie schliesst Gebärfähigkeit nicht aus.
Beratung
Bei gebärfähigen Frauen ist Pomalidomid kontraindiziert, wenn nicht alle der folgenden Bedingungen erfüllt sind:
-Die Patientin versteht das zu erwartende teratogene Risiko für das ungeborene Kind.
-Sie versteht die Notwendigkeit einer wirksamen Schwangerschaftsverhütung ohne Unterbrechung 4 Wochen vor Behandlungsbeginn, während der ganzen Behandlungsdauer inklusive Behandlungsunterbrüchen und 4 Wochen nach Beendigung der Behandlung.
-Sogar wenn eine gebärfähige Patientin amenorrhoisch ist, muss sie alle Empfehlungen zu einer wirksamen Kontrazeption befolgen.
-Sie soll fähig sein, sich an wirksame kontrazeptive Massnahmen zu halten.
-Sie ist informiert und versteht die Konsequenzen einer Schwangerschaft und die Notwendigkeit, rasch medizinischen Rat zu suchen, falls eine Schwangerschaft vermutet wird.
-Sie versteht die Notwendigkeit und ist bereit, Schwangerschaftstests alle 4 Wochen durchführen zu lassen.
-Sie hat bestätigt, dass sie die Gefahren und notwendigen Vorsichtsmassnahmen im Zusammenhang mit der Einnahme von Pomalidomid verstanden hat.
Der verschreibende Arzt muss bei gebärfähigen Frauen sicherstellen, dass
die Patientin die obenstehenden Bedingungen erfüllt.
die Patientin die Bedingungen zur Schwangerschaftsverhütung einhält, einschliesslich der Bestätigung eines genügenden Verständnisses.
die Patientin ausreichende kontrazeptive Massnahmen während mindestens 4 Wochen vor Beginn der Behandlung angewendet hat und wirksame kontrazeptive Massnahmen während der ganzen Behandlungszeit inklusive Behandlungsunterbrüchen und während mindestens 4 Wochen nach Ende der Behandlung weiterführen wird. Bei Patientinnen, bei welchen eine sofortige Behandlung mit Pomalidomid notwendig ist, muss eine adäquate Kontrazeption inkl. Verwendung von Kondomen während 7 Tagen vor Beginn der Behandlung durchgeführt werden.
ein negatives Resultat eines Schwangerschaftstests vor Beginn der Behandlung vorliegt.
Kontrazeption
Gebärfähige Frauen müssen während 4 Wochen vor Beginn der Behandlung, während der ganzen Behandlungszeit inkl. Behandlungsunterbrüchen und während 4 Wochen nach Abschluss der Behandlung wirksame kontrazeptive Methoden anwenden. Bei Patientinnen, bei denen eine sofortige Behandlung mit Pomalidomid notwendig ist, muss während 7 Tagen vor Beginn der Behandlung eine wirksame Kontrazeption inkl. Verwendung von Kondomen durchgeführt werden. Falls nicht schon vorher wirksame kontrazeptive Methoden angewendet wurden, muss die Patientin an eine medizinische Beratungsstelle überwiesen werden, wo sie eine umfassende Beratung betreffend wirksamer kontrazeptiver Methoden erhält.
Die folgenden Verfahren können als wirksame kontrazeptive Methoden angesehen werden:
- von der Patientin unabhängige Methoden:
-Implantat
-Medroxyprogesteron-Acetat-Depot
-Sterilisation
- von der Patientin abhängige Methoden:
-Abstinenz von heterosexuellem Geschlechtsverkehr
-Heterosexueller Geschlechtsverkehr nur mit einem vasektomierten männlichen Partner; die Vasektomie muss durch zweimalige negative Spermauntersuchung bestätigt werden
-Orale Kontrazeptiva nur Progesteron enthaltend.
Wegen des erhöhten Risikos venöser Thromboembolien unter Pomalidomid werden kombinierte orale Kontrazeptiva nicht empfohlen. Falls eine Patientin bereits kombinierte orale Kontrazeptiva verwendet, sollte ein Wechsel zu einer anderen kontrazeptiven Methode in Betracht gezogen werden. Das Risiko venöser Thromboembolien bleibt während 4-6 Wochen nach Abschluss der Behandlung mit kombinierten oralen Kontrazeptiva bestehen. Falls andere Methoden nicht angewendet werden können, sollte eine Thromboseprophylaxe während der weiteren Verwendung der kombinierten oralen Kontrazeptiva in Betracht gezogen werden. Die Patientin sollte angemessen über das Risiko einer venösen Thromboembolie informiert werden.
Intrauterine Systeme haben ein erhöhtes Risiko von Infektionen beim Einsetzen und können zu unregelmässigen vaginalen Blutungen führen. Diese Methoden werden daher nicht empfohlen.
Schwangerschaftstests
Es müssen Schwangerschaftstests mit einer Empfindlichkeit von mindestens 25 IU/mL hCG bei gebärfähigen Frauen durchgeführt werden.
Jeder Fall einer Patientin mit einem positiven Schwangerschaftstest muss unverzüglich dem Swiss Teratogen Information Service (STIS), Lausanne mit dem Swissmedic-Formular "Meldung einer vermuteten unerwünschten Arzneimittelwirkung (UAW)" gemeldet werden.
- Vor Beginn einer Behandlung
Ein Schwangerschaftstest muss während der Konsultation, bei welcher Pomalidomid verschrieben wird, oder innerhalb von drei Tagen vor dem Besuch des verschreibenden Arztes durchgeführt werden, nachdem die Patientin während mindestens 4 Wochen eine wirksame Kontrazeption durchgeführt hat. Der Test soll sicherstellen, dass die Patientin bei Beginn der Behandlung mit Pomalidomid nicht schwanger ist.
- Vor Beginn der Behandlung, wenn sofortige Behandlung notwendig ist
Ein quantitativer hCG-Test im Serum sollte sofort durchgeführt werden. Nach wirksamer Kontrazeption inkl. Verwendung eines Kondoms während 7 Tagen muss dieser Test wiederholt werden. Falls beide Tests bestätigen, dass die Patientin nicht schwanger ist, kann mit der Behandlung begonnen werden.
- Während und bei Abschluss der Behandlung
Ein Schwangerschaftstest muss alle 4 Wochen, einschliesslich 4 Wochen nach Abschluss der Behandlung, wiederholt werden. Diese Schwangerschaftstests sollten während der Arztbesuche zur Verschreibung von Pomalidomid oder in den drei Tagen vor dem Arztbesuch durchgeführt werden.
Am besten sollten Schwangerschaftstests, Verschreibung und Abgabe von Pomalidomid am gleichen Tag erfolgen. Die Abgabe von Pomalidomid muss innerhalb von maximal 7 Tagen nach der Verschreibung erfolgen.
Programm bei Patienten
Klinische Daten belegen, dass es bei männlichen Patienten während der Einnahme von Imnovid zum Übertritt dieses Wirkstoffs in das Sperma kommt. Patienten mit gebärfähigen Partnerinnen sollten deshalb während der Behandlung mit Imnovid und mindestens für 7 Tage nach Beendigung der Behandlung beim Geschlechtsverkehr Kondome benutzen. Männer, welche Imnovid einnehmen, müssen folgende Bedingungen erfüllen:
-Sie müssen das zu erwartende teratogene Risiko verstehen, falls sie mit einer gebärfähigen Frau Geschlechtsverkehr haben.
-Sie müssen verstehen und damit einverstanden sein, während der ganzen Behandlungsdauer, inklusive Behandlungsunterbrüchen und während 7 Tagen nach Abschluss der Behandlung ein Kondom zu benützen, wenn sie mit einer schwangeren oder gebärfähigen Frau Geschlechtsverkehr haben.
Der verschreibende Arzt muss sicherstellen, dass männliche Patienten die Notwendigkeit der Verwendung eines Kondoms während der ganzen Behandlungsdauer, inklusive Behandlungsunterbrüchen und während 7 Tagen nach Abschluss der Behandlung verstehen und damit einverstanden sind, wenn sie mit einer schwangeren oder gebärfähigen Frau Geschlechtsverkehr haben.
Die Patienten dürfen während der Behandlung mit Imnovid und 7 Tage danach kein Sperma spenden.
Zusätzliche Vorsichtsmassnahmen
Die Patienten und Patientinnen müssen angewiesen werden, dieses Arzneimittel niemals anderen Personen zu geben und nicht verwendete Kapseln ihrem Arzt oder Apotheker nach Beendigung der Therapie zurückzugeben.
Medizinisches Fachpersonal und Pflegekräfte sollten Einweghandschuhe tragen, wenn sie den Blister oder die Kapsel anfassen. Frauen, die schwanger sind oder vermuten, dass sie schwanger sein könnten, sollten den Blister oder die Kapsel nicht handhaben.
Andere Warnhinweise und Vorsichtsmassnahmen
Unerwünschte hämatologische Wirkungen
Die Patienten sind auf hämatologische Toxizitäten, insbesondere Neutropenie, zu überwachen. Das vollständige Blutbild ist in den ersten 8 Wochen wöchentlich und danach monatlich zu kontrollieren. Eine Dosismodifikation kann erforderlich werden (siehe "Dosierung/Anwendung" ).
Thromboembolische Ereignisse
Es wurde von venös thromboembolischen Ereignissen berichtet (vorwiegend tiefe Venenthrombosen und pulmonale Embolie). Deshalb wird eine Antikoagulation empfohlen (ausser wenn diese kontraindiziert ist). Die Entscheidung für Massnahmen zur Thrombose-Prophylaxe sollte nach Beurteilung der Risikofaktoren des jeweiligen Patienten mit der gebotenen Sorgfalt individuell getroffen werden.
Kardiale Erkrankungen
Fälle von Herzinsuffizienz, einschliesslich kongestive Herzinsuffizienz, Lungenödem und Vorhofflimmern wurden berichtet, vor allem bei Patienten mit vorbestehender Herzerkrankung oder kardialen Risikofaktoren. Wenn erwogen wird, solche Patienten mit Pomalidomid zu behandeln, ist entsprechende Vorsicht geboten, einschliesslich einer regelmässigen Überwachung auf Anzeichen und Symptome einer Herzinsuffizienz.
Tumorlyse-Syndrom
Es kann ein Tumorlyse-Syndrom auftreten. Bei Patienten mit einer hohen Tumorlast vor Behandlungsbeginn besteht das grösste Risiko für ein Tumorlyse-Syndrom. Diese Patienten sind engmaschig zu überwachen und es müssen geeignete Vorsichtsmassnahmen getroffen werden.
Allergische Reaktionen und schwere Hautreaktionen
Es wurde über Angioödeme, Anaphylaxie und schwere dermatologische Reaktionen, einschliesslich Stevens-Johnson-Syndrom (SJS), toxischer epidermaler Nekrolyse (TEN) und Arzneimittelexanthem mit Eosinophilie und systemischen Symptomen (DRESS), berichtet. Das DRESS-Syndrom kann sich in Form einer Hautreaktion (wie Hautausschlag oder exfoliative Dermatitis) in Verbindung mit Eosinophilie, Fieber und/oder Lymphadenopathie mit systemischen Komplikationen wie Hepatitis, Nephritis, Pneumonitis, Myokarditis und/oder Perikarditis zeigen. Diese Ereignisse können tödlich sein. Bei einem Grad-2- oder Grad-3-Hautausschlag sollte eine Unterbrechung oder das Absetzen der Behandlung mit Pomalidomid erwogen werden. Bei Angioödem, Anaphylaxie, Grad-4-Hautausschlag, exfoliativem oder bullösem Hautausschlag, oder bei Verdacht auf SJS, TEN oder DRESS muss Pomalidomid abgesetzt werden. Wurde die Behandlung wegen derartiger Reaktionen beendet, sollte sie nicht mehr aufgenommen werden.
Schwindel und Verwirrtheit
Es wurde über das Auftreten von Schwindel und Verwirrtheit berichtet. Weisen sie den Patienten zur Vorsicht auf Situationen hin, in denen Schwindel und Verwirrtheit ein Problem sein können.
Sekundäre Primärmalignome
Über sekundäre Primärmalignome wurde bei Patienten berichtet, die mit Pomalidomid behandelt wurden. Der Arzt/die Ärztin sollten die Patienten vor und während der Behandlung mithilfe der üblichen Massnahmen zur Krebsfrüherkennung hinsichtlich des Auftretens sekundärer Primärmalignome sorgfältig untersuchen und gegebenenfalls eine Therapie einleiten.
Leberfunktionsstörungen
Deutlich erhöhte Alaninaminotransferase- und Bilirubinspiegel wurden bei mit Pomalidomid behandelten Patienten beobachtet (siehe Abschnitt "Unerwünschte Wirkungen" ). Es liegen auch Fälle von Hepatitis, einschliesslich Hepatitis B-Reaktivierung vor, die zum Absetzen von Pomalidomid führten. Eine regelmässige Kontrolle der Leberfunktion wird empfohlen.
Infektionen
Bei Patienten, die eine Kombinationstherapie mit Pomalidomid in klinischen Studien erhielten, traten bei 55,0-80,2% der Patienten Infektionen auf (24,0-30,9% Grad 3 oder 4). Infektionen der oberen Atemwege und Pneumonie waren die am häufigsten auftretenden Infektionen. Tödlich verlaufende Infektionen (Grad 5) traten bei 2,7-4,0% der Patienten auf. Infektionen führten bei 2,0-2,9% der Patienten zum Absetzen von Pomalidomid.
Patienten mit bekannten Risikofaktoren für das Auftreten von Infektionen müssen engmaschig überwacht werden. Alle Patienten sind anzuweisen, beim ersten Anzeichen einer Infektion (z.B. Husten, Fieber etc.) sofort einen Arzt aufzusuchen, um so durch eine frühzeitige Behandlung eine Verminderung des Schweregrades zu ermöglichen.
In seltenen Fällen wurde bei Patienten, die Pomalidomid in Kombination mit Dexamethason erhielten und zuvor mit dem Hepatitis-B-Virus (HBV) infiziert worden waren, über eine Reaktivierung von Hepatitis B berichtet. In einigen Fällen führte dies zu einem akuten Leberversagen, was ein Absetzen von Pomalidomid zur Folge hatte. Der Hepatitis-B-Virus-Status ist vor Beginn der Behandlung mit Pomalidomid abzuklären. Bei Patienten, die positiv auf eine HBV-Infektion getestet wurden, sollte ein Arzt mit Erfahrung in der Behandlung von Hepatitis B herangezogen werden. Entsprechende Vorsicht ist geboten, wenn Pomalidomid in Kombination mit Dexamethason bei vorher mit HBV infizierten Patienten angewendet wird. Diese Patienten müssen während der gesamten Behandlung engmaschig auf Anzeichen und Symptome einer aktiven HBV-Infektion überwacht werden.
Progressive multifokale Leukenzephalopathie (PML)
Im Zusammenhang mit Pomalidomid wurden Fälle progressiver multifokaler Leukenzephalopathie, einschliesslich tödlich verlaufender Fälle, beobachtet. Dabei trat die PML einige Monate bis Jahre nach Behandlungsbeginn mit Pomalidomid auf.
Ärzte sollten die Patienten in regelmässigen Abständen überwachen und PML als Differenzialdiagnose bei Patienten mit neuen oder sich verschlechternden neurologischen Symptomen, kognitiven oder verhaltensbezogenen Zeichen oder Symptomen berücksichtigen. Die Patienten sollten angewiesen werden ihre Partner oder Pflegepersonen über ihre Behandlung zu informieren, da diese Symptome bemerken könnten, die dem Patienten nicht bewusst sind.
Die Bewertung in Bezug auf PML sollte auf einer neurologischen Untersuchung, einer Kernspintomographie des Gehirns sowie einer Liquoranalyse auf DNS des JC-Virus (JCV) mittels Polymerasekettenreaktion (PCR) oder einer Biopsie des Gehirns mit Untersuchung auf JCV beruhen. Eine negative JCV-PCR schliesst PML nicht aus. MRT-Befunde können bereits vor dem Auftreten klinischer Anzeichen und Symptome sichtbar sein. Es wurde über Fälle von PML berichtet, die auf der Basis von MRT-Befunden und dem Nachweis von JCV-DNA im Liquor ohne PML-spezifische klinische Anzeichen oder Symptome diagnostiziert wurden. Viele dieser Patienten zeigten anschliessend Symptome einer PML. Daher kann eine MRT-Überwachung auf Hinweise einer PML nützlich sein und alle verdächtigen Befunde sollten zu einer gründlicheren Untersuchung führen, um gegebenenfalls eine frühzeitige Diagnose der PML zu ermöglichen. Eine zusätzliche Nachbeobachtung und Bewertung kann notwendig sein, wenn keine alternative Diagnose gestellt werden kann.
Wenn PML vermutet wird, muss eine weitere Einnahme von Pomalidomid bis zum Ausschluss von PML ausgesetzt werden.
Falls PML bestätigt wurde, ist Pomalidomid dauerhaft abzusetzen.
Renale Störungen
Bei Patienten mit Kreatinin-Clearance ≤45 ml/min, die Pomalidomid in Kombination mit Bortezomib und Dexamethason erhielten, wurde eine erhöhte Rate an hämatologischen Nebenwirkungen (Anämie und Thrombozytopenie) und renalen Nebenwirkungen (akuter Nierenschaden) in klinischen Studien beobachtet (siehe auch "Eigenschaften/Wirkungen" ). Solche Patienten sollten sorgfältig überwacht werden.
Zur Anwendung anderer Arzneimittel in Kombination mit Pomalidomid wird auf die entsprechende Fachinformation für das jeweilige Arzneimittel verwiesen.
Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro Kapsel, d.h. es ist nahezu "natriumfrei" .
InteraktionenPotential anderer Arzneimittel zur Beeinflussung von Pomalidomid
Pomalidomid wird teilweise von CYP1A2 und CYP3A4/5 metabolisiert. Es ist ausserdem ein Substrat für P-Glycoprotein. Bei gleichzeitiger Anwendung von Pomalidomid mit Arzneistoffen, wie z.B. dem starken CYP3A4/5- und P-gp-Inhibitor Ketoconazol oder dem starken CYP3A4/5-Induktor Carbamazepin, wurde keine klinisch relevante Wirkung auf die Exposition gegenüber Pomalidomid festgestellt.
Die gleichzeitige Anwendung des starken CYP1A2-Hemmers Fluvoxamin mit Pomalidomid plus Ketoconazol erhöhte die durchschnittliche Exposition gegenüber Pomalidomid um 107% mit einem 90%-Konfidenzintervall [91% bis 124%] verglichen mit Pomalidomid plus Ketoconazol alleine. Die gleichzeitige Anwendung von Fluvoxamin (ein starker CYP1A2-Hemmer) mit Pomalidomid erhöhte die durchschnittliche Exposition gegenüber Pomalidomid um 125% mit einem 90%-Konfidenzintervall [98% bis 157%] verglichen mit Pomalidomid alleine bei gesunden Probanden. Wenn starke CYP1A2-Hemmer (z.B. Ciprofloxacin und Fluvoxamin) gleichzeitig mit Pomalidomid verabreicht werden, muss die Pomalidomid-Dosis um 50% reduziert werden.
Potential von Pomalidomid zur Beeinflussung anderer Arzneimittel
Pomalidomid hemmt nicht CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 oder CYP3A4/5 in vitro. Darüber hinaus ist Pomalidomid in vitro kein Induktor der Enzyme CYP1A2, CYP2B6, CYP2C9, CYP2C19 und CYP3A4/5.
Pomalidomid ist kein Inhibitor von P-Glycoprotein (P-gp) und zeigte in in-vitro-Untersuchungen keine oder eine nur geringe Hemmwirkung auf das Breast Cancer Resistant Protein (BCRP), Organic Anion Transporter Protein (OATP) 1B1, OATP1B3, Organic Cation Transporter OAT1 und OAT3 sowie Organic Anion Transporter Protein OCT2.
Es wird nicht damit gerechnet, dass Pomalidomid klinisch relevante pharmakokinetische Arzneimittel-Interaktionen infolge Enzymhemmung oder -induktion oder Transporter-Inhibition verursacht, wenn es zusammen mit Substraten dieser Enzyme oder Transporter angewendet wird. Das Potential für solche Arzneimittel-Interaktionen, und auch die potenziellen Auswirkungen von Pomalidomid auf die Exposition gegenüber oralen Kontrazeptiva, wurden klinisch nicht untersucht.
Schwangerschaft, StillzeitSchwangerschaft
Es ist mit einem teratogenen Effekt von Pomalidomid beim Menschen zu rechnen. Pomalidomid ist während der Schwangerschaft kontraindiziert und darf bei gebärfähigen Frauen nicht angewendet werden, ausser es sind alle Bedingungen für die Schwangerschaftsverhütung erfüllt (siehe "Warnhinweise und Vorsichtsmassnahmen" ).
Stillzeit
Es ist nicht bekannt, ob Pomalidomid beim Menschen in die Muttermilch übergeht. Bei laktierenden Ratten wurde Pomalidomid nach Gabe an das Muttertier in der Milch wiedergefunden. Wegen seines Potenzials, bei gestillten Säuglingen Nebenwirkungen auszulösen, sollte unter Berücksichtigung der Bedeutung der Pomalidomid-Behandlung für die Mutter entschieden werden, ob abgestillt oder das Arzneimittel abgesetzt werden soll.
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von MaschinenEs wurden keine Studien zu den Auswirkungen von Pomalidomid auf die Verkehrstüchtigkeit und das Bedienen von Maschinen durchgeführt. Unter der Anwendung von Pomalidomid wurde über Synkope, Fatigue und Schwindel berichtet. Daher wird zur Vorsicht geraten, wenn Patienten, welche Pomalidomid erhalten, am Verkehr teilnehmen oder Maschinen bedienen.
Unerwünschte WirkungenImnovid in Kombination mit Bortezomib und Dexamethason (PVd) bei Patienten mit multiplem Myelom, die mindestens eine vorgängige Therapie erhalten haben
In der randomisierten Studie CC-4047-MM-007 erhielten 278 Patienten Pomalidomid, Bortezomib und Dexamethason.
Die am häufigsten gemeldeten Erkrankungen des Blutes und des Lymphsystems waren Neutropenie, Thrombozytopenie und Anämie. Die am häufigsten gemeldete unerwünschte Wirkung war periphere sensorische Neuropathie. Die am häufigsten gemeldete schwerwiegende unerwünschte Wirkung war Pneumonie (11,5%).
Imnovid in Kombination mit Dexamethason (Pd) bei Patienten mit rezidiviertem und refraktärem multiplem Myelom, welche mindestens zwei vorgängige Therapien erhalten haben
In drei klinischen Studien (CC-4047-MM-003, CC-4047-MM-002 und CC-4047-IFM-2009-02) wurden 455 Patienten gegenüber 4 mg Pomalidomid exponiert.
Die am häufigsten berichteten unerwünschten Wirkungen waren Neutropenie, Anämie, Thrombozytopenie, Fatigue, Fieber, Obstipation und Diarrhö.
Die häufigste schwerwiegende unerwünschte Wirkung war Pneumonie (12,5%).
Die Häufigkeiten sind wie folgt definiert: Häufigkeitsangaben: sehr häufig (≥1/10); häufig (<1/10, ≥1/100); gelegentlich (<1/100, ≥1/1'000); selten (<1/1'000, ≥1/10'000), sehr selten (<1/10'000).
Infektionen und parasitäre Erkrankungen#
Sehr häufig: Infektionen der oberen Atemwege (20,9%), Pneumonie (19,1%), Bronchitis (14,0%), Virusinfektion der oberen Atemwege (11,2%).
Häufig: Sepsis, septischer Schock, Clostridium-difficile-Colitis, Bronchopneumonie, Influenza, Harnwegsinfektion, Atemwegsinfektion, Infektion der unteren Atemwege, Bronchiolitis, Lungeninfektion, Sinusitis, Nasopharyngitis, Candidiasis, orale Candidiasis.
Gelegentlich: Neutropenische Sepsis, Herpes Zoster*.
Selten: Reaktivierung des Hepatitis-B-Virus*, progressive multifokale Leukenzephalopathie*.
# = Es werden alle bevorzugten Begriffe der Systemorganklasse Infektionen (einschliesslich bakterielle, virale und Pilzinfektionen), ausgenommen seltene Infektionen von öffentlichen Gesundheitsinteresse, aufgeführt.
Gutartige, bösartige und unspezifische Neubildungen (inklusive Zysten und Polypen)
Häufig: Basalzellkarzinom.
Gelegentlich: Plattenepithelkarzinom der Haut*.
Erkrankungen des Blutes und des Lymphsystems
Sehr häufig: Neutropenie (47,9%), Anämie (44,0%), Thrombozytopenie (36,7%), Leukopenie (13,0%).
Häufig: Febrile Neutropenie, Lymphopenie, verminderte Leukozytenzahl, verminderte Neutrophilenzahl, verminderte Thrombozytenzahl.
Gelegentlich: Panzytopenie*.
Erkrankungen des Immunsystem
Gelegentlich: Allergische Reaktionen (z.B. Angioödeme, Urtikaria)*.
Selten: Anaphylaxie*.
Nicht bekannt: Abstossung eines transplantierten soliden Organs*.
Endokrine Erkrankungen
Selten: Hypothyreose*.
Stoffwechsel- und Ernährungsstörungen
Sehr häufig: Hypokaliämie (15,5%), Hyperglykämie (14,4%), verminderter Appetit (11,6%).
Häufig: Dehydratation, Hyponatriämie, Hyperkaliämie, Hyperkalzämie, Hypokalzämie, Hypophosphatämie, Hypoalbuminämie, Hypomagnesiämie.
Psychiatrische Erkrankungen
Sehr häufig: Schlafstörungen (16,2%).
Häufig: Verwirrtheitszustand, Angstzustände, Depression, Stimmungsänderung.
Erkrankungen des Nervensystems
Sehr häufig: Periphere sensorische Neuropathie (47,8%), Schwindel (17,3%), Tremor (10,8%).
Häufig: Periphere Neuropathie, periphere sensorimotorische Neuropathie, Synkope, Somnolenz, Lethargie, Bewusstseinstrübung, Kopfschmerzen, Dysgeusie, Parästhesie.
Augenerkrankungen
Häufig: Verschwommenes Sehen, Katarakt.
Erkrankungen des Ohrs und Labyrinths
Häufig: Vertigo.
Herzerkrankungen
Häufig: Dekompensierte Herzinsuffizienz, Vorhofflimmern, Tachykardie.
Gefässerkrankungen
Häufig: Tiefe Venenthrombose, Hypotonie, Hypertonie.
Erkrankungen der Atemwege, des Brustraums und Mediastinums
Sehr häufig: Husten (20,5%), Dyspnoe (20,2%).
Häufig: Lungenembolie, produktiver Husten, Nasenverstopfung, oropharyngeale Schmerzen, Dysphonie, Nasenbluten, Belastungsdyspnoe.
Gelegentlich: Atemnotsyndrom, interstitielle Lungenerkrankung einschliesslich Fälle mit Pneumonitis*.
Erkrankungen des Gastrointestinaltrakts
Sehr häufig: Obstipation (36,7%), Diarrhö (33,8%), Übelkeit (17,6%), Erbrechen (11,5%).
Häufig: Bauchschmerzen, Oberbauchschmerzen, Stomatitis, trockener Mund, aufgeblähter Bauch.
Gelegentlich: Gastrointestinale Blutungen*.
Leber und Gallenerkrankungen
Häufig: Alaninaminotransferase erhöht.
Gelegentlich: Hyperbilirubinämie, erhöhte Leberfunktionswerte und Hepatitis*.
Erkrankungen der Haut und des Unterhautzellgewebes
Häufig: Hautausschlag, Pruritus, trockene Haut, Hyperhidrosis, Nachtschweiss.
Sehr selten: Stevens-Johnson-Syndrom*, toxische epidermale Nekrolyse*, Arzneimittelexanthem mit Eosinophilie und systemischen Symptomen*.
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen
Sehr häufig: Rückenschmerzen (18,7%), Muskelschwäche (13,7%), Knochenschmerzen (13,6%), Muskelspasmen (13,0%).
Häufig: Arthralgie, Schmerzen des Bewegungsapparates, Schmerzen der Skelettmuskulatur im Brustbereich, Schmerzen in einer Extremität/Schmerzen in Gliedmassen.
Erkrankungen der Nieren und Harnwege
Häufig: Akuter Nierenschaden, Nierenversagen, akutes Nierenversagen, chronische Nierenerkrankung, Harnverhalt, Kreatininspiegel im Blut erhöht.
Erkrankungen der Geschlechtsorgane und der Brustdrüse
Häufig: Beckenschmerz.
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort
Sehr häufig: Fatigue (37,1%), periphere Ödeme (33,8%), Fieber (23,7%), Asthenie (18,2%).
Häufig: Verschlechterung des körperlichen Allgemeinzustands, Schmerzen im Brustkorb, Schmerzen, Schüttelfrost, nicht herzbedingte Brustschmerzen, Ödem.
Gelegentlich: Tumorlyse-Syndrom*.
Untersuchungen
Häufig: Gewichtsverlust.
Verletzung, Vergiftung und durch Eingriffe bedingte Komplikationen
Häufig: Sturz.
* = Erfahrung nach Marktzulassung
Pädiatrische Population
Die verfügbaren Daten aus zwei offenen unkontrollierten Studien sind limitiert. Es liegen keine Hinweise für neue Sicherheitsaspekte vor.
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von grosser Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdacht einer neuen oder schwerwiegenden Nebenwirkung über das Online-Portal ElViS (Electronic Vigilance System) anzuzeigen. Informationen dazu finden Sie unter www.swissmedic.ch.
ÜberdosierungPomalidomid-Dosen bis zu 50 mg als Einmalgabe bei gesunden Freiwilligen und 10 mg bei einmal täglicher wiederholter Verabreichung bei Patienten mit multiplem Myelom wurden untersucht, ohne dass überdosierungsbedingte schwerwiegende unerwünschte Ereignisse berichtet worden wären. Pomalidomid wurde durch Hämodialyse entfernt.
Eigenschaften/WirkungenATC-Code
L04AX06
Wirkungsmechanismus
Pomalidomid ist ein Derivat von Thalidomid und liegt als Racemat vor. Es besitzt sowohl immunmodulierende als auch anti-angiogenetische Eigenschaften.
Pomalidomid hemmt die Proliferation hämatopoetischer Tumorzellen und hemmt in vitro auch die Proliferation Lenalidomid-resistenter Zelllinien. Es verstärkt die T-Zell Proliferation und die NK-Zell-vermittelte Zytotoxizität, hemmt die Produktion proinflammatorischer Zytokine (z.B. TNF-α und IL-6) und blockiert die Endothelzellmigration und -adhäsion.
Pomalidomid bindet direkt an das Protein Cereblon (CRBN), das Teil eines E3-Ligase-Komplexes ist, der DDB1-Protein (DNA damage-binding protein 1), Cullin 4 (CUL4) und Roc1 umfasst und die Autoubiquitinierung von CRBN innerhalb des Komplexes hemmen kann. E3-Ubiquitinligasen sind verantwortlich für die Polyubiquitinierung verschiedener Substratproteine und können teilweise die unter der Pomalidomid-Behandlung beobachteten pleiotropischen Zellwirkungen erklären.
In vitro, in Gegenwart von Pomalidomid, werden die Substratproteine Aiolos und Ikaros ubiquitiniert und anschliessend abgebaut, mit daraus resultierender direkter zytotoxischer und immunmodulatorischer Wirkung. In vivo führte die Pomalidomid-Therapie zur Abnahme des Ikaros-Spiegels bei Patienten mit rezidiviertem Lenalidomid-refraktärem multiplem Myelom.
Pharmakodynamik
Siehe Abschnitt Wirkungsmechanismus.
Klinische Wirksamkeit
Pomalidomid in Kombination mit Bortezomib und niedrig dosiertem Dexamethason (PVd)
Eine randomisierte, offene, 2-armige, multizentrische klinische Studie der Phase 3 (CC-4047-MM-007) bewertete die Wirksamkeit und Sicherheit von Pomalidomid in Kombination mit Bortezomib und niedrig dosiertem Dexamethason (PVd) im Vergleich zu Bortezomib und niedrig dosiertem Dexamethason (Vd) bei vorbehandelten erwachsenen Patienten, welche mindestens eine vorgängige Therapie erhalten haben, von denen eine Lenalidomid enthalten haben muss.
Die Patienten im PVd-Arm erhielten 4 mg Pomalidomid oral an den Tagen 1 bis 14 eines jeden 21-tägigen Zyklus. Niedrig dosiertes Dexamethason in einer Dosis von 20 mg wurde einmal täglich an den Tagen 1, 2, 4, 5, 8, 9, 11 und 12 eines 14-tägigen Zyklus in Zyklus 1 bis einschliesslich Zyklus 8 verabreicht und anschliessend einmal pro Tag an den Tagen 1, 2, 8 und 9 eines jeden anschliessenden 21-tägigen Zyklus von Zyklus 9 an. Patienten >75 Jahre erhielten Dexamethason 10 mg nach dem gleichen Therapieplan wie jüngere Patienten. Bortezomib (1,3 mg/m2/Dosis) wurde an den Tagen 1, 4, 8 und 11 des 21-tägigen Zyklus von Zyklus 1 bis einschliesslich Zyklus 8 verabreicht und anschliessend in der gleichen Dosis an den Tagen 1 und 8 des 21-tägigen Zyklus von Zyklus 9 an. Im Vd-Arm wurden Bortezomib und Dexamethason in der gleichen Dosis und nach dem gleichen Therapieplan verabreicht wie im PVd-Arm. Die Behandlung wurde bis zum Fortschreiten der Krankheit oder Auftreten einer nicht akzeptablen Toxizität fortgesetzt. Wenn es zur Behandlung von Toxizitätserscheinungen notwendig war, wurden die Dosen reduziert oder die Behandlung vorübergehend unterbrochen bzw. abgebrochen.
Es wurden insgesamt 559 Patienten in die Studie randomisiert: 281 in den PVd-Arm und 278 in den Vd-Arm. 54% der Patienten waren männlich bei einem medianen Alter der Gesamtpopulation von 68 Jahren (Min., Max.: 27, 89 Jahre). Ungefähr 70% der Patienten waren unter Lenalidomid refraktär (71,2% im PVd-Arm, 68,7% im Vd-Arm). Insgesamt stimmten die demographischen und krankheitsbezogenen Merkmale zwischen den Behandlungsarmen allgemein überein.
Der primäre Wirksamkeitsendpunkt war das progressionsfreie Überleben (PFS). Das PFS war definiert als die Zeit zwischen der Randomisierung und der Krankheitsprogression oder dem Tod. Das Ansprechen wurde von einem unabhängigen Ausschuss zur Beurteilung des Ansprechens (IRAC, Independent Response Adjudication Committee) entsprechend den IMWG-Kriterien unter Verwendung des Intent-to-Treat-Kollektivs als primäre Analyse beurteilt. Das Gesamtüberleben war ein sekundärer Endpunkt.
Beim ITT-Kollektiv, nach einer medianen Nachbeobachtung von 15,9 Monaten, betrug die Dauer des medianen PFS 11,20 Monate (95%-KI: 9,66; 13,73) im PVd-Arm. Im Vd-Arm betrug die Dauer des medianen PFS 7,10 Monate (95%-KI: 5,88; 8,48). Das PFS war im PVd-Arm signifikant länger als im Vd-Arm: HR 0,61 (95%-KI: 0,49; 0,77) und wies auf eine 39%ige Abnahme des Risikos für eine Krankheitsprogression oder für den Tod im PVd-Arm hin.
Bei Patienten mit Baseline CrCl <45 ml/min betrug das mediane PFS 7,16 Monaten (95% KI: 1,94; 10,74) im PVd-Arm (N = 37) verglichen mit 4,44 Monaten (95% KI: 2,83; 9,49) im Vd-Arm (N = 38); HR = 1,06, 95% KI: 0,61; 1,83.
Gemäss der finalen Analyse des Gesamtüberlebens (last-patient-last-visit, 13. Mai 2022; mediane Nachbeobachtung von 64,5 Monaten) waren 197/281 (70,1%) Patienten im PVd-Arm verstorben und 193/278 (69,4%) im Vd-Arm. Das mediane Gesamtüberleben aus der Kaplan-Meier-Schätzung betrug 35,6 Monate für den PVd-Arm und 31,6 Monate für den Vd-Arm; HR = 0,94, 95% KI: 0,77, 1,15, mit einer Gesamtereignis-Rate von 69,8%. Diese beobachteten Unterschiede waren statistisch nicht signifikant.
Pomalidomid in Kombination mit niedrig dosiertem Dexamethason (Pd)
Zur Beurteilung der Wirksamkeit und Sicherheit von Imnovid wurden eine Phase III Studie (CC-4047-MM-003) und eine Phase II Studie (CC-4047-MM-002) durchgeführt.
Die Phase II
Studie MM-002 wurde bei 221 Patienten mit rezidiviertem und refraktärem multiplem Myelom, welche gegenüber ihrer zuletzt erhaltenen Myelomtherapie refraktär waren und Lenalidomid und Bortezomib erhalten hatten, durchgeführt.
Pomalidomid 4 mg wurde bis zur Progredienz, entweder allein an 21/28 Tagen verabreicht oder in Kombination mit Dexamethason (40 mg wöchentlich, verabreicht an den Tagen 1, 8, 15 und 22 eines jeden 28-tägigen Zyklus).
Ca. 81% der Patienten waren gegenüber Lenalidomid, 74% gegenüber Bortezomib und 64% gegenüber Lenalidomid und Bortezomib refraktär (definiert nach den IMWG-Kriterien).
Das mediane progressionsfreie Überleben (Primärendpunkt) betrug bei Pomalidomid plus Dexamethason 16.6 Wochen und bei Pomalidomid allein 10,7 Wochen. Die Ansprechrate betrug 30,1% mit Pomalidomid plus Dexamethason gegenüber 9,3% mit Pomalidomid alleine.
Die Phase III
Die Phase III Studie (MM-003) verglich Pomalidomid plus Dexamethason-Therapie (Pom+LD-dex) mit Dexamethason allein (HD-dex) bei 455 Patienten mit rezidiviertem und refraktärem multiplem Myelom welche mindestens zwei Behandlungen erhalten hatten bei denen sowohl Lenalidomid als auch Bortezomib versagt hatten und die unter der letzten Therapie progredient waren.
Das mediane PFS (Primärendpunkt) betrug im POM+LD-dex Arm 15,7 Wochen (95% KI:13,0; 20,1) und 8 Wochen (95% KI: 7,0; 9,0) im HD-dex Arm, Hazard Ratio (HR) von 0,45 (95% KI: 0,35; 0,59; p <0,001).
Das mediane Gesamtüberleben wurde im Pomalidomid Arm noch nicht erreicht. Der Unterschied im Gesamtüberleben zwischen den beiden Behandlungsarmen war statistisch signifikant (Hazard Ratio von 0,53 (95% KI: 0,37; 0,74; p <0,001).
PharmakokinetikAbsorption
Pomalidomid erreicht eine maximale Plasmakonzentration (Cmax) zwischen 2 und 3 Stunden p.a. und wird nach oraler Einmalgabe zu >70% resorbiert. Die Bioverfügbarkeit ist annähernd dosisproportional. Bei Gabe zusammen mit einer fett- und kalorienreichen Mahlzeit wird die Bioverfügbarkeit nicht beeinflusst. Pomalidomid kann unabhängig von den Mahlzeiten verabreicht werden.
Distribution
Das Verteilungsvolumen im Steady-State ist 62 bis 138 l. Die Konzentration in der Samenflüssigkeit gesunder Probanden betrug ca. 67% des Plasmaspiegels. Die Proteinbindung ist niedrig.
Metabolismus
Pomalidomid ist im zirkulierenden Blut die Hauptkomponente (etwa 70% der Plasmaradioaktivität). Es fanden sich keine Metaboliten, die >10% der Gesamtradioaktivität im Plasma ausmachten.
Die wichtigsten Stoffwechselwege der ausgeschiedenen Radioaktivität sind Hydroxylierung mit nachfolgender Glukuronidierung sowie Hydrolyse. In vitro wurden CYP1A2 und CYP3A4 als die an der CYP-vermittelten Hydroxylierung von Pomalidomid primär beteiligten Enzyme identifiziert, mit zusätzlichen geringfügigen Beiträgen von CYP2C19 und CYP2D6.
Bei 14 gesunden männlichen Probanden, die nach einer oralen Einzeldosis von 4 mg Pomalidomid über einen Zeitraum von 10 Tagen täglich 25 Zigaretten rauchten, kam es zu einem Anstieg der Cmax von Pomalidomid um 14%, während die AUC von Pomalidomid um 32% abnahm, im Vergleich zu 13 gesunden männlichen Freiwilligen, die Nichtraucher waren.
Elimination
Die Eliminationshalbwertszeit beträgt etwa 9,5 Stunden bei gesunden Probanden und etwa 7,5 Stunden bei Patienten mit multiplem Myelom. Die mittlere Gesamtkörper-Clearance (CL/F) beträgt 7-10 l/h.
73% der Dosis werden im Urin und 15% mit den Fäzes eliminiert, wobei als Pomalidomid etwa 2% bzw. 8% im Urin bzw. in den Fäzes ausgeschieden werden.
Kinetik spezieller Patientengruppen
Leberfunktionsstörungen
Die pharmakokinetischen Parameter waren bei Patienten mit eingeschränkter Leberfunktion (gemäss Child-Pugh-Kriterien) gering verändert verglichen mit gesunden Probanden. Die durchschnittliche Exposition gegenüber Pomalidomid war bei Patienten mit leicht eingeschränkter Leberfunktion verglichen mit gesunden Patienten um 51% erhöht bei einem 90%-Konfidenzintervall [9% bis 110%]. Die durchschnittliche Exposition gegenüber Pomalidomid war bei Patienten mit mässig eingeschränkter Leberfunktion im Vergleich zu gesunden Probanden um 58% erhöht bei einem 90%-Konfidenzintervall [13% bis 119%]. Die durchschnittliche Exposition gegenüber Pomalidomid war bei Patienten mit stark eingeschränkter Leberfunktion verglichen mit gesunden Patienten um 72% erhöht bei einem 90%-Konfidenzintervall [24% bis 138%].
Nierenfunktionsstörungen
Pharmakokinetische Populationsanalysen haben gezeigt, dass die pharmakokinetischen Parameter von Pomalidomid bei Patienten mit Nierenfunktionsstörung (definiert durch die Kreatinin-Clearance oder geschätzte glomeruläre Filtrationsrate [eGFR]) im Vergleich zu Patienten mit normaler Nierenfunktion (CrCl ≥60 ml/min) keine auffallende Beeinträchtigung aufwiesen. Die durchschnittliche normalisierte AUC-Exposition gegenüber Pomalidomid bei Patienten mit mässiger Niereninsuffizienz (eGFR ≥30 bis ≤45 ml/min/1.73 m2) betrug 98,2% mit einem 90%-Konfidenzintervall [77,4% bis 120,6%] im Vergleich zu Patienten mit normaler Nierenfunktion. Die durchschnittliche normalisierte AUC-Exposition gegenüber Pomalidomid bei nicht dialysepflichtigen Patienten mit schwerer Niereninsuffizienz (CrCl <30 oder eGFR <30 ml/min/1.73 m2) betrug 100,2% mit einem 90%-Konfidenzintervall [79,7% bis 127,0%] im Vergleich zu Patienten mit normaler Nierenfunktion. Die durchschnittliche normalisierte AUC-Exposition gegenüber Pomalidomid bei dialysepflichtigen Patienten mit schwerer Niereninsuffizienz (CrCl <30 ml/min bei Dialysepflicht) erhöhte sich um 35,8% mit einem 90%-Konfidenzintervall [7,5% bis 70,0%] im Vergleich zu Patienten mit normaler Nierenfunktion.
Ältere Patienten
Bei Patienten im Alter zwischen 61 und 82 Jahren waren die mittleren pharmakokinetischen Parameter von AUC (0-∞) und Cmax im Allgemeinen ähnlich zu denen jüngerer Patienten.
Kinder und Jugendliche
Die aktuelle Datenlage bei pädiatrischen Patienten erlaubt keine Empfehlungen für eine Anwendung in dieser Altersgruppe.
Präklinische DatenGenotoxizität/Karzinogenität
Pomalidomid war in Mutationstests an Bakterien und Säugerzellen nicht mutagen und induzierte in humanen peripheren Blutlymphozyten keine Chromosomenaberrationen und in polychromatischen Erythrozyten im Knochenmark von Ratten, denen Dosen bis zu 2'000 mg/kg/Tag verabreicht wurden, keine Mikrokernbildung. Karzinogenitätsstudien wurden nicht durchgeführt.
Fertilität und frühembryonale Entwicklung
In einer Studie bei Ratten zur Fertilität und frühembryonalen Entwicklung wurde Pomalidomid männlichen und weiblichen Tieren in Dosierungen von 25, 250 und 1'000 mg/kg/Tag verabreicht. Die Uterusuntersuchung am 13. Trächtigkeitstag ergab für alle Dosisstufen eine Abnahme der mittleren Anzahl überlebensfähiger Embryonen sowie vermehrte Postimplantationsverluste. Daher war das NOAEL für diese beobachteten Effekte <25 mg/kg/Tag (AUC24h – 39'960 ng·h/ml; 99-fach höhere Exposition bei der niedrigsten getesteten Dosis im Verhältnis zu einer 4-mg-Dosis). Wenn behandelte Männchen in dieser Studie mit unbehandelten Weibchen gepaart wurden, waren alle uterinen Parameter mit den Kontrollen vergleichbar. Auf der Grundlage dieser Resultate wurden die beobachteten Effekte der Behandlung der weiblichen Tiere zugeschrieben.
Embryo-fetale Entwicklung
Pomalidomid erwies sich sowohl bei Ratten als auch bei Kaninchen als teratogen, wenn es während der Phase der Hauptorganogenese verabreicht wurde. In der Studie zur embryo-fetalen Entwicklungstoxizität bei Ratten wurden in allen Dosisstufen (25, 250 und 1'000 mg/kg/Tag) Missbildungen oder Fehlen der Harnblase, Fehlen der Schilddrüse sowie Fusion und Fehlausrichtung lumbaler und thorakaler Wirbelelemente (Wirbelkörper- und/oder Neuralbögen) beobachtet. In dieser Studie wurde keine maternale Toxizität beobachtet. Daher betrug das maternale NOAEL 1'000 mg/kg/Tag und das NOAEL für Entwicklungstoxizität <25 mg/kg/Tag (AUC24h = 34'340 ng·h/ml am 17. Trächtigkeitstag; 85-fach höhere Exposition bei der niedrigsten getesteten Dosis im Verhältnis zur klinischen Dosis von 4 mg). Bei Kaninchen rief Pomalidomid in Dosierungen von 10 bis 250 mg/kg embryo-fetale Entwicklungsmissbildungen hervor. Bei allen Dosisstufen wurden vermehrt Herzanomalien beobachtet, wobei die Zunahme bei 250 mg/kg/Tag signifikant war. Bei 100 und 250 mg/kg/Tag fanden sich geringfügige Zunahmen der Postimplantationsverluste und geringfügige Abnahmen der fetalen Geburtsgewichte. Bei 250 mg/kg/Tag umfassten die fetalen Missbildungen Gliedmassenanomalien (geknickte und/oder rotierte Vorder- und/oder Hinterläufe, loser oder fehlender Digitus) und damit assoziierte Skelettfehlbildungen (nicht ossifiziertes Os metacarpale, Fehlausrichtung von Phalanx und Os metacarpale, fehlender Digitus, nicht ossifizierte Phalanx und kurze nicht ossifizierte oder geknickte Tibia); mässiggradige Dilatation des Lateralventrikels des Gehirns; Lageanomalie der A. subclavia dextra; fehlender Lungenmittellappen; tief liegende Niere; veränderte Lebermorphologie; unvollständig oder nicht ossifiziertes Becken; erhöhter Durchschnittswert überzähliger thorakaler Rippen und verminderter Durchschnittswert ossifizierter Ossa tarsalia. Eine geringfügige Verminderung der maternalen Körpergewichtszunahme, eine signifikante Reduktion der Triglyzeride und eine signifikante Abnahme der absoluten und relativen Milzgewichte wurden bei 100 und 250 mg/kg/Tag beobachtet. Das maternale NOAEL betrug 10 mg/kg/Tag, das NOAEL für die Entwicklung war <10 mg/kg/Tag (AUC24h = 418 ng·h/ml am 19. Trächtigkeitstag; 1-fache klinische Exposition bei der Dosis 4 mg).
Sonstige HinweiseHaltbarkeit
Das Arzneimittel darf nur bis zu dem auf der Packung mit "EXP" bezeichneten Datum verwendet werden.
Besondere Lagerungshinweise
In der Originalverpackung, nicht über 25 °C und ausser Reichweite von Kindern aufbewahren.
Hinweise für die Handhabung
Wie bei den Zytostatika ist auch bei der Handhabung und Entsorgung von Imnovid besondere Vorsicht geboten (siehe auch "Dosierung/Anwendung" ).
Medizinisches Fachpersonal und Pflegekräfte, welche Pomalidomid handhaben, sollen Schutzhandschuhe tragen.
Die Kapseln dürfen weder geöffnet noch zerstossen werden. Falls Pomalidomid-Pulver mit der Haut in Kontakt kommt, ist die Haut sofort und gründlich mit Wasser und Seife zu waschen. Falls Pomalidomid mit Schleimhäuten in Kontakt kommt, ist gründlich mit Wasser zu spülen.
Zulassungsnummer61249 (Swissmedic)
PackungenImnovid 1 mg: 14 oder 21 Hartkapseln (A)
Imnovid 2 mg: 14 oder 21 Hartkapseln (A)
Imnovid 3 mg: 14 oder 21 Hartkapseln (A)
Imnovid 4 mg: 14 oder 21 Hartkapseln (A)
ZulassungsinhaberinBristol-Myers Squibb SA, Steinhausen
Stand der InformationFebruar 2023
|


