Eigenschaften/WirkungenATC-Code
R03AL04
Wirkungsmechanismus
Ultibro Breezhaler
Aufgrund des unterschiedlichen Wirkmechanismus von Indacaterol und Glycopyrronium, der auf jeweils andere Rezeptoren und Signalwege abzielt, um eine Relaxierung kleiner Muskeln zu erreichen, addiert sich die Wirksamkeit dieser beiden Substanzen, wenn sie in Form von Ultibro Breezhaler zusammen verabreicht werden.
Indacaterol
Indacaterol ist ein "ultra" -langwirkender beta2-adrenerger Agonist zur einmal täglichen Anwendung. Die pharmakologische Auswirkung von beta2-Adrenozeptor-Agonisten, einschliesslich Indacaterol, lassen sich zumindest teilweise auf die Stimulation der intrazellulären Adenylzyklase zurückweisen, das Enzym, das die Umwandlung von Adenosintriphosphat (ATP) zu zyklischem 3', 5'-Adenosinmonophosphat (zyklisches Monophosphat) katalysiert. Eine erhöhte Konzentration an zyklischem AMP bewirkt eine Relaxierung der glatten Muskulatur in den Bronchien.
Bei Inhalation wirkt Indacaterol lokal in der Lunge als Bronchodilatator. Im isolierten humanen Bronchus setzt die Wirkung von Indacaterol rasch ein und hält lange an.
Zwar sind beta2-adrenerge Rezeptoren die vorherrschenden adrenergen Rezeptoren im bronchialen Glattmuskel, während es im menschlichen Herzen vorwiegend Beta1-adrenerge Rezeptoren sind; dennoch sind auch im Herzen beta2-adrenerge Rezeptoren zu finden und machen dort 10% bis 50% aller adrenergen Rezeptoren aus. Die genaue Funktion der beta2-adrenergen Rezeptoren im Herzen ist nicht bekannt, ihr Vorhandensein lässt jedoch die Vermutung zu, dass selbst hoch selektive beta2-adrenerge Agonisten Auswirkungen auf das Herz haben.
Glycopyrronium
Glycopyrronium ist ein inhalativer langwirkender Antagonist muskarinischer Rezeptoren (anti-cholinerg wirkend) zur einmal täglichen bronchodilatatorischen Erhaltungstherapie bei COPD. Parasympathische Nerven sind die wichtigsten bronchokonstriktiven neuralen Leitungswege in den Atemwegen und der cholinerge Tonus ist die zentrale reversible Komponente der Atemwegsobstruktion bei COPD. Die Wirkung von Glycopyrronium beruht auf der Blockade der bronchokonstriktorischen Wirkung von Acetylcholin auf die Glattmuskelzellen der Atemwege, sodass die Atemwege aufgeweitet werden.
Von den fünf bekannten Subtypen muskarinischer Rezeptoren (M1-5) haben lediglich die Subtypen M1-3 eine definierte physiologische Funktion in der menschlichen Lunge. Glycopyrroniumbromid ist ein hochaffiner Antagonist dieser drei Subtypen muskarinischer Rezeptoren. In kompetitiven Bindungsstudien zeigte die Substanz 4- bis 5-mal höhere Selektivität für die menschlichen M3- und M1- als für menschliche M2-Rezeptoren. Die Wirkung von Glycopyrroniumbromid setzt rasch ein, wie sich an den kinetischen Parametern der Rezeptorassoziation/-dissoziation und dem Wirkeintritt nach der Inhalation in klinischen Studien zeigte.
Die lange Wirkdauer lässt sich wahrscheinlich teilweise auf die anhaltende Wirkstoffkonzentration in der Lunge zurückführen, worauf die verlängerte terminalen Eliminationshalbwertszeit von Glycopyrronium nach Inhalation mit dem Glycopyrronium-Inhalator im Vergleich zur Halbwertszeit nach intravenöser Verabreichung hinweist (siehe "Pharmakokinetik" ).
Pharmakodynamik
Primärer pharmakodynamischer Effekt
Die Wirkung der Kombination von Indacaterol und Glycopyrronium in Ultibro Breezhaler setzte rasch, d.h. innerhalb von 5 Minuten nach der Dosierung, ein. Der Effekt blieb im gesamten Dosierungsintervall von 24 Stunden konstant.
Seriellen FEV1-Messungen über 24 Stunden zufolge betrug der mittlere bronchodilatatorische Effekt nach 26 Behandlungswochen im Placebovergleich 0.32 Liter. Der Effekt war bei Ultibro Breezhaler signifikant stärker als bei alleiniger Anwendung von Indacaterol, Glycopyrronium oder Tiotropium, unverblindet (Unterschied bei jedem Vergleich: 0.11 Liter), (Teilgruppe mit Durchführung einer seriellen Spirometrie).
Weder im Placebovergleich noch im Vergleich zu den Monotherapien mit den jeweiligen Einzelverbindungen ergeben sich Hinweise auf eine zeitabhängige Tachyphylaxie des Effekts von Ultibro Breezhaler.
Sekundäre pharmakodynamische Effekte
Die systemischen Nebenwirkungen inhalativer beta2-adrenerger Agonisten und inhalativer Antagonisten muskarinischer Rezeptoren resultieren aus einer Aktivierung systemischer beta2-adrenerger Rezeptoren und einer Blockade muskarinischer Rezeptoren nach systemischer Absorption der Wirkstoffe. Das Nebenwirkungsprofil von Ultibro Breezhaler wurde sowohl bei gesunden Probanden als auch bei COPD-Patienten untersucht.
Auswirkungen auf die Herzfrequenz
Die Auswirkungen auf die Herzfrequenz wurden bei gesunden Freiwilligen nach Gabe einer Einzeldosis von Ultibro Breezhaler 440/200 µg, die in vier Dosisstufen in Abständen von jeweils einer Stunde verabreicht wurde, untersucht und mit den Auswirkungen nach Gabe eines Placebo, 600 µg Indacaterol und 200 µg Glycopyrronium und 200 µg Salmeterol verglichen.
Die stärkste zeitangepasste Beschleunigung der Herzfrequenz bei Anwendung von Ultibro Breezhaler im Vergleich zum Placebo betrug +5.69 Schläge/Minute, die stärkste Verlangsamung betrug -2.51 Schläge/Minute. Insgesamt wurden, was die Herzfrequenz anbelangte, keine einheitlichen pharmakodynamischen Auswirkungen von Ultibro Breezhaler festgestellt.
Die Auswirkungen supratherapeutischer Dosisstufen auf die Herzfrequenz wurden bei COPD-Patienten mit Ultibro Breezhaler -Dosen von bis zu 150/100, 300/100 und 600/100 µg untersucht. Ultibro Breezhaler hatte keine relevanten Auswirkungen auf die Herzfrequenz nach 30 Min., 4 Std. und 24 Std. sowie auf die über 24 Stunden gemittelte Herzfrequenz.
QT-Intervall
Eine eingehende QT (TQT)-Studie bei gesunden Freiwilligen, die Indacaterol in Dosen von bis zu 600 µg inhalierten, ergab keinen klinisch relevanten Effekt auf das QT-Intervall. Auch was Glycopyrronium anbelangt, wurde nach Inhalation von 400 µg in einer TQT-Studie keine Verlängerung des QT-Intervalls gemessen.
Die Auswirkungen von Ultibro Breezhaler auf das QTc-Intervall wurden bei gesunden Freiwilligen nach Inhalation von 440/200 µg Ultibro Breezhaler in vier, im Abstand von jeweils einer Stunde angewendeten Dosisstufen untersucht. Die grösste zeitangepasste Differenz zum Placebo betrug 4.62 ms (90%-KI 0.40, 8.85 ms), die grösste zeitangepasste Verringerung betrug -2.71 ms (90%-KI -6.97, 1.54 ms), was darauf hindeutet, dass auch Ultibro Breezhaler keine relevante Auswirkung auf das QT-Intervall hat, wie ausgehend von den Eigenschaften seiner Bestandteile zu erwarten war.
Die Verabreichung supratherapeutischer Dosen zwischen 150 µg/100 µg und 600 µg/100 µg Ultibro Breezhaler führte bei COPD Patienten zu einem grösseren höheren Anteil an Patienten mit QTcF Verlängerungen zwischen 30 ms und 60 ms verglichen mit dem Wert zu Studienbeginn (von 16.0% bis 21.6% reichend, gegenüber 1.9% für das Placebo). Es wurden aber keine Verlängerungen des QTcF Intervalls >60 ms im Vergleich zum Wert bei Studienbeginn erfasst. Die höchste Dosierungsstufe von 600 µg/100 µg Ultibro Breezhaler zeigte auch den höchsten Anteil an absoluten QTcF Werten von >450 ms (12.2% gegenüber 5.7% für das Placebo).
Serumkalium und Blutzucker
Bei gesunden Freiwilligen waren die Auswirkungen auf den Serumkaliumspiegel bei Anwendung von 440/200 µg Ultibro Breezhaler sehr gering (maximale Differenz −0.14 mmol/l im Vergleich zum Placebo). Der Blutzuckerspiegel änderte sich maximal um 0.67 mmol/l. Im Vergleich zwischen 440/200 µg Ultibro Breezhaler und 200 µg Salmeterol waren die Auswirkungen auf den Serumkaliumspiegel (maximale Differenz: 0.21 mmol/l) und den Blutzuckerspiegel kleiner (maximale Differenz: 0.21 bzw. 1.19 mmol/l).
Klinische Wirksamkeit
Das klinische Phase-III-Entwicklungsprogramm für Ultibro Breezhaler [IGNITE] umfasste sechs Studien, in welchen insgesamt über 8'000 Patienten teilnahmen: eine 26-wöchige placebo- und verumkontrollierte (150 µg Indacaterol einmal täglich, 50 µg Glycopyrronium einmal täglich, 18 µg Tiotropium, unverblindet, einmal täglich) Studie [SHINE]; eine 26-wöchige verumkontrollierte (500/50 µg Salmeterol/Fluticason zweimal täglich) Studie [ILLUMINATE]; eine 64-wöchige verumkontrollierte (50 µg Glycopyrronium einmal täglich, 18 µg Tiotropium, unverblindet, einmal täglich) Studie [SPARK]; eine 52-wöchige placebokontrollierte Studie [ENLIGHTEN],eine dreiwöchige, placebo- und verumkontrollierte (Tiotropium, unverblindet, einmal täglich) Belastbarkeitsstudie [BRIGHT] sowie eine 52-wöchige aktiv kontrollierte (Salmeterol/Fluticason 500/50 µg zweimal täglich) Studie [FLAME].
Bei den Teilnehmern handelte es sich um Patienten mit klinischer Diagnose einer moderaten bis sehr schweren COPD im Alter von mindestens 40 Jahren und mit einer Raucheranamnese von mindestens 10 Packungsjahren.
Von diesen 5 Studien hatten die Probanden in [SHINE] und [ENLIGHTEN] ein post-bronchodilatatorisches FEV1 von <80% und ≥30% des vorhergesagten Normalwerts und ein post-bronchodilatatorisches FEV1/FVC-Verhältnis von unter 70%. An der 26-wöchigen verumkontrollierten Studie [ILLUMINATE] nahmen Patienten mit einem post-bronchodilatatorischen FEV1 von <80% und ≥40% des vorhergesagten Normalwerts ohne moderate oder schwerwiegende Exazerbationen innerhalb von 12 Monaten vor Studienbeginn teil. An der 64-wöchigen Studie [SPARK] nahmen dagegen Patienten mit schwerer bis sehr schwerer COPD und einer medizinischen Vorgeschichte von ≥1 moderater bis schwerer COPD Exazerbation im vergangenen Jahr sowie einem post-bronchodilatatorischen FEV1 von <50% des vorhergesagten Normalwerts teil. An der 52-wöchigen aktiv kontrollierten Studie, [FLAME], nahmen Patienten mit moderater bis sehr schwerer COPD und einer medizinischen Vorgeschichte von ≥1 moderater bis schwerer COPD Exazerbation (19% mit einer medizinischen Vorgeschichte von ≥2 Exazerbationen) im vergangenen Jahr sowie einem post-bronchodilatatorischen FEV1 von ≥25 und <60% des vorhergesagten Normalwerts teil.
Auswirkungen auf die Lungenfunktion
Bei Verabreichung von 110/50 µg Ultibro Breezhaler einmal täglich ergaben sich klinisch bedeutsame Verbesserungen der Lungenfunktion (gemessen anhand der Einsekundenkapazität ( "Forced Expiratory Volume" in einer Sekunde bzw. FEV1). In den Phase-III-Studien trat die bronchodilatatorische Wirkung innerhalb von 5 Minuten nach der ersten Dosis ein und blieb während des anschliessenden 24-Stunden-Dosierungsintervalls erhalten. In der 26-wöchigen Studie [SHINE] und der 52-wöchigen Studie [ENLIGHTEN] wurde keine zeitabhängige Abschwächung der bronchodilatatorischen Wirkung festgestellt.
Trough-FEV1
In der Studie [SHINE] war am primären Endpunkt nach 26 Wochen das Trough-FEV1 nach Dosisgabe im Placebovergleich um 200 ml erhöht (p<0.001). Die Erhöhung war im Vergleich zu jedem der Arme, in denen einer der Bestandteile (Indacaterol und Glycopyrronium) als Monotherapie angewendet wurde, sowie im Vergleich zu einem unverblindeten Tiotropium-Arm, signifikant (siehe Tabelle 1).
Tabelle 1: Trough-FEV1 nach Dosisgabe (Methode der Kleinstquadratmittelwerte, "Least Squares Mean" ) an Tag 1 und in Woche 26 (primärer Endpunkt)
Behandlungsunterschied Tag 1 Woche 26
ULTIBRO BREEZHALER - Placebo 190 ml (p<0.001) 200 ml (p<0.001)
ULTIBRO BREEZHALER - Indacaterol 80 ml (p<0.001) 70 ml (p<0.001)
ULTIBRO BREEZHALER - Glycopyrronium 80 ml (p<0.001) 90 ml (p<0.001)
ULTIBRO BREEZHALER – Tiotropium, unverblindet 80 ml (p<0.001) 80 ml (p<0.001)
Das mittlere FEV1 vor Dosisgabe (Durchschnitt der -45 Min. und -15 Min. vor der morgendlichen Dosis des Studienpräparats gemessenen Werte) war in Woche 26 verglichen mit Salmeterol/Fluticason (100 ml, p<0.001) [ILLUMINATE], in Woche 52 verglichen mit Placebo (189 ml, p<0.001) [ENLIGHTEN] und bei allen Visiten bis Woche 64 verglichen mit Glycopyrronium (70-80 ml, p-Wert <0.001) und Tiotropium, unverblindet, (60-80 ml, p-Wert <0.001) [SPARK] klinisch bedeutsam und zugunsten von Ultibro Breezhaler statistisch signifikant.
In der [FLAME] Studie war das mittlere FEV1 vor Dosisgabe verglichen mit Salmeterol/Fluticason während der doppelblinden Behandlung ü bei allen Visiten bis Woche 52 klinisch bedeutsam und zugunsten von Ultibro Breezhaler erhöht(62-86 ml).
FEV1-AUC
In der verumkontrollierten Studie [ILLUMINATE] bewirkte Ultibro Breezhaler nach 26 Wochen verglichen mit Salmeterol/Fluticason eine Erhöhung des FEV1-AUC(0-12h) nach Dosisgabe (primärer Endpunkt) um 140 ml (p<0.001)
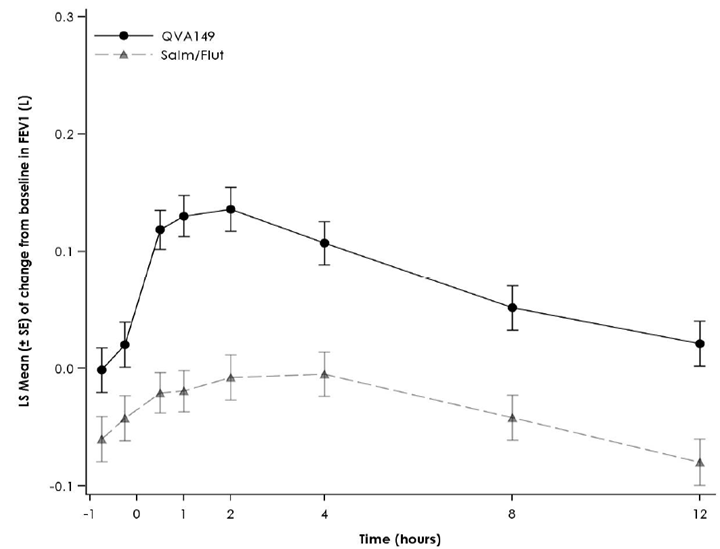
In der [FLAME] Studie wurde bei einer Subgruppe eine serielle Spirometrie durchgeführt. Bei dieser Subgruppe bewirkte Ultibro Breezhaler eine Verbesserung des FEV1 AUC0-12h von 110 ml nach 52 Behandlungswochen. Die Gruppe, die Ultibro Breezhaler erhielt, war der Salmeterol/Fluticason Gruppe von Tag 1 überlegen.
Abbildung 1: Profil der Änderung des Kleinstquadratmittelwerts, "Least Squares Mean" , des FEV1 (L) -45 min bis 12 h zu Behandlungsbeginn, in Woche 12, in Woche 26 und in Woche 52 (serielle Spirometrie der Subgruppe)
Woche 12

Woche 26

Woche 52
Symptomatische Behandlungsergebnisse
Atmungsbeschwerden
Ultibro Breezhaler bewirkte eine signifikante Reduzierung der Atmungsbeschwerden (gemessen anhand des Transitional Dyspnea Index bzw. TDI). Insbesondere führte die Anwendung von Ultibro Breezhaler zu einer klinisch bedeutsamen und statistisch signifikanten Verbesserung des fokalen TDI-Scores in Woche 26, verglichen mit Placebo (1.09, p<0.001), Tiotropium, unverblindet (0.51, p=0.007) [SHINE] und Salmeterol/Fluticason (0.76, p=0.003) [ILLUMINATE].
Unter Anwendung von Ultibro Breezhaler reagierte ein signifikant höherer Anteil der Patienten als in der Placebogruppe in Woche 26 mit einer Verbesserung des fokalen TDI um mindestens einen Punkt (68.1% bzw. 57.5%, p=0.004). Darüber hinaus zeigte unter Ultibro Breezhaler ein höherer Anteil an Patienten in Woche 26 ein klinisch bedeutsames Ansprechen als bei Anwendung von Tiotropium, unverblindet (68.1% Ultibro Breezhaler vs. 59.2% Tiotropium, p=0.016) und Salmeterol/Fluticason (65.1% Ultibro Breezhaler vs. 55.5% Salmeterol/Fluticason, p=0.088) [ILLUMINATE].
Gesundheitsbezogene Lebensqualität
Die einmal tägliche Anwendung von Ultibro Breezhaler hatte überdies statistisch signifikante Auswirkungen auf die gesundheitsbezogene Lebensqualität, wie anhand des SGRQ (St. George's Respiratory Questionnaire) gemessen wurde und wie sich an einer Reduzierung des SGRQ-Gesamtscores in Woche 26 im Vergleich zum Placebo (-3.01, p=0.002) zeigte. In [FLAME] zeigte Ultribro Breezhaler im Vergleich zu Salmeterol/Fluticason eine Reduzierung SGRQ-Gesamtscores in Woche 52 (-1.3).
Von den mit Ultibro Breezhaler behandelten Patienten reagierte ein höherer Anteil mit einer klinisch bedeutsamen Verbesserung des SGRQ-Scores (definiert als Reduzierung des Ausgangsscores um mindestens 4 Einheiten), wie in Woche 26 verglichen mit dem Placebo (63.7% bzw. 56.6%, p=0.088). In [FLAME] zeigte Ultibro Breezhaler verglichen mit Salmeterol/Fluticason eine klinisch bedeutsame Verbesserung des SGRQ-Scores in Woche 52 (49.2% Ultibro Breezhaler vs. 43.7% Salmeterol/Fluticason, ODER: 1.30) [FLAME].
Alltagsaktivitäten
Ultibro Breezhaler bewirkte über 26 Wochen hinsichtlich des prozentualen Anteils der "Tage, an denen es möglich war, den üblichen Alltagsaktivitäten nachzugehen" (8.45%, p<0.001) eine zahlenmässige Verbesserung verglichen mit Glycopyrronium (1.87; p=0.195).
COPD-Exazerbationen
In der Studie [SPARK] reduzierte Ultibro Breezhaler bei einmal täglicher Anwendung über 64 Wochen die Rate der moderaten oder schweren COPD-Exazerbationen verglichen mit Glycopyrronium um 12% (p=0.038).
Ultibro Breezhaler reduzierte die Rate aller COPD-Exazerbationen (leicht, moderat und schwer) verglichen mit Glycopyrronium um 15% (p=0.001).
Was die Zeit bis zur ersten moderaten oder schweren COPD-Exazerbation anbelangte, so bewirkte Ultibro Breezhaler verglichen mit Glycopyrronium eine Reduzierung des Risikos um 7% (p=0.319).
Die 52-wöchige aktiv kontrollierte Studie [FLAME], in welcher die Patienten einmal täglich Ultibro Breezhaler erhielten, erreichte ihr Primärziel der Nicht-Unterlegenheit für alle COPD Exazerbation (leichte, moderate oder schwere) verglichen mit Salmeterol/Fluticason. Unter Ultibro Breezhaler war die Jahresrate aller Exazerbationen (leicht, moderat und schwer) um 11% tiefer als unter Salmeterol/Fluticason (3.59 vs. 4.03, p=0.003) und die Zeit bis zur ersten Exazerbation dauerte war 16% länger (mediane Zeit: 71 Tage für Ultibro Breezhaler vs. 51 Tage für Salmeterol/Fluticason.).
Die Jahresrate moderater oder schwerer Exazerbationen war unter Ultibro Breezhaler um 17% tiefer als unter Salmeterol/Fluticason (0.98 vs. 1.19) und verzögerte die Zeit bis zur ersten moderaten oder schweren Exazerbation mit einer Reduktion des Exazerbationsrisikos um 22% (25. Perzentil: 127 Tage für Ultibro Breezhaler vs. 87 Tage für Salmeterol/Fluticason, p<0.001). Weniger als 50% der Patienten in der Gruppe, die mit Ultibro Breezhaler behandelt wurden, erlitten eine Exazerbation. Aus diesem Grund wurde stattdessen die Zeit bis zur ersten moderaten oder schweren COPD-Exazerbation für das erste Quartil der Patienten errechnet.
Ultibro Breezhaler bewirkte eine tendenzielle Verringerung der Jahresrate schwerer Exazerbationen verglichen mit Salmeterol/Fluticason (0.15 vs. 0.17). Ultibro Breezhaler verzögerte die Zeit bis zur ersten schweren Exazerbation mit einer Reduktion des Exazerbationsrisikos um 19%.
Die Inzidenz der Pneumonien (radiologisch bestätigt wie z.B. Thorax-Röntgenuntersuchung oder CT-Scan) lag bei 3.2% im Studienarm mit Ultibro Breezhaler im Vergleich zu 4.8% im Studienarm mit Salmeterol/Fluticason. Die Zeit bis zum Auftreten der ersten Pneumonie wurde durch Ultibro Breezhaler im Vergleich zu Salmeterol/Fluticason verzögert.
Anwendung von Notfallmedikamenten
Ultibro Breezhaler einmal täglich erreichte über 26 Wochen in der Studie [SHINE] einen signifikanten Rückgang der Anwendung von Notfallmedikamenten (Salbutamol) um 0.96 Hübe pro Tag (p<0.001) verglichen mit dem Placebo und um 0.54 Hübe pro Tag (p<0.001) verglichen mit Tiotropium, unverblindet, sowie in der Studie [ILLUMINATE] um 0.39 Hübe pro Tag (p=0.019) verglichen mit Salmeterol/Fluticason.
In der Studie [SPARK] reduzierte Ultibro Breezhaler im Lauf von 64 Wochen die Anwendung von Notfallmedikamenten (Salbutamol) um 0.76 Hübe pro Tag (p<0.001) verglichen mit Tiotropium, unverblindet.
Im Verlauf von 52 Wochen reduzierte die Anwendung von Ultibro Breezhaler einmal täglich im Vergleich zum Behandlungsbeginn den Bedarf an Notfallmedikation um 1.01 Sprühstösse pro Tag, während Salmeterol/Fluticason den Bedarf im Vergleich zum Behandlungsbeginn um 0.76 Sprühstösse pro Tag reduzierte
Belastungstoleranz
In der 3-wöchigen Studie [BRIGHT] zur Prüfung der Belastungstoleranz mittels Radergometrie bei submaximaler (75%) Belastung (submaximaler Belastungstoleranztest) reduzierte Ultibro Breezhaler bei morgendlicher Dosierung ab der ersten Dosis die dynamische Hyperinflation und verbesserte die Ausdauer. Bereits am ersten Behandlungstag war die Inspirationskapazität unter Belastung im Placebovergleich signifikant verbessert (250 ml, p<0.001). Verglichen mit dem Placebo hatte sich die Inspirationskapazität mit Ultibro Breezhaler nach drei Behandlungswochen weiter verbessert (320 ml, p<0.001) und die Ausdauer weiter erhöht (Belastungsdauer 59.5 Sekunden, p=0.006).
|



