Eigenschaften/WirkungenATC-Code
A10BJ06
Wirkungsmechanismus
Semaglutide ist ein GLP-1-Analogon des an der Regulation der Glukosehomöostase beteiligten humanen Peptids GLP-1. Aufgrund seiner ausgeprägten Albuminbindung verzögert sich die renale Clearance von Semaglutide. Ausserdem ist Semaglutide aufgrund seiner gegenüber dem nativen GLP-1 modifizierten Struktur unempfindlichen gegenüber dem Abbau durch DPP-4.
Semaglutide wirkt als ein Agonist am Zielrezeptor für natives GLP-1. GLP-1-Rezeptoren sind im Pankreas, im Gehirn, im Herzen, im Gefässsystem, im Immunsystem und den Nieren exprimiert. Die Stimulation von GLP-1 Rezeptoren durch Semaglutide führt abhängig vom Blutzuckerspiegel zur Stimulation der Insulinsekretion und zur Hemmung der Glucagonsekretion. Zusätzlich kommt es zur Verzögerung der Magenentleerung in der frühen postprandialen Phase.
Semaglutide reduziert das Körpergewicht und die Körperfettmasse mittels einer verringerten Energieaufnahme. Der Mechanismus umfasst einen allgemein verminderten Appetit, der erhöhtes Sättigungs- und vermindertes Hungergefühl einschliesst. Die Insulinresistenz wird reduziert. Dies erfolgt vermutlich durch die Reduktion des Körpergewichts.
Der Wirkungsmechanismus von Semaglutide zur Reduktion des kardiovaskulären Risikos ist wahrscheinlich multifaktoriell und wird teilweise durch die Reduktion des HbA1c und die Wirkungen auf bekannte kardiovaskulär-renal-metabolische Risikofaktoren vermittelt, einschliesslich der Senkung des Blutdrucks und des Körpergewichts, Verbesserungen des Lipidprofils und der Nierenfunktion sowie entzündungshemmender Effekte, gezeigt durch die Senkung des hsCRP. Der exakte Mechanismus zur Reduktion des kardiovaskulären Risikos wurde nicht geklärt.
Pharmakodynamik
Rybelsus senkt den Nüchternblutzucker sowie den selbstgemessenen Blutzuckerspiegel. Die Wirkung setzt frühzeitig ein, wobei bei Patienten mit Typ 2 Diabetes mellitus eine Senkung des NBZ (Nüchternblutzucker) in der ersten Woche eintritt.
Alle pharmakodynamischen Untersuchungen wurden nach 12 Behandlungswochen (einschliesslich der Dosiseskalierung) im Steady State mit 1 mg Semaglutide Injektionen einmal wöchentlich durchgeführt.
Nüchternblutzucker und postprandiale Anstiege
Semaglutide reduziert den Nüchternblutzucker und den postprandialen Blutzucker. Bei Patienten mit Typ 2 Diabetes mellitus führte die Behandlung mit Semaglutide zur Verringerung des Blutzuckerspiegels, sowohl hinsichtlich auf absolute Veränderung gegenüber dem Ausgangswert als auch relative Verringerung im Vergleich zum Placebo in Bezug auf Nüchternblutzucker (1.6 mmol/l/29 mg/dl; 22 %), postprandialen Blutzucker nach 2 Stunden (4.1 mmol/l/74 mg/dl; 37 %), mittleren 24-Stunden-Blutzuckerspiegel (1.7 mmol/l/30 mg/dl; Verminderung um 22 %) und postprandiale Blutzuckerexkusionen über 3 Mahlzeiten (0.6–1.1 mmol/l/11–20 mg/dl) im Vergleich zum Placebo.
Betazellfunktion und Insulinsekretion
Semaglutide verbessert die Betazellfunktion. Im Vergleich zu Placebo verbesserte Semaglutide die Erst- und Zweitphasen-Insulinantwort um das 3- bzw. 2-fache und erhöhte die maximale sekretorische Kapazität der Betazellen nach einem Arginin-Stimulationstest bei Patienten mit Typ 2 Diabetes mellitus. Darüber hinaus erhöhte die Behandlung mit Semaglutide die Nüchtern-Insulinkonzentrationen im Vergleich zum Placebo.
Glucagonsekretion
Semaglutide senkt die Nüchtern- und die postprandialen Glucagon-Konzentrationen. Bei Patienten mit Typ 2 Diabetes mellitus führte Semaglutide zu der folgenden relativen Verringerung von Glucagon im Vergleich zum Placebo: Nüchtern-Glucagon (8–21 %), postprandiale Glucagon-Antwort (14–15 %) und mittlerer 24-Stunden-Glucagonspiegel (12 %).
Glucoseabhängige Insulin- und Glucagonsekretion
Semaglutide senkte die hohen Blutzuckerspiegel durch die glukoseabhängige Stimulation der Insulinsekretion und Hemmung der Glucagonsekretion. Mit Semaglutide war die Insulinsekretionsrate bei Patienten mit Typ 2 Diabetes mellitus vergleichbar mit der der gesunden Probanden.
Während einer induzierten Hypoglykämie veränderte Semaglutide im Vergleich zu Placebo die gegenregulatorischen Reaktionen auf den erhöhten Glucagonspiegel und verringerte die Senkung des C-Peptids bei Patienten mit Typ 2 Diabetes mellitus nicht.
Magenentleerung
Semaglutide bewirkte eine geringe Verzögerung der frühen postprandialen Magenentleerung und verminderte dadurch die Glukoserate, die postprandial in den Kreislauf gelangt.
Körpergewicht und -zusammensetzung
Mit Rybelsus wurde eine grössere Gewichtsreduktion erzielt als mit den Vergleichspräparaten (Placebo, Sitagliptin, Empagliflozin und Liraglutide). Der Gewichtsverlust war vorwiegend auf den Verlust von Fettgewebe zurückzuführen, mit einem Verlust an Fettmasse, die dreimal so gross war wie der Verlust an Muskelmasse.
Appetit, Energieaufnahme und Auswahl von Lebensmitteln
Im Vergleich zu Placebo reduzierte Semaglutide die Energiezufuhr aus 3 aufeinanderfolgenden ad libitum Mahlzeiten um 18–35 %. Dies wurde durch eine durch Semaglutide induzierte Unterdrückung des Appetits im nüchternen Zustand sowie durch eine postprandiale, verbesserte Kontrolle des Essens, weniger Hunger und eine relativ geringe Präferenz für fettreiche Nahrung bewirkt.
Nüchternblutfette und postprandiale Blutfette
Semaglutide verringerte im Vergleich zu Placebo die Nüchterntriglyzerid- und die VLDL-Cholesterine (Lipoproteine sehr niedriger Dichte) Konzentration um jeweils 12 % bzw. 21 %. Die postprandiale Triglyzerid- und VLDL-Cholesterinantwort nach einer sehr fettreichen Mahlzeit waren um >40 % verringert.
Kardiale Elektrophysiologie (QTc)
Die Auswirkung von Semaglutide auf die kardiale Repolarisation wurde in einer umfassenden QTc-Studie untersucht. Bei einem durchschnittlichen Expositionsniveau, das die maximal empfohlene Dosis von Rybelsus um das 4-Fache überschritt, verlängerte Semaglutide die QTc-Intervalle in keinem klinisch relevanten Masse.
Klinische Wirksamkeit
Die Wirksamkeit und Sicherheit von Rybelsus wurden in acht globalen randomisierten, kontrollierten Phase-3a-Studien untersucht. Das primäre Ziel von sieben Studien war die Beurteilung der glykämischen Wirksamkeit, während das primäre Ziel einer weiteren Studie die Beurteilung der kardiovaskulären Sicherheit war.
Die Phase-3a-Studien umfassten 8'842 randomisierte Patienten mit Typ 2 Diabetes mellitus (5'169 wurden mit Rybelsus behandelt), einschliesslich 1'162 Patienten mit moderater Nierenfunktionsstörung. Die Wirksamkeit von Rybelsus wurde mit Placebo, Empagliflozin, Sitagliptin, Liraglutide und Dulaglutid verglichen.
In allen Studien führte die Behandlung mit Rybelsus zu einer klinisch signifikanten Verbesserung des HbA1c, des Nüchternblutzuckers (NBZ) und des Körpergewichts. Diese Wirkungen wurden bis zu einer Studiendauer von 78 Wochen beibehalten.
Eine Phase-3b, kardiovaskuläre Ergebnisstudie (SOUL) mit 9650 Patienten wurde durchgeführt, um zu zeigen, dass orales Semaglutide im Vergleich zu Placebo in Ergänzung zur Standardbehandlung das Risiko für schwerwiegende kardiovaskuläre Ereignisse (MACE) bei Patienten mit Diabetes mellitus Typ 2 und etablierter kardiovaskulärer Erkrankung und/oder chronischer Nierenerkrankung senkt.
Die Wirksamkeit von Rybelsus wurde durch Alter, Geschlecht, Rasse, ethnische Zugehörigkeit, Körpergewicht, BMI, Diabetes-Dauer, Erkrankungen des oberen Gastrointestinaltrakts und Nierenfunktion zu Beginn der Studie nicht beeinflusst.
PIONEER 1 – Monotherapie
In einer 26-wöchigen Doppelblindstudie wurden 703 Patienten mit Typ 2 Diabetes, die durch Diät und Bewegung unzureichend kontrolliert waren, auf Rybelsus 3 mg, Rybelsus 7 mg, Rybelsus 14 mg oder Placebo einmal täglich randomisiert.
Tabelle 2: Ergebnisse einer 26-wöchigen Monotherapie-Studie (PIONEER 1) in der Rybelsus mit Placebo verglichen wurde
Rybelsus7 mg Rybelsus14 mg Placebo
Population (N)1 175 175 178
HbA1c (%)
Ausgangswert2 8.0 8.0 7.9
Änderung gegenüber dem -1.3 -1.5 -0.1
Ausgangswert in Woche 263
Unterschied gegenüber Placebo3 -1.2 [-1.5; -1.0]§ -1.4 [-1.7; -1.2]§ -
[95 %-KI]
Patienten (%), die einen HbA1c 72# 80# 34
<7.0 % erreichten2
Körpergewicht (kg)
Ausgangswert2 89.0 88.1 88.6
Änderung gegenüber dem -2.5 -4.1 -1.5
Ausgangswert in Woche 263
Unterschied gegenüber Placebo3 -1.0 [-1.8; -0.2]§ -2.6 [-3.4; -1.8]§ -
[95 %-KI]
1 Full Analysis Set: Alle
randomisierten Patienten 2
Beobachtetes Mittel/Anteil 3
Geschätzt mit einem gemischten
Modell für wiederholte Messungen,
angepasst an Basiswert,
Hintergrundmedikation und Region.
Daten, die nach Absetzen des
Versuchsprodukts oder Beginn der
Notfallmedikation erfasst wurden,
sind ausgeschlossen. §
Statistisch signifikant (p<0.05)
# Die Wahrscheinlichkeit, das
Ziel zu erreichen, war mit
Rybelsus statistisch signifikant
grösser als mit Placebo (p<0.05)
PIONEER 2 – Rybelsus vs. Empagliflozin, beide in Kombination mit Metformin
In einer 52-wöchigen offenen Studie wurden 822 Patienten mit Typ 2 Diabetes mellitus zu Rybelsus 14 mg einmal täglich oder Empagliflozin 25 mg einmal täglich, beide in Kombination mit Metformin, randomisiert.
Die Behandlung mit Rybelsus 14 mg einmal täglich reduzierte das HbA1c um -1.4 %-Punkte in Woche 26. Die Reduktion war statistisch signifikant grösser als mit Empagliflozin, mit einem geschätzten Behandlungsunterschied von -0.5 %-Punkten [-0.7; -0.4]95 %-KI.
Tabelle 3: Ergebnisse einer 52-wöchigen Studie, in der Rybelsus mit Empagliflozin verglichen wurde (PIONEER 2)
Rybelsus14 mg Empagliflozin25 mg
Population (N)1 411 410
HbA1c (%)
Ausgangswert2 8.1 8.1
Änderung gegenüber dem Ausgangswert in Woche 523 -1.3 -0.8
Unterschied gegenüber Empagliflozin3 [95 %-KI] -0.5 [-0.7; -0.4]§ -
Patienten (%), die einen HbA1c <7.0 % erreichten2 72# 48
Körpergewicht (kg)
Ausgangswert2 91.9 91.3
Änderung gegenüber dem Ausgangswert in Woche 523 -4.7 -3.8
Unterschied gegenüber Empagliflozin3 [95 %-KI] -0.9 [-1.6; -0.2]§ -
1 Full Analysis Set: Alle randomisierten Patienten 2
Beobachtetes Mittel/Anteil 3 Geschätzt mit einem
gemischten Modell für wiederholte Messungen, angepasst
an Basiswert, Hintergrundmedikation und Region. Daten,
die nach dem Absetzen des Prüfpräparates oder nach der
Aufnahme der Behandlung mit der Notfallmedikation
erfasst wurden, sind ausgeschlossen § Statistisch
signifikant (p<0.05) # Die Wahrscheinlichkeit, das Ziel
zu erreichen, war mit Rybelsus statistisch signifikant
grösser als mit Empagliflozin (p<0.05)
PIONEER 3 – Rybelsus vs. Sitagliptin, beide in Kombination mit Metformin oder Metformin mit einem Sulfonylharnstoff
In einer 78-wöchigen doppelblinden Double-Dummy-Studie wurden 1'864 Patienten mit Typ 2 Diabetes auf Rybelsus 3 mg, Rybelsus 7 mg, Rybelsus 14 mg oder Sitagliptin 100 mg einmal täglich randomisiert, alle in Kombination mit Metformin oder Metformin und Sulfonylharnstoff.
Die Behandlung mit Rybelsus 7 mg und 14 mg einmal täglich reduzierte das HbA1c um -1.1 %-Punkte bzw. -1.4 %-Punkte in Woche 26; die Reduktion war statistisch signifikant grösser als mit Sitagliptin, mit einem geschätzten Behandlungsunterschied von -0.3 %-Punkten [-0.4; -0.2]95 %-KI und -0.6 %-Punkten [-0.7; -0.5]95 %-KI.
Die Reduktion des HbA1c und des Körpergewichts hielt während der gesamten Studiendauer von 78 Wochen an (Tabelle 4).
Tabelle 4: Ergebnisse einer 78-wöchigen Studie, in der Rybelsus mit Sitagliptin verglichen wurde (PIONEER 3)
Rybelsus7 mg Rybelsus14 mg Sitagliptin100 mg
Population (N)1 465 465 467
HbA1c (%)
Ausgangswert2 8.4 8.3 8.3
Änderung gegenüber dem -0.7 -1.1 -0.4
Ausgangswert in Woche 783
Unterschied gegenüber -0.3 [-1.6; -0.2]§ -0.7 [-0.8; -0.5]§ -
Sitagliptin3 [95 %-KI]
Patienten (%), die einen HbA1c 50# 52# 39
<7.0 % erreichten2
Körpergewicht (kg)
Ausgangswert2 91.3 91.2 90.9
Änderung gegenüber dem -2.7 -3.5 -1.1
Ausgangswert in Woche 783
Unterschied gegenüber -1.6 [-2.2; -0.9]§ -2.4 [-3.0; -1.7]§ -
Sitagliptin3 [95 %-KI]
1 Full Analysis Set: Alle
randomisierten Patienten 2
Beobachtetes Mittel/Anteil 3
Geschätzt mit einem gemischten
Modell für wiederholte Messungen,
angepasst an Basiswert,
Hintergrundmedikation und Region.
Daten, die nach dem Absetzen des
Prüfpräparates oder nach der
Aufnahme der Behandlung mit der
Notfallmedikation erfasst wurden,
sind ausgeschlossen § Statistisch
signifikant (p<0.05) # Die
Wahrscheinlichkeit, das Ziel zu
erreichen, war mit Rybelsus
statistisch signifikant grösser
als mit Sitagliptin (p<0.05)
PIONEER 4 – Rybelsus vs. Liraglutide und Placebo, jeweils in Kombination mit Metformin oder Metformin und einem SGLT2-Inhibitor
In einer 52-wöchigen doppelblinden Double-Dummy-Studie wurden 711 Patienten mit Typ 2 Diabetes auf Rybelsus 14 mg, Liraglutide 1.8 mg s.c. oder Placebo einmal täglich randomisiert, jeweils in Kombination mit Metformin oder Metformin und einem SGLT2-Inhibitor.
Die Behandlung mit Rybelsus 14 mg einmal täglich reduzierte das HbA1c um -1.3 %-Punkte in Woche 26; die Reduktion war statistisch signifikant grösser als mit Placebo und Liraglutide, mit einem geschätzten Behandlungsunterschied von -1.2 %-Punkten [-1.4; -1.0]95 %-KI und -0.2 %-Punkten [-0.3; -0.1]95 %-KI.
Tabelle 5: Ergebnisse einer 52-wöchigen Studie, in der Rybelsus mit Liraglutide und Placebo verglichen wurde (PIONEER 4)
Rybelsus14 mg Liraglutide1.8 mg Placebo
Population (N)1 285 284 142
HbA1c (%)
Ausgangswert2 8.0 8.0 7.9
Änderung gegenüber dem -1.2 -0.9 0.2
Ausgangswert in Woche 523
Unterschied gegenüber Liraglutid3 -0.3 [-0.4; -0.1]§ - -
[95 %-KI]
Unterschied gegenüber Placebo3 -1.4 [-1.6; -1.2]§ - -
[95 %-KI]
Patienten (%), die einen HbA1c 69* 63 18
<7.0 % erreichten2
Körpergewicht (kg)
Ausgangswert2 92.9 95.5 93.2
Änderung gegenüber dem -5,0 -3,1 -1,2
Ausgangswert in Woche 523
Unterschied gegenüber Liraglutid3 -1.8 [-2.6; -1.0]§ - -
[95 %-KI]
Unterschied gegenüber Placebo3 -3.8 [-4.8; -2.7]§ - -
[95 %-KI]
1 Full Analysis Set: Alle
randomisierten Patienten 2
Beobachtetes Mittel/Anteil 3
Geschätzt mit einem gemischten
Modell für wiederholte Messungen,
angepasst an Basiswert,
Hintergrundmedikation und Region.
Daten, die nach dem Absetzen des
Prüfpräparates oder nach der
Aufnahme der Behandlung mit der
Notfallmedikation erfasst wurden,
sind ausgeschlossen § Statistisch
signifikant (p<0.05) # Die
Wahrscheinlichkeit, das Ziel zu
erreichen, war mit Rybelsus
statistisch signifikant grösser
als mit Liraglutid (p<0.05)
PIONEER 5 – Rybelsus vs. Placebo, beide in Kombination mit einem Basalinsulin alleine, Metformin und einem Basalinsulin oder Metformin und/oder einem Sulfonylharnstoff, bei Patienten mit moderater Nierenfunktionsstörung
In einer 26-wöchigen doppelblinden Studie wurden 324 Patienten mit Typ 2 Diabetes und moderater Nierenfunktionsstörung (eGFR 30-59 ml/min/1.73 m2), die auf einer stabilen antidiabetischen Therapie waren, zusätzlich auf Rybelsus 14 mg oder Placebo einmal täglich randomisiert.
Das Wirksamkeits- und Sicherheitsprofil von Rybelsus bei Patienten mit Typ 2 Diabetes und moderater Nierenfunktion entsprach dem allgemein für GLP-1 Rezeptoragonisten beschriebenen.
Tabelle 6: Ergebnisse einer 26-wöchigen Studie, in der Rybelsus bei Patienten mit Typ 2 Diabetes und moderater Nierenfunktionsstörung mit Placebo verglichen wurde (PIONEER 5)
Rybelsus14 mg Placebo
Population (N)1 163 161
HbA1c (%)
Ausgangswert2 8.0 7.9
Änderung gegenüber dem Ausgangswert in Woche 263 -1.1 -0.1
Unterschied gegenüber Placebo3 [95 %-KI] -1.0 [-1.2; -0.8]§ -
Patienten (%), die einen HbA1c <7.0 % erreichten2 64# 21
Körpergewicht (kg)
Ausgangswert2 91.3 90.4
Änderung gegenüber dem Ausgangswert in Woche 263 -3.7 -1.1
Unterschied gegenüber Placebo3 [95 %-KI] -2.7 [-3.5; -1.9]§ -
1 Full Analysis Set: Alle randomisierten Patienten 2
Beobachtetes Mittel/Anteil 3 Geschätzt mit einem
gemischten Modell für wiederholte Messungen, angepasst
an Basiswert, Hintergrundmedikation und Region. Daten,
die nach dem Absetzen des Prüfpräparates oder nach der
Aufnahme der Behandlung mit der Notfallmedikation
erfasst wurden, sind ausgeschlossen. § Statistisch
signifikant (p<0.05) # Die Wahrscheinlichkeit, das Ziel
zu erreichen, war mit Rybelsus statistisch signifikant
grösser als mit Placebo (p<0.05)
PIONEER 7 – Rybelsus vs. Sitagliptin, jeweils in Kombination mit Metformin, SGLT2-Inhibitoren, einem Sulfonylharnstoff oder Glitazon (flexible Dosisanpassungsstudie)
In einer 52-wöchigen, offenen Studie wurden 504 Patienten mit Typ 2 Diabetes zu Rybelsus (flexible Dosisanpassung mit 3 mg, 7 mg und 14 mg einmal täglich) oder Sitagliptin 100 mg einmal täglich, jeweils in Kombination mit 1-2 oralen blutzuckersenkenden Arzneimitteln (Metformin, SGLT2-Inhibitoren, Sulfonylharnstoff oder Glitazon) randomisiert. Die Dosis von Rybelsus wurde alle 8 Wochen basierend auf dem glykämischen Ansprechen des Patienten sowie der Verträglichkeit angepasst. Die Sitagliptin-Dosis von 100 mg war fix. Die Wirksamkeit und Sicherheit von Rybelsus wurden in der Woche 52 beurteilt.
In der Woche 52 lag der Anteil der Patienten, die mit Rybelsus 3 mg, 7 mg und 14 mg behandelt wurden bei 9 %, 30 % und 60 %.
Tabelle 7: Ergebnisse einer 52-wöchigen Studie zur flexiblen Dosisanpassung von Rybelsus im Vergleich zu Sitagliptin (PIONEER 7)
RybelsusFlexible Sitagliptin100 mg
Dosis
Population (N)1 253 251
HbA1c (%)
Ausgangswert2 8.3 8.3
Änderung gegenüber dem Ausgangswert in Woche 523 -1.4 -0.7
Unterschied gegenüber Sitagliptin3 [95 %-KI] -0.7 [-0.9; -0.5]§ -
Patienten (%), die einen HbA1c <7.0 % erreichten2 63# 28
Körpergewicht (kg) 88.9 88.4
Ausgangswert2 -2.9 -0.8
Änderung gegenüber dem Ausgangswert in Woche 523 -2.2 [-2.9; -1.5]§ -
Unterschied gegenüber Sitagliptin3 [95 %-KI] 28# 13
1 Full Analysis Set: Alle randomisierten Patienten 2
Beobachtetes Mittel/Anteil 3 Geschätzt mit einem
gemischten Modell für wiederholte Messungen, angepasst
an Basiswert, Hintergrundmedikation und Region.
Geschätzt mit einem gemischten Modell für wiederholte
Messungen, angepasst an Basiswert,
Hintergrundmedikation und Region § Statistisch
signifikant (p<0.05) # Die Wahrscheinlichkeit, das Ziel
zu erreichen, war mit Rybelsus statistisch signifikant
grösser als mit Sitagliptin (p<0.05)
PIONEER 8 – Rybelsus vs. Placebo, beide in Kombination mit Insulin mit oder ohne Metformin
In einer 52-wöchigen doppelblinden Studie wurden 731 Patienten mit unzureichend kontrolliertem Typ 2 Diabetes, die mit Insulin (Basalinsulin, Basal-/Bolusinsulin oder vorgemischtes Insulin) mit oder ohne Metformin behandelt wurden, zu Rybelsus 3 mg, Rybelsus 7 mg, Rybelsus 14 mg oder Placebo einmal täglich randomisiert.
Die Behandlung mit Rybelsus 7 mg und 14 mg einmal pro Tag reduzierte das HbA1c in der Woche 26 um jeweils -1.0 %-Punkte und -1.4 %-Punkte; die Reduktion war statistisch signifikant grösser als mit Placebo, wobei die geschätzte Behandlungsdifferenz bei jeweils -1.0 %-Punkten [-1.2; -0.8]95 %-KI und -1.4 %-Punkten [-1.6; -1.2]95 %-KI lag.
Tabelle 8: Ergebnisse einer 52-wöchigen Studie, in der Rybelsus in Kombination mit Insulin mit Placebo verglichen wurde (PIONEER 8)
Rybelsus7 mg Rybelsus14 mg Placebo
Population (N)1 182 181 184
HbA1c (%)
Ausgangswert2 8.2 8.2 8.2
Änderung gegenüber dem -0.8 -1.2 0.0
Ausgangswert in Woche 523
Unterschied gegenüber Placebo3 -0.9 [-1.1; -0.6]§ -1.3 [-1.5; -1.0]§ -
[95 %-KI]
Patienten (%), die einen HbA1c 47# 64# 10
<7.0 % erreichten2
Körpergewicht (kg)
Ausgangswert2 87.1 84.6 86.0
Änderung gegenüber dem -2.9 -4.3 0.6
Ausgangswert in Woche 523
Unterschied gegenüber Placebo3 -3.5 [-4.5; -2.6]§ -4.9 [-5.9; -3.9]§ -
[95 %-KI]
1 Full Analysis Set: Alle
randomisierten Patienten 2
Beobachtetes Mittel/Anteil 3
Geschätzt mit einem gemischten
Modell für wiederholte Messungen,
angepasst an Basiswert,
Hintergrundmedikation und Region.
Geschätzt mit einem gemischten
Modell für wiederholte Messungen,
angepasst an Basiswert,
Hintergrundmedikation und Region.
§ Statistisch signifikant
(p<0.05) # Die Wahrscheinlichkeit,
das Ziel zu erreichen, war mit
Rybelsus statistisch signifikant
grösser als mit Placebo (p<0.05)
Kardiovaskuläre Ergebnisse
SOUL - Kardiovaskuläre Ergebnisstudie bei Patienten mit Diabetes mellitus Typ 2
In einer doppelblinden, placebokontrollierten, ereignisgesteuerten Studie wurden 9650 Patienten im Alter von 50 Jahren oder älter mit Diabetes mellitus Typ 2 und hohem kardiovaskulärem Risiko, definiert als etablierte kardiovaskuläre Erkrankung und/oder chronische Nierenerkrankung, randomisiert, um einmal täglich entweder Semaglutide 14 mg oder Placebo in Ergänzung zur Standardbehandlung zu erhalten.
Insgesamt hatten 5468 Patienten (56.7 %) eine etablierte kardiovaskuläre Erkrankung ohne chronische Nierenerkrankung, 1241 (12.9 %) hatten nur eine chronische Nierenerkrankung und 2620 (27.2 %) hatten sowohl eine kardiovaskuläre Erkrankung als auch eine Nierenerkrankung. Das durchschnittliche Alter zu Beginn betrug 66.1 Jahre, und 71.1 % der Patienten waren Männer. Die durchschnittliche Diabetesdauer betrug 15.4 Jahre, der durchschnittliche HbA1c-Wert betrug 8.0 %, der durchschnittliche BMI betrug 31.1 kg/m2 und die durchschnittliche eGFR betrug 73.8 ml/min/1.73m2. Die Krankengeschichte umfasste Schlaganfälle (15.4 %), Herzinfarkte (40.0 %) und periphere arterielle Verschlusskrankheit (15.7 %). Zu Beginn wurden 26.9 % der Patienten mit Natrium-Glukose-Cotransporter-2 (SGLT2)-Inhibitoren behandelt.
Der primäre Endpunkt war die Zeit von der Randomisierung bis zum ersten Auftreten eines schwerwiegenden kardiovaskulären Ereignisses (MACE): kardiovaskulärer Tod, nicht-tödlicher Herzinfarkt oder nicht-tödlicher Schlaganfall. Der primäre Endpunkt, die Zeit bis zum ersten MACE, trat bei 1247 der 9650 eingeschlossenen Patienten auf, 579 "erste MACE" (12.0 %) wurden bei den 4825 mit Semaglutide behandelten Patienten im Vergleich zu 668 "erste MACE" (13.8 %) bei den 4825 mit Placebo behandelten Patienten verzeichnet.
Die Überlegenheit von Semaglutide gegenüber Placebo hinsichtlich MACE wurde mit einem Hazard Ratio von 0.86 [0.77; 0.96] [95 %-KI] bestätigt, was einer relativen Risikoreduktion der MACE von 14 % entspricht (siehe Abbildungen 1 & 2). Die Reduktion von MACE mit Semaglutide war in allen Subgruppen hinsichtlich Alter, Geschlecht, Rasse, Ethnizität, BMI zu Beginn, und Grad der Nierenfunktionseinschränkung konsistent. Die Analyse des ersten zusammengesetzten Nierenereignisses (des ersten konfirmatorischen sekundären Endpunkts) ergab ein Hazard Ratio von 0.91 [0.80; 1.05] [95 %-KI].
Daten aus der In-Studien-Periode basierend auf dem vollständigen Analyse-Set. Kumulative Inzidenzschätzungen basieren auf der Zeit von der Randomisierung bis zum ersten von der EAC bestätigten MACE mit Nicht-KV-Tod, modelliert als konkurrierendes Risiko unter Verwendung des Aalen-Johansen-Schätzers. Teilnehmer ohne Ereignisse von Interesse wurden am Ende ihrer In-Studien-Beobachtungsperiode zensiert. Die Zeit von der Randomisierung bis zum ersten MACE wurde unter Verwendung eines Cox-Proportional-Hazard-Modells mit der Behandlung als kategorischem festen Faktor analysiert. Das Hazard Ratio und das Konfidenzintervall wurden für das gruppensequenzielle Design unter Verwendung der Likelihood-Ratio-Reihenfolge angepasst.
HR: Hazard Ratio, KI: Konfidenzintervall, KV: kardiovaskulär, EAC: Ereignisbewertungskomitee, MACE: schwerwiegendes kardiovaskuläres Ereignis.
Abbildung 1: Zeit von der Randomisierung bis zum ersten MACE - Kumulative Inzidenzfunktionsdarstellung
Daten aus der In-Studien-Periode basierend auf dem vollständigen Analyse-Set. Die Zeit von der Randomisierung bis zu jedem Endpunkt wurde unter Verwendung eines Cox-Proportional-Hazard-Modells mit der Behandlung als kategorischem festen Faktor analysiert. Teilnehmer ohne Ereignisse von Interesse wurden am Ende ihrer In-Studien-Periode zensiert. Für den primären Endpunkt wurden das HR und das KI für das gruppensequenzielle Design unter Verwendung der Likelihood-Ratio-Reihenfolge angepasst. KV-Tod umfasst sowohl kardiovaskulären Tod als auch Todesursachen, die nicht festgestellt werden konnten.
HR: Hazard Ratio. KI: Konfidenzintervall. KV: kardiovaskulär, MI: Myokardinfarkt.
Abbildung 2: Behandlungseffekt für den primären Endpunkt und seine Bestandteile (SOUL)
PIONEER 6– Kardiovaskuläre Ergebnisstudie bei Patienten mit Diabetes mellitus Typ 2
In dieser doppelblinden Studie wurden 3'183 Patienten mit Typ 2 Diabetes und hohem kardiovaskulären Risiko (2'695 [85 %] Patienten mit vorbestehender Herz-Kreislauf-Erkrankung sowie 488 [15 %] Patienten mit kardiovaskulären Risikofaktoren ohne vorbestehende Herz-Kreislauf-Erkrankung) zusätzlich zur vorbestehenden antihyperglykämischen Therapie randomisiert mit Rybelsus 14 mg einmal täglich oder Placebo behandelt (mittlere Behandlungsdauer 16 Monate). Die Behandlung konnte in beiden Armen gemäss den geltenden Therapierichtlinien intensiviert werden.
PIONEER 6 war eine vor der Zulassung durchgeführte kardiovaskuläre Ergebnisstudie, die darauf abzielte, die kardiovaskuläre Sicherheit zu etablieren.
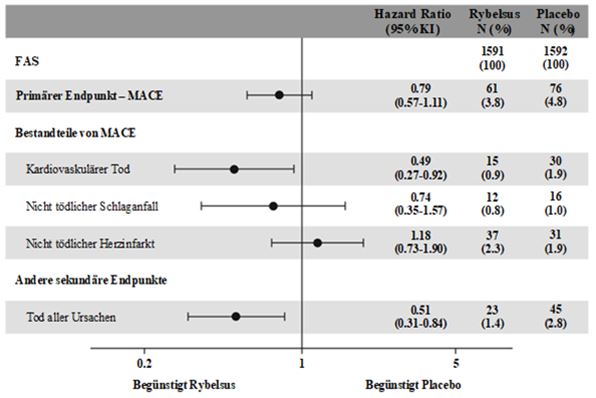
Primärer Endpunkt war die Zeit von der Randomisierung bis zum Auftreten des ersten schwerwiegenden kardiovaskulären Ereignisses (MACE: kardiovaskulärer Tod, nicht-tödlicher Herzinfarkt oder nicht-tödlicher Schlaganfall). Das kardiovaskuläre Risikos war bei den mit Semaglutide behandelten Patienten numerisch reduziert.

Abbildung 3: Forest-Plot: Behandlungseffekt auf den primären zusammengesetzten Endpunkt MACE, seine Komponenten und alle Todesursachen (PIONEER 6)
Dieser Effekt beruhte primär auf einer Abnahme der kardiovaskulären Mortalität.
SUSTAIN 6– Kardiovaskuläre Ergebnisstudie mit subkutan injiziertem Semaglutide bei Patienten mit Diabetes mellitus Typ 2
In dieser 104-wöchigen doppelblinden Studie wurden 3'297 Patienten mit Typ 2 Diabetes und hohem kardiovaskulären Risiko (2'735 [83 %] Patienten mit vorbestehender Herz-Kreislauf-Erkrankung sowie 562 [27 %] Patienten mit kardiovaskulären Risikofaktoren ohne vorbestehende Herz-Kreislauf-Erkrankung) zusätzlich zur vorbestehenden antihyperglykämischen Therapie randomisiert mit Semaglutide 0.5 mg s.c., Semaglutide 1 mg s.c. oder Placebo behandelt (mittlere Behandlungsdauer 2 Jahre).
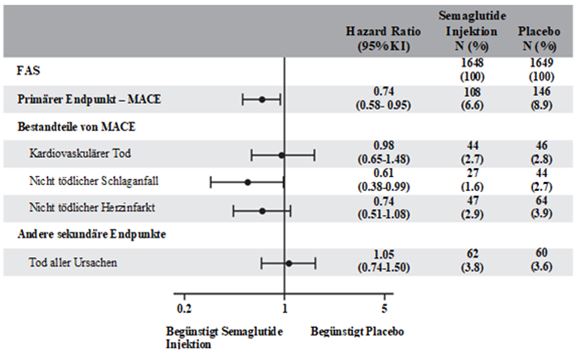
Primärer Endpunkt war die Zeit von der Randomisierung bis zum Auftreten des ersten schwerwiegenden kardiovaskulären Ereignisses (MACE: kardiovaskulärer Tod, nicht-tödlicher Herzinfarkt oder nicht-tödlicher Schlaganfall). Das kardiovaskuläre Risikos war bei den im Mittel über 2 Jahre mit Semaglutide behandelten Patienten reduziert.

Abbildung 4: Forest-Plot: Behandlungseffekt auf den primären zusammengesetzten Endpunkt MACE, seine Komponenten und alle Todesursachen (SUSTAIN 6)
Die Abnahme des kardiovaskulären Risikos beruhte primär auf eine Verringerung der Anzahl nicht-tödlicher Schlaganfälle. Abweichend von den Ergebnissen der PIONEER-6 Studie für orales Semaglutide wurde für die Behandlung mit subkutan applizierten Semaglutide kein positiver Effekt auf die kardiovaskuläre Mortalität beobachtet.
|




