Eigenschaften/WirkungenATC-Code
N06DX05
Pharmakotherapeutische Gruppe: Nervensystem, Psychoanaleptika, Antidementiva, andere Antidementiva.
Donanemab ist ein rekombinanter, humanisierter, monoklonaler Antikörper, der in Ovarzellen des chinesischen Hamsters (Chinese Hamster Ovary, CHO) hergestellt wird.
Wirkungsmechanismus
Donanemab ist ein monoklonaler Immunoglobulin-gamma-1 (IgG1) Antikörper, der sich gegen die unlösliche, pyroglutamate-modifizierte, N-terminal verkürzte Form von Amyloid-beta (N3pG Aβ) richtet, die nur in Amyloid-Plaques des Gehirns vorkommt. Donanemab bindet an N3pG Aβ und unterstützt die Auflösung der Plaques durch Mikroglia-vermittelte Phagozytose.
Pharmakodynamik
Bei Patienten, die mit Donanemab behandelt wurden, wurde mit Hilfe von Amyloid-Positronenemissionstomographie (PET) eine Reduktion der zerebralen Amyloid-Plaques beobachtet. Donanemab reduzierte die Tau-Pathophysiologie, gemessen anhand von P-Tau217 im Plasma.
Der prozentuale Anteil der mit Donanemab behandelten Patienten, die in der Studie TRAILBLAZER-ALZ 2 Amyloid-Freiheit erreichten (Amyloid clearance, das heisst, weniger als 24.1 Centiloide), betrug 32.5% in Woche 24, 69.5% in Woche 52 und 80,8% in Woche 76 in der indizierten Population.
In der Studie TRAILBLAZER-ALZ 2 war der Unterschied zwischen Donanemab und Placebo für die Veränderung der Amyloid-Konzentration ab Ausgangswert in Woche 76 in der indizierten Population signifikant (-89.24 Centiloide).
In der Studie TRAILBLAZER-ALZ 6 wurde eine ähnliche Reduktion der Amyloid-Plaques in Woche 24 für das Dosierungsschema von 350/700/1'050 mg, gefolgt von 1'400 mg alle 4 Wochen beobachtet, verglichen mit dem Dosierungsschema von 700 mg für die ersten drei Infusionen, gefolgt von 1'400 mg alle 4 Wochen, welches in der pivotalen Studie untersucht wurde.
Die Donanemab-Exposition nahm mit zunehmendem ADA-Titer ab. Eine Amyloid-Beta-Reduktion wurde unabhängig vom ADA-Titer festgestellt. Es wurde kein Zusammenhang zwischen dem Vorhandensein von ADA und den Ergebnissen im iADRS und CDR-SB beobachtet (siehe auch Rubrik “Warnhinweise und Vorsichtmassnahmen”, sowie Rubrik "Unerwünschte Wirkungen" ).
Klinische Wirksamkeit
Die Sicherheit und Wirksamkeit von Donanemab wurden in einer Studie Phase 3 (TRAILBLAZER-ALZ 2) untersucht. Es war eine doppelblinde, placebokontrollierte Studie im Parallelgruppendesign. Durchgeführt wurde sie bei Patienten im Alter von 60 bis 85 Jahren mit früher symptomatischer AD (leichte kognitive Einschränkung, Mild Cognitive Impairment, MCI) oder leichter Demenz aufgrund von AD und einem MMSE-Wert von 20 bis einschliesslich 28. Die Patienten mussten Anzeichen einer Amyloid-beta-Pathologie aufweisen, bestätigt durch einen Amyloid-PET-Scan. Die Teilnehmer wiesen in einem Flortaucipir-PET-Scan zudem Anzeichen einer pathologischen Tau-Ablagerung auf.
Supportiv gibt es Daten aus einer Studie Phase 2 (TRAILBLAZER-ALZ) mit vergleichbarem Design, Die in diesen Studien verwendeten Dosierungsschemata unterscheiden sich vom zugelassenen Dosierungsschema (siehe Rubrik "Pharmakokinetik" ).
Für die Sicherheitsauswertung wurden die Patienten über bis zu 76 Wochen oder bis zum Ende der Behandlung plus 57 Tage nach der letzten Dosis beobachtet.
TRAILBLAZER-ALZ 2 war ursprünglich als Phase 2-Studie konzipiert und wurde später in eine Phase 3-Studie umgewandelt. Die wichtigsten Änderungen waren: Ergänzung einer Titrationsphase mit 700 mg für die ersten drei Anwendungen; Anpassungen einer Phase-2- zu einer Phase-3-Studie, einschliesslich der Erhöhung des Stichprobenumfangs und der Änderung der primären Analyse von "CDR-SB in der Gesamtpopulation oder der intermediären Tau-Population" zu "iADRS in der intermediären Tau-Population" ; Ergänzung einer Langzeit-Verlängerungsphase zur weiteren Beurteilung der Wirksamkeit und Sicherheit von Donanemab im zeitlichen Verlauf.
Studie Phase 3 TRAILBLAZER-ALZ 2
In dieser Studie wurden 1736 Patienten im Verhältnis 1:1 randomisiert und erhielten eine intravenöse Infusion mit 700 mg Donanemab alle 4 Wochen für die ersten 3 Anwendungen, danach 1400 mg alle 4 Wochen (N=860) oder Placebo (N=876), über bis zu 72 Wochen insgesamt. Die Studie beinhaltete eine doppelblinde Verlängerungsphase über 78 Wochen. Die Anwendung wurde fortgesetzt bis zum Ende der Studie oder bis zur Auflösung (Clearance) der Amyloid-Plaques, definiert als Nachweis einer Plaque-Konzentration von weniger als 25 Centiloiden aus zwei aufeinanderfolgenden Amyloid-PET-Scans oder ein einzelner PET-Scan mit einer Plaque-Konzentration von weniger als 11 Centiloiden.
Darüber hinaus war eine Dosisaussetzung für behandlungsbedingte ARIA zulässig. Patienten, die zu Studieneintritt bereits eine symptomatische Behandlung erhielten (Acetylcholinesterase-Inhibitoren [AChEI] und/oder N-Methyl-D-Aspartat-Inhibitoren, Memantin), konnten diese Behandlungen fortsetzen. Während der Studie konnten symptomatische Behandlungen im Ermessen des Studienarztes ergänzt oder verändert werden. Ein Studienausschluss erfolgte für Patienten mit vorbestehenden ARIA-E mit mehr als 4 Mikroblutungen, mehr als 1 Bereich mit superfizieller Siderose, jeglicher intrazerebraler Blutung >1 cm oder schwerer Erkrankung der weissen Substanz. Zu Studienbeginn betrug das mittlere Alter 73 Jahre mit einem Bereich von 59 bis 86 Jahre, bei einem mittleren (SD) Ausgangsgewicht von 71.7 kg (15.7), einer schrittweisen und progressiven Veränderung der Gedächtnis-Funktion über mindestens 6 Monate und einem MMSE (Mini-Mental State Examination) Score von 22.29 (3.88). 57.4% der Teilnehmer waren Frauen, 91.5% Weisse, 5.7% mit hispanischer oder lateinamerikanischer Ethnizität, 6.0% asiatischer Herkunft und 2.3% waren Schwarze. 80.0% der Patienten wurden in Nordamerika, 13.9% in Europa, 5.1% in Japan und 1.0% in Australien eingeschlossen. 29% waren ApoEε 4 Nichtträger, 54% Heterozygote und 17% Homozygote.
55.6% der Patienten erhielten AChEI, 20.3% Memantin. 61% der Patienten erhielten entweder AChEI oder Memantin.
Der Mittelwert (mean, SD) an Amyloid in Centiloiden betrug bei Baseline 102.5 (34.5).
Auf Grundlage des Tau-PET-Scans im Screening mit Flortaucipir gab es zwei primäre Analysenpopulationen: 1) Population mit niedrigen bis mittleren Tau-Konzentrationen (Anteil insgesamt 68.2%), und 2) die kombinierte Population mit niedrigen bis mittleren sowie hohen Tau-Konzentrationen (Anteil insgesamt 31.8%).
Insgesamt beendeten 24.7% der Patienten frühzeitig die Behandlung (29.3% unter Donanemab, 20.1% unter Placebo).
Der primäre Wirksamkeitsendpunkt war die Veränderung von Kognition und Funktion, gemessen anhand des iADRS (integrated Alzheimer's Disease Rating Scale) Scores von Beginn bis Woche 76. Der iADRS ist eine kombinierte Untersuchung von Kognition und täglicher Funktion und besteht aus Items aus der Kognitions-Subskala der Alzheimer's Disease Assessment Scale (ADAS-Cog13, Punktzahl 0-85) und der Alzheimer's Disease Cooperative Study - instrumental Activities of Daily Living (ADCS-iADL, Punktzahl 0-59) Skala, die Kerndomänen im Verlauf der klinischen AD messen. Der Gesamtscore reicht von 0 bis 144, wobei niedrigere Scores einer schlechteren kognitiven und funktionalen Leistung entsprechen. Zu den anderen Wirksamkeitsendpunkten gehörten CDR-SB (Clinical Dementia Rating Scale - Sum of Boxes), ADAS-Cog13 und ADCS-iADL.
Die nachfolgende Tabelle 3 zeigt wichtige Studienergebnisse in der indizierten Population.
In der indizierten Population wurden 717 Teilnehmer randomisiert und Donanemab zugeteilt, 414 waren weiblich und 303 männlich, 70 waren <65 Jahre alt, 320 waren 65-74 Jahre alt und 327 waren >= 75 Jahre alt.
In der indizierten Population wurden 730 Teilnehmer randomisiert und der Placebo-Gruppe zugeteilt, 426 waren weiblich und 304 männlich, 66 waren <65 Jahre alt, 311 waren 65-74 Jahre alt und 353 waren >= 75 Jahre alt.
Tabelle 3: Ergebnisse der Wirksamkeitsanalyse aus der Donanemab-Studie TRAILBLAZER-ALZ 2 in Woche 76 in der indizierten Population (heterozygote und Nichtträger von ApoE ε4)
Klinischer Endpunkt Heterozygote ApoE ε4-Träger und ApoE
ε4-Nichtträger
Dona Placebo
iADRS (NCS)
Mittlerer Ausgangswert (SD) 104.66 (14.12) 103.83 (14.03)
Veränderung (LS mean) ab -10.21 (0.57) -13.59 (0.55)
Ausgangswert
Unterschied gegenüber Placebo (95% 3.38 (1.83, 4.92)
CI)
Frauen
Mittlerer Ausgangswert (SD) 104.92 (14.02) 103.75 (13.38)
Veränderung (LS mean) ab -10.98 (0.76) -14.77 (0.72)
Ausgangswert
Unterschied gegenüber Placebo (95% 3.80 (1.77, 5.83)
CI)
Männer
Mittlerer Ausgangswert (SD) 104.32 (14.26) 103.95 (14.87)
Veränderung (LS mean) ab -9.18 (0.87) -11.92 (0.85)
Ausgangswert
Unterschied gegenüber Placebo (95 % 2.73 (0.36, 5.10)
CI)
<65 Jahre
Mittlerer Ausgangswert (SD) 105.19 (15.46) 107.14 (14.19)
Veränderung (LS mean) ab -12.74 (1.77) -14.21 (1.86)
Ausgangswert
Unterschied gegenüber Placebo (95% 1.47 (-3.51, 6.45)
CI)
65-74 Jahre
Mittlerer Ausgangswert (SD) 106.05 (12.88) 105.09 (13.59)
Veränderung (LS mean) ab -9.33 (0.86) -13.69 (0.83)
Ausgangswert
Unterschied gegenüber Placebo (95% 4.35 (2.03, 6.68)
CI)
>75 Jahre
Mittlerer Ausgangswert (SD) 103.20 (14.83) 102.11 (14.19)
Veränderung (LS mean) ab -10.48 (0.86) -13.37 (0.80)
Ausgangswert
Unterschied gegenüber Placebo (95% 2.89 (0.61, 5.17)
CI)
CDR-SB (MMRM)
Mittlerer Ausgangswert (SD) 3.96 (2.10) 3.94 (2.04)
Veränderung (LS mean) ab 1.67 (0.11) 2.43 (0.10)
Ausgangswert
Unterschied gegenüber Placebo (95% -0.77 (-1.04, -0.49)
CI)
Frauen
Mittlerer Ausgangswert (SD) 4.03 (2.11) 3.97 (1.98)
Veränderung (LS mean) ab 1.66 (0.12) 2.49 (0.15)
Ausgangswert
Unterschied gegenüber Placebo (95% -0.83 (-1.20, -0.45)
CI)
Männer
Mittlerer Ausgangswert (SD) 3.87 (2.08) 3.89 (2.13)
Veränderung (LS mean) ab 1.48 (0.15) 2.15 (0.14)
Ausgangswert
Unterschied gegenüber Placebo (95% -0.66 (-1.07, -0.25)
CI)
<65 Jahre
Mittlerer Ausgangswert (SD) 3.81 (2.05) 3.80 (1.54)
Veränderung (LS mean) ab 2.53 (0.40) 2.81 (0.31)
Ausgangswert
Unterschied gegenüber Placebo (95% -0.28 (-1.19, 0.63)
CI)
65-74 Jahre
Mittlerer Ausgangswert (SD) 3.78 (1.88) 3.66 (1.92)
Veränderung (LS mean) ab 1.46 (0.14) 2.55 (0.16)
Ausgangswert
Unterschied gegenüber Placebo (95% -1.09 (-1.50, -0.68)
CI)
>75 Jahre
Mittlerer Ausgangswert (SD) 4.17 (2.30) 4.21 (2.19)
Veränderung (LS mean) ab 1.48 (0.15) 2.04 (0.16)
Ausgangswert
Unterschied gegenüber Placebo (95% -0.56 (-0.96, -0.16)
CI)
ADAS-Cog13 (NCS)
Mittlerer Ausgangswert (SD) 28.43 (8.91) 29.00 (8.93)
Veränderung (LS mean) ab 5.37 (0.31) 7.06 (0.29)
Ausgangswert
Unterschied gegenüber Placebo (95% -1.69 (-2.52, -0.86)
CI)
Frauen
Mittlerer Ausgangswert (SD) 28.40 (9.15) 29.45 (8.61)
Veränderung (LS mean) ab 5.59 (0.40) 7.20 (0.39)
Ausgangswert
Unterschied gegenüber Placebo (95% -1.61 (-2.71, -0.52)
CI)
Männer
Mittlerer Ausgangswert (SD) 28.46 (8.60) 28.40 (9.32)
Veränderung (LS mean) ab 5.09 (0.47) 6.88 (0.45)
Ausgangswert
Unterschied gegenüber Placebo (95% -1.79 (-3.07, -0.52)
CI)
<65 Jahre
Mittlerer Ausgangswert (SD) 27.82 (9.67) 27.11 (9.40)
Veränderung (LS mean) ab 8.34 (0.94) 7.90 (0.96)
Ausgangswert
Unterschied gegenüber Placebo (95% 0.44 (-2.19, 3.06)
CI)
65-74 Jahre
Mittlerer Ausgangswert (SD) 27.82 (8.80) 28.74 (9.39)
Veränderung (LS mean) ab 4.86 (0.45) 7.51 (0.44)
Ausgangswert
Unterschied gegenüber Placebo (95% -2.66 (-3.89, -1.42)
CI)
> 75 Jahre
Mittlerer Ausgangswert (SD) 29.16 (8.83) 29.59 (8.36)
Veränderung (LS mean) ab 5.21 (0.46) 6.47 (0.43)
Ausgangswert
Unterschied gegenüber Placebo (95% -1.26 (-2.49, -0.04)
CI)
Abkürzungen: ApoE-ε4 = Allel-Subtyp 4 des Gens, das für das Apolipoprotein Klasse E kodiert; CDR-SB = Clinical Dementia Rating Scale – Sum of boxes; CI = confidence interval, Konfidenzintervall; Dona = Donanemab; iADRS = integrated Alzheimers Disease Rating Scale; LSM = Least-Square mean, Mittelwert nach der Methode der kleinsten Quadrate; MMRM = Mixed Model for Repeated Measures, gemischtes Modell für wiederholte Messungen; SD = standard deviation, Standardabweichung.
Biomarker
Der prozentuale Anteil der Patienten unter Donanemab mit Amyloid-Clearance (d.h. weniger als 24.1 Centiloide oder visuell negativ im Amyloid-PET-Scan) in der Studie TRAILBLAZER-ALZ 2 wird in Abbildung 2 dargestellt.
Unter Donanemab wurde eine Reduktion der P-tau217-Konzentration (Log 10) im Plasma beobachtet im Vergleich zu Placebo. In der Population mit niedriger bis mittlerer Tau-Konzentration (498 Patienten unter Donanemab vs. 494 Patienten unter Placebo) betrug die mittlere Veränderung (LS mean ± SE) -0.19 ± 0.012 und -0.26 ± 0.015 in den Wochen 24 und 76, im Vergleich zu Placebo (p<0.0001 zu beiden Zeitpunkten). Damit übereinstimmend zeigte die kombinierte Population eine mittlere Veränderung (Log LS mean ± SE) von -0.17± 0.011 und -0.23± 0.013 in den Wochen 24 und 76, im Vergleich zu Placebo (p<0.0001 zu beiden Zeitpunkten).
Abbildung 2: Prozentualer Anteil der Patienten in der indizierten Population unter Donanemab mit erreichter Amyloid-Plaque-Clearance gemessen anhand von Amyloid-PET über 76 Wochen in der Studie TRAILBLAZER-ALZ 2.
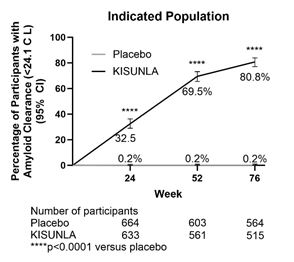
Population mit hoher Tau-Konzentration in der indizierten Population.
In der Population mit hoher Tau-Konzentration (218 unter Donanemab und 235 Patienten unter Placebo) zeigte Donanemab eine Verlangsamung der klinischen Verschlechterung um 8% (1.55 ± 1.66 [p=0.351) im iADRS und 18% (-0.60 ± 0.28 [p=0.032]) im CDR-SB in Woche 76 im Vergleich zu Placebo.
TRAILBLAZER-ALZ-6-Studie Phase-III
Das Dosierungsschema mit 350/700/1050 mg Donanemab und nachfolgend 1400 mg alle 4 Wochen wurde untersucht in einer multizentrischen, randomisierten, doppelblinden Studie der Phase IIIb bei Erwachsenen mit früher, symptomatischer AD (MCI aufgrund von AD oder leichte AD-Demenz, MMSE-Score 20 bis 28 einschliesslich) und Hinweis auf eine Amyloid-beta-Pathologie, bestätigt durch einen Amyloid-PET-Scan.
843 Patienten wurden im Verhältnis 1:1:1:1 randomisiert und erhielten Donanemab in vier unterschiedlichen Dosierungsschemata über insgesamt 72 Wochen, 700 mg in den ersten drei Infusionen, danach 1400 mg alle 4 Wochen (n=207), oder eines von drei alternativen Dosierungsschemata (einschliesslich das Dosierungsschema 350/700/1050 mg, gefolgt von 1400 mg alle 4 Wochen; n=212), wobei in allen Schemata insgesamt die gleiche Arzneimittelgesamtmenge angewendet wurde.
Der primäre Endpunkt der Studie war der Anteil der Teilnehmer mit jeglichem Auftreten von ARIA-E bis Woche 24. Die Ergebnisse zeigten, dass bei 14% der Patienten mit 350/700/1050 mg und nachfolgend 1400 mg alle 4 Wochen bis Woche 24 ein ARIA-E aufgetreten war, im Vergleich zu 24% der Patienten mit 700/700/700 mg und nachfolgend 1400 mg alle 4 Wochen, ein 41% geringeres relatives Risiko. Die in Woche 24 beobachtete Abnahme der Amyloid-Plaques war in allen Dosierungsschemata ähnlich
|

