Eigenschaften/WirkungenATC-Code
C02KX06
Wirkungsmechanismus
Sotatercept, ein rekombinantes Fusionsprotein des Activin-Rezeptors Typ IIA-Fc (ActRIIA-Fc), ist ein Activin-Signalinhibitor, der an Activin A und andere Liganden der TGF-β-Superfamilie bindet. Dadurch verbessert Sotatercept das Gleichgewicht zwischen der proproliferativen (ActRIIA/Smad2/3-vermittelten) und der antiproliferativen (BMPRII/Smad1/5/8-vermittelten) Signalübertragung, um die Gefässproliferation zu modulieren.
Pharmakodynamik
In einer klinischen Phase-II-Studie wurde der pulmonale Gefässwiderstand (PVR) bei PAH Patienten nach einer 24-wöchigen Behandlung mit Sotatercept beurteilt. Die Abnahme des PVR gegenüber dem Ausgangswert war in den Gruppen mit 0,7 mg/kg und 0,3 mg/kg Sotatercept signifikant grösser als in der Placebogruppe. Der placebobereinigte mittlere Unterschied (least square, LS) gegenüber dem Ausgangswert betrug -269,4 dyn•s/cm5 (95%-KI: -365,8; -173,0) in der Gruppe mit 0,7 mg/kg Sotatercept und -151,1 dyn•s/cm5 (95%-KI: -249,6; -52,6) in der Gruppe mit 0,3 mg/kg Sotatercept. In STELLAR war die Abnahme des PVR gegenüber dem Ausgangswert in der Gruppe mit 0,7 mg/kg Sotatercept ebenfalls signifikant grösser als in der Placebogruppe (siehe "Klinische Wirksamkeit" ). In ZENITH betrug der mediane Behandlungsunterschied in der Veränderung des PVR vom Ausgangswert zwischen der Sotatercept- und der Placebogruppe nach 24 Wochen -339,6 dyn•s/cm5 (95%-KI: -511,09; -168,06) (siehe "Klinische Wirksamkeit" ).
In PAH Rattenmodellen verringerte ein Sotatercept-Analogon die Expression von proinflammatorischen Markern an der Pulmonalarterienwand, reduzierte die Rekrutierung von Leukozyten, hemmte die Proliferation von Endothel- und glatten Muskelzellen und förderte die Apoptose in den erkrankten Gefässen. Diese zellulären Veränderungen gingen mit dünneren Gefässwänden, einer Umkehrung des arteriellen und rechtsventrikulären Remodellings und einer verbesserten Hämodynamik einher.
Klinische Wirksamkeit
STELLAR
Die Wirksamkeit von Winrevair wurde in der Studie STELLAR bei erwachsenen Patienten mit PAH beurteilt. STELLAR war eine globale, doppelblinde, placebokontrollierte, multizentrische klinische Parallelgruppenstudie, in der 323 Patienten mit PAH (WHO-Funktionsklasse II oder III) randomisiert im Verhältnis 1:1 einer Behandlung mit Winrevair (Zieldosis 0,7 mg/kg) (n = 163) oder Placebo (n = 160) subkutan einmal alle 3 Wochen erhielten.
Die demographischen und klinischen Baseline-Charakteristika waren in der Winrevair- und der Placebogruppe generell vergleichbar. Studienteilnehmende waren Erwachsene mit einem medianen Alter von 48,0 Jahren (Bereich: 18 bis 82 Jahre); das mediane Gewicht betrug 68 kg (Bereich: 38,0 bis 141,3 kg); 89,2% waren weiss und 79,3% waren nicht hispanisch oder lateinamerikanisch; 79,3% waren weiblich. Die häufigsten PAH Ätiologien waren: idiopathische PAH (58,5%), hereditäre PAH (18,3%) und PAH assoziiert mit Bindegewebserkrankungen (CTD) (14,9 %). Die mediane Zeit zwischen PAH Diagnose und Screening betrug 8,76 Jahre. Die meisten Teilnehmenden erhielten entweder eine dreifache (61,3%) oder eine zweifache (34,7%) PAH Backgroundtherapie, und mehr als ein Drittel (39,9%) erhielten Prostacyclin-Infusionen. Der Anteil von Teilnehmenden mit PAH der WHO-Funktionsklasse II (48,6%) bzw. WHO-Funktionsklasse III (51,4%) war in beiden Gruppen ähnlich. Von der Teilnahme an der STELLAR-Studie ausgeschlossen waren Patienten mit diagnostizierter PAH in Zusammenhang mit einer Infektion mit dem Humanen Immundefizienz-Virus (HIV), PAH in Zusammenhang mit portaler Hypertonie, Schistosomiasis-assoziierter PAH und pulmonaler venookklusiver Erkrankung.
Primärer Wirksamkeitsendpunkt war die Veränderung der 6-Minuten-Gehstrecke (6MWD) in Woche 24 im Vergleich zum Ausgangswert. In der Winrevair-Behandlungsgruppe betrug die placebobereinigte Veränderung der 6MWD in Woche 24 gegenüber dem Ausgangswert im Median 40,8 Meter (95%-KI: 27,5; 54,1; p < 0,001). Der Median der placebobereinigten Veränderungen der 6MWD in Woche 24 wurde auch in Subgruppen beurteilt (siehe Abbildung 1).
Abbildung 1: Veränderung der 6-Minuten-Gehstrecke (Meter) in Woche 24 gegenüber dem Ausgangswert in Subgruppen
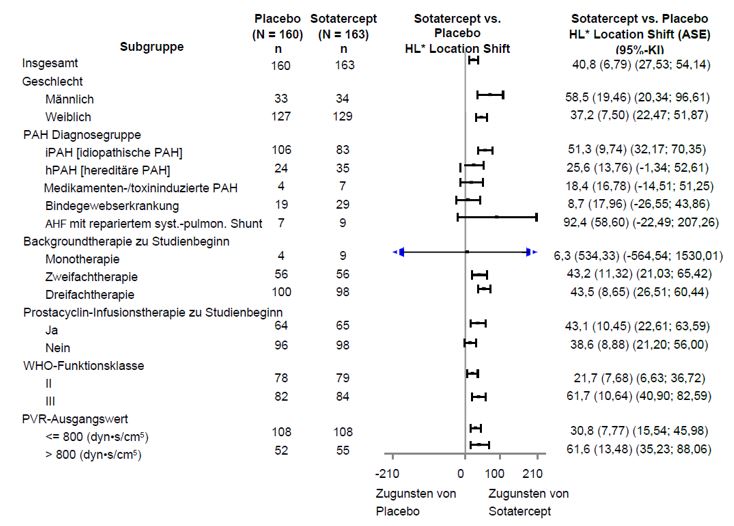
AHF = angeborener Herzfehler
* Hodges-Lehmann-Schätzer des Location Shift gegenüber Placebo (Median aller gepaarten Unterschiede). ASE = asymptotischer Standardfehler. Bei Teilnehmenden, die verstarben, wurde der Veränderung der 6MWD in Woche 24 gegenüber dem Ausgangswert ein Wert von bis zu -2000 Metern zugeordnet, um den schlechtesten Rang zu erhalten. Bei Teilnehmenden mit fehlenden Daten aufgrund einer nicht tödlichen klinischen Verschlechterung wurde für die Veränderung der 6MWD in Woche 24 gegenüber dem Ausgangswert ein Wert von bis zu -1000 Metern imputiert, um den zweitschlechtesten Rang zu erhalten.
Die klinische Verbesserung war ein vordefinierter Endpunkt, der anhand des Anteils der Patienten gemessen wurde, die in Woche 24 im Vergleich zum Ausgangszeitpunkt alle drei der folgenden Kriterien erfüllten: Verbesserung der 6MWD (Zunahme um ≥30 m), Verbesserung des N-terminalen pro-B-Typ-natriuretischen Peptids (NT-proBNP) (Abnahme des NT-proBNP um ≥30% oder Aufrechterhaltung/Erreichen eines NT-proBNP-Spiegels < 300 ng/l) und Verbesserung der WHO-Funktionsklasse oder Erhaltung der WHO-Funktionsklasse II. Das Fortschreiten der Erkrankung wurde gemessen als Zeit bis zum Tod oder bis zum ersten Auftreten eines Ereignisses einer klinischen Verschlechterung. Zu den Ereignissen einer klinischen Verschlechterung zählten eine Listung zur Lungen- und/oder Herztransplantation infolge einer Verschlechterung, die Notwendigkeit der Einleitung einer Rescue-Therapie mit einer zugelassenen PAH Backgroundtherapie oder die Notwendigkeit einer Dosiserhöhung der Prostacyclin-Infusionen um ≥10%, die Notwendigkeit einer Vorhofseptostomie, eine Hospitalisierung wegen einer sich verschlechternden PAH (≥24 Stunden) oder eine Verschlechterung der PAH (Verschlechterung der WHO-Funktionsklasse und Abnahme der 6MWD um ≥15%, wobei beide Ereignisse gleichzeitig oder zu unterschiedlichen Zeitpunkten eintreten können). Ereignisse einer klinischen Verschlechterung sowie Todesfälle wurden erfasst, bis der letzte Patient die Visite in Woche 24 absolviert hatte (Daten bis zum data cutoff; mediane Dauer der Exposition 33,6 Wochen).
Bei den mit Winrevair behandelten Patienten kam es im Vergleich zu den Patienten der Placebogruppe zu einer statistisch signifikanten klinischen Verbesserung, einer Verbesserung der WHO-Funktionsklasse und zu einem verzögerten Fortschreiten der Erkrankung, einschliesslich eines geringeren Risikos von Tod und Hospitalisierung (siehe Tabelle 4 und Abbildung 2).
In Woche 24 zeigten 38,9% der Patienten unter Sotatercept eine Verbesserung der MCI gegenüber 10,1% in der Placebogruppe (p<0,001). Der mediane Behandlungsunterschied im PVR zwischen der Sotatercept- und der Placebogruppe betrug -234,6 dyn*s/cm5 (95% KI: -288,4, -180,8; p<0,001). Der mediane Behandlungsunterschied im NT-proBNP zwischen der Sotatercept- und der Placebogruppe betrug -441,6 pg/ml (95% KI: -573,54, -309,61; p<0,001). Eine Verbesserung der Funktionsklasse gegenüber dem Ausgangswert trat bei 29% der Patienten in der Sotatercept-Gruppe gegenüber 13,8% in der Placebogruppe auf (p<0,001).
Tabelle 4: Tod oder Ereignisse einer klinischen Verschlechterung
Winrevair(N = 163) Placebo(N = 160)
Gesamtanzahl der Patienten, die verstarben oder 9 (5,5) 42 (26,3)
mindestens ein Ereignis einer klinischen
Verschlechterung erlitten, n (%)
Bewertung von Tod oder erstem Auftreten von Ereignissen
einer klinischen Verschlechterung*, n (%)
Tod 2 (1,2) 6 (3,8)
Verschlechterungsbedingte Listung zur Lungen- und/oder 1 (0,6) 1 (0,6)
Herztransplantation
Notwendigkeit der Einleitung einer Rescue-Therapie mit 2 (1,2) 17 (10,6)
einer zugelassenen PAH Therapie oder Notwendigkeit
einer Dosiserhöhung der Prostacyclin-Infusionen um ≥10 %
Notwendigkeit einer Vorhofseptostomie 0 (0,0) 0 (0,0)
PAH spezifische Hospitalisierung (≥24 Stunden) 0 (0,0) 7 (4,4)
Verschlechterung der PAH† 4 (2,5) 15 (9,4)
* Bei einem Patienten können für das erste Ereignis
einer klinischen Verschlechterung mehr als eine
Bewertung dokumentiert sein. Bei 3 Patienten unter
Placebo und 0 Patienten unter Sotatercept wurden für
ihr erstes Ereignis einer klinischen Verschlechterung
mehr als eine Bewertung dokumentiert. †
Verschlechterung der PAH ist definiert als Auftreten
beider folgender Ereignisse zu einem beliebigen
Zeitpunkt, auch wenn diese zu verschiedenen Zeiten
auftraten, verglichen mit den Ausgangswerten: (a)
Verschlechterung der WHO-Funktionsklasse (II zu III,
III zu IV, II zu IV usw.); und (b) Abnahme der 6MWD um
≥15% (bestätigt durch zwei 6-Minuten-Gehtests im
Abstand von mindestens 4 Stunden, aber höchstens einer
Woche).N = Anzahl Patienten in der FAS-Population; n =
Anzahl Patienten in der Kategorie. Prozentanteile
berechnet als (n/N)•100.
Abbildung 2: Kaplan-Meier-Kurve der Zeit bis zum Tod oder bis zum ersten Auftreten von Ereignissen einer klinischen Verschlechterung
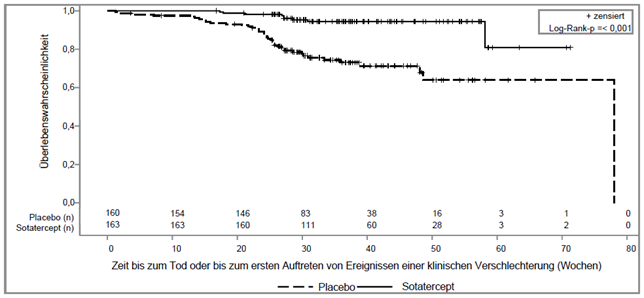
n = Anzahl subjects at risk
ZENITH
Die Wirksamkeit von Winrevair wurde in der ZENITH-Studie bei erwachsenen PAH-Patienten mit WHO FC III oder IV mit hohem Mortalitätsrisiko untersucht. ZENITH war eine globale, doppelblinde, placebokontrollierte, multizentrische klinische Parallelgruppenstudie, in der 172 Patienten im Verhältnis 1:1 randomisiert Winrevair (Zieldosis 0,7 mg/kg) (n=86) oder Placebo (n=86) erhielten, jeweils alle 3 Wochen subkutan.
Die demografischen und klinischen Baseline-Charakteristika waren in der Winrevair- und der Placebogruppe im Allgemeinen vergleichbar. Die Teilnehmer dieser Studie waren Erwachsene mit einem medianen Alter von 57,5 Jahren (Bereich: 18 bis 75 Jahre); 86,6% der Teilnehmer waren weiss, 87,8% waren nicht hispanisch oder lateinamerikanisch und 76,7% waren weiblich. Die häufigsten PAH Ätiologien waren idiopathische PAH (50,0%), PAH assoziiert mit Bindegewebserkrankungen (CTD) (27,9%) und hereditäre PAH (10,5%). Die mediane Zeit zwischen PAH-Diagnose und Screening betrug 7,68 Jahre. Zu Studienbeginn erhielten daher 72,1% bzw. 27,9% der Patienten bereits eine Dreifach- bzw. eine Zweifachkombination als PAH Backgroundtherapie, und 59,3% der Teilnehmer erhielten eine Prostacyclin-Infusionstherapie. Die Studienpopulation bestand zu 74,4% aus Patienten in WHO FC III und zu 25,6% aus Patienten in WHO FC IV. Der REVEAL Lite 2 Risk-Score lag bei 2,3% der Teilnehmer unter 9, bei 67,4% bei 9 bis 10 und bei 30,2% bei 11 oder darüber. Von der ZENITH-Studie ausgeschlossen waren Patienten, bei denen eine mit dem humanen Immundefizienzvirus (HIV) verbundene PAH, eine mit portaler Hypertonie verbundene PAH, eine pulmonale venookklusive Erkrankung oder eine pulmonalkapilläre Hämangiomatose oder offensichtliche Anzeichen einer Kapillar- und/oder Venenbeteiligung diagnostiziert wurden.
Primärer Wirksamkeitsendpunkt war die Zeit bis zum ersten "Ereignis" eines zusammengesetzten Endpunkts, d.h. bis zum/zur (i) Tod jeglicher Ursache, (ii) Lungentransplantation oder (iii) Hospitalisierung von ≥24 Stunden infolge einer Verschlechterung der PAH. Winrevair senkte das Risiko des primären Endpunkts gegenüber Placebo um 76% (HR: 0,24; 95% CI: 0,13; 0,43; p<0,0001) (siehe Tabelle 5). Zum Zeitpunkt des data cutoff hatten in der Winrevair-Behandlungsgruppe (15 [17,4%]) weniger Teilnehmer ein primäres Endpunktereignis als in der Placebogruppe (47 [54,7%]).
Aufgrund der niedrigen Ereignisrate in der Winrevair-Behandlungsgruppe war eine Schätzung der medianen Zeit bis zum ersten Ereignis des primären kombinierten Endpunktes nicht möglich; in der Placebogruppe betrug die mediane Zeit bis zum ersten Ereignis 9,6 Monate (95% KI: 6,2; 14,8). Die Kaplan-Meier-Kurven begannen sich ungefähr in Woche 5 zu separieren, und dieser Abstand vergrösserte sich im weiteren Verlauf der Studie (siehe Abbildung 3). Der Behandlungseffekt von Winrevair war in allen vorab festgelegten Subgruppen konsistent (siehe Abbildung 4).
Tabelle 5: Komponenten des primären Endpunktes
Winrevair (N=86) n Placebo (N=86) n (%) Hazard Ratio (95%
(%) KI) p-Wert*
Anzahl (%) Teilnehmer mit ≥1 15 (17,4) 47 (54,7) 0,24 (0,13; 0,43)<0,
primären Ereigniswährend oder 0001
nach ZENITH
Komponente des primären Endpunkts†
Tod jeglicher Ursache‡ 7 (8,1) 13 (15,1)
Lungentransplantation 1 (1,2) 6 (7,0)
Hospitalisierung von ≥24 Stunden 8 (9,3) 43 (50,0)
infolge PAH-Verschlechterung
* Die Analyse des primären kombinierten Endpunkts umfasst das erste Auftreten eines bestätigten Morbiditäts-Mortalitäts-Ereignisses bis zum data cutoff.
† Zeigt jede Komponente des kombinierten primären Endpunkts als eigenständiges Ergebnis. Ein Teilnehmer wird in mehr als einer Zeile aufgeführt, wenn mehrere Ereignisse beobachtet wurden, die der Definition des primären Endpunkts entsprechen.
‡ Umfasst alle Todesfälle bis zum data cut off, mit Ausnahme derjenigen nach Lungentransplantation oder nach Aufnahme in SOTERIA.
Abbildung 3: Zeit bis zum ersten Ereignis eines Todes jeglicher Ursache, einer Lungentransplantation oder einer Hospitalisierung von ≥24 Stunden infolge einer Verschlechterung der PAH: Kaplan-Meier Plot

n= Anzahl subjects at risk
Abbildung 4: Zeit bis zum primären Ereignis nach Hazard Ratio in Subgruppen

Subgruppenanalysen wurden nicht angezeigt, wenn die Anzahl der Teilnehmer in der Subgruppenkategorie weniger als 10% des FAS betrug. Teilnehmer mit einem REVEAL Lite 2.0 Risk-Score <9 beim Screening wurden für die Analysen unter "9 bis 10" gruppiert.
Gemäss vordefinierter Kriterien wurde die Studie bei der Interimsanalyse aufgrund der positiven Wirksamkeit für den primären Endpunkt frühzeitig abgebrochen. Die primäre Analyse des ersten sekundären Endpunkts in der hierarchischen Teststrategie, das Gesamtüberleben (OS), umfasste alle Todesfälle bis zum data cutoff, mit Ausnahme derjenigen, die nach Lungentransplantation oder Aufnahme in eine Langzeit-Follow-up-Studie auftraten. Es wurden 20 Ereignisse beobachtet (7 Ereignisse in der Winrevair-Behandlungsgruppe und 13 Ereignisse in der Placebogruppe). Der Punktschätzer für die OS HR favorisierte die Winrevair-Behandlungsgruppe gegenüber der Placebogruppe (HR: 0,42; 95%-KI: 0,17; 1,07; p=0,0313), aber eine statistische Signifikanz bei der Interimsanalyse (p<0,0021) wurde nicht erzielt. Die Kaplan-Meier-Kurven begannen sich vor Woche 20 zu separieren und blieben für den Rest der Studie getrennt (Abbildung 5).
Die Ergebnisse der Sensitivitätsanalyse des OS, einschliesslich aller Todesfälle bis zum data cutoff, einschliesslich nach Lungentransplantation oder Aufnahme in eine Langzeit-Follow-up-Studie, stimmten mit den Ergebnissen der Primäranalyse überein.
Weitere sekundäre Endpunkte umfassten Verbesserungen des transplantationsfreien Überlebens, NT-proBNP, des mittleren pulmonalen arteriellen Drucks (PAP), PVR, 6MWD, der kardialen Leistung und der WHO FC.
In Woche 24 begünstigte die Punkt-Schätzung für das transplantationsfreie Überleben die Winrevair-Behandlungsgruppe gegenüber der Placebo-Gruppe (HR: 0,34; 95%-KI: 0,15; 0,78). Der mediane Behandlungsunterschied im NT-proBNP zwischen der Winrevair- und der Placebo-Gruppe betrug -2339,1 pg/ml (95%-KI: -3378,7 bis -1299,4). Der mediane Behandlungsunterschied im mittleren PAP zwischen der Winrevair- und der Placebo-Gruppe betrug -21,2 mm Hg (95%-KI: -27,8 bis -14,6). Der mediane Behandlungsunterschied in PVR zwischen der Winrevair- und der Placebo-Gruppe betrug -339,6 dyn•sec/cm5 (95%-KI: -511,1 bis -168,1). Der mediane Behandlungsunterschied in 6MWD zwischen der Winrevair- und der Placebo-Gruppe betrug 63,0 m (95%-KI: 23,2 bis 102,7). Der mediane Behandlungsunterschied in der kardialen Leistung zwischen der Winrevair- und der Placebo-Gruppe betrug 0,5 l/min (95%-KI: -0,2 bis 1,2). Eine Verbesserung der WHO FC gegenüber dem Ausgangswert trat bei 55,8% der Patienten in der Winrevair-Gruppe im Vergleich zu 27,9% in der Placebo-Gruppe auf.
Abbildung 5: Kaplan-Meier-Plot zum Gesamtüberleben (OS)

n= Anzahl subjects at risk
|





