ZusammensetzungWirkstoffe
Levomethadonhydrochlorid.
Hilfsstoffe
Methyl-4-hydroxybenzoat (E 218) (1,50 mg pro ml Lösung), Betainhydrochlorid, Glycerol 85% (E 422), gereinigtes Wasser.
Indikationen/AnwendungsmöglichkeitenMittelstarke bis starke akute und prolongierte Schmerzen bzw. bei ungenügender Wirksamkeit nicht-opioider Analgetika und/oder schwacher Opioide, wie z.B. bei:
·starken Schmerzzuständen, Nieren- und Gallenkoliken, postoperativen Schmerzen;
·starken Schmerzzuständen, die als Folge maligner Geschwüre auftreten.
Orale Substitutionsbehandlung bei Opioidabhängigkeit, im Rahmen einer medizinischen, sozialen und psychologischen Behandlung.
Dosierung/AnwendungLevomethadon ist auf Massebasis (mg) etwa doppelt so wirksam wie Methadon (Razemat aus Levomethadon und Dextromethadon). Bei der Umstellung von Methadon-Razemat auf Levomethadon ist daher die bisherige Dosis zu halbieren.
Schmerzbehandlung
Behandlungsziele und Unterbrechung der Behandlung
Vor Beginn der Behandlung mit L-Polamidon sollte in Übereinstimmung mit den Leitlinien für die Schmerzbehandlung mit dem Patienten eine Behandlungsstrategie vereinbart werden, die die Behandlungsdauer und die Behandlungsziele umfasst. Während der Behandlung sollte ein regelmässiger Kontakt zwischen Arzt und Patient bestehen, um die Notwendigkeit einer Fortsetzung der Behandlung zu beurteilen, ein Absetzen des Arzneimittels in Erwägung zu ziehen und gegebenenfalls die Dosierung anzupassen. Wenn ein Patient die Behandlung mit L-Polamidon nicht länger benötigt, kann es ratsam sein, die Dosis schrittweise zu reduzieren, um Entzugserscheinungen zu vermeiden (siehe «Warnhinweise und Vorsichtsmassnahmen»). Bei unzureichender Schmerzkontrolle sollte die Möglichkeit einer Gewöhnung (Toleranz) und eines Fortschreitens der Grunderkrankung in Betracht gezogen werden (siehe «Warnhinweise und Vorsichtsmassnahmen»).
Erwachsene und Jugendliche über 16 Jahre
Als Analgetikum soll L-Polamidon in der kleinsten effektiven Dosis angewendet werden, um eine Abhängigkeit und Toleranzentwicklung zu vermeiden. Eine Dosisanpassung muss bei jungen und älteren Patienten (ab 65 Jahren) sowie bei gleichzeitiger Applikation von Medikamenten, die auf das ZNS hemmend wirken, vorgenommen werden. Abhängig von der individuellen Situation können höhere Dosen als die üblichen Maximaldosen notwendig sein.
Einzeldosis: 1,25-7,5 mg (0,25-1,5 ml Lösung zum Einnehmen), bei Bedarf bis 3-mal täglich.
Maximale Einzeldosis: 10 mg (2 ml Lösung zum Einnehmen).
Übliche maximale Tagesdosis: 30 mg (6 ml Lösung zum Einnehmen).
Umstellung von anderen starken Opioiden
Die in klinischen Leitfäden verfügbaren Empfehlungen zur Umstellung von einem oral oder parenteral verabreichten Opioid auf L-Polamidon können nur als Orientierungshilfe dienen, da deren relative Wirkstärke von Patient zu Patient variieren kann. Grundsätzlich sollte der Bedarf eines Patienten an L-Polamidon über 24 Stunden eher niedriger angesetzt werden. In der Regel wird mit der Hälfte der geschätzten Tagesdosis begonnen und anschliessend unter klinischer Kontrolle individuell auftitriert.
Substitutionsbehandlung bei Opioidabhängigkeit
Erwachsene und Jugendliche über 16 Jahre
Erfahrungsgemäss brauchen diese Patienten eine sorgfältige Überwachung bzw. Unterstützung. Aus Sicherheitsgründen wird empfohlen, die Medikation täglich in der Praxis unter Aufsicht durchzuführen und L-Polamidon nach Möglichkeit nur in trinkfertiger Form für kurze Zeit abzugeben.
Ausserdem ist auf die Risiken der Kombination mit anderen Drogen und/oder Alkohol hinzuweisen.
Zu Beginn und im Verlauf einer Substitutionsbehandlung soll der zusätzliche Konsum anderer psychotroper Substanzen zur Abschätzung der möglichen Interaktionen und der benötigten Dosierung von L-Polamidon thematisiert und auf die Gefahren hingewiesen werden (siehe auch «Interaktionen»).
Besonders während der ersten fünf Tage der Therapieeinstellung sollte die Dosiseinnahme engmaschig kontrolliert werden bzw. unter Sicht erfolgen. Ein Therapiebeginn zu Wochenanfang vermeidet den Wochenendunterbruch während der Therapieeinstellung.
Therapiebeginn bei Opioid-abhängigen Patienten ohne Vorbehandlung
Die Substitution mit L-Polamidon ist mit folgender Dosis zu beginnen:
·10 mg (2 ml Lösung zum Einnehmen) einmal täglich,
·bei hoher Toleranz 15 mg (3 ml Lösung zum Einnehmen) einmal täglich,
·bei unsicherer Toleranz 5-7,5 mg (1-1,5 ml Lösung zum Einnehmen) einmal täglich.
Bei Verdacht auf eine hohe Opioidtoleranz oder einen schnellen Metabolismus kann die Patientin bzw. der Patient nach 4 Stunden noch einmal einbestellt werden; liegen noch eindeutige Entzugssymptome vor, kann bis zu 10 mg (entsprechend 2 ml Lösung zum Einnehmen) zusätzlich verabreicht werden.
Die tägliche Dosissteigerung soll nicht mehr als 2,5-5 mg (0,5-1 ml Lösung zum Einnehmen) betragen. Leitsymptome für eine Dosissteigerung sind objektive und subjektive Entzugssymptome und zusätzlich konsumierte Opioide. Bei Intoxikationszeichen ist die Dosis unverzüglich zu reduzieren.
Die tägliche Dosis muss klinisch ermittelt werden und beträgt mindestens 30-40 mg (6-8 ml Lösung zum Einnehmen) einmal täglich, wobei auch niedrigere Dosierungen ausreichend bzw. hohe Dosen über 60 mg (über 12 ml Lösung zum Einnehmen) einmal täglich nötig sein können.
Therapiebeginn bei vorbehandelten Opioid-abhängigen Patienten
Eine Umstellung von einer laufenden Substitutionsbehandlung auf L-Polamidon sollte von einem Tag zum anderen erfolgen.
Levomethadon ist in der Substitutionstherapie im Mittel ca. 12-16x stärker wirksam verglichen mit Morphin, wobei die nötige Dosierung immer individuell, ausgehend von der kleinsten effektiven Dosis, unter Berücksichtigung von Entzugs- und Intoxikationssymptomen klinisch ermittelt werden muss.
Weiter muss die lange und je nach Anzahl der Dosierungen variierende Halbwertszeit von Levomethadon beachtet werden.
Bei einer Umstellung in einem niedrigen Dosisbereich sollte auf eine 50% niedrigere Levomethadon-Dosis als die errechnete umgestellt und individuell auftitriert werden.
Bei Bedarf und guter Verträglichkeit ist die Dosis schrittweise bis zur optimalen Tagesdosis anzupassen.
Bei einer Umstellung von Buprenorphin oder Diamorphin auf L-Polamidon ist die adäquate Dosierung klinisch zu ermitteln.
Fortsetzung der Behandlung
Bei stabilisiertem psychischem und physischem Zustand wird die geeignete Dosierung weitergeführt und je nach Klinik angepasst.
Bei Bezugsunterbrüchen von einem Tag ist eine Dosisanpassung nicht erforderlich. Bei längeren Bezugsunterbrüchen ist die nächste Dosis proportional so zu reduzieren, dass nach 5 Tagen Unterbruch eine Initialdosis von 15 mg (3 ml Lösung zum Einnehmen) erreicht wird. Eine schrittweise Dosiserhöhung bis zur optimalen Tagesdosis sollte wie bei einem Therapiebeginn ohne Vorbehandlung erfolgen.
Ist eine Beendigung der Substitutionstherapie vorgesehen, erfolgt diese über Wochen bis Monate durch schrittweise Dosisreduktionen nach Massgabe der Befindlichkeit und eventuell auftretender Entzugsbeschwerden. Die tägliche Dosis von L-Polamidon kann wöchentlich um 2,5 mg (0,5 ml Lösung zum Einnehmen) reduziert werden. Bei Tagesdosen unter 10-15 mg (2-3 ml Lösung zum Einnehmen) sind kleinere wöchentliche Dosisreduktionen empfehlenswert. Dosisreduktionen sollten erst erfolgen, wenn eventuelle Beschwerden vom vorhergehenden Reduktionsschritt abgeklungen sind (siehe auch «Warnhinweise und Vorsichtsmassnahmen»).
Spezielle Dosierungsanweisungen
Kinder und Jugendliche unter 16 Jahren
Schmerzbehandlung
Die Anwendung von L-Polamidon zur Schmerzbehandlung bei Kindern und Jugendlichen unter 16 Jahren wird aufgrund mangelnder Erfahrung nicht empfohlen.
Substitutionsbehandlung bei Opioidabhängigkeit
Es liegen keine Daten zur Unbedenklichkeit und Wirksamkeit von L-Polamidon zur Substitutionsbehandlung bei Opioid-abhängigen Kindern und Jugendlichen unter 16 Jahren vor.
Das Patientenalter sollte jedoch kein Ausschlusskriterium für eine Substitutionsbehandlung sein. Die Einleitung einer Substitutionsbehandlung entspricht den Empfehlungen für Erwachsene unter vorsichtiger Auftitration und engmaschiger Überwachung.
Ältere Patienten
Bei älteren Patienten (ab 65 Jahren) sollte generell eine niedrigere Dosierung gewählt werden (siehe «Pharmakokinetik»).
Patienten mit Leber- oder Nierenfunktionsstörungen
Bei Patienten mit Nierenerkrankungen oder Lebererkrankungen sollte generell eine niedrigere Dosierung gewählt werden (siehe «Pharmakokinetik»).
Art der Anwendung
Die Lösung zum Einnehmen darf nur oral angewendet werden. Im Allgemeinen erfolgt die Einnahme in mindestens 100 ml Wasser oder Fruchtsaft (z.B. Orangensaft, Himbeersirup).
Die Einzeldosis-Entnahme aus der 100 ml-Flasche erfolgt volumetrisch mit einer geeigneten, graduierten handelsüblichen Einmalspritze über den Luer-Kegeleinsatz.
Aus der 500 ml Glasflasche kann die Entnahme in der Apotheke z.B. über eine handelsübliche kalibrierte Dispensierhilfe erfolgen.
Weitere Hinweise zur Abgabe und Zubereitungen siehe «Sonstige Hinweise».
Kontraindikationen·Überempfindlichkeit gegenüber Levomethadon oder einem der Hilfsstoffe gemäss Zusammensetzung.
·Signifikante Atemdepression.
·Akutes oder schwerwiegendes Asthma bronchiale in einem Umfeld ohne ärztliche Überwachung oder ohne Ausrüstung zur Reanimation.
·Akutes obstruktives oder paralytisches Abdomen.
·Schwere Leberinsuffizienz oder Leberzirrhose mit begleitender Niereninsuffizienz.
·Gleichzeitige Einnahme von Monoaminoxidase-Hemmern oder innerhalb von zwei Wochen nach deren Absetzen (siehe «Interaktionen»).
·Gleichzeitige Anwendung von µ-Opioidrezeptor-Antagonisten oder -Partialagonisten (z.B. Buprenorphin), ausser zur Behandlung einer Überdosierung.
·Während der Schwangerschaft und Stillzeit darf L-Polamidon zur Schmerzbehandlung nicht eingenommen werden (siehe «Schwangerschaft, Stillzeit»).
Warnhinweise und VorsichtsmassnahmenEs ist zu beachten, dass Levomethadon auf Massebasis (mg) etwa doppelt so wirksam ist wie Methadon (Razemat aus Levomethadon und Dextromethadon).
Strenge Indikationsstellung und besondere ärztliche Überwachung sind erforderlich bei:
·Krankheitszuständen, bei denen eine Dämpfung des Atemzentrums vermieden werden muss,
·moderater bis schwerer Beeinträchtigung des Atemzentrums und der Atemfunktion,
·Asthma bronchiale, chronisch obstruktiver Lungenerkrankung, Cor pulmonale, erheblich eingeschränkter Atemreserve, zum Beispiel bei Adipositas permagna, vorbestehender Beeinträchtigung der Atemfunktion, Hypoxie oder Hyperkapnie, obstruktivem Schlafapnoe-Syndrom (OSAS),
·reduziertem Bewusstseinszustand, zum Beispiel bei akuter Alkoholvergiftung,
·erhöhtem Hirndruck, zum Beispiel nach Schädelhirntrauma, aufgrund der Eigenschaft von Opioiden, den Druck der Zerebrospinalflüssigkeit heraufzusetzen,
·Hypotension bei Hypovolämie,
·Bradykardie,
·Phäochromozytom,
·Prostatahypertrophie mit Restharnbildung,
·Pankreatitis,
·Gallenwegserkrankungen,
·entzündlichen Darmerkrankungen,
·Hypothyreose,
·Schwangerschaft und Stillzeit in der Substitutionsbehandlung (siehe «Kontraindikationen» und «Schwangerschaft, Stillzeit»).
Es wird empfohlen, bei Patienten mit Nierenerkrankungen (glomeruläre Filtrationsrate < 90 ml/min/1,73 m2), schweren chronischen Lebererkrankungen (ab Stadium C gemäss Child-Pugh (10-15 Punkte)), in höherem Lebensalter (ab 65 Jahren) oder in reduziertem Allgemeinzustand die Dosierung zu verringern (siehe «Pharmakokinetik»).
Toleranzentwicklung, Arzneimittelabhängigkeit und Missbrauchspotenzial
Levomethadon ist ein Opioid-Analgetikum und birgt selbst ein hohes Suchtpotenzial. Es hat eine lange Halbwertszeit und kann daher akkumulieren. Eine Einzeldosis, die die Symptome lindert, kann bei wiederholter täglicher Einnahme zu einer Akkumulation und möglicherweise zum Tod führen.
Wie bei anderen Opioiden können sich bei wiederholter Anwendung von Levomethadon Toleranz, physische und/oder psychische Abhängigkeit entwickeln. Bei der Behandlung von Schmerzen kann die wiederholte Einnahme von L-Polamidon zu einer Opioidgebrauchsstörung (OUD) führen. Eine höhere Dosis und eine längere Behandlung mit Opioiden können das Risiko erhöhen, eine Opioidgebrauchsstörung zu entwickeln. Vor Beginn der Behandlung L-Polamidon und während der Behandlung sollten mit dem Patienten Behandlungsziele und ein Plan zum Absetzen des Arzneimittels vereinbart werden (siehe Rubrik «Dosierung/Anwendung»). Vor und während der Behandlung sollte der Patient ausserdem über die Risiken und Anzeichen einer Opioidgebrauchsstörung aufgeklärt werden. Die Patienten sollten angewiesen werden, sich an ihren Arzt zu wenden, wenn diese Anzeichen auftreten. Missbrauch oder absichtliche Fehlanwendung von L-Polamidon kann Überdosierung und/oder Tod zur Folge haben. Das Risiko für die Entwicklung einer Opioidgebrauchsstörung ist erhöht bei Patienten mit Substanzgebrauchsstörungen (einschliesslich Alkoholgebrauchsstörung) in der persönlichen oder familiären (Eltern oder Geschwister) Vorgeschichte, bei Rauchern oder bei Patienten mit anderen psychischen Erkrankungen (z.B. Major Depression, Angst und Persönlichkeitsstörungen) in der Anamnese. Die Patienten müssen auf Anzeichen eines Suchtverhaltens (drug-seeking behaviour) überwacht werden (z.B. zu frühes Nachfragen nach Folgerezepten). Hierzu gehört auch die Überprüfung der gleichzeitigen Einnahme von Opioiden und psychoaktiven Arzneimitteln (wie Benzodiazepinen). Bei Patienten mit Anzeichen und Symptomen einer Opioidgebrauchsstörung sollte die Konsultation eines Suchtspezialisten in Betracht gezogen werden.
Atemdepression
Wie bei allen Opioiden besteht ein Risiko für eine klinisch relevante Atemdepression im Zusammenhang mit der Anwendung von L-Polamidon. Eine Atemdepression kann, wenn sie nicht sofort erkannt und behandelt wird, zu Atemstillstand und Tod führen. Die Behandlung einer Atemdepression umfasst je nach klinischem Zustand des Patienten eine engmaschige Beobachtung, unterstützende Massnahmen und die Verabreichung von Opioidantagonisten. Eine schwerwiegende, lebensbedrohliche oder tödliche Atemdepression kann zu jedem Zeitpunkt der Therapie auftreten, das Risiko ist zu Beginn der Therapie oder nach einer Dosiserhöhung am grössten.
Bei Patienten mit atopischer Prädisposition können eine Exazerbation eines bereits bestehenden Asthmas, Hautausschläge und Blutbildveränderungen (Eosinophilie) auftreten.
Schlafbezogene Atemstörungen
Opioide können schlafbezogene Atemstörungen einschliesslich zentraler Schlafapnoe (ZSA) und schlafbezogener Hypoxämie verursachen. Die Anwendung von Opioiden geht mit einer dosisabhängigen Erhöhung des Risikos für eine zentrale Schlafapnoe einher. Bei Patienten mit zentraler Schlafapnoe sollte eine Verringerung der Opioid-Gesamtdosis in Betracht gezogen werden.
Gleichzeitige Anwendung mit zentral dämpfenden Substanzen
Die gleichzeitige Anwendung von Opioiden mit Benzodiazepinen oder anderen zentral dämpfenden Substanzen kann zu starker Sedierung, Atemdepression, Koma und Tod führen. Aufgrund dieser Risiken dürfen Opioide und Benzodiazepine oder andere zentral dämpfende Arzneimittel nur an Patienten, für die keine alternative Behandlungsoption in Frage kommt, begleitend verabreicht werden. Wird entschieden, L-Polamidon begleitend zu Benzodiazepinen oder anderen zentral dämpfenden Arzneimitteln zu verschreiben, sind die jeweils niedrigste wirksame Dosierung und eine minimale Dauer der gleichzeitigen Anwendung zu wählen. Die Patienten müssen engmaschig auf Anzeichen und Symptome von Atemdepression und Sedierung überwacht werden. (siehe «Interaktionen»)
Versehentliche Exposition
Die Patienten und ihre Betreuungspersonen müssen darüber in Kenntnis gesetzt werden, dass L-Polamidon einen Wirkstoff in einer Menge enthält, die tödlich sein kann, dies gilt besonders für Kinder. Patienten und ihre Betreuungspersonen müssen darauf hingewiesen werden, alle Dosiereinheiten für Kinder unerreichbar aufzubewahren und angebrochene oder nicht verwendete Dosiereinheiten ordnungsgemäss zu entsorgen.
Neonatales Opioidentzugssyndrom
Die längere Anwendung von L-Polamidon in der Schwangerschaft kann zu einem neonatalen Opioidentzugssyndrom führen, das potenziell lebensbedrohlich ist, wenn es nicht rechtzeitig erkannt und behandelt wird. Die Therapie sollte gemäss Protokollen erfolgen, die von Neonatologie-Experten entwickelt wurden. Ist der Einsatz von Opioiden bei einer Schwangeren über einen längeren Zeitraum notwendig, weisen Sie die Patientin auf das Risiko des neonatalen Opioidentzugssyndroms hin und stellen Sie sicher, dass die geeignete Behandlung gegebenenfalls zur Verfügung steht.
Nebenniereninsuffizienz
Opioide können eine reversible Nebenniereninsuffizienz hervorrufen, die eine Überwachung und Glukokortikoid-Ersatztherapie erfordert. Symptome der Nebenniereninsuffizienz können u.a. Folgendes umfassen: Übelkeit, Erbrechen, Appetitverlust, Müdigkeit, Schwäche, Schwindel oder niedrigen Blutdruck.
Verminderte Sexualhormone und erhöhtes Prolaktin
Die Langzeitanwendung von Opioiden kann mit erniedrigten Sexualhormon-Spiegeln und einem erhöhten Prolaktinspiegel verbunden sein. Die Symptome beinhalten verminderte Libido, Impotenz oder Amenorrhoe.
Hypoglykämie
Im Zusammenhang mit einer Methadon-Überdosis oder Dosiseskalation ist Hypoglykämie beobachtet worden. Eine regelmässige Überwachung des Blutzuckerspiegels wird bei der Dosiseskalation empfohlen.
Spasmus des Sphincter Oddi/Pankreatits
Opioide können eine Funktionsstörung und einen Spasmus des Sphincter Oddi verursachen, wodurch der intrabiliäre Druck zunimmt und das Risiko für Gallenwegsymptome und Pankreatitis steigt.
Herzrhythmusstörungen
Eine Verlängerung der QT-Zeit im EKG und potenziell lebensbedrohliche ventrikulären Arrhythmien (Torsades de pointes) wurden in seltenen Fällen und bei hohen Dosen von Methadon (Razemat aus Levomethadon und Dextromethadon) beobachtet. Die Patienten sind darauf hinzuweisen, dass sie bei Auftreten von Synkopen, ungewöhnlichen Schwindelepisoden oder Palpitationen umgehend den Arzt kontaktieren sollten.
In den folgenden Situationen ist das Risiko für Herzrhythmusstörungen erhöht und der Nutzen der Behandlung sorgfältig abzuwägen:
·Kongenitale QT-Verlängerung, relevante ventrikuläre Arrhythmien, klinisch relevante Bradykardie, klinisch relevante Herzinsuffizienz mit reduzierter linksventrikulärer Auswurffraktion.
·Elektrolytstörungen (Hypokaliämie, Hypomagnesiämie) und Situationen, die diese begünstigen (z.B. anhaltendes Erbrechen oder Diarrhö, Diuretikatherapie).
·Gleichzeitige Anwendung von Antiarrhythmika der Klassen IA und III und anderen Arzneimitteln, die das QT-Intervall verlängern (siehe «Interaktionen»).
·Gleichzeitige Anwendung von Medikamenten, die potenziell den Metabolismus von Levomethadon hemmen können (siehe «Interaktionen»).
In diesen Situationen sollten vor und zwei Wochen nach Beginn der Behandlung mit L-Polamidon sowie bei Dosiserhöhung und einmal jährlich eine klinische Untersuchung und wenn möglich ein EKG erfolgen. Bei ungeklärten Synkopen sollte die Möglichkeit einer kardialen Ursache in Betracht gezogen werden. Wenn zusätzliche Arzneimittel verändert werden sollen, müssen mögliche Interaktionen, die das QT-Intervall beeinflussen, in Betracht gezogen werden.
Missbrauchspotenzial
L-Polamidon ist ausschliesslich für die orale Einnahme bestimmt. Die missbräuchliche intravenöse Anwendung von L-Polamidon kann zu schweren unerwünschten Wirkungen, auch mit potenziell tödlichem Ausgang, zum Beispiel Sepsis, Venenentzündungen oder Lungenembolien, führen.
Dopingkontrollen
Die Anwendung von L-Polamidon kann bei Dopingkontrollen zu positiven Ergebnissen führen. Zudem kann es bei Anwendung von L-Polamidon als Dopingmittel zu einer Gefährdung der Gesundheit kommen.
Schmerzbehandlung
Hyperalgesie
Opioid-induzierte Hyperalgesie (OIH) tritt auf, wenn ein Opioid-Analgetikum paradoxerweise eine Zunahme der Schmerzen oder eine Steigerung der Schmerzempfindlichkeit verursacht. Dieser Zustand unterscheidet sich von der Toleranz, bei der zur Aufrechterhaltung einer bestimmten Wirkung höhere Opioiddosen erforderlich sind. Zu den Symptomen der OIH gehören unter anderem eine Zunahme der Schmerzen bei Erhöhung der Opioiddosis, eine Abnahme der Schmerzen bei Verringerung der Opioiddosis oder Schmerzen bei normalerweise nicht schmerzhaften Reizen (Allodynie). Wenn bei einem Patienten der Verdacht auf eine OIH besteht, ist eine Verringerung der Opioiddosis oder eine Opioidrotation zu prüfen.
Substitutionsbehandlung bei Opioidabhängigkeit
Besondere Risiken bei Patienten unter Substitutionsbehandlung
Die Einnahme von hohen Dosen von L-Polamidon durch nicht Opioid-tolerante Personen ist lebensgefährlich und kann zum Tod durch Atemstillstand führen (siehe auch «Überdosierung»).
Der Patient ist darüber aufzuklären, dass der gleichzeitige Konsum von illegalen Opioiden, Benzodiazepinen, Alkohol oder anderen zentral dämpfenden Substanzen oder Arzneimitteln in Anbetracht der Potenzierung der Atemdepression zum Tod durch Atemstillstand führen kann (siehe «Interaktionen»). Informationen über alle früher oder aktuell konsumierten psychotropen Substanzen sowie über alle eingenommenen Arzneimittel sind von grösster Wichtigkeit zur Abschätzung von Interaktionen.
Bei der Substitutionsbehandlung ist besonders aufmerksam auf das Auftreten von Symptomen, die auf eine Überdosierung hinweisen, sowie auf Entzugssymptome zu achten. Die Patienten müssen daher engmaschig ärztlich überwacht werden und, falls angemessen, muss die Dosierung entsprechend angepasst werden (siehe «Dosierung/Anwendung»). Nur das Fehlen von Entzugssymptomen erlaubt es den Patienten, auf zusätzlichen Opioidkonsum zu verzichten.
Bei Beendigung der Substitutionsbehandlung ist eine langsame Dosisreduktion über Wochen bis Monate angezeigt (siehe «Dosierung/Anwendung»). Die Patienten müssen über den Toleranzverlust und die erhöhte Gefahr einer Überdosierung bei erneutem Opioidkonsum informiert werden.
Gleichzeitige Substitutions- und Schmerzbehandlung
Schmerzen sind grundsätzlich nach dem WHO-Schema zu behandeln. Aufgrund der Kreuztoleranz für die analgetische Wirkung von Opioiden müssen solche zur Erreichung der Schmerzfreiheit meist in einer hohen Dosierung verabreicht werden. Die Substitutionsdosierung soll beibehalten und nicht reduziert werden.
Abhängigkeitsstörungen können eine Hyperalgesie begünstigen.
InteraktionenPharmakodynamische Interaktionen
Die gleichzeitige Anwendung anderer, das ZNS beeinflussende Arzneimittel wie andere Opioide, Sedativa, wie Benzodiazepine oder Hypnotika, Allgemeinanästhetika, Phenothiazine, Tranquilizer, Skelettmuskelrelaxantien, sedierende Antihistaminika, Gabapentinoide (Gabapentin und Pregabalin) und Alkohol kann additive dämpfende Effekte ergeben, die zu Atemdepression, Hypotonie, starker Sedierung oder Koma führen und manchmal tödlich verlaufen können (siehe «Warnhinweise und Vorsichtsmassnahmen»).
L-Polamidon ist nicht für die gleichzeitige Therapie mit MAO-Hemmern oder innerhalb 14 Tagen nach Unterbruch solcher Therapie vorgesehen (siehe auch «Kontraindikationen»).
Bei gleichzeitiger Einnahme von QTc-Zeit verlängernden Arzneimitteln ist das Arrhythmierisiko erhöht (siehe «Warnhinweise und Vorsichtsmassnahmen» und «Eigenschaften/Wirkungen»):
Antiarrhythmika der Klassen IA (z.B. Chinidin, Disopyramid, Procainamid u.a.) und III (z.B. Amiodaron, Sotalol), gewisse Neuroleptika (z.B. Phenothiazin, Thioridazin), bestimmte Antidepressiva, bestimmte antimikrobielle Wirkstoffe (Moxifloxazin, Sparfloxacin, Erythromycin i.v., Pentamidin, Malariamittel, besonders Halofantrin), bestimmte Antihistaminika (Mizolastin) und andere (Cisaprid, Vincamin i.v.) (siehe auch «Warnhinweise und Vorsichtsmassnahmen»).
Die gleichzeitige Anwendung von partiellen Agonisten der µ-Opioidrezeptoren (z.B. Buprenorphin) kann die Wirksamkeit von Levomethadon reduzieren und ggf. zu Entzugserscheinungen führen. Buprenorphin darf frühestens 20 Stunden nach Absetzen von L-Polamidon angewendet werden.
Die mögliche blutdrucksenkende Wirkung von Levomethadon kann durch Antihypertensiva wie Clonidin, Urapidil und Prazosin verstärkt werden.
Ein Serotonin-Syndrom kann auftreten bei gleichzeitiger Verabreichung von Opioiden mit Monoaminoxidase-Hemmern (MAO-Hemmern) und serotonergen Wirkstoffen, wie selektiven Serotonin-Wiederaufnahmehemmern (SSRI), Serotonin-Norepinephrin-Wiederaufnahmehemmern (SNRI) und trizyklischen Antidepressiva (TCA). Zu den Symptomen eines Serotonin-Syndroms können Änderungen des Bewusstseinszustands, autonome Instabilität, neuromuskuläre Anomalien und/oder gastrointestinale Symptome gehören.
Pharmakokinetische Interaktionen
Bei gleichzeitiger Anwendung von Levomethadon mit weiteren Arzneimitteln bzw. Substanzen, die durch Leberenzyme metabolisiert werden oder die Proteinbindung beeinflussen können (Levomethadon wird überwiegend an alpha-saures Glykoprotein und Albumin gebunden, siehe «Pharmakokinetik»), sowie nach Absetzen dieser Arzneimittel bzw. Substanzen werden eine sorgfältige Überwachung der Patienten in Hinblick auf klinische Symptome von Überdosierungen, Unterdosierungen bzw. Entzugssymptome und eine entsprechende Dosisanpassung empfohlen.
Durch Arzneimittel und Substanzen, die den enzymatischen Abbau von Levomethadon in der Leber (Cytochrom-P450-System) hemmen, kann die Plasmakonzentration von Levomethadon erhöht bzw. die Wirkdauer verlängert werden, wie z.B. durch:
·Cimetidin,
·Azol-Antimykotika (z.B. Fluconazol, Itraconazol, Voriconazol),
·Makrolidantibiotika (u.a. Erythromycin, Clarithromycin),
·Antiarrhythmika (über CYP3A4: Amiodaron, Lidocain; über CP2D6: Flecainid, Propafenon),
·Antidepressiva der Klasse der Serotoninwiederaufnahmehemmer wie z.B. Sertralin, Fluvoxamin, Fluoxetin und Paroxetin,
·Ciprofloxacin,
·Amitriptylin,
·Cannabidiol.
Beim Menschen wird Levomethadon durch mehrere CYP-Isoenzyme N-demethyliert, wobei CYP3A4, CYP2B6, CYP2C19 und CYP2D6 eine wesentliche Rolle spielen. Durch Arzneimittel und Substanzen, die den enzymatischen Abbau von Levomethadon in der Leber fördern (Enzyminduktoren), kann die Plasmakonzentration von Levomethadon verringert bzw. die Wirkdauer verkürzt werden. Daher ist mit Entzugserscheinungen zu rechnen bei gleichzeitiger Anwendung von Levomethadon mit z.B.:
·Carbamazepin,
·Phenobarbital,
·Phenytoin,
·Rifampicin,
·Johanniskraut,
·Fusidinsäure,
·Spironolacton,
·Nevirapin,
·Efavirenz,
·HIV-Proteaseinhibitoren (Fosamprenavir, Ritonavir, Nelfinavir),
·Kontrazeptiva (Östrogene),
·Metamizol.
Bei gleichzeitiger Anwendung von Methadon (als Methadonrazemat) und antiretroviralen Arzneimitteln wurde beschrieben, dass sich bei unveränderter Plasmakonzentration von Methadon die Plasmakonzentration der antiretroviralen Arzneimittel entweder erniedrigt (Didanosin und Stavudin) oder erhöht (Zidovudin). Für diese Patienten ist eine engmaschige Überwachung auf adäquates klinisches Ansprechen auf die Behandlung mit Levomethadon bzw. auf Anzeichen einer Toxizität von Levomethadon erforderlich.
Schwangerschaft, StillzeitSchwangerschaft
Tierexperimentelle Studien mit Methadon (dem Razemat aus Levomethadon und Dextromethadon) haben eine Reproduktionstoxizität gezeigt (siehe «Präklinische Daten»).
Methadon bzw. Levomethadon passiert die Plazenta.
Epidemiologische Studien zum Risiko von Herz- und anderen angeborenen Missbildungen bei Kindern, die in der Gebärmutter Methadon ausgesetzt sind, sind widersprüchlich und nicht ausreichend, um einen kausalen Zusammenhang zwischen Methadoneinnahme bei Schwangeren und dem Risiko von Herz- und anderen angeborenen Missbildungen herzustellen.
Die längere Anwendung von L-Polamidon in der Schwangerschaft kann zu einem neonatalen Opioidentzugssyndrom führen, das potenziell lebensbedrohlich ist, wenn es nicht rechtzeitig erkannt und behandelt wird. Die Therapie sollte gemäss Protokollen erfolgen, die von Neonatologie-Experten entwickelt wurden. Ist der Einsatz von Opioiden bei einer Schwangeren über einen längeren Zeitraum notwendig, weisen Sie die Patientin auf das Risiko des neonatalen Opioidentzugssyndroms hin und stellen Sie sicher, dass die geeignete Behandlung gegebenenfalls zur Verfügung steht (siehe auch «Warnhinweise und Vorsichtsmassnahmen»).
Schmerzbehandlung
Zur Schmerzbehandlung darf L-Polamidon während der Schwangerschaft nicht angewendet werden (siehe «Kontraindikationen»).
Substitutionsbehandlung bei Opioidabhängigkeit
Bei schwangeren Opioidabhängigen ist die Einleitung bzw. die Fortsetzung einer Substitutionsbehandlung empfohlen. Eine ausreichende Substitution zur Vermeidung von Entzugssymptomen verringert das Ausmass der Schädigung des Fötus.
Aufgrund der physiologischen Änderungen während der Schwangerschaft (siehe «Pharmakokinetik») kann es notwendig sein, die Dosis zu erhöhen oder die Tagesdosis aufzuteilen.
Stillzeit
Levomethadon tritt in geringen Mengen in die Muttermilch über.
Für Methadon (das razemische Gemisch von Levomethadon und Dextromethadon) wurden unerwünschte Wirkungen einschliesslich Atemdepression und Bewusstseinsstörungen, die tödlich sein können, bei Säuglingen berichtet, die Methadon mit der Muttermilch aufgenommen hatten. Als Faktoren, die dazu beigetragen haben könnten, wurden die Anwendung von ZNS-dämpfenden Arzneimitteln, die genetische Konstitution und Überdosierung beobachtet.
Schmerzbehandlung
Zur Schmerzbehandlung darf L-Polamidon während der Stillzeit nicht angewendet werden (siehe «Kontraindikationen»).
Substitutionsbehandlung bei Opioidabhängigkeit
Während der Behandlung mit Levomethadon sollte das Stillen vermieden werden. Falls die Mutter bis zum Ende der Schwangerschaft mit Levomethadon behandelt wurde, kann das Stillen in Betracht gezogen werden, um ein neonatales Entzugssyndrom abzumildern. Zur Entscheidungsfindung, ob das Stillen unter Levomethadon empfohlen werden kann, sollte der Rat eines klinischen Spezialisten eingeholt werden. Des Weiteren ist zu berücksichtigen, ob die Frau auf eine stabile Levomethadon-Erhaltungsdosis eingestellt ist und ob sie weiterhin eine illegale Substanz anwendet. Wenn das Stillen in Betracht gezogen wird, sollte die Levomethadon-Dosis so niedrig wie möglich gewählt werden. Verschreibende Ärzte sollten stillende Frauen darauf hinweisen, ihr Kind hinsichtlich Sedierung und Schwierigkeiten beim Atmen zu beobachten und im Fall eines Auftretens sofort ärztliche Hilfe in Anspruch zu nehmen. Obwohl die Menge an Levomethadon, die in die Muttermilch übertritt, nicht zur vollständigen Unterdrückung der Entzugserscheinungen bei gestillten Säuglingen ausreicht, kann es die Schwere eines neonatalen Entzugssyndroms mildern. Falls ein Abstillen erforderlich ist, sollte dieses schrittweise erfolgen, da eine plötzliche Entwöhnung die Entzugserscheinungen beim Säugling verstärken könnte.
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von MaschinenL-Polamidon hat einen ausgeprägten Einfluss auf die Fahrtüchtigkeit oder die Fähigkeit, Maschinen zu bedienen. Dies ist insbesondere zu Beginn der Therapie, nach Dosiserhöhung oder einer Umstellung auf L-Polamidon sowie beim Zusammenwirken von L-Polamidon mit Alkohol oder anderen ZNS-dämpfenden Substanzen zu erwarten. Deshalb sollten Patienten mit ihrem behandelnden Arzt besprechen, ob sie Auto fahren oder Maschinen bedienen dürfen.
Unerwünschte WirkungenDie Häufigkeiten sind eingeteilt in «häufig» (≥1/100, <1/10), «gelegentlich» (≥1/1'000, <1/100), «selten» (≥1/10'000, <1/1'000), «sehr selten» (<1/10'000), «nicht bekannt» (Häufigkeit aufgrund der verfügbaren Daten nicht abschätzbar).
Erkrankungen des Blutes und des Lymphsystems
Selten: bei Langzeitanwendung Lymphozytose, Hyperalbuminämie, Hyperglobulinämie.
Erkrankungen des Immunsystems
Häufigkeit nicht bekannt: Überempfindlichkeitsreaktionen bis hin zum Schock.
Stoffwechsel- und Ernährungsstörungen
Häufigkeit nicht bekannt: Appetitlosigkeit, Hypoglykämie.
Psychiatrische Erkrankungen
Gelegentlich: Unruhe, Dysphorie, Euphorie.
Häufigkeit nicht bekannt: Verwirrtheit, Desorientiertheit, Schlaflosigkeit, Arzneimittelabhängigkeit.
Erkrankungen des Nervensystems
Gelegentlich: Schläfrigkeit, Sedierung, Nervosität, Schwindel.
Häufigkeit nicht bekannt: Benommenheit, Kopfschmerzen, Krämpfe.
Augenerkrankungen
Häufigkeit nicht bekannt: Sehstörungen, Miosis.
Herzerkrankungen
Gelegentlich: Hypotonie.
Selten: Verlängerung der QT-Zeit im EKG/ventrikuläre Arrhythmien (Synkopen), Torsades de pointes (siehe «Warnhinweise und Vorsichtsmassnahmen»).
Häufigkeit nicht bekannt: kardiovaskuläre Insuffizienz, Palpitationen, Bradykardie, Herzstillstand.
Gefässerkrankungen
Häufigkeit nicht bekannt: orthostatische Hypotonie.
Schock, Sickerblutungen (Hämorrhagie).
Erkrankungen der Atemwege, des Brustraums und Mediastinums
Gelegentlich: Atemdepression, nicht-kardiogenes Lungenödem bei intensivmedizinisch behandelten Patienten.
Häufigkeit nicht bekannt: Atemstillstand, zentrales Schlafapnoe-Syndrom.
Erkrankungen des Gastrointestinaltrakts
Häufig: Übelkeit, Erbrechen, Obstipation.
Häufigkeit nicht bekannt: Mundtrockenheit, Pankreatitis.
Leber- und Gallenerkrankungen
Gelegentlich: Spasmen des Sphincter Oddi, Gallenkoliken.
Erkrankungen der Haut und des Unterhautgewebes
Gelegentlich: Hyperhydrosis.
Häufigkeit nicht bekannt: Urtikaria, Rash, Pruritus.
Erkrankungen der Nieren und Harnwege
Gelegentlich: Harnretention.
Häufigkeit nicht bekannt: verminderte Harnmenge.
Erkrankungen der Geschlechtsorgane und der Brustdrüse
Häufig: bei längerdauernder Anwendung verminderte Libido, Erektionsstörungen.
Sehr selten: Hyperprolaktinämie.
Allgemeine Erkrankungen
Häufigkeit nicht bekannt: Müdigkeit, Schwächeanfälle, Ödeme, Flush.
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von grosser Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdacht einer neuen oder schwerwiegenden Nebenwirkung über das Online-Portal ElViS (Electronic Vigilance System) anzuzeigen. Informationen dazu finden Sie unter www.swissmedic.ch.
ÜberdosierungWie bei allen Opioiden ist die Gefahr einer Intoxikation bzw. Überdosierung für Nicht-Gewöhnte hoch.
Anzeichen und Symptome
Akute Symptome umfassen Miosis, Atemdepression, Somnolenz bis Stupor oder Koma. Weitere mögliche Symptome sind Übelkeit, Erbrechen, Hypotonie, Bradykardie, Verlängerung des QT-Intervalls, Arrhythmien, verminderter Muskeltonus und Darmatonie. Es wurden Hypoglykämien berichtet. In Fällen schwerer Überdosierung können Atemstillstand, nicht-kardiogenes Lungenödem, Kreislaufversagen und Tod eintreten.
Toxische Leukenzephalopathie wurde bei Überdosierung von Opioiden beobachtet
Substitutionsbehandlung bei Opioidabhängigkeit
In der substitutionsgestützten Behandlung können Mischintoxikationen u.a. mit Benzodiazepinen, Alkohol und Kokain auftreten, die die typischen Symptome einer Levomethadon-Intoxikation verschleiern können. Aus diesem Grund muss bei der Abklärung auf die Symptome geachtet werden.
Behandlung
Überwachung von Atmung und Bewusstsein, bei klinisch signifikanter Atem- oder ZNS-Depression: künstliche Beatmung, Stabilisieren des Kreislaufs und Gabe von Naloxon.
Dosierung: 0,4-2 mg Naloxon intravenös (Kinder: 0,01-0,1 mg/kg Körpergewicht).
Falls notwendig 2-3x jeweils nach 2-3 Minuten wiederholen oder als Dauerinfusion verabreichen (siehe entsprechende Fachinformation). In der substitutionsgestützten Behandlung kann es vorkommen, dass aufgrund schlechter oder kollabierter Venen eine intramuskuläre oder intranasale Applikation notwendig ist.
Die Wirkungsdauer von Naloxon ist relativ kurz (Plasmahalbwertszeit: t½ Naloxon = 1-1,5 Stunden, t½ Levomethadon = 16-53 Stunden), die Atemdepression kann langanhaltend sein. Der Patient ist deshalb auch nach Naloxon-Gabe längerfristig zu überwachen und wiederholte Naloxon-Gaben können notwendig sein.
Naloxon sollte mit Vorsicht bei Personen verwendet werden, die möglicherweise einen Langzeitgebrauch mit Opioiden (Toleranz) aufweisen. Eine abrupte oder vollständige Aufhebung der Opioidwirkung kann zu einem akuten Entzugssyndrom führen. Empfohlen wird eine Initialdosis von 0,04 mg Naloxon.
In speziellen Situationen kann nach Einnahme eine primäre Dekontamination mit Aktivkohle in Erwägung gezogen werden.
Eigenschaften/WirkungenATC-Code
N02AC06
Wirkungsmechanismus
Levomethadon ist das wirksame R(-)-Enantiomer von Methadon.
Levomethadon gehört zur Gruppe der stark wirksamen Analgetika vom Morphin-Typ. Methadon bindet selektiv an Opioid-spezifische Rezeptoren (v.a. μ-Agonist) im Gehirn.
Pharmakodynamik
Levomethadon reguliert die Schmerzleitung und Schmerzempfindung durch Stimulation des endogenen schmerzhemmenden Systems. Zentrale Wirkungen sind ferner Sedierung, Atemdepression, Hemmung des Hustenzentrums, Verengung der Pupillen, Erbrechen sowie Antidiurese. In der Peripherie wird der Tonus der glatten Muskulatur erhöht, dadurch wird die Entleerung von Magen-, Gallen- und Harnblase gehemmt und die Darmpassage verlangsamt.
Als Opioid-Agonist erzeugt Levomethadon morphinartige Wirkungen, die bei der Behandlung von opioidabhängigen Personen Entzugssymptome unterdrücken. Die orale Einnahme verhindert zusätzlich einen raschen Konzentrationsanstieg im Gehirn und vermindert so die euphorisierende Wirkung.
Levomethadon blockiert 3,5-mal schwächer die kardialen humanen hERG-Kaliumkanäle (hERG = human ether-a-go-go related gene), die für die Repolarisierung der Herzmuskelzellen verantwortlich sind, als Dextromethadon.
Levomethadon reduziert wie andere Opioide die gastrointestinale Motilität und erhöht den Tonus der glatten Muskulatur, v.a. im Magenantrum und Sphincter Oddi.
Klinische Wirksamkeit
Nach oraler Gabe von Levomethadon erreicht die analgetische Wirkung nach 1-2 Stunden ihr Maximum. Die Analgesiedauer von 4-6 Stunden ist trotz längerer Halbwertszeit gleich lang wie bei Morphin. Bei längerer oraler Applikation kann die Wirkdauer bis auf 22-48 Stunden ansteigen.
PharmakokinetikAbsorption
Levomethadon wird nach oraler Applikation schnell und fast vollständig absorbiert und kann nach ca. einer halben Stunde im Plasma nachgewiesen werden. Maximale Plasmapeaks werden innerhalb von 3 Stunden bei oraler Applikation gefunden. Die mittlere absolute Bioverfügbarkeit beträgt mindestens 80%.
Nach Einmalverabreichung von 5 mg L-Polamidon an gesunde erwachsene Probanden betrug der durchschnittliche maximale Levomethadon-Plasmaspiegel 8,8 ng/ml.
Distribution
Levomethadon hat ein grosses Verteilungsvolumen und die Plasmaproteinbindung beträgt ca. 85%. Die Substanz wird an verschiedene Gewebsproteine - insbesondere im Hirn - gebunden. Dies erklärt die kumulativen Effekte und die langsame Elimination von Methadon. Bei wiederholter Gabe ist eine sorgfältige Dosiseinstellung erforderlich.
Levomethadon passiert die Plazenta und tritt in die Muttermilch über.
Metabolismus
Levomethadon wird in der Leber über das Cytochrom-P450-Enzymsystem (primär über CYP2B6-Enzyme, ausserdem über CYP3A4) hauptsächlich zu den inaktiven Metaboliten 2-Ethyl-1,5-dimethyl-3,3-diphenylpyrrolidin (EDDP) und 2-Ethyl-5-methyl-3,3-diphenylpyralin (EMDP) abgebaut. In geringerem Ausmass spielen CYP2D6 und CYP2C19 eine Rolle.
Elimination
Levomethadon und seine Metaboliten werden überwiegend mit dem Urin und über die Faeces ausgeschieden. Die Methadonausscheidung im Urin ist pH-abhängig, je niedriger der Harn-pH-Wert, desto grösser die Clearance.
Die terminale Halbwertszeit von Levomethadon unterliegt starken individuellen Schwankungen und beträgt 16-53 Stunden.
Kinetik spezieller Patientengruppen
Ältere Patienten
Die terminale Halbwertszeit kann im höheren Alter (ab 65 Jahren) verlängert sein.
Schwangerschaft
Mit zunehmender Dauer der Schwangerschaft können die gastrointestinale Resorption erniedrigt und die Verteilung und die Clearance (durch Induktion vom CYP3A4-Isoenzym) von Levomethadon erhöht sein.
Genetische Polymorphismen
Bei langsamen CYP2B6-Metabolisierern (7-8% aller Kaukasier) sind höhere Levomethadon-Plasmaspiegel und ein erhöhtes Risiko für unerwünschte Wirkungen möglich.
Leberfunktionsstörung
Da Levomethadon in der Leber metabolisiert wird, besteht bei Patienten mit schweren chronischen Lebererkrankungen das Risiko erhöhter Levomethadon-Plasmaspiegel.
Nierenfunktionsstörung
Besteht eine Niereninsuffizienz, wird Levomethadon vermehrt über die Galle ausgeschieden. Bei Anurie wurden keine erhöhten Plasmakonzentrationen beobachtet. Die Kumulationsgefahr scheint daher gering zu sein. Aufgrund der limitierten Datenlage kann jedoch das Risiko erhöhter Levomethadon-Plasmaspiegel bei Nierenfunktionsstörung nicht ausgeschlossen werden.
Levomethadon ist nur geringfügig dialysierbar. Modellberechnungen zufolge werden während einer vierstündigen Hämodialyse ca. 12 ng/ml Methadon (bezogen auf das Razemat aus Levomethadon und Dextromethadon) aus dem systemischen Kreislauf entfernt.
Präklinische DatenPräklinisch wurde Levomethadon nicht ausreichend untersucht. Zur Bewertung der präklinischen Sicherheit können jedoch Erkenntnisse zu Methadon (dem Razemat aus Levomethadon und Dextromethadon) herangezogen werden.
Mutagenität und Karzinogenität
In vitro- und in vivo-Untersuchungen zur Genotoxizität von Methadon ergaben teilweise widersprüchliche Befunde mit Hinweisen auf ein schwach klastogenes Potenzial. Ein Risiko für den Menschen lässt sich nach derzeitigem Kenntnisstand daraus nicht ableiten. Langzeitstudien an Maus und Ratte zeigten keine karzinogenen Eigenschaften von Methadon.
Reproduktionstoxizität
Die Nachkommen von einigen Tagen vor der Paarung mit Methadon behandelten männlichen Nagern (bis zu 38 mg/kg/Tag) zeigten eine erhöhte neonatale Sterblichkeit von bis zu 74%. In Embryotoxizitätsstudien bei Ratten und Kaninchen war Methadon nicht teratogen. Die Verabreichung von Methadon an Labortiere während der Trächtigkeit bzw. der Säugezeit führte jedoch zu Exenzephalie (Hamster und Maus), embryotoxischen Effekten und einer erhöhten neonatalen Sterblichkeit sowie zu einer verzögerten körperlichen und neurologischen postnatalen Entwicklung bei den Jungtieren. Die Befunde korrelierten mit dem Auftreten einer maternalen Toxizität.
Sonstige HinweiseHaltbarkeit
Das Arzneimittel darf nur bis zu dem auf dem Behälter mit «EXP» bezeichneten Datum verwendet werden.
Haltbarkeit nach Anbruch
Nach Anbruch der Flasche ist die Lösung 3 Monate haltbar.
Für die gebrauchsfertigen Zubereitungen wurde die Stabilität wie folgt geprüft und nachgewiesen:
·Mischung mit Himbeersirup: bis zu 7 Tage im Kühlschrank (2-8°C) oder bei Raumtemperatur,
·Mischung mit Orangensaft: bis zu 2 Tage im Kühlschrank (2-8°C) oder bei Raumtemperatur.
Besondere Lagerungshinweise
Nicht über 30°C lagern.
Den Behälter im Umkarton aufbewahren, um den Inhalt vor Licht zu schützen.
Ausser Reichweite von Kindern aufbewahren.
Hinweise für die Handhabung
L-Polamidon, Lösung zum Einnehmen 1 x 100 ml und 3 x 100 ml
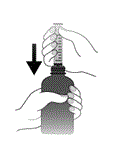
Für die Entnahme der Lösung wird eine handelsübliche Dosierspritze mit Luer-Ansatz ohne Nadel (nicht in der Packung enthalten) benötigt. Es ist dabei folgendermassen vorzugehen:
|
1.
|
Die Spritze auf den Luer-Kegeleinsatz aufsetzen.
|
|
| |
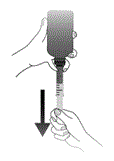
2.
|
Die Flasche mit aufgesetzter Spritze umdrehen und die gewünschte Menge Lösung von unten abziehen.
|
|
| |
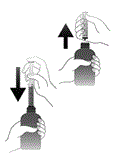
3.
|
Die Flasche mit der Spritze wieder aufrecht hinstellen und ggf. zu viel entnommene Lösung in die Flasche zurückgeben. Die Spritze von der Flasche trennen.
|
|
|
L-Polamidon, Lösung zum Einnehmen 500 ml
Für die Entnahme der Lösung wird eine handelsübliche kalibrierte Dispensierhilfe mit Rundgewinde GL 25 DIN 168 benötigt.
Im Falle einer Mitgabe wird L-Polamidon portionsweise, entsprechend der Tagesdosis, kindergesichert abgefüllt und gekennzeichnet.
Zulassungsnummer65042 (Swissmedic)
PackungenL-Polamidon, Lösung zum Einnehmen 5 mg/ml 1 x 100 ml (A+)
L-Polamidon, Lösung zum Einnehmen 5 mg/ml 3 x 100 ml (A+)
L-Polamidon, Lösung zum Einnehmen 5 mg/ml 1 x 500 ml (A+)
ZulassungsinhaberinSandoz Pharmaceuticals AG, Risch; Domizil: Rotkreuz
Stand der InformationMärz 2024
|



