CompositionPrincipes actifs
Risperidonum.
Excipients
Poudre de principe actif (flacon): Poly (DL-lactidum-co-glycolidum).
Solution pour la mise en suspension de la poudre (seringue pré-remplie): Carmellosum natricum, polysorbatum 20, dinatrii phosphas dihydricus, acidum citricum, natrii chloridum, natrii hydroxidum, aqua ad injectabilia q.s. ad solutionem pro 2 ml. Teneur totale en sodium: 9,872 mg.
Forme pharmaceutique et quantité de principe actif par unitéPoudre et solvant pour la reconstitution d'une suspension injectable à libération prolongée dans une seringue pré-remplie
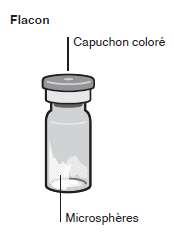
Risperdal Consta contient de la rispéridone incorporée dans des microsphères (billes de polymère), qui la libèrent de façon retardée.
Poudre de principe actif pour la reconstitution de la suspension injectable (flacon): Praeparatio sicca à 25 mg, 37,5 mg ou 50 mg de rispéridone.
Solvant pour la mise en suspension de la poudre (seringue pré-remplie): 2 ml.
Indications/Possibilités d’emploiTraitement d'entretien des maladies psychotiques de type schizophrénique, après instauration du traitement par un neuroleptique à libération non retardée.
Posologie/Mode d’emploiPosologie habituelle
Adultes
La posologie recommandée est de 25 mg en intramusculaire toutes les deux semaines. Certains patients pourront tirer bénéfice d'un dosage plus élevé de 37,5 mg ou de 50 mg. Un dosage de 75 mg n'a montré aucun bénéfice supplémentaire dans les études cliniques, de plus on a observé une incidence légèrement plus élevée d'effets secondaires extrapyramidaux. Les posologies supérieures à 50 mg toutes les deux semaines ne sont pas recommandées.
Attention: Après la 1re injection de Risperdal Consta, un effet clinique thérapeutique ne peut pas être attendu immédiatement, mais seulement après une période de latence de trois ou même quatre semaines. Il est donc nécessaire de compléter la couverture antipsychotique avec un autre antipsychotique pendant cette période ou, si c'est possible, en administrant Risperdal sous forme orale. Lorsque les patients sont déjà traités par un neuroleptique retard, il peut s'avérer judicieux de les placer transitoirement sous traitement oral avant de passer à Risperdal Consta (si le tableau clinique le permet).
Les augmentations de dosage ne doivent pas être effectuées avant 4 semaines, car l'effet de la première injection avec le dosage augmenté met au moins 3 semaines à se manifester.
Instructions posologiques particulières
Patients présentant des troubles de la fonction hépatique ou de la fonction rénale
L'emploi de Risperdal Consta n'a pas été étudié chez les insuffisants hépatiques ou rénaux.
Le schéma suivant est recommandé pour les insuffisants hépatiques ou rénaux nécessitant un traitement par Risperdal Consta: commencer par de la rispéridone orale (sous forme de comprimés ou de solution) à raison de 0,5 mg 2×/jour la 1re semaine, puis passer à 1 mg 2×/jour ou 2 mg 1×/jour la 2e semaine. On peut passer à une injection de Risperdal Consta 25 mg toutes les 2 semaines si le patient tolère bien la dose orale journalière d'au moins 2 mg.
Patients âgés
La posologie recommandée est de 25 mg en intramusculaire toutes les 2 semaines. Après la 1re injection de Risperdal Consta, il est nécessaire de compléter la couverture antipsychotique avec un antipsychotique oral pendant les trois semaines suivantes (phase de latence, voir "Pharmacocinétique" ).
Des patients âgés atteints de symptômes psychotiques dans le cadre d'une démence ont eu un risque de mortalité accru sous traitement par des antipsychotiques atypiques. Risperdal Consta n'est pas autorisé pour traiter les patients souffrant de symptômes psychotiques liés à une démence.
Enfants et adolescents
Aucune expérience n'est encore disponible chez les enfants et les adolescents de moins de 18 ans.
Schéma d'administration
Chez les patients qui n'ont encore jamais reçu de rispéridone, il est recommandé de tester la tolérance à la rispéridone orale avant de commencer le traitement par Risperdal Consta.
Mode d'administration
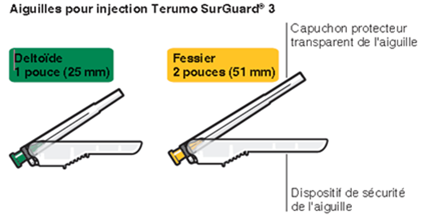
Risperdal Consta doit être administré toutes les deux semaines par injection intramusculaire profonde au niveau du muscle deltoïde ou du muscle fessier. Utiliser à cette fin l'aiguille d'injection adaptée munie d'un dispositif de protection. Pour l'injection au niveau du deltoïde, utiliser l'aiguille de 1 pouce (25 mm) en alternant à chaque fois les injections entre les deux bras. Pour l'injection dans le muscle fessier, utiliser l'aiguille de 2 pouces (51 mm), en alternant l'injection entre chacune des deux fesses. Risperdal Consta ne doit pas être administré par voie intraveineuse (voir "Mises en garde et précautions" , paragraphe "Administration" ). Pour la préparation et l'administration de la suspension, voir "Remarques particulières" : "Remarques concernant la manipulation" .
Contre-indicationsHypersensibilité connue à la rispéridone ou à l'un des excipients.
Patients atteints de démence avec symptômes parkinsoniens tels que rigidité musculaire, bradykinésie et troubles posturaux de type parkinsonien.
Patients atteints de démence avec une suspicion d'une démence à corps de Lewy (outre les symptômes typiques de la démence, présence d'au moins deux des trois symptômes suivants: parkinsonisme, hallucinations visuelles, évolution fluctuante).
Mises en garde et précautionsLorsqu'un patient n'a jamais reçu de rispéridone, il est recommandé d'effectuer un test de tolérance à la rispéridone par voie orale avant de le traiter par Risperdal Consta.
Enfants et adolescents
Faute d'expériences en la matière, Risperdal Consta ne doit pas être administré aux enfants ni aux adolescents de moins de 18 ans.
Patients âgés atteints de démence
Augmentation de la mortalité globale
Une méta-analyse de 17 études contrôlées menées avec des antipsychotiques atypiques y compris Risperdal a montré une mortalité augmentée chez les patients âgés atteints de démence sous antipsychotiques par rapport à ceux sous placebo. Pour cette population, le taux de mortalité dans les études contrôlées par placebo était de 4,0% chez les patients traités par Risperdal administré par voie orale et de 3,1% dans le groupe placebo. Les patients décédés avaient une moyenne d'âge de 86 ans (intervalle 67–100 ans).
Un profil de facteurs de risque spécifique pour la mortalité accrue sous Risperdal n'est pas identifiable. Par contre, les motifs de décès étaient habituels pour le groupe d'âge >65 ans: évènements cardiovasculaires et cérébro-vasculaires, tumeurs, infections (p.ex. pneumonie) et diabète.
Augmentation de la mortalité lors d'administration simultanée de furosémide:
Dans les études contrôlées par placebo menées chez des patients âgés atteints de démence, une augmentation du taux de mortalité a été observée lors d'un traitement simultané par la rispéridone et le furosémide (7,3%; âge moyen 89 ans, intervalle 75–97 ans) comparée à un traitement par rispéridone seule (3,1%; âge moyen 84 ans, intervalle 70–96 ans) ou furosémide seul (4,1%; âge moyen 80 ans, intervalle 67– 90 ans). L'augmentation du taux de mortalité chez les patients traités par rispéridone plus furosémide a été observée dans deux des quatre études cliniques. Aucune augmentation du taux de mortalité n'a été observée chez les patients ayant pris d'autres diurétiques en association à la rispéridone.
Aucun mécanisme physiopathologique évident n'a été identifié pouvant expliquer ce résultat. De même, la cause des décès n'était pas uniforme. Toutefois, la prudence est de mise et le rapport bénéfice/risque de cette association ou du traitement simultané avec d'autres diurétiques puissants doit être évalué avant l'utilisation.
Indépendamment du traitement, une déshydratation était un facteur général de risque pour la mortalité. En conséquence, elle sera soigneusement évitée chez les patients âgés atteints de démence.
Augmentation des accidents vasculaires cérébraux
Dans les études contrôlées par placebo et menées auprès de patients âgés atteints de démence, l'incidence des accidents cérébro-vasculaires (accidents vasculaires cérébraux et accidents ischémiques transitoires [AIT]) y compris ceux avec issue fatale, a été significativement plus élevée chez les patients traités par Risperdal administré par voie orale que chez les patients sous placebo (âge moyen 85 ans; intervalle 73–97 ans).
Hypotension orthostatique
En raison de son activité α1-lytique, la rispéridone peut entraîner une hypotension (orthostatique), notamment durant le premier ajustement posologique. La prudence s'impose chez les patients atteints d'une maladie cardio-vasculaire confirmée (p.ex. insuffisance cardiaque, infarctus du myocarde, trouble de la conduction, déshydratation, hypovolémie ou maladie vasculaire cérébrale) (voir "Effets indésirables" ). L'administration de Risperdal Consta n'est pas recommandée en présence d'un état cardio-vasculaire instable aigu (comme p.ex. lors d'infarctus du myocarde aigu).
En présence d'une hypotension orthostatique persistante et cliniquement manifeste, une évaluation bénéfice/risque s'impose avant de poursuivre le traitement par Risperdal Consta.
Allongement de l'intervalle QT
Dans les études cliniques, la rispéridone n'a pas été associée à un allongement de l'intervalle QTc. Après le lancement, on a très rarement signalé un allongement du QT. Comme pour d'autres antipsychotiques, la prudence est recommandée lorsqu'on prescrit la rispéridone chez les patients atteints d'une maladie cardio-vasculaire et/ou d'une bradycardie, de troubles électrolytiques connus (hypokaliémie, hypomagnésémie) ou présentant un allongement du QT dans leur anamnèse familiale. La prudence est également de rigueur en association avec d'autres médicaments qui allongent l'intervalle QT (voir "Interactions" ).
Leucopénie, neutropénie et agranulocytose
Des cas de leucopénie, de neutropénie et d'agranulocytose ont été rapportés lors de l'utilisation d'antipsychotiques (y compris Risperdal Consta) au cours d'études cliniques et/ou depuis la commercialisation. Une agranulocytose a très rarement été observée (<1/10'000 patients) depuis la commercialisation.
Les patients présentant une diminution cliniquement significative du nombre de globules blancs dans les antécédents ou une leucopénie/neutropénie induite par un médicament doivent être surveillés pendant les premiers mois du traitement. L'arrêt du traitement par Risperdal Consta doit être envisagé dès les premiers signes d'une diminution significative des globules blancs, s'il n'existe pas d'autres facteurs étiologiques.
Les patients présentant une neutropénie cliniquement significative doivent être étroitement surveillés afin de déceler une fièvre ou d'autres symptômes ou signes d'une infection et doivent être immédiatement traités en cas d'apparition de tels symptômes ou signes. Chez les patients présentant une neutropénie marquée (nombre absolu de neutrophiles <1× 109/l), il convient d'arrêter le traitement par Risperdal Consta et de contrôler les globules blancs jusqu'à leur normalisation.
Thromboembolie veineuse
Des cas de thromboembolies veineuses (TEV) ont été rapportés en rapport avec l'utilisation d'antipsychotiques. Étant donné que les patients traités par antipsychotiques présentent fréquemment des facteurs de risques acquis de TEV, il convient d'identifier tous les éventuels facteurs de risque de TEV avant et pendant le traitement par Risperdal Consta et de prendre les mesures de précaution nécessaires.
Dyskinésie tardive/symptômes extrapyramidaux (EPS)
Les médicaments ayant des propriétés antidopaminergiques ont été impliqués dans l'induction d'une dyskinésie tardive, qui peut se manifester par des mouvements rythmiques involontaires, surtout de la langue et/ou du visage. L'apparition de symptômes extrapyramidaux est un facteur de risque de dyskinésies tardives. Si des signes ou symptômes d'une dyskinésie tardive apparaissent, il faut envisager l'interruption de la prise de tous les antipsychotiques.
Symptômes extrapyramidaux et psychostimulants – La prudence est recommandée chez les patients recevant en même temps des psychostimulants (par ex. du méthylphénidate) et de la rispéridone, car des symptômes extrapyramidaux sont susceptibles de survenir lors de l'ajustement de l'un des médicaments ou des deux médicaments. Une diminution progressive de la posologie de l'un des traitements ou des deux traitements doit être envisagée (voir "Interactions" ).
Maladie de Parkinson et démence à corps de Lewy
La prudence est recommandée lorsque Risperdal est prescrit à des patients ayant une maladie de Parkinson ou une démence à corps de Lewy. Risperdal peut provoquer une aggravation de la maladie de Parkinson. Ces deux groupes peuvent présenter un risque accru de syndrome malin des neuroleptiques et une sensibilité accrue aux antipsychotiques (p.ex. avec confusion, émoussement affectif, trouble de l'équilibre avec chutes fréquentes, en plus des symptômes extrapyramidaux).
Syndrome malin des neuroleptiques
Dans de rares cas, les antipsychotiques peuvent provoquer un syndrome malin des neuroleptiques, qui se manifeste par une hyperthermie, une rigidité musculaire, une dystonie neurovégétative, des troubles de la conscience et une élévation des taux sériques de la créatine phosphokinase. D'autres symptômes peuvent être une myoglobinurie (rhabdomyolyse) et une défaillance rénale aiguë. Dans un tel cas, arrêter tous les médicaments antipsychotiques, y compris Risperdal Consta. La rispéridone est encore détectable dans le plasma pendant 6 semaines au moins après la dernière injection de Risperdal Consta.
Réactions d'hypersensibilité
Bien que la tolérance à la rispéridone administrée par voie orale doive être évaluée avant le début du traitement par Risperdal Consta, de très rares cas de réactions anaphylactiques sont survenus pendant la surveillance post-commercialisation chez des patients ayant préalablement bien toléré la rispéridone administrée par voie orale (voir "Posologie/Mode d'emploi" et "Effets indésirables" ). Les symptômes d'anaphylaxie comprennent éruption cutanée, urticaire, œdème périphérique, tuméfaction des yeux, tuméfaction de la langue, tuméfaction du visage, forte sudation (hyperhidrose), détresse respiratoire et chute de la tension artérielle (hypotension).
Les patients présentant une hypersensibilité à la rispéridone orale, à la palipéridone ou à l'un des autres composants de la formulation ou du récipient ne doivent pas être traités par Risperdal Consta (voir "Contre-indications" ).
L'apparition de réactions d'hypersensibilité impose l'arrêt de l'utilisation de Risperdal Consta; des mesures de soutien générales doivent être instaurées en fonction de l'indication clinique et le patient doit être surveillé jusqu'à la disparition des signes et des symptômes (voir "Contre-indications" et "Effets indésirables" ).
Hyperglycémie et diabète sucré
Une hyperglycémie, un diabète sucré et l'exacerbation d'un diabète préexistant ont été rapportés pendant le traitement par Risperdal Consta. L'évaluation de la relation entre l'utilisation d'antipsychotiques atypiques et des anomalies du glucose est compliquée par la possibilité d'une élévation du risque de fond de diabète chez les patients schizophrènes et par l'incidence croissante du diabète dans la population générale. Vu ces facteurs de confusion, le rapport entre l'utilisation d'antipsychotiques atypiques et la survenue d'effets indésirables reliés à une hyperglycémie n'est pas complètement élucidé. Les études épidémiologiques suggèrent cependant qu'il existe un risque accru de survenue d'effets indésirables liés à une hyperglycémie chez les patients traités par des antipsychotiques atypiques. Les patients traités par des antipsychotiques atypiques, y compris par Risperdal Consta, doivent être surveillés à la recherche de symptômes d'une hyperglycémie et d'un diabète.
Prise de poids
Une prise de poids significative a été rapportée lors de l'utilisation de Risperdal Consta. Une surveillance régulière du poids est donc recommandée.
Priapisme
Selon certains rapports, les antagonistes des récepteurs α-adrénergiques peuvent provoquer un priapisme. Un priapisme a été rapporté avec Risperdal depuis la commercialisation (voir rubrique "Effets indésirables" ).
Régulation de la température corporelle
Les antipsychotiques peuvent altérer la capacité de l'organisme à diminuer la température corporelle centrale. La prudence est donc recommandée lorsque Risperdal Consta est prescrit à des patients exposés à des situations pouvant contribuer à une augmentation de la température corporelle centrale (p.ex. activité physique fatigante, exposition à une chaleur extrême, administration simultanée de médicaments à effet anticholinergique ou déshydratation).
Effet antiémétique
Les essais précliniques réalisés avec la rispéridone ont révélé un effet antiémétique. L'apparition de cet effet chez l'être humain pourrait masquer les signes et les symptômes d'un surdosage de certaines substances ou de maladies telles qu'occlusion intestinale, syndrome de Reye ou tumeur cérébrale.
Crises épileptiques
Comme tous les antipsychotiques, Risperdal Consta doit être utilisé avec prudence chez les patients ayant des antécédents de crises épileptiques ou présentant d'autres états pouvant s'accompagner d'une diminution du seuil épileptogène.
Syndrome de l'iris hypotonique peropératoire
Des cas de syndrome d'iris hypotonique peropératoire (IFIS) ont été observés lors d'opérations de la cataracte chez des patients traités par des médicaments dotés d'un effet antagoniste sur les récepteurs α1a-adrénergiques, y compris Risperdal Consta.
L'IFIS peut augmenter le risque de complications oculaires pendant et après l'intervention. Avant l'intervention, le chirurgien ophtalmologue doit être informé de la prise actuelle ou antérieure de médicaments dotés d'un effet antagoniste sur les récepteurs α1a-adrénergiques. Le bénéfice potentiel de l'interruption du traitement par les antagonistes α1 avant l'opération de la cataracte n'a pas été étudié et doit être évalué par rapport au risque d'une interruption du traitement antipsychotique.
Tumeurs prolactinodépendantes
Risperdal Consta doit être utilisé uniquement avec prudence chez les patients présentant une tumeur prolactinodépendante (p.ex. prolactinome hypophysaire) ou vraisemblablement prolactinodépendante (p.ex. tumeurs épithéliales du sein).
Administration
Il faut faire très attention à ce que Risperdal Consta ne soit pas injecté par mégarde dans un vaisseau sanguin (voir "Effets indésirables – occlusion de l'artère rétinienne" ).
Ce médicament contient moins de 1 mmol (23 mg) de sodium par injection, c.-à-d. qu'il est essentiellement "sans sodium" .
InteractionsLes interactions de Risperdal Consta lors de l'utilisation concomitante d'autres médicaments n'ont pas fait l'objet d'études systématiques. Les interactions décrites dans cette rubrique reposent sur des études réalisées avec la rispéridone orale.
Interactions pharmacocinétiques
La rispéridone est essentiellement métabolisée par le CYP2D6 et dans une moindre mesure par le CYP3A4. La rispéridone et son métabolite actif, la 9-hydroxyrispéridone, sont des substrats de la glycoprotéine P (P-gp). Les substances qui modifient l'activité du CYP2D6 ou les inhibiteurs ou inducteurs puissants de l'activité du CYP3A4 et/ou de la P-gp peuvent influencer la pharmacocinétique de la fraction antipsychotique active de la rispéridone.
Interactions pharmacodynamiques
Médicaments à effet central et alcool
Compte tenu des effets primaires de Risperdal sur le SNC, la co-administration avec d'autres médicaments à action centrale ou avec de l'alcool requiert de la prudence.
Lévodopa et agonistes de la dopamine
La rispéridone peut diminuer l'action de la lévodopa et d'autres agonistes de la dopamine. Si cette association est considérée comme nécessaire, notamment au stade terminal de la maladie de Parkinson, la dose efficace la plus faible doit être prescrite lors de chaque traitement.
Psychostimulants
L'utilisation de psychostimulants (p.ex. méthylphénidate) en combinaison avec la rispéridone peut, en cas de modification de l'un des traitements ou des deux traitements, entraîner l'apparition de symptômes extrapyramidaux (voir "Mises en garde et précautions" ).
Médicaments hypotenseurs
Une hypotension cliniquement significative a été observée après la commercialisation lors de l'utilisation concomitante de la rispéridone et d'antihypertenseurs.
Médicaments connus pour allonger l'intervalle QT
La prudence est de rigueur lors de la prescription de Risperdal Consta avec des médicaments connus pour allonger l'intervalle QT.
Inducteurs enzymatiques
Inducteurs du CYP3A4 et/ou de la P-gp
L'utilisation concomitante de Risperdal Consta et d'un inducteur puissant du CYP3A4 et/ou de la Pgp peut diminuer la concentration plasmatique de la fraction antipsychotique active de la rispéridone. Lors de l'instauration ou de l'arrêt de la co-administration de la carbamazépine ou d'un autre inducteur puissant du CYP3A4 et/ou de la Pgp, le médecin doit réévaluer la posologie de Risperdal Consta.
Inhibiteurs enzymatiques
Inhibiteurs puissants du CYP2D6
L'utilisation concomitante de Risperdal Consta et d'un inhibiteur puissant du CYP2D6 peut augmenter la concentration plasmatique de rispéridone, mais la fraction antipsychotique active est moins fortement touchée. À fortes doses, les inhibiteurs puissants du CYP2D6 peuvent augmenter la concentration de la fraction antipsychotique active de la rispéridone (p.ex. paroxétine, voir ci-dessous). Lors de l'instauration ou de l'arrêt de la co-administration de paroxétine, de bupropion ou d'un autre inhibiteur puissant du CYP2D6, surtout s'ils sont administrés à fortes doses, le médecin doit réévaluer la posologie de Risperdal Consta.
Inhibiteurs du CYP3A4 et/ou de la P-gp
L'utilisation concomitante de Risperdal Consta et d'un inhibiteur puissant du CYP3A4 et/ou de la Pgp peut entraîner une augmentation importante de la concentration plasmatique de la fraction antipsychotique active de la rispéridone. Lors de l'instauration ou de l'arrêt de la co-administration d'itraconazole ou d'un autre inhibiteur puissant du CYP3A4 et/ou de la Pgp, le médecin doit réévaluer la posologie de Risperdal Consta.
Autres interactions
Substances fortement liées aux protéines
Lors de l'utilisation concomitante de Risperdal Consta et de médicaments fortement liés aux protéines, aucun des principes actifs ne fait l'objet d'un déplacement cliniquement significatif de sa liaison aux protéines plasmatiques.
Lors de l'utilisation de médicaments associés, il convient de respecter les indications portant sur les voies métaboliques et sur l'éventuelle nécessité d'un ajustement posologique figurant dans l'information professionnelle correspondante.
Patients pédiatriques
Des études d'interactions n'ont été réalisées que chez l'adulte. La pertinence des résultats de ces études pour les patients pédiatriques n'est pas connue.
Exemples
Des exemples de médicaments interagissant potentiellement avec la rispéridone ou n'interagissant pas de manière avérée avec la rispéridone sont répertoriés ci-dessous:
Effet de Risperdal Consta sur d'autres médicaments
Anticonvulsivants:
-La rispéridone n'a pas d'influence cliniquement significative sur la pharmacocinétique du valproate ou du topiramate.
Lithium:
-La rispéridone n'a pas d'influence cliniquement significative sur la pharmacocinétique du lithium.
Effet d'autres médicaments sur Risperdal Consta
Substances antibactériennes:
-L'érythromycine, un inhibiteur modéré du CYP3A4, ne modifie pas la pharmacocinétique de la rispéridone et de la fraction antipsychotique active.
-La rifampicine, un inducteur puissant du CYP3A4 et un inducteur de la P-gp, diminue la concentration plasmatique de la fraction antipsychotique active.
Anticholinestérases:
-La galantamine et le donépézil, deux inhibiteurs de la cholinestérase qui sont des substrats du CYP2D6 et du CYP3A4, n'ont pas d'influence cliniquement significative sur la pharmacocinétique de la rispéridone et de la fraction antipsychotique active.
Anticonvulsivants:
-La carbamazépine, un inducteur puissant du CYP3A4 et un inducteur de la P-gp, diminue la concentration plasmatique de la fraction antipsychotique active de la rispéridone.
-Le topiramate diminue modérément la biodisponibilité de la rispéridone, mais n'a pas d'influence sur la biodisponibilité de la fraction antipsychotique active. Cette interaction n'est donc vraisemblablement pas cliniquement significative.
Antimycosiques:
-L'itraconazole, un inhibiteur puissant du CYP3A4 et un inhibiteur de la P-gp, administré à une posologie de 200 mg/jour, a entraîné une augmentation d'environ 70% des concentrations plasmatiques de la fraction antipsychotique active, à des doses de rispéridone de 2 à 8 mg/jour.
-Le kétoconazole, un inhibiteur puissant du CYP3A4 et un inhibiteur de la P-gp, administré à une posologie de 200 mg/jour, a augmenté la concentration plasmatique de la rispéridone et a diminué la concentration plasmatique de la 9-hydroxyrispéridone.
Antipsychotiques:
-Les phénothiazines peuvent augmenter la concentration plasmatique de la rispéridone, mais n'ont pas d'influence sur la concentration plasmatique de la fraction antipsychotique active.
-Pour l'aripiprazole, un substrat du CYP2D6 et du CYP3A4, il n'existe pas de preuve clinique suffisante permettant d'évaluer un effet éventuel de Risperdal sur la pharmacocinétique de l'aripiprazole et de son métabolite actif, le déhydro-aripiprazole.
Virostatiques:
-Inhibiteurs de la protéase: aucune donnée tirée d'études formelles n'est disponible. Cependant, comme le ritonavir est un inhibiteur puissant du CYP3A4 et un inhibiteur faible du CYP2D6, le ritonavir et les inhibiteurs de la protéase potentialisés par le ritonavir sont susceptibles d'augmenter la concentration de la fraction antipsychotique active de la rispéridone.
Bêtabloquants:
-Certains bêtabloquants peuvent augmenter la concentration plasmatique de la rispéridone, mais n'ont pas d'influence sur la concentration plasmatique de la fraction antipsychotique active.
Inhibiteurs des canaux calciques:
-Le vérapamil, un inhibiteur modéré du CYP3A4 et un inhibiteur de la P-gp, augmente la concentration plasmatique de la rispéridone et de la fraction antipsychotique active.
Glycosides digitaliques:
-La rispéridone n'a pas d'influence cliniquement significative sur la pharmacocinétique de la digoxine.
Diurétiques:
-Furosémide: tenir compte des indications figurant à la rubrique "Mises en garde et précautions" en ce qui concerne la mortalité accrue chez les patients âgés atteints de démence recevant simultanément un traitement par le furosémide.
Médicaments gastro-intestinaux:
-Antagonistes des récepteurs H2: la cimétidine et la ranitidine, deux inhibiteurs faibles du CYP2D6 et du CYP3A4, ont augmenté la biodisponibilité de la rispéridone, mais seulement de manière marginale celle de la fraction antipsychotique active.
ISRS et antidépresseurs tricycliques:
-La fluoxétine, un inhibiteur puissant du CYP2D6, augmente la concentration plasmatique de la rispéridone, mais la fraction antipsychotique active est moins fortement touchée.
-La paroxétine, un inhibiteur puissant du CYP2D6, augmente la concentration plasmatique de la rispéridone, mais à des posologies allant jusqu'à 20 mg/jour, la fraction antipsychotique active est moins fortement touchée. À des doses plus élevées de paroxétine, la concentration de la fraction antipsychotique active de la rispéridone peut cependant augmenter de manière dose-dépendante.
-Les antidépresseurs tricycliques peuvent augmenter la concentration plasmatique de la rispéridone, mais n'ont pas d'influence sur la concentration plasmatique de la fraction antipsychotique active. L'amitriptyline n'a pas d'influence sur la pharmacocinétique de la rispéridone ou de la fraction antipsychotique active.
-La sertraline, un inhibiteur faible du CYP2D6, et la fluvoxamine, un inhibiteur faible du CYP3A4, n'entraînent pas de variations cliniquement significatives de la concentration de la fraction antipsychotique active de la rispéridone, à des posologies allant jusqu'à 100 mg/jour. Cependant, à des doses de sertraline ou de fluvoxamine supérieures à 100 mg/jour, la concentration de la fraction antipsychotique active de la rispéridone peut augmenter.
Grossesse, allaitementGrossesse
La sécurité de la rispéridone pour l'utilisation pendant la grossesse n'a pas été étudiée.
Une étude de cohorte rétrospective d'observation, basée sur une banque de données américaine comportant des prestations de soins de santé remboursées, avait comparé le risque de malformations congénitales chez les enfants nés vivants chez des femmes ayant utilisé des antipsychotiques ou non au cours du premier trimestre de la grossesse. Lors de cette étude, une évaluation concrète de la palipéridone, le métabolite actif de la rispéridone, n'avait pas été effectuée. Après ajustement prenant en compte les variantes confondantes dans la banque de données, le risque de malformations congénitales en cas d'utilisation de rispéridone était augmenté par rapport à la non utilisation d'antipsychotiques (risque relatif = 1,26, IC 95%: 1,02-1,56). Aucun mécanisme biologique susceptible d'expliquer cette constatation n'avait pu être identifié et, lors des études précliniques, aucun effet tératogène n'avait été observé. En se fondant sur les résultats de cette unique étude d'observation, aucune relation causale entre l'exposition in utero à la rispéridone et les malformations congénitales n'a été mise en évidence.
Bien que les expérimentations animales n'aient pas mis en évidence de toxicité directe pour la reproduction, quelques effets indirects médiés par la prolactine et par le SNC ont été observés (voir rubrique "Données précliniques" ).
Risperdal Consta ne doit pas être administré pendant la grossesse, sauf en cas de nécessité absolue. Si un arrêt du traitement s'avère nécessaire pendant la grossesse, celui-ci devra ne pas être brutal.
Troisième trimestre
Les nouveau-nés dont les mères ont pris des antipsychotiques (dont la rispéridone) pendant le troisième trimestre de la grossesse présentent un risque de symptômes extrapyramidaux et/ou de symptômes de sevrage après la naissance. Ces symptômes chez le nouveau-né peuvent comprendre: agitation, augmentation ou diminution inhabituelle du tonus musculaire, tremblements, somnolence, difficultés respiratoires ou problèmes d'alimentation. Ces complications peuvent avoir un degré de sévérité variable. Dans certains cas, ils ont été autolimitants; dans d'autres cas, les nouveau-nés ont nécessité une surveillance en service de soins intensifs ou une hospitalisation prolongée.
Allaitement
Les études expérimentales effectuées chez l'animal ont montré que la rispéridone et la 9-hydroxyrispéridone sont excrétées dans le lait. Le passage de la rispéridone et de la 9-hydroxyrispéridone dans le lait maternel humain a été démontré. Dans un seul cas, 4,3% de la fraction active (par rapport à la dose de la mère) ont été mesurés dans le lait maternel. En conséquence, les mères traitées par la rispéridone ne devraient pas allaiter.
Effet sur l’aptitude à la conduite et l’utilisation de machinesRisperdal Consta peut influencer négativement toute activité demandant de la concentration et de la vigilance. En conséquence, les patients seront avisés de ne pas conduire un véhicule ou manier des machines compliquées avant que leur capacité de réaction individuelle ait été clarifiée et que le médecin traitant ait parlé de cette évaluation avec eux et la leur ait expliquée.
Effets indésirablesLes effets indésirables les plus fréquemment rapportés (fréquence ≥1/10) sont: insomnie, anxiété, céphalées, infection des voies respiratoires supérieures, parkinsonisme et dépression.
La palipéridone est le métabolite actif de la rispéridone. Les profils d'effets indésirables de ces deux substances (y compris leurs formulations orales et injectables) ont de ce fait une importance réciproque. Ci-après se trouve une liste complète des effets indésirables qui ont été rapportés avec la rispéridone et/ou la palipéridone dans le cadre d'études cliniques et depuis la mise sur le marché. Les termes et fréquences suivantes sont utilisés: très fréquents (≥1/10), fréquents (≥1/100 à <1/10), occasionnels (≥1/1000 à <1/100), rares (≥1/10'000 à <1/1000), très rares (<1/10'000) ainsi que fréquence inconnue (la fréquence ne peut pas être estimée sur la base des données disponibles).
A l'intérieur de chaque groupe de fréquence, les effets indésirables sont présentés suivant un ordre décroissant de gravité.
Effets indésirables par classe de systèmes d'organes et par fréquence
Infections et infestations
Très fréquents: infections des voies respiratoires supérieures.
Fréquents: pneumonie, bronchite, sinusite, infection urinaire, grippe.
Occasionnels: infection des voies respiratoires, cystite, infection de l'oreille, infection oculaire, amygdalite, onychomycose, cellulite, infection, infection localisée, infection virale, acrodermatite, abcès sous-cutané.
Affections hématologiques et du système lymphatique
Fréquents: anémie.
Occasionnels: diminution de nombre de globules blancs, thrombopénie, diminution de l'hématocrite.
Rares: neutropénie.
Fréquence inconnue: agranulocytose, diminution de nombre de granulocytes éosinophiles.
Affections du système immunitaire
Occasionnels: hypersensibilité.
Fréquence inconnue: réaction anaphylactique.
Affections endocriniennes
Fréquents: hyperprolactinémiea.
Rares: sécrétion inadéquate de l'hormone antidiurétique.
Troubles du métabolisme et de la nutrition
Fréquents: hyperglycémie, prise de poids, augmentation de l'appétit, perte de poids, baisse de l'appétit.
Occasionnels: diabèteb, anorexie, augmentation des triglycérides, augmentation du cholestérol, glycosurie.
Rares: hypoglycémie, polydipsie.
Très rares: acidocétose diabétique.
Fréquence inconnue: intoxication à l'eau, hyperinsulinémie, coma diabétique.
Affections psychiatriques
Très fréquents: insomniec, dépression, anxiété.
Fréquents: troubles du sommeil, agitation, diminution de la libido.
Occasionnels: manie, confusion, anorgasmie, cauchemars.
Rares: catatonie, somnambulisme, émoussement affectif.
Fréquence inconnue: troubles du comportement alimentaire liés au sommeil (ingestion de nourriture incontrôlée lors des crises de somnambulisme).
Affections du système nerveux
Très fréquents: parkinsonismec, céphalées.
Fréquents: akathisiec, somnolence, dystoniec, vertiges, dyskinésiec, tremblements.
Occasionnels: ischémie cérébro-vasculaire, perte de connaissance, convulsionsc, syncopes, dyskinésie tardive, hyperactivité psychomotrice, troubles de l'équilibre, vertige positionnel, troubles de l'attention, dysarthrie, dysgueusie, hypoesthésie, paresthésie.
Rares: syndrome malin des neuroleptiques, diminution du degré de conscience, tremblements de la tête.
Fréquence inconnue: absence de réponse aux stimuli.
Affections oculaires
Fréquents: vision floue.
Occasionnels: conjonctivite, sécheresse oculaire, sécrétion lacrymale accrue, hyperhémie oculaire.
Rares: troubles de la motricité oculaire, révulsion oculaire, photophobie.
Fréquence inconnue: occlusion de l'artère rétinienne, glaucome, croûtes du bord des paupières, syndrome de l'iris hypotonique peropératoire.
Affections de l'oreille et du labyrinthe
Occasionnels: vertiges, acouphènes, otalgie.
Affections cardiaques
Fréquents: tachycardie.
Occasionnels: fibrillation auriculaire, bloc auriculo-ventriculaire, troubles de la conduction, allongement de l'intervalle QT à l'électrocardiogramme, bradycardie, anomalies à l'électrocardiogramme, palpitations.
Rares: arythmies sinusales.
Fréquence inconnue: syndrome de tachycardie orthostatique posturale.
Affections vasculaires
Fréquents: hypotension, hypertension.
Occasionnels: hypotension orthostatique.
Rares: embolie pulmonaire, thrombose veineuse profonde.
Fréquence inconnue: flush.
Affections respiratoires, thoraciques et médiastinales
Fréquents: dyspnée, douleurs pharyngo-laryngées, toux, nez bouché.
Occasionnels: hyperventilation, obstruction des voies respiratoires, respiration haletante, épistaxis.
Rares: syndrome d'apnées du sommeil, pneumonie d'aspiration, congestion pulmonaire, râle pulmonaire, dysphonie, trouble respiratoire.
Affections gastro-intestinales
Fréquents: gêne abdominale, vomissements, nausées, constipation, gastroentérite, diarrhée, dyspepsie, sécheresse buccale, douleur dentaire.
Occasionnels: incontinence fécale, dysphagie, flatulence.
Rares: pancréatite, obstruction intestinale.
Très rare: iléus.
Fréquence inconnue: gonflement de la langue, fécalome, chéilite.
Affections hépatobiliaires
Fréquents: augmentation des transaminases, augmentation du taux de gamma-glutamyl transférase.
Occasionnels: augmentation du taux des enzymes hépatiques.
Rares: ictère.
Affections de la peau et du tissu sous-cutané
Fréquents: éruption cutanée.
Occasionnels: prurit, alopécie, eczéma, sécheresse cutanée, érythème, coloration de la peau, acné, dermatite séborrhéique.
Rares: exanthème médicamenteux, urticaire, hyperkératose, maladies cutanées, lésion cutanée.
Très rares: angio-œdème.
Fréquence inconnue: syndrome de Stevens-Johnson/nécrolyse épidermique toxique.
Affections musculosquelettiques et du tissu conjonctif
Fréquents: crampes musculaires, douleurs musculosquelettiques, douleur dorsale, arthralgie.
Occasionnels: augmentation du taux de créatine phosphokinase, raideur articulaire, gonflement des articulations, faiblesse musculaire, douleurs de la nuque.
Rares: rhabdomyolyse, posture anormale.
Affections du rein et des voies urinaires
Fréquents: incontinence urinaire.
Occasionnels: pollakiurie, rétention urinaire, dysurie.
Affections gravidiques, puerpérales et périnatales
Très rares: symptômes extrapyramidaux moteurs et/ou phénomènes de sevrage chez le nouveau-né.
Affections des organes de reproduction et du sein
Fréquents: dysfonction érectile, aménorrhée, galactorrhée.
Occasionnels: trouble de l'éjaculation, retard des règles, trouble menstruelc, gynécomastie, dysfonction sexuelle, gêne des seins, pertes vaginales.
Rares: gonflement des glandes mammaires, écoulement mammaire.
Fréquence inconnue: priapisme.
Lésions, intoxications et complications liées aux interventions
Fréquents: chute.
Occasionnels: douleur liée à l'administration.
Troubles généraux et anomalies au site d'administration
Fréquents: œdèmec, pyrexie, gêne thoracique, asthénie, fatigue, douleurs, douleurs au site d'injection, chute.
Occasionnels: œdème facial, frissons, augmentation de la température corporelle, démarche anormale, soif, sensation de maladie, sensation anormale, induration.
Rares: hypothermie, gêne.
Très rares: Réaction anaphylactique après une injection de Risperdal Consta chez des patients qui ont déjà toléré la rispéridone orale.
Fréquence inconnue: diminution de la température corporelle, sensation de froid périphérique, syndrome de sevrage médicamenteux.
a Une hyperprolactinémie peut dans certains cas provoquer une gynécomastie, des troubles menstruels, une aménorrhée et une galactorrhée.
b Des études contrôlées contre placebo ont fait état d'un diabète sucré chez 0,18% des patients traités par la rispéridone contre 0,11% des patients traités par placebo. L'incidence globale de toutes les études cliniques était de 0,43% chez tous les patients ayant reçu de la rispéridone.
c L'insomnie comprend: trouble de l'endormissement, insomnie du milieu de la nuit;
Le parkinsonisme comprend: akinésie, bradykinésie, phénomène de la roue dentée, salivation, symptômes extrapyramidaux moteurs, réflexe fronto-orbiculaire pathologique, raideur musculaire, contractures musculaires, raideur musculosquelettique;
L'akathisie comprend: hyperkinésie, syndrome des jambes sans repos, agitation;
La dystonie comprend: blépharospasme, spasmes cervicaux, emprosthotonos, crampe faciale, hypertonie musculaire, laryngospasme, contractions musculaires involontaires, myotonie, crise oculogyre, opisthotonos, crampe oropharyngée, pleurothotonos, rictus sardonique, tétanie, paralysie de la langue, crampe de la langue, torticolis, trismus;
La dyskinésie comprend: athétose, chorée, mouvements choréoathétosiques, troubles moteurs, secousses musculaires, myoclonie;
Les convulsions comprennent: crises de grand mal;
Les œdèmes comprennent: œdèmes généralisés, œdèmes périphériques, œdème prenant le godet ( "pitting edema" );
Les troubles menstruels comprennent: règles irrégulières, oligoménorrhée.
Description de certains effets indésirables
Effets de classe
Allongement de l'intervalle QT
Comme pour d'autres antipsychotiques, de très rares cas d'allongement du QT sous rispéridone ont été rapportés après la commercialisation. D'autres effets de classe cardiaques rapportés sous antipsychotiques allongeant l'intervalle QT incluent une arythmie ventriculaire, une fibrillation ventriculaire, une tachycardie ventriculaire, une mort subite, un arrêt cardiaque et des torsades de pointes (voir rubrique "Mises en garde et précautions" ).
Prise de poids
Dans une étude contrôlée contre placebo, en double aveugle, d'une durée de 12 semaines, une prise de poids de ≥7% du poids corporel a été constatée en fin d'étude chez 9% des patients traités avec Risperdal Consta par rapport à une augmentation de 6% chez les patients traités par placebo. Durant une étude ouverte d'une année consacrée à Risperdal Consta, les modifications du poids corporel chez quelques patients se situaient en général dans une fourchette de ±7% du poids initial; chez 25% des patients a été enregistrée une prise de poids de ≥7%.
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageLes cas de surdosage documentés sont limités à la formulation orale:
Signes et symptômes
Les symptômes escomptés sont le résultat d'une amplification des effets pharmacologiques connus. Ils se présentent sous forme de somnolence, de sédation, de tachycardie, d'hypotension et de symptômes extrapyramidaux. Rarement, le surdosage a donné lieu à un prolongement de l'intervalle QT et à des convulsions. Des cas de torsades de pointes ont été rapportés en rapport avec un surdosage simultané de Risperdal et de paroxétine.
Traitement
En cas de surdosage, libérer les voies aériennes et les garder dégagées, assurer un apport suffisant en oxygène et appliquer une ventilation assistée. Surveillance immédiate des fonctions cardiaques et vasculaires. Contrôle ECG permanent, pour détecter une éventuelle arythmie.
Il n'existe pas d'antidote spécifique à Risperdal Consta. Par conséquent, préparer les mesures adéquates. En cas d'intoxication aiguë, prendre en compte la possibilité d'une polyintoxication. Une hypotension et un collapsus circulatoire doivent être traités par les mesures adéquates, comme une perfusion intraveineuse et/ou des médicaments sympathomimétiques. Administrer un anticholinergique en cas de symptômes extrapyramidaux sévères. Maintenir le patient sous étroite surveillance médicale jusqu'à ce qu'il ait récupéré.
Propriétés/EffetsCode ATC
N05AX08
Mécanisme d'action
Risperdal Consta (rispéridone) est un antipsychotique appartenant à une nouvelle classe: les dérivés du benzisoxazole. Il présente une forte affinité pour les récepteurs D2-dopaminergiques et 5HT2-sérotoninergiques. La rispéridone occupe également les récepteurs α1-adrénergiques et, avec une moindre affinité, les récepteurs H1-histaminiques et α2-adrénergiques. La rispéridone ne possède aucune affinité pour les récepteurs cholinergiques. Bien qu'elle soit un puissant antagoniste des récepteurs D2, une caractéristique connue pour influencer favorablement les symptômes positifs de la schizophrénie, la rispéridone diminue moins fortement l'activité motrice et provoque moins souvent une catalepsie que les neuroleptiques classiques. En raison de son antagonisme équilibré des systèmes sérotoninergique et dopaminergique centraux, elle risque moins de provoquer des effets secondaires extrapyramidaux et peut également agir sur les symptômes négatifs et affectifs de la schizophrénie.
L'efficacité de Risperdal Consta (25 mg et 50 mg) dans le traitement des troubles psychotiques (schizophrénie, troubles schizo-affectifs) a été démontrée dans une étude contrôlée contre placebo, d'une durée de 12 semaines, menée auprès de patients psychotiques hospitalisés et ambulatoires et répondant aux critères de schizophrénie du DSM-IV.
Une étude comparative de 12 semaines, menée auprès de patients schizophrènes avec symptomatologie stable, a démontré que l'efficacité de Risperdal Consta était semblable à celle de la formulation orale sous forme de comprimés.
L'efficacité et la sécurité d'emploi de Risperdal Consta lors d'un traitement à long terme (50 semaines) ont fait l'objet d'une étude ouverte menée auprès de patients psychotiques stabilisés, hospitalisés et ambulatoires, répondant aux critères de schizophrénie ou de troubles schizo-affectifs du DSM-IV. L'effet de Risperdal Consta s'est maintenu sur toute la durée de l'étude. (Cette étude n'a pas inclus de groupe de comparaison.)
Pharmacodynamique
Voir Mécanisme d'action
Efficacité clinique
Voir Mécanisme d'action
PharmacocinétiqueLibération du principe actif
Après administration intramusculaire unique de Risperdal Consta, une faible quantité de principe actif est initialement libérée (<1% de la dose). Il s'ensuit une phase de latence de 3 semaines. La libération du principe actif entre dans sa phase principale dès la 3e semaine. Le débit du principe actif reste constant de la 4e à la 6e semaine, et commence à décliner dès la 7e semaine. C'est pourquoi l'administration d'un antipsychotique supplémentaire s'impose au cours des 3 premières semaines de traitement par Risperdal Consta. Lors des essais cliniques, des comprimés de rispéridone ont assuré cette couverture antipsychotique pendant les trois premières semaines.
L'association du profil de libération du principe actif et de l'intervalle entre les injections (injection i.m. toutes les 2 semaines) assure le maintien de taux plasmatiques thérapeutiques. Le taux de principe actif demeure dans l'intervalle thérapeutique 4 à 6 semaines après la dernière injection.
L'élimination se termine 7 à 8 semaines après la dernière injection de Risperdal Consta.
Absorption
Une fois libérée, la rispéridone est entièrement absorbée.
Distribution
La rispéridone se distribue rapidement dans l'organisme. Son volume de distribution apparent (Vd) varie entre 1 et 2 l/kg. La liaison à l'albumine et à l'α1-glycoprotéine acide de la rispéridone s'élève à 88%, celle de son métabolite actif, la 9-hydroxyrispéridone, s'élève à 77%.
Les concentrations plasmatiques minimales et maximales moyennes de la fraction active, obtenues après injections intramusculaires de Risperdal Consta répétées toutes les 2 semaines, sont de 9,9 et 19,2 ng/ml pour le dosage à 25 mg, et de 17,9 et 45,5 ng/ml pour le dosage à 50 mg. La rispéridone présente une pharmacocinétique linéaire dans l'intervalle des dosages situés entre 25 et 50 mg administrés toutes les deux semaines par injections. Les injections de 25 à 50 mg toutes les deux semaines lors d'une utilisation à long terme (12 mois) n'ont occasionné aucune accumulation de rispéridone.
Les études mentionnées ont été menées sur l'injection dans le muscle fessier. Les injections intramusculaires au niveau du muscle deltoïde et du muscle fessier, de dose identique, sont bioéquivalentes et de ce fait sont interchangeables.
Métabolisme
La rispéridone est essentiellement métabolisée dans le foie par le CYP 2D6. Elle est essentiellement dégradée en 9-hydroxyrispéridone, qui exerce une action pharmacologique comparable à celle de la rispéridone. La rispéridone et la 9-hydroxyrispéridone forment ensemble la fraction antipsychotique active.
Le CYP 2D6 présente un polymorphisme génétique (débrisoquine/dextrométhorphane). La transformation de la rispéridone en 9-hydroxyrispéridone est rapide chez les métaboliseurs rapides et lente chez les métaboliseurs lents. C'est pourquoi, chez les métaboliseurs rapides, les taux plasmatiques de rispéridone sont plus bas et ceux de la 9-hydroxyrispéridone plus élevés que chez les métaboliseurs lents. Comme la rispéridone et la 9-hydroxyrispéridone possèdent à peu près la même activité antipsychotique, c'est la somme de leurs concentrations qui est déterminante. C'est pourquoi aucune différence cliniquement pertinente n'a été observée entre les métaboliseurs rapides et les métaboliseurs lents.
La voie de métabolisation par N-désalkylation, qui s'effectue probablement par le CYP3A4, est moins importante.
Élimination
La clairance de la fraction antipsychotique active et de la rispéridone se monte à 5,0 l/h et 13,7 l/h chez les métaboliseurs rapides (concernant le CYP 2D6) et à 3,2 l/h et 3,3 l/h chez les métaboliseurs lents.
Cinétique pour certains groupes de patients
Après administration orale d'une dose unique à des patients âgés et à des insuffisants rénaux, une élévation des taux plasmatiques de la fraction antipsychotique active (la Cmax était environ 1,1 et 1,5 fois plus élevée et l'AUC environ 1,5 et 2,5 fois plus élevée) a été observée. Cela reflète probablement une diminution de la clairance de la fraction antipsychotique active de 30% chez le patient âgé et de 60% chez le patient avec insuffisance rénale. Les concentrations plasmatiques de la rispéridone étaient dans la norme chez les patients ayant une insuffisance hépatique mais la fraction libre moyenne de la rispéridone dans le plasma était augmentée d'environ 35%.
Ces populations de patients n'ont pas fait l'objet d'études pharmacocinétiques spécifiques avec Risperdal Consta. Certaines analyses pharmacocinétiques indiquent cependant que, à la posologie recommandée de 25 mg toutes les 2 semaines, les concentrations plasmatiques chez les patients âgés (>65 ans) et chez les insuffisants rénaux légers à modérés se situent à l'intérieur de l'intervalle observé chez l'adulte normal. Les analyses reposent sur les concentrations de principe actif communiquées dans les études de phase III avec Risperdal Consta (voir "Instructions spéciales pour la posologie" ).
Relation entre pharmacocinétique et pharmacodynamique
Aucune des études de phase III, destinées à évaluer l'efficacité et la sécurité d'emploi de Risperdal Consta, n'a décelé de relation entre taux plasmatiques de la fraction antipsychotique active et variation des scores PANSS total (Positive and Negative Syndrome Scale) et ESRS (Extrapyramidal Symptom Rating Scale).
Données précliniquesLors d'études de toxicité avec administrations répétées chez des rats et des chiens, ce sont principalement des effets pharmacologiques, tels que sédation et effets médiés par la prolactine sur les glandes mammaires et les organes génitaux, qui ont été observés.
Mutagénicité
La rispéridone n'était pas génotoxique dans les tests standards.
Carcinogénicité
Comme prévu pour un puissant antagoniste D2, une étude de carcinogénicité effectuée sur des rats ayant reçu des doses i.m. de 40 mg/kg a relevé une incidence accrue de néoplasies endocriniennes du pancréas, de l'hypophyse et de la médullosurrénale, médiée par la prolactine. Des carcinomes mammaires se sont déclarés aux doses de 5 et 40 mg/kg. L'hypercalcémie observée dans les deux groupes de dosage pourrait avoir contribué à la hausse de l'incidence des tumeurs médullosurrénales. Des rats mâles ont présenté un adénome tubulaire rénal. Aucune tumeur rénale n'est apparue au dosage le plus faible, dans le groupe de contrôle avec NaCl 0,9% ou celui avec microsphères. Le mécanisme par lequel les rats traités par Risperdal Consta ont développé une tumeur rénale reste inconnu. Les études de carcinogénicité de la rispéridone orale sur le rat et la souris n'ont relevé aucune hausse de l'incidence des tumeurs rénales liées au traitement.
Toxicité sur la reproduction
Bien qu'au cours des études sur la rispéridone chez l'animal aucun trouble direct sur la reproduction n'ait été constaté, des effets indirects médiés par la prolactine ont été observés.
La rispéridone n'a entraîné aucun effet tératogène chez le rat et chez le lapin.
Chez le rat, des effets négatifs sur le comportement d'accouplement, le poids à la naissance et la survie de la progéniture ont été observés. D'éventuels troubles comportementaux de la progéniture n'ont pas fait l'objet d'études.
Remarques particulièresIncompatibilités
Risperdal Consta ne doit être mélangé à aucune autre solution ni à aucun autre médicament que la solution pour suspension fournie.
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention "EXP" sur le récipient.
Stabilité après ouverture
La stabilité chimique et physique de la suspension à une température de 25 °C est garantie pendant 24 heures après la préparation. D'un point de vue microbiologique, il est cependant préférable d'utiliser la suspension immédiatement après sa préparation. Si la suspension n'est pas administrée immédiatement après reconstitution, l'utilisateur prend lui-même la responsabilité de la durée et des conditions de conservation. De manière générale, il est déconseillé de dépasser 6 heures à 25 °C, sauf si la reconstitution s'est déroulée dans des conditions d'asepsie contrôlées et validées.
Remarques particulières concernant le stockage
Conserver l'intégralité du conditionnement au réfrigérateur (2-8 °C).
En l'absence de réfrigérateur, Risperdal Consta peut être conservé pendant 7 jours au maximum avant administration à une température ne dépassant pas 25 °C. Ne pas exposer à une température supérieure à 25 °C.
Conserver le récipient dans son emballage en carton pour le protéger de la lumière.
Conserver hors de portée des enfants.
Remarques concernant la manipulation
Il est important de respecter, étape par étape, les "Remarques concernant la manipulation" , afin de garantir une administration réussie de Risperdal Consta et d'éviter des difficultés lors de l'emploi du kit.
Les microsphères à libération retardée de principe actif (poudre dans le flacon) de Risperdal Consta doivent uniquement être mises en suspension avec la solution jointe (seringue pré-remplie). Concernant l'injection, seule l'aiguille à injection correspondante pour injection dans le muscle fessier (aiguille 2 pouces, 51 mm) ou injection dans le muscle deltoïde (aiguille 1 pouce, 25 mm) présente dans l'emballage doit être utilisée. Ne remplacez aucun des éléments du kit d'injection.
Pour s'assurer que la dose de rispéridone prévue est libérée, l'ensemble du contenu du flacon doit être administré. En cas d'administration incomplète du contenu, la dose de rispéridone prévue risque de ne pas être libérée. Il est recommandé d'administrer le produit immédiatement après la reconstitution.
Sortez l'emballage de Risperdal Consta du réfrigérateur et attendez env. 30 minutes qu'il soit à température ambiante avant de reconstituer la suspension.
Contenu du kit d'injection
-Un flacon contenant des microsphères à libération retardée de principe actif.
-Une seringue pré-remplie contenant le solvant.
-Un adaptateur pour flacon perforable destiné à fixer la seringue pré-remplie (raccord pour la reconstitution de la suspension).
-Deux aiguilles Terumo SurGuard-3 pour injection intramusculaire (une aiguille à injection 21G UTW 1 pouce (25 mm) munie d'un dispositif de protection de l'aiguille pour injection au niveau du deltoïde, et une aiguille d'injection 20G TW 2 pouces (51 mm) munie d'un dispositif de protection de l'aiguille pour injection dans le muscle fessier).
Instructions d'emploi, manipulation et élimination
Remarques importantes
Afin de garantir une administration réussie de Risperdal Consta, veuillez suivre ces instructions d'emploi étape par étape.
Attendre 30 min
Sortez le conditionnement unitaire du réfrigérateur et laissez-le à température ambiante pendant au moins 30 minutes avant de commencer la reconstitution.
Ne pas le réchauffer d'une autre manière.
Utiliser les éléments fournis
Les éléments contenus dans ce conditionnement unitaire sont spécialement conçus pour l'emploi de Risperdal Consta. Risperdal Consta doit uniquement être reconstitué avec le solvant fourni dans le conditionnement unitaire.
Ne substituer AUCUN des éléments de ce conditionnement unitaire.
Ne pas conserver la suspension reconstituée.
Après la reconstitution, administrer la dose aussi rapidement que possible afin d'éviter la formation d'un sédiment.
Dosage correct
Pour s'assurer que la dose de Risperdal Consta prévue est délivrée, la totalité du contenu du flacon doit être administrée.
DISPOSITIF MÉDICAL À USAGE UNIQUE
Ne pas réutiliser. Les dispositifs médicaux exigent des caractéristiques spécifiques du matériau pour fonctionner comme prévu. Ces caractéristiques ont été vérifiées pour un usage unique. Toute tentative visant à retraiter le dispositif médical pour une réutilisation ultérieure peut nuire à l'intégrité du produit ou altérer sa fonction.
1re étape Assemblage des éléments
Sortez le conditionnement unitaire du réfrigérateur et laissez-le à température ambiante pendant au moins 30 minutes avant de commencer la reconstitution. Ne pas le réchauffer d'une autre manière.
Connexion de l'adaptateur pour flacon perforable avec le flacon
Retrait du capuchon du flacon
Retirez la capsule colorée du flacon. Nettoyez le dessus du bouchon gris avec un tampon d'alcool. Laissez sécher à l'air. Ne pas retirer le bouchon en caoutchouc gris (Fig. A).
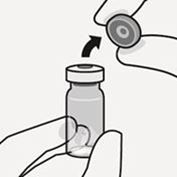
Fig. A
Préparation de l'adaptateur pour flacon perforable
Tenez le blister stérile comme indiqué (Fig. B). Retirez le papier protecteur. Ne pas sortir le dispositif du blister. Ne toucher à aucun moment le perforateur. Ceci provoquerait une contamination.
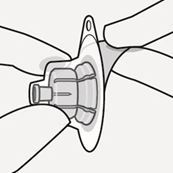
Fig. B
Connexion de l'adaptateur pour flacon perforable avec le flacon
Posez le flacon sur une surface dure et tenez-le par sa base. Tenez l'adaptateur pour flacon perforable au-dessus du centre du bouchon en caoutchouc gris. Enfoncez l'adaptateur pour flacon perforable verticalement sur le dessus du flacon jusqu'à ce qu'il soit bien enclenché (Fig. C).
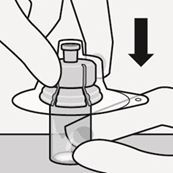
Fig. C
Ne mettez pas l'adaptateur pour flacon perforable en biais, car le solvant pourrait fuir lors du transfert dans le flacon (Fig. D).
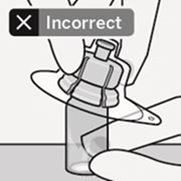
Fig. D
Connexion de la seringue pré-remplie à l'adaptateur pour flacon perforable
Retrait du blister stérile
Ne sortez l'adaptateur pour flacon perforable du blister stérile que lorsque vous êtes prêt à retirer le capuchon blanc de la seringue pré-remplie. Tenez le flacon verticalement pour empêcher toute fuite. Tenez le flacon par sa base et retirez le blister stérile vers le haut.
Ne pas agiter.
Ne pas toucher l'embout Luer exposé sur l'adaptateur pour flacon perforable. Ceci provoquerait une contamination (Fig. E).
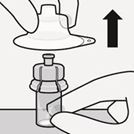

Fig. E
Maintien correct
Tenez la seringue par l'anneau blanc situé à son extrémité. Ne tenez pas la seringue par le cylindre en verre lors de l'assemblage (Fig. F)
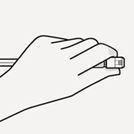
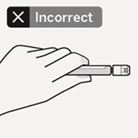
Fig. F
Retrait du capuchon
Tenez l'anneau blanc et cassez net le capuchon blanc.
Ne pas toucher l'extrémité de la seringue. Ceci provoquerait une contamination.
L'aspect de la seringue après le retrait du capuchon est illustré dans la Fig. G. Le capuchon rompu peut être éliminé.
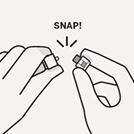
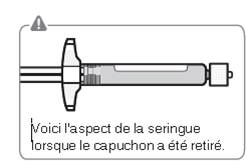
Fig. G.
Connexion de la seringue avec l'adaptateur pour flacon perforable
Maintenez l'adaptateur pour flacon perforable en position, en le tenant par la collerette.
Tenez la seringue par l'anneau blanc et introduisez le perforateur dans l'embout Luer situé sur l'adaptateur pour flacon perforable (Fig. H).
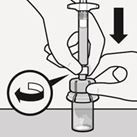
Fig. H
Ne tenez pas la seringue par le cylindre en verre. Ceci pourrait provoquer le desserrement ou le détachement de l'anneau blanc. Connectez la seringue à l'adaptateur pour flacon perforable en tournant fermement dans le sens des aiguilles d'une montre jusqu'à ce qu'elle soit bien fixée. Ne pas serrer trop fortement. Un serrage excessif peut entrainer la rupture de l'extrémité de la seringue.
2e étape Reconstitution des microsphères
Injection du solvant
Injectez la totalité du solvant de la seringue dans le flacon.
Le contenu du flacon est alors sous pression. Maintenez le piston enfoncé avec le pouce (Fig. I).

Fig. I
Mise en suspension des microsphères dans le solvant
Tout en maintenant le piston enfoncé, agitez vigoureusement la seringue et le flacon pendant au moins 10 secondes (Fig. J).
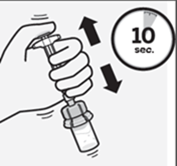
Fig. J
Examinez la suspension. Dès que le mélange est correct, la suspension prend un aspect homogène, visqueux et laiteux. Les microsphères deviennent visibles dans le liquide. Passez immédiatement à l'étape suivante afin que la suspension ne sédimente pas.
Transfert de la suspension dans la seringue
Retournez le flacon à l'envers. Tirez lentement sur le piston pour aspirer la totalité du contenu du flacon dans la seringue (Fig. K).
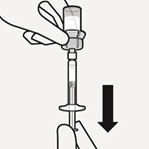
Fig. K
Retrait de l'adaptateur pour flacon perforable
Tenez la seringue par l'anneau blanc et dévissez-la de l'adaptateur pour flacon perforable. Déchirez la partie détachable de l'étiquette du flacon le long des perforations. Apposez cette étiquette sur la seringue dans un but d'identification (Fig. L).

Fig. L
Éliminez le flacon et l'adaptateur pour flacon perforable selon les normes en vigueur.
3e étape Fixation de l'aiguille
Choix de l'aiguille appropriée
Choisissez l'aiguille correspondant au site d'injection (muscle fessier ou deltoïde) (Fig. M).
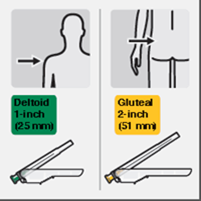
Fig. M
Fixation de l'aiguille
Retirez à moitié le blister et utilisez celui-ci pour saisir l'aiguille par sa base, comme illustré (Fig. N).
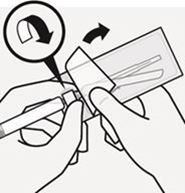
Fig. N
Tout en tenant l'anneau blanc de la seringue, fixez l'embout Luer de l'aiguille sur la seringue en tournant fermement son extrémité dans le sens des aiguilles d'une montre, jusqu'à ce qu'elle soit bien fixée.
Ne pas toucher l'embout Luer de l'aiguille. Ceci provoquerait une contamination.
Remise en suspension des microsphères
Retirez complètement le blister. Immédiatement avant l'injection, agitez encore une fois vigoureusement la seringue, car quelques microsphères pourraient avoir sédimenté (Fig. O).
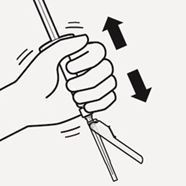
Fig. O
4e étape Injection de la dose
Retrait du capuchon protecteur transparent de l'aiguille
Rabattez le dispositif de sécurité de l'aiguille vers l'arrière, comme indiqué. Puis tenez l'anneau blanc de la seringue et retirez prudemment le capuchon protecteur transparent de l'aiguille en tirant dans l'axe (Fig. P).
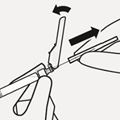
Fig. P
Ne pas dévisser le capuchon protecteur transparent de l'aiguille, car l'embout Luer pourrait se désolidariser.
Élimination des bulles d'air
Tenez l'aiguille verticalement et tapotez doucement pour faire remonter les bulles d'air. Poussez lentement et prudemment sur le piston pour faire sortir l'air (Fig. Q).
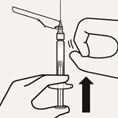
Fig. Q
Injection
Injectez immédiatement tout le contenu de la seringue en intramusculaire (i.m.) dans le muscle fessier ou deltoïde du patient. L'injection dans le muscle fessier s'effectue dans le quart supéro-externe de la région fessière (Fig. R).
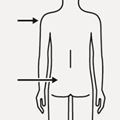
Fig. R
Ne pas administrer par voie intraveineuse.
Recouvrir l'aiguille avec le dispositif de sécurité
Tenez le dispositif de sécurité de l'aiguille d'une main, à un angle de 45 degrés contre une surface dure et plane. Appuyez-le vers le bas par un mouvement rapide et vigoureux jusqu'à ce que l'aiguille s'enclenche complètement dans le dispositif de sécurité de l'aiguille (Fig. S).

Fig. S
Évitez les blessures par piqûre d'aiguille:
N'utilisez pas les deux mains.
Ne détachez pas intentionnellement le dispositif de sécurité de l'aiguille et ne l'utilisez pas de manière incorrecte.
N'essayez pas de redresser l'aiguille ou d'enclencher le dispositif de sécurité si l'aiguille est courbée ou endommagée.
Élimination correcte des aiguilles
Assurez-vous que le dispositif de sécurité de l'aiguille est complètement enclenché. Éliminez la seringue et l'aiguille dans un collecteur de seringues conforme à la réglementation.
Éliminez également l'aiguille non utilisée, fournie dans le conditionnement unitaire (Fig. T).

Fig. T
Numéro d’autorisation56092 (Swissmedic).
PrésentationRisperdal Consta kit d'injection contenant un flacon de 25 mg et une seringue pré-remplie de solvant. [B]
Risperdal Consta kit d'injection contenant un flacon de 37,5 mg et une seringue pré-remplie de solvant. [B]
Risperdal Consta kit d'injection contenant un flacon de 50 mg et une seringue pré-remplie de solvant. [B]
Chaque emballage contient 1 adaptateur pour flacon perforable pour la reconstitution et 2 aiguilles Terumo SurGuard-3 pour injection i.m. (une aiguille à injection 21G UTW 1 pouce (25 mm) munie d'un capuchon protecteur pour l'injection dans le muscle deltoïde et une aiguille à injection 20G TW 2 pouces (51 mm) munie d'un capuchon protecteur pour l'injection dans le muscle fessier).
Titulaire de l’autorisationJanssen-Cilag AG, Zug, ZG.
Mise à jour de l’informationSeptembre 2020
Éléments fournis dans le conditionnement unitaire
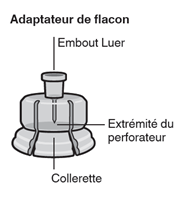
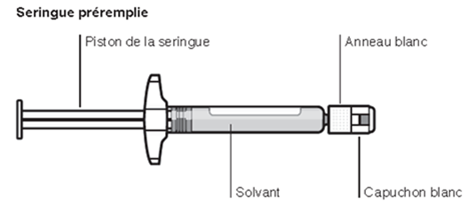
|



























