CompositionPrincipe actif: Fluconazolum.
Excipients
50 mg: Maydis amylum pregelificatum, 16,6 mg lactosum, cellulosum microcristallinum, magnesii stearas, silica colloidalis dioxidum, natrii laurilsulfas E487 (corresp. 0,01 mg de sodium)
150 mg: Maydis amylum pregelificatum, 49,8 mg lactosum, cellulosum microcristallinum, magnesii stearas, silica colloidalis dioxidum, natrii laurilsulfas E487 (corresp. a 0,04 mg de sodium)
200 mg: Maydis amylum pregelificatum, 49,8 mg lactosum, cellulosum microcristallinum, magnesii stearas, silica colloidalis dioxidum, natrii laurilsulfas E487 (corresp. a 0.05 mg de sodium)
corps de la capsule:
50 mg: Gelatina, titanii dioxidum (E171), chinolinum flavum (E104), ferrum oxydatum flavum (E172), bleu patenté V (E131)
150 mg: Gelatina, titanii dioxidum (E171), chinolinum flavum (E104), 0,02 mg jaune orangé S (E110)
200 mg: Gelatina, titanii dioxidum (E171)
Forme pharmaceutique et quantité de principe actif par unitéCapsules dure à 50 mg, 150 mg, 200 mg de fluconazolum.
Indications/Possibilités d’emploiCandidoses des muqueuses. Celles-ci comprennent l’infection de l’oropharynx et de l’œsophage ainsi que les candidoses mucocutanées et les candidoses orales atrophiques chroniques (irritation chez les porteurs de prothèse dentaire).
Les patients sans comorbidités ainsi que les patients immunodéficients peuvent être traités.
Candidose vaginale aiguë ou récidivante.
Prophylaxie des infections à Candida chez les patients atteints de tumeurs malignes et prédisposés à ce type d’infections en raison d’une chimiothérapie anticancéreuse ou d’une radiothérapie.
Dermatomycoses, y compris tinea pedis, tinea corporis, tinea cruris, infections cutanées à Candida.
Pityriasis versicolor lorsqu'un traitement topique n'est pas envisageable ou ne s'est pas avéré suffisamment efficace.
L’utilisation dans le traitement de l’onychomycose n’est pas documentée cliniquement.
Candidémie.
Méningite à Cryptococcus et prophylaxie des récidives de cette maladie chez les patients sidéens. Chez certains patients atteints de méningite à Cryptococcus, l’effet antifongique du fluconazole se développe plus lentement que celui de l’amphotéricine B ou de l’association d’amphotéricine B et de flucytosine, mais il n’existe cependant pas de différence significative par rapport au taux de guérison.
Fluconax peut également être utilisé pour traiter d'autres cryptococcoses (par ex. pulmonaire ou cutanée). Les patients sans comorbidités, les patients sidéens, les transplantés et les autres patients immunosupprimés peuvent également être traités par fluconazole.
Fluconax ne doit pas être utilisé pour le traitement de la teigne (tinea capitis) chez les enfants et les adolescents.
Posologie/Mode d’emploiLa dose journalière de fluconazole doit être déterminée en fonction de la nature et du degré de sévérité de l’infection fongique. La plupart des cas de candidose vaginale répondent à l’administration d’une dose unique. Le traitement des infections qui nécessitent l’administration de doses multiples doit être poursuivi jusqu’à ce que les paramètres cliniques ou les analyses de laboratoire indiquent la disparition de l’infection fongique active. Un traitement de trop courte durée peut conduire à une récidive de l’infection active.
Les directives thérapeutiques en vigueur émanant des associations professionnelles européennes et américaines doivent également être prises en compte pour le traitement des mycoses invasives. En outre, lors de leur spécification, la concentration minimale inhibitrice (CMI) de chaque espèce doit être prise en compte.
Adultes
Indication Posologie Recommandations
Candidose oropharyngée Dose initiale de 200 à 400 Le traitement peut éventuellement
mg le premier jour, puis être poursuivi plus longtemps chez
100 à 200 mg une fois par les patients fortement immunodéprimés
jour les jours suivants .
pendant 7 à 21 jours
(jusqu'à l'obtention d'une
rémission).
Candidose œsophagienne Dose initiale de 200 à 400 La durée du traitement peut être
mg le premier jour, puis prolongée chez les patients
100 à 200 mg une fois par fortement immunodéprimés.
jour les jours suivants
pendant 14 à 30 jours
(jusqu'à l'obtention d'une
rémission).
Candidémie Dose initiale de 800 mg le La durée du traitement dépend de la
premier jour, puis 400 mg réponse clinique. En général, il est
une fois par jour les jours recommandé de poursuivre le
suivants. traitement pendant les 2 semaines
qui suivent la première hémoculture
négative et l'amélioration clinique.
Prophylaxie des infections à 200 à 400 mg une fois par Le traitement doit être instauré
Candida chez les patients jour, en fonction du risque plusieurs jours avant la date prévue
présentant une neutropénie du patient de développer d'apparition de la neutropénie et
persistante une infection à Candida. poursuivi pendant encore 7 jours
après l'atteinte d'un nombre de
neutrophiles >1'000 cellules/mm3.
Prophylaxie des récidives de 100 à 200 mg une fois par Chez les patients présentant une
candidose des muqueuses chez jour ou 200 mg trois fois immunosuppression chronique, la
les patients immunodéprimés par semaine. prophylaxie doit être poursuivie
pour une durée indéterminée.
Candidose orale atrophique 50 mg une fois par jour Traitement par voie orale. Un
chez les porteurs de pendant 14 jours. traitement antiseptique de la
prothèses dentaires prothèse dentaire doit être
entrepris parallèlement.
Candidose vaginale aiguë 150 mg de fluconazole en Traitement par voie orale.
dose unique par voie orale.
Traitement et prophylaxie des 150 mg tous les 3 jours Traitement par voie orale.
candidoses vaginales pour un total de 3 doses
récidivantes (jour 1, 4 et 7), suivi
d'une dose d'entretien de
150 mg une fois par semaine
pendant 6 mois.
Traitement de la méningite à Dose initiale de 400 mg le En cas d'infection menaçant le
Cryptococcus premier jour, puis 200 à pronostic vital, la dose journalière
400 mg une fois par jour peut être augmentée à 800 mg. La
les jours suivants. durée du traitement dépend de la
réponse clinique et mycologique.
Elle est généralement d'au moins 6 à
8 semaines.
Prophylaxie des récidives de 200 mg une fois par jour. Durée du traitement: illimitée.
méningite à Cryptococcus chez
les patients présentant un
risque élevé de récidive
(c.-à-d. les patients
séropositifs ou autrement
immunodéprimés)
Dermatomycoses (par ex. tinea 150 mg une fois par semaine Le tinea pedis peut cependant
pedis, tinea corporis, tinea ou 50 mg une fois par jour nécessiter une durée de traitement
cruris) et candidoses cutanées pendant 2 à 4 semaines. allant jusqu'à 6 semaines.
Pityriasis versicolor 300 à 400 mg une fois par
semaine pendant 1 à 3
semaines ou 50 mg une fois
par jour pendant 2 à 4
semaines.
Mode d'administration
Le fluconazole est disponible aussi bien pour une administration par voie orale (capsules ou poudre pour suspension) que pour une administration intraveineuse (solution pour perfusion). La voie d'administration dépend de l'état clinique du patient.
La biodisponibilité étant similaire entre l'administration par voie orale et intraveineuse, le passage d'une administration intraveineuse à une administration orale (ou vice versa) est possible sans ajustement posologique.
Fluconax peut être pris avec ou sans nourriture.
Instructions posologiques particulières
Enfants et adolescents
Les capsules de Fluconax ne conviennent pas à une utilisation chez les enfants.
D'autres préparations de fluconazole sous une forme galénique appropriée (suspension orale ou solution pour perfusion) doivent être administrées aux enfants. Il faut en particulier tenir compte du fait que les recommandations posologiques suivantes (en mg/kg) ne peuvent pas être appliquées dans tous les cas avec les dosages de capsules disponibles, surtout lorsque le poids corporel est faible.
La posologie chez les enfants et les adolescents est fonction du poids corporel (voir ci-dessous). La dose d'entretien maximale de 400 mg par jour ne doit pas être dépassée.
En principe, le fluconazole est administré une fois par jour.
Pour l'adaptation posologique chez les patients pédiatriques présentant une insuffisance rénale, voir la rubrique "Patients présentant des troubles de la fonction rénale" .
Comme c'est le cas chez les adultes, la durée du traitement dépend de la réponse clinique et mycologique à l'infection correspondante.
Adolescents à partir de 12 ans
La clairance du fluconazole est plus élevée chez les enfants que chez les adultes (voir "Pharmacocinétique" , rubrique "Cinétique pour certains groupes de patients" ). L'exposition des enfants aux doses de 3, 6 et 12 mg/kg est comparable à celle obtenue chez les adultes aux doses de 100, 200 et 400 mg. Chez les adolescents >12 ans, une évaluation individuelle doit être effectuée en fonction du poids corporel et du stade de développement pubertaire afin de déterminer si la dose pour adulte est adaptée ou un ajustement posologique est nécessaire. En cas d'ajustement posologique, les posologies suivantes sont recommandées:
Indication Posologie Recommandations
Candidoses invasives* Dose initiale de 25 selon le degré de sévérité de l'affection.
mg/kg le premier jour Les patients atteints de candidose systémique
(max. 800 mg), suivie doivent être traités pendant au moins 3
de 12 mg/kg une fois semaines et jusqu'à au moins 2 semaines après
par jour (max. 400 mg) la disparition des symptômes.
Candidoses des muqueuses Dose initiale de 6
mg/kg, suivie de 3
mg/kg une fois par jour
Prophylaxie des 3-12 mg/kg une fois par selon le degré de sévérité et la durée de la
infections à Candida jour neutropénie présente (voir posologie chez les
chez les patients adultes)
immunodéprimés
Méningite à Cryptococcus 6-12 mg/kg une fois par selon le degré de sévérité de l'affection
jour
Prophylaxie des 6 mg/kg une fois par
récidives de méningite jour
à Cryptococcus chez les
enfants présentant un
risque élevé de récidive
* Pour le traitement des candidoses invasives, le schéma posologique recommandé pour les patients pédiatriques vise à atteindre une exposition systémique comparable à celle observée chez l'adulte, c'est-à-dire le maintien d'une ASC0-24 comprise entre 400 et 800 mg*h/l.
Patients âgés
Si la fonction rénale est normale (voir ci-dessous), il n’est pas nécessaire de modifier la posologie.
Patients présentant des troubles de la fonction rénale
Le fluconazole est principalement excrété avec l’urine sous forme inchangée. En cas de traitement par dose unique, il n’est pas nécessaire de modifier la posologie.
Lorsqu'un traitement par doses multiples de Fluconax est nécessaire chez des patients présentant une insuffisance rénale, une dose initiale de 50 à 400 mg doit être administrée. Ensuite, la dose journalière (selon l’indication) doit être adaptée comme suit.
Clairance de la créatinine (ml/min) Pourcentage de la dose recommandée
>50 100%
≤50 (sans dialyse) 50%
Hémodialyse 100% après chaque hémodialyse
Si seule la concentration de la créatinine sérique (Ccr) est connue, la clairance de la créatinine (Cl) peut être estimée au moyen de la formule suivante:
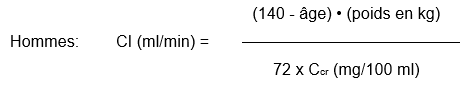
Femmes: résultat de la formule ci-dessus, multiplié par 0,85.
Cet ajustement en fonction de la clairance de la créatinine s'applique également aux enfants et aux adolescents (voir aussi la recommandation posologique pour "Enfants et adolescents" ).
Patients présentant des troubles de la fonction hépatique
Les données disponibles chez les patients atteints d'insuffisance hépatique étant limitées, le fluconazole doit être utilisé avec prudence chez les patients présentant des troubles de la fonction hépatique.
Contre-indicationshypersensibilité connue au fluconazole ou à l'un des excipients de Fluconax, ainsi qu'à d'autres dérivés azolés.
traitement simultané par des médicaments métabolisés par l'iso-enzyme CYP3A4 du cytochrome P450 et susceptibles d'allonger l'intervalle QT, tels que l'amiodarone, la quinidine, l'érythromycine ou le sertindole (voir "Mises en garde et précautions" ).
Mises en garde et précautionsIntervalle QT
Il n'existe pas d'étude approfondie de l'intervalle QT du fluconazole. Certains dérivés azolés ont toutefois été mis en relation avec un allongement du segment QT sur l’ECG et de très rares cas d'allongements de l'intervalle QTc ainsi que de torsades de pointes ont été rapportés depuis l'introduction du fluconazole sur le marché.
En présence de facteurs de risque potentiels de proarythmies, le fluconazole doit donc être utilisé avec prudence. Ces facteurs de risque englobent un allongement congénital ou acquis de l'intervalle QT, des cardiomyopathies (en particulier en présence d'une insuffisance cardiaque), des arythmies symptomatiques préexistantes, une bradycardie sinusale et des déséquilibres électrolytiques (en particulier une hypokaliémie). En outre, le risque est augmenté en cas de traitement concomitant par d'autres médicaments connus pour allonger l'intervalle QTc. Cela vaut en particulier pour les substrats du CYP3A4 ayant un potentiel d'allongement de l'intervalle QT et pour les antiarythmiques tels que l'amiodarone.
Le traitement simultané par des médicaments de ce type peut par conséquent être contre-indiqué (voir aussi "Interactions" et "Contreindications" ).
Avant de débuter et pendant le traitement par le fluconazole, l'équilibre électrolytique doit être surveillé et tout déséquilibre tel qu'une hypokaliémie, une hypomagnésémie et une hypocalcémie doit être corrigé.
Hépatotoxicité
De rares cas d'hépatotoxicité sévère ont été observés avec le fluconazole, dont certains ont eu une issue fatale, en particulier chez des patients atteints de graves maladies de fond. Dans les cas d’hépatotoxicité liée au fluconazole, aucune relation manifeste avec la dose journalière totale, la durée du traitement, le sexe ou l’âge des patients n’a été constatée. En règle générale, l’hépatotoxicité du fluconazole était réversible après l’arrêt du traitement.
Des tests de la fonction hépatique doivent être effectués régulièrement durant un traitement par le fluconazole.
Les patients qui, lors du traitement par le fluconazole, présentent des valeurs anormales des tests de la fonction hépatique doivent être surveillés afin de prévenir le développement d'une lésion hépatique plus grave. Le traitement par le fluconazole doit être arrêté lors de l'apparition d'indices cliniques d’une affection hépatique pouvant être imputée au fluconazole.
La prudence est de rigueur lors de l’administration de fluconazole à des patients présentant des troubles préexistants de la fonction hépatique.
Réactions cutanées
Dans des cas rares, des patients ont développé, durant le traitement par le fluconazole, des réactions cutanées sévères telles qu'un syndrome de Stevens-Johnson, une nécrolyse épidermique toxique, une PEAG (pustulose exanthématique aiguë généralisée) ou un syndrome DRESS. Un syndrome DRESS (Drug Reaction with Eosinophilia and Systemic Symptoms) est caractérisé par trois des symptômes suivants ou plus: réaction cutanée (telle qu'exanthème ou dermite exfoliative), éosinophilie, fièvre et lymphadénopathie ainsi qu'une ou plusieurs complications systémiques telles qu'hépatite, myocardite, néphrite, péricardite, pneumonie interstitielle ou vasculite. Le syndrome DRESS peut survenir avec une latence de plusieurs semaines.
En cas d'apparition d'un exanthème pouvant être mis en relation avec le fluconazole chez un patient traité pour une infection fongique superficielle, le traitement doit être arrêté. Lorsqu'un exanthème apparaît chez un patient atteint d'une infection fongique invasive/systémique, une surveillance stricte s'impose et l'administration de fluconazole doit être arrêtée si des éruptions bulleuses, un érythème multiforme ou des symptômes systémiques supplémentaires tels que fièvre ou lymphadénopathie se développent.
Les patients sidéens sont davantage exposés à l'apparition de réactions cutanées graves.
Utilisation chez les femmes en âge de procréer
Des cas d'anomalies congénitales ont été rapportés chez des enfants dont les mères avaient été exposées au fluconazole pendant la grossesse (surtout pendant le premier trimestre) (voir "Grossesse/Allaitement" ). Des cas d'avortements spontanés ont également été rapportés. Par conséquent, les femmes en âge de procréer doivent utiliser une méthode de contraception fiable pendant le traitement et environ 1 semaine (c.-à-d. 5 à 6 demi-vies) après la dernière dose du traitement
Effets endocriniens
Une insuffisance surrénalienne a été rapportée dans le cadre de l'utilisation d'antifongiques azolés (y compris le fluconazole). Celle-ci était réversible dans la plupart des cas. Il convient de surveiller sur ce point en particulier les patients ayant des facteurs de risque préexistants d'insuffisance surrénalienne et ceux traités par un glucocorticoïde systémique.
Insuffisance rénale
Chez les patients présentant des troubles de la fonction rénale, la prudence est de rigueur lors de l'administration de fluconazole (voir aussi "Instructions posologiques particulières" ).
InteractionsLe fluconazole est un inhibiteur modéré des iso-enzymes CYP2C9 et CYP3A4 du cytochrome P450, ainsi qu'un inhibiteur de l'iso-enzyme CYP2C19. L'administration de fluconazole à des patients recevant en même temps des substances métabolisées par le CYP2C9, le CYP2C19 ou le CYP3A4 peut entraîner une élévation des taux sériques de ces substances (voir "Interactions" ). Lorsque ces substances ont une marge thérapeutique étroite, les patients doivent être surveillés attentivement.
Hypersensibilité
De rares cas d'anaphylaxie ont été décrits.
Les capsules de Fluconax 50/150/200 mg contiennent respectivement 16.60//49.8/66.4 mg de lactose par capsule. Les patients présentant la rare intolérance au galactose, un déficit total en lactase ou un syndrome de malabsorption du glucose et du galactose ne doivent-ils pas prendre ce médicament.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par capsule, c’est-à-dire qu'il est essentiellement „sans sodium“.
Fluconax 150 mg contient jaune orangé S (E110) et peut provoquer des réactions allergiques.
Interactions
Interactions pharmacocinétiques
Le fluconazole est un inhibiteur modéré des enzymes hépatiques CYP3A4 et CYP2C9, ainsi qu'un inhibiteur du CYP2C19. En raison de ces propriétés, le principe actif possède un potentiel d'interactions considérable et il n'est pas possible de nommer ici tous les partenaires d'interaction potentiels. En cas d'administration concomitante d'autres médicaments, il convient donc en principe de consulter aussi leurs informations professionnelles respectives afin de s'informer sur leurs voies métaboliques et sur les ajustements posologiques (ou d'autres mesures) éventuellement nécessaires. Cela s'applique en particulier chez les patients présentant une insuffisance hépatique ou rénale ainsi que chez ceux qui prennent plusieurs comédications.
Influence d’autres substances sur la pharmacocinétique du fluconazole
Rifampicine
L’administration concomitante de fluconazole et de rifampicine, un inducteur puissant des enzymes CYP, a entraîné une réduction de 25% de l’ASC (aire sous la courbe de concentration en fonction du temps) du fluconazole et de 20% de la demi-vie du fluconazole. Lors d’un traitement concomitant par la rifampicine, une augmentation de la dose de fluconazole peut donc s’avérer nécessaire.
L’influence d’autres inducteurs enzymatiques n’a pas été étudiée. Il est toutefois vraisemblable que l’administration concomitante d’autres inducteurs puissants du CYP3A4 (tels que carbamazépine, phénytoïne, mitotane, enzalutamide ou préparations de millepertuis) entraîne des modifications comparables. Il faut dès lors prendre en compte le fait qu'une induction enzymatique peut persister au moins 4 semaines après l'arrêt de l'inducteur.
Hydrochlorothiazide
L'administration concomitante d'hydrochlorothiazide (doses multiples) et de fluconazole a entrainé une augmentation de 40% de la concentration plasmatique du fluconazole. Chez les sujets sains, aucune adaptation posologique n'est nécessaire. Chez les patients atteints d'insuffisance rénale, il faut toutefois tenir compte de cette exposition accrue au fluconazole.
Influence du fluconazole sur la pharmacocinétique d'autres substances
En cas d'administration concomitante avec des médicaments métabolisés par le CYP2C9, le CYP2C19 ou le CYP3A4, le fluconazole peut entraîner une élévation des taux sériques de ces substances. Le risque d'effets indésirables peut être augmenté en conséquence. Les répercussions de cette association dépendent du principe actif et de sa marge thérapeutique. Les patients recevant des traitements concomitants de ce type doivent par conséquent être étroitement surveillés et un ajustement posologique est éventuellement à envisager. Il faut tenir compte du fait que l'effet inhibiteur enzymatique du fluconazole persiste 4 à 5 jours au-delà de l'arrêt du traitement en raison de sa longue demi-vie. En cas d'administration concomitante de substances présentant une fenêtre thérapeutique étroite (telles que la ciclosporine), leur concentration plasmatique doit donc également être surveillée après l'arrêt du fluconazole et la dose doit éventuellement être adaptée.
Il faut également tenir compte du fait qu'en cas d'utilisation de médicaments dont le principe actif est appliqué en tant que prodrogue et la transformation en fraction active implique une participation importante du CYP3A4, du CYP2C9 ou du CYP2C19, l'administration concomitante d'un inhibiteur enzymatique tel que le fluconazole peut entraîner une diminution cliniquement significative des concentrations plasmatiques de la fraction active et ainsi une efficacité réduite. Ceci s'applique par ex. au losartan. Dans le cas d'un traitement concomitant par le fluconazole, la pression artérielle de ces patients doit être étroitement surveillée. D'autres exemples sont la carbamazépine, le clopidogrel, la primidone ou l'acide valproïque.
Substrats du CYP3A4
Dans des études cliniques, l'administration concomitante de fluconazole et de substrats du CYP3A4 a entraîné une augmentation de l'exposition à ces substrats. En cas d'administration concomitante de fluconazole et de substrats du CYP3A4 ayant le potentiel d'allonger l'intervalle QT, le risque de tachyarythmies ventriculaires, y compris de torsades de pointes, est ainsi accru. L'administration concomitante de fluconazole avec de tels principes actifs est donc contre-indiquée. Ceci s'applique par ex. à l'amiodarone, à la quinidine, à l'érythromycine ou au sertindole.
Substrats du CYP2C9/CYP2C19
L'administration concomitante de fluconazole et de substrats du CYP2C9 ou du CYP2C19 peut entraîner une exposition accrue à ces principes actifs. Les patients traités à la fois par du fluconazole et des substrats de ces iso-enzymes doivent faire l'objet d'une surveillance étroite quant aux effets indésirables.
Le tableau suivant présente des exemples de médicaments dont la pharmacocinétique peut être influencée par le fluconazole. Cette liste ne prétend pas être exhaustive. En cas d'administration concomitante d'autres médicaments et de fluconazole, il convient donc en principe de consulter aussi leurs informations professionnelles respectives. Des effets similaires sont également à prévoir avec d'autres principes actifs qui sont aussi des substrats du CYP3A4, du CYP2C9 ou du CYP2C19.
Les recommandations suivantes sont définies comme suit:
· "contre-indiqué" : substrats du CYP3A4, du CYP2C9 ou du CYP2C19 associés à des effets indésirables potentiellement graves et irréversibles dans certains cas (par ex. torsades de pointes, rhabdomyolyse, etc.). Le médicament ne doit en aucun cas être co-administré avec du fluconazole (voir "Contreindications" ).
· "déconseillé" : substrats du CYP3A4, du CYP2C9 ou du CYP2C19 s'accompagnant d'une augmentation ou d'une réduction des concentrations plasmatiques associées à un risque significativement accru d'effets indésirables cliniquement pertinents ou dont une efficacité réduite représente un risque pertinent pour le patient. L'utilisation de ce type de médicament pendant le traitement ou au cours des deux semaines suivant l'arrêt du fluconazole doit être évitée, sauf si le bénéfice l'emporte sur les risques potentiellement accrus. Si, en raison de l'absence d'alternatives ou d'une intolérance aux autres principes actifs, l'administration concomitante est inévitable, le patient doit faire l'objet d'une surveillance minutieuse et étroite, et la posologie du médicament co-administré doit éventuellement être adaptée. Pour les principes actifs pour lesquels des concentrations cibles sont définies, il est recommandé de surveiller les concentrations plasmatiques ( "Therapeutic Drug Monitoring" , TDM).
· "à utiliser avec précaution" : substrats du CYP3A4, du CYP2C9 ou du CYP2C19 pour lesquels des concentrations plasmatiques accrues ou réduites peuvent représenter un risque cliniquement pertinent. Si le médicament est co-administré avec le fluconazole, une surveillance minutieuse est recommandée. Pour les principes actifs pour lesquels des concentrations cibles sont définies, un TDM est recommandé. La posologie du médicament co-administré doit éventuellement être adaptée.
· "utilisation possible" : aucune interaction cliniquement pertinente. L'utilisation concomitante du principe actif et de fluconazole est possible et aucun ajustement posologique n'est nécessaire.
Type de recommandati Exemples de principes actifs concernés
on
contre-indiqué substrats du CYP3A4 connus pour allonger l'intervalle QT (par ex. amiodarone,
quinidine, citalopram, érythromycine, sertindole)
déconseillé alcaloïdes de l'ergot de seigle métabolisés par le CYP3A4 vénétoclax (pendant
la titration de dose) voriconazole différents principes actifs
antinéoplasiques (par ex. olaparib, vinca-alcaloïdes)
à utiliser avec abrocitinib aprépitant avanafil benzodiazépines de courte durée d'action (par
précaution (et ex. midazolam, triazolam) inhibiteurs calciques (par ex. amlodipine,
éventuellement avec félodipine) carbamazépine célécoxib ciclosporine évérolimus isavuconazole
un ajustement ivabradine ivacaftor glucocorticoïdes métabolisés par le CYP3A4 méthadone
posologique) AINS (par ex. diclofénac, ibuprofène, naproxène) opiacés de courte durée
d'action (alfentanil, fentanyl) opiacés de longue durée d'action (par ex.
oxycodone) inhibiteurs de la pompe à protons ranolazine sildénafil sirolimus
statines sulfonylurées tacrolimus tadalafil théophylline antidépresseurs
tricycliques (amitriptyline, nortriptyline) vardénafil antagonistes de la
vitamine K différents principes actifs antinéoplasiques (par ex. bortézomib,
cyclophosphamide, géfitinib, ibrutinib, tofacitinib) différents principes
actifs antiviraux (par ex. atazanavir, darunavir, névirapine, tipranavir,
zidovudine) zopiclone
ajustement posologiq bosentan carbamazépine préparations de millepertuis phénobarbital phénytoïne
ue du fluconazole rifabutine/rifampicine
éventuellement
nécessaire
En cas d'administration concomitante d'associations d'antiviraux (VIH ou VHC), il faut tenir compte du fait que l'effet net de l'interaction attendue dépend fortement des propriétés pharmacocinétiques des principes actifs contenus (substrats, inducteurs, inhibiteurs enzymatiques).
Pour les médicaments pour lesquels il existe des études d'interactions spécifiques avec le fluconazole, les résultats sont présentés en détail dans le tableau ci-dessous.
Médicament Schéma thérapeutique Modification des Recommandation
paramètres PKa
abrocitinib 100 mg d'abrocitinib/400 abrocitinib et métabolite à utiliser avec
mg de fluconazole le s actifs: ASC ↑ 2.55 précaution
jour 1 suivis de 200 mg (2.42-2.69) Cmax ↑ 1.23
de fluconazole QD les (1.08-1.42)
jours 2-7
alfentanil 20 µg/kg d'alfentanil/400 clairance ↓ 55% Vss ↓ à utiliser avec
mg de fluconazole oral 19%b t½ ↑ 67% ASC ↑ 97% précaution
20 µg/kg d'alfentanil/400 clairance ↓ 58% Vss ↓
mg de fluconazole IV 19% t½ ↑ 80% AUC ↑ 107%
azithromycine 1200 mg d'azithromycine Cmax ↔ASC ↔ utilisation possible
orale/800 mg de fluconazo
le oral
benzodiazépines à utiliser avec
(courte durée précaution
d'action):
midazolam oral 7.5 mg de midazolam/400 ASC ↑ 200% Cmax ↑ 150%
mg de fluconazole oral t½ ↑ 150%
7.5 mg de midazolam/400 ASC ↑ 100% Cmax ↑ 100%
mg de fluconazole IV t½ ↑ 150%
triazolam 0.25 mg de triazolam/50 ASC 1.6 (1.30, 2.34)
mg de fluconazole oral QD Cmax 1.47 (1.08, 2.07)
t½ 1.3 (1.02, 1.70)
0.25 mg de triazolam/100 ASC 2.10 (1.42, 3.57)
mg de fluconazole oral QD Cmax 1.40 (0.94, 2.34)
t½ 1.8 (1.40, 2.29)
0.25 mg de triazolam/200 ASC 4.40 (2.38, 9.49)
mg de fluconazole oral QD Cmax 2.33 (1.33, 4.44)
t½ 2.30 (1.67, 3.23)
carbamazépine 400 mg de carbamazépine clairance ↓ 50% concentra à utiliser avec
TID/150 mg de fluconazole tion sérique de carbamazé précaution
QD pendant 3 jours pine ↑ 100%
célécoxib célécoxib 200 mg avec Cmax ↑ 68%ASC ↑ 134% à utiliser avec
fluconazole 200 mg par précaution
jour
éthinylestradiol/ après administration éthinylestradiol ASC L'influence sur
lévonorgestrel concomitante de 50 mg de ↔lévonorgestrel ASC ↔ l'efficacité contracepti
(0.03 mg/0.15 mg) fluconazole par jour: ve est improbable.
(contraceptif Aucune étude n'a été
hormonal combiné) menée avec des contracep
tifs contenant d'autres
composants progestatifs.
après administration éthinylestradiol ASC ↑
concomitante de 200 mg 40% lévonorgestrel AUC ↑
de fluconazole par jour: 24%
fentanyl 5 µg/kg de fentanyl IV clairance 0.81 (0.69, à utiliser avec
le jour 2/400 mg de 0.95) ASC 1.23 (1.05, précaution
fluconazole oral le jour 1.45) t½ ↔
1, suivis de 200 mg de
fluconazole oral le jour
2
AINS flurbiprofène 100 mg de flurbiprofène ASC ↑ 81%Cmax ↑ 23% à utiliser avec
oral/200 mg de fluconazol précaution
e oral
ibuprofène 400 mg d'ibuprofène Isomère pharmacologiqueme
oral/400 mg de fluconazol nt actif [S-(+)-ibuprofèn
e oral le jour 1, suivis e]: ASC 1.82 (1.72,
de 200 mg de fluconazole 1.92) Cmax 1.15 (1.06,
oral 1.24)
rifabutine 300 mg de rifabutine ASC ↑ 76%Cmax ↑ 91% à utiliser avec
orale/200 mg de fluconazo précaution
le oral
saquinavir 1200 mg de saquinavir ASC ↑ 50%Cmax ↑ 56%claira à utiliser avec
oral/200 mg de fluconazol nce ↓ 50% précaution
e oral QD
tacrolimus 0.1 mg/kg/jour de Ctrough médiane ↑ 40% à utiliser avec
tacrolimus IV le jour 1, (100 mg/jour de fluconazo précaution
suivi de 0.15 mg/kg par le) et ↑ 210% (200
voie orale BID/100 mg ou mg/jour de fluconazole)
200 mg QD de fluconazole
oral
théophylline 240 mg de théophylline Kel ↓ 19%cclairance ↓ 18% à utiliser avec
orale/100 mg BID de précaution
fluconazole pendant 14
jours
voriconazole voriconazole oral (400 Cmax 1.57 (1.20, déconseillé
mg toutes les 12 h 2.07)ASCτ 1.79 (1.41,
pendant 1 jour, puis 200 2.28) Une réduction de
mg toutes les 12 h la dose et/ou un
pendant 2.5 jours), allongement de l'interval
fluconazole oral (400 mg le posologique n'ont pas
le jour 1, puis 200 mg entraîné de diminution
toutes les 24 h pendant de l'interaction.
4 jours)
zidovudine 200 mg de zidovudine ASC ↑ 74%,Cmax ↑ à utiliser avec
orale TID/400 mg de 84%,clairance ↓ 43%,t½ ↑ précaution
fluconazole oral QD 128%.
pendant 7 jours
a si disponible: rapport test/référence (geometric mean changes) avec un intervalle de confiance de 90% ou de 95%; sinon, modification de chaque paramètre en pourcentage.
b "Vss" : Steady-state volume of distribution (volume de distribution à l'état d'équilibre).
c "kel" : elimination rate constant (constante de vitesse d'élimination).
"QD" : une fois par jour, "BID" : deux fois par jour, "TID" : trois fois par jour.
Interactions pharmacodynamiques
Antagonistes de la vitamine K
Dans une étude d'interactions, un allongement du temps de prothrombine de 12% a été observé lors de l'administration concomitante de fluconazole et de warfarine à des sujets en bonne santé. Il n'existe aucune étude avec l'acénocoumarol ou la phenprocoumone. Après la commercialisation, des saignements (épistaxis, hématurie, méléna, hémorragies gastro-intestinales) ont été décrits en relation avec une augmentation du temps de prothrombine chez des patients recevant simultanément du fluconazole et de la warfarine. Chez les patients qui reçoivent des anticoagulants antagonistes de la vitamine K conjointement avec du fluconazole, il faut contrôler étroitement l'INR et, le cas échéant, adapter la posologie des anticoagulants.
Amphotéricine B
Des études in vitro ont mis en évidence un antagonisme entre l'amphotéricine B et les dérivés azolés. Le mécanisme d'action des imidazolés repose sur l'inhibition de la synthèse de l'ergostérol au niveau de la membrane cellulaire fongique. L'amphotéricine B se lie aux stéroïdes dans la membrane cellulaire et modifie la perméabilité de celle-ci. Un effet semblable peut survenir avec l'amphotéricine B liposomale. La pertinence clinique de cet antagonisme est encore inconnue.
Dans le cadre d'expériences animales, l'administration concomitante de fluconazole et d'amphotéricine B à des souris immunodéficientes ou immunocompétentes infectées a donné les résultats suivants: antagonisme des deux principes actifs dans les cas d'infection systémique à A. fumigatus; aucune interaction dans les cas d'infection intracrânienne à Cryptococcus neoformans; léger effet antifongique additif dans les cas d'infection systémique à C. albicans. La pertinence clinique de ces résultats n'est pas connue.
Grossesse, allaitementGrossesse
L'utilisation du fluconazole pendant la grossesse doit être évitée sauf si, en présence d'une infection fongique sévère ou potentiellement létale, les bénéfices attendus du fluconazole l'emportent sur les risques encourus par le fœtus. Une grossesse doit être exclue avant le début du traitement. (pour l'utilisation chez les femmes en âge de procréer, voir "Mises en garde et précautions" ).
Des cas d’anomalies congénitales multiples ont été rapportés chez des enfants dont les mères avaient été traitées (surtout pendant le premier trimestre de la grossesse) pendant trois mois ou plus par des doses élevées de fluconazole (400 à 800 mg/jour). Il s’agit ici d’un schéma de malformations caractéristique rare qui a comporté les anomalies suivantes: brachycéphalie, fentes palatines et autres malformations faciales, développement anormal de la voûte crânienne, os anormalement longs, côtes anormalement minces, fémurs arqués et arthrogrypose, ainsi que des anomalies cardiaques congénitales. Un lien entre l’administration du fluconazole et ces événements indésirables ne peut pas être exclu.
Des cas d'avortements spontanés et d'anomalies congénitales (en particulier du système cardiovasculaire) chez des enfants ont également été rapportés lorsque les mères avaient été traitées par seulement 150 mg de fluconazole en doses uniques ou multiples au cours du premier trimestre de grossesse.
Dans les études chez l’animal, des effets indésirables sur le fœtus ont été également observés lorsque des doses, toxiques pour la mère, étaient administrées (voir "Données précliniques" ).
Allaitement
Le fluconazole passe dans le lait maternel. Des concentrations de fluconazole dans le lait maternel semblables aux concentrations plasmatiques ont été observées (voir "Pharmacocinétique" ). L'absorption quotidienne de fluconazole par le nourrisson à travers le lait maternel (lors d'une absorption de 150 ml/kg/jour de lait maternel) est estimée à environ 40% de la dose néonatale recommandée (pour les nourrissons de moins de 2 semaines) ou de 13% de la dose recommandée pour les nourrissons souffrant de candidose des muqueuses.
Il est déconseillé d'allaiter pendant l'utilisation de fluconazole, en particulier à des doses élevées.
En revanche, l'allaitement peut être poursuivi après une dose unique de 150 mg de fluconazole. Il est toutefois recommandé de tirer le lait et de l'éliminer pendant les 48 heures suivant la prise du médicament.
Effet sur l’aptitude à la conduite et l’utilisation de machinesAucune étude concernant l'influence du fluconazole sur l’aptitude à la conduite n’a été menée. Le fluconazole peut cependant entraîner des effets indésirables tels que des vertiges et, occasionnellement, des crises convulsives, qui sont susceptibles d’altérer la capacité à conduire des véhicules et à utiliser des machines.
Effets indésirablesLes effets indésirables suivants ont été observés pendant le traitement par le fluconazole avec la fréquence suivante: très fréquents (≥1/10), fréquents (≥1/100 à <1/10), occasionnels (≥1/1'000 à <1/100), rares (≥1/10'000 à <1/1'000), très rares (<1/10'000), fréquence inconnue (événements obtenus le plus souvent à partir de notifications spontanées de surveillance du marché et dont la fréquence exacte ne peut être estimée de manière fiable).
Affections hématologiques et du système lymphatique
Rares: neutropénie, leucopénie, thrombopénie, agranulocytose.
Affections du système immunitaire
Rares: anaphylaxie, angioœdème.
Troubles du métabolisme et de la nutrition
Rares: hypokaliémie, hypertriglycéridémie, hypercholestérémie.
Affections psychiatriques
Occasionnels: insomnie, somnolence.
Affections du système nerveux
Fréquents: céphalées.
Occasionnels: vertiges, paresthésies, dysgueusie, convulsions.
Rares: tremblements.
Affections de l'oreille et du labyrinthe
Occasionnels: vertige rotatoire.
Affections cardiaques
Rares: allongement du QT, torsades de pointes.
Affections gastrointestinales
Fréquents: douleur abdominale, diarrhée, nausées, vomissements.
Occasionnels: bouche sèche, flatulence, dyspepsie.
Affections hépatobiliaires
Fréquents: augmentation de l'ALAT et/ou de l'ASAT, augmentation des phosphatases alcalines.
Occasionnels: hyperbilirubinémie, ictère, cholestase.
Rares: hépatite, nécrose hépatocellulaire, insuffisance hépatique (avec issue fatale dans des cas isolés).
Affections de la peau et du tissu sous-cutané
Fréquents: exanthème.
Occasionnels: prurit, urticaire, transpiration accrue, exanthème médicamenteux (y compris exanthème médicamenteux fixe).
Rares: alopécie, œdème de la face, dermite exfoliative, réactions cutanées sévères (par ex. syndrome de Stevens-Johnson, nécrolyse épidermique toxique, PEAG et syndrome DRESS; voir "Mises en garde et précautions" ).
Affections musculo-squelettiques et du tissu conjonctif
Occasionnels: myalgie.
Troubles généraux
Occasionnels: fatigue, malaise, asthénie, fièvre.
Chez certains patients, en particulier chez ceux souffrant de maladies primaires sévères telles que le SIDA ou de tumeurs malignes, des anomalies des fonctions rénale et hépatique et des troubles hématologiques tels qu’une éosinophilie et une anémie (voir "Mises en garde et précautions" ) ont été observées pendant le traitement par le fluconazole ou par d’autres préparations comparables. Leur signification clinique et leur lien de causalité avec le traitement par le fluconazole ne sont toutefois pas clairs.
Pédiatrie
Dans les études cliniques, le profil et la fréquence des effets indésirables (y compris les modifications des paramètres biologiques) étaient comparables chez les enfants et chez les adultes.
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageSignes et symptômes
Des cas d’hallucinations et/ou de comportements paranoïdes ont été rapportés après un surdosage du fluconazole (avec des doses supposées allant jusqu’à 8200 mg).
Traitement
Il n’existe aucun antidote spécifique. Un traitement symptomatique (avec des mesures de soutien et un lavage gastrique si nécessaire) doit éventuellement être mis en place.
Le fluconazole est essentiellement excrété dans l’urine; une diurèse forcée pourrait donc favoriser son élimination. Une séance d’hémodialyse de 3 heures réduit les concentrations plasmatiques de 50% environ.
Propriétés/EffetsCode ATC: J02AC01
Antifongique à usage systémique, dérivé triazolé.
Mécanisme d'action
Le fluconazole est un antifongique triazolé qui inhibe de façon spécifique la synthèse des stérols fongiques. Le fluconazole présente une plus grande sélectivité pour les enzymes fongiques dépendantes du cytochrome P450 que pour les systèmes enzymatiques du cytochrome P450 des mammifères.
Pharmacodynamique
Microbiologie/développement de résistances
In vitro, le spectre d'action antifongique du fluconazole comprend la plupart des espèces de Candida cliniquement pertinentes (telles que notamment C. albicans, C. parapsilosis et C. tropicalis).
La concentration minimale inhibitrice (CMI) a tendance à être supérieure pour C. glabrata.
C'est également le cas pour C. dubliniensis et C. guilliermondii. Les preuves d'une efficacité adéquate du fluconazole sur ces espèces sont insuffisantes.
C. krusei est intrinsèquement résistant au fluconazole.
C. auris a tendance à se montrer relativement résistant au fluconazole.
Des surinfections par des espèces non albicans pas ou peu sensibles au fluconazole (telles que C. krusei) ont été décrites. Dans ce cas, un traitement antifongique alternatif est alors nécessaire.
De plus, le fluconazole affiche une efficacité in vitro contre Cryptococcus neoformans et Cryptococcus gattii.
Des résistances croisées avec d'autres antifongiques azolés sont possibles.
Valeurs critiques EUCAST (European Committee on Antimicrobial Susceptibility Testing)
Sur la base d'une analyse des données pharmacocinétiques/pharmacodynamiques, ainsi que des données sur la sensibilité in vitro et la réponse clinique, l'EUCAST-AFST (European Committee on Antimicrobial Susceptibility Testing – Subcommittee on Antifungal Susceptibility Testing) a défini des valeurs critiques du fluconazole pour les différentes espèces de Candida (EUCAST Fluconazole rational document (2020) – v. 3; European Committee on Antimicrobial Susceptibility Testing, antifungal agents, breakpoint tables for interpretation of MICs, v. 10.0, 04.02.2020). Ces valeurs critiques sont présentées dans le tableau suivant:
Pathogène Valeur critique CMI
(mg/l)
S (sensible) R (résistant)
Candida albicans ≤2 >4
Candida dubliniensis ≤2 >4
Candida glabrata ≤0.001 >16*
Candida parapsilosis ≤2 >4
Candida tropicalis ≤2 >4
Candida krusei -- --
S = sensible, R = résistant -- = test de sensibilité
non recommandé, car le fluconazole n'est que peu adapté
à cette espèce. * Une part considérable des infections
a concerné C. glabrata avec une CMI de 2–16 mg/l pour
le fluconazole et une absence de mécanisme de
résistance. Le fluconazole peut être un choix
convenable dans les soins médicaux de base, seuls
quelques principes actifs étant à disposition pour le
traitement des infections des voies urinaires et de la
muqueuse. Dans les cas où le fluconazole est le seul
antifongique disponible pour le traitement des
infections par C. glabrata, un dosage supérieur peut
être nécessaire.
Efficacité clinique
Aucune donnée d'étude clinique disponible.
Dans le modèle animal, le fluconazole s'est avéré efficace aussi bien après administration intraveineuse qu'après administration orale pour le traitement des infections fongiques suivantes:
·infections à Candida sp., y compris la candidose systémique chez l'animal immunodéficient,
·infections à Cryptococcus neoformans, y compris les infections intracrâniennes,
·infections à Microsporum sp.,
·infections à Trichophyton sp..
PharmacocinétiqueAbsorption
Les propriétés pharmacocinétiques du fluconazole en administration intraveineuse et orale sont semblables. Après administration orale, le fluconazole est bien résorbé, les concentrations plasmatiques et la biodisponibilité systémique atteignent plus de 90% de celles obtenues après administration intraveineuse.
Les concentrations plasmatiques sont proportionnelles à la dose administrée. Les pics de concentration plasmatique après une administration unique orale de 100 mg et de 400 mg de fluconazole sont de 1,9 mg/l et de 6,7 mg/l respectivement. Une administration orale pendant 6 à 10 jours conduit à une concentration plasmatique maximale 2,5 fois plus élevée que celle obtenue après une dose unique.
Les concentrations plasmatiques à l'état d'équilibre sont atteintes en 5 à 10 jours lors d'une administration orale de 50 à 400 mg une fois par jour. Si la dose est doublée le premier jour de traitement, les 90% de la concentration plasmatique observée à l’état d’équilibre sont atteints dès le 2e jour.
La résorption après administration orale n'est pas influencée par la prise simultanée de nourriture. Chez le sujet à jeun, les concentrations plasmatiques maximales surviennent environ 0.5 à 1.5 heure après l'administration du médicament.
Distribution
Le volume de distribution est proche de celui de l’eau corporelle totale (0,8 l/kg). La liaison aux protéines plasmatiques est faible (12%). Les concentrations dans la salive et dans les expectorations sont semblables aux concentrations plasmatiques. Chez les patients atteints de méningite fongique, les concentrations de fluconazole dans le liquide céphalorachidien atteignent 80% des concentrations plasmatiques. En l’absence d’inflammation méningée, les concentrations dans le liquide céphalorachidien représentent 60% des concentrations plasmatiques.
Dans la couche cornée, dans l’épiderme et dans les glandes sudoripares de la peau, le fluconazole atteint des concentrations élevées, qui dépassent les concentrations sériques. Le fluconazole s’accumule dans la couche cornée. Lors de l’administration d’une dose journalière de 50 mg en une seule prise pendant 12 jours, les concentrations de fluconazole dans la couche cornée étaient de 73,3 µg/g après 12 jours; elles atteignaient encore 5,8 µg/g sept jours après l’arrêt du traitement. Pour une posologie de 150 mg une fois par semaine pendant 2 semaines, la concentration maximale dans la couche cornée était de 23,4 µg/g le 7e jour et de 7,1 µg/g 7 jours après la deuxième dose.
Le fluconazole passe la barrière placentaire et passe dans le lait maternel. Dans une étude menée sur n = 10 sujets, le fluconazole était détectable dans le lait maternel pendant 48 heures après l'administration d'une dose unique de 150 mg. La concentration moyenne dans le lait maternel correspondait à environ 98% de celle dans le plasma de la mère.
Métabolisme
Aucun métabolite circulant n'a été détecté.
Élimination
La demi-vie plasmatique est d’environ 30 heures. Le fluconazole est essentiellement excrété par voie rénale; 80% de la dose administrée sont éliminés sous forme inchangée dans l’urine. La clairance du fluconazole est proportionnelle à la clairance de la créatinine.
La longue demi-vie plasmatique permet l’administration d’une dose unique en cas de candidose vaginale et l’administration d’une dose quotidienne ou d’une dose hebdomadaire dans les autres indications.
Le fluconazole agit spécifiquement sur les enzymes fongiques dépendantes du cytochrome P450. Le fluconazole n’influence ni les concentrations plasmatiques de testostérone chez l’homme ni les concentrations d’hormones stéroïdes chez la femme en âge de procréer.
Cinétique pour certains groupes de patients
Enfants et adolescents
Chez les enfants, la clairance systémique est environ deux fois plus élevée que chez les adultes. Par conséquent, la demi-vie est plus courte chez les enfants (environ 20 heures) que chez les adultes. Lors d’une administration une fois par jour, l’état d’équilibre a été atteint après environ 4 à 5 jours chez les enfants.
Le volume de distribution est plus élevé chez les enfants que chez les adultes: 950 ml/kg chez les enfants dont l’âge moyen est de 6 mois et 880 ml/kg chez les enfants dont l’âge moyen est de 10 ans.
Données pharmacocinétiques chez les enfants et les adolescents
Âge Posologie (mg/kg) N Demi-vie(heures) Vd(ml/kg) Cmax(μg/ml) AUC(μg-h/ml)
9 mois-13 ans Suspension orale, 16 25.0(16-45) - 2.9 94.7(48-164)
dose unique de 2
mg/kg
9 mois-13 ans Suspension orale, 14 19.5(10-59) - 9.77 362.5(131-725)
dose unique de 8
mg/kg
5 ans–15 ans IV, doses multiples 4 17.4*(15-20) 722(484-1004) 5.5 N=5 67.4(51-84)
de 2 mg/kg
5 ans–15 ans IV, doses multiples 5 15.2*(9-24) 729(467-1044) 11.4 N=7 139.1(58-192)
de 4 mg/kg
5 ans–15 ans IV, doses multiples 7 17.6*(10-26) 1069(725-1680) 14.1 N=8 196.7(134-247)
de 8 mg/kg
5 ans–15 ans Suspension orale, 11 15.5(11-22) - 5.27 41.6(32-59)
doses multiples de
3 mg/kg
* Déterminée le dernier jour.
Patients âgés
La pharmacocinétique d’une dose orale unique de 50 mg de fluconazole a été étudiée chez 22 volontaires d’un âge ≥65 ans. 10 de ces patients ont reçu simultanément un diurétique. Par rapport aux données de populations d'adultes plus jeunes, la concentration plasmatique maximale était augmentée d’un facteur d'environ 1.4 et elle a été atteinte 1,2 heure après la prise. Par rapport aux sujets jeunes, l’ASC moyenne était augmentée d’un facteur d'environ 2.2 et la demi-vie était allongée d’un facteur d'environ 2.1. De plus, la clairance rénale estimée ainsi que le pourcentage de substance inchangée dans l’urine étaient plus bas chez les volontaires âgés que chez les sujets plus jeunes. Les valeurs de la clairance de la créatinine étaient en général aussi diminuées (en moyenne à 74 ml/min) chez les sujets âgés. Ces résultats indiquent que la modification de la pharmacocinétique du fluconazole chez les patients âgés par rapport aux patients plus jeunes est due à la limitation de la fonction rénale.
Troubles de la fonction rénale
Une réduction de la fonction rénale influence fortement la pharmacocinétique du fluconazole. Il existe un rapport inverse entre la demi-vie d'élimination de la substance et la clairance de la créatinine. En cas d'insuffisance rénale, il peut s'avérer nécessaire de réduire la dose de Fluconax (voir "Instructions posologiques particulières: Patients présentant des troubles de la fonction rénale" ).
Hémodialyse: une hémodialyse de 3 heures réduit les concentrations plasmatiques de fluconazole de 50% environ.
Troubles de la fonction hépatique
La pharmacocinétique du fluconazole n'a pas été étudiée chez les patients présentant une insuffisance hépatique.
Données précliniquesMutagénicité
Les études de mutagénicité avec le fluconazole portant sur quatre souches de S. typhimurium et sur le système des cellules L5178Y de lymphome chez la souris, avec et sans activité métabolique, sont restées négatives. Les études cytogénétiques in vivo (cellules de moelle osseuse de souris après administration orale de fluconazole) et les études in vitro (lymphocytes humains dans une solution contenant 1000 µg/ml de fluconazole) n'ont mis en évidence aucun indice de mutations chromosomiques.
Carcinogénicité
Des études au long cours menées sur des souris et des rats qui ont reçu du fluconazole durant 24 mois à des doses journalières orales de 2,5 mg/kg, 5 mg/kg ou 10 mg/kg (environ 2 à 7 fois la dose recommandée chez l’homme) n’ont mis en évidence aucun indice de potentiel cancérogène du fluconazole.
Les rats mâles, traités par 5 mg et 10 mg de fluconazole/kg/jour, ont présenté une incidence accrue d’adénomes hépatocellulaires.
Fertilité
La fertilité des rats mâles et femelles n’a pas été influencée par l’administration quotidienne de 5 mg, 10 mg ou 20 mg de fluconazole p.o., ou de 5 mg, 25 mg ou 75 mg de fluconazole/kg en IV bien que la gestation ait été légèrement prolongée pour des doses orales de 20 mg/kg.
Toxicité sur la reproduction
Dans des études d'embryotoxicité menées sur des rats, des dosages de 5 ou 10 mg/kg n’ont pas eu d’influence sur le fœtus. À des dosages de 25 mg/kg et 50 mg/kg ou plus, des anomalies anatomiques (côte supplémentaire, dilatation des bassinets) ainsi qu’un retard de l’ossification ont été observés à une fréquence accrue. Chez les rats qui ont reçu des doses allant de 80 mg/kg (environ 20 à 60 fois la dose recommandée chez l’homme) à 320 mg/kg, des anomalies fœtales telles que des côtes ondulées, une fente palatine et une ossification craniofaciale défectueuse ont été fréquemment observées. En outre, le taux de mortalité était accru. Ces effets s’accompagnent d’une inhibition de la synthèse des œstrogènes chez les rats et sont probablement la conséquence de l’effet connu d’une diminution du taux d’œstrogènes sur la grossesse, l’organogenèse et la mise bas.
Chez les lapines en gestation, une altération du gain pondéral a été observée pour tous les dosages du fluconazole. À des doses supérieures à 20 mg/kg, des avortements se sont produits.
Dans une étude périnatale menée sur des rats traités par 5 mg/kg, 20 mg/kg et 40 mg/kg de fluconazole IV, une dystocie et une prolongation de la mise bas ont été observées chez certains animaux à la posologie de 20 mg/kg (environ 5 à 15 fois la posologie recommandée chez l’homme) et à la posologie de 40 mg/kg; ces manifestations n’ont cependant pas été observées pour une posologie de 5 mg/kg.
À ces doses, les mises bas compliquées étaient accompagnées d’une légère augmentation du nombre de mort-nés et d’une diminution de celui des nouveau-nés survivants.
Chez les rats, l’effet sur la mise bas peut être imputé à l’effet antiœstrogénique, spécifique à l’espèce, des hautes doses de fluconazole. Chez les femmes traitées par fluconazole, ces modifications hormonales n’ont pas été observées.
Remarques particulièresStabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention "EXP" sur l’emballage.
Remarques particulières concernant le stockage
Conserver hors de portée des enfants et à température ambiante (15°C-25°C) dans l’emballage d’origine.
Remarques concernant la manipulation
Les capsules doivent être avalées entières.
Numéro d’autorisation57'182 (Swissmedic).
PrésentationFluconax 50 mg: emballages à 7 et 28 capsules.
Fluconax 150 mg: emballages à 1 et 4 capsules.
Fluconax 200 mg: emballages à 2 et 7 capsules.
Titulaire de l’autorisationDrossapharm SA, 4002 Bâle.
Mise à jour de l’informationJuillet 2025
|