Propriétés/EffetsCode ATC
N06DX05
Groupe pharmaco-thérapeutique: système nerveux, psychoanaleptiques, médicaments anti-démence, autres médicaments anti-démence.
Le Donanemab est un anticorps monoclonal humanisé recombinant produit dans des cellules ovariennes de hamster chinois (Chinese Hamster Ovary, CHO).
Mécanisme d'action
Le donanemab est un anticorps monoclonal d'immunoglobuline 1 (IgG1) dirigé contre la forme tronquée N terminale insoluble modifiée avec du pyroglutamate de la protéine bêta-amyloïde (N3pG Aβ), qui n'est présente que dans les plaques amyloïdes du cerveau. Le donanemab se lie à N3pG Aβ et aide à la clairance des plaques par phagocytose médiée par les microglies.
Pharmacodynamique
Chez les patients traités par donanemab, une réduction des plaques amyloïdes cérébrales a été observée par tomographie par émission de positrons (PET) à l'amyloïde. Le donanemab a réduit la physiopathologie Tau mesurée par la P-Tau217 dans le plasma.
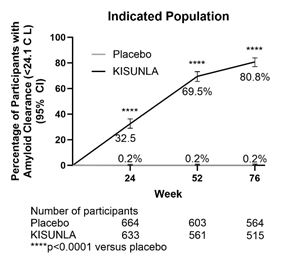
Le pourcentage de patients traités par donanemab ayant atteint une clairance amyloïde (amyloid clearance, c'est-à-dire inférieure à 24.1 centiloïdes) dans l'étude TRAILBLAZER-ALZ 2 était de 32.5% à la semaine 24, de 69.5% à la semaine 52 et de 80,8% à la semaine 76 dans la population indiquée.
Dans l'étude TRAILBLAZER-ALZ 2, la différence entre le donanemab et le placebo concernant la modification de la concentration d'amyloïde entre la valeur initiale et la semaine 76 était statistiquement significative dans la population indiquée (-89.24 centiloïdes).
Dans l'étude TRAILBLAZER-ALZ 6, une réduction similaire des plaques amyloïdes a été observée à la semaine 24 pour la posologie de 350/700/1050 mg, puis de 1400 mg toutes les 4 semaines, par rapport à celle observée avec la posologie de 700 mg pour les trois premières perfusions, puis de 1400 mg toutes les 4 semainesétudiée dans l'étude pivot.
L'exposition au donanemab a diminué avec l'augmentation du titre d'ADA. Une réduction de bêta-amyloïde a été constatée indépendamment du titre d'ADA. Une association entre la présence d'ADA et les résultats sur l'iADRS et le CDR-SB n'a pas été obeservée (voir la rubrique "Mises en garde et précautions" et la rubrique "Effets indésirables" ).
Efficacité clinique
La sécurité et l'efficacité du donanemab ont été évaluées dans le cadre d'une étude de phase 3 (TRAILBLAZER-ALZ 2). L'étude a été menée en double aveugle, contrôlée par placebo et en groupes parallèles. Elle a été réalisée auprès de patients âgés de 60 à 85 ans atteints de maladie d'Alzheimer symptomatique débutante (trouble cognitif léger, Mild Cognitive Impairment, MCI) ou de démence légère due à une maladie d'Alzheimer et ayant un score MMSE de 20 à 28 inclus. Les patients devaient présenter des signes de pathologie bêta-amyloïde confirmés par PET à l'amyloïde. Les patients présentaient en outre des signes de dépôt pathologique de Tau sur le PET au flortaucipir.
À l'appui des résultats de cette étude, il y a des données d'une étude de phase 2 (TRAILBLAZER-ALZ) de conception comparable. Les posologies utilisées dans cette étude se distinguent de la posologie enregistrée (voir la rubrique "Pharmacocinétique" ).
Pour évaluer la sécurité, les patients ont été observés pendant une période allant jusqu'à 76 semaines ou jusqu'à la fin du traitement plus 57 jours après la dernière dose.
TRAILBLAZER-ALZ 2 a été conçue à l'origine comme une étude de phase 2 et elle a été modifiée plus tard en étude de phase 3. Les principales modifications ont été: ajout d'une phase de titration avec 700 mg pour les trois premières utilisations; adaptation de l'étude de phase 2 en une étude de phase 3, notamment avec une augmentation de la taille de l'échantillon et une modification de l'analyse principale de "CDR-SB dans la population totale ou dans la population avec Tau intermédiaire" en "iADRS dans la population avec Tau intermédiaire" ; ajout d'une phase d'extension à long terme, pour évaluer l'efficacité et la sécurité du donanemab au cours du temps.
Étude de phase 3 TRAILBLAZER-ALZ 2
Dans cette étude, 1736 patients ont été randomisés selon un rapport de 1:1 pour recevoir une perfusion intraveineuse de 700 mg de donanemab toutes les 4 semaines pour les 3 premières utilisations, puis 1400 mg toutes les 4 semaines (N=860) ou de placebo (N=876), pour une durée totale allant jusqu'à 72 semaines. L'étude incluait une phase d'extension en double aveugle sur 78 semaines. L'utilisation a été poursuivie jusqu'à la fin de l'étude ou jusqu'à la dissolution (clairance) des plaques amyloïdes, définie comme une concentration en plaques inférieure à 25 centiloïdes lors de deux PET à l'amyloïde consécutifs ou lorsqu'un seul PET mesurait une concentration en plaques inférieure à 11 centiloïdes.
De plus, la suspension du traitement était autorisée en cas d'ARIA du au traitement. Si les patients recevaient déjà un traitement symptomatique (inhibiteurs de l'acétylcholinestérase et/ou inhibiteurs du N-méthyle-D-aspartate, mémantine) lors de l'inclusion dans l'étude, ces traitements pouvaient être poursuivis. Les traitements symptomatiques pouvaient être complétés ou modifiés durant l'étude, à la discrétion du médecin investigateur. L'étude a exclu les patients présentant un ARIA-E préexistant avec plus de 4 microhémorragies, plus d'une zone de sidérose superficielle, toute hémorragie intracérébrale >1 cm ou une maladie sévère de la substance blanche. À l'inclusion, l'âge moyen était de 73 ans, avec une fourchette de 59 à 86 ans, pour un poids moyen (SD) initial de 71.7 kg (15.7), un changement graduel et progressif des fonctions mnésiques pendant au moins 6 mois et un score MMSE (Mini-Mental State Examination) de 22.29 (3.88). 57.4% des participants étaient des femmes, 91.5% des Caucasiens, 5.7% étaient d'origine ethnique hispanique ou latino-américaine, 6.0% d'origine asiatique et 2.3% étaient Afro-américains. 80.0% des patients ont été inclus en Amérique du Nord, 13.9% en Europe, 5.1% au Japon et 1.0% en Australie. 29% étaient non-porteurs de l'ApoE ε4, 54% hétérozygotes et 17% homozygotes.
55.6% des patients étaient sous AChEI, 20.3% sous mémantine. 61% des patients recevaient soit un AChEI soit de la mémantine.
La moyenne (mean, SD) de l'amyloïde en à l'inclusion était de 102.5 (34.5) centiloïdes.
Deux populations d'analyse principale ont été définies lors du screening par Tau-PET au flortaucipir: 1) Une population avec des concentrations faibles à modérées de Tau (68.2% du total), et 2) la population combinée avec soit une concentration faible à modérée, soit une concentration élevée de Tau (31.8% du total).
Dans l'ensemble, 24.7% des patients ont arrêté prématurément le traitement (29.3% sous donanemab, 20.1% sous placebo).
Le critère d'efficacité principal était le changement de la cognition et de la fonction mesuré avec le score iADRS (integrated Alzheimer's Disease Rating Scale) entre l'inclusion et la semaine 76. L'iADRS est un examen combiné de la cognition et des fonctions du quotidien incluant des items du sous-score de l'Alzheimer's Disease Assessment Scale (ADAS-Cog13, nombre de points 0-85) et de l'Alzheimer's Disease Cooperative Study - instrumental Activities of Daily Living (ADCS-iADL, nombre de points 0-59), qui mesurent des domaines-clés de l'évolution de la maladie d'Alzheimer. Le score total varie de 0 à 144, les scores les plus bas indiquant des performances cognitives et fonctionnelles plus faibles. Les autres critères d'évaluation de l'efficacité comprenaient le CDR-SB (Clinical Dementia Rating Scale - Sum of Boxes), l'ADAS-Cog13 et l'ADCS-iADL.
La Table 3 ci-dessous présente les résultats importants de l'étude pour la population indiquée.
Dans la population indiquée, 717 participants ont été randomisés pour recevoir du donanemab, 414 étaient de sexe féminin et 303 de sexe masculin, 70 avaient <65 ans, 320 avaient de 65 à 74 ans et 327 avaient 75 ans ou plus.
Dans la population indiquée, 730 participants ont été randomisés pour recevoir du placebo, 426 étaient de sexe féminin et 304 de sexe masculin, 66 avaient <65 ans, 311 avaient de 65 à 74 ans et 353 avaient 75 ans ou plus.
Table 3: Résultats de l'analyse d'efficacité à la semaine 76 de l'étude TRAILBLAZER-ALZ 2 sur le donanemab dans la population indiquée (hétérozygotes et non-porteurs de l'ApoE ε4)
Critère clinique Porteurs hétérozygotes del'ApoE ε4 et
non-porteurs de l'ApoE ε4
Dona Placebo
iADRS (NCS)
Moyenne à l'inclusion (SD) 104.66 (14.12) 103.83 (14.03)
Changement (LS mean) par rapport à -10.21 (0.57) -13.59 (0.55)
l'inclusion
Différence par rapport au placebo 3,38 [1,83, 4,92]
[IC à 95 %]
Femmes
Moyenne à l'inclusion (SD) 104.92 (14.02) 103.75 (13.38)
Changement (LS mean) par rapport à -10.98 (0.76) -14.77 (0.72)
l'inclusion
Différence par rapport au placebo 3,80 [1,77, 5,83]
[IC à 95 %]
Hommes
Moyenne à l'inclusion (SD) 104.32 (14.26) 103.95 (14.87)
Changement (LS mean) par rapport à -9.18 (0.87) -11.92 (0.85)
l'inclusion
Différence par rapport au placebo 2,73 [0,36, 5,10]
[IC à 95 %]
<65 ans
Moyenne à l'inclusion (SD) 105.19 (15.46) 107.14 (14.19)
Changement (LS mean) par rapport à -12.74 (1.77) -14.21 (1.86)
l'inclusion
Différence par rapport au placebo 1,47 [-3,51, 6,45]
[IC à 95 %]
65 à 74 ans
Moyenne à l'inclusion (SD) 106.05 (12.88) 105.09 (13.59)
Changement (LS mean) par rapport à -9.33 (0.86) -13.69 (0.83)
l'inclusion
Différence par rapport au placebo 4,35 [2,03, 6,68]
[IC à 95 %]
>75 ans
Moyenne à l'inclusion (DS) 103.20 (14.83) 102.11 (14.19)
Changement (LS mean) par rapport à -10.48 (0.86) -13.37 (0.80)
l'inclusion
Différence par rapport au placebo 2,89 [0,61, 5,17]
[IC à 95 %]
CDR-SB (MMRM)
Moyenne à l'inclusion (SD) 3.96 (2.10) 3.94 (2.04)
Changement (LS mean) par rapport à 1.67 (0.11) 2.43 (0.10)
l'inclusion
Différence par rapport au placebo -0,77 [-1,04, -0,49]
[IC à 95 %]
Femmes
Moyenne à l'inclusion (DS) 4.03 (2.11) 3.97 (1.98)
Changement (LS mean) par rapport à 1.66 (0.12) 2.49 (0.15)
l'inclusion
Différence par rapport au placebo -0,83 [-1,20, -0,45]
[IC à 95 %]
Hommes
Moyenne à l'inclusion (SD) 3.87 (2.08) 3.89 (2.13)
Changement (LS mean) par rapport à 1.48 (0.15) 2.15 (0.14)
l'inclusion
Différence par rapport au placebo -0,66 [-1,07, -0,25]
[IC à 95 %]
<65 ans
Moyenne à l'inclusion (DS) 3.81 (2.05) 3.80 (1.54)
Changement (LS mean) par rapport à 2.53 (0.40) 2.81 (0.31)
l'inclusion
Différence par rapport au placebo -0,28 [-1,19, 0,63]
[IC à 95 %]
65 à 74 ans
Moyenne à l'inclusion (SD) 3.78 (1.88) 3.66 (1.92)
Changement (LS mean) par rapport à 1.46 (0.14) 2.55 (0.16)
l'inclusion
Différence par rapport au placebo -1,09 [-1,50, -0,68]
[IC à 95 %]
>75 ans
Moyenne à l'inclusion (DS) 4.17 (2.30) 4.21 (2.19)
Changement (LS mean) par rapport à 1.48 (0.15) 2.04 (0.16)
l'inclusion
Différence par rapport au placebo -0,56 [-0,96, -0,16]
[IC à 95 %]
ADAS-Cog13 (NCS)
Moyenne à l'inclusion (SD) 28.43 (8.91) 29.00 (8.93)
Changement (LS mean) par rapport à 5.37 (0.31) 7.06 (0.29)
l'inclusion
Différence par rapport au placebo -1,69 [-2,52, -0,86]
[IC à 95 %]
Femmes
Moyenne à l'inclusion (SD) 28.40 (9.15) 29.45 (8.61)
Changement (LS mean) par rapport à 5.59 (0.40) 7.20 (0.39)
l'inclusion
Différence par rapport au placebo -1,61 [-2,71, -0,52]
[IC à 95 %]
Hommes
Moyenne à l'inclusion (SD) 28.46 (8.60) 28.40 (9.32)
Changement (LS mean) par rapport à 5.09 (0.47) 6.88 (0.45)
l'inclusion
Différence par rapport au placebo -1,79 [-3,07, -0,52]
[IC à 95 %]
<65 ans
Moyenne à l'inclusion (SD) 27.82 (9.67) 27.11 (9.40)
Changement (LS mean) par rapport à 8.34 (0.94) 7.90 (0.96)
l'inclusion
Différence par rapport au placebo 0,44 [-2,19, 3,06]
[IC à 95 %]
65 à 74 ans
Moyenne à l'inclusion (SD) 27.82 (8.80) 28.74 (9.39)
Changement (LS mean) par rapport à 4.86 (0.45) 7.51 (0.44)
l'inclusion
Différence par rapport au placebo -2,66 [-3,89, -1,42]
[IC à 95 %]
> 75 ans
Moyenne à l'inclusion (SD) 29.16 (8.83) 29.59 (8.36)
Changement (LS mean) par rapport à 5.21 (0.46) 6.47 (0.43)
l'inclusion
Différence par rapport au placebo -1,26 [-2,49, -0,04]
[IC à 95 %]
Abréviations: ApoE-ε4 = allèle de sous-type 4 du gène qui code pour l'apolipoprotéine de classe E; CDR-SB = Clinical Dementia Rating Scale – Sum of boxes; IC = intervalle de confiance; Dona = donanemab; iADRS = integrated Alzheimers Disease Rating Scale; LSM = Least-Square mean, moyenne selon la méthode des moindres carrés; MMRM = Mixed Model for Repeated Measures, modèle mixte pour mesures répétées; SD = standard deviation.
Biomarqueurs
Le pourcentage de patients sous donanemab présentant une clairance amyloïde (c.-à-d. avec un PET à l'amyloïde au-dessous de 24.1 centiloïdes ou avec une lecture visuelle négative) dans l'étude TRAILBLAZER-ALZ 2 est présenté dans la Figure 2.
Sous donanemab, une réduction de la concentration plasmatique de P-tau217 (Log 10) a été observée par rapport au placebo. Dans la population avec une concentration faible à modérée de Tau (498 patients sous donanemab vs. 494 patients sous placebo), la variation moyenne (LS mean ± SE) était de -0.19 ± 0.012 et de -0.26 ± 0.015 aux semaines 24 et 76 par rapport au placebo (p<0.0001 pour les deux points temporels). En accord avec ces données, la population combinée présentait une variation moyenne (Log LS mean ± SE) de -0.17± 0.011 et -0.23± 0.013 aux semaines 24 et 76 par rapport au placebo (p<0.0001 pour les deux points temporels).
Figure 2. Pourcentage de patients dans la population indiquée sous donanemab ayant atteint une clairance des plaques amyloïdes mesurée par PET à l'amyloïde sur une période de 76 semaines dans l'étude TRAILBLAZER-ALZ 2.
Population avec une concentration élevée de Tau dans la population indiquée
Dans la population avec une concentration élevée de Tau (218 patients sous donanemab et 235 patients sous placebo), le donanemab a ralenti de 8% (1.55 ± 1.66 [p=0.351) le déclin clinique mesuré avec l'iADRS et de 18% (-0.60 ± 0.28 [p=0.032]) avec le CDR-SB à la semaine 76 par rapport au placebo.
Étude de phase 3 TRAILBLAZER-ALZ-6
La posologie de 350/700/1050 mg de donanemab puis 1400 mg toutes les 4 semaines a été étudiée dans une étude multicentrique randomisée, en double aveugle de phase IIIb, menée chez des adultes atteints de maladie d'Alzheimer symptomatique débutante (MCI dû à une maladie d'Alzheimer ou démence légère due à la maladie d'Alzheimer, score MMSE de 20 à 28 inclus) et présentant des signes de pathologie bêta-amyloïde confirmée par PET à l'amyloïde.
843 patients ont été randomisés dans un rapport de 1:1:1:1 et ont reçu quatre posologies différentes sur un total de 72 semaines, à savoir 700 mg lors des trois premières perfusions, puis 1400 mg toutes les 4 semaines (n=207), ou l'une des trois posologies alternatives (y compris la posologie de 350/700/1050 mg, puis de 1400 mg toutes les 4 semaines; n=212), la même quantité totale de médicament étant finalement utilisée dans tous les schémas.
Le critère principal de l'étude a été le pourcentage de participants avec toute apparition d'ARIA-E jusqu'à la semaine 24. Les résultats ont montré qu'un ARIA-E est apparu chez 14% des patients ayant reçu 350/700/1050 mg puis 1400 mg toutes les 4 semaines jusqu'à la semaine 24, par rapport à 24% des patients ayant reçu 700/700/700 mg puis 1400 mg toutes les 4 semaines, ce qui correspond à un risque relatif réduit de 41%. La diminution des plaques amyloïdes observée à la semaine 24 était similaire quelle que soit la posologie.
|

