CompositionPrincipes actifs
ADAMTS13r*
Excipients
Chlorure de sodium (correspondant à 3,7 mg de sodium), chlorure de calcium dihydraté, L-histidine, mannitol, saccharose, polysorbate 80 2,7 mg (E 433), eau pour préparations injectables
Forme pharmaceutique et quantité de principe actif par unitéPoudre et solvant pour solution injectable.
ADZYNMA 500 UI poudre et solvant pour solution injectable
Chaque flacon de poudre contient nominalement 500 unités internationales (UI) d'activité d'ADAMTS13r*, mesuré en termes de puissance.
Après reconstitution avec les 5 ml de solvant fournis, la solution a une activité d'environ 100 UI/ml.
ADZYNMA 1 500 UI poudre et solvant pour solution injectable
Chaque flacon de poudre contient nominalement 1 500 UI d'activité d'ADAMTS13r*, mesuré en termes de puissance.
Après reconstitution avec les 5 ml de solvant fournis, la solution a une activité d'environ 300 UI/ml. Poudre lyophilisée blanche.
Le solvant est une solution limpide et incolore.
La solution reconstituée a un pH de 6,7 - 7,3 et une osmolalité qui est d'au moins 240 mOsmol/kg. *ADZYNMA est une protéine recombinante humaine bivariante purifiée "A Disintegrin and Metalloproteinase with Thrombospondin Motifs 13“-Protein" (ADAMTS13r) (Une désintégrine et une métalloprotéinase avec des motifs de thrombospondine 13) exprimée dans des cellules d'Ovaire de Hamster Chinois (CHO) à l'aide de la technologie de l'ADN recombinant (un mélange de ADAMTS13r Q23 natif et de variant ADAMTS13r R23 avec une gamme contrôlée de rapport à deux variantes), appelée ADAMTS13r.
Indications/Possibilités d’emploiADZYNMA est indiqué dans le traitement enzymatique substitutif (TES) chez les patients adultes et enfants atteints de purpura thrombotique thrombocytopénique congénital (PTTc) dû à un déficit en ADAMTS13.
ADZYNMA peut être utilisé dans tous les groupes d'âge.
Posologie/Mode d’emploiLe traitement par ADZYNMA doit être instauré sous la supervision d'un médecin expérimenté dans la prise en charge des patients atteints de troubles hématologiques.
Posologie
Traitement enzymatique substitutif prophylactique
-40 UI/kg de poids corporel une fois toutes les deux semaines.
-La fréquence d'administration de la prophylaxie peut être ajustée à 40 UI/kg de poids corporel une fois par semaine en fonction de la réponse clinique (voir "Propriétés/Effets" et "Pharmacocinétique" ).
Traitement enzymatique substitutif à la demande en cas d'épisode aigu de PTT
En cas d'épisode aigu de purpura thrombotique thrombocytopénique (PTT), la posologie recommandée d'ADZYNMA pour traiter les épisodes aigus de PTT est la suivante:
-40 UI/kg de poids corporel le jour 1.
-20 UI/kg de poids corporel le jour 2.
-15 UI/kg de poids corporel à partir du jour 3, une fois par jour, jusqu'à deux jours après la résolution de l'épisode aigu (voir "Propriétés/Effets" ).
Populations particulières
Personnes âgées
Les données sur l'utilisation d'ADZYNMA chez les patients de plus de 65 ans sont limitées. Sur la base des résultats de l'analyse pharmacocinétique de population, aucun ajustement posologique n'est nécessaire chez les patients âgés (voir "Pharmacocinétique" ).
Troubles de la fonction rénale
L'ADAMTS13r étant une protéine recombinante à haut poids moléculaire, elle n'est pas excrétée par voie rénale et aucun ajustement posologique n'est nécessaire chez les patients présentant un trouble de la fonction rénale (voir "Pharmacocinétique" ).
Troubles de la fonction hépatique
L'ADAMTS13r étant une protéine recombinante de haut poids moléculaire, elle est éliminée par catabolisme (plutôt que par métabolisme hépatique) et aucun ajustement posologique n'est nécessaire chez les patients présentant un trouble de la fonction hépatique (voir "Pharmacocinétique" ).
Population pédiatrique
Le schéma posologique recommandé en fonction du poids corporel chez les patients pédiatriques est le même que chez les adultes.
Sur la base des résultats de l'analyse pharmacocinétique de population, il pourrait être plus probable que les enfants pesant moins de 10 kg nécessitent un ajustement de la fréquence d'administration d'une semaine sur deux à une dose hebdomadaire (voir "Pharmacocinétique" ).
Mode d'administration
À utiliser par voie intraveineuse après reconstitution uniquement.
ADZYNMA 500 UI et ADZYNMA 1 500 UI poudre et solvant pour solution injectable sont administrés à une vitesse de 2 à 4 ml par minute.
Administration à domicile ou auto-administration
L'administration à domicile ou l'auto-administration sous la supervision d'un professionnel de santé peut être envisagée pour les patients qui tolèrent bien leurs injections. La décision de faire passer un patient à l'administration à domicile ou à l'auto-administration doit être prise après évaluation et recommandation du médecin prescripteur. Le médecin prescripteur et/ou l'infirmier/ère doivent dispenser une formation appropriée au patient et/ou à l'aidant avant de commencer l'administration à domicile ou l'auto-administration. La dose et le débit d'administration doivent rester constants à domicile et ne pas être modifiés sans avis du médecin prescripteur. Si le patient présente des signes précoces d'hypersensibilité pendant l'administration à domicile, le processus d'administration doit être arrêté immédiatement et un traitement approprié doit être instauré (voir "Mises en garde et précautions" ). Les injections suivantes doivent être effectuées dans un établissement clinique. Le traitement doit être étroitement surveillé par le médecin prescripteur.
Pour les instructions concernant la reconstitution du médicament avant administration, voir "Remarques particulières" .
Contre-indicationsHypersensibilité à la substance active ou à l'un des excipients mentionnés à "Composition" pouvant mettre en jeu le pronostic vital.
Mises en garde et précautionsTraçabilité
Afin d'améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés.
Réactions d'hypersensibilité
Une hypersensibilité de type allergique, incluant des réactions anaphylactiques, peut survenir. Les patients doivent être informés des signes précoces de réactions d'hypersensibilité, notamment tachycardie, oppression thoracique, respiration sifflante et/ou détresse respiratoire aiguë, hypotension, urticaire généralisée, prurit, rhino-conjonctivite, oedème de Quincke, léthargie, nausées, vomissements, paresthésie, agitation, qui peuvent évoluer vers un choc anaphylactique. En cas de signes et symptômes de réactions allergiques graves, l'administration de ce médicament doit être immédiatement interrompue et des soins de support appropriés doivent être prodigués au patient.
Immunogénicité
Comme pour toutes les protéines thérapeutiques, il existe un risque d'immunogénicité. Les patients peuvent développer des anticorps dirigés contre l'ADAMTS13r après un traitement par ADZYNMA, ce qui pourrait entraîner une diminution de la réponse à l'ADAMTS13r (voir "Propriétés/Effets" ). Si la présence de tels anticorps est soupçonnée et qu'un manque d'efficacité est constaté, il convient d'envisager d'autres stratégies thérapeutiques.
Excipients
Ce médicament contient moins de 1 mmol (23 mg) de sodium par flacon, c.-à-d. qu'il est essentiellement "sans sodium" .
Ce médicament contient 2,7 mg de polysorbate 80 par flacon, correspondant à une quantité maximale de 0,216 mg/kg de poids corporel à une dose de 40 UI d'ADZYNMA. Les polysorbates peuvent provoquer des réactions allergiques.
InteractionsAucune étude d'interaction n'a été réalisée.
Grossesse, allaitementGrossesse
Il n'existe pas de données ou il existe des données limitées sur l'utilisation d'ADZYNMA chez la femme enceinte. Les études effectuées chez l'animal n'ont pas mis en évidence d'effets délétères directs ou indirects sur la reproduction (voir "Données précliniques" ). L'utilisation d'ADZYNMA pendant la grossesse ne peut être envisagée qu'après une analyse individuelle approfondie des risques et des bénéfices par le médecin prescripteur avant et pendant le traitement.
Allaitement
Il n'existe pas de données suffisantes sur l'excrétion de l'ADAMTS13r dans le lait maternel ou animal, mais au vu de son poids moléculaire élevé (172 kDa), il est peu probable qu'elle soit excrétée dans le lait maternel. La décision d'interrompre l'allaitement ou d'arrêter ADZYNMA doit s'appuyer sur l'importance du médicament pour la mère.
Fertilité
On ne dispose d'aucune donnée humaine sur les effets de l'ADAMTS13r sur la fertilité masculine et féminine. Les données animales n'indiquent pas d'effets délétères directs ou indirects sur la fertilité des mâles et des femelles (voir "Données précliniques" ).
Effet sur l’aptitude à la conduite et l’utilisation de machinesL'ADAMTS13r peut avoir une légère influence sur l'aptitude à conduire des véhicules et à utiliser des machines. Une sensation vertigineuse et une somnolence peuvent survenir suite à l'administration d'ADZYNMA (voir "Effets indésirables" ).
Effets indésirablesRésumé du profil de sécurité
Les effets indésirables les plus fréquents rapportés dans les études cliniques étaient les céphalées (31,5 %), la diarrhée (17,8 %), la sensation vertigineuse (16,4 %), l'infection des voies aériennes supérieures (15,1 %), la nausée (13,7 %) et la migraine (11 %).
Tableau résumant les effets indésirables
Les effets indésirables (EI) sont énumérés dans le tableau 1.
Les effets indésirables sont répertoriés par classe de systèmes d'organes MedDRA et par fréquence. Les fréquences sont définies comme suit: très fréquent (≥1/10); fréquent (≥1/100, < 1/10); occasionnel (≥1/1 000, < 1/100); rare (≥1/10 000, < 1/1 000); très rare (< 1/10 000); fréquence inconnue (ne peut être estimée sur la base des données disponibles). Au sein de chaque classe de systèmes d'organes, les effets indésirables sont présentés par ordre décroissant de fréquence. Au sein de chaque groupe de fréquence, les EI sont présentés par ordre décroissant de gravité.
Tableau 1 : Effets indésirables rapportés chez les patients traités par ADZYNMA
Classe de systèmes d'organes MedDRA Effet indésirable par terme Catégorie de fréquence
préférentiel par participant
Infections et infestations Infection des voies aériennes Très fréquent
supérieures (15,1 %)
Affections hématologiques et du Thrombocytose Fréquent
système lymphatique
Affections du système nerveux Céphalée (31,5 %) Très fréquent
Sensation vertigineuse (16,4 %) Très fréquent
Migraine (11 %) Très fréquent
Somnolence Fréquent
Affections gastro-intestinales Diarrhée (17,8 %) Très fréquent
Nausée (13,7 %) Très fréquent
Constipation Fréquent
Distension abdominale Fréquent
Troubles généraux et anomalies au Asthénie Fréquent
site d'administration
Sensation de chaud Fréquent
Investigations Activité ADAMTS13 anormale Fréquent
Population pédiatrique
Il existe peu d'informations issues d'études contrôlées sur ADZYNMA chez les patients pédiatriques. L'évaluation de la sécurité chez les patients pédiatriques repose sur les données de sécurité d'une étude clinique de phase 3 comparant ADZYNMA à des plasmathérapies (plasma frais congelé [PFC], plasma traité par solvant/détergent [S/D] ou concentrés de facteur VIII:facteur de von Willebrand [FVIII:FVW], selon l'assignation de l'investigateur) et d'une étude de phase 3b. Ces études ont porté sur 21 patients pédiatriques âgés de 2 à 17 ans répartis dans 2 cohortes (20 recevant le traitement prophylactique et 1 le traitement à la demande). Dans l'ensemble, le profil de sécurité chez ces patients pédiatriques était similaire à celui observé dans la population adulte.
Un nouveau-né âgé de 36 heures a été traité par ADZYNMA dans le cadre d'un programme d'usage compassionnel et n'a pas eu de problèmes de sécurité ou d'immunogénicité signalés après 2 ans de traitement prophylactique.
La fréquence, le type et la sévérité des effets indésirables chez les enfants devraient être les mêmes que chez les adultes.
Déclaration des effets indésirables suspectés
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageDans les études cliniques, des doses uniques allant jusqu'à 160 UI/kg ont été utilisées, et leur profil de sécurité était généralement cohérent avec les résultats des études cliniques chez les patients atteints de PTTc.
En cas de surdosage, compte tenu de l'action pharmacologique de l'ADAMTS13r, il existe un risque potentiel accru de saignement (voir "Propriétés/Effets" ).
Propriétés/EffetsCode ATC
B01AD13
Mécanisme d'action
L'ADAMTS13r est une forme recombinante de l'ADAMTS13 endogène. L'ADAMTS13 est une métalloprotéase à zinc plasmatique qui régule l'activité du facteur de von Willebrand (FVW) en clivant les multimères FVW de haut et de très haut poids moléculaire en unités plus petites et en réduisant ainsi les propriétés de liaison plaquettaire du FVW et sa capacité à former des microthrombi. L'ADAMTS13r devrait réduire ou éliminer la formation spontanée de microthrombi de plaquettes-FVW qui conduit à la consommation de plaquettes et à la thrombocytopénie chez les patients atteints de PTTc.
Immunogénicité
Des anticorps anti-médicaments (ADA) ont été très couramment détectés. Aucune preuve de l'impact des anticorps anti-médicaments sur la pharmacocinétique, l'efficacité ou la sécurité n'a été observée, mais les données restent limitées. Aucun anticorps neutralisant anti-rADAMTS13 n'a été détecté chez les patients atteints de PTTc (voir "Mises en garde et précautions" ).
Efficacité clinique
L'efficacité et la sécurité cliniques ont été évaluées dans deux études en cours (étude 281102 et étude 3002).
Étude 281102
ADZYNMA a fait l'objet d'une étude internationale de phase 3, prospective, randomisée, contrôlée, ouverte, multicentrique, croisée sur deux périodes (cross-over), suivie d'une période de continuation mono-bras (étude 281102) évaluant l'efficacité et la sécurité d'un TES prophylactique et à la demande avec ADZYNMA par rapport aux plasmathérapies chez les patients atteints de PTTc sévère.
Traitement prophylactique enzymatique substitutif chez les patients atteints de PTTc
L'efficacité d'ADZYNMA dans le traitement prophylactique des patients atteints de PTTc a été évaluée chez 45 patients de la cohorte prophylactique qui ont été randomisés pour recevoir 6 mois de traitement prophylactique avec soit 40 UI/kg (±4 UI/kg) d'ADZYNMA, soit des plasmathérapies (période 1) une fois par semaine (pour les patients qui étaient traités avec des plasmathérapies une fois par semaine avant de rejoindre l'étude) ou toutes les deux semaines, puis sont passés à l'autre traitement pendant 6 mois (période 2). Après les périodes 1 et 2, tous les patients sont entrés dans une période de traitement de 6 mois à bras unique avec ADZYNMA (période 3). La fréquence initiale d'administration du traitement prophylactique avec ADZYNMA était la suivante: une semaine sur deux pour 34 (75,6 %) patients et une fois par semaine pour 9 (20,0 %) patients.
L'âge moyen (écart-type) était de 30,4 (16,2) ans (intervalle: 3 à 58 ans). Sur les 45 patients, 4 (8,9 %) étaient âgés de moins de 6 ans, 4 (8,9 %) étaient âgés de ≥6 à < 12 ans, 4 (8,9 %) étaient âgés de ≥12 à < 18 ans, et 33 (73,3 %) étaient âgés de ≥18 ans. Le poids moyen (écart-type) était de 65,5 kg (21,8) (intervalle: 18,5 à 102,4 kg), et la majorité des patients étaient blancs (64,4 %) et étaient des femmes (57,8 %), dont 73,1 % étaient en âge de procréer.
Avant de rejoindre l'étude, la majorité (68,9 %) des patients ont reçu un traitement par PFC, 24,4 % ont reçu du plasma au solvant-détergent (S/D) et 6,7 % ont reçu du concentré de FVIII-FVW.
L'efficacité du traitement prophylactique avec ADZYNMA chez les patients atteints de PTTc a été évaluée sur la base de l'incidence des épisodes aigus de PTT (définis par une baisse de la numération plaquettaire [≥50 % par rapport à la valeur initiale ou une numération plaquettaire < 100 x 109/l] et une élévation de la lactate déshydrogénase [LDH] [> 2 fois la valeur initiale ou > 2 fois la limite supérieure de la normale (LSN)]), des épisodes subaigus de PTT (définis par un événement de thrombocytopénie ou d'anémie hémolytique microangiopathique, des signes et symptômes spécifiques aux organes, notamment des événements de dysfonctionnement rénal, de symptômes neurologiques, de fièvre, de fatigue/léthargie et/ou de douleurs abdominales) et des manifestations de PTT (comme une thrombocytopénie, une anémie hémolytique microangiopathique, des symptômes neurologiques, un dysfonctionnement rénal et des douleurs abdominales); ainsi que l'incidence de doses supplémentaires administrées en raison d'épisodes subaigus de PTT (voir tableau 2).
Tableau 2 : Résultats de la cohorte sur l'efficacité prophylactique chez les patients atteints de PTTc (périodes 1 et 2)
ADZYNMA N = 44 Plasmathérapies N =
45
Épisodes aigus de PTT
Nombre de patients avec épisode (nombre d'épisodes) 0 (0) 1 (1)
Épisodes subaigus de PTT
Nombre de patients avec épisode (nombre d'épisodes) 1 (1) 6 (7)
Nombre de patients ayant reçu une dose supplémentaire 0 4
en raison d'un épisode subaigu
Nombre de doses supplémentaires administrées en raison 0 9
d'un épisode subaigu
Manifestations de PTT
Événements de thrombocytopéniea
Nombre de patients avec évènement (nombre d'événements) 13 (50) 21 (89)
Taux d'événements annualisé basé sur un modèleb, MMC 0,91 (0,268) 1,62 (0,453)
(ES)
Événements d'anémie hémolytique microangiopathiquec
Nombre de patients avec évènement (nombre d'événements) 8 (23) 12 (31)
Taux d'événements annualisé basé sur un modèleb, MMC 0,38 (0,139) 0,59 (0,195)
(ES)
Événements de symptômes neurologiquesd
Nombre de patients avec évènement (nombre d'événements) 4 (18) 7 (28)
Taux d'événements annualisé basé sur un modèleb, MMC 0,14 (0,072) 0,23 (0,111)
(ES)
Événements de dysfonctionnement rénale
Nombre de patients avec évènement (nombre d'événements) 5 (11) 2 (5)
Taux d'événements annualisé basé sur un modèleb, MMC 0,18 (0,093) 0,08 (0,054)
(ES)
Événements de douleurs abdominales
Nombre de patients avec évènement (nombre d'événements) 2 (4) 6 (8)
Taux d'événements annualisé basé sur un modèleb, MMC 0,09 (0,056) 0,17 (0,088)
(ES)
MMC = moyenne des moindres carrés; ES = erreur standard; PTT = purpura thrombotique thrombocytopénique.
a Baisse de la numération plaquettaire ≥25 % par rapport à la valeur initiale ou numération plaquettaire < 150 x 109/l.
b D'après un modèle binominal négatif à effets mixtes.
c Élévation du taux de LDH > 1,5 fois la valeur initiale ou > 1,5 fois la LSN.
d Affections du système nerveux liés au PTT (p.ex. céphalée, confusion mentale, troubles de la mémoire, irritabilité, paresthésie, dysarthrie, dysphonie, troubles visuels, symptômes moteurs focaux ou généraux dont convulsions).
e Augmentation de la créatinine sérique > 1,5 fois la valeur initiale.
Les résultats globaux de l'efficacité d'ADZYNMA ont été cohérents tout au long de l'étude, y compris pendant la période 3 et dans tous les groupes d'âge.
Traitement enzymatique substitutif à la demande en cas d'épisode aigu de PTT
L'efficacité du traitement enzymatique substitutif à la demande en cas d'épisode aigu de PTT a été évaluée sur la base de la proportion d'épisodes aigus de PTT répondant à ADZYNMA dans les cohortes prophylactiques et à la demande pendant toute la durée de l'étude.
Un épisode aigu de PTT répondant à ADZYNMA a été défini comme un épisode de PTT résolu lorsque la numération plaquettaire était ≥150 x 109/l ou que la numération plaquettaire était inférieure à 25 % par rapport à la valeur initiale, selon la première éventualité, et que le taux de LDH était ≤1,5 fois la valeur initiale ou ≤1,5 fois la LSN, sans nécessiter l'utilisation d'un autre agent contenant de l'ADAMTS13.
La cohorte à la demande comprenait 5 patients adultes (≥18 ans) et 1 patient pédiatrique (< 6 ans). Les patients qui faisaient partie de cette cohorte ont présenté un total de 7 épisodes aigus de PTT. Sur ces 6 patients, 2 ont été randomisés pour recevoir un traitement à la demande avec ADZYNMA et 4 ont été randomisés pour recevoir des plasmathérapies. Six sur sept épisodes aigus de PTT ont disparu dans les 5 jours après un traitement par ADZYNMA ou par des plasmathérapies, tandis qu'un épisode s'est résolu 14,75 jours après le traitement par une plasmathérapie.
La plupart des patients (66,7 %) étaient des hommes, blancs (50 %), avec un âge médian (min, max) de 20 (5, 36) ans, un poids moyen (ET) de 56,4 (18,6) kg et un poids médian (min, max) de 64,3 (23,0, 74,0) kg.
Étude 3002 (étude de continuation)
Les patients qui ont terminé l'étude de phase 3 (étude 281102) étaient éligibles pour participer à une étude de continuation à long terme (étude 3002). La cohorte prophylactique contenait 65 patients, dont 40 provenaient de l'étude 281102 et 25 étaient des patients naïfs de tout traitement. Parmi les 40 patients provenant de l'étude, 7 (17,5 %) étaient âgés de ≥12 à < 18 ans, et 33 (82,5 %) étaient âgés de ≥18 ans. Sur les 25 patients naïfs de tout traitement, 3 (12 %) étaient âgés de moins de 6 ans, 3 (12 %) étaient âgés de ≥6 à < 12 ans, 3 (12 %) étaient âgés de ≥12 à < 18 ans, et 16 (64 %) étaient âgés de ≥18 ans. La cohorte à la demande contenait 1 patient âgé de ≥6 à < 12 ans. Tous les patients ont été traités avec ADZYNMA. La durée moyenne et la durée maximale du traitement prophylactique ont été respectivement de 0,98 an et de 2,17 ans. Les taux d'incidence des épisodes aigus et subaigus de PPT et des manifestations de PPT étaient cohérents avec les résultats de l'étude 281102.
Population pédiatrique
Dans l'ensemble, l'efficacité chez les patients pédiatriques était similaire à celle observée dans la population adulte.
PharmacocinétiqueAbsorption
Le profil pharmacocinétique d'ADZYNMA a été déterminé sur la base des données d'activité d'ADAMTS13 analysée lors des études cliniques.
Après l'administration intraveineuse d'une dose unique d'ADZYNMA à raison de 5 UI/kg, 20 UI/kg et 40 UI/kg à des adultes et des adolescents, des augmentations liées à la dose de l'activité d'ADAMTS13 individuelle ont été observées et ont atteint un maximum environ 1 heure après l'administration ou plus tôt. À la dose clinique de 40 UI/kg, la demi-vie moyenne (ET) et le temps de résidence moyen (TRM) chez les adultes et les adolescents étaient respectivement de 47,8 (13,7) heures et 63,8 (16,0) heures.
Les paramètres pharmacocinétiques de population de l'activité d'ADAMTS13, après l'administration IV d'ADZYNMA à raison de 40 UI/kg chez les adultes, les adolescents et les jeunes enfants sont décrits dans le tableau 3.
Tableau 3 : Paramètres pharmacocinétiques de l'activité d'ADAMTS13 après l'administration IV d'ADZYNMA chez les patients atteints de PTTc
Paramètre(unité) Moyenne (ET)Min; Max (N = 83)
Cmax (UI/ml) 1,13 (0,29) 0,72; 2,29
AUC (UI*h/ml) 72,8 (37,4) 38,7; 274
Durée d'activité d'ADAMTS13 supérieure à 10 % (jours) 8,85 (2,45) 4,51; 14,0
AUC = aire sous la courbe activité d'ADAMTS13-temps; Cmax = activité maximale ADAMTS13.
Remarque: 1 UI/ml d'activité d'ADAMTS13 correspond à une activité normale moyenne de 100 %.
L'administration intraveineuse d'ADZYNMA à raison de 40 UI/kg a entraîné une augmentation approximative de plus de 5 fois des expositions à l'activité d'ADAMTS13 (Cmax, AUC et durée supérieure à 10 % d'activité d'ADAMTS13) et une variabilité plus faible par rapport aux plasmathérapies.
Cinétique pour certains groupes de patients
Âge, sexe, groupe ethnique et autres facteurs intrinsèques
Outre le schéma posologique basé sur le poids corporel, aucun facteur intrinsèque tel que l'âge, le sexe, le groupe ethnique, le débit de filtration glomérulaire estimé (DFGe) à l'inclusion et la bilirubine initiale n'a été identifié comme covariable ayant une incidence sur la pharmacocinétique de l'ADAMTS13.
Les caractéristiques pharmacocinétiques de l'activité d'ADAMTS13 (TRM, volume de distribution à l'état d'équilibre [Vss] et clairance [CL]) étaient comparables dans tous les groupes d'âge chez les patients atteints de PTTc. La posologie d'ADZYNMA basée sur le poids corporel fournit des paramètres pharmacocinétiques de l'activité d'ADAMTS13 comparables (Cmax et activité d'ADAMTS13 moyenne [Cmoy]) dans les différents groupes d'âge, y compris les patients pédiatriques âgés de < 12 ans.
Chez les nourrissons de < 10 kg de poids corporel, la durée médiane au-dessus de 10 % de l'activité d'ADAMTS13 a été estimée plus courte (environ 5 à 6 jours) que chez les adultes (environ 10 jours).
Données précliniquesLes données précliniques issues des études conventionnelles sur la pharmacologie de sécurité, la toxicité en administration répétée, la toxicité sur les fonctions de reproduction et de développement, la tolérance locale et l'immunogénicité n'ont pas révélé de risque particulier pour l'homme.
Les données pharmacodynamiques/toxicologiques issues d'études animales ont montré que rADAMTS13 traverse le placenta et est présent dans le plasma fœtal à 0,6 % de la concentration maternelle. Cependant, aucun effet sur le développement des fœtus et des petits n'a été observé dans des études de développement embryo-fœtal ainsi que de développement pré- et postnatal chez le rat.
Aucune étude n'a été réalisée pour évaluer le potentiel mutagène et cancérogène de rADAMTS13.
Remarques particulièresIncompatibilités
En l'absence d'études de compatibilité, ce médicament ne doit pas être mélangé avec d'autres médicaments.
Stabilité
Flacon non ouvert
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention "EXP" sur l'emballage.
Après reconstitution
La préparation ne contient pas de conservateurs. La stabilité chimique et physique pendant l'utilisation a été démontrée pendant 6 heures à 25 °C. Pour des raisons microbiologiques, la préparation prête à l'emploi doit être utilisée immédiatement après ouverture.
Remarques particulières concernant le stockage
Poudre
À conserver au réfrigérateur (entre 2 °C et 8 °C).
Ne pas congeler.
À conserver dans l'emballage d'origine, à l'abri de la lumière.
Après reconstitution
Pour les conditions de conservation du médicament après reconstitution, voir "Stabilité" sous "Remarques particulières" .
Tenir hors de portée des enfants.
Remarques concernant la manipulation
ADZYNMA doit être administré par voie intraveineuse après reconstitution de la poudre avec l'eau pour préparations injectables fournie.
Instructions générales
-Calculer la dose et le volume d'administration en fonction du poids corporel du patient.
-Utiliser une technique aseptique tout au long de la procédure.
-Vérifier la date de péremption du produit avant de l'utiliser.
-Ne pas utiliser ADZYNMA si la date de péremption est dépassée.
-Si le patient a besoin de plus d'un flacon d'ADZYNMA par injection, reconstituer chaque flacon conformément aux instructions mentionnées dans la rubrique "Reconstitution" . Veuillez noter que le dispositif BAXJECT II Hi-Flow est destiné à être utilisé avec un seul flacon d'ADZYNMA et d'eau pour préparations injectables uniquement, par conséquent, la reconstitution et le prélèvement d'un deuxième flacon dans la seringue nécessitent un deuxième dispositif BAXJECT II Hi-Flow.
-La solution reconstituée doit être inspectée visuellement pour détecter la présence de particules et de décoloration avant l'administration. La solution d'ADZYNMA reconstituée doit être limpide et incolore.
-Ne pas administrer si des particules ou une décoloration sont observées.
-Administrer ADZYNMA dans les 3 heures suivant la reconstitution.
-Ne pas administrer ADZYNMA dans une tubulure déjà utilisée, dilué dans une poche de perfusion ou avec d'autres médicaments administrés en même temps.
Reconstitution
1. Préparer une surface plane et propre et rassembler tout le matériel dont vous aurez besoin pour la reconstitution et l'administration (Figure A).
Figure A
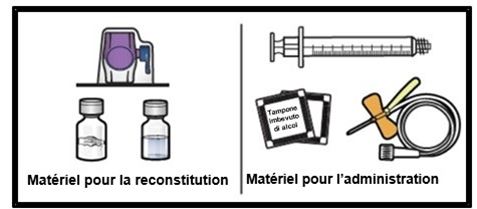
2. Laisser les flacons d'ADZYNMA et le solvant revenir à température ambiante avant utilisation.
3. Se laver les mains et les sécher soigneusement.
4. Retirer les bouchons en plastique des flacons d'ADZYNMA et de solvant et poser les flacons sur une surface plane (Figure B).
Figure B

5. Essuyer les bouchons en caoutchouc à l'aide d'un tampon d'alcool et les laisser sécher avant utilisation (Figure C).
Figure C

6. Ouvrir l'emballage du dispositif BAXJECT II Hi-Flow en retirant l'opercule, sans toucher l'intérieur (Figure D).
-Ne pas retirer le dispositif BAXJECT II Hi-Flow de l'emballage.
-Ne pas toucher la pointe en plastique transparent.
Figure D

7. Retourner l'emballage du dispositif BAXJECT II Hi-Flow et le placer au-dessus du flacon de solvant. Enfoncer bien droit jusqu'à ce que la pointe en plastique transparent perce le bouchon du flacon de solvant (Figure E).
Figure E
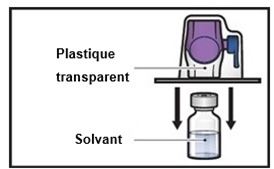
8. Saisir l'emballage du dispositif BAXJECT II Hi-Flow par ses rebords et retirer l'emballage du dispositif (Figure F).
-Ne pas retirer le capuchon bleu du dispositif BAXJECT II Hi-Flow.
-Ne pas toucher la pointe en plastique violet exposée.
Figure F

9. Retourner le système de façon à ce que le flacon de solvant soit sur le dessus. Appuyer sur le dispositif BAXJECT II Hi-Flow jusqu'à ce que la pointe en plastique violet perce le bouchon du flacon de poudre d'ADZYNMA (Figure G). Le vide aspirera le solvant dans le flacon de poudre d'ADZYNMA.
-Vous remarquerez peut-être des bulles ou de la mousse; ceci est normal et devrait disparaître rapidement.
Figure G
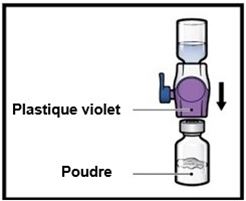
10. Agiter doucement et continuellement les flacons reliés jusqu'à ce que la poudre soit complètement dissoute (Figure H).
-Ne pas secouer le flacon.
Figure H

11. Inspecter visuellement la solution reconstituée pour détecter la présence de particules avant de l'administrer.
-Ne pas utiliser le produit si des particules ou une décoloration sont observées.
12. Si la dose nécessite plus d'un flacon d'ADZYNMA, reconstituer chaque flacon en suivant les étapes ci-dessus.
-Utiliser un dispositif BAXJECT II Hi-Flow différent pour reconstituer chaque flacon d'ADZYNMA et de solvant.
Instructions d'administration
13. Retirer le capuchon bleu du dispositif BAXJECT II Hi-Flow (Figure I). Fixer une seringue Luer-lock (Figure J).
-Ne pas injecter d'air dans le système.
Figure I Figure J
14 Retourner le système (le flacon d'ADZYNMA est maintenant au-dessus). Aspirer la solution reconstituée dans la seringue en tirant lentement sur le piston (Figure K).
Figure K
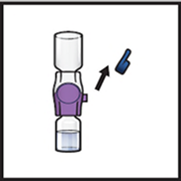
15. Si un patient doit recevoir plus d'un flacon d'ADZYNMA, le contenu de plusieurs flacons peut être prélevé dans la même seringue. Répéter ce processus pour tous les flacons reconstitués d'ADZYNMA jusqu'à ce que le volume total à administrer soit atteint.
16. Retirer la seringue et fixer une aiguille d'injection appropriée ou un set de perfusion.
17. Diriger l'aiguille vers le haut et éliminer les bulles d'air en tapotant doucement la seringue avec votre doigt et en poussant lentement et avec précaution l'air hors de la seringue et de l'aiguille.
18. Poser un garrot et nettoyer le site d'injection choisi à l'aide d'un tampon d'alcool (Figure L).
Figure L

19. Insérer l'aiguille dans la veine et retirer le garrot.
20. Administrer l'ADZYNMA reconstitué lentement, à raison de 2 à 4 ml par minute (Figure M).
-Un pousse-seringue peut être utilisé pour contrôler la vitesse d'administration.
Figure M

21. Retirer l'aiguille de la veine et exercer une pression sur le site d'injection pendant plusieurs minutes.
-Ne pas replacer le capuchon sur l'aiguille.
22. Placer l'aiguille, la seringue et les flacons vides dans un collecteur d'objets tranchants.
-Ne pas jeter les seringues et les aiguilles dans les ordures ménagères.
Numéro d’autorisation69562 (Swissmedic)
PrésentationADZYNMA 500 UI poudre et solvant pour solution injectable
Chaque boîte contient:
poudre dans un flacon (verre de type I), muni d'un bouchon en caoutchouc butyle
-5 ml de solvant dans un flacon (verre de type I), muni d'un bouchon en caoutchouc butyle
un dispositif de reconstitution (BAXJECT II Hi-Flow)
une seringue à usage unique de 10 ml
un set de perfusion 25G
deux tampons d'alcool
ADZYNMA 1 500 UI poudre et solvant pour solution injectable
Chaque boîte contient:
poudre dans un flacon (verre de type I), muni d'un bouchon en caoutchouc butyle
-5 ml de solvant dans un flacon (verre de type I), muni d'un bouchon en caoutchouc butyle
un dispositif de reconstitution (BAXJECT II Hi-Flow)
une seringue à usage unique de 20 ml
un set de perfusion 25G
deux tampons d'alcool
Titulaire de l’autorisationTakeda Pharma AG, 8152 Opfikon.
Mise à jour de l’informationOctobre 2025
|











