| ||||||||||||||||
|
| Home - FI zu Kerendia® |
| Fachinformation zu Kerendia®: | Bayer (Schweiz) AG |
Eigenschaften/WirkungenATC-Code Patienten mit
chronischer Nierener
krankung und Typ-2-D
iabetes
Finerenon* 10 oder Placebo* n = 2838 Behandlungseffekt
20 mg 1x täglich n Finerenon/Placebo
= 2824
Primäre und sekundär n (%) Ereignisrate (100 n (%) Ereignisrate (100 Hazard Ratio (95%-KI p-Wert
e Ereigniszeit-Endpu Pt.j.) Pt.j.) )
nkte:
Primärer kombinierte 498 (17.6 %) 7.53 600 (21.1 %) 9.09 0.82 [0.73; 0.92] 0.0009
r Endpunkt "Nierenve
rsagen, anhaltende
eGFR-Abnahme ≥40 %
oder nierenbedingter
Tod"
Nierenversagen 205 (7.3 %) 2.96 235 (8.3 %) 3.39 0.86 [0.72; 1.05] -
Anhaltende eGFR-Abna 473 (16.7 %) 7.15 577 (20.3 %) 8.74 0.81 [0.72; 0.91] -
hme ≥40 %
Nierenbedingter Tod 2 (< 0.1 %) - 2 (< 0.1 %) - - -
Sekundärer kombinier 366 (13.0 %) 5.11 420 (14.8 %) 5.93 0.86 [0.75; 0.99] 0.0344
ter Endpunkt "KV
Tod, nichttödlicher
MI, nichttödlicher
Schlaganfall oder
Hospitalisierung
wegen Herzinsuffizie
nz"
KV Tod 128 (4.5 %) 1.70 150 (5.3 %) 1.99 0.86 [0.68; 1.09] -
Nichttödlicher MI 70 (2.5 %) 0.94 87 (3.1 %) 1.18 0.80 [0.58; 1.09] -
Nichttödlicher 90 (3.2 %) 1.22 87 (3.1 %) 1.18 1.03 [0.77; 1.38] -
Schlaganfall
Hospitalisierung 138 (4.9 %) 1.88 162 (5.7 %) 2.22 0.85 [0.68; 1.07] -
wegen Herzinsuffizie
nz
* Behandlung zusätzl
ich zu maximal
verträglichen
zugelassenen Dosen
von ACEI oder ARB.
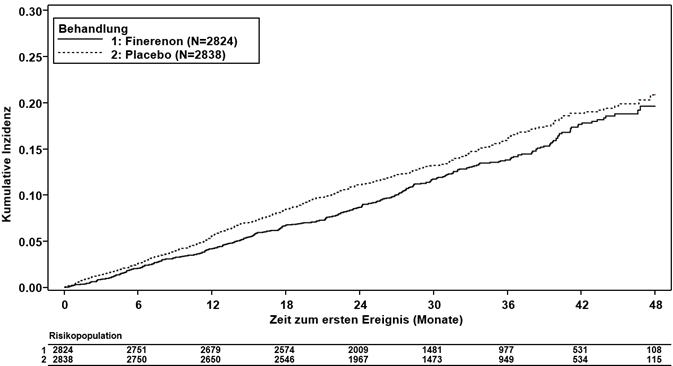
Abbildung 2: Zeit bis zum ersten Auftreten von KV Tod, nichttödlichem MI, nichttödlichem Schlaganfall oder Hospitalisierung wegen Herzinsuffizienz in der FIDELIO-DKD-Studie
Die FIGARO-DKD Studie untersuchte die Wirkung von Finerenon gegenüber Placebo auf das Eintreten kardiovaskulärer und renaler Ereignisse bei erwachsenen Patienten mit Typ-2-Diabetes und chronischer Nierenerkrankung (Einschlusskriterien: a) moderate Albuminurie [UACR ≥30 - < 300 mg/g] und eGFR 25 - 90 ml/min/1.73 m2 ODER b) schwere Albuminurie [UACR ≥300 mg/g] und eGFR ≥60 ml/min/1.73 m2). Um in die Studie eingeschlossen zu werden, mussten die Patienten ausserdem einen Serumkaliumspiegel von ≤4.8 mmol/l aufweisen sowie bereits eine Vorbehandlung mit einer Standardtherapie, inklusive einer maximal verträglichen Dosis eines Angiotensin-Converting-Enzyme-Hemmers (ACEI [43 %]) oder eines Angiotensinrezeptorblockers (ARB [57%]) erhalten. Die Indikation für eine Behandlung mit einem MRA gemäss Leitlinien (wie symptomatische chronische Herzinsuffizienz mit reduzierter Auswurffraktion) war ein Ausschlusskriterium. Patienten mit
chronischer Nierener
krankung und Typ-2-D
iabetes
Finerenon* 10 oder Placebo* n = 3654 Behandlungseffekt
20 mg 1x täglich n Finerenon/Placebo
= 3674
Primäre und sekundär n (%) Ereignisrate (100 n (%) Ereignisrate (100 Hazard Ratio (95%-KI p-Wert
e Ereigniszeit-Endpu Pt.j.) Pt.j.) )
nkte:
Primärer kombinierte 457 (12.4 %) 3.88 518 (14.2 %) 4.46 0.87 [0.76; 0.98] 0.0254
r Endpunkt "KV Tod,
nichttödlicher MI,
nichttödlicher
Schlaganfall oder
Hospitalisierung
wegen Herzinsuffizie
nz"
KV Tod 193 (5.3 %) 1.56 214 (5.9 %) 1.75 0.89 [0.73; 1.08] -
Nichttödlicher MI 103 (2.8 %) 0.85 101 (2.8 %) 0.84 1.00 [0.76; 1.32] -
Nichttödlicher 108 (2.9 %) 0.89 111 (3.0 %) 0.93 0.97[0.74; 1.26] -
Schlaganfall
Hospitalisierung 117 (3.2 %) 0.97 163 (4.5 %) 1.36 0.71 [0.56; 0.90] -
wegen Herzinsuffizie
nz
Kombinierter Endpunk 350 (9.5 %) 3.17 395 (10.8 %) 3.59 0.87 [0.75; 1.01] 0.0635**
t "Nierenversagen,
anhaltende eGFR-Abna
hme ≥40 % oder
nierendbedingter
Tod"
Nierenversagen 46 (1.3 %) 0.40 62 (1.7 %) 0.55 0.72 [0.49; 1.05] -
Anhaltende eGFR-Abna 338 (9.2 %) 3.06 385 (10.5 %) 3.50 0.86 [0.74; <1.00] -
hme ≥40 %
Nierenbedingter Tod 0 - 2 (<0.1 %) - - -
* Behandlung zusätzl
ich zu maximal
verträglichen
zugelassenen Dosen
von ACEI oder ARB.
** Nicht signifikant
.
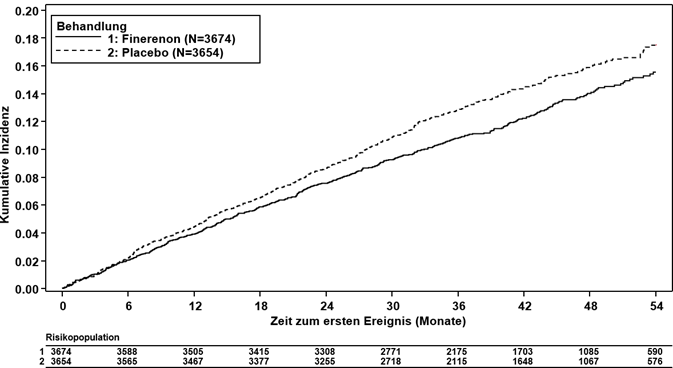
Abbildung 4: Zeit bis zum ersten Auftreten von Nierenversagen, anhaltender eGFR-Abnahme ≥40 % vs. Ausgangswert oder nierenbedingtem Tod in der FIGARO-DKD-Studie
In einer vorgegebenen gepoolten Analyse der Studien FIDELIO-DKD und FIGARO-DKD reduzierte Finerenon das Risiko für den kombinierten kardiovaskulären Endpunkt "Zeit bis zum Eintritt von KV Tod, nichttödlichem MI, nichttödlichem Schlaganfall oder Hospitalisierung wegen Herzinsuffizienz" verglichen mit Placebo (HR 0.86 [95%-KI 0.78; 0.95]) (siehe Abbildung 5). Das Risiko für den kombinierten renalen Endpunkt "Zeit bis zum Eintritt von Nierenversagen, anhaltender eGFR-Abnahme ≥40 % gegenüber dem Ausgangswert oder nierenbedingtem Tod" war ebenfalls reduziert mit Finerenon verglichen mit Placebo (HR 0.84 [95%-KI 0.77; 0.92]), ebenso wie der kombinierte Endpunkt aus Zeit bis zum Eintritt von Nierenversagen, anhaltender eGFR-Abnahme ≥57 % (entspricht etwa einer Verdoppelung des Serumkreatinins) gegenüber dem Ausgangswert oder nierenbedingtem Tod (HR 0.76 [95%-KI 0.66; 0.88]) (siehe Abbildung 5).
Herzinsuffizienz Patienten mit
Herzinsuffizienz
und LVEF ≥40 %
Finerenon 10 oder Placebo n = 2998 Behandlungseffekt
20 oder 40 mg 1x Finerenon/Placebo
täglich n = 3003
Primäre und sekundär [Ereignisse gesamt] Ereignisrate(100 [Ereignisse gesamt] Ereignisrate (100 Hazard Ratio (HR) p-Wert
e Wirksamkeitsendpun n (%) {LS-Mittelwert Pt.j) n (%) {LS-Mittelwert Pt.j) Odds Ratio (OR)
kte: } } Rate Ratio (RR)
LS-Mittelwert-Differ
enz (LSM) [95%-KI]
Primärer kombinierte [1083] 624 (20.8%) 14.88 [1283] 719 (24.0%) 17.70 RR 0.84[0.74, 0.95] 0.0072
r Endpunkt aus KV
Tod und gesamten
Herzinsuffizienzerei
gnissen
Gesamte Herzinsuffiz [842] 479 (16.0%) 11.57 [1024] 573 (19.1%) 14.12 RR 0.82[0.71, 0.94] 0.0062
ienzereignisse
KV Tod 242(8.1%) 3.33 260(8.7%) 3.59 HR 0.93[0.78, 1.11] -
Veränderung des {7.99} - {6.43} - LSM 1.56[0.79, 2.34] <0.0001
KCCQ-TSS gegenüber
Ausgangswert
Verbesserung der 557† (18.6%) - 553(18.4%) - OR 1.01[0.88, 1.15] 0.9295*
NYHA-Klasse
* Nicht signifikant
(Testverfahren
gestoppt) † N = 3002
| |
| ||||||||||||
|
|