Was ist ADZYNMA und wann wird es angewendet?ADZYNMA enthält den Wirkstoff rADAMTS13, eine künstlich hergestellte Kopie des natürlichen Enzyms (Proteins) ADAMTS13. Bei Menschen mit kongenitaler (angeborener) thrombotisch-thrombozytopenischer Purpura (cTTP) fehlt dieses Enzym.
Die kongenitale TTP ist eine sehr seltene erbliche Blutkrankheit, bei der sich in kleinen Blutgefässen im Körper Blutgerinnsel bilden. Diese Gerinnsel können den Blut- und Sauerstofffluss zu den Körperorganen blockieren, was dazu führt, dass die Anzahl der Blutplättchen (Bestandteile, die die Blutgerinnung unterstützen) im Blut niedriger als normal ist.
Die kongenitale TTP wird durch einen Mangel des Enzyms ADAMTS13 im Blut verursacht. ADAMTS13 hilft, die Bildung von Blutgerinnseln zu verhindern, indem es grosse Moleküle des von Willebrand-Faktors (VWF) abbaut. Wenn die VWF-Moleküle zu gross sind, können sie gefährliche Blutgerinnsel verursachen. ADZYNMA wird angewendet, um den Mangel an ADAMTS13 auszugleichen. Dadurch werden diese grösseren Moleküle in kleinere Moleküle zerlegt, was die Wahrscheinlichkeit verringert, dass sich Blutgerinnsel bilden und potenziell niedrige Blutplättchenwerte bei Patienten mit cTTP verhindert.
ADZYNMA darf nur auf Verschreibung des Arztes oder der Ärztin angewendet werden.
Wann darf ADZYNMA nicht angewendet werden?ADZYNMA darf nicht angewendet werden
wenn Sie in der Vergangenheit schwere oder möglicherweise lebensbedrohliche allergische Reaktionen auf den Wirkstoff rADAMTS13 oder einen der in Abschnitt "Was ist in ADZYNMA enthalten?" genannten Hilfsstoffe dieses Arzneimittels hatten.
Wann ist bei der Anwendung von ADZYNMA Vorsicht geboten?Bitte sprechen Sie mit Ihrem Arzt oder Apotheker bzw. Ihrer Ärztinoder Apothekerin, bevor Sie ADZYNMA anwenden.
Allergische Reaktionen
Es besteht das Risiko, dass Sie eine allergische Überempfindlichkeitsreaktion auf ADZYNMA entwickeln. Ihr Arzt bzw. Ihre Ärztin sollte Sie über erste Anzeichen einer schweren allergischen Reaktion informieren. Dazu gehören z. B.:
ein schneller Herzschlag
-Engegefühl in der Brust
-Keuchen und/oder plötzlich einsetzende Atemnot
niedriger Blutdruck
-Nesselsucht, Hautausschlag und juckende Haut
laufende oder verstopfte Nase
gerötete Augen
-Niesen
rasch auftretende Schwellungen unter der Haut in Bereichen wie dem Gesicht, dem Hals, den Armen und Beinen
-Müdigkeit
-Übelkeit
-Erbrechen
-Empfindungen wie Taubheit, Kribbeln, Nadelstiche
-Unruhe
-Anaphylaxie (eine schwere allergische Reaktion, die zu Schluck- und/oder Atembeschwerden, gerötetem oder geschwollenem Gesicht und/oder Händen führen kann).
Wenn eines dieser Symptome auftritt, wird Ihr Arzt bzw. Ihre Ärztin entscheiden, ob Ihre Behandlung mit ADZYNMA abgebrochen werden muss und Ihnen entsprechende Medikamente verabreichen, um die allergische Reaktion zu behandeln. Schwere Symptome, einschliesslich Atemnot und Schwindelgefühl, erfordern eine sofortige Notfallbehandlung.
Inhibitoren
Bei einigen Patienten, die ADZYNMA erhalten, können sich neutralisierende Antikörper (sogenannte Inhibitoren) entwickeln. Diese Inhibitoren können dazu führen, dass die Behandlung nicht mehr richtig wirkt. Informieren Sie Ihren Arzt bzw. Ihre Ärztin, wenn Sie glauben, dass Ihr Arzneimittel bei Ihnen nicht wirkt.
Anwendung von ADZYNMA zusammen mit anderen Arzneimitteln
Informieren Sie Ihren Arzt, Apotheker bzw. Ihre Ärztin, Apothekerin oder das medizinische Fachpersonal, wenn Sie andere Arzneimittel einnehmen, kürzlich andere Arzneimittel eingenommen haben oder beabsichtigen, andere Arzneimittel einzunehmen.
Verkehrstüchtigkeit und Fähigkeit zum Bedienen von Maschinen
Dieses Arzneimittel kann einen geringen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen haben. Nach der Anwendung von ADZYNMA können Schwindelgefühl und Somnolenz (Schläfrigkeit) auftreten.
ADZYNMA enthält Natrium
Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro Durchstechflasche, d.h. es ist nahezu "natriumfrei" .
ADZYNMA enthält Polysorbat 80
Dieses Arzneimittel enthält 2,7 mg Polysorbat 80 pro Durchstechflasche ADZYNMA 500 I.E. oder 1 500 I.E., entsprechend einer maximalen Menge von 0,216 mg/kg Körpergewicht bei einer Dosis von 40 I.E. ADZYNMAv. Polysorbate können allergische Reaktionen hervorrufen. Teilen Sie Ihrem Arzt bzw. Ihrer Ärztin mit, ob bei Ihnen in der Vergangenheit schon einmal eine allergische Reaktion beobachtet wurde.
Informieren Sie Ihren Arzt oder Apotheker bzw. Ihre Ärztin oder Apothekerin, wenn Sie
an anderen Krankheiten leiden,
-Allergien haben oder
andere Arzneimittel (auch selbst gekaufte!) einnehmen.
Darf ADZYNMA während einer Schwangerschaft oder in der Stillzeit angewendet werden?Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Anwendung dieses Arzneimittels Ihren Arzt oder Apotheker bzw. Ihre Ärztin oder Apothekerin um Rat.
Sie dürfen ADZYNMA während der Schwangerschaft nicht erhalten, es sei denn, Ihr Arzt bzw. Ärztin empfiehlt dies ausdrücklich. Sie und Ihr Arzt bzw. Ihre Ärztin müssen entscheiden, ob Sie ADZYNMA erhalten können, wenn Sie stillen.
Wie verwenden Sie ADZYNMA?Die Behandlung mit ADZYNMA wird Ihnen unter Aufsicht eines Arztes bzw. einer Ärztin verabreicht, der in der Behandlung von Patienten mit Blutkrankheiten erfahren ist.
ADZYNMA wird Ihnen als intravenöse Injektion (in eine Vene) verabreicht. Es wird Ihrem Arzt bzw. Ihrer Ärztin als Pulver geliefert, das vor der Verabreichung mit dem mitgelieferten Lösungsmittel (eine Flüssigkeit, in der das Pulver aufgelöst wird) aufgelöst (rekonstituiert) wird.
Die Dosis wird auf der Grundlage Ihres Körpergewichts berechnet.
Verabreichung des Arzneimittels zu Hause
Ihr Arzt bzw. Ihre Ärztin kann die Möglichkeit in Betracht ziehen, dass Sie ADZYNMA zu Hause anwenden, wenn Sie Ihre Injektionen gut vertragen. Wenn Sie nach entsprechender Schulung durch den behandelnden Arzt bzw. die behandelnde Ärztin und/oder das Pflegepersonal in der Lage sind, sich ADZYNMA selbst zu injizieren (oder es von einer Betreuungsperson verabreicht wird), wird Ihr Arzt bzw. Ihre Ärztin Ihr Ansprechen auf die Behandlung weiter überwachen. Wenn bei Ihnen während der Verabreichung zu Hause irgendwelche Nebenwirkungen auftreten, müssen Sie die Injektion sofort abbrechen und ärztliche Hilfe aufsuchen.
Empfohlene Dosis
Vorbeugende Enzymersatztherapie
Die übliche Dosis beträgt 40 I.E. pro kg Körpergewicht und wird alle zwei Wochen verabreicht.
Ihr Arzt bzw. Ihre Ärztin kann die Häufigkeit der Verabreichung auf einmal wöchentlich umstellen, wenn ADZYNMA alle zwei Wochen bei Ihnen nicht wirkt.
Bedarfsorientierte Enzymersatztherapie für plötzlich auftretende TTP-Episoden
Wenn Sie eine plötzliche Episode einer thrombotisch-thrombozytopenischen Purpura (TTP) entwickeln, ist die empfohlene Dosis von ADZYNMA wie folgt:
-40 I.E./kg Körpergewicht an Tag 1.
-20 I.E./kg Körpergewicht an Tag 2.
-15 I.E./kg Körpergewicht ab Tag 3, einmal täglich bis zwei Tage nach Abklingen der plötzlichen TTP-Episode.
Wenn Sie eine grössere Menge von ADZYNMA angewendet haben, als Sie sollten
Die Anwendung zu grosser Mengen dieses Arzneimittels kann zu Blutungen führen.
Wenn Sie die Anwendung von ADZYNMA vergessen haben
Wenn Sie eine Injektion von ADZYNMA vergessen haben, informieren Sie bitte so schnell wie möglich Ihren Arzt bzw. Ihre Ärztin. Wenden Sie nicht die doppelte Menge an, wenn Sie die vorherige Anwendung vergessen haben.
Wenn Sie die Anwendung von ADZYNMA abbrechen
Sprechen Sie mit Ihrem Arzt bzw. Ihrer Ärztin, wenn Sie die Behandlung mit ADZYNMA abbrechen möchten. Die Symptome Ihrer Krankheit können sich verschlimmern, wenn Sie die Behandlung abbrechen.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt, Apotheker bzw. Ihre Ärztin, Apothekerin oder das medizinische Fachpersonal.
Ändern Sie nicht von sich aus die verschriebene Dosierung. Wenn Sie glauben, das Arzneimittel wirke zu schwach oder zu stark, so sprechen Sie mit Ihrem Arzt oder Apotheker bzw. mit Ihrer Ärztin oder Apothekerin.
Welche Nebenwirkungen kann ADYZNMA haben?Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Die folgenden Nebenwirkungen wurden im Zusammenhang mit ADZYNMA berichtet:
Sehr häufig (betrifft mehr als einen von 10 Behandelten)
-Infektion der Nase und des Rachens
-Kopfschmerzen
-Schwindelgefühl
-Migräne
-Durchfall
-Übelkeit
Häufig (betrifft 1 bis 10 von 100 Behandelten)
-Erhöhte Anzahl von Blutplättchen im Blut (Thrombozytose)
-Schläfrigkeit
-Verstopfung
-Blähungen (aufgetriebener Bauch)
-Schwäche (Asthenie)
-Wärmegefühl
-ADAMTS13-Aktivität anormal
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker bzw. Ihre Ärztin oder Apothekerin. Dies gilt insbesondere auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind.
Was ist ferner zu beachten?Ausser Reichweite von Kindern aufbewahren.
Das Arzneimittel darf nur bis zu dem auf dem Behälter mit "EXP" bezeichneten Datum verwendet werden. Das Verfalldatum bezieht sich auf den letzten Tag des angegebenen Monats.
Ungeöffnete Durchstechflaschen.
Im Kühlschrank lagern (2 °C - 8 °C).
Nicht einfrieren.
In der Originalverpackung aufbewahren, um den Inhalt vor Licht zu schützen.
Nach Herstellung der Injektionslösung (Rekonstitution)
Verwenden Sie ADZYNMA innerhalb von 3 Stunden nach Herstellung der Injektionslösung bzw. nach dem Auflösen des Pulvers mit dem Lösungsmittel. Entsorgen Sie unbenutzte Injektionslösung nach 3 Stunden.
Sie dürfen die Injektionslösung nicht verwenden, wenn Sie bemerken, dass diese nicht klar und farblos ist.
Entsorgen Sie keine Arzneimittel in das Abwasser oder den Haushaltsabfall. Abgelaufene oder nicht mehr benötigte Arzneimittel aus Haushalten können in Apotheken oder Sammelstellen abgegeben werden. Diese Massnahmen tragen zum Schutz der Umwelt bei. Weitere Auskünfte erteilt Ihnen Ihr Arzt oder Apotheker bzw. Ihre Ärztin oder Apothekerin. Diese Personen verfügen über die ausführliche Fachinformation.
Was ist in ADZYNMA enthalten?Wirkstoffe
rADAMTS13 (gereinigtes rekombinantes humanes Protein).
Hilfsstoffe
Natriumchlorid, Calciumchlorid-Dihydrat, L-Histidin, Mannitol, Saccharose, Polysorbat 80 (E433), Wasser für Injektionszwecke.
Wo erhalten Sie ADZYNMA? Welche Packungen sind erhältlich?In Apotheken nur gegen ärztliche Verschreibung.
ADZYNMA 500 I.E.:
Jede Packung enthält eine Durchstechflasche mit Pulver (500 I.E. rADAMTS13), eine Durchstechflasche mit 5 ml Lösungsmittel, eine Rekonstitutionshilfe (BAXJECT II Hi-Flow), eine Einwegspritze, ein Infusionsset und zwei Alkoholtupfer.
ADZYNMA 1500 I.E.:
Jede Packung enthält eine Durchstechflasche mit Pulver (1500 I.E. rADAMTS13), eine Durchstechflasche mit 5 ml Lösungsmittel, eine Rekonstitutionshilfe (BAXJECT II Hi-Flow), eine Einwegspritze, ein Infusionsset und zwei Alkoholtupfer.
Zulassungsnummer69562 (Swissmedic)
ZulassungsinhaberinTakeda Pharma AG, 8152 Opfikon
Diese Packungsbeilage wurde im Oktober 2025 letztmals durch die Arzneimittelbehörde (Swissmedic) geprüft.Hinweise für den Gebrauch
Hinweise für den Gebrauch
Diese Hinweise für den Gebrauch enthalten Informationen darüber, wie das Pulver mit dem Lösungsmittel aufgelöst und die gebrauchsfertige Injektionslösung von ADZYNMA hergestellt und intravenös verabreicht wird.
Diese Hinweise für den Gebrauch richten sich an medizinisches Fachpersonal sowie an Patienten/Betreuungspersonen, die ADZYNMA nach entsprechender Schulung durch medizinisches Fachpersonal zu Hause verabreichen werden.
Die Behandlung mit ADZYNMA muss von einem Arzt bzw. einer Ärztin verschrieben und überwacht werden, der Erfahrung in der Behandlung von Patienten mit Bluterkrankungen hat.
Wichtig:
-Nur zur intravenösen Injektion nach Rekonstitution (Auflösen des Pulvers mit dem Lösungsmittel und Herstellung der gebrauchsfertigen Injektionslösung).
-Wenden Sie während des gesamten Verfahrens eine aseptische Technik an.
-Überprüfen Sie vor der Anwendung das Verfalldatum des Arzneimittels. Verwenden Sie ADZYNMA nicht mehr, wenn das auf dem Umkarton bzw. auf der Etikette nach "EXP" angegebene Datum überschritten ist.
-Wenn der Patient mehr als eine Durchstechflasche ADZYNMA pro Injektion benötigt, rekonstituieren Sie jede Durchstechflasche gemäss den Anweisungen unter „Rekonstitution“.
-Prüfen Sie die rekonstituierte, gebrauchsfertige ADZYNMA-Lösung vor der Verabreichung auf Partikel (Teilchen) und Verfärbungen. Die Lösung muss klar und farblos sein.
-Verabreichen Sie die Lösung nicht, wenn Partikel oder Verfärbungen erkennbar sind.
-Verwenden Sie ADZYNMA innerhalb von 3 Stunden nach der Rekonstitution.
-Verabreichen Sie ADZYNMA nicht gleichzeitig mit anderen Infusionspräparaten über denselben Infusionsschlauch oder -behälter.
Rekonstitution (Herstellung der gebrauchsfertigen Injektionslösung)
1.Bereiten Sie eine saubere, ebene Fläche vor, und legen Sie alle Materialien bereit, die Sie für die Rekonstitution und Verabreichung benötigen (Abbildung A).
Abbildung A
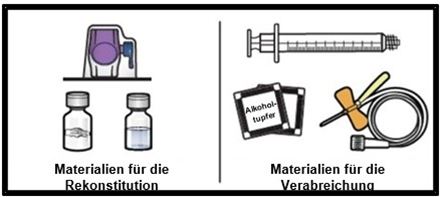
2.Lassen Sie die Durchstechflaschen mit ADZYNMA bzw. dem Lösungsmittel vor Gebrauch Raumtemperatur annehmen.
3.Waschen und trocknen Sie Ihre Hände gründlich.
4.Entfernen Sie die Kunststoffkappen von den Durchstechflaschen mit ADZYNMA bzw. dem Lösungsmittel, und stellen Sie die Durchstechflaschen auf eine saubere, ebene Fläche (Abbildung B).
Abbildung B

5.Wischen Sie die Gummistopfen mit einem Alkoholtupfer ab, und lassen Sie sie vor dem Gebrauch trocknen. (Abbildung C).
Abbildung C

6.Öffnen Sie die Verpackung des BAXJECT II Hi-Flow-Systems, indem Sie den Deckel abziehen, ohne die darunter liegende Fläche zu berühren (Abbildung D).
-Nehmen Sie das BAXJECT II Hi-Flow-System nicht aus der Verpackung.
-Berühren Sie nicht den durchsichtigen Kunststoffdorn.
Abbildung D

7.Drehen Sie die Packung mit dem BAXJECT II Hi-Flow-System auf den Kopf, und setzen Sie sie auf den Stopfen der Durchstechflasche mit dem Lösungsmittel. Drücken Sie gerade nach unten, bis der durchsichtige Kunststoffdorn den Stopfen der Durchstechflasche mit dem Lösungsmittel durchstösst (Abbildung E).
Abbildung E

8.Greifen Sie die Verpackung des BAXJECT II Hi-Flow-Systems am Rand, und ziehen Sie sie vom System ab (Abbildung F).
-Entfernen Sie nicht die blaue Kappe vom BAXJECT II Hi-Flow-System.
-Berühren Sie nicht den freiliegenden violetten Kunststoffdorn.
Abbildung F

9.Drehen Sie das ganze System um, sodass sich die Durchstechflasche mit dem Lösungsmittel nun oben befindet. Drücken Sie das BAXJECT II Hi-Flow-System gerade nach unten, bis der violette Kunststoffdorn den Stopfen der Durchstechflasche mit dem ADZYNMA-Pulver durchstösst (Abbildung G). Das Vakuum wird das Lösungsmittel in die Durchstechflasche mit dem ADZYNMA-Pulver ziehen.
-Eventuell bemerken Sie ein paar Bläschen oder Schaumbildung – das ist normal und sollte rasch wieder verschwinden.
Abbildung G

10.Schwenken Sie die verbundenen Durchstechflaschen vorsichtig und gleichmässig, bis das Pulver vollständig aufgelöst ist (Abbildung H).
-Schütteln Sie die Durchstechflaschen nicht.
Abbildung H

11.Unterziehen Sie die rekonstituierte Lösung vor der Verabreichung einer Sichtprüfung auf Partikel und Verfärbungen.
-Verwenden Sie die Lösung nicht, wenn Sie Partikel oder Verfärbungen erkennen.
12.Wenn die Dosis mehr als eine Durchstechflasche ADZYNMA erfordert, wiederholen Sie für jede Durchstechflasche die oben beschriebenen Schritte zur Rekonstitution.
-Verwenden Sie jedes Mal ein neues BAXJECT II Hi-Flow-System, um jede Durchstechflasche mit ADZYNMA und Lösungsmittel zu rekonstituieren.
Verabreichung von ADZYNMA
13.Nehmen Sie die blaue Kappe vom BAXJECT II Hi-Flow-System ab (Abbildung I). Setzen Sie eine Luerlock-Spritze auf (Abbildung J).
-Injizieren Sie keine Luft in das System.
Abbildung I Abbildung J
14.Drehen Sie das System auf den Kopf (die ADZYNMA-Durchstechflasche befindet sich nun oben). Ziehen Sie die rekonstituierte Lösung in die Spritze auf, indem Sie den Kolben der Spritze langsam zurückziehen (Abbildung K).
Abbildung K

15.Wenn ein Patient mehr als eine Durchstechflasche ADZYNMA erhalten soll, kann der Inhalt mehrerer Durchstechflaschen in dieselbe Spritze aufgezogen werden. Wiederholen Sie diesen Vorgang für alle rekonstituierten Durchstechflaschen mit ADZYNMA, bis die zu verabreichende Gesamtmenge erreicht ist.
16.Ziehen Sie die Spritze ab, und schliessen Sie eine geeignete Injektionsnadel oder ein Infusionsset an.
17.Halten Sie die Nadel so, dass sie nach oben zeigt, und entfernen Sie eventuell vorhandene Luftblasen durch leichtes Antippen der Spritze mit dem Finger. Drücken Sie dabei die Luft langsam und vorsichtig aus Spritze und Nadel.
18.Legen Sie eine Staubinde an, und reinigen Sie die Injektionsstelle mit einem Alkoholtupfer (Abbildung L).
Abbildung L

19.Führen Sie die Nadel in die Vene ein, und nehmen Sie die Staubinde ab.
20.Infundieren Sie das rekonstituierte ADZYNMA langsam, mit einer Rate von 2 bis 4 ml pro Minute (Abbildung M).
-Sie können eine Spritzenpumpe verwenden, um die Verabreichungsrate zu kontrollieren.
Abbildung M

21.Ziehen Sie die Nadel aus der Vene, und üben Sie mehrere Minuten lang Druck auf die Injektionsstelle aus.
-Setzen Sie die Kappe nicht wieder auf die Nadel.
Aufbewahrung von ADZYNMA
-Bewahren Sie ADZYNMA im Kühlschrank (2 °C - 8 °C) auf. Nicht einfrieren. In der Originalverpackung aufbewahren, um den Inhalt vor Licht zu schützen.
Nach dem auf dem Etikett und Umkarton nach "EXP" angegebenen Verfalldatum nicht mehr verwenden.
-Verwenden Sie ADZYNMA innerhalb von 3 Stunden nach der Rekonstitution. Entsorgen Sie nicht gebrauchte Injektionslösung, wenn Sie sie nicht innerhalb von 3 Stunden nach der Rekonstitution verwenden.
Entsorgung von ADZYNMA
-Die Durchstechflaschen sind nur zum einmaligen Gebrauch bestimmt.
-Entsorgen Sie die benutzten Nadeln, Spritzen und leeren Durchstechflaschen in einem durchstichfesten Abwurfbehälter.
-Entsorgen Sie keine Arzneimittel in das Abwasser oder den Haushaltsabfall. Abgelaufene oder nicht mehr benötigte Arzneimittel aus Haushalten können in Apotheken oder Sammelstellen abgegeben werden. Diese Massnahmen tragen zum Schutz der Umwelt bei.
| 










