Zusammensetzung
Wirkstoffe
Pirtobrutinib
Hilfsstoffe
Hypromelloseacetatsuccinat, mikrokristalline Cellulose, Lactose-Monohydrat, Croscarmellose-Natrium, Magnesiumstearat, Siliciumdioxid-Hydrat
Hypromellose (E464), Titandioxid (E171), Triacetin, Indigocarmin (E132)
Jaypirca 50 mg Filmtabletten
Jede Filmtablette enthält 38.3 mg Lactose (als Monohydrat).
Jede Filmtablette enthält 0.7 mg Natrium (als Croscarmellose-Natrium).
Jaypirca 100 mg Filmtabletten
Jede Filmtablette enthält 76.5 mg Lactose (als Monohydrat).
Jede Filmtablette enthält 1.4 mg Natrium (als Croscarmellose-Natrium).
Darreichungsform und Wirkstoffmenge pro Einheit
Filmtabletten zu 50 mg bzw. 100 mg Pirtobrutinib.
Jaypirca 50 mg Filmtabletten
Blaue, 9 x 9 x 4 mm, gewölbte, dreieckige Tablette mit der Prägung "Lilly 50" auf einer Seite und "6902" auf der anderen Seite.
Jaypirca 100 mg Filmtabletten
Blaue, 10 x 6 mm, runde Tablette mit der Prägung "Lilly 100" auf einer Seite und "7026" auf der anderen Seite.
Indikationen/Anwendungsmöglichkeiten
Befristet zugelassene Indikation
Jaypirca ist als Monotherapie indiziert zur Behandlung von erwachsenen Patienten mit rezidiviertem oder refraktärem Mantelzelllymphom (MCL), die zuvor mindestens zwei Linien systemische Behandlungen erhalten haben, einschliesslich einem anti-CD20-Antikörper und einem Bruton-Tyrosinkinase (BTK)-Inhibitor, und wenn die Patienten für eine CAR-T Therapie nicht geeignet sind (siehe "Klinische Wirksamkeit" ).
Aufgrund einer zum Zeitpunkt der Begutachtung des Gesuches unvollständigen klinischen Datenlage, wird diese Indikation befristet zugelassen (Art. 9a Heilmittelgesetz). Die befristete Zulassung ist zwingend an die zeitgerechte Erfüllung von Auflagen gebunden. Nach deren Erfüllung kann die befristete Zulassung in eine ordentliche Zulassung überführt werden.
Nicht befristet zugelassene Indikation
Jaypirca ist als Monotherapie indiziert zur Behandlung von erwachsenen Patienten mit rezidivierter oder refraktärer chronischer lymphatischer Leukämie (CLL), die zuvor mindestens zwei Behandlungslinien einschliesslich einem BTK-Inhibitor erhalten haben (siehe "Klinische Wirksamkeit" ).
Dosierung/Anwendung
Übliche Dosierung
Die empfohlene Dosis beträgt 200 mg Pirtobrutinib einmal täglich.
Die Behandlung sollte bis zum Progress oder nicht-akzeptablen Toxizität fortgeführt werden.
Dosisanpassungen
Empfohlene Dosisanpassungen für Nebenwirkungen vom Grad 3 oder 4 sind in der folgenden Tabelle beschrieben.
Tabelle 1. Empfohlene Dosisanpassungen für bestimmte Nebenwirkungen
Art der Nebenwirkunga Auftreten derselben Anpassung
Nebenwirkung, die eine
Dosisanpassung erforderlich
macht
-Grad 3 oder 4 nicht-hämatologische Zum 1. Mal Unterbrechung der Einnahme
Toxizitätb -Absolute Neutrophilenzahl von Jaypirca bis zur
<1 bis 0.5 x 109/l mit Fieber und/oder Erholung auf Grad 1 oder
Infektion -Absolute Neutrophilenzahl den Ausgangszustand.
<0.5 x 109/l über ≥7 Tage Fortsetzung der Therapie
-Thrombozytenzahl <50 bis 25 x 109/l mit der ursprünglichen
mit Blutung -Thrombozytenzahl <25 x Dosis von 200 mg einmal
109/l täglich.
Zum 2. Mal Unterbrechung der Einnahme
von Jaypirca bis zur
Erholung auf Grad 1 oder
den Ausgangszustand.
Fortsetzung der Therapie
mit einer reduzierten
Dosis von 100 mg einmal
täglich.
Zum 3. Mal Unterbrechung der Einnahme
von Jaypirca bis zur
Erholung auf Grad 1 oder
den Ausgangszustand.
Fortsetzung der Therapie
mit einer reduzierten
Dosis von 50 mg einmal
täglich.
Zum 4. Mal Absetzen von Jaypirca.
a Bei einer asymptomatischen Lymphozytose wird keine Dosisanpassung empfohlen. Bei einem asymptomatischen Lipaseanstieg ist eine Dosisanpassung nicht zwangsläufig erforderlich.
b Nach einer nicht-hämatologischen Toxizität Grad 4 sind Nutzen und Risiken zu beurteilen, bevor die Behandlung mit derselben Dosis fortgesetzt wird.
Die Zuweisung der Schweregrade basiert auf National Cancer Institute Common Terminology Criteria for Adverse Events (NCI CTCAE).
Dosisanpassung bei begleitender Anwendung von CYP3A-Induktoren
Die Anwendung von Jaypirca in Kombination mit starken oder moderaten CYP3A-Induktoren ist zu vermeiden. Lässt sich die Kombination mit moderaten CYP3A-Induktoren nicht vermeiden und die derzeitige Dosis Jaypirca beträgt 200 mg einmal täglich, ist die Dosis auf 300 mg zu erhöhen. Beträgt die derzeitige Dosis 50 mg oder 100 mg einmal täglich, ist die Dosis um 50 mg zu erhöhen.
Dosisanpassungen bei begleitender Anwendung von starken CYP3A-Inhibitoren
Die Anwendung von Jaypirca in Kombination mit starken CYP3A-Inhibitoren ist zu vermeiden (siehe "Interaktionen" und "Pharmakokinetik" ). Wenn sich die Kombination mit einem starken CYP3A-Inhibitor nicht vermeiden lässt, ist die Dosis von Jaypirca um 50 mg zu reduzieren. Beträgt die derzeitige Dosis 50 mg einmal täglich, wird die Behandlung mit Jaypirca für die Dauer der Anwendung des starken CYP3A-Inhibitors unterbrochen. Fünf Halbwertszeiten nach Beendigung der Anwendung eines starken CYP3A-Inhibitors, wird die Behandlung mit Jaypirca mit der Dosis fortgesetzt, die vor Beginn des starken CYP3A-Inhibitors angewendet wurde.
Vergessene Einnahme
Wenn seit Vergessen der Einnahme mehr als 12 Stunden vergangen sind, weisen Sie den Patienten an, die nächste Dosis zum vorgesehenen Zeitpunkt einzunehmen; eine zusätzliche Dosis sollte nicht eingenommen werden. Bei Erbrechen wird keine zusätzliche Dosis eingenommen, sondern die Behandlung mit der nächsten planmässigen Dosis fortgesetzt.
Ältere Patienten
Dosisanpassungen aufgrund des Alters sind nicht erforderlich (siehe Rubriken "Pharmakokinetik" und "Unerwünschte Wirkungen" ).
Nierenfunktionsstörungen
Bei Patienten mit schwerer Nierenfunktionsstörung (eGFR 15-29 ml/min) und einer derzeitigen Dosis von 200 mg einmal täglich, ist die Dosis von Jaypirca auf 100 mg einmal täglich zu reduzieren, sonst wird die Dosis um 50 mg reduziert. Wenn die derzeitige Dosis 50 mg beträgt, ist Jaypirca abzusetzen (siehe Rubrik "Pharmakokinetik" ).
Bei Patienten mit leichter oder mittelschwerer Nierenfunktionsstörung (eGFR 30-89 ml/min) ist keine Dosisanpassung erforderlich.
Es liegen keine Daten zu Dialysepatienten vor (siehe Rubrik "Pharmakokinetik" ).
Leberfunktionsstörungen
Bei Patienten mit leichter, mittelschwerer oder schwerer Leberfunktionsstörung ist keine Dosisanpassung erforderlich (siehe Rubrik "Pharmakokinetik" ).
Pädiatrische Population
Jaypirca ist für die Anwendung in der pädiatrischen Population nicht zugelassen.
Art der Anwendung
Zum Einnehmen.
Die Tablette sollte als Ganzes geschluckt werden, um eine gleichbleibende Wirkung zu gewährleisten (Patienten sollten die Tabletten vor dem Schlucken nicht kauen, zerkleinern oder teilen). Sie kann unabhängig von den Mahlzeiten eingenommen werden.
Patienten sollten die Dosis jeden Tag ungefähr zur gleichen Uhrzeit einnehmen.
Kontraindikationen
Überempfindlichkeit gegen den Wirkstoff oder einem der Hilfsstoffe, die in der Rubrik "Zusammensetzung" aufgeführt sind.
Warnhinweise und Vorsichtsmassnahmen
Infektionen
Bei Patienten, die mit Jaypirca behandelt wurden, sind schwerwiegende und tödlich verlaufende Infektionen (einschliesslich Infektionen durch Bakterien, Viren oder Pilze), sowie opportunistische Infektionen berichtet worden. In den klinischen Studien wurden Infektionen Grad 3 oder höher von 25.4% der 704 Patienten berichtet, am häufigsten Pneumonie (8.9%), mit fatalen Infektionen bei 5.0% der Patienten. Sepsis wurde bei 5.8% der Patienten berichtet, febrile Neutropenie bei 3.8%. Zu den opportunistischen Infektionen nach Behandlung mit Jaypirca gehörten (jedoch nicht nur) Pneumocystis jirovecii Pneumonie und Pilzinfektion.
Ziehen Sie bei Patienten mit erhöhtem Risiko für Infektionen, einschliesslich opportunistischer Infektionen, vorbeugende Massnahmen in Erwägung, einschliesslich Impfungen und prophylaktische antimikrobielle Therapie. Überwachen Sie die Patienten auf Anzeichen und Symptome einer Infektion, klären Sie umgehend ab, und behandeln Sie angemessen. Abhängig vom Schweregrad ist die Dosis zu reduzieren, die Behandlung zu unterbrechen, oder Jaypirca dauerhaft abzusetzen (siehe Rubrik "Dosierung/Anwendung" ).
Tumorlysesyndrom
Ein Tumorlysesyndrom (TLS) wurde während der Therapie mit Jaypirca selten berichtet. Hochrisikopatienten für ein TLS sind diejenigen Patienten, die vor der Behandlung eine hohe Tumorlast hatten. Patienten sollten auf ein mögliches Risiko für TLS untersucht und entsprechend medizinischer Indikation engmaschig überwacht werden.
Hämorrhagien
Mit Jaypirca sind schwerwiegende und tödlich verlaufende Blutungen aufgetreten. Schwere Blutungsereignisse (definiert als Grad 3 oder höher oder jegliche zentralnervöse Blutung) wurden bei 3.1% der 704 Patienten unter Jaypirca berichtet, einschliesslich gastrointestinaler Blutungen; fatale Blutungen wurden bei 0.3% der Patienten berichtet. Blutungsereignisse jeglicher Schweregrade, ausgenommen Blutergüsse und Petechien, wurden bei 19.2% der Patienten berichtet.
Schwere Blutungsereignisse traten bei 2.4% der Patienten mit Jaypirca ohne antithrombotische Medikation und 0.7% der Patienten mit Jaypirca und antithrombotischer Medikation auf. Berücksichtigen Sie Nutzen und Risiko von Antithrombotika bei gleichzeitiger Verabreichung mit Jaypirca. Überwachen Sie Patienten auf Anzeichen einer Blutung. Abhängig vom Schweregrad der Blutung ist die Dosis zu reduzieren, die Behandlung zu unterbrechen, oder Jaypirca dauerhaft abzusetzen (siehe Rubrik "Dosierung/Anwendung" ).
Berücksichtigen Sie Nutzen und Risiko einer Unterbrechung von Jaypirca für 3 bis 7 Tage vor und nach Operationen, abhängig von der Art der Operation und dem Blutungsrisiko.
Zytopenien
Zytopenien Grad 3 und 4, einschliesslich Neutropenie (23.2%), Anämie (10.4%) und Thrombozytopenie (8.9%) traten bei Patienten unter Jaypirca auf.
Überwachen Sie das vollständige Blutbild regelmässig während der Behandlung. Abhängig vom Schweregrad ist die Dosis zu reduzieren, die Behandlung zu unterbrechen, oder Jaypirca dauerhaft abzusetzen (siehe Rubrik "Dosierung/Anwendung" ).
Vorhofflimmern/-flattern
Bei mit Jaypirca behandelten Patienten wurden Vorhofflimmern und Vorhofflattern beobachtet. Vorhofflimmern und -flattern wurde bei 3.4% der Patienten berichtet, Vorhofflimmern und -flattern Grad 3 oder 4 bei 1.6% von 704 Patienten in den klinischen Studien. Patienten mit kardialen Risikofaktoren wie Hypertonie oder vorbestehende Arrhythmien können ein erhöhtes Risiko aufweisen.
Überwachen Sie Patienten auf Anzeichen und Symptome von Arrhythmien (z.B. Palpitationen, Schwindel, Synkope, Dyspnoe) und behandeln Sie sie angemessen. Abhängig vom Schweregrad ist die Dosis zu reduzieren, die Behandlung zu unterbrechen oder Jaypirca dauerhaft abzusetzen (siehe Rubrik "Dosierung/Anwendung" ).
Sekundäre Primärmalignome
Sekundäre Primärmalignome, einschliesslich nicht-Haut-Karzinome, entwickelten sich bei 8.7% der 704 Patienten unter Jaypirca Monotherapie. Die häufigste maligne Erkrankung war nichtmelanozytärer Hautkrebs, dieser wurde bei 4.4% der 704 Patienten berichtet. Andere sekundäre Primärmalignome umfassten solide Tumore (einschliesslich Urogenital- und Brustkrebs) und Melanome. Empfehlen Sie den Patienten die Verwendung von Sonnenschutz, und überwachen Sie die Patienten auf die Entwicklung sekundärer Primärmalignome.
Hepatotoxizität einschliesslich arzneimittelinduzierte Leberschädigung (drug-induced liver injury, DILI)
Hepatotoxizität, einschliesslich schwerer, lebensbedrohlicher und potenziell tödlicher Fälle von arzneimittelinduzierter Leberschädigung (drug-induced liver injury, DILI), ist bei Patienten aufgetreten, die mit Bruton-Tyrosinkinase-Inhibitoren, einschliesslich Jaypirca, behandelt wurden. Vor Beginn und während der Behandlung mit Jaypirca sind die Bilirubin- und Transaminasenwerte zu überwachen. Patienten, die nach Anwendung von Jaypirca abnormale Leberfunktionswerte entwickeln, sollten häufiger auf Abnormalitäten in Leberfunktionstests und klinische Anzeichen einer Hepatotoxizität überwacht werden. Bei Verdacht auf eine DILI ist die Therapie mit Jaypirca auszusetzen. Nach Bestätigung einer DILI muss Jaypirca abgesetzt werden.
Embryofetale Toxizität
Jaypirca kann den Fötus schädigen, wenn es einer schwangeren Frau verabreicht wird (siehe "Schwangerschaft/Stillzeit" ).
Lactose
Patienten mit der seltenen hereditären Galactose-Intoleranz, völligem Lactasemangel oder Glucose-Galactose-Malabsorption sollten dieses Arzneimittel nicht anwenden.
Natriumgehalt
Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro Dosiereinheit, d.h. es ist nahezu ‚natriumfrei'.
Interaktionen
Auswirkungen von Pirtobrutinib auf andere Arzneimittel
Cytochrom P450 (CYP)-Enzyme: In vitro hemmt Pirtobrutinib CYP2C8, CYP2C9, CYP3A, CYP1A2, CYP2B6, CYP2C19 und CYP2D6. In vitro induziert Pirtobrutinib CYP3A4, CYP3A5, CYP2B6 und CYP2C19.
Transporter-Systeme: In vitro hemmt Pirtobrutinib P-gp und BCRP, jedoch nicht OAT1, OAT3, OCT1, OCT2, OATP1B1, OATP1B3, MATE1 oder MATE2-K.
Tabelle 2. Klinische Auswirkungen von Pirtobrutinib auf andere Arzneimittel
Begleitmedikation Dosierung der Dosierung von GMRa (90% KIb) Dosierungsempfehlung
(Enzym oder Transpor Begleitmedikation Pritobrutinib für die Begleitmedi
ter) kation
Cmax AUC0-inf
Midazolam (CYP3A-Sub Midazolam 250 µg IV 200 mg QD 0.99 (0.83, 1.18) 1.12 (1.04, 1.21) Bei Substraten, bei
strat) Einzeldosis denen geringe
Konzentrations-änder
ungen das Risiko
für unerwünschte
Ereignisse erhöhen,
sind die Empfehlunge
n in deren Fachinfor
mation zur Anwendung
in Kombination mit
Inhibitoren von
CYP2C8, CYP2C19,
CYP3A, P-gp oder
BCRP zu beachten.
Midazolam 500 µg 200 mg QD 1.58 (1.40, 1.78) 1.70 (1.55, 1.86)
oral Einzeldosis
Coffein (CYP1A2-Subs Coffein 200 mg 200 mg QD 0.99 (0.93, 1.05) 0.94 (0.91, 0.98)
trat) Einzeldosis
S-Warfarin (CYP2C9-S Warfarin 10 mg 200 mg QD 1.02 (0.97, 1.06) 1.11 (1.08, 1.14)
ubstrat) Einzeldosis
Omeprazol (CYP2C19-S Omeprazol 40 mg 200 mg QD 1.49 (1.31, 1.70) 1.56 (1.35, 1.80)
ubstrat) Einzeldosis
Repaglinid (CYP2C8-S Repaglinid 0.5 mg 200 mg QD 1.98 (1.62, 2.43) 2.30 (1.86, 2.84)
ubstrat) Einzeldosis
Digoxin (P-gp-Substr Digoxin 0.25 mg 200 mg Einzeldosis 1.51 (1.32, 1.73) 1.17 (1.11, 1.23)c
at) BID/QDd
200 mg QD 1.55 (1.35, 1.78) 1.35 (1.29, 1.42)c
Rosuvastatin (BCRP-S Rosuvastatin 20 mg 200 mg Einzeldosis 2.43 (2.18, 2.71) 2.18 (2.00, 2.37)
ubstrat) Einzeldosis
200 mg QD 2.46 (2.20, 2.75) 2.40 (2.21, 2.62)
a GMR – Verhältnis der geometrischen Mittelwerte definiert als die Exposition (maximale Konzentration oder Fläche unter der Kurve AUC) gegenüber der Begleitmedikation bei Anwendung mit Pirtobrutinib dividiert durch die Exposition gegenüber der Begleitmedikation ohne Pirtobrutinib
b KI = Konfidenzintervall
c AUCtau
d BID (zweimal täglich) an Tag 1, anschliessend QD (einmal täglich).
Auswirkungen anderer Arzneimittel auf Pirtobrutinib
Metabolisierende Enzyme: In vitro ist Pirtobrutinib ein Substrat von CYP3A4, UGT1A8 und UGT1A9.
Transporter-Systeme: In vitro ist Pirtobrutinib ein Substrat von P-gp und BCRP, jedoch nicht von OCT1, OATP1B1, OATP1B3 oder BSEP. Pirtobrutinib ist kein Substrat der hepatischen Transporter.
Tabelle 3 Klinische Auswirkungen anderer Arzneimittel auf Pirtobrutinib
Begleitmedikation Dosierung der Dosierung von GMRa (90% KIb) Dosierungsempfehlung
(Enzym oder Transpor Begleitmedikation Pirtobrutinib für Pirtobrutinib
ter)
Cmax AUC0-inf
Itraconazol (Starker 200 mg Itraconazol 200 mg Einzeldosis 1.04 (0.95, 1.13) 1.49 (1.40, 1.58) Die Anwendung in
CYP3A-Inhibitor BID (zweimal täglich Kombination mit
und P-gp-Inhibitor) ) an Tag 1, danach starken CYP3A-Inhibi
QD (einmal täglich) toren ist zu vermeid
über 10 Tage. en. Wenn sich die
Kombination mit
einem starken
CYP3A-Inhibitor
nicht vermeiden
lässt, ist die
Dosis um 50 mg zu
reduzieren. Wenn
die derzeitige
Dosis 50 mg einmal
täglich beträgt,
ist die Behandlung
während der Anwendun
g des starken
CYP3A-Inhibitors zu
unterbrechen (siehe
Rubrik "Dosierung/An
wendung" ). Bei
Anwendung in Kombina
tion mit P-gp-Inhibi
toren ist keine
Dosisanpassung
erforderlich (siehe
auch Ergebnisse
nach einer Einzeldos
is Rifampicin).
Verapamilc (moderate 80 mg dreimal 200 mg QD 1.21 (1.20, 1.22) 1.30 (1.29, 1.32)d Bei Anwendung in
r CYP3A-Inhibitor) täglich Kombination mit
moderaten CYP3A-Inhi
bitoren ist keine
Dosisanpassung
erforderlich.
Diltiazemc (moderate 60 mg dreimal 200 mg QD 1.14 (1.13, 1.14) 1.20 (1.19, 1.21)d
r CYP3A-Inhibitor) täglich
Rifampicin (OATP1B-/ 600 mg Rifampicin 200 mg Einzeldosis 0.93 (0.87, 1.00) 0.97 (0.94, 1.00)e Bei Anwendung in
P-gp-Inhibitor und QD über 16 Tage Tag 8 Kombination mit
starker CYP3A-Indukt (Tage 8 bis 23) OATP1B- und P-gp-Inh
or) ibitoren ist keine
Dosisanpassung
erforderlich.
200 mg Einzeldosis 0.58 (0.54, 0.62) 0.29 (0.27, 0.32) Die Anwendung in
Tag 17 Kombination mit
starken CYP3A-Indukt
oren ist zu vermeide
n (siehe Rubrik
"Dosierung/Anwendung
" ).
Efavirenzc (Moderate 600 mg QD 200 mg QD 0.67 (0.65, 0.69) 0.51 (0.48, 0.54)d Wenn die Anwendung
r CYP3A-Induktor) mit einem moderaten
CYP3A-Induktor
unvermeidbar ist
und die derzeitige
Dosis 200 mg einmal
täglich beträgt,
ist die Dosis auf
300 mg zu erhöhen.
Beträgt die derzeiti
ge Dosis 50 mg oder
100 mg einmal
täglich, ist die
Dosis um 50 mg zu
erhöhen (siehe
Rubrik "Dosierung/An
wendung" ).
Bosentanc (moderater 125 mg BID 200 mg QD 0.80 (0.79, 0.81) 0.73 (0.72, 0.75)d
CYP3A-Induktor)
Omeprazol (Substanz 40 mg QD 200 mg Einzeldosis 1.01 (0.86, 1.18) 1.11 (1.02, 1.22) Bei Anwendung in
zur Reduktion der Kombination mit
Magensäure) Substanzen zur
Reduktion der
Magensäure ist
keine Dosisanpassung
erforderlich.
a GMR – Verhältnis der geometrischen Mittelwerte definiert als die Exposition (maximale Konzentration oder Fläche unter der Kurve AUC) gegenüber Pirtobrutinib bei Anwendung mit der Begleitmedikation dividiert durch die Exposition gegenüber Pirtobrutinib ohne Begleitmedikation
b KI = Konfidenzintervall
c Prognostizierte Interaktion basierend auf PBPK Modellierung
d GMR der AUCtau
e GMR der AUC0-24h
Schwangerschaft, Stillzeit
Empfängnisverhütung
Frauen im gebärfähigen Alter müssen während der Behandlung und für mindestens 1 Woche nach der letzten Anwendung von Pirtobrutinib eine zuverlässige Verhütungsmethode anwenden.
Schwangerschaft
Es liegen keine Erfahrungen zur Anwendung von Jaypirca bei Schwangeren vor. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt (siehe Rubrik "Präklinische Daten" ). Schwangere Frauen sind auf das potenzielle Risiko für das ungeborene Kind hinzuweisen. Jaypirca sollte während einer Schwangerschaft nicht angewendet werden.
Stillzeit
Es gibt keine Daten zum Vorhandensein von Jaypirca in der Muttermilch oder zu den Auswirkungen auf das gestillte Kind oder die Milchbildung. Aufgrund der Möglichkeit von schwerwiegenden Nebenwirkungen beim gestillten Kind sind Frauen darauf hinzuweisen, während der Behandlung mit Jaypirca und bis eine Woche nach der letzten Anwendung nicht zu stillen.
Fertilität
Es liegen keine klinischen Daten zu Auswirkungen von Jaypirca auf die Fertilität beim Menschen vor. Die Fertilitätsstudien in Tieren wurden nicht durchgeführt. In Toxizitätsstudien mit wiederholter Gabe mit einer Dauer von bis zu 3 Monaten hatte Pirtobrutinib keine Auswirkung auf die männlichen oder weiblichen Fortpflanzungsorgane.
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von Maschinen
Es wurden keine Studien zu den Auswirkungen von Pirtobrutinib auf die Fahrtüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durchgeführt. Unter Therapie mit Jaypirca traten unerwünschte Wirkungen auf, z.B. verändertes Sehen, Herzrhythmusstörungen, Übelkeit, Müdigkeit, und Schwindel, welche die Fahrtüchtigkeit und das Bedienen von Maschinen beinträchtigen können.
Unerwünschte Wirkungen
Zusammenfassung des Sicherheitsprofils
Die Zusammenfassung des Sicherheitsprofils und Tabelle 4 listen die während der Behandlung aufgetretenen Nebenwirkungen im Zusammenhang mit Jaypirca als Monotherapie aus klinischen Studiendaten. Die unerwünschten Wirkungen basieren auf gepoolten Daten von 704 Patienten, die in klinischen Studien mit Jaypirca Monotherapie 200 mg QD behandelt wurden.
Die Patienten wurden wegen MCL, chronischer lymphatischer Leukämie/kleinzelligem lymphatischem Lymphom (CLL/SLL) und anderen Non-Hodgkin-Lymphomen (NHL) behandelt.
Die häufigsten unerwünschten Wirkungen jeglicher Schweregrade (≥15%), waren Blutungen (34.7%) Neutropenie (27.1%), Fatigue (26.1%), Diarrhö (23.2%), Anämie (18.8%), Hautausschlag (17.9%), Prellung (17.2%), Ödeme (16.2%) und Übelkeit (16.1%) und Thrombozytopenie (15.5%). Laboranomalien Grad 3 oder höher, die bei ≥5 % der Patienten auftraten, waren eine verringerte Lymphozytenzahl (10.6 %) und eine Zunahme der Lipase (7.2 %).
Schwerwiegende unerwünschten Wirkungen wurden bei 25.3% der Patienten unter Jaypirca berichtet. Schwerwiegende unerwünschte Wirkungen, die bei ≥2% der Patienten berichtet wurden, waren Pneumonie (8.1%), Sepsis (4.7%), Neutropenie (3.1%), Zweite Primärmalignome (2.7%), Blutungen (2.6%) und Anämie (2.1%).
Fatale unerwünschte Wirkungen wurden bei 2.3% der Patienten berichtet, am häufigsten durch Infektionen (1.4%) einschliesslich Pneumonie (0.4%) und Sepsis (1.0%).
Unerwünschte Wirkungen führten zu Dosisreduktionen bei 4.5%, einer Therapieunterbrechung bei 27.7% und dauerhaftem Absetzen von Jaypirca bei 5.8%. Unerwünschte Wirkungen, die bei >5% der Patienten zur Dosisanpassung führten war Neutropenie.
Tabellarische Auflistung der Nebenwirkungen
Die Nebenwirkungen von Patienten, die Jaypirca bei maligner B-Zell-Erkrankung erhalten haben, sind nachfolgend nach Systemorganklasse und Häufigkeit aufgelistet. Häufigkeitsgruppen werden durch die folgende Konvention definiert: sehr häufig (≥1/10); häufig (≥1/100, <1/10); gelegentlich (≥1/1'000, <1/100); selten (≥1/10'000, <1/1'000); sehr selten (<1/10'000) und nicht bekannt (kann aus verfügbaren Daten nicht abgeschätzt werden). Innerhalb jeder Häufigkeitsgruppe sind die Nebenwirkungen nach abnehmendem Schweregrad geordnet.
Tabelle 4: Unerwünschte Wirkungen bei Patienten, die mit 200 mg Jaypirca QD als Monotherapiea behandelt wurden
Systemorganklasse (MedDRA) Unerwünschte Wirkung Häufigkeitskategorie Grad ≥3a (%)
(%) (Alle Grade) N=704
Erkrankungen des Blutes und Neutropenieb Sehr häufig (27.1) 23.2
des Lymphsystems
Anämieb Sehr häufig (18.8) 10.4
Thrombozytopenieb Sehr häufig (15.5) 8.9
Lymphozytoseb Häufig 4.0
Verminderte Lymphozytenzahl Sehr häufig (30.3) 10.6
Augenerkrankungen Verändertes Sehenc Häufig 0.4
Herzerkrankungen Vorhofflimmern/Vorho Häufig 1.6
fflattern
Erkrankungen des Gastrointesti Diarrhö Sehr häufig (23.2) 1.0
naltraktes
Übelkeit Sehr häufig (16.1) 0.3
Bauchschmerzen Sehr häufig (10.5) 0.9
Leber- und Gallenerkrankungen AST erhöht Sehr häufig (18.0) 0.9
ALT erhöht Sehr häufig (23.4) 2.0
Lipase erhöht Sehr häufig (18.7) 7.2
Allgemeine Erkrankungen und Fatigue Sehr häufig (26.1) 1.8
Beschwerden am Verabreichungso
rt
Pyrexie Sehr häufig (14.3) 1.0
Ödemec Sehr häufig (16.2) 0.7
Infektionen und parasitäre Pneumonie Sehr häufig (13.2) 8.9
Erkrankungen
Infektionen der oberen Häufig 0.1
Atemwege
Harnwegsinfektion Häufig 1.0
Sepsisc Häufig 5.4
Verletzung, Vergiftung und Prellung Sehr häufig (17.2) 0.1
durch Eingriffe bedingte
Komplikationen
Skelettmuskulatur-, Arthralgie Sehr häufig (14.2) 1.0
Bindegewebs- und Knochenerkran
kungen
Gutartige, bösartige und Zweite Primärmaligno Häufig 3.1
unspezifische Neubildungen mec
(einschl. Zysten und Polypen)
Erkrankungen des Nervensystems Kopfschmerzen Sehr häufig (12.1) 0.7
Periphere Neuropathiec Sehr häufig (13.6) 1.6
Schwindel Häufig 0.0
Erkrankungen der Nieren und Hämaturie Häufig 0.0
Harnwege
Erhöhte Kreatinin-Werte im Sehr häufig (23.1) 0.5
Blut
Erkrankungen der Atemwege, Epistaxis Häufig 0.0
des Brustraums und Mediastinum
s
Erkrankungen der Haut und des Hautausschlagb Sehr häufig (17.9) 1.1
Unterhautgewebes
Petechien Häufig 0.0
Gefässerkrankungen Hämatom Häufig 0.1
Blutungenc Sehr häufig (34.7) 2.8
Untersuchungen Calcium erniedrigt Sehr häufig (30.4) 1.3
Kalium erniedrigt Sehr häufig (15.4) 1.9
Natrium erniedrigt Sehr häufig (27.3) 0.7
Alkalische Phosphatase erhöht Sehr häufig (16.1) 0.3
Kalium erhöht Sehr häufig (14.1) 1.4
Stoffwechsel- und Ernährungsst Tumorlysesyndrom Gelegentlich 0.7
örungen
a Schweregradzuweisung basierend auf National Cancer Institute Common Terminology Criteria for Adverse Events (NCI CTCAE) Version 5.0.
b Umfasst mehrere Nebenwirkungsbegriffe.
c Der genannte Begriff umfasst weitere damit zusammenhängende Begriffe.
Beschreibung spezifischer unerwünschter Wirkungen und Zusatzinformationen
Lymphozytose
In der allgemeinen Sicherheitspopulation von Patienten der BRUIN-Studie, die eine tägliche Dosis von 200 mg erhalten haben, wurde bei 45% der gepoolten Sicherheitspopulation, nach Beginn mit Jaypirca ein vorübergehender Anstieg der Lymphozytenzahl beobachtet (definiert als ein Anstieg der absoluten Lymphozytenzahl ≥50% gegenüber dem Ausgangswert und ein Wert ≥5'000/μl nach Studienbeginn). Die mediane Zeit bis zum Beginn der Lymphozytose betrug 1.1 Wochen, wobei 75% der Fälle innerhalb von 1.3 Wochen aufgetreten waren, und die mediane Dauer betrug 15.0 Wochen.
Besondere Patientengruppen
Ältere Patienten
In der kombiniert ausgewerteten Sicherheitspopulation der Patienten mit malignen hämatologischen Erkrankungen waren 467 (66.3%) Patienten 65 Jahre oder älter, und 181 (25.7%) waren 75 Jahre oder älter. Patienten im Alter von 65 Jahren oder älter berichteten höhere Raten von Nebenwirkungen Grad 3 oder höher, und höhere Raten von schwerwiegenden Nebenwirkungen im Vergleich zu Patienten unter 65 Jahre.
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von grosser Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdacht einer neuen oder schwerwiegenden Nebenwirkung über das Online-Portal ElViS (Electronic Vigilance System) anzuzeigen. Informationen dazu finden Sie unter www.swissmedic.ch.
Überdosierung
Im Fall einer Überdosierung ist eine angemessene, unterstützende Behandlung einzuleiten. Es gibt kein bekanntes Antidot für eine Überdosierung von Pirtobrutinib.
Eigenschaften/Wirkungen
ATC-Code
L01EL05
Wirkungsmechanismus
Pirtobrutinib ist ein reversibler, nicht-kovalenter Inhibitor von BTK (Bruton's tyrosine kinase). BTK ist ein Signalprotein des B-Zell-Antigenrezeptors (BCR) und des Zytokinrezeptorweges. In B-Zellen führt die BTK-Signalgebung zur Aktivierung von Signalwegen, die für die Proliferation, den Transport, die Chemotaxis und die Adhäsion von B-Zellen erforderlich sind. Pirtobrutinib bindet sowohl an die Wildtyp-BTK als auch an die BTK mit C481-Mutationen, was zu einer Hemmung der BTK-Kinase-Aktivität führt. In nicht-klinischen Studien hemmte Pirtobrutinib die BTK-vermittelte B-Zell CD69-Expression und die Proliferation maligner B-Zellen. Pirtobrutinib zeigte eine dosisabhängige Hemmung des Tumorwachstums und induzierte eine Tumorregression in BTK-Wildtyp- und BTK-C481S-Mutanten-Maus-Xenotransplantatmodellen.
Pharmakodynamik
Bei empfohlener Dosierung von 200 mg einmal täglich waren die Talwerte der Pirtobrutinib-Konzentration höher als die BTK-IC96. Die BTK-Belegung blieb während des Dosierungsintervalls erhalten, unabhängig von der intrinsischen Rate des BTK-Umsatzes.
Kardiale Elektrophysiologie
Die Wirkung einer Einzeldosis von 900 mg Pirtobrutinib auf das QTc-Intervall wurde in einer Studie mit Placebo und Positivkontrollen bei 30 gesunden Probanden untersucht. Die gewählte Dosis entspricht etwa dem 2-Fachen der Konzentrationen, die im Steady-State bei der empfohlenen Dosierung von 200 mg einmal täglich erreicht werden. Pirtobrutinib hatte keinen klinisch relevanten Einfluss auf die Veränderung des QTcF-Intervalls (d.h. >10 ms). Es gab keinen Zusammenhang zwischen der Pirtobrutinib-Exposition und der Veränderung des QTc-Intervalls.
Klinische Wirksamkeit
Mantelzelllymphom
Die Wirksamkeit von Jaypirca bei Patienten mit MCL wurde in der BRUIN-Studie [NCT03740529] untersucht, einer offenen, internationalen, einarmigen Studie mit Jaypirca in Monotherapie. Die Wirksamkeit basierte auf 120 Patienten mit MCL, die zuvor einen BTK-Inhibitor erhalten hatten, und mit Jaypirca behandelt wurden. Jaypirca wurde oral in einer Dosierung von 200 mg einmal täglich gegeben, und fortgesetzt bis zum Progress oder nicht-akzeptablen Toxizität. Patienten mit Lymphom mit aktiver Beteiligung des zentralen Nervensystems oder allogenetischer hämatopoetischer Stammzelltransplantation (HSCT) oder CAR-T-Zelltherapie innerhalb von 60 Tagen wurden ausgeschlossen.
Das mediane Alter betrug 71 Jahre (Bereich: 46 bis 88 Jahre); 79% waren Männer; 78% waren weisser, 14% asiatischer, 1.7% schwarzer oder afroamerikanischer Herkunft. 78% hatten die klassische/leukämische Variante des MCL, 12% ein pleomorphes MCL und 11% ein blastoides MCL. Der vereinfachte MCL International Prognostic Index (sMIPI)-Score war bei 15% niedrig, bei 59% im mittleren Bereich und bei 26% der Patienten hoch. Die Patienten hatten zuvor median 3 Therapielinien erhalten (Bereich: 1 bis 9), 93% hatten zuvor 2 oder mehr Linien erhalten. Alle hatten zuvor 1 oder mehrere Linien mit einem BTK-Inhibitor erhalten; zu den anderen vorausgegangenen Therapien gehörten eine Chemoimmunotherapie bei 88%, HSCT bei 20%, Lenalidomid bei 18% und CAR-T-Therapie bei 9%. Die häufigsten zuvor erhaltenen BTK-Inhibitoren waren Ibrutinib (67%), Acalabrutinib (30%) und Zanubrutinib (8%); 83% der Patienten hatten den letzten BTK-Inhibitor aufgrund refraktärer Erkrankung oder Progress abgebrochen, 10% aufgrund von Toxizität und 5% aus anderen Gründen.
Die Wirksamkeit basierte auf dem Gesamtansprechen (overall response rate, ORR) und der Ansprechdauer (duration of response, DOR), und wurde durch ein unabhängiges Review-Komitee (IRC) anhand der 2014 Lugano-Kriterien beurteilt.
Bei 120 für die Wirksamkeit geeigneten Patienten betrug die ORR 50%, (95% CI: 41, 59), einschliesslich 13% mit vollständigem Ansprechen (complete response, CR).
Die Zeit bis zum Ansprechen betrug 1.8 Monate (95% CI: 0.8, 4.2) und die Ansprechdauer 8.3 Monate (95% CI: 5.7, NE).
Zudem betrug die Kaplan-Meier Schätzung für die DOR-Rate nach 6 Monaten 65.3% (95% CI: 49.8, 77.1).
Chronische lymphatische Leukämie
Die Wirksamkeit von Jaypirca bei 189 Patienten, die zuvor mindestens zwei Behandlungslinien einschliesslich einem BTK-Inhibitor erhalten hatten, wurde in einer randomisierten, multizentrischen, internationalen, offenen, aktiv kontrollierten Studie (BRUIN CLL-321, Studie 20020) untersucht. Die Patienten wurden im Verhältnis 1:1 randomisiert auf Jaypirca einmal täglich oral in einer Dosis von 200 mg bis zum Progress oder nicht-akzeptablen Toxizität, oder in den Kontrollarm mit einer der folgenden 2 Behandlungsoptionen nach Wahl des Studienarztes:
-Idelalisib plus Rituximab-Produkt (IR): Idelalisib 150 mg zweimal täglich oral bis zum Progress oder nicht-akzeptablen Toxizität, in Kombination mit 8 Infusionen eines Rituximab-Produkts (375 mg/m2 intravenös an Tag 1 von Zyklus 1, gefolgt von 500 mg/m2 alle 2 Wochen für 4 Anwendungen und dann alle 4 Wochen für 3 Anwendungen), bei einem 28-Tage-Zyklus.
-Bendamustin plus Rituximab-Produkt (BR): Bendamustin 70 mg/m2 intravenös (Tag 1 und 2 eines 28-Tage-Zyklus), in Kombination mit einem Rituximab-Produkt (375 mg/m2 intravenös an Tag 1 von Zyklus 1, gefolgt von 500 mg/m2 an Tag 1 der folgenden Zyklen), für bis zu 6 Zyklen.
Die Studie schloss Patienten aus bei bekannter oder vermuteter Richter-Transformation, aktiver Beteiligung des Zentralnervensystems (ZNS) durch Lymphome, signifikanter Herz-Kreislauf-Erkrankung einschliesslich unkontrollierter oder symptomatischer Arrhythmien, schwerer Blutung bei vorheriger Behandlung mit einem kovalenten BTK-Inhibitor, arzneimittelinduzierter Pneumonitis, arzneimittelinduzierter Leberschädigung, Leberzirrhose und/oder extrahepatischen Obstruktionen, aktiven Infektionen (Hepatitis B oder C, CMV, HIV oder anderen klinisch relevanten Infektionen), vorausgegangener allogener oder autologer Stammzelltransplantation oder CAR-T-Therapie in den letzten 60 Tagen, oder Impfung mit einem Lebendimpfstoff in den letzten 28 Tagen.
Die Randomisierung war stratifiziert nach 17p-Deletion-Status (Ja/Nein) und vorheriger Behandlung mit Venetoclax (Ja/Nein).
Von den 189 Patienten wurden 98 einer Jaypirca Monotherapie zugeordnet, 64 erhielten IR und 27 erhielten BR. Nach Bestätigung des Progresses hatten auf IR oder BR randomisierte Patienten die Möglichkeit, in die Jaypirca Monotherapie zu wechseln (Cross-over). Das mediane Alter betrug 67 Jahre (Bereich: 42 bis 90 Jahre), 69% waren Männer und 83% waren weiss. Der ECOG-Performance-Status zu Beginn betrug 0 oder 1 bei 95% der Patienten, 50% der Patienten hatten ein RAI-Stadium III oder IV. 46% (87 von 189 Patienten) hatten eine 17p-Deletion und/oder TP53-Mutation, 72% (137 von 189 Patienten) hatten ein unmutiertes IGHV und 45% (85 von 189) hatten einen komplexen Karyotyp.
Die Patienten hatten zuvor median 3 Behandlungslinien erhalten (Bereich: 2 bis 13), wobei 71% zuvor mindestens 3 Behandlungslinien erhalten hatten und 63% zuvor einen BCL2-Inhibitor. Die am häufigsten zuvor verwendeten BTK-Inhibitoren war Ibrutinib (89%), Acalabrutinib (16%) und Zanubrutinib (7%). 74% der Patienten hatten den letzten BTK-Inhibitor aufgrund refraktärer Erkrankung oder Progress abgebrochen, 16% aufgrund von Toxizität und 10% aus anderen/fehlenden Gründen.
Die Wirksamkeit basierte auf dem PFS, beurteilt durch ein unabhängiges Komitee (IRC). Tabelle 5 zeigt die Wirksamkeitsergebnisse für die 189 Patienten die zuvor mindestens zwei Behandlungslinien einschliesslich einem BTK-Inhibitor erhalten hatten, nach einer medianen Beobachtungszeit von 19.4 Monaten (Bereich 0.03 bis 33.3 Monate) für Pirtobrutinib und 17.7 Monate (Bereich 0.03 bis 25.0 Monate) im Kontrollarm.
Tabelle 5: Wirksamkeitsergebnisse gemäss IRC für Patienten mit CLL und vorheriger Behandlung mit mindestens zwei Behandlungslinien einschliesslich einem BTK-Inhibitor (Studie 20020), Cut-off: August 2024
Pirtobrutinib 200 mg Idelalisib plus Rituximab oder Bendamustin plus
einmal täglich (N=98) Rituximab nach Wahl des Studienarztes (N=91)
Progressionsfreies
Überleben (PFS)a
Anzahl Ereignisse, n 64 (65%) 66 (72%)
Progress 53 (54%) 54 (59%)
Tod 11 (11%) 12 (13%)
Medianes PFS (95% 13.9 (11.1, 16.5) 8.3 (5.8, 9.0)
CI), Monateb
HR (95% CI) c 0.45 (0.31, 0.65)
CI, confidence interval, Konfidenzintervall; HR, Hazardratio.
a Beurteilung der Wirksamkeit unter Verwendung der 2018-iwCLL-Leitlinien (International Workshop for Chronic Lymphocytic Leukemia guidelines 2018)
b Auf Basis einer Kaplan-Meier-Schätzung.
c Auf Basis eines stratifizierten Cox-proportional-Hazards-Modells.
Von den 189 Patienten und bei einer medianen Beobachtungszeit für das Gesamtüberleben (overall survival, OS) von 20.5 Monaten für Pirtobrutinib und 19.2 Monaten im Kontrollarm starben 33 Patienten (33.7%) mit Pirtobrutinib und 29 Patienten (31.9%) im Kontrollarm. Das mediane OS betrug 29.7 Monate (95% CI: 26.3, NE) für Pirtobrutinib und war nicht erreicht im Kontrollarm. Die HR betrug 1.021 (95% CI: 0.618, 1.688). Die OS-Auswertung kann durch 41 von 91 Patienten verzerrt worden sein, die aus dem Kontrollarm zu Pirtobrutinib gewechselt sind (Cross-over). Zusatzlich zeigt die Abbildung 1 das OS beider Therapieoptionen im Kontrollarm (IR und BR) separat.
Abbildung 1: Kaplan-Meier-Kurve für das OS bei Patienten mit CLL und vorausgegangener Behandlung mit mindestens zwei Therapielinien, einschliesslich einem BTK-Inhibitor – Studie 20020, Cut-off August 2024
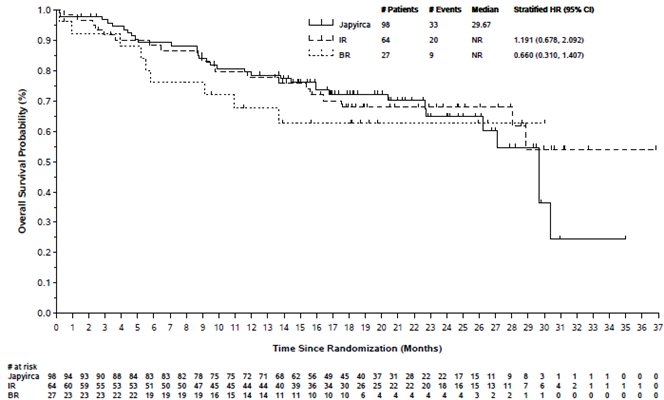
Pharmakokinetik
Die Pharmakokinetik von Pirtobrutinib wurde bei gesunden Probanden und bei Patienten mit maligner Erkrankung beschrieben. Nach Einmalgabe von 300 mg bis 800 mg oral (das 1.5- bis 4-Fache der zugelassenen empfohlenen Dosierung) und nach einmal täglichen Anwendungen von Dosierungen im Bereich von 25 – 300 mg (das 0.125- bis 1.5-Fache der empfohlenen Dosierung) stiegen Exposition (AUC) und Cmax von Pirtobrutinib proportional. Das Steady state wurde innerhalb von 5 Tagen mit einmal täglicher Anwendung erreicht, die mittlere (CV%) Akkumulationsrate betrug 1.63 (26.7%) auf Basis der AUC nach Gabe einer Dosis von 200 mg. Nach Anwendung der empfohlenen Dosis betrugen die geometrischen Mittelwerte (CV%) der AUC und Cmax von Pirtobrutinib im Steady state 92'600 h*ng/ml (39%) und 6'500 ng/ml (25%). Die geometrischen Mittelwerte (CV%) der AUC0-24 und Cmax von Pirtobrutinib im Zyklus 1 Tag 8 betrugen 81'800 h*ng/ml (66.6%) und 3'670 ng/ml (89.5%).
Absorption
Die absolute Bioverfügbarkeit von Pirtobrutinib nach einer oralen Einzeldosis von 200 mg betrug bei gesunden Probanden 85.5%. Die mediane Zeit bis zum Erreichen der maximalen Plasmakonzentration (tmax) betrug bei Patienten mit Krebserkrankung und auch bei gesunden Probanden etwa 2 Stunden.
Einfluss von Nahrung
Bei gesunden Probanden verringerte eine fettreiche, kalorienreiche Mahlzeit die Cmax von Pirtobrutinib um 23% und verzögerte die tmax um 1 Stunde. Es gab keine Auswirkung auf die AUC von Pirtobrutinib.
Distribution
Das mittlere scheinbare zentrale Verteilungsvolumen von Pirtobrutinib beträgt bei Patienten mit Krebserkrankung 34.2 l. Die Plasmaproteinbindung beträgt 96% und war zwischen 0.5 und 50 µM konzentrationsunabhängig. Das mittlere Blut-zu-Plasma Verhältnis beträgt 0.79.
Metabolismus
Der Metabolismus von Pirtobrutinib erfolgt in-vitro überwiegend durch CYP3A4 und direkter Glucuronidierung durch UGT1A8 und UGT1A9.
Elimination
Die mittlere scheinbare Clearance von Pirtobrutinib beträgt 2.05 l/h bei einer effektiven Halbwertszeit von etwa 19 Stunden. Bei gesunden Probanden wurden nach einer radioaktiv markierten Einzeldosis von 200 mg Pirtobrutinib 37% der Dosis im Stuhl (18% unverändert) und 57% im Urin (10% unverändert) wiedergefunden.
Kinetik spezieller Patientengruppen
Alter, Geschlecht und Körpergewicht
Basierend auf einer populationspharmakokinetischen Analyse bei Patienten mit Krebserkrankung hatten Alter (Bereich 22–95 Jahre), Geschlecht (523 Männer und 257 Frauen), Körpergewicht (Bereich 35.7–152 kg) und Herkunft (weiss 84%, asiatisch 8%) keine klinisch relevante Auswirkung auf die Pirtobrutinib-Exposition.
Die Auswirkungen anderer Herkünfte oder ethnischer Abstammungen auf die Pharmakokinetik von Pirtobrutinib sind nicht bekannt.
Leberfunktionsstörungen
In einer Studie zu Leberfunktionsstörungen zeigte eine Leberfunktionsstörung (Child-Pugh A, B und C) keine klinisch relevanten Auswirkungen auf die Pharmakokinetik von Pirtobrutinib im Vergleich zu normaler Leberfunktion.
In einer populationspharmakokinetischen Analyse bei Patienten mit Krebs gab es keine klinisch signifikanten Unterschiede in der Pharmakokinetik von Pirtobrutinib bei Patienten mit leichter (Gesamtbilirubin = obere Grenze des Normalbereichs (ULN) und Aspartataminotransferase (AST)>ULN oder Gesamtbilirubin >1 bis 1,5×ULN und jeder AST), mässiger (Gesamtbilirubin >1.5 bis 3×ULN und jeder AST), oder schwerer (Gesamtbilirubin >3×ULN und jeder AST) Leberfunktionsstörung.
Nierenfunktionsstörungen
Nach Einmalgabe von 200 mg oral bei Patienten mit schwerer Nierenfunktionsstörung (eGFR 15-29 ml/min) stieg die AUC von Pirtobrutinib um 62% und die mittlere ungebundene AUC um 68% im Vergleich zu gesunden Probanden mit normaler Nierenfunktion. Bei Teilnehmern mit leichter (eGFR 60-89 ml/min) oder mittelschwerer (eGFR 30-59 ml/min) Nierenfunktionsstörung zeigten sich keine klinisch relevanten Unterschiede in der Pharmakokinetik von Pirtobrutinib. Die Auswirkungen einer dialysepflichtigen Nierenfunktionsstörung auf die Pharmakokinetik von Pirtobrutinib sind nicht bekannt.
Präklinische Daten
Sicherheitspharmakologie / Toxizität nach wiederholter Gabe
Die Studien mit wiederholter Gabe zur Charakterisierung der Toxizität wurden bei Ratten und Hunden durchgeführt. Wichtige Auswirkungen bei Ratten und Hunden waren verminderte Grösse, Gewicht oder Zellularität der Lymphorgane sowie Verminderung von B-Lymphozyten und anderen Markern der Immunsystemfunktion. Minimale bis leichte Hornhautläsionen wurden nur bei Hunden beobachtet. Leichte bis mittelstarke vaskuläre Nekrosen sowie vaskuläre/perivaskuläre Entzündung grosser pulmonaler Blutgefässe wurden nur bei Ratten beobachtet. Diese Wirkungen traten bei klinisch relevanten Expositionsniveaus auf.
Karzinogenität
Mit Pirtobrutinib wurden keine Studien zur Karzinogenität durchgeführt.
Genotoxizität
Pirtobrutinib war in einem bakteriellen Mutagenitätstest (Ames) nicht mutagen. Pirtobrutinib war in in-vitro Mikronukleus-Tests mit humanen peripheren Blutlymphozyten aneugen. Pirtobrutinib zeigte keine Wirkung in einem in-vivo Mikronukleus-Test im Knochenmark von Ratten.
Reproduktionstoxizität
In einer tierexperimentellen Reproduktionsstudie führte die Gabe von Pirtobrutinib an trächtige Ratten während der Organogenese zu nachteiligen Entwicklungsergebnissen, einschliesslich struktureller Anomalien, verändertem fötalem Wachstum und embryofetaler Mortalität bei maternalen Expositionen, die etwa 3-mal höher waren im Vergleich zu Patientinnen bei der empfohlenen Tagesdosis von 200 mg.
Sonstige Hinweise
Haltbarkeit
Das Arzneimittel darf nur bis zu dem auf der Packung mit "EXP" bezeichneten Datum verwendet werden.
Besondere Lagerungshinweise
Nicht über 30°C lagern.
In der Orignialverpackung aufbewahren.
Ausser Reichweite von Kindern aufbewahren.
Zulassungsnummer
68733 (Swissmedic)
Packungen
Jaypirca 50 mg Filmtabletten, Blister: 28 (A)
Jaypirca 50 mg Filmtabletten, Flasche: 30 (A)
Jaypirca 100 mg FilmTabletten, Blister: 28, 56 (A)
Jaypirca 100 mg FilmTabletten, Flasche: 30, 60 (A)
Zulassungsinhaberin
Eli Lilly (Suisse) SA, Vernier/Genève
Stand der Information
Juli 2025