ZusammensetzungWirkstoffe
Hepatitis B-Oberflächenantigen (HBsAg).
Hergestellt in Hefezellen (Saccharomyces cerevisiae) durch rekombinante DNA-Technologie
Hilfsstoffe
Aluminiumhydroxid (wasserhaltiges, zur Adsorption), Natriumchlorid, Natriummonohydrogenphosphat-Dihydrat, Natriumdihydrogenphosphat-Dihydrat, Wasser für Injektionszwecke
Gesamtnatriumgehalt:
Engerix-B 10: 1.75 mg
Engerix-B 20: 3.52 mg
Indikationen/AnwendungsmöglichkeitenEngerix-B wird zur aktiven Immunisierung gegen Infektionen mit Hepatitis B-Viren (HBV) aller bekannten Subtypen bei nicht-immunen Personen gemäss den Empfehlungen des Bundesamtes für Gesundheit eingesetzt.
Die Hepatitis D tritt nur in Verbindung mit einer Hepatitis B-Infektion auf, somit schützt eine Impfung auch vor der Hepatitis D.
Die Impfung ist für alle nicht immunen Personen angezeigt, besonders für solche, die einem erhöhten Infektionsrisiko ausgesetzt sind. Die Impfung ist von Geburt an in jedem Lebensalter möglich.
Eine begonnene Grundimmunisierung mit konventionellen aus Plasma gewonnenen oder biotechnologisch hergestellten Impfstoffen kann mit Engerix-B fortgesetzt werden, ebenso ist eine Auffrischung mit Engerix-B nach Grundimmunisierung mit aus Plasma-/biotechnologisch hergestelltem Impfstoff möglich.
Dosierung/AnwendungGrundimmunisierung
Je nach Alter der zu impfenden Person können folgende Dosierungsschemata verwendet werden:
|
Alter
|
Impfschema
|
Schnellimpfschemata / Bemerkungen
| |
ab Geburt bis zum 16. Geburtstag
|
3 Dosen Engerix-B 10:
1. Dosis: zu Beginn der Impfserie
2. Dosis: 1 Monat später
3. Dosis: 6 Monate nach der 1. Dosis
|
In Fällen, wo ein möglichst schneller Impfschutz wünschenswert ist, mit 4 Dosen Engerix-B 10:
1. Dosis: zu Beginn der Impfserie
2. Dosis: 1 Monat später
3. Dosis: 2 Monate nach der 1. Dosis
4. Dosis: 12 Monate nach der 1. Dosis
| |
11. Geburtstag bis zum 16. Geburtstag
|
2 Dosen Engerix-B 20:
1. Dosis: zu Beginn der Impfserie
2. Dosis: 6 Monate später
|
In klinischen Studien wurde ein Zeitintervall von 6 bis 12 Monaten zwischen den beiden Impfdosen untersucht.
| |
ab dem 16. Geburtstag
|
3 Dosen Engerix-B 20:
1. Dosis: zu Beginn der Impfserie
2. Dosis: 1 Monat später
3. Dosis: 6 Monate nach der 1. Dosis
|
In Fällen, wo ein möglichst schneller Impfschutz wünschenswert ist, mit 4 Dosen Engerix-B 20:
1. Dosis: zu Beginn der Impfserie
2. Dosis: 1 Monat später
3. Dosis: 2 Monate nach der 1. Dosis
4. Dosis: 12 Monate nach der 1. Dosis
| |
ab dem 18. Geburtstag
|
|
Alternatives Schnell-Impfschema ab dem 18. Geburtstag:
1. Dosis: zu Beginn der Impfserie
2. Dosis: 7 Tage später
3. Dosis: 21 Tage nach der 1. Dosis
4. Dosis: 12 Monate nach der 1. Dosis
|
Engerix-B 20 kann bei Jugendlichen ab dem 11. Geburtstag bis zum 16. Geburtstag in einem 2-Dosen-Schema gegeben werden und zwar in Situationen, wo ein relativ kleines Risiko einer Hepatitis B-Infektion während des Impfkurses besteht und wenn die Compliance während des gesamten Impfkurses gesichert werden kann.
Auffrischimpfung
Nach derzeitiger Datenlage ist eine Auffrischimpfung bei immunkompetenten Personen, die auf die komplette Grundimmunisierung angesprochen haben, nicht angezeigt (BAG-Empfehlung, Lancet 2000, 333: 561). Dennoch sollte bei immundefizienten Personen (z.B. Personen mit chronischem Nierenversagen, Hämodialyse und HIV-positive Personen) eine Auffrischimpfung verabreicht werden, um einen Anti-HBs-Antikörpertiter zu gewährleisten, der über dem einen Impfschutz gewährenden Titer von 10 IE/l liegt. Bei immundefizienten Personen wird eine Überprüfung des Immunstatus alle 6-12 Monate nach der Impfung empfohlen.
|
Immunantwort
|
Auffrischimpfung
|
Nachträgliche Anti-HBs-Antikörperbestimmung(en)
| |
Non-/ Hyporesponder:
Anti-HBs <100 mI.E./ml nach 3 Dosen1
|
1.unmittelbare Auffrischimpfung
2.Wenn nach der Auffrischimpfung Anti-HBs nach wie vor unter 100 mI.E./ml: Auffrischimpfungen alle 6 bis 12 Monate (je nach Exposition)².
|
1 Monat nach jeder Auffrischimpfung
|
1 Non- und Hyporesponder unter den im Gesundheitsbereich tätigen Personen sind über das erhöhte Hepatitis B-Risiko nach Exposition zu informieren. Die betreffenden Personen sollten ermutigt werden, entsprechende Ereignisse unverzüglich dem Personalarzt zu melden und sich einer passiven Immunisierung zu unterziehen.
2 Lassen sich nach der 1. Auffrischimpfung (d.h. nach 4 Dosen) überhaupt keine Anti-HBs nachweisen, muss abgeklärt werden, ob nicht eine HBV-Infektion vorbesteht (Bestimmung von HBsAg und Anti-HBc).
Wenn die Anti-HBs-Antikörperkonzentration nach 3 Auffrischimpfungen kleiner als 10 mI.E./ml ist, sollte die Indikation für zusätzliche Dosen individuell gestellt werden.
Bei Personen mit bekannter Immunsuppression, die häufig eine ungenügende Immunantwort aufzeigen, können mehrere Nachimpfungen innerhalb kurzer Zeit (2 bis 3 im Abstand von 1 bis 2 Monaten) in Betracht gezogen werden, bevor eine Anti-HBs-Kontrolle veranlasst wird.
Spezielle Dosierungsanweisung
Patienten im 16. Lebensjahr und älter mit Niereninsuffizienz und Hämodialyse-Patienten
Das Schema einer Grundimmunisierung für Patienten mit Niereninsuffizienz und Hämodialyse-Patienten besteht aus vier doppelten Dosen (2× 20 μg) zu gewähltem Zeitpunkt 1 Monat, 2 Monate und 6 Monate nach dem Zeitpunkt der 1. Dosis. Zur Sicherstellung eines Impfschutzes mit HBs-Antikörpertitern von mindestens 10 IE/l oder höher sollte das Immunisierungs-Schema angepasst werden.
1. Dosis: zu Beginn der Impfserie
2. Dosis: 1 Monat später
3. Dosis: 2 Monate nach der 1. Dosis
4. Dosis: 6 Monate nach der 1. Dosis
Der Antikörpertiter dieser Personen soll regelmässig überprüft werden, und eine Boosterdosis ist empfohlen, wenn der Titer auf 10 mI.E./ml gesunken ist.
Dosierungsempfehlung für Neugeborene von HBsAg-positiven Müttern
Die Immunisierung dieser Neugeborenen mit Engerix-B 10 (10 µg) sollte unmittelbar nach der Geburt beginnen. Zwei Impfschemata sind bereits zur Anwendung gekommen. Es kann sowohl das 0/1/2/12- als auch das 0/1/6-Monatsschema verwendet werden, wobei ersteres eine raschere Immunantwort ermöglicht. Soweit verfügbar, empfiehlt sich die gleichzeitige Gabe (kontralateral) von Hepatitis B-Immunglobulinen mit der ersten Impfung, um einen optimalen Schutz zu gewährleisten.
Dosisempfehlung bei erfolgter oder Verdacht auf erfolgte HBV-Exposition
Bei kürzlich erfolgter HBV-Exposition (z.B. nach Verletzung mit einer kontaminierten Nadel) kann die erste Dosis Engerix-B gleichzeitig mit Hepatitis B-Immunglobulinen verabreicht werden, allerdings müssen die Injektionen an verschiedenen Stellen vorgenommen werden. Es wird empfohlen, das schnellere Impfschema anzuwenden (0/1/2/12).
Art der Anwendung
Engerix-B wird intramuskulär injiziert. Bei Erwachsenen und älteren Kindern erfolgt die Injektion in den Deltamuskel, bei jüngeren Kindern und Neugeborenen anterolateral am Oberschenkel.
In Ausnahmefällen (z.B. bei Patienten mit starker Blutungsneigung, wie Hämophilie oder Thrombozytopenie) kann der Impfstoff subkutan injiziert werden.
Eine intradermale Verabreichung oder die Injektion in die Glutealmuskulatur sollten unterbleiben, da diese Applikationswege möglicherweise zu einer nicht-optimalen Immunantwort führen können.
KontraindikationenÜberempfindlichkeit (Allergie) gegen eine der im Impfstoff enthaltenen Substanzen sowie aufgetretene Überempfindlichkeit nach einer bereits erfolgten Engerix-B-Impfung.
Im Falle einer akuten, mit Fieber einhergehenden Infektionskrankheit sollte die Impfung mit Engerix-B aufgeschoben werden. Leichte Infekte sowie eine HIV-Infektion stellen hingegen keine Kontraindikation für eine Impfung dar.
Warnhinweise und VorsichtsmassnahmenEngerix-B darf unter keinen Umständen intravenös injiziert werden!
Besonders bei Jugendlichen kann es als psychogene Reaktion auf die Nadelinjektion nach oder sogar vor einer Impfung zu einer Synkope (Ohnmacht) kommen. Diese kann während der Erholungsphase von verschiedenen neurologischen Symptomen wie vorübergehende Sehstörung, Parästhesie und tonisch-klonische Bewegungen der Gliedmassen begleitet sein. Es ist wichtig, Massnahmen zu ergreifen, um Verletzungen durch die Ohnmacht zu verhindern.
Bedingt durch die lange Inkubationszeit des Hepatitis B-Virus ist es möglich, dass eine unerkannte Infektion bereits zum Zeitpunkt der Impfung vorliegt. Engerix-B verhindert möglicherweise in solchen Fällen eine Hepatitis B nicht. Der Impfstoff verhindert eine Infektion, die durch andere Krankheitserreger verursacht wird, wie Hepatitis A, Hepatitis C und Hepatitis E sowie andere pathogene Keime, von denen man weiss, dass sie die Leber infizieren, nicht.
Wie bei allen Impfstoffen wird eine schützende Immunreaktion möglicherweise nicht bei allen Impflingen hervorgerufen.
Die Immunantwort auf Hepatitis B-Impfstoffe hängt von verschiedenen Faktoren, einschliesslich Alter, männlichem Geschlecht, Obesitas, Rauchergewohnheiten, Anwendungsort und einigen chronischen Grundkrankheiten ab. Für Impflinge, die weniger gut auf die Hepatitis B-Impfstoffe ansprechen (z.B. bei mehr als 40-Jährigen, usw.), können zusätzliche Dosen in Erwägung gezogen werden.
Die Fertigspritze enthält kein Konservierungsmittel.
Wie bei allen injizierbaren Impfstoffen soll eine Adrenalin-Lösung 1:1000 für den sofortigen Gebrauch im Falle einer anaphylaktischen Reaktion griffbereit sein.
Im Falle des Auftretens allergischer Reaktionen sind die dem Arzt bekannten Behandlungsmassnahmen einzuleiten.
Patienten mit chronischen Lebererkrankungen oder HIV oder Träger von Hepatitis C sollten nicht von der Impfung gegen Hepatitis B ausgeschlossen werden. Die Impfung sollte aufgrund der Schwere einer Hepatitis B-Infektion bei solchen Patienten empfohlen werden: Die Hepatitis B-Impfung sollte demnach in einer Fall-zu-Fall-Entscheidung durch den Arzt abgewogen werden. Patienten mit einer HIV-Infektion, Patienten mit Niereninsuffizienz und Patienten mit einem beeinträchtigten Immunsystem werden möglicherweise nach Komplettierung des ersten Impfschemas keine adäquaten Titer mit Anti-HBs-Antikörpern entwickeln. Diese Patienten benötigen daher möglicherweise zusätzliche Dosen des Impfstoffes.
Das potentielle Risiko von Apnoen und die Notwendigkeit einer Überwachung der Atmung über 48 – 72 Stunden sollte im Rahmen der Grundimmunisierung von sehr unreifen Frühgeborenen (geboren vor der vollendeten 28. Schwangerschaftswoche) in Betracht gezogen werden. Dies gilt insbesondere für diejenigen, die in der Vorgeschichte Zeichen einer Lungenunreife gezeigt haben.
Da der Nutzen der Impfung für diese Säuglingsgruppe hoch ist, sollte sie ihnen weder vorenthalten noch sollte sie verschoben werden.
Engerix-B enthält weniger als 1 mmol Natrium (23 mg) pro Dosis, d.h. es ist nahezu «natriumfrei».
InteraktionenDie gleichzeitige Verabreichung von Engerix-B mit einer Standarddosis von Hepatitis B-Immunglobulinen bewirkt keinen niedrigeren Anti-HBs-Antikörpertiter, vorausgesetzt, dass die Injektionen kontralateral verabreicht wurden.
Engerix-B darf gleichzeitig mit den folgenden Impfstoffen, aber stets an unterschiedlichen (kontralateralen) Injektionsstellen verabreicht werden: Polio-Impfstoff; DTP-, DT-Impfstoffe; Impfstoffe, die Masern-Mumps-Röteln-Komponenten enthalten; Haemophilus influenzae Typ b-, Hepatitis A- und Tuberkulose-(BCG-) Impfstoffe.
Engerix-B kann gleichzeitig mit einem Impfstoff gegen humane Papillomaviren (HPV) (Cervarix) verabreicht werden.
Bei der gleichzeitigen Verabreichung von Engerix-B und Cervarix zeigte sich keine klinisch relevante Beeinträchtigung der Antikörperantwort auf die HPV-Antigene. Die geometrischen mittleren Konzentrationen der Anti-HBs-Antikörper fielen bei der gleichzeitigen Verabreichung niedriger aus; die Seroprotektionsraten zeigten leichte Unterschiede. Die klinische Bedeutung dieser Beobachtung ist nicht bekannt. Den Einfluss von Cervarix auf die Responderraten und Anti-HBs-Antikörpertiter nach gleichzeitiger Verabreichung von Engerix-B zeigt die folgende Tabelle.
|
|
Cervarix zusammen mit Engerix-B
(N=194)
|
Engerix-B alleine
(N=181)
| |
Anteil Personen mit einer Anti-HBs-Antikörperkonzentration ≥10 mI.E./ml
|
97,9%
(n=190)
|
100%
(n=181)
| |
Anteil Personen mit einer Anti-HBs-Antikörperkonzentration ≥100 mI.E./ml
|
88,7%
(n=172)
|
97,2%
(n=176)
| |
Absolute Anti-HBs-Antikörperkonzentration in mI.E./ml
|
1'280,9
(973,3 - 1'685,7)*
|
3'107,7
(2'473,1 - 3'905,1)*
|
* 95%-Konfidenzintervall
Wenn Engerix-B zeitgleich mit einem anderen injizierbaren Impfstoff angewendet wird, sollten die Impfstoffe stets an verschiedenen Injektionsstellen verabreicht werden.
Engerix-B kann zur Beendigung einer Grundimmunisierung verwendet werden, die mit aus Blutplasma gewonnenen bzw. gentechnisch hergestellten Hepatitis B-Impfstoffen begonnen wurde. Wird eine Auffrischimpfung gewünscht, kann Engerix-B auch Personen verabreicht werden, die vorher eine Grundimmunisierung mit aus Plasma gewonnenen oder mit anderen, gentechnisch hergestellten Hepatitis B-Impfstoffen erhalten haben.
Schwangerschaft, StillzeitSchwangerschaft
Der Einfluss von HBsAg auf die Fötalentwicklung des Menschen wurde nicht untersucht. Wie bei allen inaktivierten Virusimpfstoffen ist jedoch keine Schädigung des Fœtus zu erwarten. Engerix-B sollte während der Schwangerschaft nur dann verabreicht werden, wenn die Impfung wirklich erforderlich ist und wenn die erwarteten Vorteile die möglichen Risiken für den Fœtus überwiegen.
Stillzeit
Die Auswirkung auf gestillte Säuglinge nach Verabreichung von Engerix-B an deren Mütter wurde in klinischen Studien nicht untersucht, da Informationen über das Vorhandensein des Impfstoffes oder seiner Bestandteile in der Muttermilch nicht vorliegen.
Die Stillzeit stellt keine Kontraindikation dar.
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von MaschinenEinige der unerwünschten Wirkungen können eine Auswirkung auf die Fahrtüchtigkeit oder die Fähigkeit zur Bedienung von Maschinen haben.
Unerwünschte WirkungenKlinische Studien
Die nachfolgend aufgeführten unerwünschten Wirkungen basieren auf Daten von mehr als 5'300 Probanden.
Die Häufigkeiten werden wie folgt angegeben:
«Sehr häufig» (≥1/10), «häufig» (≥1/100, <1/10), «gelegentlich» (≥1/1'000, <1/100), «selten» (≥1/10'000, <1/1'000), «sehr selten» (<1/10'000).
Erkrankungen des Blutes und des Lymphsystems
Selten: Lymphadenopathie.
Stoffwechsel- und Ernährungsstörungen
Gelegentlich: Appetitlosigkeit.
Psychiatrische Erkrankungen
Sehr häufig: Reizbarkeit (Engerix-B 10: 10,0%).
Erkrankungen des Nervensystems
Häufig: Kopfschmerzen (sehr häufig unter Engerix-B 10: 13,1%), Schläfrigkeit.
Gelegentlich: Schwindel.
Selten: Parästhesien.
Erkrankungen des Gastrointestinaltrakts
Gelegentlich: Gastrointestinale Störungen (wie Übelkeit, Erbrechen, Durchfall, Bauchschmerzen).
Erkrankungen der Haut und des Unterhautgewebes
Selten: Ausschlag, Juckreiz, Urtikaria.
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen
Gelegentlich: Myalgie.
Selten: Arthralgie.
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort
Sehr häufig: Schmerz (Engerix-B 20: 36,4%; Engerix-B 10: 15,2%) und Rötung an der Injektionsstelle (Engerix-B 20: 13,0%, Engerix-B 10: 17,2%), Müdigkeit (Engerix-B 20: 12,3%; Engerix-B 10: 12,6%).
Häufig: Schwellung an der Injektionsstelle, Unwohlsein, Reaktionen an der Injektionsstelle (wie Verhärtungen), Fieber (>37,5°C).
Gelegentlich: grippeähnliche Symptome.
Die Boosterdosis wird so gut vertragen wie die Impfdosen der Grundimmunisierung.
In einer Vergleichsstudie bei Personen im Alter von 11 bis und mit 15 Jahren war die Inzidenz von lokalen und allgemeinen berichteten Symptomen nach dem 2-Dosen-Schema mit 20 μg Engerix-B ähnlich derjenigen, die nach dem Standard 3-Dosen-Schema mit 10 μg Engerix-B berichtet wurde.
Unerwünschte Wirkungen nach Markteinführung
Infektionen und parasitäre Erkrankungen
Meningitis.
Erkrankungen des Blutes und des Lymphsystems
Thrombozytopenie.
Erkrankungen des Immunsystems
Anaphylaxie, allergische Reaktionen einschliesslich anaphylaktoide Reaktionen und Serumkrankheit-ähnliche Symptome.
Erkrankungen des Nervensystems
Paralyse, Konvulsionen, Hypoästhesie, Enzephalitis, Enzephalopathie, Neuropathie, Neuritis (einschliesslich Guillain-Barré-Syndrom, Opticus-Neuritis und Multiple Sklerose), Meningitis.
Gefässerkrankungen
Hypotension, Vaskulitis.
Erkrankungen der Atemwege, des Brustraums und Mediastinums
Apnoe bei sehr unreifen Frühgeborenen (geboren vor der vollendeten 28. Schwangerschaftswoche) (vgl. «Warnhinweise und Vorsichtsmassnahmen»).
Erkrankungen der Haut und des Unterhautgewebes
Angioödem, Lichen planus, Erythema multiforme.
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen
Arthritis, Muskelschwäche.
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von grosser Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdacht einer neuen oder schwerwiegenden Nebenwirkung über das Online-Portal ElViS (Electronic Vigilance System) anzuzeigen. Informationen dazu finden Sie unter www.swissmedic.ch.
ÜberdosierungNach Markteinführung wurden Fälle von Überdosierung berichtet. Die beobachteten unerwünschten Wirkungen nach Überdosierung sind vergleichbar mit denen nach vorschriftsmässiger Verabreichung des Impfstoffes.
Eigenschaften/WirkungenATC-Code
J07BC01
Wirkungsmechanismus
Siehe «Pharmakodynamik».
Pharmakodynamik
Engerix-B besteht aus hochgereinigtem Oberflächenantigen des Hepatitis B-Virus (HBsAg). Das HBsAg wird aus Kulturen von Hefezellen (Saccharomyces cerevisiae) gewonnen, die die genetische Information zur Bildung des Proteins exprimieren. Das Oberflächenantigen wird in einer Reihe von physikalisch-chemischen Schritten gereinigt, anschliessend an Aluminiumhydroxid adsorbiert und steht dann als Impfstoff zur aktiven Immunisierung zur Verfügung. Die Reinheit dieses Impfstoffes erfüllt die WHO-Anforderungen.
Dank dieser biotechnologischen Herstellungsmethode kann während der Produktion von Engerix-B auf die Verwendung von Bestandteilen humanen Ursprungs verzichtet werden. Übertragungen von Krankheitserregern sind bei der Engerix-B-Impfung ausgeschlossen, und eine gleichbleibende Qualität der einzelnen Chargen ist gewährleistet.
Klinische Wirksamkeit
Schutzwirkung
Antikörperkonzentrationen (Anti-HBs) ≥10 mI.E./ml gelten als protektiv.
In Feldstudien bei Neugeborenen, Kindern und Erwachsenen wurde eine Schutzwirkung zwischen 95% und 100% gezeigt.
Untenstehende Tabelle zeigt die Seroprotektionsraten (prozentualer Anteil geimpfter Personen mit schützendem Antikörpertiter), wie sie in klinischen Studien mit den angegebenen Dosierungsschemata beobachtet wurden:
|
Population
|
Schema
|
N
|
Seroprotektionsrate
(anti-HBs ≥10 mI.E./ml)
|
Seroprotektionsrate
(anti-HBs ≥100 mI.E./ml)
|
GMC
(mI.E./ml)
| |
Gesunde Personen
(16 Jahre alt und älter)
|
0, 1, 6 Monate
|
|
Monat 7: ≥96,0%
|
|
| |
|
0, 1, 2–12 Monate
|
|
Monat 1: 15,0%
Monat 3: 89,0%
Monat 13: 95,8%
|
|
| |
Gesunde Personen
(18 Jahre alt und älter)
|
0, 7, 21 Tage – 12 Monate
|
|
Tag 28: 65,2%
Monat 2: 76,0%
Monat 13: 98,6%
|
|
| |
Gesunde Personen
(11-15 Jahre alt)*
|
20 μg: 0, 6 Monate
|
240
|
Monat 2: 11,3%
|
2,1%
|
17,6
| |
|
|
239
|
Monat 6: 26,4%
|
2,1%
|
18,8
| |
|
|
241
|
Monat 7: 96,7%
|
88,8%
|
2'738,5
| |
|
|
140
|
Monat 30: 87,1%
|
59,3%
|
229,0
| |
|
|
166
|
Monat 42: 83,7%
|
56,6%
|
159,7
| |
|
|
147
|
Monat 54: 84,4%
|
55,1%
|
123,6
| |
|
|
132
|
Monat 66: 79,5%
|
43,9%
|
82,1
| |
|
10 μg: 0, 1, 6 Monate
|
113
|
Monat 2: 55,8%
|
11,5%
|
29,4
| |
|
|
113
|
Monat 6: 87,6%
|
46,0%
|
90,0
| |
|
|
113
|
Monat 7: 98,2%
|
97,3%
|
7'238,3
| |
|
|
64
|
Monat 30: 96,9%
|
78,1%
|
708,3
| |
|
|
80
|
Monat 42: 92,5%
|
71,3%
|
417,9
| |
|
|
76
|
Monat 54: 94,7%
|
67,1%
|
277,6
| |
|
|
70
|
Monat 66: 91,4%
|
68,6%
|
225,2
| |
Patienten mit beeinträchtigter Nierenfunktion einschliesslich Hämodialyse-Patienten (16 Jahre und älter)
|
0, 1, 2, 6 Monate
(je 2× 20 μg)
|
|
Monat 3: 55,4%
Monat 7: 87,1%
|
|
|
Das Datenmaterial dieser Tabelle stammt aus Untersuchungen mit Impfstoffen, die Thiomersal enthielten. Zwei zusätzliche klinische Studien bei gesunden Kindern und Erwachsenen mit der gegenwärtigen Zusammensetzung von Engerix-B, das kein Thiomersal enthält, zeigt vergleichbare Seroprotektionsraten zu den früheren, Thiomersal-enthaltenden Zusammensetzungen von Engerix-B.
* Die langfristige Immunantwort wurde in einer klinischen Studie an Probanden untersucht, die zum Zeitpunkt der Grundimmunisierung 11 bis einschliesslich 15 Jahre alt waren. Die mit den beiden verschiedenen Dosierungen und Impfschemata erzielten Seroprotektionsraten wurden über einen Zeitraum von bis zu 66 Monaten nach der ersten Dosis der Grundimmunisierung beurteilt.
Alle Probanden beider Impfgruppen erhielten 72 bis 78 Monate nach der Grundimmunisierung eine Booster-Dosis. Einen Monat später hatte sich bei allen Probanden eine anamnestische Antwort gebildet (108- bzw. 95-fache GMC-Erhöhung einen Monat nach der Booster-Dosis im Vergleich zum Zeitpunkt vor der Impfung, in den Gruppen mit dem 2-Dosen- bzw. 3-Dosen-Grundimmunisierungsschema) und eine Seroprotektion gezeigt. Diese Daten deuten darauf hin, dass ein Immungedächtnis bei allen Probanden, die auf die Grundimmunisierung ansprachen, induziert wurde, auch bei solchen, die im Monat 66 keine Seroprotektion mehr hatten.
|
Gruppe
|
Zeitpunkt
|
N
|
Responderrate
≥10 mI.E./ml
|
Responderrate
≥100 mI.E./ml
|
GMC
(mI.E./ml)
| |
Gruppe 1
(20 μg: 0, 6 Monate)
|
Vor Booster
|
53
|
77,4%
|
28,3%
|
57,7
| |
|
Ein Monat nach Booster
|
53
|
100%
|
94,3%
|
6'214,1
| |
Gruppe 2
(10 μg: 0, 1, 6 Monate)
|
Vor Booster
|
21
|
95,2%
|
52,4%
|
175,2
| |
|
Ein Monat nach Booster
|
21
|
100%
|
95,2%
|
16'564,3
| |
Gruppe 1 & Gruppe 2 kombiniert
|
Vor Booster
|
74
|
82,4%
|
35,1%
|
80,4
| |
|
Ein Monat nach Booster
|
74
|
100%
|
94,6%
|
8'207,6
|
Die langfristige Persistenz wurde in der offenen, unkontrollierten, klinischen Phase IV-Studie HBV-319 an Probanden (N = 292) im Alter von 15 bis 16 Jahren untersucht, die in ihren ersten beiden Lebensjahren mit 3 Dosen Engerix-B 10 immunisiert worden waren. Der primäre Endpunkt war die anti-HBs Antwort 31 Tage nach einer Booster Impfung mit Engerix-B 10 mit dem Anteil Personen, die eine Seroprotektionsrate von anti-HBs ≥100 mI.E./ml erreichten. Die anti-HBs-Seroprotektion ≥100 mI.E./ml betrug 14 Jahre (Spanne: 13,5–15,5 Jahre) nach der Grundimmunisierung 23.3%. Zu diesem Zeitpunkt erhielten alle Probanden eine Provokationsdosis Engerix-B 10. Einen Monat nach der Provokationsdosis zeigten 90.8% der Probanden eine Seroprotektion ≥100 mI.E./ml. Die folgende Tabelle zeigt die Daten inkl. der Seroprotektionsschwellen ≥10 mI.E./ml und ≥100 mI.E./ml jeweils vor und nach der Booster Impfung.
|
|
≥10 mI.E./ml
|
≥100 mI.E./ml
| |
|
|
95% CI
|
|
95% CI
| |
Antikörper
|
Zeitpunkt
|
N
|
n
|
%
|
LL
|
UL
|
n
|
%
|
LL
|
UL
| |
Anti-HBs-Antikörper
|
Prä-PD
|
292
|
191
|
65,4
|
59,6
|
70,9
|
68
|
23,3
|
18,6
|
28,6
| |
|
Post-PD
|
292
|
286
|
97,9
|
95,6
|
99,2
|
265
|
90,8
|
86,8
|
93,8
|
Prä-PD: = Vor Verabreichung der Provokationsdosis
Post-PD = Nach Verabreichung der Provokationsdosis
n = Anzahl der Probanden mit einer Konzentration von 10 mI.E./ml resp. 100 mI.E./ml oder mehr
% = Prozentsatz der Probanden mit einer Konzentration von 10 mI.E./ml resp. 100 mI.E./ml oder mehr
95% CI = 95% Konfidenzintervall; LL = Untergrenze, UL = Obergrenze
Bei Neugeborenen von HBeAg-positiven Frauen wurde bei Immunisierung nach dem 0/1/2-Monatsschema, gefolgt von einer Auffrischimpfung 12 Monate nach der 1. Dosis, ebenso wie nach dem 0/1/6-Monatsschema (ohne gleichzeitige Gabe von Hepatitis B-Immunglobulinen bei der Geburt) eine protektive Wirksamkeit von 95% beobachtet. Wurden jedoch gleichzeitig mit der 1. Impfung auch Hepatitis B-Immunglobuline gegeben, konnte eine Steigerung der protektiven Wirksamkeit auf 98% beobachtet werden.
Langfristig bewirkt die Immunisierung gegen Hepatitis B nicht nur eine Verringerung der Inzidenz der Krankheit selbst, sondern auch ihrer Komplikationen wie die chronisch aktive Hepatitis B und die posthepatitische Zirrhose. Nach einer nationalen Impfaktion gegen Hepatitis B konnte in Taiwan ein signifikanter Rückgang der Inzidenz des hepatozellulären Karzinoms bei Kindern im Alter von 6-14 Jahren festgestellt werden. Dies resultierte aus der starken Abnahme der Prävalenz von Hepatitis B-Antigenen als entscheidender Faktor für die Entwicklung des hepatozellulären Karzinoms.
PharmakokinetikFür Impfstoffe werden in der Regel keine Absorptions-, Distributions- oder Eliminations-Studien durchgeführt.
Absorption
Nicht zutreffend.
Distribution
Nicht zutreffend.
Metabolismus
Nicht zutreffend.
Elimination
Nicht zutreffend.
Präklinische DatenDie präklinischen Sicherheitsdaten erfüllen die WHO-Bestimmungen.
Sonstige HinweiseInkompatibilitäten
Engerix-B sollte nicht mit anderen Impfstoffen in derselben Spritze gemischt werden.
Haltbarkeit
Das Arzneimittel darf nur bis zu dem auf dem Behälter mit «EXP» bezeichneten Datum verwendet werden.
Engerix-B ist während drei Jahren vom Herstellungsdatum gerechnet voll wirksam, wenn der Impfstoff zwischen +2°C und +8°C aufbewahrt wird.
Besondere Lagerungshinweise
Im Kühlschrank (2°C bis 8°C) lagern. Nicht einfrieren. Den Behälter im Umkarton aufbewahren, um den Inhalt vor Licht zu schützen. Ausser Reichweite von Kindern aufbewahren.
Daten zur Stabilität deuten darauf hin, dass Engerix-B bei Temperaturen bis 37°C drei Tage lang, bei Temperaturen bis 25°C sieben Tage lang stabil ist. Diese Daten sollen dem medizinischen Fachpersonal als Richtwerte bei kurzzeitigen Temperaturabweichungen dienen.
Hinweise für die Handhabung
Bei der Lagerung kann sich eine feine weisse Ablagerung mit einem klaren, farblosen Überstand bilden. Der Impfstoff soll vor Gebrauch gut geschüttelt werden, um eine homogene weisslich-trübe Suspension zu erhalten. Zudem soll er vor Gebrauch visuell auf Fremdpartikel und/oder Veränderungen im Aussehen kontrolliert werden. Im Falle einer Veränderung ist der Impfstoff nicht zu verabreichen.
Gebrauchsanweisung für die Fertigspritze
|
|
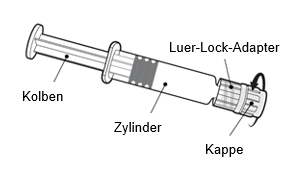
|
Halten Sie die Spritze am Zylinder, nicht am Kolben.
Schrauben Sie die Spritzenkappe ab, indem Sie sie gegen den Uhrzeigersinn drehen.
| |
|
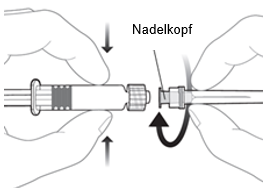
|
Um die Nadel an der Spritze anzubringen, verbinden Sie den Nadelkopf mit dem Luer-Lock-Adapter und drehen Sie die Nadel eine Vierteldrehung im Uhrzeigersinn, bis Sie spüren, dass sie einrastet.
Ziehen Sie den Spritzenkolben nicht aus dem Zylinder heraus. Sollte dies geschehen, verabreichen Sie den Impfstoff nicht.
|
Entsorgung
Nicht verwendeter Impfstoff oder Abfallmaterial ist entsprechend den lokalen Anforderungen zu entsorgen.
ZulassungsnummerEngerix-B 20: 00534 (Swissmedic)
Engerix-B 10: 00551 (Swissmedic)
PackungenEngerix-B 20
1 Packung mit 1 Fertigspritze (mit separater Nadel), vorgefüllt mit der Impfstoff-Suspension (20 µg/1 ml). (B)
1 Packung mit 10 Fertigspritzen (mit separaten Nadeln), vorgefüllt mit der Impfstoff-Suspension (20 µg/1 ml). (B)
Engerix-B 10
1 Packung mit 1 Fertigspritze (mit separater Nadel), vorgefüllt mit der Impfstoff-Suspension (10 µg/0,5 ml). (B)
ZulassungsinhaberinGlaxoSmithKline AG, 6340 Baar
Stand der InformationOktober 2024
|


