Sonstige HinweiseInkompatibilitäten
Glucosehaltige Lösungen dürfen nicht verwendet werden, da Cancidas in glucosehaltigen Lösungen nicht stabil ist. Cancidas darf nicht mit anderen Arzneimitteln gemischt oder zusammen mit diesen infundiert werden, da keine Daten zur Kompatibilität von Cancidas mit anderen intravenös applizierten Substanzen, Hilfsstoffen oder Arzneimitteln vorliegen. Die Infusionslösung ist auf sichtbare Partikel oder Verfärbung zu prüfen.
Haltbarkeit
Das Arzneimittel darf nur bis zu dem auf der Packung mit «EXP» bezeichneten Datum verwendet werden.
Haltbarkeit nach Anbruch
Stammlösung Cancidas: Kann bis zu 24 Stunden vor Zubereitung der Infusionslösung für den Patienten bei maximal 25°C gelagert werden.
Verdünnte Infusionslösung für den Patienten: Die verdünnte Infusionslösung für den Patienten kann in einem Infusionsbeutel oder –flasche bis zu 24 Stunden lang bei maximal 25°C oder bis zu 48 Stunden im Kühlschrank (2–8°C) gelagert werden.
Cancidas enthält keine Konservierungsstoffe. Aus mikrobiologischer Sicht sollte das Produkt sofort verwendet werden. Wird das Produkt nicht sofort verwendet, sollten die Aufbewahrungszeiten und -bedingungen vor dem Gebrauch die oben genannten Bedingungen nicht überschreiten.
Stabilität der rekonstituierten Lösung
Cancidas-Stammlösung: Die Lösung sollte sofort verwendet werden. Stabilitätsdaten haben gezeigt, dass die Infusionslösung für den Patienten 24 Stunden im Voraus zubereitet werden kann, wenn die Durchstechflasche nicht über 25°C aufbewahrt wird und die Rekonstitution mit Wasser für Injektionszwecke erfolgt.
Verdünnte Infusionslösung für den Patienten: Die Lösung muss sofort verwendet werden. Stabilitätsdaten haben gezeigt, dass das Produkt innerhalb von 24 Stunden verwendet werden kann, wenn es nicht über 25°C aufbewahrt wird, oder innerhalb von 48 Stunden, wenn der (die) Infusionsbeutel (-flasche) gekühlt (2-8°C) aufbewahrt wird und die Verdünnung mit 0,9%iger, 0,45%iger oder 0,225%iger Natriumchloridlösung für Injektionszwecke oder mit Ringer-Laktat-Lösung erfolgt.
Besondere Lagerungshinweise
Im Kühlschrank (2-8°C) lagern.
Ausser Reichweite von Kindern aufbewahren.
Hinweise für die Handhabung
Rekonstitution von Cancidas
Cancidas wird in zwei Schritten zubereitet. Im ersten Schritt wird aus dem lyophilisierten Pulver die Stammlösung zubereitet, aus welcher in einem zweiten Schritt die Infusionslösung hergestellt wird. Die Infusionslösung ist auf sichtbare Partikel oder Verfärbung zu prüfen.
Hinweise für erwachsene Patienten
1. Schritt: Zubereitung der Stammlösung:
Um das pulverisierte Arzneimittel aufzulösen, wird Cancidas in der gekühlten Durchstechflasche an die Raumtemperatur angeglichen. Unter aseptischen Bedingungen werden 10,5ml Wasser oder 0,9% Natriumchloridlösung für Injektionszwecke zugegeben. Die Konzentration der Lösung in der Durchstechflasche beträgt dann 7,2mg/ml (70-mg-Durchstechflasche) bzw. 5,2mg/ml (50-mg-Durchstechflasche).
Die weissliche Substanz löst sich völlig auf. Sie wird so lange vorsichtig gemischt, bis die Lösung klar ist. Diese Stammlösung ist auf sichtbare Partikel oder Verfärbung zu prüfen. Sie sollte aus mikrobiologischen Gründen sofort weiterverwendet werden, da Cancidas keine Konservierungsmittel enthält. Chemisch und physikalisch ist die Lösung bei ≤25°C bis zu 24 Stunden stabil. Nicht über 25°C lagern.
2. Schritt: Herstellung der Infusionslösung für den Patienten aus der Stammlösung:
Folgende Lösungen können für die gebrauchsfertige Infusionslösung, die dem Patienten verabreicht wird, verwendet werden: sterile physiologische Kochsalzlösung für Injektionszwecke oder Ringer-Laktat-Lösung. Unter aseptischen Bedingungen wird die entsprechende Menge der Cancidas-Stammlösung (siehe Tabelle 1) in eine(n) Infusionsbeutel oder –flasche mit 250ml Inhalt gegeben. Wenn es medizinisch notwendig ist, können Tagesdosen von 50mg oder 35mg auch in einem geringeren Infusionsvolumen von 100ml verabreicht werden. Sollte die Infusionslösung trüb sein oder Ausfällungen aufweisen, darf sie nicht verwendet werden. Die Infusionslösung sollte aus mikrobiologischen Gründen sofort verwendet werden, da Cancidas keine Konservierungsmittel enthält. Chemisch und physikalisch ist die Lösung bei ≤25°C bis zu 24 Stunden und im Kühlschrank (2–8°C) bis zu 48 Stunden stabil. Nicht über 25°C lagern. Cancidas sollte langsam intravenös über ca. 1 Stunde infundiert werden.
Werden Tagesdosen >70mg verabreicht, sollte die Infusion langsamer erfolgen (2 Stunden).
Tabelle 1: Herstellung der Infusionslösungen für den erwachsenen Patienten
|
Dosis*
|
Volumen der Cancidas-Stammlösung für die Zugabe in eine(n) Infusionsbeutel oder -flasche
|
Übliche Herstellung
(Zugabe der Cancidas-Stammlösung zu 250ml)
Endkonzentration
|
Volumenreduzierte Infusion
(Zugabe der Cancidas-Stammlösung zu 100ml)
Endkonzentration
| |
70mg
|
10ml
|
0,28mg/ml
|
Nicht empfohlen
| |
70mg
(aus zwei 50-mg-Durchstechflaschen)**
|
14ml
|
0,28mg/ml
|
Nicht empfohlen
| |
50mg
|
10ml
|
0,20mg/ml
|
0,47mg/ml
| |
35mg
für Patienten mit mässig eingeschränkter Leberfunktion
(aus einer 70-mg-Durchstechflasche)
|
5ml
|
0,14mg/ml
|
0,34mg/ml
| |
35mg
für Patienten mit mässig eingeschränkter Leberfunktion
(aus einer 50-mg-Durchstechflasche)
|
7ml
|
0,14mg/ml
|
0,34mg/ml
|
* 10,5ml sollten zur Auflösung des Pulvers für alle Durchstechflaschen verwendet werden.
** Sollte keine 70-mg-Durchstechflasche zur Verfügung stehen, kann die 70-mg-Dosis aus zwei 50-mg-Durchstechflaschen hergestellt werden.
Hinweise für die Anwendung bei Kindern und Jugendlichen
Berechnung der Körperoberfläche (BSA) für pädiatrische Dosierungen
Berechnen Sie vor der Zubereitung der Infusion die Körperoberfläche (BSA) des Patienten, indem Sie folgende Formel verwenden (Mosteller-Formel):
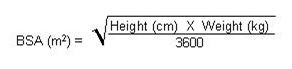
Zubereitung der 70mg/m2-Infusion für Kinder ≥3 Monate aus einer 70mg-Durchstechflasche:
1.Bestimmen Sie die Initialdosis, welche beim Kind angewendet werden soll, indem Sie die BSA des Patienten (wie oben berechnet) in folgender Gleichung einsetzen:BSA (m2) × 70mg/m2 = InitialdosisDie maximale Initialdosis am Tag 1 sollte nicht höher sein als 70mg, unabhängig von der berechneten Dosis für den Patienten.
2.Um das pulverisierte Arzneimittel aufzulösen, wird Cancidas in der gekühlten Durchstechflasche an die Raumtemperatur angeglichen.
3.Unter aseptischen Bedingungen werden 10,5ml Wasser oder 0,9% Natriumchloridlösung für Injektionszwecke zugegeben. Die Konzentration der Lösung in der Durchstechflasche beträgt dann 7,2mg/ml.
4.Folgende Lösungen können für die gebrauchsfertige Infusionslösung, die dem Patienten verabreicht wird, verwendet werden: sterile physiologische Natriumchloridlösung für Injektionszwecke oder Ringer-Laktat-Lösung. Unter aseptischen Bedingungen wird das der berechneten Initialdosis entsprechende Volumen (siehe Punkt 1) aus der Durchstechflasche entnommen und in eine(n) Infusionsbeutel oder –flasche mit 250ml Inhalt gegeben. Die Infusionslösung sollte aus mikrobiologischen Gründen sofort verwendet werden, da Cancidas keine Konservierungsmittel enthält. Chemisch und physikalisch ist die Lösung bei ≤25°C bis zu 24 Stunden und im Kühlschrank (2–8°C) bis zu 48 Stunden stabil. Nicht über 25°C lagern. Cancidas sollte langsam intravenös über ca. 1 Stunde infundiert werden.
5.Wenn die berechnete Initialdosis <50mg ist, kann die Dosis mit einer 50mg-Durchstechflasche zubereitet werden. Folgen Sie dabei den Schritten 2 bis 4 von «Zubereitung der 50mg/m2-Infusion für Kinder ≥3 Monate aus einer 50mg-Durchstechflasche». Die Konzentration der Lösung in der Durchstechflasche beträgt dann 5,2mg/ml.
Zubereitung der 50mg/m2-Infusion für Kinder ≥3 Monate aus einer 50mg-Durchstechflasche:
1.Bestimmen Sie die tägliche Erhaltungsdosis, welche beim Kind angewendet werden soll, indem Sie die BSA des Patienten (wie oben berechnet) in folgender Gleichung einsetzen:BSA (m2) × 50mg/m2 = tägliche ErhaltungsdosisDie maximale tägliche Erhaltungsdosis sollte nicht höher sein als 70mg, unabhängig von der berechneten Dosis für den Patienten.
2.Um das pulverisierte Arzneimittel aufzulösen, wird Cancidas in der gekühlten Durchstechflasche an die Raumtemperatur angeglichen.
3.Unter aseptischen Bedingungen werden 10,5ml Wasser für Injektionszwecke zugegeben. Die Konzentration der Lösung in der Durchstechflasche beträgt dann 5,2mg/ml.
4.Folgende Lösungen können für die gebrauchsfertige Infusionslösung, die dem Patienten verabreicht wird, verwendet werden: sterile physiologische Natriumchloridlösung für Injektionszwecke oder Ringer-Laktat-Lösung. Unter aseptischen Bedingungen wird das der berechneten Initialdosis entsprechende Volumen (siehe Punkt 1) aus der Durchstechflasche entnommen und in eine(n) Infusionsbeutel oder –flasche mit 250ml Inhalt gegeben. Die Infusionslösung sollte aus mikrobiologischen Gründen sofort verwendet werden, da Cancidas keine Konservierungsmittel enthält. Chemisch und physikalisch ist die Lösung bei ≤25°C bis zu 24 Stunden und im Kühlschrank (2–8°C) bis zu 48 Stunden stabil. Nicht über 25°C lagern. Cancidas sollte langsam intravenös über ca. 1 Stunde infundiert werden.
5.Wenn die berechnete tägliche Erhaltungsdosis >50mg ist, kann die Dosis mit einer 70mg-Durchstechflasche zubereitet werden. Folgen Sie dabei den Schritten 2 bis 4 von «Zubereitung der 70mg/m2-Infusion für Kinder ≥3 Monate aus einer 70mg-Durchstechflasche». Die Konzentration der Lösung in der Durchstechflasche beträgt dann 7,2mg/ml.
Die zubereitete Lösung ist fast so klar wie dieselbe Menge des Lösungsmittels oder gereinigten Wassers bei entsprechender Prüfung in einem ähnlichen Gefäss. Sollte die Lösung trüb sein oder Ausfällungen aufweisen, darf sie nicht verwendet werden.
|

