ZusammensetzungWirkstoffe
Radium Ra-223-Dichlorid.
Hilfsstoffe
Acidum hydrochloridum, Natrii chloridum (38 mg), Natrii citras (43 mg), Aqua ad injectabilia.
Der Natriumgehalt pro Durchstechflasche ist 26.4 mg.
Spezifikation der gebrauchsfertigen Injektionslösung:
Volumen: 6 ml Injektionslösung.
Aussehen: klare, farblose Lösung.
pH-Wert: 6,0-8,0.
Indikationen/AnwendungsmöglichkeitenXofigo ist indiziert für die Behandlung von Patienten mit kastrationsresistentem Prostatakarzinom (CRPC) und symptomatischen Knochenmetastasen ohne bekannte viszerale Metastasen. Bei nicht orchiektomierten Patienten soll eine antiandrogene Behandlung zur Suppression des Testosteronspiegels auf Kastrationsniveau weitergeführt werden.
Dosierung/AnwendungArt der Anwendung
Xofigo kann ambulant eingesetzt werden. In jedem Fall sind die Vorsichtsmassnahmen gemäss der Strahlenschutzverordnung zu beachten.
Xofigo wird langsam intravenös injiziert (in der Regel bis zu 1 Minute).
Der intravenöse Zugang bzw. die Kanüle muss vor und nach der Injektion von Xofigo mit isotoner Kochsalzlösung gespült werden.
Weitere Hinweise zur Anwendung des Produkts siehe Rubrik «Hinweise für die Handhabung».
Dosierung bei Erwachsenen
Xofigo wird nach folgendem Dosierungsregime verabreicht: 6 Injektionen mit jeweils 55 kBq pro kg Körpergewicht in Abständen von 4 Wochen.
Sicherheit und Wirksamkeit von Xofigo bei Verabreichung von mehr als 6 Injektionen sind nicht untersucht.
Das zu verabreichende Volumen für einen bestimmten Patienten wird anhand der folgenden Werte errechnet:
·Körpergewicht des Patienten (kg)
·Dosierungsniveau (55 kBq /kg Körpergewicht)
·Konzentration der Radioaktivität in dem Produkt (1100 kBq/ml) am Referenzdatum. Das Referenzdatum ist auf der Durchstechflasche und auf dem Etikett des Blei-Behältnisses angegeben.
·Korrekturfaktor für den Zerfall (Decay correction factor, DK-Faktor) zum Ausgleichen des physikalischen Zerfalls von Radium-223. Zu jeder Durchstechflasche wird eine Tabelle mit den DK-Faktoren mitgeliefert.
Das zu verabreichende Gesamtvolumen für einen Patienten wird nach der folgenden Formel berechnet:
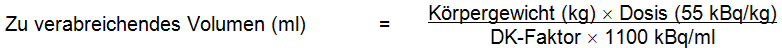
Dosierung bei speziellen Patientenklassen
Eingeschränkte Nierenfunktion
Bei leichter bis mässiger Niereninsuffizienz ist keine Dosisanpassung erforderlich. Bei schwerer Niereninsuffizienz gibt es keine Daten zur Anwendung von Xofigo.
Eingeschränkte Leberfunktion
Eine Dosisanpassung ist nicht erforderlich.
Ältere Patienten (>65 Jahre)
Eine Dosisanpassung ist nicht erforderlich.
Kinder und Jugendliche
Sicherheit und Wirksamkeit von Xofigo sind bei Kindern und Jugendlichen unter 18 Jahren nicht untersucht. Für die Anwendung bei Kindern und Jugendlichen besteht keine Indikation.
Frauen
Für die Anwendung bei Frauen besteht keine Indikation.
Strahlenexposition
Die absorbierte Strahlendosis wurde auf der Grundlage der klinischen Daten zur biologischen Verteilung unter Verwendung der Software OLINDA/EXM (Organ Level INternal Dose Assessment/EXponential Modeling) berechnet, die auf der von Medical Internal Radiation Dose (MIRD) entwickelten Methode beruht. Bei etablierten Beta- und Gammastrahlern ist diese Methode weithin gebräuchlich. Für Radium-223 als hauptsächlich Alphastrahlung emittierendes Radioisotop wurden zusätzliche Annahmen getroffen, die sich auf den Darm, auf das rote Knochenmark und die Knochen/knochenbildenden Zellen beziehen. Dadurch sollen, unter Einbeziehung der beobachteten biologischen Verteilung und spezifischer Merkmale, die bestmöglichen Berechnungen der absorbierten Xofigo-Dosen gewährleistet werden.
Bei einer verabreichten Aktivität von 4,02 MBq (55 kBq pro kg Körpergewicht bei einem 73 kg schweren Erwachsenen) betragen die von den Knochen (knochenbildenden Zellen) und vom roten Knochenmark absorbierten Dosen dieser Berechnung zufolge 4,6255 Gy bzw. 0,5572 Gy. Für die Hauptausscheidungsorgane ergeben die Berechnungen absorbierte Strahlendosen von 0,0292 Gy für die Dünndarmwand, 0,1298 Gy für die Wand des proximalen Kolons und 0,1865 Gy für die Wand des distalen Kolons (siehe auch Tabelle 1).
Die Berechnungen der absorbierten Strahlendosen für andere Organe ergaben niedrige Werte, so z.B. für die Herzwand (0,0069 Gy), die Lungen (0,0048 Gy), die Leber (0,0119 Gy), die Nieren (0,0129 Gy), die Harnblasenwand (0,0162 Gy), die Hoden (0,0003 Gy) und die Milz (0,0004 Gy).
In den klinischen Studien zu Xofigo waren Häufigkeit und Schwere der beobachteten hämatologischen Nebenwirkungen viel geringer, als aufgrund der Berechnungen der vom roten Knochenmark absorbierten Strahlendosen hätte erwartet werden können. Dies könnte auf die räumliche Verteilung der Alphastrahlung und die dadurch bedingte, ungleichmässige Belastung des roten Knochenmarks zurückzuführen sein.
Tabelle 1: Berechnete in den Organen absorbierte Strahlendosis
|
Zielorgan
|
Alpha-Strahlung1
(mGy/MBq)
|
Beta-Strahlung
(mGy/MBq)
|
Gamma-Strahlung
(mGy/MBq)
| |
Nebennieren
|
0,00
|
0,02
|
0,09
| |
Gehirn
|
0,00
|
0,02
|
0,08
| |
Brüste
|
0,00
|
0,02
|
0,03
| |
Gallenblasenwand
|
0,00
|
0,02
|
0,21
| |
Wand des UDD2
|
0,00
|
45,60
|
0,85
| |
Dünndarmwand
|
3,19
|
3,60
|
0,47
| |
Magenwand
|
0,00
|
0,02
|
0,12
| |
Wand des ODD3
|
0,00
|
31,50
|
0,82
| |
Herzwand
|
1,61
|
0,07
|
0,05
| |
Nieren
|
2,99
|
0,11
|
0,11
| |
Leber
|
2,79
|
0,10
|
0,08
| |
Lungen
|
1,09
|
0,07
|
0,05
| |
Muskulatur
|
0,00
|
0,02
|
0,10
| |
Ovarien
|
0,00
|
0,02
|
0,46
| |
Pankreas
|
0,00
|
0,02
|
0,09
| |
Rotes Knochenmark
|
132,00
|
6,42
|
0,20
| |
Osteogene Zellen
|
1140,00
|
14,90
|
0,30
| |
Haut
|
0,00
|
0,02
|
0,05
| |
Milz
|
0,00
|
0,02
|
0,07
| |
Hoden
|
0,00
|
0,02
|
0,06
| |
Thymus
|
0,00
|
0,02
|
0,03
| |
Schilddrüse
|
0,00
|
0,02
|
0,05
| |
Harnblasenwand
|
3,71
|
0,16
|
0,16
| |
Uterus
|
0,00
|
0,02
|
0,23
| |
Gesamtkörper
|
22,20
|
0,81
|
0,12
|
1 Da in den meisten Weichgeweben keine Aufnahme von Radium-223 zu beobachten war, wurde der Alphastrahlenanteil an der Gesamtorgandosis bei diesen Organen auf Null gesetzt.
2 UDD: unterer Dickdarm.
3 ODD: oberer Dickdarm.
KontraindikationenXofigo ist kontraindiziert in Kombination mit Abirateronacetat plus Prednison/Prednisolon (siehe auch Rubrik «Warnhinweise und Vorsichtsmassnahmen»).
Xofigo ist in der Schwangerschaft, bei Frauen, die schwanger sein könnten, und in der Stillzeit kontraindiziert.
Warnhinweise und VorsichtsmassnahmenKombination mit Abirateronacetat plus Prednison/Prednisolon
Eine multizentrische, randomisierte, placebokontrollierte, doppelblinde Phase-III-Studie (ERA-223-Studie) untersuchte die Wirksamkeit und Sicherheit einer Behandlung mit Radium-223-Dichlorid in Kombination mit Abirateronacetat plus Prednison/Prednisolon bei 806 Patienten mit asymptomatischem oder leicht symptomatischem kastrationsresistentem Prostatakrebs mit Knochenmetastasen. Die Studie wurde auf Empfehlung des Independent Data Monitoring Committee vorzeitig entblindet.
In der primären Analyse wurde ein vermehrtes Auftreten von Frakturen (28.6% vs. 11.4%) und Todesfällen (38.5% vs 35.5%) beobachtet bei Patienten, die mit Xofigo in Kombination mit Abirateronacetat plus Prednison/Prednisolon behandelt wurden, im Vergleich zu Patienten, die mit Placebo in Kombination mit Abirateronacetat plus Prednison/Prednisolon behandelt wurden.
Deshalb ist Xofigo kontraindiziert in Kombination mit Abirateronacetat plus Prednison/Prednisolon (siehe Rubrik «Kontraindikationen»).
Es liegen nur begrenzt Daten dazu vor, wieviel Zeit nach einer Behandlung mit Abirateronacetat plus Prednison/Prednisolon vergehen muss, bevor Xofigo sicher angewendet werden kann bzw. umgekehrt. Ausgehend von den Halbwertszeiten von Xofigo und Abirateron wird empfohlen, eine nachfolgende Behandlung mit Xofigo frühestens 5 Tage nach der letzten Gabe von Abirateronacetat in Kombination mit Prednison/Prednisolon zu beginnen. Eine nachfolgende systemische Tumortherapie sollte frühestens 30 Tage nach der letzten Gabe von Xofigo eingeleitet werden.
Behandlung von Patienten mit asymptomatischen Knochenmetastasen
Ein erhöhtes Sterbe- und Frakturrisiko wurde in einer klinischen Studie beobachtet, in der Xofigo zusätzlich zu Abirateronacetat plus Prednison/Prednisolon bei Patienten mit asymptomatischem oder leicht symptomatischem kastrationsresistentem Prostatakarzinom angewendet wurde. Der Nutzen einer Therapie mit Xofigo bei Erwachsenen mit kastrationsresistentem Prostatakarzinom und nur asymptomatischen Knochenmetastasen wurde bisher nicht nachgewiesen. Die Anwendung von Xofigo bei Erwachsenen mit kastrationsresistentem Prostatakarzinom und nur asymptomatischen Knochenmetastasen wird daher nicht empfohlen.
Die gleichzeitige Gabe von Bisphosphonaten oder Denosumab verringerte das Auftreten von Frakturen in beiden Behandlungsarmen.
Knochenmarkssuppression
Als Nebenwirkung kam es bei Patienten, die mit Xofigo behandelt wurden, zu Knochenmarkssuppression, insbesondere zu Thrombozytopenie, Neutropenie, Leukopenie und Panzytopenie (siehe Rubrik «Unerwünschte Wirkungen»).
Deshalb muss vor Beginn der Behandlung eines Patienten mit Xofigo und vor jeder weiteren Dosis eine hämatologische Untersuchung durchgeführt werden. Vor der ersten Xofigo-Dosis sollte die absolute Neutrophilenzahl (ANC) ≥1,5× 109/l, die Thrombozytenzahl ≥100× 109/l und das Hämoglobin ≥10,0 g/dl betragen. Vor den weiteren Dosen sollte der ANC-Wert 1,0× 109/l und die Thrombozytenzahl 50× 109/l nicht unterschreiten. Sollten sich diese Parameter in den 6 Wochen seit der letzten Xofigo-Dosis trotz der üblichen Standardbehandlung nicht erholt haben, darf die Behandlung mit Xofigo nur nach sorgfältiger Nutzen/Risiko-Abwägung fortgesetzt werden.
Bei der Behandlung von Patienten mit nachgewiesener Einschränkung der Knochenmarksreserve ist Vorsicht geboten.
Morbus Crohn und Colitis ulcerosa
Sicherheit und Wirksamkeit von Xofigo bei Patienten mit Morbus Crohn oder Colitis ulcerosa sind nicht untersucht.
Rückenmarkskompression
Bei Patienten mit unbehandelter drohender, oder manifester Rückenmarkskompression sollte vor Beginn oder Wiederaufnahme einer Behandlung mit Xofigo eine der klinischen Indikation entsprechende Standardbehandlung durchgeführt werden.
Knochenfrakturen
Bei Patienten mit Knochenfrakturen sollten diese vor Beginn oder Wiederaufnahme einer Behandlung mit Xofigo orthopädisch stabilisiert werden.
Fertilität
Es besteht ein potenzielles Risiko, dass die von Xofigo ausgehende Strahlung unerwünschte Wirkungen auf die Hoden und die Spermien haben könnte (siehe Rubrik «Präklinische Daten»). Die Patienten sollten darüber informiert werden. Wegen potentieller Strahlenwirkung auf die Spermatogenese sind die Männer auf die Notwendigkeit hinzuweisen, während und bis zu 6 Monate nach der Behandlung mit Xofigo zuverlässige Kontrazeptionsmethoden anzuwenden.
Andere Hinweise
Xofigo enthält 0.2 mmol Natrium (entspricht 4.4 mg Natrium pro ml Lösung). Diese Menge entspricht 0.2% der für einen Erwachsenen empfohlenen maximalen täglichen Natriumaufnahme mit der Nahrung von 2 g.
InteraktionenSicherheit und Wirksamkeit einer Kombinationsbehandlung mit Xofigo plus Chemotherapie sind nicht untersucht. Bei Patienten, die gleichzeitig mit Xofigo eine Chemotherapie erhalten, können sich die Wirkungen hinsichtlich der Knochenmarkssuppression addieren (siehe Rubrik «Warnhinweise und Vorsichtsmassnahmen»).
Schwangerschaft, StillzeitXofigo ist nicht indiziert bei Frauen. Xofigo ist in der Schwangerschaft, bei Frauen, die schwanger sein könnten, und in der Stillzeit kontraindiziert.
Schwangerschaftsverhütung
Wegen potenzieller Strahlenwirkungen auf die Spermatogenese sind die Männer auf die Notwendigkeit hinzuweisen, während und bis zu 6 Monate nach der Behandlung mit Xofigo zuverlässige Kontrazeptionsmethoden anzuwenden.
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von MaschinenEs ist nicht zu erwarten, dass Xofigo die Fahrtüchtigkeit oder die Fähigkeit, Maschinen zu bedienen, beeinträchtigt. Doch kann diese Fähigkeit durch die Grunderkrankung beeinträchtigt sein.
Unerwünschte WirkungenDas Gesamtsicherheitsprofil von Xofigo basiert auf Daten von 600 Patienten, die im Rahmen einer Phase-III-Studie mit Xofigo behandelt wurden.
Die schwerwiegendsten unerwünschten Wirkungen waren Thrombozytopenie und Neutropenie (siehe Rubrik «Warnhinweise und Vorsichtsmassnahmen» und «Beschreibung ausgewählter Nebenwirkungen» weiter unten in diesem Abschnitt).
Die häufigsten Nebenwirkungen (≥10%) bei Patienten, die mit Xofigo behandelt wurden, waren Diarrhoe, Übelkeit, Erbrechen und Thrombozytopenie.
Die unerwünschten Arzneimittelwirkungen sind innerhalb jeder Frequenzgruppierung und Organsystemklasse (gemäss MedDRA) dargestellt. Der am besten passende MedDRA-Term wird verwendet, um eine bestimmte Reaktion und deren Synonyme und ähnliche Erkrankungen zu beschreiben.
Die folgenden Angaben der Häufigkeit werden verwendet:
Sehr häufig: >10%
Häufig: 1%-10%
Gelegentlich: 0,1%–1%
Selten: 0,01%–0,1%
Erkrankungen des Blutes und des Lymphsystems
Sehr häufig: Thrombozytopenie.
Häufig: Neutropenie, Panzytopenie, Leukopenie.
Gelegentlich: Lymphopenie.
Erkrankungen des Gastrointestinaltrakts
Sehr häufig: Diarrhoe, Erbrechen, Übelkeit.
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort
Häufig: Reaktionen an der Injektionsstelle.
Beschreibung spezifischer unerwünschter Wirkungen
Thrombozytopenie und Neutropenie
Thrombozytopenien (aller Schweregrade) traten bei 11,5% der Patienten, die mit Xofigo behandelt wurden, und 5,6% der Patienten auf, die Placebo erhielten. Thrombozytopenien der Schweregrade 3 und 4 wurden bei 6,3% der Patienten unter Xofigo und 2% der Patienten unter Placebo festgestellt (siehe Rubrik «Warnhinweise und Vorsichtsmassnahmen»). Insgesamt war die Häufigkeit von Thrombozytopenien der Schweregrade 3 und 4 bei den Patienten, die nicht mit Docetaxel vorbehandelt waren, geringer (2,8% unter Xofigo und 0,8% in der Placebogruppe) als bei den Patienten, die früher Docetaxel erhalten hatten (8,9% unter Xofigo und 2,9% in der Placebogruppe).
Neutropenien (aller Schweregrade) traten bei 5% der Patienten, die mit Xofigo behandelt wurden, und 1% der Patienten, die Placebo erhielten, auf. Neutropenien der Schweregrade 3 und 4 wurden bei 2,2% der Patienten unter Xofigo und 0,7% der Patienten unter Placebo festgestellt. Insgesamt war die Häufigkeit von Neutropenien der Schweregrade 3 und 4 bei den Patienten, die nicht mit Docetaxel vorbehandelt waren, geringer (0,8% unter Xofigo und 0,8% in der Placebogruppe) als bei den Patienten, die früher Docetaxel erhalten hatten (3,2% unter Xofigo und 0,6% in der Placebogruppe).
In einer Phase-I-Studie wurde der Tiefpunkt der Neutrophilen- und der Thrombozytenzahl 2 bis 3 Wochen nach der intravenösen Verabreichung einer Einzeldosis Xofigo erreicht.
Beschwerden am Verabreichungsort
Bei 1,2% der Patienten unter Xofigo und 0% der Patienten unter Placebo traten an der Injektionsstelle Beschwerden der Schweregrade 1 und 2 auf, z.B. Erytheme, Schmerzen und Schwellungen.
Sekundäre Malignome
Xofigo trägt zur langfristigen kumulativen Gesamtstrahlenbelastung des Patienten bei. Diese ist mit einem erhöhten Risiko für Malignome und hereditäre Defekte assoziiert. Bei den Teilnehmern der klinischen Studien wurden während einer Beobachtungszeit von bis zu drei Jahren keine Fälle Xofigo-induzierter Malignome registriert.
Unerwünschte Wirkungen aus der Postmarketingphase
Seit der Markteinführung wurde über die folgende unerwünschte Wirkung in zeitlichem Zusammenhang mit der Anwendung von Ra-223-dichlorid berichtet. Die Häufigkeit dieser Nebenwirkung, die im Rahmen der Erfahrungen seit der Marktzulassung gemeldet wurde, ist unbekannt.
Erkrankungen des Blutes und des Lymphsystems: Anämie.
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von grosser Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdacht einer neuen oder schwerwiegenden Nebenwirkung über das Online-Portal ElViS (Electronic Vigilance System) anzuzeigen. Informationen dazu finden Sie unter www.swissmedic.ch.
ÜberdosierungWährend der klinischen Studien wurden keine Fälle einer Überdosierung von Xofigo gemeldet.
Ein spezifisches Antidot gibt es nicht. Im Falle einer versehentlichen Überdosierung sind allgemein supportive Massnahmen, einschliesslich Überwachung auf potenzielle hämatologische und gastrointestinale Toxizität, durchzuführen.
In einer klinischen Phase-I-Studie wurden Xofigo-Einmaldosen von maximal 276 kBq pro kg Körpergewicht geprüft. Dosislimitierende Toxizitäten wurden dabei nicht festgestellt.
Eigenschaften/WirkungenATC-Code: V10XX03
Physikalische Eigenschaften
Radium Ra-223 ist ein Alphateilchen-Emitter mit einer Halbwertszeit von 11,4 Tagen. Seine spezifische Aktivität beträgt 1,9 MBq/ng.
Bei dem sechsstufigen Zerfallsprozess von Radium-223 zu Blei-207 entstehen kurzlebige Tochterisotope, und es kommt zu einer Reihe von Alpha-, Beta- und Gamma-Emissionen mit unterschiedlichen Werten für Energie und Emissionswahrscheinlichkeit.
Wirkungsmechanismus
Xofigo ist ein Alphateilchen emittierendes therapeutisches Radiopharmakon mit gezielter Antitumorwirkung gegen Knochenmetastasen.
Die wirksame Einheit von Xofigo ist das Radioisotop Radium-223 (als Radium Ra-223-Dichlorid), das sich im menschlichen Körper ähnlich wie Kalzium verhält. Es bildet Komplexe mit dem Knochenmineral Hydroxylapatit und wird auf diese Weise selektiv in das Knochengewebe eingelagert, insbesondere in den Bereichen von Knochenmetastasen. Der hohe lineare Energietransfer von Alphastrahlern (80 keV/Mikrometer) führt in den benachbarten Zellen zu zahlreichen Brüchen in den DNA-Doppelsträngen und infolgedessen zu einem starken lokalen Antitumoreffekt. Die Reichweite der von Radium-223 emittierten Alphateilchen beträgt dabei weniger als 100 Mikrometer (weniger als 10 Zelldurchmesser), so dass das umgebende gesunde Gewebe nur minimal geschädigt wird.
Pharmakodynamik
Im Vergleich zu Placebo bestand ein signifikanter Unterschied zugunsten von Xofigo bei allen fünf Biomarkern des Knochenumsatzes im Serum, die in einer randomisierten Phase-II-Studie untersucht wurden (Marker für die Knochenneubildung: knochenspezifische alkalische Phosphatase [ALP], Gesamt-ALP und Prokollagen Typ I N-Propeptid [PINP]; Marker für die Knochenresorption: quervernetztes C-terminales Typ-I-Kollagen-Telopeptid [S-CTX-I] und Kollagen-Typ-I-C-Telopeptid [ICTP]).
Klinische Wirksamkeit
Die klinische Sicherheit und Wirksamkeit von Xofigo wurde in einer randomisierten, doppelblinden, multizentrischen Mehrfach-Dosis-Studie der Phase III (ALSYMPCA) bei symptomatischen Patienten mit progredientem kastrationsresistentem Prostatakarzinom und mindestens zwei Knochenmetastasen untersucht. Patienten mit viszeralen Metastasen oder mit maligner Lymphadenopathie von mehr als 3 cm Grösse waren ausgeschlossen worden.
Primärer Wirksamkeitsendpunkt war die Gesamtüberlebenszeit.
Am Stichtag für die vorab geplante Interimsanalyse waren insgesamt 809 Patienten nach Zufallskriterien (Randomisierungsverhältnis 2:1) einer Behandlung mit 6 Zyklen Xofigo 55 kBq/kg intravenös alle 4 Wochen plus optimaler Standardversorgung (n=541) bzw. einer entsprechenden Behandlung mit Placebo plus optimaler Standardversorgung (n=268) zugewiesen. Die optimale Standardversorgung bestand z.B. in externer lokaler Bestrahlung, Gabe von Biphosphonaten, Kortikosteroiden, Antiandrogenen bei Patienten ohne vorausgegangene Orchiektomie, Östrogenen, Estramustin oder Ketoconazol. Auf Empfehlung der unabhängigen Datenüberwachungskommission wurde die Studie nach der Interimsanalyse entblindet, da der Nachweis der Wirksamkeit gemäss den vorab definierten Abbruchkriterien erbracht war. Diese Analyse gilt als Hauptanalyse der Studie.
Bevor den Patienten der Placebogruppe die Weiterbehandlung mit Xofigo angeboten wurde, erfolgte eine aktualisierte deskriptive Sekundär-Analyse der Daten zu Sicherheit und Gesamtüberlebenszeit von 921 randomisierten Patienten.
Hinsichtlich der demografischen Daten und der Ausgangsmerkmale der Krankheit waren die Gruppen unter Xofigo bzw. Placebo (Kollektiv der Interimsanalyse) vergleichbar. Für die Xofigo-Gruppe wurden folgende Daten registriert:
·Durchschnittsalter der Patienten: 70 Jahre (Spanne 49 bis 90 Jahre).
·87% der aufgenommenen Patienten hatten einen ECOG-Leistungsstatus von 0–1.
·41% erhielten gleichzeitig Bisphosphonate.
·42% der Patienten waren nicht mit Docetaxel vorbehandelt, weil sie als ungeeignet für diese Behandlung betrachtet wurden oder die Docetaxel-Behandlung ablehnten.
·46% der Patienten hatten keine Schmerzen oder den WHO-Schmerzscore 1 (keine oder milde Symptome), 54% hatten WHO-Schmerzscore 2–3.
·Von den Patienten erhielten 83% gleichzeitig Luteinizing-Hormon-Releasing-Hormon-(LHRH-) Agonisten und 21% gleichzeitig Antiandrogene.
·Die Szintigrafie ergab bei 16% der Patienten <6 Knochenmetastasen, bei 44% zwischen 6 und 20 Knochenmetastasen und bei 40% mehr als 20 Knochenmetastasen oder ein «Superscan».
Die Ergebnisse sowohl der Interimsanalyse (Hauptanalyse) als auch der aktualisierten Analyse zeigten, dass die Patienten unter Xofigo plus optimale Standardversorgung insgesamt signifikant länger überlebten als die Patienten, die Placebo plus optimale Standardversorgung erhielten (siehe Tabelle 2, Abbildung 1). Beiden Datensets zufolge betrug die Verbesserung des Gesamtüberlebens 44%, berechnet anhand der Hazard Ratios.
Bei der Interimsanalyse wurde eine Zunahme der medianen Gesamtüberlebenszeit (Overall Survival=OS) um 2,8 Monate unter Xofigo plus optimale Standardversorgung versus Placebo plus optimale Standardversorgung festgestellt (HR=0,695 (95%-KI 0,552/0,875), p=0,00185, medianes OS: 14,0 Monate versus 11,2 Monate) bei einer Reduktion des Sterberisikos um mehr als 30%.
Die aktualisierte Analyse ergab eine Zunahme des medianen OS um 3,6 Monate unter Xofigo plus optimale Standardversorgung versus Placebo plus optimale Standardversorgung (HR=0,695 (95%-KI 0,581/0,832), medianes OS 14,9 Monate versus 11,3 Monate).
Tabelle 2: Überlebensdaten aus der Phase-III-Studie ALSYMPCA
|
Wirksamkeitsparameter
|
Xofigo
|
Placebo
| |
Interimsanalyse (Hauptanalyse)
|
n=541
|
n=268
| |
Zahl der Todesfälle (%)
|
191 (35,3%)
|
123 (45,9%)
| |
Mediane Gesamtüberlebenszeit (Monate) (95%-KI)
|
14,0 (12,1–15,8)
|
11,2 (9,0–13,2)
| |
p-Werta (2-seitig)
|
0,00185
| |
Hazard Ratiob (95%-KI)
|
0,695
(0,552/0,875)
| |
Aktualisierte Analyse
|
n=614
|
n=307
| |
Zahl der Todesfälle (%)
|
333 (54,2%)
|
195 (63,5%)
| |
Mediane Gesamtüberlebenszeit (Monate) (95%-KI)
|
14,9 (13,9–16,1)
|
11,3 (10,4–12,8)
| |
Hazard Ratiob (95%-KI)
|
0,695
(0,581/0,832)
|
HR=Hazard Ratio (Xofigo versus Placebo), KI=Konfidenzintervall
a Die Phase-III-Studie (ALSYMPCA) wurde nach der Interimsanalyse wegen nachgewiesener Wirksamkeit abgebrochen. Da die Ergebnisse der aktualisierten Analyse nur zu deskriptiven Zwecken dargestellt sind, ist kein p-Wert angegeben.
b Hazard Ratio <1 zugunsten von Xofigo.
Abbildung 1: Kaplan-Meier-Kurven der Gesamtüberlebenszeit (Interimsanalyse)
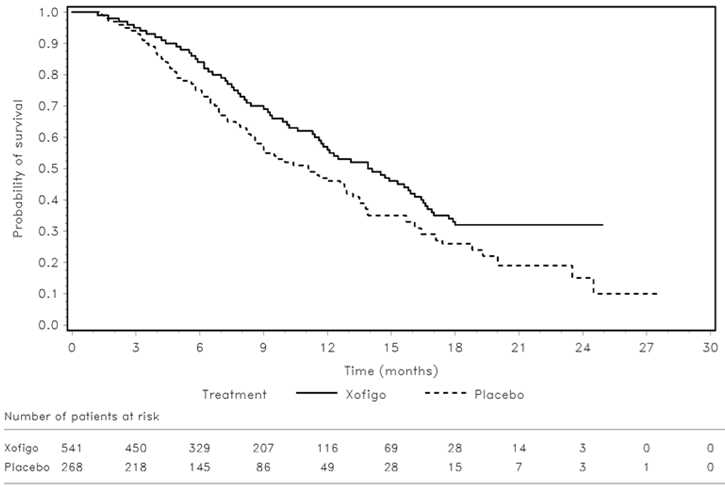
Interimsanalyse und aktualisierte Analyse ergaben auch eine signifikante Verbesserung aller wichtigen sekundären Endpunkte in der Xofigo-Gruppe, verglichen mit der Placebogruppe (siehe Tabelle 3).
Symptomatische skelettbezogene Ereignisse (Symptomatic Skeletal Events, SSE), definiert als: externe Bestrahlung zwecks Schmerzlinderung oder symptomatische pathologische Fraktur oder Rückenmarkskompression oder tumorbedingte orthopädische Operation) traten bei den Patienten, die Xofigo erhielten, signifikant später auf als bei den Patienten der Placebogruppe (Interimsanalyse: HR=0,610, 95%-KI 0,461–0,807, p=0,00046, mediane Zeit bis zum ersten SSE=13,5 Monate unter Xofigo versus 8,4 Monate unter Placebo; aktualisierte Analyse: HR=0,658, 95%-KI 0,522–0,830, mediane Zeit bis zum ersten SSE=15,6 Monate unter Xofigo versus 9,8 Monate unter Placebo).
·Bei den Patienten, die Xofigo erhielten, war im Vergleich zu den Patienten unter Placebo eine Verlängerung der Zeit bis zum Auftreten einer Rückenmarkskompression zu beobachten (Interimsanalyse: HR=0,443, 95%-KI 0,223–0,877, 17/541=3,1% versus 16/268=6,0%, p=0,01647; aktualisierte Analyse: HR=0,516, 95%-KI 0,286–0,931; die mediane Zahl der Monate war nicht feststellbar, da der Median zum Zeitpunkt des Daten-Cut-off noch nicht erreicht war).
·Bei den Patienten, die Xofigo erhielten, war im Vergleich zu den Patienten unter Placebo eine Verlängerung der Zeit bis zu einer Knochenfraktur zu beobachten (Interimsanalyse: HR=0,450, 95%-KI 0,236–0,856, 20/541=3,7% versus 18/268=6,7%, p=0,01255; aktualisierte Analyse: HR=0,620, 95%-KI 0,351–1,093; die mediane Zahl der Monate war nicht feststellbar, da der Median zum Zeitpunkt des Daten-Cut-off noch nicht erreicht war).
·Die Zeit bis zur externen Bestrahlung zwecks Schmerzlinderung war unter Xofigo signifikant verlängert (Interimsanalyse: HR=0,649, 95%-KI 0,483–0,871, 122/541=22,6% versus 72/268=26,9%, p=0,00375, mediane Zeit=17,0 Monate unter Xofigo versus 10,8 Monate unter Placebo; aktualisierte Analyse: HR=0,670, 95%-KI 0,525–0,854, mediane Zeit=17,1 Monate unter Xofigo versus 17,5 Monate unter Placebo). In der Placebogruppe war der Anteil der verstorbenen Patienten höher und als Folge davon die Zahl der EBRT-Ereignisse (External Beam Radiation Therapy, EBRT) geringer; zum Zeitpunkt der aktualisierten Analyse führte dies zu einer Bias in Form einer längeren medianen Zeit bis zur EBRT.
Tabelle 3: Sekundäre Endpunkte der ALSYMPCA-Studie: Zeit bis zum Auftreten symptomatischer skelettbezogener Ereignisse (SSE), Zeit bis zur externen Bestrahlung (EBRT), Zeit bis zur Rückenmarkskompression und Zeit bis zu einer Knochenfraktur
|
|
Symptomatisches skelettbezogenes
Ereignis (SSE)a
|
SSE-Komponenten
| |
EBRT zur Schmerzlinderung
|
Rückenmarkskompression
|
Knochenfrakturen
| |
Xofigo
|
Pbo
|
Xofigo
|
Pbo
|
Xofigo
|
Pbo
|
Xofigo
|
Pbo
| |
Interimsanalyse (Xofigo: n=541 Patienten; Placebo: n=268 Patienten)
| |
Inzidenz
[Zahl (%) der Patienten]
|
132
(24,4%)
|
82
(30,6%)
|
122
(22,6%)
|
72
(26,9%)
|
17
(3,1%)
|
16
(6,0%)
|
20
(3,7%)
|
18
(6,7%)
| |
Analyse der Zeit bis zum Ereignis
(95%-KI) [mediane Zahl der Monate]
|
13,5
(12,2–19,6)
|
8,4
(7,2–NEd)
|
17,0
(12,9–NE)
|
10,8
(7,9–NE)
|
NE
|
NE
|
NE
|
NE
| |
p-Wertb (2-seitig)
|
0,00046
|
0,00375
|
0,01647
|
0,01255
| |
HRc (95%-KI)
|
0,610
(0,461–0,807)
|
0,649
(0,483–0,871)
|
0,443
(0,223–0,877)
|
0,450
(0,236–0,856)
| |
Aktualisierte Analyse (Xofigo: n=614 Patienten; Placebo: n=307 Patienten)
| |
Inzidenz
[Zahl (%) der Patienten]
|
202 (32,9%)
|
116 (37,8%)
|
186 (30,3%)
|
105
(34,2%)
|
25
(4,1%)
|
21
(6,8%)
|
32
(5,2%)
|
20
(6,5%)
| |
Analyse der Zeit bis zum Ereignis
(95%-KI) [mediane Zahl der Monate]
|
15,6
(13,5–18,0)
|
9,8
(7,3–23,7)
|
17,1
(14,1–19,8)
|
17,5
(7,9–29,0)e
|
NE
|
NE
|
NE
|
NE
| |
HRc (95%-KI)
|
0,658
(0,522–0,830)
|
0,670
(0,525–0,854)
|
0,516
(0,286–0,931)
|
0,620
(0,351–1,093)
|
EBRT=Externe Bestrahlung, HR=Hazard Ratio (Xofigo versus Placebo), KI=Konfidenzintervall, Pbo=Placebo.
a Ein SSE war definiert als: externe Bestrahlung zwecks Schmerzlinderung oder pathologische Fraktur oder Rückenmarkskompression oder tumorbedingte orthopädische Operation.
b Die Phase-III-Studie (ALSYMPCA) wurde nach der Interimsanalyse wegen nachgewiesener Wirksamkeit abgebrochen. Da die aktualisierte Analyse nur deskriptiven Zwecken dient, ist kein p-Wert angegeben.
c Hazard Ratio <1 zugunsten von Xofigo.
d NE: nicht ermittelbar, weil der Median zum Zeitpunkt des Daten-Cut-off noch nicht erreicht war.
e In der Placebogruppe war der Anteil der verstorbenen Patienten höher und als Folge davon die Zahl der EBRT-Ereignisse geringer; zum Zeitpunkt der aktualisierten Analyse führte dies zu einer Bias in Form einer längeren medianen Zeit bis zur EBRT.
Die Ergebnisse der Phase-III-Studie ALSYMPCA bezüglich der Zeit bis zur externen Bestrahlung (EBRT) belegen durch Verlängerung des Zeitintervalls bis zum Auftreten einer schmerzhaften Skelettmetastase eine positive Wirkung bezüglich des Krankheitsverlaufs.
Analyse der Studiendaten nach drei Jahren
Die Auswertungen der Daten von Patienten der Phase III Studie ALSYMPCA nach drei Jahren haben das Wirksamkeits- und Nebenwirkungsprofil der ursprünglichen Hauptanalyse bestätigt.
Untergruppenanalyse der Überlebensdaten
Die Analyse der Überlebensdaten nach Untergruppen ergab einen konsistenten Überlebensvorteil für die Patienten, die mit Xofigo behandelt wurden, unabhängig von der Gesamt-ALP, der Anwendung von Bisphosphonaten zu Studienbeginn und einer Vorbehandlung mit Docetaxel.
Anschliessende Anwendung von Zytostatika
Im Verlauf der ALSYMPCA-Studie erhielten 93 Patienten (15.5%) in der Xofigo-Gruppe und 54 Patienten (17.9%) in der Placebogruppe eine zytotoxische Chemotherapie zu verschiedenen Zeitpunkten nach der letzten Behandlung. Zwischen den beiden Gruppen waren keine Unterschiede hinsichtlich der hämatologischen Laborwerte zu erkennen.
PharmakokinetikAbsorption
Daten zu Pharmakokinetik, biologischer Verteilung und Dosimetrie von Xofigo wurden in 3 Phase-I-Studien erhoben. Pharmakokinetische Daten wurden von 25 Patienten erhoben, die Dosen zwischen 51 und 276 kBq /kg erhielten. Weitere Daten zur Pharmakokinetik sowie Daten zur biologischen Verteilung und zur Dosimetrie stammen von 6 Patienten, denen zwei Dosen von jeweils 110 kBq/kg im Abstand von 6 Wochen verabreicht wurden, und von 10 Patienten, die eine Einmaldosis von 55, 110 oder 221 kBq/kg erhielten.
Xofigo wird als intravenöse Injektion verabreicht; seine Bioverfügbarkeit beträgt daher 100%.
Distribution
Nach intravenöser Injektion verweilt Radium-223 nur kurz im Blut und wird hauptsächlich in Knochen und Knochenmetastasen eingelagert oder in den Darm ausgeschieden.
Fünfzehn Minuten nach der Injektion sind noch ca. 20%, 4 Stunden nach der Injektion noch ca. 4% der injizierten Aktivität im Blut nachweisbar. Innerhalb von 24 Stunden nach der Injektion geht dieser Anteil auf weniger als 1% zurück. Das Verteilungsvolumen ist grösser als das Blutvolumen, ein Zeichen dafür, dass eine Verteilung in periphere Kompartimente stattfindet.
Zehn Minuten nach der Injektion ist Aktivität in den Knochen und im Darm nachweisbar. 4 Stunden nach der Injektion betrug der mittlere Prozentsatz für die im Knochen bzw. im Darm vorhandene Radioaktivität 61% bzw. 49%.
Eine signifikante Aufnahme in andere Organe wie z.B. Herz, Leber, Nieren, Harnblase oder Milz ist 4 Stunden nach der Injektion nicht zu beobachten.
Metabolismus
Radium- 223 ist ein Isotop, das zerfällt und nicht verstoffwechselt wird.
Elimination
Die Elimination aus dem Körper erfolgt hauptsächlich mit dem Stuhl. Rund 5% werden mit dem Urin ausgeschieden. Hinweise auf eine hepatobiliäre Ausscheidung wurden nicht gefunden.
Ganzkörpermessungen an Tag 7 nach der Injektion zeigen (nach Korrektur für den Zerfall), dass median 76% der verabreichten Aktivität aus dem Körper eliminiert sind. Die Eliminationsrate von Radium Ra-223-Dichlorid aus dem Gastrointestinaltrakt wird von der hohen Variabilität der intestinalen Transitgeschwindigkeiten innerhalb der Bevölkerung beeinflusst; die normale Häufigkeit der Darmentleerung reicht von einmal täglich bis einmal wöchentlich.
Linearität
Die Pharmakokinetik von Radium Ra-223-Dichlorid war im untersuchten Dosierungsbereich (51 bis 276 kBq/kg) linear.
Kinetik spezieller Patientengruppen
Ältere Patienten (>65 Jahre)
Von den 600 Patienten, die im Rahmen der Phase-III-Studie mit Xofigo behandelt wurden, waren 447 (74,5%) 65 Jahre oder älter und 196 (32,7%) 75 Jahre oder älter.
Leberfunktionsstörungen
Sicherheit und Wirksamkeit von Xofigo bei Patienten mit eingeschränkter Leberfunktion sind nicht untersucht.
Da Radium-223 weder von der Leber verstoffwechselt noch mit der Galle ausgeschieden wird, sind von einer Einschränkung der Leberfunktion keine Auswirkungen auf die Pharmakokinetik von Radium Ra-223-Dichlorid zu erwarten.
Nierenfunktionsstörungen
In der klinischen Phase-III-Studie wurden hinsichtlich Sicherheit und Wirksamkeit von Xofigo keine relevanten Unterschiede zwischen Patienten mit leicht eingeschränkter (Kreatinin-Clearance [CLCR] 50–80 ml/min) und Patienten mit normaler Nierenfunktion beobachtet. Von Patienten mit mässig eingeschränkter Nierenfunktion (CLCR 30–50 ml/min) liegen nur in begrenztem Umfang Daten vor. Von Patienten mit stark eingeschränkter (CLCR <30 ml/min) Nierenfunktion oder terminaler Niereninsuffizienz sind keine Daten verfügbar.
Da jedoch nur ein sehr geringer Anteil einer verabreichten Dosis im Urin ausgeschieden wird und die Ausscheidung hauptsächlich über den Stuhl erfolgt, sind von einer Einschränkung der Nierenfunktion keine Auswirkungen auf die Pharmakokinetik von Radium Ra-223-Dichlorid zu erwarten.
Kardiale Elektrophysiologie/QT Verlängerung
In einer Subgruppe von 29 Patienten der ALSYMPCA Studie konnte nach intravenöser Injektion von Xofigo im Vergleich zu Placebo keine signifikante QTc-Verlängerung beobachtet werden.
Präklinische DatenSicherheitspharmakologie
Nach einmaliger Verabreichung von 497 bis 1100 kBq pro kg Körpergewicht (das 9- [Hund] bis 20-Fache [Ratte] der klinisch empfohlenen Dosis) wurden keine signifikanten Auswirkungen auf die lebenswichtigen Organsysteme (Herz-Kreislauf-System [Hund], Atmungsorgane oder Zentralnervensystem [Ratte]) beobachtet.
Systemische Toxizität
In Toxizitätsstudien an Ratten wurden Befunde ermittelt, die vorallem auf einer strahlenbedingten Beeinträchtigung der Hämatopoiese und Osteogenese beruhen. Diese traten bei der Gabe von Radium Ra-223 Dichlorid in Dosierungen ab 22 kBq pro kg Körpergewicht auf.
Bei Hunden wurde eine dosislimitierende Myelotoxizität nach einmaliger Verabreichung von 497 kBq Radium Ra-223-Dichlorid pro kg Körpergewicht (das 9-Fache der klinisch empfohlenen Dosis) beobachtet.
Bei 2 Hunden wurden nach wiederholter Gabe der empfohlenen Dosis von 55 kBq/kg Körpergewicht alle 4 Wochen über 6 Monate Beckenfrakturen (ohne Knochenverschiebungen) festgestellt. Da an anderen Knochen von behandelten Hunden Osteolyse an der trabekulären Struktur in unterschiedlicher Ausprägung beobachtet wurde, kann nicht ausgeschlossen werden, dass es sich bei den Beckenfrakturen um spontane Frakturen aufgrund von Osteolyse handelte. Die klinische Relevanz dieser Beobachtungen ist allerdings unklar.
Ebenfalls bei Hunden wurden Netzhautablösungen nach einmaliger Injektion von 166 oder 497 kBq pro kg Körpergewicht (das 3- bzw. 9-Fache der klinisch empfohlenen Dosis) beobachtet, nicht jedoch nach wiederholter Verabreichung der klinisch empfohlenen Dosis von 55 kBq pro kg Körpergewicht einmal alle 4 Wochen über 6 Monate. Radium Ra-223-Dichlorid reichert sich spezifisch in das Tapetum lucidum des Hundeauges an. Da das menschliche Auge aber kein Tapetum lucidum aufweist, ist die klinische Relevanz dieser Beobachtung für den Menschen unklar. Histologische Veränderungen in den Organen, die an der Ausscheidung von Radium Ra-223-Dichlorid beteiligt sind, wurden nicht beobachtet.
Bei Ratten wurden 7–12 Monate nach Beginn einer Behandlung mit klinisch relevanten Dosen Osteosarkome beobachtet. Diese stellen eine bekannte Folge von knochensuchenden Radionukliden dar. Dagegen traten in Studien mit Hunden keine Osteosarkome auf. Die klinische Relevanz dieser Beobachtung für den Menschen ist unklar. In den längerfristigen (12- bis 15-monatigen) Toxizitätsstudien an Ratten wurden neben Osteosarkomen auch andere neoplastische Veränderungen beobachtet. Aufgrund seines Wirkmodus kann Radium Ra-223-Dichlorid potentiell Sekundärmalignome induzieren (siehe Rubrik «Nebenwirkungen/Sekundäre Malignome»), wie auch bei konventioneller Radiotherapie und anderen Radiotherapeutika zu beobachten.
Reproduktionstoxizität
Studien zur Reproduktions- und Entwicklungstoxizität wurden nicht durchgeführt. Im Allgemeinen induzieren Radionuklide Reproduktions- und Entwicklungsschäden.
In einigen Samenkanälchen von Hoden männlicher Ratten wurde nach einmaliger Gabe von ≥2270 kBq/kg Körpergewicht Radium-223-dichlorid (dem ≥41-fachen der klinisch empfohlenen Aktivität) eine geringfügige Anzahl abnormer Spermatozyten festgestellt. Ansonsten schienen die Hoden normal zu funktionieren und die Nebenhoden zeigten einen normalen Gehalt an Spermatozyten. In weiblichen Ratten wurden nach einzelnen oder wiederholten Gaben von ≥359 kBq/kg Köpergewicht Radium-223-dichlorid (dem ≥6,5-fachen der klinisch empfohlenen Aktivität) Uteruspolypen (Endometriumstroma) beobachtet.
Genotoxizität
Studien zum mutagenen Potenzial von Xofigo wurden nicht durchgeführt. Allgemein werden Radionuklide als genotoxisch betrachtet.
Kanzerogenität
Studien zum kanzerogenen Potenzial von Xofigo wurden nicht durchgeführt. Allgemein werden Radionuklide als karzinogen betrachtet.
Sonstige HinweiseInkompatibilitäten
Da keine Kompatibilitätsstudien vorliegen, darf Xofigo nicht mit anderen Arzneimitteln gemischt werden.
Haltbarkeit
Das Arzneimittel darf nur bis zu dem auf der Packung mit «EXP» bezeichnetem Datum verwendet werden. Nicht über 30°C lagern. Die chemische und physikalische Stabilität wurde für 28 Tage bei 60°C gezeigt.
Das Referenzdatum ist auf der Durchstechflasche und auf dem Etikett des Blei-Behältnisses angegeben.
Besondere Lagerungshinweise
Nicht zutreffend.
Hinweise für die Handhabung
Allgemeine Hinweise
Xofigo (ein Alphateilchen emittierendes Radiotherapeutikum) darf nur von autorisiertem Personal in dazu bestimmten Bereichen entgegengenommen, verwendet und verabreicht werden. Eingang, Lagerung, Verwendung, Weiterleitung und Entsorgung von Xofigo unterliegen besonderen Bestimmungen und/oder bedürfen entsprechender Genehmigungen durch die zuständigen Behörden.
Bei der Handhabung von Xofigo müssen vom Anwender die Anforderungen sowohl zum Strahlenschutz als auch zur Sicherstellung der pharmazeutischen Qualität erfüllt werden. Geeignete aseptische Vorsichtsmassnahmen sind zu beachten.
Strahlenschutz
Die Anwendung radioaktiver Stoffe am Menschen ist in der Schweiz durch die aktuell gültige Version der Strahlenschutzverordnung geregelt. Entsprechend ist für die Anwendung von Radiopharmazeutika nur autorisiert, wer über die erforderliche Bewilligung des Bundesamtes für Gesundheit verfügt. Um jede unnötige Bestrahlung von Patienten und Personal zu vermeiden, sind beim Umgang mit radioaktiven Stoffen sowie bei der Beseitigung radioaktiven Abfalls die Schutzvorkehrungen der oben erwähnten Verordnung und der Verordnung über den Umgang mit offenen radioaktiven Strahlenquellen zu beachten.
Die beim Zerfall von Radium-223 und dessen Tochterisotopen frei werdende Gammastrahlung erlaubt die Messung der Radioaktivität von Xofigo und den Nachweis von Kontaminierungen mittels Standardinstrumenten.
Die Verabreichung von Xofigo ist mit potenziellen Risiken für andere Personen (z.B. medizinisches Fachpersonal, Bezugspersonen und Personen, die im gleichen Haushalt leben wie der Patient) aufgrund externer Strahlung oder Kontamination durch Kontakt mit Körperflüssigkeiten wie Urin, Stuhl oder Erbrochenem verbunden. Bei den Massnahmen zum Strahlenschutz sind deshalb die nationalen und lokalen Vorschriften zu beachten. Radium-223 ist zwar vorwiegend ein Alphastrahler, doch ist mit dem Zerfall von Radium-223 und seinen radioaktiven Tochterisotopen auch die Emission von Gamma- und Betastrahlung verbunden. Die externe Strahlenexposition, die mit der Handhabung der Patientendosen assoziiert ist, ist beträchtlich geringer als bei anderen Radiopharmaka, die zu therapeutischen Zwecken eingesetzt werden, da die verabreichte Radioaktivität in der Regel weniger als 8 MBq beträgt. Jedoch wird gemäss dem ALARA-Prinzip («As Low As Reasonably Achievable» = So wenig, wie sinnvoller Weise möglich), zur Minimierung der Strahlenbelastung empfohlen, die Aufenthaltsdauer im Strahlungsbereich so kurz wie möglich zu halten, sich so weit wie möglich von den Strahlenquellen entfernt aufzuhalten und ausreichende Abschirmungen zu verwenden.
Abfallbeseitigung
Nicht verwendetes Arzneimittel und Materialien, die bei der Zubereitung oder Verabreichung des Arzneimittels verwendet wurden, sind als radioaktive Abfälle zu behandeln und müssen in Übereinstimmung mit den hierfür geltenden lokalen Bestimmungen entsorgt werden.
Xofigo kann geringe Spuren von Actinium-227 (Halbwertszeit 21,77 Jahre) und Thorium-227 (Halbwertszeit 18,7 Tage) enthalten. Bei der Abfallentsorgung muss das Actinium-227 mitberücksichtigt werden. Die Abfälle sind auf geeignete Weise für 6 Monate ab Verfalldatum im Betrieb zu lagern, bis zum Abklingen des Radium-223 und möglicher Thorium-227 Spuren unter die Werte gemäss Artikel 24 und Anhang 7 der Strahlenschutzverordnung. Danach können die Abfälle bei Vorliegen einer entsprechenden Bewilligung für die Entsorgung von Actinium-227 via Abwasser unter Beachtung der Schweizer Gesetzesanforderungen entsorgt werden gemäss der entsprechenden Entsorgungsanweisung des BAG als flüssiger Abfall über das Abwasser oder als fester Abfall unter Beachtung der Schweizer Gesetzesanforderungen.
Bestattung von Patienten
Bei der Bestattung von Patienten, die kurz zuvor mit Xofigo behandelt worden waren, sind die Bestimmungen gemäss Art. 56 und Anhang 4 der Verordnung des EDI über den Umgang mit radioaktivem Material einzuhalten. Bei der Kremation kann dies zu einer Wartefrist, abhängig von der injizierten Radium-223 Menge, führen (z.B. Wartefrist von ca. 25 Tagen von 4 MBq Radium-223). Der Patient muss vor der Therapie über die mögliche Wartezeit bei der Kremation informiert werden und sich damit einverstanden erklären.
Anweisungen für die Zubereitung
Dieses Arzneimittel ist vor der Anwendung visuell zu prüfen. Xofigo ist eine klare, farblose Lösung und darf nicht verwendet werden, wenn Verfärbungen oder Partikel erkennbar sind oder das Behältnis beschädigt ist.
Die Radioaktivitätsmenge im dispensierten Volumen ist durch Messung in einem ordnungsgemäss kalibrierten Aktivimeter zu bestätigen.
Xofigo ist eine gebrauchsfertige Lösung und darf nicht mit anderen Lösungen verdünnt oder gemischt werden.
Jede Durchstechflasche ist nur für den einmaligen Gebrauch bestimmt.
Zulassungsnummer62732 (Swissmedic).
Packungen1 Injektionsflasche à 6 ml Lösung mit 6600 kBq (A)
ZulassungsinhaberinBayer (Schweiz) AG, 8045 Zürich.
Stand der InformationMai 2021
Korrekturtabelle zum radioaktiven Zerfall von RADIUM-223
Veränderungen durch Zeitumstellungen sind in dieser Tabelle nicht berücksichtigt, da eine einstündige Abweichung bei einem Radionuklid mit einer Halbwertszeit von 11,4 Tagen nicht als ausschlaggebend betrachtet wird.
|
EUROPA
| |
12 Uhr mittags Mitteleuropäische Zeit (MEZ)
| |
Tag ab Referenztag
|
Physikalischer Zerfallsfaktor
| |
-14
|
2,34
| |
-13
|
2,20
| |
-12
|
2,07
| |
-11
|
1,95
| |
-10
|
1,83
| |
-9
|
1,73
| |
-8
|
1,62
| |
-7
|
1,53
| |
-6
|
1,44
| |
-5
|
1,35
| |
-4
|
1,27
| |
-3
|
1,20
| |
-2
|
1,13
| |
-1
|
1,06
| |
0
|
1,00
| |
1
|
0,94
| |
2
|
0,89
| |
3
|
0,83
| |
4
|
0,78
| |
5
|
0,74
| |
6
|
0,69
| |
7
|
0,65
| |
8
|
0,62
| |
9
|
0,58
| |
10
|
0,55
| |
11
|
0,51
| |
12
|
0,48
| |
13
|
0,45
| |
14
|
0,43
|
|