ZusammensetzungWirkstoffe
Lidocaini hydrochloridum anhydricum ut Lidocaini hydrochloridum monohydricum
Hilfsstoffe
Natrii chloridum, Natrii hydroxidi solutio 1 mol/L ad pH, Acidum hydrochloridum concentratum ad pH, Aqua ad iniectabilie
Jeder ml Injektionslösung enthält 2,0 mg Natrium.
Jede 5-ml-Fertigspritze enthält 10 mg Natrium.
Indikationen/AnwendungsmöglichkeitenBehandlung schwerer ventrikulärer Arrhythmien bei Erwachsenen, die nach Einschätzung des Arztes lebensbedrohlich sind.
Dosierung/AnwendungDosierung
Erwachsene
Die Dosierung ist entsprechend dem individuellen Bedarf und der therapeutischen Wirkung anzupassen.
Initialdosis:
Die übliche Initialdosis beträgt 50 – 100 mg durch langsame intravenöse Injektion über 2-4 Minuten oder 1 – 1,5 mg/kg Körpergewicht Ryligency durch direkte intravenöse Injektion, was ungefähr 2,5 – 5 ml oder 0,05 – 0,075 ml/kg Körpergewicht entspricht.
Die Injektionsgeschwindigkeit darf 25 – 50 mg/min nicht überschreiten, entsprechend etwa 1,25 – 2,5 ml/min.
Wenn die therapeutische Wirkung der ersten Dosis innerhalb der ersten 5 – 10 Minuten nicht ausreichend ist, kann die Initialdosis ein- oder zweimal bis zu einer Höchstdosis von 200 – 300 mg innerhalb 1 Stunde wiederholt werden.
Die Tageshöchstdosis als Bolus beträgt 300 mg.
Patienten mit eingeschränkter Nierenfunktion
Die Patienten sollten überwacht werden, da eine Niereninsuffizienz aufgrund der Akkumulation aktiver Metaboliten toxische Wirkungen hervorrufen kann (siehe Abschnitte «Warnhinweise und Vorsichtsmassnahmen» und «Pharmakokinetik»). Ryligency ist mit Vorsicht anzuwenden.
Patienten mit eingeschränkter Leberfunktion oder Herzinsuffizienz
Bei Patienten mit Herz- oder Leberinsuffizienz ist die Dosis maximal um die Hälfte zu reduzieren (siehe Abschnitt «Warnhinweise und Vorsichtsmassnahmen»).
Ältere Patienten
Bei älteren Patienten werden die Dosierungen auf der Grundlage von Alter und Körpergewicht des Patienten individuell berechnet. Eine Dosisanpassung kann erforderlich sein, da Herzzeitvolumen und Leberdurchblutung mit zunehmendem Alter abnehmen, was auf eine verringerte Clearance von Lidocain schliessen lässt (siehe Abschnitt «Pharmakokinetik»).
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit bei Kindern und Jugendlichen ist nicht erwiesen. Die Fertigspritze ist nicht zur Anwendung bei Kindern und Jugendlichen geeignet, da die Graduierung keine genaue Dosierung bei Kindern erlaubt.
Anwendung
Ryligency ist als langsame intravenöse Injektion zu verabreichen. Die Fertigspritze ist nicht zur Anwendung mit einer Spritzenpumpe geeignet.
Kontraindikationen·Schwere Erregungsleitungsstörungen (z. B. AV-Block vom Typ II-III) ohne Versorgung mit einem Schrittmacher.
·Überempfindlichkeit gegen den Wirkstoff, Lokalanästhetika vom Amid-Typ (z. B. Prilocain, Mepivacain und Bupivacain) oder einem der im Abschnitt «Pharmazeutische Hilfsstoffe» genannten Hilfsstoffe.
Warnhinweise und VorsichtsmassnahmenEine Überdosierung kann systemische toxische Wirkungen hervorrufen.
Während der Verabreichung von Lidocain ist eine kontinuierliche Überwachung von EKG, Blutdruck, Bewusstseinslage und Atmung erforderlich. Insbesondere bei einer Dosisanpassung des Antiarrhythmikums ist eine sorgfältige kardiologische Überwachung erforderlich. Eine kardiologische Notfallausrüstung muss bereitstehen. Falls einer oder mehrere Parameter auf eine Verschlechterung der Herzfunktion hinweisen, muss die Therapie neu überdacht werden, die ggf. den Abbruch der Lidocain-Behandlung umfassen kann.
Ryligency ist mit Vorsicht anzuwenden bei Patienten mit:
·Epilepsie: Patienten mit zerebralen Anfallsleiden müssen sehr engmaschig auf das Auftreten zentralnervöser Symptome überwacht werden. Selbst niedrige Dosen Lidocain können die Krampfbereitschaft erhöhen;
·Hypovolämie;
·Nieren- oder Leberinsuffizienz;
·Myasthenia gravis;
·Herzleitungsblock;
·Herzinsuffizienz oder Herzfehler;
·Atemdepression;
·Schwerer Schock.
Die für die Überwachung und für intensivmedizinische Notfallmassnahmen nötige Ausrüstung und Arzneimittel sind bereitzuhalten.
Bei Azidose ist die Plasmaproteinbindung von Lidocain reduziert und die Konzentration von freiem Lidocain daher erhöht. Aus diesem Grund kann die Wirkung von Lidocain bei Azidose verstärkt sein.
Hypokaliämie, Hypoxie und Störungen des Säure-Basen-Haushalts müssen bei Patienten, die hohe Dosen von Antiarrhythmika benötigen, vor der Anwendung von Lidocain korrigiert werden.
Hinweis: Bei narkotisierten Patienten können zentralnervöse Störungen unbemerkt bleiben und unerwünschte kardiale Wirkungen ohne vorherige Warnsymptome plötzlich auftreten.
Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro Fertigspritze, d.h. es ist nahezu «natriumfrei».
InteraktionenPharmakodynamische Interaktionen
Antiarrhythmika der Klasse I
Die gleichzeitige Verabreichung von Lidocain und anderen Antiarrhythmika der Klasse I sollte vermieden werden, da das Risiko besteht, dass schwerwiegende unerwünschte kardiale Wirkungen auftreten.
Andere Antiarrhythmika
Wenn Lidocain mit anderen antiarrhythmisch wirkenden Arzneimitteln wie Betablockern oder Kalziumantagonisten kombiniert wird, kann der Hemmeffekt auf die atrioventrikuläre und intraventrikuläre Reizleitung und auf die Kontraktilität verstärkt werden.
Kombination mit anderen Lokalanästhetika
Die Kombination verschiedener Lokalanästhetika kann zu additiven Effekten auf das Herz-Kreislauf- und das zentrale Nervensystem führen.
Muskelrelaxanzien
Die Wirkung von Muskelrelaxanzien (z. B. Suxamethonium) wird durch Lidocain verlängert.
Beruhigungsmittel, Hypnotika
Lidocain ist bei Patienten, die Beruhigungsmittel erhalten, die auch die ZNS-Funktion beeinträchtigen und daher die Lidocain-Toxizität verändern können, mit Vorsicht zu verabreichen. Es kann ein additiver Effekt zwischen der lokalanästhetischen Wirkung und Sedativa oder Hypnotika auftreten.
Inhalationsnarkotika
Bei gleichzeitiger Anwendung von Lidocain und Inhalationsnarkotika können sich die depressiven Wirkungen gegenseitig verstärken.
Arzneimittel, die die Krampfschwelle senken können
Da Lidocain selbst die Krampfschwelle senken kann, kann die gleichzeitige Verabreichung anderer Arzneimittel, die die Krampfschwelle senken (z. B. Tramadol oder Bupropion), das Risiko für Krampfanfälle erhöhen.
Arzneimittel, die die Krampfschwelle erhöhen können
Die gleichzeitige Gabe von Diazepam erhöht die Krampfschwelle von Lidocain. Dies muss bei der Überwachung der Patienten auf Anzeichen einer Toxizität von Lidocain beachtet werden.
Vasokonstriktoren
Die lokalanästhetische Wirkung wird in Kombination mit einem Vasokonstriktor, z. B. Adrenalin, verlängert. Wenn Lidocain als Antiarrhythmikum angewendet wird, kann die zusätzliche Behandlung mit Adrenalin oder Noradrenalin zur Verstärkung der unerwünschten kardialen Wirkungen führen.
Pharmakokinetische Interaktionen
Lidocain wird hauptsächlich durch die Cytochrom P 450-Isoenzyme CYP 3A4 und CYP 1A2 metabolisiert (siehe Abschnitt «Pharmakokinetik»). Die gleichzeitige Anwendung von Wirkstoffen, die Substrate, Inhibitoren oder Induktoren der hepatischen Isoenzyme CYP3A4 und CYP1A2 sind, kann die Pharmakokinetik von Lidocain und daher auch seine Wirkung beeinflussen.
CYP 3A4- und/oder CYP 1A2-Inhibitoren
Die gleichzeitige Verabreichung von Lidocain und CYP3A4- und/oder CYP1A2-Inhibitoren kann zu erhöhten Plasmakonzentrationen von Lidocain führen. Über erhöhte Plasmakonzentrationen wurde beispielsweise berichtet bei:
·Amiodaron (CYP3A4-Inhibitor): Amiodaron vermindert den Lebermetabolismus von Lidocain und führt so zum Risiko einer Erhöhung des Lidocain-Spiegels mit anschliessender Zunahme der neurologischen und kardiovaskulären Toxizität. Eine klinische Überwachung, EKG-Kontrollen und auch eine Kontrolle der Plasmakonzentration von Lidocain sind durchzuführen. Bei Bedarf ist die Lidocain-Dosierung während und nach der Amiodaron-Behandlung anzupassen.
·Cimetidin (CYP3A4- und CYP1A2-Inhibitor): Cimetidin in Dosen von 800 mg/Tag oder mehr: Erhöhte Plasmakonzentration von Lidocain mit anschliessender Zunahme der neurologischen und kardiovaskulären Toxizität. Eine klinische Überwachung, EKG-Kontrollen und auch eine Kontrolle der Plasmakonzentration von Lidocain sind durchzuführen. Bei Bedarf sollte die Lidocain-Dosierung während und nach der Behandlung mit Cimetidin angepasst werden.
·Fluvoxamin (CYP3A4- und CYP1A2-Inhibitor): Erhöhte Plasmakonzentration von Lidocain, wodurch das Risiko einer neurologischen und kardiovaskulären Toxizität steigt. Eine klinische Überwachung, EKG-Kontrollen und auch eine Kontrolle der Plasmakonzentration von Lidocain sind durchzuführen. Bei Bedarf ist die Lidocain-Dosierung während und nach der Kombinationstherapie anzupassen.
·Betablocker (ausser Esmolol): Intravenöses Lidocain: erhöhte Plasmakonzentration von Lidocain mit anschliessender Zunahme der neurologischen und kardiovaskulären Toxizität. Eine klinische Überwachung, EKG-Kontrollen und auch eine Kontrolle der Plasmakonzentration von Lidocain sind durchzuführen. Bei Bedarf ist die Dosierung von Lidocain während und nach der Behandlung mit Betablockern anzupassen.
·Andere bekannte CYP3A4-Inhibitoren: Proteasehemmer (z. B. Ritonavir), Makrolidantibiotika (z. B. Erythromycin), Antimykotika (z. B. Ketoconazol, Itraconazol).
·Andere bekannte CYP1A2-Inhibitoren: Ciprofloxacin
CYP 3A4- und/oder CYP 1A2-Induktoren
Arzneimittel, die den Stoffwechsel, die Leberdurchblutung, das Herzzeitvolumen oder die periphere Distribution von Lidocain verändern, können die Plasmakonzentrationen von Lidocain verändern.
Andere pharmakokinetische Interaktionen
Arzneimittel, die den Stoffwechsel, die Leberdurchblutung, das Herzzeitvolumen oder die periphere Distribution von Lidocain verändern, können die Plasmakonzentrationen von Lidocain verändern.
Arzneimittel, die eine Hypokaliämie verursachen
Die elektrophysiologischen Wirkungen von Lidocain hängen stark von der extrazellulären Kaliumkonzentration ab und können durch eine Hypokaliämie fast vollständig blockiert werden. Die gleichzeitige Anwendung von Arzneimitteln, die eine schwere Hypokaliämie verursachen können (z. B. Acetazolamid, Schleifendiuretika und Thiazide), sollte daher vermieden werden oder nur unter sorgfältiger Überwachung der Kaliumkonzentration im Serum erfolgen.
Schwangerschaft, StillzeitSchwangerschaft
Es liegen keine ausreichenden Daten über die Anwendung von Lidocain bei Schwangeren vor.
Lidocain passiert die Plazentaschranke (siehe Abschnitt «Pharmakokinetik»). Es ist davon auszugehen, dass eine grosse Zahl schwangerer Frauen und Frauen im gebärfähigen Alter Lidocain erhielten. Bisher wurden keine spezifischen Störungen des Fortpflanzungsprozesses gemeldet, beispielsweise kein erhöhtes Auftreten von Missbildungen oder direkte oder indirekte Auswirkungen auf den Fötus. Jedoch sind die Risiken für den Menschen noch nicht vollständig untersucht.
Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt (siehe Abschnitt «Präklinische Daten»).
Das Nutzen-Risiko-Verhältnis einer kurzfristigen Anwendung während der Schwangerschaft und Geburt sollte sorgfältig geprüft werden.
Stillzeit
Lidocain geht in geringen Mengen in die Muttermilch über. Bei Anwendung in den empfohlenen Dosen sind Auswirkungen auf den Säugling unwahrscheinlich. Daher kann während der Behandlung mit Lidocain weiterhin gestillt werden.
Fruchtbarkeit
Es liegen keine Daten zur Wirkung von Lidocain auf die Fertilität beim Menschen vor.
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von MaschinenRyligency hat einen mässigen Einfluss auf die Fahrtüchtigkeit oder die Fähigkeit, Maschinen zu bedienen. Deshalb muss der Arzt nach Anwendung von Lidocain entscheiden, ob der Patient in der Lage ist, aktiv am Strassenverkehr teilzunehmen oder Maschinen zu bedienen.
Unerwünschte WirkungenZusammenfassung des Sicherheitsprofils
Häufigkeit und Schweregrad der unerwünschten Wirkungen von Lidocain hängen von Dosis, Art der Anwendung und der individuellen Empfindlichkeit des Patienten ab.
Bei Lidocain-Plasmakonzentrationen über 5–10 mg/l sind systemische unerwünschte Wirkungen zu erwarten. Diese äussern sich in ZNS- und kardiovaskulären Symptomen.
Tabellarische Auflistung der unerwünschten Wirkungen
Unerwünschte Wirkungen werden nach MedDRA-Systemorganklasse und Häufigkeit anhand der folgenden Konvention klassifiziert: Sehr häufig (≥1/10); häufig (≥1/100 bis < 1/10); gelegentlich (≥1/1000 bis < 1/100); selten (≥1/10.000 bis < 1/1.000); sehr selten (< 1/10000); nicht bekannt (kann aus den verfügbaren Daten nicht abgeschätzt werden).
In der folgenden Tabelle sind unerwünschte Wirkungen aufgeführt, die mit der Verwendung von Lidocain als Antiarrhythmikum verbunden sind.
|
Systemorganklassen
|
Sehr häufig
|
Häufig
|
Gelegentlich
|
Selten
|
Sehr selten
|
Nicht bekannt
| |
Störungen des Blut- und Lymphsystems
|
|
|
|
|
|
Methämoglobinämie
| |
Störungen des Immunsystems
|
|
|
|
Anaphylaktische Reaktionen äussern sich durch Urtikaria, Ödeme, Bronchospasmen, Atemnot und Kreislaufbeschwerden bis hin zum anaphylaktischen Schock.
|
|
| |
Psychiatrische Erkrankungen
|
Dysphorie.
|
Verwirrtheit, Unruhe, Reizbarkeit, Euphorie,Halluzinationen und Depression.
|
|
|
|
| |
Erkrankungen des Nervensystems
|
|
Schläfrigkeit, Benommenheit, Schwindel, Dysarthrie, Tinnitus, Zittern, Kribbeln und Parästhesien (Haut), verschwommene Sicht
|
|
Muskelzucken bis hin zu generalisierten Konvulsionen, Bewusstseinsstörungen bis hin zum Koma
|
|
| |
Herzerkrankungen
|
|
|
|
Bradykardie, AV-Block bis hin zum Herzstillstand
|
Ventrikuläre Tachykardie
|
| |
Gefässerkrankungen
|
|
|
|
Hypotonie
|
|
| |
Erkrankungen der Atemwege, des Brustraums und Mediastinums
|
|
|
|
Atemdepression bis hin zum -stillstand
|
|
| |
Erkrankungen des Gastrointestinaltrakts
|
Übelkeit, Erbrechen, Dysphagie.
|
|
|
|
|
|
Weitere spezifische Populationen
Bei älteren Menschen kann die Inzidenz von unerwünschten Wirkungen erhöht sein.
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von grosser Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdacht einer neuen oder schwerwiegenden Nebenwirkung über das Online-Portal ElViS (Electronic Vigilance System) anzuzeigen. Informationen dazu finden Sie unter www.swissmedic.ch.
ÜberdosierungAbhängig von der individuellen Empfindlichkeit kommt es ab einer Konzentration von etwa 5 – 10 mg Lidocain pro Liter venösem Blut zu toxischen Reaktionen.
Die letale Plasmakonzentration beim Menschen liegt im Bereich von 6 – 33 mg Lidocain pro Liter.
Eine Überdosierung führt zu Anzeichen einer akuten Toxizität, die zu sehr schwerwiegenden unerwünschten Wirkungen führen kann. Die toxischen Wirkungen von Lidocain hängen von der Höhe der Plasmakonzentration ab; je höher die Plasmakonzentration und je schneller ihr Anstieg, desto häufiger und schwerwiegender sind die toxischen Reaktionen. Derartige toxischen Reaktionen wirken sich auf das Zentralnervensystem und das Herz-Kreislauf-System aus.
Symptome
Leichte toxische Überdosierungen von Lidocain führen zu einer ZNS-Stimulation. Eine starke Überdosierung, die zu hohen toxischen Plasmakonzentrationen führt, verursacht eine Depression der zentralen Funktionen.
Die ZNS-Toxizität ist eine abgestufte Reaktion mit Symptomen und Anzeichen von ansteigendem Schweregrad.
Die ersten beobachteten Symptome sind wie folgt: Benommenheit, Schwindel, Erregung, Halluzination, Euphorie, Angst, Gähnen, Logorrhö, Kopfschmerzen, Übelkeit, Erbrechen, Parästhesie der Lippen, Taubheitsgefühl an der Zunge, Tinnitus und Dysarthrie, Hör- und Sehstörungen.
Zu den weiteren subjektiven Symptomen des Zentralnervensystems gehören: Orientierungslosigkeit, gelegentliches Schläfrigkeitsgefühl. Es wurden auch Fälle von Tachykardie, Bluthochdruck und Gesichtsrötung berichtet.
Bei diesen Alarmzeichen ist eine sorgfältige Überwachung erforderlich: Muskelzucken, Tremor, Schüttelfrost und generalisierte Krampfanfälle.
Bei Verabreichung sehr hoher Dosen: generalisierte ZNS-Depression, Atemdepression, Koma und Atemstillstand.
In schweren Fällen kann eine kardiovaskuläre Toxizität auftreten: Herzrhythmusstörungen (wie z. B. ventrikuläre Extrasystolen, Kammerflimmern), nicht tastbarer Puls, Blässe, erhebliche Bradykardie, atrioventrikuläre Erregungsleitungsstörungen, Abnahme der kardialen Kontraktilität, Hypotonie und Herzstillstand.
Behandlung
Bei Anzeichen einer akuten Toxizität während der Anwendung von RYLIGENCY ist die Verabreichung des Produktes umgehend zu beenden. Da Lidocain auch als Lokalanästhetikum wirkt, sollte intravenöse Flüssigkeit gegeben werden, um eine Hypoxie und Azidose zu vermeiden, die die lokalanästhetische systemische Toxizität (LAST) verstärken und die Progression zu Herz-Kreislauf- Kollaps und Krampfanfällen begünstigen.
Bei Krämpfen und ZNS-Depression ist eine Behandlung erforderlich, um die Sauerstoffversorgung aufrechtzuerhalten, die Krämpfe zu stoppen und die Durchblutung zu unterstützen. Um die Krämpfe zu stoppen, muss sofort eine Beatmung mit reinem Sauerstoff durch eine Maske eingeleitet werden: Dies ist in einigen Fällen ausreichend, um die Krämpfe zu stoppen. Ausserdem ist darauf zu achten, dass die Atemwege frei sind.
Falls erforderlich, sollte sofort eine kardiopulmonale Reanimation eingeleitet werden.
Falls die Krampfanfälle nicht aufhören, muss umgehend intravenös ein Antikonvulsivum wie Thiopental oder ein Benzodiazepin (Diazepam oder Midazolam) verabreicht werden. Die Verabreichung einer intravenösen Lipidemulsion sollte in Erwägung gezogen werden. Zur Sicherstellung einer Muskelrelaxation wird intravenöses Succinylcholin verwendet, sofern der Arzt eine endotracheale Intubation durchführen und einen vollständig paralysierten Patienten versorgen kann.
Nach Abklingen der Krampfanfälle und bei ausreichender Lungenventilation ist gewöhnlich keine weitere Behandlung erforderlich. Im Fall einer Hypotonie sollte jedoch eine geeignete Behandlung mit einem intravenösen Vasopressor in Erwägung gezogen werden. Eine durch einen erhöhten Vagotonus verursachte Bradykardie sollte mit intravenös verabreichtem Atropin behandelt werden.
Patienten mit offensichtlichen Anzeichen von LAST sollten mindestens 12 Stunden lang überwacht werden, da eine kardiovaskuläre Depression nach der Behandlung bestehen bleiben oder erneut auftreten kann.
Zentral wirkende Analeptika sind kontraindiziert.
Es existiert kein spezifisches Gegenmittel.
Lidocain kann nicht mittels Hämodialyse entfernt werden.
Eigenschaften/WirkungenATC-Code
C01BB01
Pharmakotherapeutische Gruppe: Antiarrhythmika der Klasse Ib.
Lidocain ist ein Antiarrhythmikum der Klasse Ib nach der Klassifikation von Vaughan Williams.
Wirkmechanismus/Pharmakodynamik
Es wurde gezeigt, dass Lidocain ventrikuläre Arrhythmien aufgrund des Wiedereintrittsphänomens in der späten Myokardphase beseitigt, indem es den Wiedereintrittsleitungsweg unterdrückt und blockiert.
Die antiarrhythmische Wirkung von Lidocain ist bei erhöhter Erregungsfrequenz (z. B. bei Hyperkaliämie und/oder Myokardischämie) aufgrund der schnelleren Bindung von Natriumkanälen mit Lidocain besonders ausgeprägt. In Situationen mit Hyperpolarisation, z. B. infolge einer Hypokaliämie, ist die Wirkung von Lidocain reduziert.
Studien haben gezeigt, dass Lidocain die diastolische Depolarisation der Phase 4 abschwächt, den Automatismus reduziert und eine Abnahme (aber manchmal keine Veränderung) der Erregbarkeit und Membranreaktivität verursacht.
Die Aktionspotentialdauer (APD) und die effektive Refraktärzeit (ERP) der Purkinje-Fasern und des ventrikulären Myokards werden reduziert, während das ERP/APD-Verhältnis erhöht wird. Lidocain erhöht die Erregbarkeits- und Flimmerschwellen des Myokards.
Es wurden keine signifikanten Interaktionen zwischen Lidocain und dem autonomen Nervensystem beschrieben und daher hat Lidocain nur minimale bis gar keine Auswirkungen auf den Tonus des autonomen Nervensystems. Klinische Untersuchungen zur Elektrophysiologie mit Lidocain ergaben keine Änderung der Erholungszeit des Sinusknotens oder der sinuatrialen Überleitungszeit. Die Überleitungszeit im AV- Knoten bleibt unverändert oder verkürzt sich und die His-Purkinje-Überleitungszeit bleibt unverändert. Normalerweise bewirkt Lidocain keine EKG-Veränderungen. Das QT-Intervall kann jedoch manchmal geringfügig verkürzt sein.
Therapeutische Plasmakonzentrationen sollten zwischen 1,5 und 5 Mikrogramm/ml liegen. Über 5 Mikrogramm/ml ist mit toxischen Wirkungen auf das ZNS und das Herz-Kreislauf-System zu rechnen.
Klinische Wirksamkeit
Keine Daten verfügbar.
PharmakokinetikAbsorption
Nach intravenöser Verabreichung beträgt die Bioverfügbarkeit 100 %.
Nach intravenöser Verabreichung setzt die therapeutische Wirkung von Lidocain schnell ein. Therapeutische Plasmakonzentrationen (1,5 – 5 Mikrogramm/ml) werden innerhalb von 1 bis 2 Minuten erreicht. Der Effekt einer Bolusinjektion hält 10 – 20 Min. an. Um die therapeutische Wirkung von Lidocain aufrechtzuerhalten, muss die Verabreichung fortgesetzt werden und erfolgt dann durch intravenöse Infusion.
Nach kontinuierlicher Infusion und sofern keine Sättigungsdosis verabreicht wird, erreicht die Plasmakonzentration frühestens 5 Stunden (zwischen 5 und 10 Stunden) nach Beginn der Infusion einen Steady-State. Therapeutische Konzentrationen werden jedoch bereits nach 30 bis 60 Minuten erreicht.
Distribution
Lidocain folgt einer biphasischen Eliminationskinetik. Nach intravenöser Verabreichung verteilt sich der Wirkstoff zuerst schnell von dem zentralen Kompartiment in stark durchblutete Gewebe und Organe (Alpha-Distributionsphase). Auf diese Phase folgt eine Umdistribution in die Skelettmuskulatur und das Fettgewebe. Die Halbwertszeit während der Alpha-Distributionsphase beträgt etwa 4 – 8 Minuten. Die Distribution in periphere Gewebe erfolgt voraussichtlich innerhalb von 15 Minuten.
Die Plasmaproteinbindungsrate beträgt bei Erwachsenen etwa 60–80 %. Sie hängt von der Wirkstoffkonzentration und der Konzentration des sauren Alpha-1-Glykoproteins (AGP) ab. AGP ist ein Akute-Phase-Protein, das freies Lidocain bindet und je nach pathophysiologischem Zustand des Patienten beispielsweise nach Traumata, Operationen oder Verbrennungen erhöht sein kann. Im Gegensatz dazu wurde gezeigt, dass die AAG-Konzentrationen bei Neugeborenen und bei Patienten mit Leberfunktionsstörungen niedrig sind, was zu einer deutlichen Abnahme der Plasmaproteinbindung von Lidocain führt.
Das Distributionsvolumen im Steady State beträgt 91 Liter. Das Distributionsvolumen kann bei Patienten mit weiteren Erkrankungen verändert sein, z. B. bei Patienten mit Herzinsuffizienz, Leberinsuffizienz oder Niereninsuffizienz.
Metabolismus
Lidocain wird in der Leber schnell durch Monooxygenasen metabolisiert; dies erfolgt in erster Linie durch die oxidative N-Desalkylierung, die Hydroxylierung am aromatischen Ring und die Hydrolyse der Amidbindung. Hydroxylderivate unterliegen einer Konjugation.
Insgesamt werden etwa 90 % des Lidocains zu 4-Hydroxy-2,6-Xylidin, 4-Hydroxy-2,6-Xylidinglucuronid und in geringerem Masse zu den aktiven Metaboliten Monoethylglycinxylidid (MEGX) und Glycin-Xylidid (GX) verstoffwechselt.
Die letztgenannten Metaboliten können sich aufgrund ihrer im Vergleich zu Lidocain längeren Halbwertszeit bei länger dauernden Infusionen oder bei schwerer Niereninsuffizienz anreichern. Bei Lebererkrankungen kann die Metabolisierungsrate auf 10 bis 50 % des Normalwerts abfallen.
Ergebnisse mit menschlichen Lebermikrosomen und rekombinanten menschlichen CYP-Isoformen zeigten, dass die Enzyme CYP1A2 und CYP3A4 die wichtigsten CYP-Isoformen sind, die an der N-Deethylierung von Lidocain beteiligt sind.
Elimination
Weniger als 10 % der Lidocain-Dosis werden unverändert im Urin ausgeschieden. Der restliche Anteil wird in Form von Metaboliten eliminiert.
Die Eliminationshalbwertszeit beträgt bei Erwachsenen 1,5 – 2 Stunden und bei Neugeborenen etwa 3 Stunden. Die Eliminationshalbwertszeit kann bei schwerer Herzinsuffizienz (bis zu 4 – 12 Stunden) oder chronischer Lebererkrankung (bis zu 4,5 – 6 Stunden) verlängert sein.
Die Halbwertszeiten der aktiven Metaboliten Monoethylglycinxylidid (MEGX) und Glycinxylidid (GX) betragen 2–6 Stunden bzw. 10 Stunden. Da ihre Plasmahalbwertszeit länger ist als die von Lidocain, ist bei längerer Infusion eine Akkumulation von Metaboliten, insbesondere GX, möglich.
Die Eliminationsrate ist zudem pH-abhängig und kann durch Ansäuerung des Harns erhöht werden. Die Plasma-Clearance liegt bei 0,95 ml/min.
Die Leberdurchblutung scheint den Lidocain-Metabolismus zu limitieren.
Kinetik spezieller Patientengruppen
Patienten mit Niereninsuffizienz
Die Plasma-Halbwertszeit von Lidocain scheint bei diesen Patienten unverändert zu sein. Lediglich bei einer Infusion über 12 Stunden oder länger kam es zu einer gewissen Kumulation von GX. Diese Kumulation stand offenbar in Zusammenhang mit der langdauernden Verabreichung des Arzneimittels. Allerdings war bei Patienten mit schwerer Nierenfunktionsstörung die Lidocain-Clearance etwa halbiert und die Halbwertszeit von Lidocain etwa doppelt so hoch wie bei gesunden Probanden.
Patienten mit Leberinsuffizienz
Die Plasmahalbwertszeit von Lidocain und seinen Metaboliten kann verlängert sein und es ist mit erheblichen Auswirkungen auf die Pharmakokinetik zu rechnen. Eine Dosisanpassung ist bei Patienten mit eingeschränkter Leberperfusion erforderlich, z. B. nach einem akuten Herzinfarkt, bei Herzinsuffizienz oder Lebererkrankungen.
Ältere Patienten
Die Eliminationshalbwertszeit und das Distributionsvolumen können bei älteren Patienten aufgrund einer verminderten Herzleistung und/oder einer verringerten Leberdurchblutung verlängert sein.
Schwangere oder Stillzeit
Lidocain passiert die Placentaschranke durch einfache Diffusion und erreicht innerhalb weniger Minuten nach der Verabreichung den Fötus.
Der Fötus kann Lidocain metabolisieren. Die Spiegel im fötalen Blut betragen etwa 60 % der Konzentrationen im mütterlichen Blut. Aufgrund einer geringeren Plasmaproteinbindung im fötalen Blut beträgt die Konzentration von pharmakologisch aktivem freiem Lidocain etwa das 1,4-Fache der mütterlichen Konzentration.
Lidocain geht nur in geringen Mengen in die Muttermilch über.
Präklinische DatenIn tierexperimentellen Studien führte die nach Verabreichung hoher Lidocain-Dosen berichtete Toxizität zu Auswirkungen auf das ZNS und das Herz-Kreislauf-System.
Lidocain zeigte in In-vitro- und In-vivo-Genotoxizitätsstudien kein genotoxisches Potenzial. Jedoch war für 2,6-Xylidin, einen Metaboliten von Lidocain, eine genotoxische Aktivität nachweisbar.
Es wurden keine Krebsstudien mit Lidocain durchgeführt. In klinischen toxikologischen Studien zur Bewertung chronischer Exposition wurde gezeigt, dass 2,6-Xylidin ein kanzerogenes Potenzial hat. Die klinische Relevanz dieser Befunde ist nicht bekannt.
In Studien zur Reproduktionstoxizität wurden bei Kaninchen in Dosen von 25 mg/kg s.c. embryotoxische oder fetotoxische Effekte von Lidocain festgestellt. Bei Ratten hat Lidocain in Dosen, die unter den maternaltoxischen Werten liegen, keinen Einfluss auf die postnatale Entwicklung der Nachkommen. Eine Beeinträchtigung der Fertilität männlicher oder weiblicher Ratten durch Lidocain wurde nicht beobachtet.
Lidocain passiert die Placentaschranke durch einfache Diffusion (siehe Abschnitt «Pharmakokinetik»).
Sonstige HinweiseInkompatibilitäten
Da keine Kompatibilitätsstudien durchgeführt wurden, darf das Arzneimittel nicht mit anderen Arzneimitteln gemischt werden.
Haltbarkeit
3 Jahre
Das Arzneimittel darf nur bis zu dem auf der Packung mit «EXP» bezeichneten Datum verwendet werden.
Nach dem Öffnen muss das Arzneimittel sofort verwendet werden.
Besondere Lagerungshinweise
Ausser Reichweite von Kindern aufbewahren.
Einmaliger Gebrauch bei einem einzelnen Patienten. Die Spritze nach Gebrauch entsorgen. Nicht verwenden, wenn die Verschlussspitze der Fertigspritze beschädigt ist. Die Aussenfläche der Spritze ist bis zum Öffnen der Blisterpackung steril.
In der Originalverpackung aufbewahren. Bei 15–30 °C lagern. Die Fertigspritze bis zur Verwendung im ungeöffneten Blister aufbewahren. Nicht einfrieren.
Hinweise für die Handhabung
Gebrauchsanleitung:
Die Fertigspritze bitte sorgfältig wie folgt vorbereiten.
Die Fertigspritze ist nur zur Verwendung bei einem einzelnen Patienten bestimmt. Die Fertigspritze nach Gebrauch entsorgen. NICHT WIEDERVERWENDEN.
Der Inhalt der ungeöffneten und unbeschädigten Blisterpackung ist steril und darf bis zur Verwendung nicht geöffnet werden.
Das Arzneimittel sollte vor der Verabreichung visuell auf Schwebeteilchen und Verfärbungen geprüft werden. Es darf nur klare und farblose Lösung frei von Schwebeteilchen oder Ausfällungen verwendet werden.
Das Arzneimittel darf nicht verwendet werden, wenn der Originalitätsverschluss auf der Spritze beschädigt ist.
Die Aussenfläche der Fertigspritze ist bis zum Öffnen der Blisterpackung steril.
Bei Handhabung unter aseptischen Bedingungen kann dieses Arzneimittel auf eine sterile Fläche gelegt werden.
|
1) Die Fertigspritze aus der sterilen Blisterpackung entnehmen.
| |
|
|
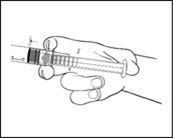
2) Auf den Kolben drücken, um den Stopfen zu lösen. Der Sterilisationsprozess kann zur Adhäsion des Stopfens an den Körper der Fertigspritze geführt haben.
| |
|
|
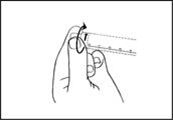
3) Den Deckel abdrehen, um den Verschluss aufzubrechen. Die exponierte Luer-Verbindung nicht berühren, um eine Kontamination zu vermeiden.
| |
|
|
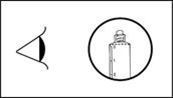
4) Überprüfen, dass die Spitze des Verschlusses der Fertigspritze vollständig entfernt wurde. Falls dies nicht der Fall ist, den Deckel wieder aufsetzen und erneut abdrehen.
| |
|
|
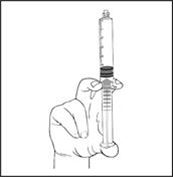
5) Durch vorsichtiges Drücken des Kolbens die Luft entfernen.
| |
6) Die Fertigspritze an den intravenösen Zugang anschliessen. Den Kolben langsam herunterdrücken, um das benötigte Volumen zu injizieren.
|
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu entsorgen.
Zulassungsnummer69478 (Swissmedic)
Packungen5-ml-Fertigspritze aus Polypropylen, einzeln im Blister verpackt. Die Fertigspritze ist mittels eines selbstklebenden Etiketts von 0 bis 5 ml (in 0,5-ml-Schritten) abgestuft.
Karton mit 1 oder 10 Fertigspritzen (B).
Es werden möglicherweise nicht alle Packungen in den Verkehr gebracht.
ZulassungsinhaberinAguettant Suisse SA
Route de Jussy 35
1226 Thônex
Schweiz
Stand der InformationJanuar 2024
|




