Mekinist® Pulver zur Herstellung einer Lösung zum Einnehmen
Was ist MEKINIST und wann wird es angewendet?
Mekinist enthält den Wirkstoff Trametinib und hemmt das Wachstum von Krebszellen. Es wird in Kombination mit Tafinlar (Dabrafenib) angewendet zur Behandlung von:
·Melanomen (einer Form von Hautkrebs), die auf andere Bereiche des Körpers übergegriffen haben oder chirurgisch nicht entfernt werden können.
·bei Patienten, deren Melanom chirurgisch entfernt werden konnte, zur Verhinderung eines erneut auftretenden Melanoms.
·einer Form von Lungenkarzinom (nicht-kleinzelliges Lungenkarzinom (NSCLC)).
·Gliomen, einer Art von Gehirntumoren, bei Kindern ab 1 Jahr, die nach alternativen Behandlungsoptionen eine weitere Behandlung erfordern.
·erwachsenen Patienten, bei denen ein nicht resezierbarer oder metastasierter solider Tumor mit einer BRAF-V600E-Mutation vorliegt, der nach einer früheren Behandlung fortgeschritten ist und für den es keine zufriedenstellenden alternative Behandlungsmöglichkeite gibt.
Mekinist ist in zwei Darreichungsformen erhältlich: als Pulver zur Herstellung einer Lösung zum Einnehmen (vor allem für Kinder geeignet) und als Filmtablette (für Erwachsene geeignet). Diese Packungsbeilage beschreibt Mekinist als Pulver zur Herstellung einer Lösung zum Einnehmen.
In dieser Packungsbeilage wird auch auf die aktive Substanz Dabrafenib (Handelsname Tafinlar) Bezug genommen, da diese in Kombination mit Mekinist (Trametinib) verabreicht wird. Lesen Sie bitte neben dieser Packungsbeilage auch die Packungsbeilage für Tafinlar (Dabrafenib) sorgfältig durch.
Mekinist in Kombination mit Tafinlar (Dabrafenib) kann nur bei Personen angewendet werden, deren Krebs eine bestimmte Veränderung (Mutation) am so genannten BRAF-Gen aufweist. Mekinist in Kombination mit Dabrafenib wirkt auf Proteine (Eiweissstoffe), die der Körper aufgrund dieses veränderten Gens herstellt, und verlangsamt oder stoppt damit die Entwicklung Ihrer Krebserkrankung. Ihr Arzt bzw. Ihre Ärztin entnimmt eine Probe des Tumorgewebes, um zu prüfen, ob in Ihrem Fall die Behandlung mit Mekinist möglich ist.
Auf Verschreibung des Arztes oder der Ärztin.
Wann darf MEKINIST nicht eingenommen werden?
Wenn Sie auf die Wirkstoffe oder sonstige Bestandteile allergisch reagieren.
Wann ist bei der Einnahme von MEKINIST Vorsicht geboten?
Falls Ihr Krebs mit einer Kombination von Mekinist und Tafinlar (Dabrafenib) behandelt wird, lesen Sie bitte auch die Packungsbeilage zu Tafinlar (Dabrafenib) sorgfältig durch. Mekinist in Kombination mit Dabrafenib darf bei Patienten mit kolorektalem Karzinom nicht angewendet werden.
Bevor und während Sie Mekinist einnehmen, muss Ihr Arzt/ Ihre Ärztin wissen:
·ob Sie Herzprobleme haben, z.B. Herzinsuffizienz oder Probleme mit Ihrem Herzschlag, so dass sie kurzatmig sind, beim Liegen Atembeschwerden haben, ein Anschwellen der Beine und Füsse bemerken. Ihr Arzt sollte Ihre Herzfunktion vor Beginn der Behandlung mit Mekinist und während der Behandlung untersuchen;
·ob Sie Augenprobleme haben, z.B. eine Blockade der Vene, die zur Flüssigkeitsansammlung im Auge führt (Netzhautvenenverschluss) oder eine Schwellung im Auge, die vielleicht durch einen Flüssigkeitsstau verursacht wird (Chorioretinopathie), Sehen von Lichtblitzen, Verlust des Sehvermögens (Ablösung des Netzhautpigmentepithels/Netzhautablösung). Dies kann sich z.B. durch Verschwommensehen oder andere Sehstörungen äussern. Bevor und während Sie Mekinist einnehmen, kann Ihr Arzt für Sie eine Augenuntersuchung organisieren;
·ob Sie ein Augenproblem mit der Bezeichnung Uveitis haben (es handelt es sich dabei um eine Entzündung der inneren Augenhaut). Symptome sind:
·Rötung und Reizung der Augen
·verschwommene Sicht
·Augenschmerzen
·verstärkte Lichtempfindlichkeit
·schwebende Punkte vor dem Auge
·ob Sie Nierenprobleme haben oder früher schon einmal hatten;
·ob Sie Probleme mit Ihrer Haut haben, z.B. einen Hautausschlag oder akneartige Erscheinungen;
·ob Sie Diabetes (Zuckerkrankheit) oder erhöhte Blutzuckerwerte haben. Ihr Arzt/ Ihre Ärztin wird in diesem Fall Ihre Blutzuckerwerte engmaschiger überwachen.
·ob Sie Lungen- oder Atemprobleme haben, z.B. Atemschwierigkeiten, häufig begleitet von Ohnmacht, schnellem Herzschlag, bläulicher Verfärbung der Haut oder Brustschmerzen. Ihr Arzt ordnet möglicherweise vor Beginn der Behandlung mit Mekinist einen Lungenfunktionstest an. Wenn diese Anzeichen während der Behandlung auftreten oder sich verschlechtern, so konsultieren Sie sofort Ihren Arzt bzw. Ihre Ärztin;
·ob Sie anhaltend hohe Körpertemperatur bekommen, die von starkem Schüttelfrost, Dehydration (Austrocknung) und niedrigem Blutdruck begleitet sein können. Wenn Sie Fieber ab 38 °C entwickeln, kontaktieren Sie unverzüglich Ihren Arzt bzw. Ihre Ärztin. Er wird Tests durchführen, um herauszufinden, ob es andere Ursachen für das Fieber gibt, und das Problem behandeln;
·Während und nach schweren Fieberereignissen können einige Substanzen (Enzyme) abnormale erhöhte Werte aufweisen, Ihr Arzt wird die Enzymwerte messen und überprüfen, ob Ihre Nieren richtig funktionieren.
·ob Sie bei sich Hautveränderungen bemerken, z. B.:
·neue Warzen
·raue Haut oder rötliche Erhebungen, die bluten oder nicht abheilen
·Änderung von Grösse oder Farbe eines Leberflecks.
Vor und während der Behandlung mit Mekinist in Kombination mit Tafinlar wird Ihr Arzt bzw. Ihre Ärztin regelmässige Hautuntersuchungen durchführen.
·Wenn bei Ihnen Blutungen auftreten, insbesondere, wenn bei Ihnen folgende Anzeichen einer intrakraniellen Blutung auftreten: Benommenheit, Übelkeit, Erbrechen, Schwindel, extrem starke Kopfschmerzen und Nackensteifigkeit
·wenn bei Ihnen Brustschmerzen, plötzliche Kurzatmigkeit, Atembeschwerden, Schmerzen in den Beinen mit oder ohne Schwellung, eine Schwellung an Arm oder Bein oder ein kühler, blasser Arm bzw. ein kühles, blasses Bein auftreten, da es sich dabei um Anzeichen eines Blutgerinnsels in den Venen des Armes oder Beines, der Lunge oder anderer Körperteile handeln kann.
·wenn bei Ihnen gleichzeitig mehrere Symptome wie Fieber, geschwollene Drüsen, Blutergüsse oder Hautausschlag auftreten. Diese können Anzeichen für eine hämophagozytische Lymphohistiozytose (HLH) sein, eine Erkrankung, bei der das Immunsystem zu viele Zellen zur Infektionsbekämpfung (so genannte Histiozyten und Lymphozyten) produziert.
·wenn bei Ihnen mehrere Symptome wie unregelmässiger Herzschlag, Abnahme der Urinausscheidung, Verwirrtheit, starke Übelkeit und Erbrechen, Kurzatmigkeit, Muskelkrämpfe oder -zuckungen gleichzeitig auftreten, die Anzeichen für ein Tumorlysesyndrom oder TLS sein können, ein Krankheitsbild, das durch einen schnellen Abbau von Krebszellen entsteht.
·wenn Sie Durchfall, Bauchschmerzen und Fieber bekommen. Dies sind mögliche Symptome einer Entzündung des Dickdarms.
·wenn bei Ihnen Magenschmerzen, Übelkeit, Erbrechen von Blut, schwarzer oder blutiger Stuhl auftreten. Das sind mögliche Symptome einer Perforation des Magens oder der Darmwand (Magen-/Darmdurchbruch).
·ob Sie an einer Tiefenvenenthrombose leiden. Mögliche Anzeichen können Schwellungen, rötliche oder bläuliche Verfärbungen, Wärmegefühl, Schmerzen, sowie ein Ziehen oder Spannungsgefühl in den Beinen oder Beschwerden ähnlich wie bei einem Muskelkater sein. Wenn Sie diese Anzeichen bei sich feststellen, kontaktieren Sie unverzüglich Ihren Arzt bzw. Ihre Ärztin.
·wenn bei Ihnen schwere Nebenwirkungen an der Haut auftreten:
·Ausschlag, rote Haut, Blasenbildung an Lippen, Augen oder Mund, Hautschälung mit oder ohne Fieber; dabei kann es sich um mögliche Anzeichen eines Stevens-Johnson-Syndroms handeln.
·ausgedehnter Hautausschlag, Fieber und vergrösserte Lymphknoten (dabei kann es sich um Anzeichen eines Arzneimittelexanthems mit Eosinophilie und systemischen Symptomen (DRESS) handeln.
Sprechen Sie mit Ihrem Arzt bzw. Ihrer Ärztin, wenn Sie glauben, dass eine der genannten Erkrankungen bei Ihnen vorliegt oder während der Therapie mit Mekinist und Tafinlar (Dabrafenib) auftritt.
Fertilität: Mekinist kann die Fortpflanzungsfähigkeit sowohl von Männern als auch von Frauen beeinträchtigen. Männliche Patienten (auch solche, bei denen eine Vasektomie durchgeführt wurde) mit Partnerinnen, die schwanger sind oder werden könnten, sollten während der Behandlung sowie für mindestens 16 Wochen nach dem Absetzen von Mekinist beim Geschlechtsverkehr Kondome verwenden.
Mekinist kann zu einer Verschlechterung bestimmter vorbestehender Erkrankungen führen oder schwerwiegende Nebenwirkungen hervorrufen. Sie müssen daher wissen, auf welche wichtigen Anzeichen und Symptome Sie während der Behandlung mit Mekinist achten müssen (siehe auch: «Welche Nebenwirkungen kann Mekinist haben?»).
Wechselwirkungen mit anderen Arzneimitteln
Teilen Sie Ihrem Arzt bzw. Ihrer Ärztin mit, wenn Sie kürzlich andere Arzneimittel eingenommen haben oder beabsichtigen, andere Arzneimittel einzunehmen. Dazu gehören auch Arzneimittel, die nicht verschreibungspflichtig sind.
Führen Sie eine Liste der Arzneimittel, die Sie anwenden, und legen Sie diese Ihrem Arzt bzw. Ihrer Ärztin vor, wenn Sie ein neues Arzneimittel bekommen.
Informieren Sie Ihren Arzt, Apotheker bzw. Ihre Ärztin, Apothekerin wenn Sie an anderen Krankheiten leiden, Allergien haben oder andere Arzneimittel (auch selbst gekaufte!) einnehmen.
Hilfsstoffe
Sulfobutylbetadex-Natrium
Dieses Arzneimittel enthält 100 mg Cyclodextrin pro mL. Wenden Sie dieses Arzneimittel nicht bei Kindern unter 2 Jahren an, es sei denn, Ihr Arzt bzw. Ihre Ärztin hat es empfohlen.
Methylparahydroxybenzoat (E218)
Kann allergische Reaktionen, auch Spätreaktionen, hervorrufen.
Kalium
Dieses Arzneimittel enthält Kalium, jedoch weniger als 1 mmol (39 mg) Kalium pro 2 mg Trametinib (Maximaldosis), d.h. es ist nahezu «kaliumfrei»
Natrium
Dieses Arzneimittel enthält 79.2 mg Natrium (Hauptbestandteil von Kochsalz/Speisesalz) pro 2 mg Trametinib (Maximaldosis). Dies entspricht 4% der für eine oder einen Erwachsenen empfohlenen maximalen täglichen Natriumaufnahmemit der Nahrung.
Darf MEKINIST während einer Schwangerschaft oder in der Stillzeit eingenommen / angewendet werden?
Mekinist sollte während der Schwangerschaft nicht angewendet werden, es sei denn, es ist klar notwendig. Vor Beginn der Behandlung soll ein Schwangerschaftstest durchgeführt werden.
Informieren Sie vor Beginn der Behandlung Ihren Arzt oder Ihre Ärztin, wenn Sie schwanger sind oder wenn Sie vermuten, schwanger zu sein, oder beabsichtigen, schwanger zu werden. Mekinist kann dem Ungeborenen schaden.
Frauen im gebärfähigen Alter müssen während der Behandlung mit Mekinist sowie in den ersten 4 Monaten nach Behandlungsende eine zuverlässige Methode zur Empfängnisverhütung (Kontrazeption) anwenden.
Da Sie Mekinist in Kombination mit Tafinlar (Dabrafenib) anwenden, ist eine hormonelle Empfängnisverhütung (z.B. die Pille, Injektionen oder Pflaster) möglicherweise nicht wirksam. Deshalb müssen Sie eine andere zuverlässige Methode der Empfängnisverhütung anwenden, z.B. Kondome, damit Sie während der Einnahme von Mekinist nicht schwanger werden. Bitten Sie Ihren Arzt oder Ihre Ärztin um Rat.
Tritt während der Behandlung mit Mekinist eine Schwangerschaft ein, ist der Arzt bzw. die Ärztin sofort zu informieren.
Wenn Sie stillen oder beabsichtigen zu stillen, müssen Sie dies Ihrem Arzt bzw. Ihrer Ärztin mitteilen. Während der Einnahme von Mekinist sollte nicht gestillt werden. Sie und Ihr Arzt bzw. Ihre Ärztin werden darüber entscheiden, ob Sie Mekinist einnehmen oder stillen.
Wie verwenden Sie MEKINIST?
Mekinist in Kombination mit Tafinlar (Dabrafenib) wird Ihnen in der Regel von einem Tumorspezialisten bzw. einer Tumorspezialistin verschrieben und dessen/deren Anweisungen sollten streng befolgt werden.
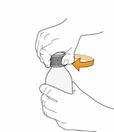
Pulver zur Herstellung einer Lösung zum Einnehmen: Bei Kindern ab 1 Jahr wird die empfohlene tägliche Dosis Mekinist entsprechend dem Körpergewicht von Ihrem Arzt bzw. Ihrer Ärztin bestimmt.Wenn Sie Mekinist als Lösung zum Einnehmen erhalten, befolgen Sie bitte die Anleitung in der Packungsbeilage zur Zubereitung und Einnahme der Mekinist Lösung zum Einnehmen. Sprechen Sie mit Ihrem Arzt oder Apotheker bzw. bei Ihrer Ärztin oder Apothekerin, wenn Sie sich nicht sicher sind.
Wenn sich bei Ihnen Nebenwirkungen einstellen, verordnet Ihr Arzt bzw. Ihre Ärztin Ihnen möglicherweise eine niedrigere Dosis, unterbricht die Behandlung oder bricht die Mekinist Therapie ganz ab. Es ist wichtig, dass Sie Mekinist und Tafinlar (Dabrafenib) nicht zusammen mit einer Mahlzeit einnehmen. Die beiden Arzneimittel sollten jeden Tag zur gleichen Tageszeit entweder mindestens eine Stunde vor oder mindestens zwei Stunden nach einer Mahlzeit eingenommen werden.
Die einmal tägliche Dosis Mekinist ist jeden Tag zur selben Uhrzeit vorzugsweise mit der morgendlichen Tafinlar (Dabrafenib)-Dosis einzunehmen. Falls Sie eine Dosis Mekinist vergessen haben und das Versäumnis innerhalb von 12 Stunden bemerken, holen Sie die Einnahme nach. Wenn bis zur nächsten planmässigen Einnahme von Mekinist weniger als 12 Stunden verbleiben, überspringen Sie die vergessene Dosis und nehmen die nächste Dosis zur gewohnten Zeit am nächsten Tag ein. Falls Sie eine Dosis Tafinlar vergessen haben, können Sie diese bis 6 Stunden vor der nächsten planmässigen Dosis nachholen. Überspringen Sie die versäumte Dosis, wenn bis zur nächsten Dosis weniger als 6 Stunden verbleiben. Fahren Sie anschliessend im gewohnten Rhythmus mit der Einnahme von Mekinist fort. Nehmen Sie nicht die doppelte Menge ein, wenn Sie die vorherige Einnahme vergessen haben. Wenn Sie zu viel Mekinist und/oder Tafinlar (Dabrafenib) eingenommen haben, wenden Sie sich bitte an Ihren Arzt bzw. Ihre Ärztin. Zeigen Sie diesen nach Möglichkeit die Mekinist- sowie die Tafinlar- (Dabrafenib) Packung.
Ändern Sie nicht von sich aus die verschriebene Dosierung. Wenn Sie glauben, das Arzneimittel wirke zu schwach oder zu stark, so sprechen Sie mit Ihrem Arzt oder Apotheker bzw. mit Ihrer Ärztin oder Apothekerin.
Setzen Sie das Arzneimittel nur auf Anweisung Ihres Arztes bzw. Ihrer Ärztin ab.
Mekinist wird bei Kindern im Alter von weniger als 1 Jahr nicht empfohlen.
Welche Nebenwirkungen kann MEKINIST haben?
Wie alle Arzneimittel kann Mekinist Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Lesen Sie auch die Packungsbeilage zu Tafinlar (Dabrafenib) sorgfältig, um sich über Nebenwirkungen wie bestimmte Typen von Hautkrebs (Plattenepithelkarzinom, andere Karzinome, neue Melanome) und Augenprobleme zu informieren.
Bei anhaltendem Fieber während der Behandlung mit Mekinist und Tafinlar (Dabrafenib) kontaktieren Sie unverzüglich Ihren Arzt bzw. Ihre Ärztin. Dieses kann zusammen mit niedrigem Blutdruck und Schwindel in Erscheinung treten. Ein Unterbruch der Behandlung ist möglicherweise notwendig, um das Fieber zu behandeln.
Achten Sie auf wichtige Anzeichen und Symptome:
Erkrankungen des Herzens
Mekinist kann die Pumpleistung Ihres Herzens beeinflussen. Bei vorbestehenden Herzleiden tritt diese Nebenwirkung mit grösserer Wahrscheinlichkeit auf. Während der Behandlung mit Mekinist werden Sie regelmässig auf Herzprobleme untersucht. Zu den Anzeichen und Symptomen eines Herzleidens gehören:
·spürbares Herzklopfen, Herzrasen oder unregelmässiger Herzschlag
·Schwindelgefühl
·Müdigkeit
·Benommenheit
·Kurzatmigkeit
·geschwollene Beine
Wenden Sie sich möglichst umgehend an Ihren Arzt bzw. Ihre Ärztin, wenn Sie eines der genannten Symptome erstmals bemerken oder eine Verschlechterung dieser Symptome feststellen.
Blutungen
Die Einnahme von Mekinist in Kombination mit Tafinlar (Dabrafenib) kann schwerwiegende Blutungen, insbesondere in Gehirn oder Magen verursachen. Rufen Sie Ihren Arzt oder Krankenpfleger bzw. Ihre Ärztin oder Krankenpflegerin an und holen Sie sich sofort medizinische Hilfe, wenn Sie ungewöhnliche Anzeichen für Blutungen haben, z. B.:
·Kopfschmerzen, Schwindel oder Schwäche
·Aufhusten von Blut oder Blutgerinnseln
·Erbrechen, wobei das Erbrochene Blut enthält oder ähnlich wie Kaffeesatz aussieht
·Nasenbluten
·roter oder schwarzer, teerähnlicher Stuhl
Augenerkrankungen (Sehstörungen)
Mekinist kann Probleme an den Augen verursachen. Mekinist wird nicht empfohlen, wenn Sie bereits einen Verschluss der Augenvene (Netzhautvenenverschluss) erlitten haben. Unter Umständen hält Ihr Arzt bzw. Ihre Ärztin vor Beginn der Behandlung mit Mekinist sowie während der Behandlung eine augenärztliche Untersuchung für angezeigt. Möglicherweise bittet Sie Ihr Arzt/Ihre Ärztin, Mekinist nicht mehr einzunehmen, oder überweist Sie an einen Facharzt/ -ärztin, wenn Sie Anzeichen und Symptome entwickeln, die Ihre Sehfunktion betreffen, z. B.:
·farbige Flecken im Gesichtsfeld
·Sehen eines verschwommenen Hofs um die Kontur eines Objekts
·verschwommene Sicht
Mögliche Nebenwirkungen wenn Mekinist zusammen mit Tafinlar eingenommen wird
Sehr häufig (betrifft mehr als einen von 10 Anwendern)
Entzündung der Nase und des Rachens, verminderter Appetit, Kopfschmerzen, Schwindelgefühl, Bluthochdruck, Blutungen (Hämorrhagie, meist leichte Blutungen, jedoch bis hin zu tödlichen Blutungen), Husten, Übelkeit, Durchfall, Erbrechen, Bauchschmerzen, Verstopfung, ungewöhnliche Leberwerte (erhöhte Alaninaminotransferase, erhöhte Aspartataminotransferase), Ausschlag, trockene Haut, Juckreiz, Rötung der Haut, Gelenkschmerzen, Muskelschmerzen oder Schmerzen in Händen und Füssen, Muskelkrämpfe, Fieber, Müdigkeit, Schüttelfrost, Schwellungen an Händen, Füssen, fehlende Energie, Schwächegefühl, grippeähnliche Erkrankung
Häufig (betrifft 1 bis 10 von 100 Anwendern)
Harnwegsinfektion, Cellulitis, Entzündung der Haarfollikel in der Haut, Nagelerkrankungen, z.B. Nagelbettveränderung, Nagelschmerzen, Infektion und Schwellung der Nagelhaut, Auswirkungen auf die Haut, z.B. spröde, schuppige Hautstellen, Hautausschlag mit eitrigen Bläschen, ,kutanes Plattenepithelkarzinom (eine Art Hautkrebs), Papillom (eine Art Hauttumor, der in der Regel gutartig ist), braune oder gelbliche Verdickungen der Haut (Keratose und Hypekeratose), Verminderte Anzahl einer Art weisser Blutkörperchen (Neutropenie), Müdigkeit, Erschöpfung, bleiche Haut (Anämie), verminderte Anzahl der Blutplättchen - Zellen, die die Blutgerinnung unterstützen (Thrombozytopenie), Fieber, Schüttelfrost, Halsschmerzen oder Mundfäule aufgrund von Infektionen als Anzeichen einer verringerten Anzahl weisser Blutkörperchen (Leukopenie), Dehydration (Flüssigkeitsmangel), niedriger Natriumgehalt im Blut, niedriger Phosphatgehalt im Blut, Übermässiger Durst, grosse Harnmenge, dunkler Urin, erhöhter Appetit mit Gewichtsabnahme, trockene und gerötete Haut, Reizbarkeit als Anzeichen eines hohen Zuckeranteils (Glukose) im Blut (Zeichen einer Überzuckerung), verschwommene Sicht, Sehverschlechterung, Entzündung des Auges (Uveitis), weniger effizientes Pumpen des Herzens, niedriger Blutdruck, Flüssigkeitsansammlung in den Extremitäten (Lymphödem), Kurzatmigkeit, Mundtrockenheit, wunder Mund oder Mundgeschwüre, Zunahme einiger von der Leber gebildeter Substanzen (Enzyme wie z.B. Gamma-Glutamyltransferase und alkalische Phosphatase), akneähnliche Hautentzündungen, Nachtschweiss, ungewöhnlicher Haarausfall oder Haarausdünnung, warzenähnliche Wucherungen oder Rötung und Schwellung von Handflächen, Fingern und Fusssohlen, Hautläsionen (Verletzung der Haut), Hautrisse, Übermässiges Schwitzen, Entzündung der Fettschicht unter der Haut, Lichtempfindlichkeit, erhöhte Kreatinphosphokinase im Blut, ein Enzym, das sich vor allem in Herz, Gehirn und Skelettmuskulatur befindet, Nierenversagen (Nierenerkrankung, welche zu eingeschränkter Urinausscheidung führen kann) und akutes Nierenversagen, Entzündung der Schleimhaut (nicht nur im Mundbereich), lokale Gewebeschwellung, z.B. Gesichtsschwellung.
Brustschmerzen, plötzliche Kurzatmigkeit, Atembeschwerden, Schmerzen in den Beinen mit oder ohne Schwellung, eine Schwellung an Arm oder Bein oder ein kühler, blasser Arm bzw. ein kühles, blasses Bein; dabei kann es sich um Anzeichen eines Blutgerinnsels in den Venen des Armes oder Beines, der Lunge oder anderer Körperteile handeln, unregelmässiger Herzschlag (atrioventrikulärer Block). Probleme mit den Nerven, die Schmerzen, Gefühlsverlust oder Kribbeln in Händen und Füssen/Muskelschwäche verursachen können (periphere Neuropathie).
Gelegentlich (betrifft 1 bis 10 von 1000 Anwendern)
Neues Primärmelanom, Fibrome (Stielwarzen), Sarkoidose (Entzündliche Erkrankung, welche hauptsächlich die Atemwege, die Haut, das Herz und die Augen betrifft), Allergische Reaktionen gegenüber Arzneimitteln, Augenveränderungen, z.B. Schwellung im Auge, die durch Flüssigkeitsaustritt verursacht wird (Chorioretinopathie), Ablösung der lichtempfindlichen Membran auf der Rückseite des Auges (der Netzhaut) von den Trägerschichten (Ablösung des Netzhautpigmentepithels/Netzhautablösung), Schwellung in der Augengegend, verlangsamter Herzschlag (Bradykardie), unregelmässiger Herzschlag (Schenkelblock).Lungenentzündung (Pneumonitis) und weitere Lungenerkrankungen (interstitielle Lungenerkrankung), Entzündung der Bauchspeicheldrüse, Durchfall, Bauchschmerzen, Fieber (Anzeichen einer Kolitis), , Nephritis, Entzündung der Niere, Veränderungen darin, wie das Herz das Blut pumpt (linksventrikuläre Dysfunktion), Herzinsuffizienz (verminderte Herzfunktion, welche zu Atemproblemen beim Liegen führen kann, Müdigkeit oder Anschwellen der Beine), Auflösung von Muskelgewebe (Rhabdomyolyse), welche zu Schmerzen, Fieber und rot-braunem Urin führen kann.
Nervenentzündung, die zu Schmerzen, Taubheitsgefühl, Muskelschwäche und Lähmung der Arme und Beine führen kann (Guillain-Barré-Syndrom).
Selten (betrifft 1 bis 10 von 10'000 Anwendern)
Entzündung des Herzmuskelgewebes, starke Magenschmerzen, Übelkeit (Anzeichen eines Magen- oder Darmdurchbruchs (Perforation))
Nicht bekannt (kann aus den verfügbaren Daten nicht abgeschätzt werden)
Hämophagozytische Lymphohistiozytose (ein Zustand, bei dem das Immunsystem zu viele Zellen zur Infektionsbekämpfung produziert).Mehrere gleichzeitig auftretende Symptome wie unregelmässiger Herzschlag, Abnahme der Urinausscheidung, Verwirrtheit, starke Übelkeit und Erbrechen, Kurzatmigkeit, Muskelkrämpfe oder zuckungen («Tumorlysesyndrom» oder TLS). Erhabene, schmerzhafte, rote bis dunkelrot-violette Hautflecken oder -wunden, die vor allem an Armen, Beinen, Gesicht und Hals auftreten und mit Fieber einhergehen (Anzeichen einer akuten febrilen neutrophilen Dermatose oder des Sweet-Syndroms).
Mögliche Nebenwirkungen bei Kindern, wenn Mekinist zusammen mit Tafinlar eingenommen wird
Die bei Kindern beobachteten Nebenwirkungen ähnelten insgesamt den Nebenwirkungen bei Erwachsenen. Eine Gewichtszunahme (sehr häufig) wurde bisher nur bei Kindern beobachtet. Weitere Nebenwirkungen bei Kindern, die im Vergleich zu erwachsenen Patienten häufiger auftraten, waren:
Sehr häufig (betrifft mehr als einen von 10 Anwendern)
verminderte Anzahl einer Art weisser Blutkörperchen (Neutropenie), akneähnliche Hautentzündungen, Nagelbettentzündung (Paronychie), Blutarmut (Anämie), verminderte Gesamtzahl der weissen Blutkörperchen (Leukopenie)
Häufig (betrifft 1 bis 10 von 100 Anwendern)
verlangsamter Herzschlag (Bradykardie), Rötung und Schuppen der Haut über grosse Bereiche des Körpers (generalisierte exfoliative Dermatitis), Überempfindlichkeit und Entzündung der Bauchspeicheldrüse (Pankreatitis), Papillom der Haut.
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt, Apotheker bzw. Ihre Ärztin, Apothekerin. Dies gilt insbesondere auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind.
Was ist ferner zu beachten?
Das Arzneimittel darf nur bis zu dem auf dem Behälter mit «EXP» bezeichneten Datum verwendet werden.
Aufbrauchfrist nach Anbruch
Die fertig zubereitete Lösung ist 35 Tage haltbar. Die Flasche mit der fertig zubereiteten Lösung ist im Umkarton unter 25°C zu lagern und darf nicht eingefroren werden.
Nicht verwendete Lösung ist 35 Tage nach der Zubereitung zu entsorgen.
Lagerungshinweis
Arzneimittel sind für Kinder unerreichbar aufzubewahren.
Bis zum Auflösen im Kühlschrank bei 2°C bis 8°C aufbewahren.
In der Originalverpackung aufbewahren, um das Pulver vor Licht und Feuchtigkeit zu schützen.
Die Flasche fest verschlossen halten.
Weitere Hinweise
Weitere Auskünfte erteilt Ihnen Ihr Arzt, Apotheker bzw. Ihre Ärztin, Apothekerin. Diese Personen verfügen über die ausführliche Fachinformation.
Was ist in MEKINIST enthalten?
Pulver zur Herstellung einer Lösung zum Einnehmen:
Das Pulver für die Herstellung einer Lösung zum Einnehmen ist weiss oder nahezu weiss.
Wirkstoffe
Der Wirkstoff von Mekinist Pulver zur Herstellung einer Lösung zum Einnehmen ist Trametinib.
1 Flasche enthält 4.7 mg Trametinib (als Trametinibdimethylsulfoxid)
1 mL der fertig zubereiteten Lösung enthält 0.05 mg Trametinib
Hilfsstoffe
Pulver zur Herstellung einer Lösung zum Einnehmen:
Sucralose (E 955), Zitronensäure-Monohydrat (E 330), Natriummonohydrogenphosphat (E 339), Sulfobutylbetadex-Natrium, Kaliumsorbat (E 202), Methylparahydroxybenzoat (E 218), Erdbeeraroma.
Wo erhalten Sie MEKINIST Pulver zur Herstellung einer Lösung zum Einnehmen? Welche Packungen sind erhältlich?
In Apotheken gegen ärztliche Verschreibung, die nur zum einmaligen Bezug berechtigt.
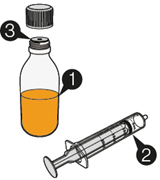
Mekinist 4.7 mg: 1 Flasche mit Pulver zur Herstellung einer Lösung zum Einnehmen, 1 orale Dosierspritze und 1 Flaschenadaptor.
Zulassungsnummer
69134 (Swissmedic)
Zulassungsinhaberin
Novartis Pharma Schweiz AG, Risch; Domizil: 6343 Rotkreuz
Diese Packungsbeilage wurde im Februar 2025 letztmals durch die Arzneimittelbehörde (Swissmedic) geprüft.
Hinweise für die Anwendung und Handhabung
|
GEBRAUCHSANWEISUNG | |||
|
Diese Gebrauchsanweisung enthält Informationen zur Einnahme von Mekinist | |||
|
Wichtige Informationen, die Sie vor der Einnahme von Mekinist wissen müssen | |||
|
·Bitte lesen Sie diese Gebrauchsanweisung sorgfältig durch, bevor Sie mit der Anwendung von Mekinist beginnen. | |||
|
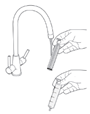
Wenn Mekinist auf die Haut gelangt, waschen Sie den Bereich gut mit Wasser und Seife ab. Wenn Mekinist in die Augen gelangt, spülen Sie Ihre Augen mit Wasser aus. | |||
|
Pulver für die Zubereitung |
|
| |
|
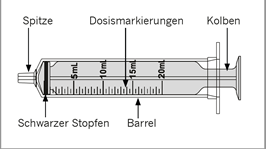
Übersicht über wiederverwendbare Applikationsspritzen für Zubereitungen zum Einnehmen: |
Lesen Sie die wichtigen Informationen über Mekinist oben und gehen Sie dann zu den Anweisungen für die Zubereitung in Abschnitt A weiter. | ||
|
Weiter zu Abschnitt A | |||
|
ODER | |||
|
Gebrauchsfertige Lösung |
|
| |
|
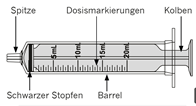
Übersicht über wiederverwendbare Applikationsspritzen für Zubereitungen zum Einnehmen: |
Lesen Sie die wichtigen Informationen über Mekinist oben und gehen Sie dann zu den Anweisungen zur Verabreichung in Abschnitt B. | ||
|
Weiter zu Abschnitt B | |||
|
ABSCHNITT A. ZUBEREITUNG | |||
|
Befolgen Sie die Anweisungen in Abschnitt A zur Zubereitung, wenn Sie Mekinist als Pulver erhalten haben. |
|
| |
|
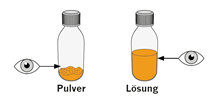
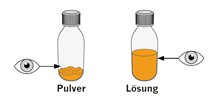
1. Prüfen Sie, ob sich in der Flasche Pulver oder eine flüssige Lösung befindet. |
|
| |
|
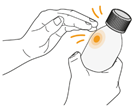
2. Schütteln Sie die Flasche nicht. |
|
| |
|
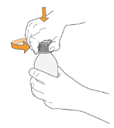
3. Entfernen Sie die kindersichere Schutzkappe, indem Sie sie herunterdrücken und gegen den Uhrzeigersinn drehen. |
|
| |
|
4. Nehmen Sie den Adapter von der Spritze ab. |
|
| |
|
5. Füllen Sie ein Trinkglas mit stillem Trinkwasser.* |
|
| |
|
6. Setzen Sie die Schutzkappe wieder auf die Flasche und drehen Sie sie zum Verschliessen im Uhrzeigersinn. Vergewissern Sie sich, dass die Schutzkappe sicher auf der Flasche aufsitzt, bevor Sie mit dem nächsten Schritt fortfahren. |
|
| |
|
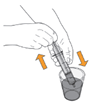
7. Drehen Sie die Flasche wiederholt auf den Kopf und dann wieder in eine aufrechte Position, bis sich das Pulver vollständig aufgelöst hat. Sie können die Flasche auch leicht schütteln. |
|
| |
|
8. Stellen Sie die Flasche für mindestens 5 Minuten aufrecht auf eine flache Oberfläche. |
|
| |
|
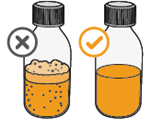
9. Nachdem sich das Pulver vollständig aufgelöst hat, befindet sich das Wasser in der Flasche möglicherweise unterhalb des blauen Pfeils.* |
|
| |
|
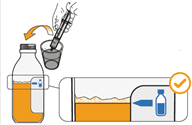
10. Stellen Sie die Flasche auf den Tisch und halten Sie sie fest. Stecken Sie mit der anderen Hand den Adapter mit dem Daumen oder der Handfläche in die Flasche. |
|
|
|
|
11. Setzen Sie die Schutzkappe wieder auf die Flasche und drehen Sie sie zum Verschliessen im Uhrzeigersinn. |
|
| |
|
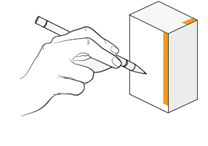
12. Schreiben Sie das Verfalldatum auf den Umkarton. Das Verfalldatum beträgt 35 Tage nach Herstellung der Lösung. |
|
| |
|
13. Um die Lösung zu verabreichen, folgen Sie den Anweisungen in Abschnitt B. | |||
|
ABSCHNITT B. ANWENDUNG | |||
|
Zur Verabreichung von Mekinist als gebrauchsfertige Lösung benötigen Sie: |
|
| |
|
1. Prüfen Sie, ob sich in der Flasche Pulver oder eine flüssige Lösung befindet. |
|
| |
|
2. Überprüfen Sie das Datum der Rekonstitution (Zubereitung) der Lösung auf dem Flaschenkarton. Verabreichen Sie Mekinist nicht, wenn das Verfalldatum überschritten ist oder kein Datum angegeben ist. |
|
| |
|
3. Schwenken Sie die Flasche vorsichtig 30 Sekunden lang, um die Lösung zu mischen. |
|
| |
|
·Entfernen Sie die kindersichere Schutzkappe, indem Sie die Schutzkappe herunterdrücken und gegen den Uhrzeigersinn drehen. |
|
| |
|
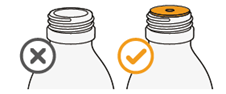
·Prüfen Sie, ob bereits ein Flaschenadapter in den Flaschenhals eingesetzt ist. |
|
| |
|
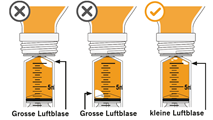
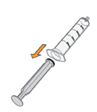
·Drücken Sie den Kolben bis zum Anschlag in die Applikationsspritze für Zubereitungen zum Einnehmen, um die gesamte Luft darin zu entfernen. |
|
| |
|
4. Stellen Sie die Flasche auf eine flache Oberfläche und halten Sie sie aufrecht. |
|
| |
|
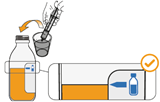
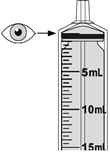
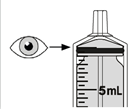
5. Drehen Sie die Flasche vorsichtig auf den Kopf und ziehen Sie am Kolben, um Ihre Dosis abzumessen. Mit der Spitze nach oben muss die Oberseite des schwarzen Stopfens mit Ihrer verschriebenen Dosis übereinstimmen. |
|
|
|
|
6. Halten Sie den Kolben weiterhin fest, drehen Sie die Flasche wieder um und stellen Sie sie auf eine flache Oberfläche. Während Sie den Kolben noch festhalten, ziehen Sie die Applikationsspritze für Zubereitungen zum Einnehmen vorsichtig nach oben aus der Flasche. |
|
| |
|
7. Vergewissern Sie sich, dass die Oberseite des schwarzen Stopfens auf die vorgeschriebene Dosis eingestellt ist. Wenn nicht, wiederholen Sie die Schritte 5-6. |
|
| |
|
8. WICHTIGER HINWEIS: Achten Sie bei der Verabreichung an ein Kind darauf, dass es aufrecht sitzt. |
|
| |
|
9. Stellen Sie sicher, dass sich keine Lösung mehr in der Spritze befindet. |
|
| |
|
10. Entfernen Sie den Adapter nicht. |
|
| |
|
11. Anweisungen zur Reinigung und Lagerung finden Sie in Abschnitt C. |
| ||
|
ABSCHNITT C. REINIGUNG | |||
|
Im Falle eines Verschüttens oder eines Kontakts von Mekinist-Lösung mit der Haut oder den Augen, befolgen Sie die Informationen im Abschnitt «Reinigung von verschütteten Flüssigkeiten». | |||
|
1. Füllen Sie ein Glas mit warmem Seifenwasser. |
|
| |
|
2. Legen Sie die Applikationsspritze in das Glas mit dem warmen Wasser. Ziehen Sie vier- bis fünfmal Wasser in die Applikationsspritze hinein und wieder heraus. |
|
| |
|
3. Entfernen Sie den Kolben aus dem Spritzenzylinder. |
|
| |
|
4. Spülen Sie das Glas, den Kolben und den Spritzenzylinder unter warmem Leitungswasser ab. |
|
| |
|
5. Lassen Sie den Kolben und den Spritzenzylinder vor dem nächsten Gebrauch auf einer trockenen Oberfläche an der Luft trocknen. |
|
| |
|
AUFBEWAHRUNG | |||
|
Lagerung des Pulvers für die Herstellung der Lösung |
|
| |
|
Aufbewahrung der gebrauchsfertigen Lösung |
|
| |
|
Aufbewahrung von Applikationsspritze für Zubereitungen zum Einnehmen |
|
| |
|
ENTSORGUNG | |||
|
·Fragen Sie Ihren Apotheker, wie Sie abgelaufene oder nicht mehr benötigte Arzneimittel entsorgen können. | |||