Eigenschaften/WirkungenATC-Code
A10AD06
Wirkungsmechanismus
Insulin Degludec und Insulin Aspart bindet spezifisch an den Humaninsulin-Rezeptor und hat die gleiche pharmakologische Wirkung wie Humaninsulin.
Die blutzuckersenkende Wirkung von Insulin beruht auf der verbesserten Aufnahme von Glukose nach der Bindung des Insulins an die Insulin-Rezeptoren auf Muskel- und Fettzellen und der gleichzeitigen Hemmung der Freisetzung von Glukose aus der Leber.
Pharmakodynamik
Die pharmakodynamische Wirkung der beiden Komponenten in Ryzodeg ist deutlich separiert (siehe Abbildung 1) und das daraus resultierende Wirkprofil spiegelt die einzelnen Komponenten, das rasch wirkende Insulin Aspart und die basale Komponente Insulin Degludec deutlich wider.
Die lang wirkende basale Komponente von Ryzodeg (Insulin Degludec) bildet nach subkutaner Injektion lösliche Multihexamere, die ein Depot bilden, aus dem kontinuierlich und langsam Insulin Degludec in den Blutkreislauf abgegeben wird, was zu einer flachen und stabilen blutzuckersenkenden Wirkung führt. Diese Wirkung bleibt in der Kombination mit Insulin Aspart erhalten und interferiert nicht mit den rasch wirkenden Insulin Aspart Monomeren.
Nach Verabreichung von Ryzodeg erfolgt der Wirkungseintritt sehr rasch und deckt die Mahlzeiten ab. Die basale Komponente weist ein flaches, stabiles und lang wirkendes Profil auf, was zu einer kontinuierlichen Abdeckung des Insulin Basalbedarfs führt. Die Wirkdauer einer Einzeldosis Ryzodeg beträgt mehr als 24 Stunden.
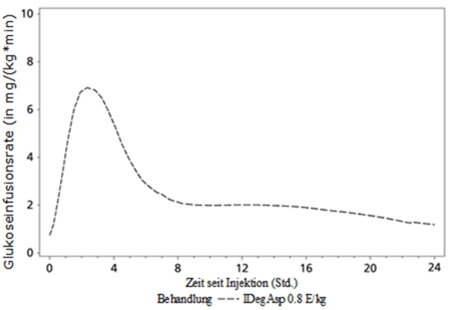
Abbildung 1: durchschnittliche Glukoseinfusionsrate von Ryzodeg nach Verabreichung einer Einzeldosis von 0,8 E/kg bei Typ 1 Diabetikern
Die Gesamt- und die maximale blutzuckersenkende Wirkung von Ryzodeg nimmt mit zunehmender Dosierung linear zu. Das Steady-State wird 2-3 Tage nach erster Verabreichung erreicht.
Die pharmakodynamische Wirkung von Ryzodeg unterscheidet sich zwischen älteren und jüngeren Patienten nicht.
Klinische Wirksamkeit
Es wurden sieben multinationale, randomisierte, kontrollierte, nicht verblindete klinische Treat-to-Target-Studien mit einer Dauer zwischen 26 bis 52 Wochen durchgeführt. Hierbei wurden insgesamt 1'761 Patienten mit Diabetes mellitus (1 Studie mit 362 Patienten mit Diabetes mellitus Typ 1 und 6 Studien mit 1'399 Patienten mit Diabetes mellitus Typ 2) mit Ryzodeg behandelt.
Die Anwendung von einmal täglich Ryzodeg wurde mit Insulin glargin (IGlar) (einmal täglich) in zwei Studien zu Typ 2 Diabetes mellitus verglichen (Tabelle 1).
In zwei Studien zu Typ 2 Diabetes mellitus wurde Ryzodeg zweimal täglich mit biphasischem Insulin Aspart 30 (BIAsp 30) zweimal täglich sowie in einer Studie zu Typ 2 Diabetes mellitus mit Insulin degludec (IDeg) einmal täglich plus 2-4 mal täglich Insulin aspart (IAsp) verglichen (Tabelle 2).
In einer Studie zu Typ 2 Diabetes mellitus wurde Ryzodeg einmal täglich mit Insulin glargin (IGlar) einmal täglich plus IAsp einmal täglich verglichen. Nach 26 Behandlungswochen konnte die Ryzodeg Dosis in eine zweimal tägliche Dosierung aufgeteilt werden (Tabelle 3). In allen Studien zu Typ 2 Diabetes mellitus waren orale Antidiabetika (OADs) erlaubt.
Ryzodeg einmal täglich plus Insulin Aspart (IAsp) wurde ebenfalls mit einmal täglich oder zweimal täglich Insulin Detemir (IDet) plus IAsp bei Diabetes mellitus Typ 1 verglichen (Tabelle 4).
Die Nichtunterlegenheit hinsichtlich der Veränderung des HbA1c-Ausgangswert bis zum Studienende wurde in 6 von 7 Studien gegenüber allen Vergleichspräparaten gemäss dem Treat-to-Target-Prinzip bestätigt, während die Nichtunterlegenheit in einer Studie (Vergleich von Ryzodeg zweimal täglich mit IDeg einmal täglich plus 2-4 mal IAsp täglich) mit Diabetes mellitus Typ 2 Patienten nicht bestätigt wurde (Tabelle 2).
In Kombination mit OAD zeigt Ryzodeg einmal täglich sowohl bei Insulin naïven als auch bei mit Insulin vorbehandelten Typ 2 Diabetikern eine vergleichbare Blutzuckerkontrolle wie Insulin Glargin. Ryzodeg wies eine verbesserte prandiale Blutzuckerkontrolle mit einer niedrigeren Rate nächtlicher Hypoglykämien (definiert als Episoden zwischen Mitternacht und 6 Uhr morgens mit einem bestätigten Plasmaglukosewerte von <3,1 mmol/l oder wenn der Patient auf fremde Hilfe angewiesen war) (Tabelle 1) im Vergleich zu Insulin Glargin auf.
Ryzodeg zweimal täglich verabreicht zeigte eine vergleichbare Blutzuckerkontrolle (HbA1c) wie BIAsp 30 zweimal täglich. Mit Ryzodeg wurde ein besserer Nüchternblutzuckerwert erreicht und die Patienten erreichten den Plasmaglukosezielwert von 5 mmol/l rascher als mit BIAsp 30. Ryzodeg zeigte eine geringere Gesamtrate an Hypoglykämien sowie nächtlicher Hypoglykämien (Tabelle 2).
Ryzodeg zweimal täglich wurde bei Patienten mit Typ-2-Diabetes mellitus, die mit Basalinsulin behandelt werden und eine Therapieintensivierung mit einem prandialen Insulin benötigen, mit IDeg einmal täglich plus IAsp (2-4 Injektionen pro Tag) verglichen. Beide Behandlungen haben die glykämische Kontrolle verbessert, jedoch hat die Behandlung mit Ryzodeg die vordefinierte Nichtunterlegenheitsgrenze von 0.4% gegenüber IDeg plus IAsp für den primären Endpunkt der Veränderung des HbA1c-Ausgangswerts bis zur Woche 26 nicht erreicht (Tabelle 2). Es gab keine statistisch signifikanten Unterschiede zwischen den beiden Behandlungsgruppen.
In einer Studie mit Patienten mit Typ 2 Diabetes mellitus, die mit Basalinsulin behandelt wurden und eine Therapieintensivierung mit einem prandialen Insulin benötigten, wurde Ryzodeg einmal täglich mit IGlar einmal täglich plus IAsp einmal täglich über 26 Wochen verglichen. Nach 26 Wochen konnte die Ryzodeg Dosis im Ryzodeg-Arm in eine zweimal tägliche Dosierung aufgeteilt werden. Im IGlar-Arm konnten zusätzliche Dosen IAsp während der anderen Mahlzeiten (bis zu dreimal täglich) verabreicht werden. Ryzodeg einmal täglich erreichte im Vergleich zu IGlar einmal täglich plus IAsp einmal täglich nach 26 Wochen eine ähnliche glykämische Kontrolle (HbA1c). Ryzodeg einmal täglich oder zweimal täglich erreichte im Vergleich zu IGlar einmal täglich plus IAsp ein- bis dreimal täglich nach 38 Wochen eine ähnliche glykämische Kontrolle (HbA1c). Ryzodeg zeigte während der 26 und der 38 Wochen eine niedrigere Rate der nächtlichen Hypoglykämien (Tabelle 3).
Bei Typ 1 Diabetikern zeigte die Behandlung mit Ryzodeg einmal täglich plus Insulin Aspart zu den verbleibenden Mahlzeiten eine vergleichbare Blutzuckerkontrolle (HbA1c und Nüchternplasmaglukose) bei einer geringeren Rate nächtlicher Hypoglykämien im Vergleich zu einer Basis-Bolus-Behandlung mit Insulin Detemir plus Insulin Aspart zu allen Mahlzeiten (Tabelle 4).
Tabelle 1: Resultat von zwei 26-wöchigen Studien mit Typ 2 Diabetikern
|
|
Ryzodeg
(einmal täglich)1
Insulin naïv
|
IGlar
(einmal täglich)1
Insulin naïv
|
Ryzodeg
(einmal täglich)2
Insulin-Anwender
|
IGlar
(einmal täglich)2
Insulin-Anwender
| |
N
|
266
|
263
|
230
|
233
| |
Mittlerer HbA1c-Wert (%)
| |
Studienende
Änderung im Mittel
|
7,2
-1,65
|
7,2
-1,72
|
7,3
-0,98
|
7,4
-1,00
| |
|
Unterschied:
0,03 [-0,14; 0,20]
|
Unterschied:
-0,03 [-0,20; 0,14]
| |
Nüchternplasmaglukose (mmol/l)
| |
Studienende
Änderung im Mittel
|
6,8
-3,32
|
6,3
-4,02
|
6,3
-1,68
|
6,0
-1,88
| |
|
Unterschied:
0,51 [0,09; 0,93]
|
Unterschied:
0,33 [-0,11; 0,77]
| |
Blutzucker (Plasma) 90 Minuten nach den Mahlzeiten am Studienende (in mmol/l)
| |
nach dem Frühstück
Änderung im Mittel
|
1,9
-1,5
|
3,4
-0,3
|
|
| |
nach dem Abendessen
Änderung im Mittel
|
|
|
1,2
-1,5
|
2,6
-0,6
| |
Hypoglykämie-Rate (pro Patientenjahr Expositionszeit)
| |
Schwer
|
0,01
|
0,01
|
0,00
|
0,04
| |
Bestätigt3
|
4,23
|
1,85
|
4,31
|
3,20
| |
|
Verhältnis:
2,17 [1,59; 2,94]
|
Verhältnis: 1,43
[1,07; 1,92]
| |
Bestätigt nächtlich3
|
0,19
|
0,46
|
0,82
|
1,01
| |
|
Verhältnis:
0,29 [0,13;0,65]
|
Verhältnis:
0,80 [0,49;1,30]
|
1 Einmal tägliche Gabe + Metformin
2 Einmal tägliche Gabe + Metformin ± Pioglitazon ± DPP-4-Inhibitor
3 Bestätigte Hyperglykämien wurden als Episoden definiert, die durch einen Plasmaglukosewert von <3,1 mmol/l oder dadurch bestätigt wurden, dass der Patient Fremdhilfe benötigte. Bestätigte nächtliche Hypoglykämien wurden als Episoden zwischen Mitternacht und 06:00 Uhr definiert.
IGlar = Insulin Glargin
Tabelle 2: Resultat von drei 26-wöchigen Studien mit Typ 2 Diabetikern
|
|
Ryzodeg
(zweimal täglich)1
Insulin-Anwender
|
BIAsp 30
(zweimal täglich)1
Insulin-Anwender
|
Ryzodeg
(zweimal täglich)2
Insulin-Anwender
|
BIAsp 30
(zweimal täglich)2
Insulin-Anwender
|
Ryzodeg (zweimal täglich)3
Insulin-Anwender
|
IDeg (einmal täglich) + IAsp4
Insulin-Anwender
| |
N
|
224
|
222
|
280
|
142
|
138
|
136
| |
Mittlerer HbA1c-Wert (%)
| |
Studienende
Änderung im Mittel
|
7,1
-1,28
|
7,1
-1,30
|
7,1
-1,38
|
7,0
-1,42
|
7,0
-1,31
|
6,8
-1,50
| |
|
Unterschied:
-0,03 [-0,18; 0,13]
|
Unterschied:
0,05 [-0,10; 0,20]
|
Unterschied:
0,18 [-0,04; 0,41]
| |
Nüchternplasmaglukose (mmol/l)
| |
Studienende
Änderung im Mittel
|
5,8
-3,09
|
6,8
-1,76
|
5,4
-2,55
|
6,5
-1,47
|
6,8
-2,25
|
7,1
-1,78
| |
|
Unterschied:
-1,14 [-1,53; -0,76]
|
Unterschied:
-1,06 [-1,43; -0,70]
|
Unterschied:
-0,31 [-0,97; 0,34]
| |
Hypoglykämie Rate (pro Patientenjahr Expositionszeit)
| |
Schwer
|
0,09
|
0,25
|
0,05
|
0,03
|
0,47
|
0,24
| |
Bestätigt5
|
9,72
|
13,96
|
9,56
|
9,52
|
11,55
|
13,62
| |
|
Verhältnis:
0,68 [0,52; 0,89]
|
Verhältnis:
1,00 [0,76; 1,32]
|
Verhältnis:
0,81 [0,61; 1,07]
| |
Bestätigt nächtlich5
|
0,74
|
2,53
|
1,11
|
1,55
|
1,23
|
1,55
| |
|
Verhältnis:
0,27 [0,18; 0,41]
|
Verhältnis:
0,67 [0,43; 1,06]
|
Verhältnis:
0,80 [0,50; 1,29]
| |
Totale Insulin Dosis (Einheiten)
| |
Studienende
|
|
106,7
|
130,6
| |
Verhältnis: 0,81
[0,69; 0,95]
|
1 Zweimal tägliche Gabe ± Metformin ± Pioglitazon ± DPP-4-Inhibitor
2 Zweimal tägliche Gabe ± Metformin
3 Zweimal tägliche Gabe ± Metformin ± Insulin Sekretagoge ± DPP-4 Inhibitor ± α-Glucosidase-Inhibitor
4 Einmal täglich Gabe + Insulin Aspart 2-4 mal täglich als prandiales Insulin ± Metformin ± Insulin Sekretagoge ± DPP-4 Inhibitor ± α-Glucosidase-Inhibitor
5 Bestätigte Hypoglykämien wurden als Episoden definiert, die durch einen Plasmaglukosewert von <3,1 mmol/l oder dadurch bestätigt wurden, dass der Patient Fremdhilfe benötigte. Bestätigte nächtliche Hypoglykämien wurden als Episoden zwischen Mitternacht und 06:00 Uhr definiert.
Tabelle 3: Resultat einer 38-wöchigen Studie mit Typ 2 Diabetikern
|
|
Ryzodeg
(einmal täglich)1
26 Wochen
|
IGlar (einmal täglich) +
IAsp (einmal täglich)1
26 Wochen
|
Ryzodeg
(einmal täglich/
zweimal täglich)2
38 Wochen
|
IGlar (einmal täglich) +
IAsp (1-3 mal täglich)3
38 Wochen
| |
N
|
267
|
265
|
267
|
265
| |
Mittlerer HbA1c-Wert (%)
|
|
| |
Studienende
Änderung im Mittel
|
7,1
-1,1
|
7,1
-1,1
|
7,0
-1,2
|
6,9
-1,2
| |
|
Unterschied:
0,07 [-0,06; 0,21]
|
Unterschied:
0,09 [-0,04; 0,22]
| |
Nüchternplasmaglukose (mmol/l)
|
|
| |
Studienende
Änderung im Mittel
|
6,7
-2.3
|
6.5
-2,3
|
6,3
-2,7
|
6,5
-2,3
| |
|
Unterschied:
0,04 [-0,34; 0,42]
|
Unterschied:
-0,24 [-0,60; 0,13]
| |
Hypoglykämierate (pro Patientenjahr Expositionszeit)
|
|
| |
Schwer oder Plasmaglukose bestätigt4
|
2,58
|
2,96
|
2,87
|
3,43
| |
|
Verhältnis:
0,90 [0,67; 1,22]
|
Verhältnis:
0,86 [0,65; 1,14]
| |
Schwer nächtlich oder Plasmaglukose bestätigt4
|
0,48
|
0,93
|
0,60
|
1,01
| |
|
Verhältnis:
0,55 [0,34; 0,90]
|
Verhältnis:
0,61 [0,40; 0,93]
| |
Totale Insulin Dosis (Einheiten)
| |
Studienende
|
70,9
|
79,4
|
83,4
|
89,3
| |
|
Verhältnis:
0,88 [0,81; 0,95]
|
Verhältnis:
0,91 [0,83; 0,99]
|
1 Einmal tägliche Gabe ± OADs
2 Einmal oder Zweimal tägliche Gabe ± OADs
3 Einmal täglich Insulin glargin + Insulin aspart 1-3 mal täglich ± OADs
4 Schwere oder Plasmaglukose bestätigte symptomatische Hypoglykämie wurde als Episode definiert, die bestätigt wurde durch einen Plasmaglukosewert von <3,1 mmol/l mit Symptomen, welche mit einer Hypoglykämie übereinstimmen. Bestätigte nächtliche Hypoglykämien wurden als Episoden zwischen Mitternacht und 06:00 definiert.
Bemerkung: OADs können jede beliebige Kombination von Metformin, DPP-4-Inhibitoren, α-Glukosidase-Inhibitoren oder SGLT2-Inhibitoren beinhalten.
Tabelle 4: Resultat einer 26-wöchigen Studie mit Typ 1 Diabetikern
|
|
Ryzodeg
(einmal täglich)1
|
IDet
(einmal/zweimal täglich)2
| |
N
|
366
|
182
| |
Mittlerer HbA1c-Wert (%)
| |
Studienende
Änderung im Mittel
|
7,6
-0,73
|
7,6
-0,68
| |
|
Unterschied:
-0,05 [-0,18; 0,08]
| |
Nüchternplasmaglukose (mmol/l)
| |
Studienende
Änderung im Mittel
|
8,7
-1,61
|
8,6
-2,41
| |
|
Unterschied:
0,23 [-0,46; 0,91]
| |
Hypoglykämierate (pro Patientenjahr Expositionszeit)
| |
Schwer
|
0,33
|
0,42
| |
Bestätigt3
|
39,2
|
44,3
| |
|
Verhältnis:
0,91 [0,76; 1,09]
| |
Bestätigt nächtlich3
|
3,71
|
5,72
| |
|
Verhältnis:
0,63 [0,49; 0,81]
|
1 Einmal tägliche Gabe + Insulin aspart zur Abdeckung des mahlzeitenbezogenen Insulinbedarfs
2 Einmal oder zweimal tägliche Gabe + Insulin aspart zur Abdeckung des mahlzeitenbezogenen Insulinbedarfs
3 Bestätigte Hypoglykämien wurden als Episoden definiert, die durch einen Plasmaglukosewert von <3,1 mmol/l oder dadurch bestätigt wurden, dass der Patient Fremdhilfe benötigte. Bestätigte nächtliche Hypoglykämien wurden als Episoden zwischen Mitternacht und 06:00 definiert.
Kardiovaskuläre Beurteilung
Bei DEVOTE handelt es sich um eine randomisierte, doppelblinde klinische Studie, bei der die kardiovaskuläre Sicherheit von Insulin degludec mit derjenigen von Insulin glargin (100 Einheiten/ml) bei 7'637 Patienten mit Typ 2 Diabetes mellitus und hohem Risiko für kardiovaskuläre Ereignisse verglichen wurde. Die Dauer der Studie war «ereignisgesteuert», d.h., bis ≥633 Ereignisse erreicht waren. Die Behandlungsdauer betrug im Median 1.83 Jahre, die Beobachtungszeit im Median 1.99 Jahre.
Die Primäranalyse umfasste den Zeitraum von der Randomisierung bis zum ersten Auftreten eines schweren unerwünschten, kardiovaskulären Ereignisses (MACE, major adverse cardiovaskulare event). MACE umfasste drei Komponenten: «kardiovaskulärer Tod», «nicht tödlicher Herzinfarkt» oder «nicht tödlicher Schlaganfall».
Um einen Anstieg des relativen kardiovaskulären Risikos um mehr als 30% auszuschliessen, wurde die Studie als non-inferiority-Studie konzipiert. Die Obergrenze des 95.%-Konfidenzintervalls (KI) für die MACE-HR lag unter dieser vordefinierten Schwelle von 1.3, womit die kardiovaskuläre Sicherheit von Insulin degludec im Vergleich zu Insulin glargin (Abbildung 2) belegt wurde.

N: Anzahl von Probanden mit einem ersten EAC-bestätigten Ereignis während der Studie.
%: Prozentualer Anteil von Probanden mit erstem EAC-bestätigten Ereignis im Vergleich zur Anzahl der randomisierten Probanden.
EAC: Event Adjudication Commitee.
KI: Konfidenzintervall
Abbildung 2: Forest plot der Analyse des kombinierten 3-Komponenten-MACE und der einzelnen kardiovaskulären Endpunkte in DEVOTE.
Die Verbesserung des HbA1c, die mit Insulin degludec und Insulin glargin erreicht wurden, waren ebenso vergleichbar (Tabelle 5).
Die Behandlung mit Insulin degludec resultierte im Vergleich zur Behandlung mit Insulin glargin in einer Verringerung der Rate schwerer hypoglykämischer Ereignisse und des Anteils an Patienten mit mindestens einer schweren Hypoglykämie (Tabelle 4).
Tabelle 5: Ergebnisse aus DEVOTE
|
|
Insulin degludec1
|
Insulin glargin1
| |
N
|
3'818
|
3'819
| |
Mittlerer HbA1c (%)
| |
Ausgangswert
|
8.44
|
8.41
| |
2 Jahre der Behandlung
|
7.50
|
7.47
| |
|
Differenz:
0.008 [-0.05; 0.07]95%KI
| |
Hypoglykämie (pro 100 Patientenjahre Beobachtung)
| |
Schwer
|
3.70
|
6.25
| |
|
Hazard-Ratio:
0.60 [0.48; 0.76]95%KI
| |
Anteil der Patienten mit Hypoglykämie (Prozentualer Anteil der Patienten)
| |
Schwer
|
4.9
|
6.6
| |
|
Hazard-Ratio:
0.73 [0.60; 0.89]95%KI
|
Sicherheit und Wirksamkeit bei pädiatrischen Patienten
Die Wirksamkeit und Sicherheit von Ryzodeg wurden bei Kindern und Jugendlichen mit Diabetes mellitus Typ 1 in einer randomisierten, kontrollierten klinischen Studie über einen Zeitraum von 16 Wochen (n=362) untersucht. Patienten im Ryzodeg Studienarm waren 40 Kinder im Alter von 2-5 Jahren, 61 Kinder im Alter von 6-11 Jahren und 80 Jugendliche im Alter von 12-17 Jahren. Die einmal tägliche Gabe von Ryzodeg zusammen mit der Hauptmahlzeit zuzüglich der Gabe von Insulin Aspart zusammen mit den übrigen Mahlzeiten zeigte eine ähnliche Senkung des HbA1c-Werts zum Zeitpunkt Woche 16 und keine Unterschiede des Nüchternplasmaglucose- sowie des selbstgemessenen Plasmaglucosewerts gegenüber dem Vergleichspräparat Insulin Detemir, das einmal oder zweimal täglich gegeben wurde, zuzüglich der mahlzeitenbezogenen Gabe von Insulin Aspart. Zum Zeitpunkt Woche 16 betrug die mittlere tägliche Gesamtinsulindosis 0,88 gegenüber 1,01 Einheiten/kg im Ryzodeg bzw. Insulin Detemir Studienarm. Die Raten (Ereignisse pro Patientenjahr der Exposition) bestätigter Hypoglykämien (ISPAD [Internationale Gesellschaft für Kinder- und Jugenddiabetologie]-Definition 2009: 46,23 gegenüber 49,55) und nächtlicher bestätigter Hypoglykämien (5,77 gegenüber 5,40) waren bei Ryzodeg und Insulin Detemir vergleichbar. Jedoch war die Rate schwerer Hypoglykämien (0,26 gegenüber 0,07) im Ryzodeg numerisch höher (HR 3.2 [0.88; 11.66]95% KI).
Langzeitdaten
Es gibt keine klinisch relevante Entwicklung von Insulin-Antikörpern nach einer Langzeit-Behandlung mit Ryzodeg.
Weitere Informationen
Fruchtbarkeit
In Fortpflanzungsstudien mit Insulin Degludec bei Tieren wurden keinerlei nachteilige Auswirkungen auf die Fruchtbarkeit nachgewiesen.
|


