Eigenschaften/WirkungenATC-Code
R05DB29
Wirkungsmechanismus
Gefapixant ist ein selektiver Antagonist des P2X3-Rezeptors. Gefapixant besitzt auch eine Aktivität gegen den P2X2/3-Rezeptor-Subtyp. P2X3-haltige Rezeptoren gehören zur Familie der purinergen Rezeptoren und sind ATP-abhängige Ionenkanäle, die sich unter anderem auch auf sensorischen C-Fasern des N. vagus in den Atemwegen befinden. C-Fasern werden in Reaktion auf Entzündungen oder chemische Reizstoffe aktiviert. Unter Entzündungsbedingungen kommt es zur Freisetzung von ATP durch Schleimhautzellen der Atemwege. Die Bindung von extrazellulärem ATP an P2X3-Rezeptoren wird von C-Fasern als Schädigungssignal erkannt und wird vom Patienten als Hustenreiz wahrgenommen, was wiederum einen Hustenreflex auslöst. Gefapixant blockiert die ATP-vermittelte Aktivierung von P2X3-Rezeptoren, die vermutlich für chronischen Husten verantwortlich sind und lindert so den Husten des Patienten.
Pharmakodynamik
Kardiale Elektrophysiologie
Die Wirkung von Gefapixant auf das QTc-Intervall wurde im Rahmen einer randomisierten, placebokontrollierten Einzeldosisstudie an gesunden Probanden untersucht. Nach einer Einzeldosis von 1800 mg, die zu einer mindestens 15-fach höheren Spitzenkonzentration führt als eine Dosis von 45 mg zweimal täglich, induzierte Lyfnua keine klinisch relevante Verlängerung des QTc-Intervalls.
Klinische Wirksamkeit
Studien bei chronisch refraktärem oder chronischem Husten ohne erklärbare Ursache zur Bewertung der objektiven Hustenfrequenz
Die Wirksamkeit von Lyfnua in der Behandlung des chronisch refraktären oder chronischen Hustens ohne erklärbare Ursache wurde in zwei 52-wöchigen, multizentrischen, randomisierten, doppelblinden, placebokontrollierten Studien mit Erwachsenen nachgewiesen, die entweder an einem chronisch refraktären oder an chronischen Husten ohne erklärbare Ursache litten. Refraktärer chronischer Husten (refractory chronic cough, RCC) war definiert als Husten in Verbindung mit einer Begleiterkrankung (z.B. Asthma, gastroösophageale Refluxkrankheit oder Hustensyndrom der oberen Atemwege), der trotz adäquater Behandlung der Begleiterkrankung persistierte. Chronischer Husten ohne erklärbare Ursache (unexplained chronic cough, UCC) war definiert als Husten, der trotz gründlicher klinischer Abklärung nicht mit einer Begleiterkrankung assoziiert war.
Das primäre Ziel der beiden Phase-3-Studien bestand im Nachweis der Wirksamkeit von Lyfnua hinsichtlich der Reduktion der 24-Stunden-Hustenfrequenz gegenüber Placebo. Als sekundäre Ziele wurden die Verminderung der Hustenfrequenz im Wachzustand sowie die Verbesserung der hustenspezifischen gesundheitsbezogenen Lebensqualität beurteilt. In beiden Studien wurden die Patienten auf zweimal tägliche Dosen von Lyfnua 45 mg, 15 mg oder Placebo randomisiert. Der primäre Wirksamkeitszeitraum in COUGH-1 (NCT03449134) betrug 12 Wochen, gefolgt von einer 40-wöchigen verblindeten Verlängerungsphase. Der primäre Wirksamkeitszeitraum in COUGH-2 (NCT03449147) betrug 24 Wochen, gefolgt von einer 28-wöchigen verblindeten Verlängerungsphase.
In COUGH-1 und COUGH-2 aufgenommene Patienten waren aktuelle Nichtraucher, erhielten keine ACE-Hemmer, wiesen einen diagnostizierten RCC oder UCC auf und litten seit mehr als 1 Jahr an chronischem Husten. Die meisten Patienten waren weiblichen Geschlechts (75 %), hellhäutig (80 %) und stammten aus Europa (53 %); das mittlere Alter betrug 58 Jahre (Spanne: 19 bis 89). Bei insgesamt 61,5 % der Patienten wurde ein RCC diagnostiziert, bei 38,5 % ein UCC, und der chronische Husten bestand im Mittel seit 11 Jahren.
Hustenfrequenz
In COUGH-1 und COUGH-2 zeigte sich bei Patienten, die mit Lyfnua 45 mg zweimal täglich behandelt wurden, eine signifikante Verminderung der 24-Stunden-Hustenfrequenz gegenüber Placebo (Tabelle 2). Die Verminderung der 24-Stunden-Hustenfrequenz wurde ab Woche 4 beobachtet und hielt während des gesamten primären Wirksamkeitszeitraum an (12 Wochen in COUGH-1 und 24 Wochen in COUGH-2; Abbildung 1).
In vorab geplanten Analysen über die gepoolten Daten der Subgruppen beider Studien in Woche 12 war die Reduktion der 24-Stunden-Hustenfrequenz bei Patienten unter Behandlung mit Lyfnua 45 mg zweimal täglich gegenüber Placebo unabhängig von Geschlecht, Alter, Region, Primärdiagnose, Hustendauer, Schweregrad des Hustens zu Studienbeginn oder Häufigkeit des Hustens zu Studienbeginn (Abbildung 2).
Tabelle 2: Ergebnisse zur 24-Stunden-Hustenfrequenz und Hustenfrequenz im Wachzustand unter Lyfnua 45 mg BID (COUGH-1 und COUGH-2)
|
|
COUGH-1
|
COUGH-2
| |
|
Lyfnua
|
Placebo
|
Lyfnua
|
Placebo
| |
N
|
217
|
222
|
409
|
419
| |
24-Stunden-Hustenfrequenz (Hustenereignisse pro Stunde)
| |
Studienbeginn
(geometrischer Mittelwert)
|
18,24
|
22,83
|
18,55
|
19,48
| |
Woche 12 (COUGH-1) oder Woche 24 (COUGH-2)
(geometrischer Mittelwert)
|
7,05
|
10,33
|
6,83
|
8,34
| |
Woche 12 (COUGH-1) oder Woche 24 (COUGH-2)
(%-Reduktion gegenüber Studienbeginn)
|
-61,35
|
-54,77
|
-63,17
|
-57,19
| |
Reduktion gegenüber Placebo
(%-Reduktion und 95%-KI)*
|
-18,45†
(-32,92; -0,86)
|
|
-14,64†
(-26,07; -1,43)
|
| |
Hustenfrequenz im Wachzustand (Hustenereignisse pro Stunde)
| |
Studienbeginn
(geometrischer Mittelwert)
|
|
|
24,26
|
25,83
| |
Woche 12 (COUGH-1) oder Woche 24 (COUGH-2)
(geometrischer Mittelwert)
|
|
|
8,63
|
10,82
| |
Woche 12 (COUGH-1) oder Woche 24 (COUGH-2)
(%-Reduktion gegenüber Studienbeginn)
|
|
|
-64,41
|
-58,11
| |
Reduktion gegenüber Placebo
(%-Reduktion und 95%-KI)*
|
|
|
-15,79†
(-27,27; -2,50)
|
| |
N = Anzahl der in die Analyse einbezogenen Teilnehmer.
KI = Konfidenzintervall.
* Basierend auf der longitudinalen Analyse des Kovarianzmodells unter Verwendung der log-transformierten Hustenfrequenz als abhängige Variable und unter Einbeziehung der Faktoren für die Behandlungsgruppe, der Visite, die Interaktion der Behandlungsgruppe mit der Visite, das Geschlecht, die Region, den log-transformierten Ausgangswert und die Interaktion des log-transformierten Ausgangswerts mit der Visite als Kovariaten.
† (p < 0,05) versus Placebo
|
Abbildung 1: Analyse der 24-Stunden-Hustenfrequenz im Zeitverlauf unter Lyfnua 45 mg BID (COUGH-1 und COUGH-2)

Abbildung 2: Analyse der 24-Stunden-Hustenfrequenz unter Lyfnua 45 mg BID in Woche 12 nach Subgruppe in den gepoolten Phase-3-Studien (COUGH-1 und COUGH-2)

Hustenspezifische gesundheitsbezogene Lebensqualität
COUGH-2 war konzipiert, um auch den Einfluss von Lyfnua auf die hustenspezifische gesundheitsbezogene Lebensqualität im Vergleich mit Placebo zu beurteilen, gemessen anhand des Leicester Cough Questionnaire (LCQ) (möglicher Score von 3 bis 21, wobei ein höherer Score eine bessere gesundheitsbezogene Lebensqualität anzeigt). In COUGH-2 war die Quote einer Verbesserung ≥1,3 Punkte der hustenspezifischen gesundheitsbezogenen Lebensqualität in der Behandlungsgruppe mit Lyfnua 45 mg signifikant höher als in der Placebogruppe (Tabelle 3).
Tabelle 3: Hustenspezifische gesundheitsbezogene Lebensqualität LCQ Ergebnisse unter Lyfnua 45 mg BID (COUGH-2)
|
|
Lyfnua
|
Placebo
| |
N (%)
|
342 (76,6)
|
355 (69,0)
| |
Geschätzte Odds Ratio vs. Placebo (95%-KI)*
|
1,41 (1,02; 1,96)
|
| |
p-Wert*
|
0,040
|
| |
KI = Konfidenzintervall.
LCQ = Leicester Cough Questionnaire.
N = Anzahl von Teilnehmern mit verfügbaren Daten in Woche 24; (%) = Prozent Responder in Woche 24.
* Basierend auf dem logistischen Regressionsmodell. Die Kovariaten umfassen Behandlung, Visite, Interaktion der Behandlung mit der Visite, Geschlecht, Region, LCQ Gesamtscore zu Studienbeginn und die Interaktion des LCQ Gesamtscores zu Studienbeginn mit der Visite.
|
Studien bei chronisch refraktärem oder chronischem Husten ohne erklärbare Ursache zur Bewertung von Patient Reported Outcomes
Chronisch refraktärer oder chronischer Husten ohne erklärbare Ursache (RCC oder UCC) mit husteninduzierter Stress-Harninkontinenz (C-SUI)
Die Wirksamkeit von Lyfnua in Bezug auf die Reduktion der Frequenz von C-SUI bei Frauen mit einem BMI von ≤40 mg/kg2 mit RCC oder UCC wurde in einer multizentrischen, randomisierten, doppelblinden, placebokontrollierten Studie (NCT04193176) gezeigt. Das primäre Ziel der C-SUI Studie war zu zeigen, dass Lyfnua wirksam war in Bezug auf eine Reduktion der SUI gemessen als Prozent Veränderung vom Ausgangswert betreffend die durchschnittlichen C-SUI Episoden pro Tag bei Woche 12. Die Auswirkung auf die Hustenhäufigkeit wurde in dieser Studie nicht in der primären Analyse erfasst. Die Patientinnen wurden zu zweimal täglichen Dosen von Lyfnua 45 mg oder Placebo randomisiert.
In die Studie aufgenommene Patientinnen waren aktuelle Nichtraucherinnen, erhielten keine ACE-Hemmer, wiesen einen diagnostizierten RCC oder UCC auf, hatten einen chronischen Husten seit mehr als 1 Jahr, hatten einen Score von ≥40 mm auf der Cough Severity VAS, hatten Symptome einer SUI seit ≥3 Monaten und hatten durchschnittlich ≥2 C-SUI Episoden pro Tag. Die meisten Patientinnen waren hellhäutig (74%) und stammten aus Europa (54%) mit einem mittleren Alter von 56 Jahren (Spanne 22 bis 83 Jahre). Bei insgesamt 77,1% der Patientinnen wurde ein RCC, bei 22,9% ein UCC diagnostiziert und die mittlere Dauer des chronischen Hustens betrug 5,2 Jahre. Die mittlere Dauer der SUI war 4,0 Jahre.
Husteninduzierte SUI Episoden
Patientinnen unter Lyfnua 45 mg zweimal täglich zeigten eine signifikant grössere Prozent Reduktion der durchschnittlichen C-SUI Episoden pro Tag im Vergleich zur Placebogruppe bei Woche 12 (Tabelle 4).)
Tabelle 4: Analyse der C-SUI Episoden pro Tag für Lyfnua 45 mg zweimal täglich
|
Behandlung
|
N
|
Ausgangswert
Mittel (SD)
|
Woche 12 Mittel (SD)
|
Prozent Änderung vs. Ausgangswert
LS Mittel (95% KI)*
| |
Placebo
|
185
|
4,73 (4,22)
|
2,60 (2,24)
|
-41,09 (-46,74, -35,45)
| |
Lyfnua
|
183
|
4,73 (3,00)
|
2,23 (2,53)
|
-52,76 (-58,44, -47,09)
| |
Behandlungsdifferenz
|
Geschätzte Differenz und (95% KI)
|
p-Wert
| |
Lyfnua vs. Placebo
|
-11,67 (-19,67, -3,67)
|
0,004
| |
N = Anzahl der in die Analyse einbezogenen Teilnehmerinnen. KI = Konfidenz Intervall. SD = Standart Abweichung. LS= Kleinste Quadrate.
SUI = Stress-Harninkontinenz. BMI = Body Mass Index.
*Berechnet als (Woche 12-Ausgangswert)/Ausgangswert und basierend auf der longitudinalen Analyse des Kovarianzmodells bestehend aus der prozentualen Änderung vom Ausganswert der mittleren C-SUI Episoden pro Tag zu jeder Visite nach Studienbeginn (bis zu Woche 12) als Antwort. Das Modell schliesst Terme für Behandlung, Visite, Interaktion der Behandlung mit der Visite, BMI und die bei Studienbeginn mittleren C-SUI Episoden pro Tag ein.
|
Abbildung 3: Analyse der Prozent Änderung der husteninduzierten SUI Episoden pro Tag im Zeitverlauf
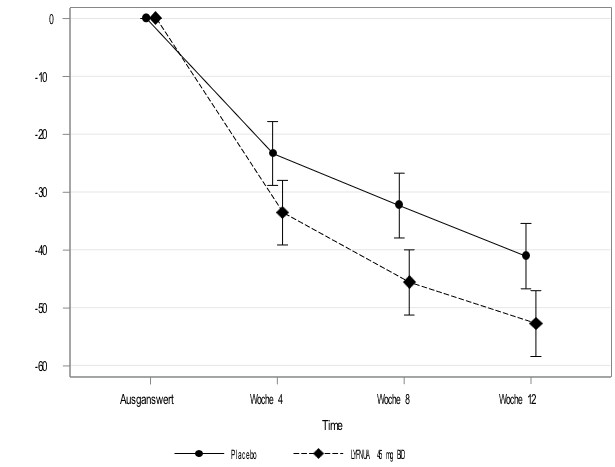
LS = Kleinste Quadrate
Kürzlich aufgetretener chronisch refraktärer oder chronischer Husten ohne erklärbare Ursache (RCC oder UCC)
Die Wirksamkeit von Lyfnua bei Erwachsenen mit kürzlich aufgetretenem RCC oder UCC wurde in einer multizentrischen, randomisierten, doppelblinden, placebokontrollierten Studie (NCT04193202) gezeigt. Kürzlich aufgetreten ist definiert als vorhandener RCC oder UCC für <12 Monate.
Das primäre Studienziel war zu zeigen, dass Lyfnua wirksam war in Bezug auf eine Verbesserung von hustenspezifischer gesundheitsbezogener Lebensqualität, gemessen als Änderung vom Ausgangswert im Leicester Cough Questionnaire (LCQ) Gesamtscore zum Zeitpunkt von 12 Wochen. Die Patienten wurden zu zweimal täglich Lyfnua 45 mg oder Placebo randomisiert.
Die in die Studie aufgenommenen Patienten waren aktuelle Nichtraucher, erhielten keine ACE-Hemmer, wiesen einen diagnostizierten RCC oder UCC auf, hatten einen Score von ≥40 mm auf der Cough Severity VAS und hatten einen chronischen Husten für <12 Monate. Die meisten Patienten (beide Gruppen) waren weiblichen Geschlechts (65%), hellhäutig (72%) und stammten aus Europa (59%) mit einem mittleren Alter von 53 Jahren (Spanne 18 bis 83 Jahre). Bei insgesamt 70,8% der Patienten wurde ein RCC, bei 29,2% ein UCC diagnostiziert und die mittlere Dauer des chronischen Hustens betrug 7,2 Monate.
Hustenspezifische gesundheitsbezogene Lebensqualität
Patienten unter Lyfnua 45 mg zweimal täglich hatten im Vergleich zu Placebo bei Woche 12 eine signifikant grössere Verbesserung des LCQ Gesamtscores vom Ausgangswert (Tabelle 5).
Tabelle 5: Analyse des LCQ Gesamtscores für Lyfnua 45 mg BID
|
Behandlung
|
N
|
Ausgangswert
Mittel (SD)
|
Woche 12
Mittel (SD)
|
Änderung vom Ausgangswert
LS Mittel (95% KI)*
| |
Placebo
|
199
|
11,30 (2,80)
|
14,73 (3,48)
|
3,59 (3,09, 4,09)
| |
Lyfnua
|
199
|
10,82 (3,08)
|
15,32 (3,91)
|
4,34 (3,84, 4,83)
| |
Behandlungsdifferenz
|
Geschätzte Differenz und (95% KI)
|
p-Wert
| |
Lyfnua vs. Placebo
|
0,75 (0,06, 1,44)
|
0,034
| |
N = Anzahl der in die Analyse einbezogenen Teilnehmer. KI = Konfidenz Intervall. SD = Standard Abweichung.
LCQ = Leicester Cough Questionnaire. LS = Kleinste Quadrate
*Berechnet als (Woche 12-Ausgangswert)/Ausgangswert und basierend auf der longitudinalen Analyse des Kovarianzmodells bestehend aus der prozentualen Änderung vom Ausganswert des LCQ Gesamtscores zu jeder Visite nach Studienbeginn (bis zu Woche 12) als Antwort. Das Modell schliesst Terme für Behandlung, Visite, Interaktion der Behandlung mit der Visite, Geschlecht und den LCQ Gesamtscore bei Studienbeginn ein.
|
|



