ZusammensetzungWirkstoffe
Propofolum (2,6-Diisopropylphenol)
Hilfsstoffe
Sojae oleum 100 mg/ml, Phosphatidum ovi depuratum, Glycerolum, Dinatrii edetas, Natrii hydroxidum, Aqua ad iniectabile.
1 ml Emulsion (Disoprivan / Disoprivan PFS 10 mg/ml, 20 mg/ml) enthält max. 0.086 mg Natrium.
Indikationen/AnwendungsmöglichkeitenInduktion und Erhaltung einer Allgemeinanästhesie bei Erwachsenen und Kindern ab 6 Monaten.
Kurzzeitige Sedierung bei chirurgischen und diagnostischen Verfahren bei Erwachsenen und Kindern ab 1 Monat.
Sedierung von beatmeten Erwachsenen während der Intensivbehandlung. Die Sedierung von Kindern unter 16 Jahren während der Intensivbehandlung mit Disoprivan ist kontraindiziert.
Dosierung/AnwendungAnwendungsempfehlungen
Zusätzlich zu Disoprivan werden im Allgemeinen Analgetika benötigt.
Besteht ein spezielles Risiko für ein Fettüberladungssyndrom (Fat Overload) wird empfohlen, die Blutfette zu überwachen und die Verabreichung von Disoprivan entsprechend den Daten anzupassen.
Falls der Patient gleichzeitig intravenös zusätzlich Lipide erhält, sollten diese reduziert werden, mit Berücksichtigung der Menge der Lipide, die als Bestandteil der Disoprivan-Emulsion zugeführt wird; 1,0 ml Disoprivan 10 mg/ml und 20 mg/ml enthalten ungefähr 0,1 g Fett.
Disoprivan 20 mg/ml soll nur als Infusion, jedoch nie als Bolusinjektion verwendet werden (siehe «Warnhinweise und Vorsichtsmassnahmen»).
Dosierungsempfehlungen
Anwendung bei Erwachsenen
Induktion einer Allgemeinanästhesie bei Erwachsenen
Bei nicht prämedizierten und prämedizierten Patienten wird empfohlen, Disoprivan gegen die Reaktion des Patienten zu titrieren, bis klinische Zeichen den Eintritt der Anästhesie zeigen (ca. 40 mg/10 Sek. bei durchschnittlichen gesunden Erwachsenen als Bolus oder Infusion). Erwachsene unter 55 Jahre benötigen in der Regel 1,5 bis 2,5 mg/kg Propofol.
Die benötigte Gesamtdosis kann durch Verringern der Verabreichungsgeschwindigkeit (20-50 mg/Min.) reduziert werden.
Disoprivan 10 mg/ml: Zur Induktion kann Disoprivan 10 mg/ml als langsame Injektion oder Infusion verabreicht werden. Um den Injektionsschmerz zu reduzieren, kann Disoprivan 10 mg/ml mit Lidocain gemischt werden.
Disoprivan 20 mg/ml: Disoprivan 20 mg/ml ist nur als Infusion und nur bei Patienten zu verwenden, bei welchen die Anästhesie anschliessend mit Disoprivan 20 mg/ml aufrechterhalten wird.
Aufrechterhaltung einer Allgemeinanästhesie bei Erwachsenen
Die Anästhesie kann entweder mittels einer Infusion (Disoprivan 10 mg/ml und 20 mg/ml) oder durch wiederholte Bolusinjektionen (Disoprivan 10 mg/ml) aufrechterhalten werden.
Infusion: Disoprivan 10 mg/ml und 20 mg/ml können verwendet werden. Die benötigte Verabreichungsgeschwindigkeit ist von Patient zu Patient verschieden. Mit 4 bis 12 mg/kg/h sollte sich eine zufriedenstellende Anästhesietiefe erzielen lassen. In den ersten 10-20 Minuten können etwas höhere Infusionsgeschwindigkeiten nötig sein.
Wiederholte Bolusinjektionen:
Als Alternative zur Infusion können wiederholte Bolusinjektionen mit Disoprivan 10 mg/ml angewendet werden. Je nach Reaktion des Patienten werden Einzeldosen von 25 bis 50 mg (2,5 bis 5 ml) empfohlen.
Kurzzeitige Sedierung von Erwachsenen bei chirurgischen und diagnostischen Verfahren
Die Dosierung wird nach der gewünschten Tiefe der Sedierung und dem klinischen Ansprechen gewählt.
Zur Einleitung werden bei den Erwachsenen im Allgemeinen 0,5 - 1,0 mg Propofol/kg KG über 1 - 5 Minuten verabreicht.
Bei der Aufrechterhaltung wird die Dosierung durch die gewünschte Tiefe der Sedierung bestimmt und liegt bei den Erwachsenen im Allgemeinen zwischen 1,5 und 4,5 mg Propofol/kg KG/h.
Falls eine rasche Vertiefung der Sedierung erforderlich ist, kann zusätzlich zur Infusion 10 bis 20 mg Propofol mit Disoprivan 10 mg/ml als Bolus injiziert werden.
Patienten mit ASA Grad 3 und 4 benötigen möglicherweise eine Reduktion der Dosis und der Infusionsgeschwindigkeit. Auch bei Patienten über 55 Jahren kann eine niedrigere Dosierung notwendig sein.
Sedierung von beatmeten Erwachsenen während der Intensivbehandlung
Zur Sedierung von beatmeten Erwachsenen in der Intensivbehandlung wird die kontinuierliche Infusion empfohlen. Die Sedierungstiefe soll regelmässig überwacht werden. Die Infusionsrate sollte auf die minimale Dosis, die zur Erhaltung einer zufriedenstellenden Sedierung notwendig ist, eingestellt werden. Mit Dosen von 0,3-4,0 mg/kg/h sollte eine zufriedenstellende Sedierung erreicht werden (vgl. «Warnhinweise und Vorsichtmassnahmen»).
Um das Risiko von Entzugserscheinungen (Agitation, Angst) zu minimieren, sollte die Infusion stufenweise abgesetzt werden.
Spezielle Dosierungsanweisungen
ASA Grad 3 und 4
Bei diesen Patienten sollte die Induktion langsamer erfolgen (ungefähr 20 mg alle 10 Sekunden).
Ältere Patienten (Patienten über 55 Jahre)
Patienten über 55 Jahre benötigen sowohl für die Induktion und die Aufrechterhaltung der Anästhesie wie auch zur Sedierung auf der Intensivstation niedrigere Dosen bzw. Zielkonzentrationen (TCI) von Disoprivan. Bei der Festlegung der Dosisreduktion sollte der Allgemeinzustand und das Alter des Patienten mitberücksichtigt werden. Disoprivan soll gegen die Reaktion des Patienten titriert werden.
Patienten mit ASA Grad 3 und 4 benötigen eine weitere Reduktion der Dosis und der Infusionsgeschwindigkeit.
Bei älteren Patienten sollten keine Bolusinjektionen angewendet werden, da diese zu einer kardiorespiratorischen Depression führen können.
Anwendung bei Kindern
Disoprifusor TCI soll bei Kindern (<16 Jahren) generell nicht angewendet werden.
Induktion einer Allgemeinanästhesie bei Kindern
Kinder unter 6 Monate sollen nicht mit Disoprivan anästhetisiert werden.
Zur Induktion der Anästhesie bei Kindern (über 6 Monaten) wird empfohlen, Disoprivan langsam zu geben, bis die klinischen Zeichen des Beginns der Anästhesie sichtbar sind. Die Dosis sollte dem Alter und/oder dem Gewicht angepasst werden. Die meisten Patienten über 8 Jahre benötigen ca. 2,5 mg/kg Propofol zur Induktion der Anästhesie. Bei Kindern zwischen 6 Monaten und 8 Jahren wird möglicherweise mehr gebraucht. Bei Kindern mit ASA Grad 3 und 4 wird eine niedrigere Dosis empfohlen (siehe auch unter «Warnhinweise und Vorsichtsmassnahmen» und «Unerwünschte Wirkungen»).
Um den Injektionsschmerz zu reduzieren, kann Disoprivan 10 mg/ml mit Lidocain in einer Injektionsspritze aseptisch gemischt werden; 20 Teile Disoprivan 10 mg/ml werden mit 1 Teil 0,5%- oder 1%iger Lidocain-Injektionslösung (ohne antimikrobielle Zusätze) unmittelbar vor Gebrauch gemischt (siehe «Interaktionen»).
Aufrechterhaltung einer Allgemeinanästhesie bei Kindern
Disoprivan soll bei Kindern unter 6 Monaten nicht angewendet werden.
Die Anästhesie kann mittels Infusion oder durch wiederholte Bolusinjektionen aufrechterhalten werden. Zur Bolusinjektion soll nur Disoprivan 10 mg/ml verwendet werden.
Die Dosiserfordernisse variieren stark bei verschiedenen Patienten; mit Dosen von 9-15 mg/kg/h wird gewöhnlich eine zufriedenstellende Anästhesie erreicht.
Kurzzeitige Sedierung von Kindern ab 1 Monat bei chirurgischen und diagnostischen Verfahren
Disoprivan 10 mg/ml soll bei Kindern unter 1 Monat nicht angewendet werden.
Disoprivan 20 mg/ml soll bei Kindern unter 3 Jahren nicht angewendet werden.
Kleinkindern zwischen 1 Monat und 3 Jahre soll Disoprivan 10 mg/ml verabreicht werden. Kindern über 3 Jahre kann Disoprivan 10 mg/ml und Disoprivan 20 mg/ml verabreicht werden.
Die Dosierung wird nach der gewünschten Tiefe der Sedierung und dem klinischen Ansprechen gewählt. Für die Einleitung ist bei den meisten pädiatrischen Patienten eine Dosis von 1 bis 2 mg Propofol/kg KG während mindestens 1 Minute erforderlich. Die Aufrechterhaltung der Sedierung erfolgt durch Titration von Disoprivan per Infusion bis zur gewünschten Sedierungstiefe. Die meisten pädiatrischen Patienten benötigen für eine zufriedenstellende Sedierung 1,5 bis 9 mg Propofol/kg KG/h.
Falls eine rasche Vertiefung der Sedierung erforderlich ist, kann zusätzlich zur Infusion 1 mg Propofol/kg als Bolus mit Disoprivan 10 mg/ml injiziert werden.
Pädiatrische Patienten mit ASA Grad 3 und 4 benötigen möglicherweise eine Reduktion der Dosis und der Infusionsgeschwindigkeit
Sedierung von Kindern während der Intensivbehandlung
Zur Sedierung von Kindern (<16 Jahren) darf Disoprivan nicht verwendet werden, da Sicherheit und Wirksamkeit nicht nachgewiesen sind (siehe «Warnhinweise und Vorsichtsmassnahmen»).
Target Controlled Infusion (TCI)
Anwendung von Disoprivan mittels Disoprifusor TCI bei Erwachsenen
Die Verabreichung von Disoprivan mittels Disoprifusor TCI Systems (Target Controlled Infusion) ist beschränkt auf die Induktion und die Aufrechterhaltung einer Anästhesie und zur Sedierung bei beatmeten Erwachsenen auf der Intensivstation. Disoprifusor TCI soll bei Kindern (<16 Jahren) nicht angewendet werden.
Mit dem Disoprifusor TCI System kann der Anästhesist durch Eingeben einer Zielkonzentration von Propofol die gewünschte Induktionszeit und Anästhesietiefe bzw. Sedierung bestimmen und regulieren. Das Disoprifusor TCI System passt die Infusionsrate automatisch der erkannten Disoprivan-Konzentration an. Bei gewissen Disoprifusoren sind alternative Verabreichungsarten möglich, bei welchen nur TCI empfohlen wird, die auf vorausgesagten Propofol-Konzentrationen im Blut basiert.
Bitte beachten Sie die „Dosierungsrichtlinien für Disoprifusor TCI“ weiter unten. Das speziell zur Anwendung von Disoprivan entwickelte System heisst Disoprifusor TCI und enthält die Disoprifusor Software. Dieses System funktioniert nur nach Erkennen der elektronisch markierten Disoprivan PFS 10 mg/ml oder PFS 20 mg/ml.
Das Disoprifusor TCI-System geht davon aus, dass die initiale Propofol-Konzentration im Patienten Null ist. Wenn die Propofol-Plasmakonzentration beim Start nicht null ist, soll das Disoprifusor-TCI-System nicht angewendet werden. Wird bei einem Patienten, welcher mit Disoprifusor TCI-System sediert wurde, die Pumpe abgeschaltet, so soll das TCI-System nicht wieder eingeschaltet werden, weil durch die Löschung der pharmakokinetischen Daten und der Patientendaten eine falsche Targetkonzentration vorgespielt wird. In diesem Falle wird empfohlen, mit der konventionellen Disoprivan-Infusion den Patienten weiter zu sedieren.
Dosierungsrichtlinien für Disoprifusor TCI
Pharmakokinetik und Pharmakodynamik von Propofol ist unterschiedlich zwischen prämedizierten und nicht prämedizierten Patienten. Die Zielkonzentration soll gegen das Ansprechen des Patienten titriert werden, bis die gewünschte Anästhesietiefe erreicht ist.
Induktion einer Allgemeinanästhesie mittels Disoprifusor TCI
Erwachsene unter 55 Jahre: Eine Anästhesie kann normalerweise mit Propofol-Zielkonzentrationen von 4 bis 8 µg/ml induziert werden. Für prämedizierte Patienten wird zu Beginn ein Zielwert von 4 µg/ml empfohlen, und bei nicht prämedizierten Patienten ein solcher von 6 µg/ml. Die Induktionszeit liegt bei diesen Zielkonzentrationen in der Regel zwischen 60 und 120 Sekunden. Höhere Zielkonzentrationen ermöglichen eine schnellere Induktion, können aber zu einer stärkeren hämodynamischen und respiratorischen Depression führen.
Patienten über 55 Jahre und Patienten mit ASA Grad 3 oder 4: Zu Beginn soll eine tiefere Zielkonzentration verwendet werden. Diese kann dann in Abständen von einer Minute um je 0,5 bis 1,0 µg/ml erhöht werden, um eine allmähliche Induktion zu erreichen.
Aufrechterhaltung einer Allgemeinanästhesie mittels Disoprifusor TCI
Im Allgemeinen ist eine ergänzende Analgesie notwendig. Die Dosis dieser begleitenden Medikamente reduziert die Zielkonzentration von Disoprivan, die zur Aufrechterhaltung der Anästhesie benötigt wird. Mit Zielkonzentrationen im Bereich von 3 bis 6 µg/ml wird normalerweise eine zufriedenstellende Anästhesie aufrechterhalten.
Der Patient erwacht in der Regel bei einer Zielkonzentration von 1,0 bis 2,0 µg/ml; dies ist abhängig von der verabreichten Menge der Analgetika während der Anästhesie.
Anwendung bei Kindern
Disoprifusor TCI soll bei Kindern unter 16 Jahren nicht angewendet werden (siehe «Warnhinweise und Vorsichtsmassnahmen»).
Sedierung von Erwachsenen auf der Intensivstation mittels Disoprifusor TCI
Zur Sedierung auf der Intensivstation ist im Allgemeinen eine Zielkonzentration im Bereich von 0,2 bis 2,0 µg/ml erforderlich. Die Anwendung sollte mit einer tiefen Zielkonzentration begonnen und gegen das Ansprechen des Patienten titriert werden, bis die gewünschte Sedierungstiefe erreicht ist.
Wurde das Disoprifusor TCI System für die Anästhesie verwendet, kann es mit einer angepassten Zielkonzentration während der postoperativen Periode zur Sedierung auf der Intensivstation ebenfalls eingesetzt werden.
KontraindikationenDisoprivan darf nicht angewendet werden bei Überempfindlichkeit gegenüber dem Wirkstoff oder einem der Hilfsstoffe gemäss Zusammensetzung.
Disoprivan darf nicht angewendet werden bei Überempfindlichkeit gegenüber Sojaöl.
Disoprivan ist kontraindiziert zur Sedierung von Kindern unter 16 Jahren auf der Intensivstation (siehe «Warnhinweise und Vorsichtsmassnahmen»).
Warnhinweise und VorsichtsmassnahmenDisoprivan sollte von ausgebildetem Anästhesiepersonal oder speziell ausgebildetem Personal der Intensivpflegestation verabreicht werden. Die Patienten sind ständig zu überwachen, und Einrichtungen für die Offenhaltung der Atemwege, zur künstlichen Beatmung und Wiederbelebung sowie Sauerstoff sollten vorhanden sein.
Disoprivan soll nicht von derselben Person verabreicht werden, die den diagnostischen oder chirurgischen Eingriff vornimmt.
Während der Anästhesieinduktion können eine Hypotonie und eine transitorische Apnoe auftreten, was von der Dosierung des Mittels sowie der Prämedikation und anderen verwendeten Medikamenten abhängt.
Disoprivan besitzt keine vagolytischen Eigenschaften. Verbunden mit einer Erhöhung des Vagus-Tonus, wie er durch eine chirurgische Prozedur oder den gleichzeitigen Gebrauch von anderen Narkotika und Muskelrelaxantien zustande kommen kann, kann eine Bradykardie bis zum Herzstillstand/Asystolie oder kompletten Herzblock eintreten. Es wird deshalb empfohlen, speziell in Fällen, wo eine vagale Dominanz zu erwarten ist, oder wenn andere Medikamente mit neg. chronotroper Wirkung eingesetzt werden, zur Prämedikation oder während der Anästhesie ein Anticholinergikum zu verabreichen.
Sehr selten kann postoperativ eine Periode mit Bewusstseinsverlust auftreten, während welcher der Muskeltonus erhöht sein kann. Die Bewusstlosigkeit kann auch auftreten, nachdem der Patient bereits ansprechbar war. Obwohl der Zustand spontan reversibel ist, sollte der bewusstlose Patient adäquat betreut werden. Der Möglichkeit dieser Komplikation soll im Rahmen der ambulanten Anästhesie besondere Beachtung geschenkt werden.
Wird Disoprivan zur Sedierung während chirurgischen Eingriffen eingesetzt, können, wie auch mit anderen sedierenden Substanzen, unwillkürliche Bewegungen auftreten. Dies kann bei Operationen, die völlige Bewegungslosigkeit erfordert, gefährlich sein.
Disoprivan 20 mg/ml soll nicht als Bolusinjektion verwendet werden.
Bei Kombination von Propofol mit anderen Anästhetika (wie z.B. Alfentanil oder Sevofluran o.ä.) ist besondere Sorgfalt anzuwenden, da additive Wirkungen auftreten können (siehe „Interaktionen“).
Ein Anstieg der Körpertemperatur wird beobachtet, wenn Propofol zusammen mit Dexmedetomidin verabreicht wird; daher ist in diesem Fall Vorsicht geboten (siehe „Interaktionen“).
Bei Patienten mit beeinträchtigter Herz-, Lungen-, Nieren- oder Leberfunktion und bei hypovolämischen oder geschwächten Patienten ist Vorsicht geboten (siehe «Spezielle Dosierungsanweisungen»).
Wenn Disoprivan Epileptikern verabreicht wird, besteht möglicherweise ein Risiko für Konvulsionen.
Bei Patienten mit Störungen des Fettstoffwechsels oder in anderen Situationen, wo beim Gebrauch von Lipidemulsionen Vorsicht geboten ist, sollte mit der nötigen Umsicht vorgegangen werden.
Pädiatrische Neurotoxizität
Präklinische Studien zeigen, dass die Anwendung von Anästhetika (Flurane) oder Sedativa (Propofol, Ketamin), welche die NMDA-Rezeptoren blockieren und/oder die GABA-Aktivität verstärken, während der Zeit des schnellen Hirnwachstums oder der Synaptogenese zu einem Zellverlust im sich entwickelnden Gehirn führt, was mit anhaltenden kognitiven Defiziten verbunden sein kann. Die klinische Bedeutung dieser Befunde ist nicht bekannt (siehe unter
«Schwangerschaft, Stillzeit» und «Präklinische Daten»).
Kinder unter 6 Monaten sollen nicht mit Disoprivan anästhesiert werden.
Zur Sedierung von Kindern (<16 Jahren) während der Intensivbehandlung darf Disoprivan nicht verwendet werden, da Sicherheit und Wirksamkeit nicht nachgewiesen sind.
Es gibt Berichte über schwere Nebenwirkungen bei nicht bestimmungsgemässer Anwendung von Propofol zur Sedierung von Patienten unter 16 Jahren (einschliesslich Todesfälle); ein ursächlicher Zusammenhang wurde jedoch nicht gesichert. Insbesondere wurden metabolische Azidose, Hyperlipidämie, Rhabdomyolyse und/oder Herzversagen beobachtet. Am häufigsten traten diese Nebenwirkungen bei Kindern mit Atemwegsinfektionen auf, denen höhere Dosen verabreicht wurden als für die Sedierung Erwachsener im Rahmen einer Intensivbehandlung empfohlen.
Propofol-Infusionssyndrom
Ebenso gibt es Berichte über Fälle von metabolischer Azidose, Rhabdomyolyse, Hyperkaliämie, Hepatomegalie, Nierenversagen, Hyperlipidämie, Herzrhythmusstörungen, EKG-Veränderungen (gewölbte ST-Streckenerhebung, ähnliche EKG-Veränderungen wie beim Brugada-Syndrom) und/oder rasch progredientem Herzversagen (in einigen Fällen mit tödlichem Ausgang), das für gewöhnlich nicht auf inotrope, unterstützende Behandlung ansprach. Die Kombination dieser Nebenwirkungen wird als Propofol-Infusionssyndrom (PRIs) bezeichnet. Hauptsächlich (aber nicht ausschliesslich) waren Patienten mit Kopfverletzungen und erhöhtem intrakraniellem Druck oder Kinder mit Infektionen der Atemwege betroffen, die höhere Dosierungen als die bei Erwachsenen für eine Sedierung im Rahmen der Intensivbehandlung empfohlen erhielten. Die folgenden Faktoren scheinen das Risiko für die Entwicklung dieser Nebenwirkungen zu erhöhen: verringerte Sauerstoffzufuhr ins Gewebe, schwere neurologische Schäden und/oder Sepsis, hohe Dosen von einem oder mehreren der folgenden pharmakologischen Substanzen – Vasokonstriktoren, Steroide, Inotropika und/oder Propofol (meist nach einer Erhöhung der Dosis mit Dosen über 4 mg/kg/Std. länger als 48 Stunden). Anwender sollten daher beachten, dass eine Dosierung von 4 mg Propofol/kg KG/h möglichst nicht überschritten wird. Auf das Auftreten der genannten Nebenwirkungen ist sorgfältig zu achten.
Bei ersten Anzeichen der Symptome ist die Dosierung zu vermindern oder das Sedativum zu wechseln. Im Fall solcher Änderungen der Behandlung ist bei Patienten mit erhöhtem intrakraniellem Druck die Hirndurchblutung durch geeignete Massnahmen zu unterstützen.
EDTA bildet Komplexe mit Metallionen, einschliesslich Zink. Bei längerer Anwendung von Disoprivan sollte die Substitution von Zink bedacht werden, da der Serumspiegel von Zink um ca. 5% sinken kann. Dies gilt insbesondere für Patienten, die für einen Zinkmangel prädisponiert sind (Patienten mit Verbrennungen, Diarrhoe, schweren Infektionen und Patienten mit Leberzirrhose). Zinkmangel kann bekannterweise Wachstumsverzögerung, Alopezie, Dermatitis, Diarrhoe, Immunologie-Funktionsstörungen, Entwicklungsstörungen, psychologische Störungen, Gonaden-Atrophie, beeinträchtigte Spermatogenese oder angeborene Missbildungen auslösen.
Natrium
Diese Arzneimittel (Disoprivan/Disoprivan PFS 10 mg/ml, 20 mg/ml) enthalten weniger als 1 mmol Natrium (23 mg) pro 1 ml, d.h. sie sind nahezu „natriumfrei“.
InteraktionenDisoprivan wurde zusammen mit Spinal- und Epiduralanästhesien, mit den üblichen Prämedikationen, neuromuskulären Blockern, Inhalationsanästhetika und Analgetika verwendet; es wurden dabei keine pharmakologischen Inkompatibilitäten beobachtet.
Alfentanil
Die Kombination aus Propofol und Alfentanil verstärkt die sedierende und anästhetische Wirkung. Darüber hinaus steigert Alfentanil die dämpfende Wirkung von Propofol auf den systolischen Blutdruck und die Herzfrequenz. Bei gleichzeitiger Anwendung sollte eine Dosisanpassung von Propofol oder Alfentanil erwogen werden.
Dexmedetomidin
Die gleichzeitige Gabe von Dexmedetomidin und Propofol führt wahrscheinlich zu einem Anstieg der Körpertemperatur (Pyrexie). Die für eine Sedierung und Anästhesieeinleitung erforderliche Propofol-Dosis muss bei Anwendung von Dexmedetomidin möglicherweise gesenkt werden.
Sevofluran
Propofol und Sevofluran haben bei kombinierter Anwendung eine additive Wirkung auf die Anästhesie. Daher sollte bei gleichzeitiger Anwendung eine Dosisanpassung von Propofol oder Sevofluran erwogen werden.
Fentanyl
In der Gegenwart von Fentanyl können die Blutspiegel von Disoprivan erhöht sein.
Ciclosporin
Bei Patienten unter Ciclosporin-Therapie, welche gleichzeitig Lipidemulsionen (wie z.B. Propofol) erhielten, wurde über Leukoencephalopathie berichtet.
Valproat
Bei Patienten, die Valproat einnehmen, wurde die Notwendigkeit niedrigerer Propofol-Dosen beobachtet. Bei gleichzeitiger Anwendung muss eine Reduzierung der Propofol-Dosis in Betracht gezogen werden.
Midazolam
Es wurde beobachtet, dass Patienten, die Midazolam anwenden, eine niedrigere Propofol-Dosis benötigen. Die gleichzeitige Anwendung von Midazolam mit Propofol führt wahrscheinlich zu einer verstärkten Sedierung und Atemdepression. Bei gleichzeitiger Anwendung sollte eine Dosisreduktion von Propofol in Betracht gezogen werden.
Schwangerschaft, StillzeitSchwangerschaft
Es liegen keine klinischen Daten mit Anwendung bei Schwangeren vor. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt (siehe «Präklinische Daten» und «Warnhinweise und Vorsichtsmassnahmen»). Das potenzielle Risiko für den Menschen ist nicht bekannt.
Publizierte tierexperimentelle Studien mit Anästhetika/sedierenden Medikamenten berichteten von unerwünschten Wirkungen auf die Gehirnentwicklung im frühen Stadium (siehe «Warnhinweise und Vorsichtsmassnahmen und «Präklinische Daten»).
Disoprivan sollte deshalb während einer Schwangerschaft nicht angewendet werden.
Propofol durchquert die Plazentaschranke und kann eine neonatale Depression verursachen. Disoprivan sollte daher nicht bei geburtshilflichen Eingriffen eingesetzt werden.
Stillzeit
Studien mit stillenden Frauen haben gezeigt, dass Propofol in geringen Mengen in die Muttermilch übergeht. Mütter sollten daher bis zu 24 Stunden nach der Gabe von Propofol mit dem Stillen aussetzen und die entsprechende Muttermilch verwerfen.
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von MaschinenNach einer Allgemeinanästhesie ist eine angemessene Erholungszeit vor der Entlassung des Patienten sicherzustellen.
Die Patienten sollten informiert werden, dass die Fahrtüchtigkeit oder die Fähigkeit Maschinen zu bedienen nach einer Allgemeinanästhesie für einige Zeit beeinträchtigt sein kann.
Unerwünschte WirkungenDie am häufigsten berichteten unerwünschten Wirkungen, wie Hypotension, sind pharmakologisch vorhersehbare unerwünschte Wirkungen von Anästhetika.
Weil Anästhesie und Patienten auf der Intensivstation an sich schon ein erhöhtes Risiko aufweisen, können Ereignisse, welche in Zusammenhang mit Anästhesie und Intensivmedizin rapportiert werden, auch durch medizinische Eingriffe oder den Zustand des Patienten mitverursacht werden.
Sehr häufig: >1/10; häufig: >1/100, <1/10; gelegentlich: >1/1000, <1/100; selten: >1/10’000, <1/1000; sehr selten: <1/10’000, Häufigkeit nicht bekannt (kann aus den verfügbaren Daten nicht abgeschätzt werden).
Infektionen und parasitäre Erkrankungen
Sehr selten: Postoperatives Fieber.
Erkrankungen des Immunsystems
Sehr selten Angioödem, Bronchospasmus, Erythem und Hypotonie, Anaphylaxie einschliesslich anaphylaktischen Schocks.
Erkrankungen des Nervensystems
Bei der Induktion der Anästhesie mit Disoprivan können Anzeichen von Exzitation auftreten.
Häufig: Kopfschmerzen während der Aufwachphase.
Selten: Epileptiforme Bewegungen, einschliesslich Konvulsionen und Opisthotonus während Induktion, Aufrechterhaltung und Aufwachphase.
Sehr selten: Postoperativ kann eine Periode mit Bewusstseinsverlust auftreten, während welcher der Muskeltonus erhöht sein kann.
Psychiatrische Erkrankungen
Selten: Euphorische Stimmung
Herzerkrankungen
Häufig: Bradykardie. Ernsthafte Bradykardien sind selten. Vereinzelte Fälle einer Progression zur Asystolie wurden berichtet (siehe «Warnhinweise und Vorsichtsmassnahmen»).
Gelegentlich: Thrombosen und Phlebitiden.
Sehr selten: Lungenödem.
Gefässerkrankungen
Häufig: Hypotension; gelegentlich kann eine intravenöse Zufuhr von Flüssigkeit und eine Verringerung der Verabreichungsgeschwindigkeit von Disoprivan erforderlich sein.
Erkrankungen der Atemwege, des Brustraums und Mediastinums
Häufig: Vorübergehende Apnoe während der Induktion.
Erkrankungen des Gastrointestinaltrakts
Häufig: Nausea und Erbrechen während der Aufwachphase.
Leber- und Gallenerkrankungen
Sehr selten: Pankreatitis.
*Nicht bekannt: Hepatitis, akutes Leberversagen.
*Sowohl nach Langzeit- als auch nach Kurzzeitbehandlung und bei Patienten ohne zugrundeliegende Risikofaktoren.
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen
Sehr selten: Rhabdomyolyse.
Erkrankungen der Nieren und Harnwege
Sehr selten: Verfärbung des Urins nach längerer Anwendung von Disoprivan.
Erkrankungen der Geschlechtsorgane und der Brustdrüse
Sehr selten: Sexuelle Enthemmung und Priapismus.
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort
Sehr häufig: lokale Schmerzen; diese können unter Umständen während der Injektion an der Injektionsstelle auftreten und können minimal gehalten werden, wenn Disoprivan 10 mg/ml in die grösseren Venen des Unterarms oder der Ellenbeuge injiziert wird. Um den Injektionsschmerz zu reduzieren, kann Disoprivan 10 mg/ml auch mit Lidocain gemischt werden (siehe «Sonstige Hinweise»: «Hinweise für die Handhabung»).
Unerwünschte Wirkungen aus der Postmarketingphase
Berichte aus „off-label use” zeigten, dass bei Anwendung des pädiatrischen Dosierungsschemas (6 Monate bis 16 Jahre) bei Neugeborenen während der Induktion einer Anästhesie, eine kardiorespiratorische Depression auftreten kann (siehe «Dosierung/Anwendung»).
Propofol-Infusionssyndrom: Es traten metabolische Azidose, Rhabdomyolyse, Hyperkaliämie, Hepatomegalie, Nierenversagen, Hyperlipidämie, Herzrhythmusstörungen, EKG-Veränderungen und/oder Herzversagen im Rahmen einer Intensivbehandlung auf, in einigen Fällen mit tödlichem Ausgang (siehe «Warnhinweise und Vorsichtsmassnahmen»).
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von grosser Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdacht einer neuen oder schwerwiegenden Nebenwirkung über das Online-Portal ElViS (Electronic Vigilance System) anzuzeigen. Informationen dazu finden Sie unter www.swissmedic.ch.
ÜberdosierungEine akzidentielle Überdosierung kann eine kardiorespiratorische Depression bewirken.
Behandlung
Die Atemdepression sollte mittels künstlicher Beatmung mit Sauerstoff behandelt werden. Eine kardiovaskuläre Depression würde die Kopftieflagerung des Patienten und bei schweren Fällen die Anwendung von Plasmaexpandern und Vasopressoren erfordern.
Eigenschaften/WirkungenATC-Code
N01AX10
Wirkungsmechanismus / Pharmakodynamik
Propofol ist ein kurz wirksames, intravenöses Allgemeinanästhetikum mit einem raschen Wirkungseintritt nach etwa 30 Sekunden. Das Aufwachen erfolgt in der Regel schnell. Der Wirkungsmechanismus ist, wie bei allen Allgemeinanästhetika, kaum bekannt.
Normalerweise wird bei der Anwendung zur Einleitung und Aufrechterhaltung einer Allgemeinanästhesie mit Disoprivan eine Senkung des arteriellen Blutdruckes und eine Reduktion der Herzfrequenz beobachtet. Selten treten ungünstige Veränderungen der Hämodynamik auf.
Nach dem Verabreichen von Disoprivan kann eine Atemdepression auftreten. Diese verläuft qualitativ ähnlich jener anderer intravenöser Anästhetika.
Disoprivan reduziert den zerebralen Blutfluss, den intrakraniellen Druck und den zerebralen Metabolismus. Die Senkung des intrakraniellen Druckes ist bei Patienten mit erhöhtem Druck ausgeprägter.
Im Allgemeinen treten nach einer Anästhesie mit Disoprivan postoperative Übelkeit und Erbrechen seltener auf als nach einer Anästhesie mit Inhalationsanästhetika.
Klinische Wirksamkeit
Es sind keine Daten vorhanden.
PharmakokinetikAbsorption
Zwei Minuten nach einer i.v. Injektion von 2,5 mg/kg (Induktionsdosis) beträgt die Blutkonzentration ungefähr 4 µg/ml. Der Patient erwacht bei einer Blutkonzentration von etwa 1 µg/ml.
Wird Disoprivan zur Aufrechterhaltung der Anästhesie infundiert, nähert sich der Blutspiegel asymptotisch der Steady-State-Konzentration für die entsprechende Infusionsrate.
Distribution
Propofol ist zu etwa 98% an Plasmaeiweisse gebunden. Das Verteilungsvolumen beträgt ca. 10 l/kg Körpergewicht.
Metabolismus
Propofol wird durch Konjugation sowie durch Hydroxylierung und nachfolgender Konjugation vor allem in der Leber inaktiviert.
Elimination
Der Abfall der Blutkonzentration nach einer Bolusinjektion oder am Ende einer Anästhesie kann mit einem Dreikompartiment-Modell beschrieben werden. In der ersten Phase, der a-Phase, beträgt die Halbwertszeit 2 bis 4 Minuten. Sie wird gefolgt von der b-Phase. Die Halbwertszeit für diese Phase beträgt 30 bis 60 Minuten. Die langsamere Endphase ist gekennzeichnet durch eine Redistribution aus dem schlechter durchbluteten Gewebe.
Die totale Clearance beträgt 1,5 bis 2 l/Min. Die Konjugate von Propofol und dem entsprechenden Chinol werden durch die Nieren ausgeschieden.
Propofol ist stark lipophil mit einer extrarenalen Dosisfraktion (Qo) von 1,0.
Linearität/Nicht Linearität
Die Pharmakokinetik ist über den empfohlenen Dosierungsbereich linear.
Kinetik spezieller Patientengruppen
Es sind keine Daten vorhanden.
Präklinische DatenMutagenität
Propofol war in Genotoxizitäts-Studien nicht mutagen.
Kanzerogenität
Kanzerogenitätsstudien wurden nicht durchgeführt.
Reproduktions- und Entwicklungstoxizität
Unter hohen Dosen wurden embryotoxische Effekte beobachtet, aber teratogene Effekte traten nicht auf.
Veröffentlichte Tierstudien (einschliesslich bei Primaten) zu Dosierungen, die zu einer leichten bis mässigen Anästhesie führen, zeigen, dass die Anwendung von Anästhetika (Flurane) oder Sedativa (Propofol, Ketamin), welche die NMDA Rezeptoren blockieren und/oder die GABA-Aktivität verstärken, während der Phase des schnellen Gehirnwachstums oder der Synaptogenese einen Zellverlust in dem sich entwickelnden Gehirn zur Folge hat, der mit langfristigen kognitiven Defiziten verbunden sein kann. Die klinische Bedeutung dieser nicht-klinischen Befunde ist nicht bekannt.
Sonstige HinweiseInkompatibilitäten
Disoprivan ist mit Injektions- und Infusionslösungen inkompatibel und soll vor der Anwendung nicht mit diesen gemischt werden (inkompatibel z.B. mit NaCl-Lösung, Ringer-Laktatlösung). Wird der venöse Zugang auch für andere Medikamente verwendet, so sind sie am Ende der Infusionsleitung zuzufügen. Inkompatibel mit Disoprivan sind unter anderem Atracurium und Mivacurium.
Atracurium und Mivacurium sollen daher ohne vorheriges Spülen nicht durch dieselbe Infusionslinie wie Disoprivan gegeben werden.
Ausnahmen: siehe unter «Hinweise für die Handhabung».
Haltbarkeit
Das Arzneimittel darf nur bis zu dem auf der Packung mit „EXP“ bezeichneten Datum verwendet werden.
Nach Öffnen und Verdünnen innerhalb von maximal 6 Stunden verbrauchen. Sämtliche Reste wegwerfen.
Jede Durchstechflasche oder Fertigspritze ist nur für eine Anwendung an einem einzigen Patienten bestimmt. Bei Mehrfachanwendung besteht das Risiko für Sepsis. Disoprivan ist erst unmittelbar vor der Verwendung zu öffnen und wie andere Lipidemulsionen, innerhalb von maximal 8 Stunden, zu verwenden.
Besondere Lagerungshinweise
Die Emulsion nicht über 25 °C lagern. Nicht einfrieren.
Ausser Reichweite von Kindern aufbewahren.
Hinweise für die Handhabung
Jede Packung vor der Verwendung schütteln.
Disoprivan enthält kein Konservierungsmittel und bietet für Mikroorganismen günstige Wachstumsbedingungen. Während der gesamten Handhabung müssen deshalb sämtliche Vorsichtsmassregeln der Asepsis berücksichtigt werden. Keimfilter sind nicht verwendbar.
Ist die Verabreichung beendet, spätestens jedoch nach maximal 8 Stunden, müssen sowohl das Disoprivan-Reservoir als auch das Infusionsbesteck ersetzt werden. Das restliche Disoprivan darf nicht weiter verwendet werden.
Disoprivan kann durch ein Y-Stück nahe der Injektionsstelle parallel mit Infusionen von Glukose 5%, Kochsalz 0,9% oder Glukose 4% mit Kochsalz 0,18% (Infusionsflüssigkeiten Ph. Helv. VII) verabreicht werden. Vor der Anwendung soll Disoprivan jedoch nicht mit NaCl-Lösung gemischt werden.
Disoprivan 10 mg/ml: Disoprivan 10 mg/ml kann auch mit Glukose 5% (Infusionslösung Ph. Helv. VII) verdünnt werden. Sowohl Glas- als auch PVC-Infusionsflaschen und PVC-Infusionsbeutel sind geeignet. Die Verdünnung sollte nicht höher sein als 1:5 (2 mg Propofol pro ml). Sie soll unmittelbar vor der Verwendung aseptisch hergestellt und innerhalb von maximal 6 Stunden verbraucht werden.
Disoprivan 10 mg/ml kann mit Alfentanil-Injektionslösung 0,5 mg/ml im Verhältnis 20:1 bis 50:1 (V/V) gemischt werden. Die Mischungen sollen unmittelbar vor der Verwendung aseptisch hergestellt und innerhalb von maximal 6 Stunden verbraucht werden. Um den Injektionsschmerz zu reduzieren, kann Disoprivan 10 mg/ml mit Lidocain aseptisch in einer Injektionsspritze gemischt werden; 20 Teile Disoprivan 10 mg/ml werden mit 1 Teil 0,5%- oder 1%iger Lidocain-Injektionslösung (ohne antimikrobielle Zusätze) unmittelbar vor Gebrauch gemischt.
Disoprivan kann unverdünnt aus Infusionsflaschen, Plastikspritzen oder Disoprivan PFS (Fertigspritze) verabreicht werden. Wird Disoprivan unverdünnt zur Aufrechterhaltung einer Anästhesie verwendet, so wird empfohlen, eine Spritzen- oder volumetrische Pumpe einzusetzen, um die Infusionsrate zu steuern.
Die Infusion von verdünntem Disoprivan muss über ein kontrollierbares Infusionssystem (Bürette, Tropfenzähler oder volumetrische Pumpe) erfolgen, um die versehentliche Verabreichung grösserer Mengen Disoprivan zu vermeiden. Beim Festlegen des maximalen Volumens an Infusionsflüssigkeit im System sollte das Risiko einer unkontrollierten Infusion berücksichtigt werden.
Wird ein PVC-Infusionsbesteck verwendet, sollte der Infusionsbehälter immer voll sein. Deshalb sollte das für das Disoprivan benötigte Volumen dem Infusionssack entnommen und vollständig durch dasselbe Volumen von Disoprivan 10 mg/ml ersetzt werden.
Die Glasspritze von Disoprivan PFS hat einen geringeren Reibungswiderstand als übliche Plastikspritzen. Wird Disoprivan mittels einer von Hand gehaltenen Disoprivan PFS verabreicht, soll deshalb die Infusionslinie zwischen der Spritze und dem Patienten nicht unüberwacht offengelassen werden.
Werden Disoprivan PFS mit einer Spritzenpumpe verwendet, so ist auf eine entsprechende Kompatibilität zu achten. Insbesondere sollte der Pumpenaufbau einen Siphon-Effekt ausschliessen und die Pumpe sollte mit einem Okklusionsalarm (nicht grösser als 1000 mmHG) ausgestattet sein. Wird eine programmierbare Pumpe verwendet, welche verschiedene Spritzentypen zulässt, so ist für Disoprivan PFS die Einstellung «BD 50/60 ml PLASTIPAK» zu wählen.
Benützer des TCI-Systems sollten ausser mit der Funktionsweise der Infusionspumpe auch mit der Anwendung von Disoprivan mittels TCI und dem korrekten Gebrauch des Spritzen-Identifikationssystems vertraut sein.
Hinweise zur Vorbereitung der Disoprivan PFS Fertigspritze sind am Ende der Fachinformation aufgeführt.
Zulassungsnummer47162 / 53943 (Swissmedic)
PackungenDisoprivan 10 mg/ml:
5 Durchstechflaschen zu 20 ml [B]
Infusionsflaschen zu 50 ml und 100 ml [B]
Fertigspritze (PFS) zu 50 ml [B]
Disoprivan 20 mg/ml:
Infusionsflaschen zu 50 ml [B]
Fertigspritze (PFS) zu 50 ml [B]
ZulassungsinhaberinAspen Pharma Schweiz GmbH, Baar
Stand der InformationJuni 2025
Hinweise zur Vorbereitung der Disoprivan PFS Fertigspritze
1.Glas-Spritzenzylinder entnehmen und überprüfen; schütteln. Plastikdeckel entfernen. Gummiverschluss mit Alkohol 70% desinfizieren und trocknen lassen.
2.Luer-Anschluss entnehmen, Nadelhülse entfernen.
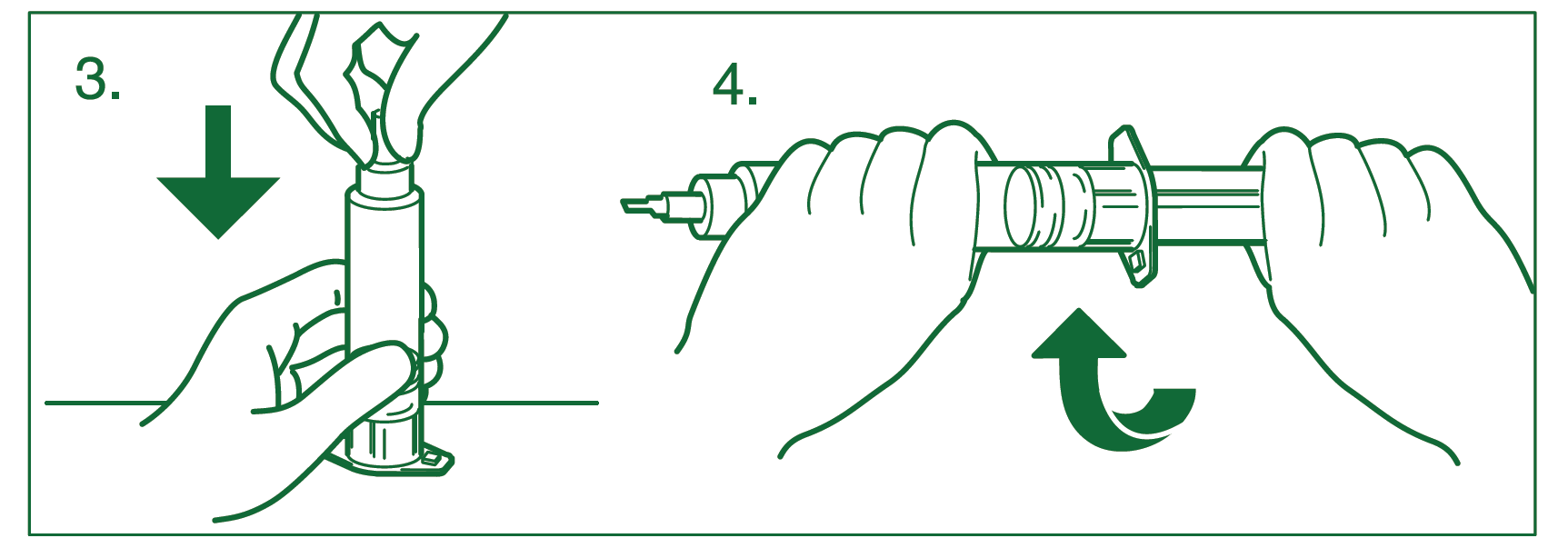
3.Glas-Spritzenzylinder senkrecht auf solide Unterlage stellen. Der Luer-Anschluss wird fest auf das Behältnis gedrückt, so dass die Nadel die Gummimembran durchdringt und der Ansatz die Bördelkappe vollständig verdeckt.
4.Kolben im Uhrzeigersinn in den Glas-Spritzenzylinder hineindrehen. Vorsicht: Kolben vollständig einschrauben.
5.Luer-Anschluss aufschrauben und Luftblasen aus der Spritze herausdrücken. Spritze mit Leitung verbinden. Angeschlossene Spritze in die Infusionspumpe einlegen.
DOC-01-09-2025
|

