ZusammensetzungHuminsulin Basal (NPH) 100 I.E./ml
Wirkstoffe
Insulinum Humanum ADNr isophanum100 U.I.
Humaninsulin aus genetisch verändertem Escherichia coli hergestellt.
Hilfsstoffe
Protamini sulfas, Zinci oxidum, Glycerolum, Dinatrii phosphas heptahydricus, Metacresolum, Phenolum, natrii hydroxidum, acidum hydrochloridum dilutum, aqua ad iniectabile q.s. ad suspens. pro 1 ml.
Gesamt-Natriumgehalt: 0,6 mg/ml.
Indikationen/AnwendungsmöglichkeitenDiabetes mellitus, sofern eine Insulinbehandlung notwendig ist.
Dosierung/AnwendungÜbliche Dosierung
Die Dosierung erfolgt aufgrund der individuellen Stoffwechselsituation und Lebensweise des Patienten.
Der Patient muss angewiesen werden, die verordnete Insulinmenge, den Abstand von Injektion und Einnahme der Mahlzeit, Diätvorschriften und tägliche körperliche Aktivität gewissenhaft einzuhalten und nicht eigenmächtig zu verändern.
Die Dosis wird im Allgemeinen 30-45 Minuten vor dem ersten Frühstück und dem Abendessen unter die Haut gespritzt.
Die Tagesdosis soll auf zwei Injektionen ungefähr im Verhältnis 2:1 (zwei Drittel morgens, ein Drittel abends) aufgeteilt werden. Darf nicht intravenös gespritzt werden.
Die Einstichstelle ist bei jeder Injektion zu wechseln und soll nicht massiert werden.
Um die Rückverfolgbarkeit von biotechnologisch hergestellten Arzneimitteln sicherzustellen, wird empfohlen Handelsname und Chargennummer bei jeder Behandlung zu dokumentieren.
Umstellung von einem Insulin auf andere Insuline
Die Umstellung von tierischen Insulinen auf biosynthetisches Humaninsulin kann bei manchen Diabetikern eine Dosisreduktion erforderlich machen, besonders wenn sie sehr genau, also auf eher niedrige Blutzuckerspiegel eingestellt waren. Die Dosisverminderung kann dann sofort nach der Umstellung stattfinden oder als schrittweiser Prozess über mehrere Wochen durchgeführt werden. Wenn der Insulinbedarf sinkt, besteht das Risiko der Hypoglykämie, dessen sich sowohl der Arzt als auch der Patient bewusst sein sollten. Wenn die tägliche Dosis 40 I.E. unterschreitet, ist das Risiko gering.
Insulinresistente Patienten, die mehr als 100 I.E. pro Tag benötigen, sollten nur im Spital umgestellt werden. Umstellung nur unter ärztlicher Kontrolle! (Siehe auch den Hinweis unter Hypoglykämie im Kapitel «Unerwünschte Wirkungen».)
Spezielle Dosierungsanweisungen
Bei Krankheit: Der Insulinbedarf kann sich während einer endokrinen Krankheit wie Nebennierenrindeninsuffizienz, Hypothyreose oder Hypophysenkrankheit wesentlich ändern. Eine Anpassung der Insulindosis kann auch bei erhöhter körperlicher Belastung oder Diätfehlern erforderlich sein. Der Bedarf kann auch bei psychischer Belastung ansteigen, bei Vorliegen einer renalen oder hepatischen Störung absinken. Solche Effekte sind auch bei gleichzeitiger Gabe verschiedener Medikamente möglich (siehe «Interaktionen»).
Kinder und Jugendliche
Es gibt nur wenige Daten aus klinischen Studien mit Huminsulin bei Kindern unter 3 Jahren.
Art der Anwendung
Wie bei allen Insulinen muss die Injektionsstelle bei jeder Injektion innerhalb des gewählten Injektionsbereichs gewechselt werden, um das Risiko einer Lipodystrophie oder einer kutanen Amyloidose zu verringern.
KontraindikationenInsulin ist bei Hypoglykämie und Insulinom kontraindiziert.
Huminsulin Basal darf nie intravenös appliziert werden.
Bei Überempfindlichkeit gegenüber der Hilfsstoffe (unter anderem der Konservierungsmittel und Protamin) sollte auf ein Insulinpräparat ohne diese Zusätze übergegangen werden.
Bei Speziesspezifischer Überempfindlichkeit gegenüber Insulin ist die Verträglichkeit von Huminsulin-Präparaten durch Hauttests (intrakutan) zu prüfen.
Eine schwere Insulinallergie vom Soforttyp muss eine völlige Neukonzeption der Diabetestherapie nach sich ziehen.
Eine immunologische Kreuzreaktion zwischen Humaninsulin und tierischem Insulin ist möglich.
Warnhinweise und VorsichtsmassnahmenBeim mit Insulin behandelten Zuckerkranken besteht grundsätzlich das Risiko einer Hypoglykämie, besonders bei unregelmässigen Verabreichungen, unregelmässiger Nahrungsaufnahme mit stark schwankenden oder bei durchschnittlich tiefen Blutzuckerwerten, oder zu Beginn der Behandlung. Dies kann die Sicherheit z.B. bei Führen eines Autos oder bei der Bedienung von Maschinen beeinträchtigen.
Alkoholkonsum erhöht die Gefährdung zusätzlich.
Vorsicht ist auch geboten, wenn der Patient früher schwere Hypoglykämien durchgemacht hat oder wenn mittels Mehrfachinjektionen nach dem Basis-Bolus-Prinzip mit Pens versucht wird, besonders tiefe Blutzuckerwerte zu erreichen. Unbehandelte hypoglykämische und hyperglykämische Reaktionen können zu Bewusstlosigkeit, Koma und Tod führen.
Abgeschwächte Warnsymptome einer Hypoglykämie
In gewissen Situationen, so u.a. auch nach der Umstellung von tierischem auf humanes Insulin, können die Warnzeichen der Hypoglykämie abgeschwächt sein, sodass diese überraschend auftreten kann (siehe unter «Unerwünschte Wirkungen»). Bestimmte Umstände wie lange Diabetes-Dauer, intensivierte Insulintherapie, diabetische Nervenerkrankung oder Medikation mit Beta-Blockern können die frühen Warnsymptome einer Hypoglykämie unterschiedlich oder weniger ausgeprägt erscheinen lassen.
Um der Hypoglykämie vorbeugen zu können, sollte der Patient Trauben- oder Würfelzucker oder ähnliches (keine Zuckerersatzstoffe) mit sich tragen und bei ersten Anzeichen einnehmen. Der Diabetikerausweis sollte immer mit sich geführt werden.
Die Behandlung mit Huminsulin kann zur Bildung von Antikörpern führen, diese Antikörpertiter liegen dann allerdings niedriger als solche, die sich aufgrund einer Gabe von gereinigtem Insulin tierischen Ursprungs aufbauen.
·β-Blocker können die üblichen Hypoglykämie-Warnsymptome abschwächen bzw. maskieren.
·Alkoholkonsum kann die Hypoglykämie-Gefahr erhöhen (Hemmung der hepatischen Glukoneogenese).
·Marihuana-Konsum kann möglicherweise eine Verschlechterung der Glukosetoleranz bewirken.
Es gibt nur wenig Information betreffend der Wirkung anderer illegaler Substanzen auf den Blutzucker. Andere Interaktionen: siehe Rubrik «Interaktionen»!
Huminsulin enthält Metacresol, das in seltenen Fällen allergisch Reaktionen auslösen kann.
Kombination von Thiazolidindionen (TZD) mit Insulin:
Die Kombination von TZD mit Insulin ist mit einem erhöhten Risiko für Ödeme und Herzinsuffizienz verbunden, insbesondere bei Patienten mit vorbestehender Herzerkrankung.
Patienten müssen angewiesen werden, die Einstichstelle kontinuierlich innerhalb des gegebenen Injektionsbereiches zu wechseln, um das Risiko zu verringern, eine Lipodystrophie oder eine kutane Amyloidose zu entwickeln. Injektionen in einen Bereich, der von Lipodystrophie oder kutaner Amyloidose betroffen ist, birgt die Gefahr einer verzögerten Insulinresorption. Ein plötzlicher Wechsel der Einstichstelle (in einen nicht betroffenen Bereich) kann zu einer Hypoglykämie führen.
Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro Dosiereinheit, d.h. es ist nahezu «natriumfrei».
Interaktionen1. Der Insulinbedarf kann vermindert sein in Gegenwart von Substanzen, welche die Insulinwirkung verbessern (Insulinsensitivität erhöhen), die Insulinsekretion steigern, die hepatische Glukoneogenese hemmen oder die intestinale Glukoseaufnahme beeinflussen. Bei gleichbleibender Insulinmenge besteht somit erhöhte Hypoglykämie-Gefahr durch gleichzeitige Einnahme von:
Oralen Antidiabetika; Alkohol; ACE-Hemmern (z.B. Captopril und Enalapril); Angiotensin II Rezeptorblocker; antiarrhythmischen Substanzen wie Disopyramid; α-Blockern und Clonidin; SSRI; Fenfluramine; MAO-Hemmern; trizyklischen Antidepressiva; Salicylaten und (selten) anderen NSAIDs; Fibraten; Tetracyclinen; Pentamidin (Hypoglykämie; gelegentlich mit nachfolgender Hyperglykämie); Anti-Malariamitteln (Chinin, Chloroquin, Mefloquin); Sulfonamiden (z.B. Cotrimoxazol); Cimetidin und Ranitidin.
2. Der Insulinbedarf kann erhöht sein bei gleichzeitiger Anwendung der folgenden Substanzen bzw. Substanzgruppen:
Orale Kontrazeptiva und andere Oestrogen- oder Progestagen-Präparate; Kortikosteroide und ACTH; GH (Somatotropin); Danazol; Schilddrüsenhormone; Sympathikomimetika (vor allem β2-Sympathikomimetika wie Ritodrin, Salbutamol, Terbutalin, aber auch α-selektive Sympathikomimetika, sowie nicht selektive wie Epinephrin; Diazoxid; Nikotinsäure und –Derivate; Chlorpromazin (vor allem in hohen Dosen) und andere Phenothiazin-Derivate; Diuretika (z.B. Thiazid-Diuretika, Indapamid und Furosemid); Anti-retrovirale Substanzen; Immunosuppressive Substanzen (Ciclosporin, Tacrolimus, Sirolimus); atypische Antipsychotika.
3. Bei Anwendung der folgenden Substanzen kann die Insulinwirkung je nach Dosis verstärkt bzw. abgeschwächt werden:
Octreotid-, Salicylsäure-Derivate, Lithium-Salze (selten).
β-Blocker können zu einer Verstärkung der Insulinresistenz, aber auch, in gewissen Fällen, zu einer Hypoglykämie führen. Ausserdem können die Hypoglykämie-Warnsymptome abgeschwächt bzw. maskiert werden.
Der Arzt sollte konsultiert werden, wenn andere Medikamente zusätzlich zu Huminsulin verwendet werden (siehe «Warnhinweise und Vorsichtsmassnahmen»).
Schwangerschaft, StillzeitSchwangerschaft
Es ist wesentlich, während der ganzen Schwangerschaft die insulinabhängigen Diabetespatientinnen gut einzustellen.
Erstes Trimenon
Der Insulinbedarf fällt gewöhnlich während des ersten Trimenons.
Zweites Trimenon
Der Insulinbedarf steigt während des zweiten Trimenons.
Drittes Trimenon
Der Insulinbedarf steigt während des dritten Trimenons, er vermindert sich wieder nach der Geburt.
Stillzeit
Während der Stillzeit können bei Diabetikerinnen Anpassungen der Insulindosierung und/oder Diät erforderlich sein.
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von MaschinenEine Hypoglykämie kann die Konzentrations- und Reaktionsfähigkeit eines Patienten herabsetzen. Dies kann in Situationen, in denen diese Fähigkeiten von besonderer Bedeutung sind (z.B. beim Fahren eines Autos oder beim Bedienen von Maschinen), ein Risiko darstellen.
Dem Patienten sollte geraten werden, Vorsichtsmassnahmen zur Vermeidung von Hypoglykämien beim Führen von Kraftfahrzeugen zu treffen. Dieses ist bei Patienten mit häufigen Hypoglykämie-Episoden oder verringerter oder fehlender Wahrnehmung von Hypoglykämie-Warnsymptomen besonders wichtig. In diesen Fällen sollte überlegt werden, ob das Führen eines Kraftfahrzeugs überhaupt ratsam ist.
Unerwünschte WirkungenDie unerwünschten Wirkungen aus den klinischen Studien und aus Post-marketing Daten sind unten gemäss MedDRA System Organklassen, und nach absteigendem Schweregrad klassifiziert.
Häufigkeitseinteilung: Sehr häufig (≥1/10), häufig (≥1/100, <1/10), gelegentlich (≥1/1000, <1/100), selten (≥1/10000, <1/1000), sehr selten (<1/10000).
Erkrankungen des Immunsystems
Häufig: Urtikaria, Rötung.
Sehr selten: Generalisierte, systemische allergische Reaktionen.
Es können generalisierte, systemische allergische Reaktionen gegen Insulin auftreten. Diese können einen Hautausschlag am ganzen Körper (Urtikaria), Kurzatmigkeit (Dyspnoe), Röcheln, einen Blutdruckabfall (arterielle Hypotonie), einen beschleunigten Puls (Tachycardie) oder Schwitzen hervorrufen.
Schwere allergische Reaktionen (Soforttyp) können eine Unterbrechung der Therapie oder entsprechende andere Massnahmen erforderlich machen. In schweren Fällen können generalisierte allergische Reaktionen lebensbedrohlich sein.
Stoffwechsel und Ernährungsstörungen
Hypoglykämie, Hyperglykämie.
Augenerkrankungen
Vorübergehende Änderung der Sehschärfe.
Bei Beginn der Therapie kann es zu vorübergehender Änderung der Sehschärfe kommen. Diese Nebenwirkung geht im weiteren Behandlungsverlauf meist von selbst zurück.
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort
Häufig: Ausschlag.
Gelegentlich kommt es bei Patienten zu Ödemen, lokalen allergischen Reaktionen wie Rötung, Schwellung und Juckreiz am Injektionsort.
Funktionsstörungen der Haut und des Unterhautzellgewebes
Gelegentlich: Lipodystrophie.
Unbekannt: kutane Amyloidose.
Bei Beginn der Therapie und bei gleichzeitiger Insulintherapie wurde über Ödeme berichtet, insbesondere dann, wenn eine vorherige unzureichende Stoffwechselkontrolle durch eine Intensivierung der Insulintherapie verbessert wurde. Diese sind transitorisch und gehen im weiteren Behandlungsverlauf meist von selbst zurück.
Der Patient ist darüber aufzuklären, bei welchen Symptomen er unbedingt sofort seinen Arzt verständigen muss, etwa bei starken Rötungen, die mit Juckreiz und Quaddelbildung einhergehen und sich schnell über die Injektionsstelle hinaus ausdehnen.
In manchen Fällen können die lokalen allergischen Reaktionen auf andere Ursachen als auf das Insulin zurückzuführen sein, beispielsweise auf irritierende Bestandteile des Hautdesinfektionsmittels oder auf eine schlechte Injektionstechnik.
Beschreibung ausgewählter Nebenwirkungen
Hypoglykämie
Die Hypoglykämie (Blutzuckerabfall < 2-3 mmol/l) ist, wie bei allen Insulinen, die häufigste unerwünschte Wirkung, welche auftreten kann. Anzeichen dafür sind:
a) Neurovegetative Zeichen: Schwitzen, Hungergefühl, Zittern, Blässe, Herzklopfen, Kopfschmerzen.
b) Neuroglykopenische Zeichen: Konzentrationsstörungen, Verhaltensauffälligkeiten (Unruhe, Reizbarkeit, Aggressivität, Verwirrtheit, u.a.), Bewusstseinsstörungen, Koordinations-, Seh- und Sprachstörungen. Diese können über Benommenheit und Somnolenz bis Bewusstlosigkeit zum Koma fortschreiten. Die Hypoglykämie kann auch zu epileptischen Anfällen führen, oder als zerebraler Insult, z.B. mit (meist vorübergehender) Hemiparese, Aphasie, positivem Babinskizeichen, imponieren.
c) Abgeschwächte/veränderte Warnsymptome: besonders bei Einstellung auf tiefe Blutzuckerwerte (z.B. bei Mehrfachinjektionen nach dem Basis-Bolus-Prinzip), aber auch bei lang bestehendem Diabetes (u.U. mit Neuropathie), bei Präparatwechsel, u.a. können die Warnsymptome der Hypoglykämie verändert und die neurovegetativen Symptome abgeschwächt sein oder erst spät auftreten. Dies wurde von einigen Patienten auch nach Umstellung von tierischem auf humanes Insulin, aber auch sonst gelegentlich bei Präparatwechsel, beobachtet.
Überdosierung von Insulin, aussergewöhnliche körperliche Belastung, Versäumen einer Mahlzeit, Erbrechen oder Durchfall, endokrine Krankheiten wie Nebennierenrindeninsuffizienz und Hypothyreose können zu starker Unterzuckerung führen.
Alkoholgenuss jeglicher Art kann eine Unterzuckerung gefährlich verstärken!
Wenige Patienten, bei denen eine Unterzuckerung nach Umstellung auf Humaninsulin auftrat, haben berichtet, dass die Frühwarnsymptome verändert oder weniger ausgeprägt waren als unter tierischem Insulin.
Der Patient ist anzuweisen, über hypoglykämische Reaktionen so rasch wie möglich zu berichten, damit die Einstellung überprüft werden kann.
Die Umstellung auf ein anderes Insulinpräparat soll nur unter sorgfältiger ärztlicher Kontrolle und nach genauer Instruktion erfolgen. Auch Dosis und Zeitpunkt der Injektion sollen nur nach Absprache mit dem Arzt oder auf seine Anweisung geändert werden.
Dem Patienten ist zu empfehlen, seine nähere Umgebung (Freunde, Arbeitskollegen) über seine Zuckerkrankheit zu informieren sowie über die entsprechenden Verhaltensregeln; unter anderem auch wie man Glukagon subkutan injiziert.
Hyperglykämie
Ein diabetisches Koma kann die Folge von überhöhtem Blutzucker sein. Als Ursache kommen in Frage: Auslassen oder Verringern von Insulininjektionen oder erhöhter Insulinbedarf wegen Infektionen oder anderen Krankheiten. Das diabetische Koma entwickelt sich langsam über Stunden und Tage. Erste Anzeichen sind Durst, grosse Urinmengen, Appetitlosigkeit, Müdigkeit, trockene Haut, schnelle und tiefe Atmung sowie hohe Glucose- und Acetonwerte im Urin. Auch in diesen Fällen ist der Patient zu instruieren, den Arzt sofort zu kontaktieren.
Erkrankungen der Haut und des Unterhautzellgewebes
Wie bei jeder Insulintherapie kann es an der Injektionsstelle zu einer Lipodystrophie und kutaner Amyloidose kommen, die die Insulinresorption im betroffenen Bereich verzögert. Ein ständiger Wechsel der Einstichstelle im gegebenen Injektionsbereich kann helfen, diese Reaktionen abzuschwächen oder zu vermeiden (siehe auch Rubrik «Warnhinweise und Vorsichtsmassnahmen).»
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von grosser Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdacht einer neuen oder schwerwiegenden Nebenwirkung über das Online-Portal ElViS (Electronic Vigilance System) anzuzeigen. Informationen dazu finden Sie unter www.swissmedic.ch.
ÜberdosierungÜberdosierung verursacht Hypoglykämie und ist zunächst bei milden hypoglykämischen Episoden mit oraler Verabreichung von Traubenzucker oder Zucker zu behandeln. Mässig schwere Hypoglykämie kann durch i.m. oder s.c. Verabreichung von Glucagon kontrolliert werden. Wenn der Patient jedoch komatös ist, sollte Glucagon oder Glucose i.v. verabreicht werden.
Es kann notwendig sein, die Kohlenhydrataufnahme und die Beobachtung fortzuführen, da eine Hypoglykämie nach nur scheinbarer Genesung wieder auftreten kann.
Eigenschaften/WirkungenATC-Code
A10AC01
Wirkungsmechanismus
Die Hauptwirkung des Insulins ist die Regulierung des Glucosestoffwechsels.
Ausserdem haben Insuline zahlreiche anabole und anti-katabole Wirkungen in einer Vielzahl unterschiedlicher Gewebe. Im Muskelgewebe umfasst dies eine Steigerung der Glykogen-, Fettsäure-, Glycerol- und Proteinsynthese sowie der Aminosäureaufnahme; gleichzeitig werden die Glukogenolyse, die Glukoneogenese, die Ketogenese, die Lipolyse, der Proteinkatabolismus und der Aminosäuretransport aus der Zelle vermindert.
Das typische Aktivitätsprofil (Glucosverwendungskurve) nach subkutaner Injektion ist unten mit fetter Linie illustriert. Schwankungen, welche bei einem Patienten bezüglich zeitlichem Verlauf und/oder Intensität oder Insulinaktivität auftreten können, werden durch die schattierte Fläche illustriert. Individuelle Variabilität hängt von Faktoren wie applizierte Dosis, dem Injektionsort, Temperatur und körperlicher Aktivität des Patienten ab.
Huminsulin Basal
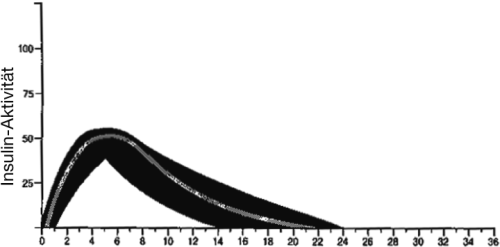
Zeit (Stunden)
Pharmakodynamik
Keine Daten vorhanden.
Klinische Wirksamkeit
Keine Daten vorhanden.
PharmakokinetikAbsorption
Nicht zutreffend.
Distribution
Nicht zutreffend.
Metabolismus
Die Pharmakokinetik von Insulin widerspiegelt nicht die Stoffwechselwirkung dieses Hormons. Deshalb ist angezeigter, die Glucoseverwendungskurven (wie oben besprochen) zur Betrachtung der Insulinwirkung heranzuziehen.
Elimination
Nicht zutreffend.
Präklinische DatenHuminsulin-Präparate enthalten Insulin, das seiner Struktur nach identisch mit menschlichem Insulin ist. Es wird gentechnologisch über Proinsulin hergestellt.
Langzeittoxizität (bzw. Toxizität bei wiederholter Verabreichung)
Aus subchronischen Toxizitätsstudien wurden keine schwerwiegenden Ereignisse gemeldet.
Mutagenität
Huminsulin zeigte in einer Reihe in vitro und in vivo gentoxikologischer Untersuchungen keine mutagenen Effekte.
Sonstige HinweiseInkompatibilitäten
Die Wirkung einer Mischung von Humaninsulin verschiedener Hersteller wurde nicht untersucht.
Huminsulin-Darreichungsformen sollen nicht mit Insulinpräparaten anderer Hersteller oder mit Insulinen tierischen Ursprungs gemischt werden.
Hinweise
Der Patient muss darauf hingewiesen werden, bei unvorhergesehenem Arztwechsel (Unfall oder Erkrankung auf Reisen) den behandelnden Arzt auf die Zuckerkrankheit hinzuweisen (Diabetikerpass).
Haltbarkeit
Das Arzneimittel darf nur bis zu dem auf dem Behälter mit «EXP» bezeichneten Datum verwendet werden.
Haltbarkeit nach Anbruch
Huminsulin Patrone
Nach Einsetzen der Insulin-Patrone in den Pen beträgt die Haltbarkeit des Insulins bei Raumtemperatur (15-25°C) für die 3.0 ml Patronen 4 Wochen (Vermeidung direkter Sonneneinstrahlung). Danach sollen die Patronen nicht mehr verwendet werden, auch dann nicht, wenn noch Insulin enthalten ist.
Huminsulin KwikPen
Nach Anbruch des Fertigpens beträgt die Haltbarkeit des Insulins bei Raumtemperatur (15-25°C) 4 Wochen (Vermeidung direkter Sonneneinstrahlung). Danach soll Huminsulin KwikPen nicht mehr verwendet werden, auch dann nicht, wenn noch Insulin enthalten ist.
Besondere Lagerungshinweise
Huminsulin-Präparate sollen weder grosser Hitze oder Sonnenlicht ausgesetzt werden.
Im Kühlschrank (2-8°C) lagern.
Nicht einfrieren.
Ausser Reichweite von Kindern aufbewahren.
Hinweise für die Handhabung
Zur Vermeidung einer möglichen Übertragung von Krankheiten darf jeder KwikPen oder Patrone nur von einer einzigen Person benutzt werden, auch wenn die Nadel gewechselt wird.
Patronen
Achtung! Dieses Insulin enthält 100 I.E./ml. Die Patronen wurden ausschliesslich für die Anwendung in einem Lilly Pen entwickelt und getestet.
Bei der Applikation mittels dafür geeignetem Lilly-Pen wird das Insulin subkutan injiziert. Vor der Anwendung soll sichergestellt werden, dass in der dem Pen beigelegten Bedienungsanleitung Huminsulin oder Lilly Patronen erwähnt werden.
Das Präparat darf nicht intravenös gespritzt werden. Die Einstichstelle ist bei jeder Injektion zu wechseln und soll nicht massiert werden.
Vor der Anwendung sollte die Patrone 10x zwischen den Handflächen hin und her gerollt und 10x langsam um 180° gewendet werden, um das in der Patrone enthaltenen kleine Glaskügelchen bei jeder Inversion von einer Extremität der Patrone zur anderen Extremität rollen zu lassen. Das Insulin sollte nach Durchmischen ein einheitlich wolkiges oder milchiges Aussehen haben. Sollte dies nicht der Fall sein, wiederholen Sie dieses Vorgehen, bis der Inhalt gut gemischt ist. Die Patronen im Pen sollen regelmässig überprüft und bei Anwesenheit von Klümpchen oder festen, weissen Teilchen am Boden oder an den Wänden der Patronen, die ihnen ein «frostiges» Aussehen verleihen, nicht mehr verwendet werden. Die Patronen sind so konstruiert, dass sie eine Mischung mit anderen Insulinen in der Patrone nicht erlauben.
Die Patronen können nach Aufbrauchen nicht wieder gefüllt werden.
Die Bedienungsanleitungen für den Pen hinsichtlich des Einlegens der Patrone, des Aufsetzens der Nadel und der Verabreichung der Insulin-Injektion sind genau zu befolgen.
Huminsulin KwikPen
Huminsulin KwikPen sind Fertigpens zur subkutanen Verabreichung von Insulin. Huminsulin KwikPen dürfen nicht für eine intravenöse Applikation verwendet werden. Die Einstichstelle ist bei jeder Injektion zu wechseln und soll nicht massiert werden. Vor der Anwendung sollte der KwikPen 10x zwischen den Handflächen hin und her gerollt und 10x langsam um 180° gewendet werden, um das in der Patrone enthaltenen kleine Glaskügelchen bei jeder Inversion von einer Extremität der Patrone zur anderen Extremität wandern zu lassen. Das Insulin sollte nach Durchmischen ein einheitlich wolkiges oder milchiges Aussehen haben. Sollte dies nicht der Fall sein, wiederholen Sie dieses Vorgehen, bis der Inhalt gut gemischt ist. Der KwikPen sollte regelmässig überprüft und bei Anwesenheit von Klümpchen oder festen, weissen Teilchen am Boden oder an den Wänden der Patronen, die ihnen ein «frostiges» Aussehen verleihen, nicht mehr verwendet werden.
Für Instruktionen zur Verabreichung der Insulin-Injektion ist die Bedienungsanleitung des Huminsulin KwikPen genau zu befolgen.
Fertigpens Huminsulin KwikPen können nach dem Aufbrauchen nicht nachgefüllt werden, sondern werden verworfen oder dem Recycling zugeführt.
Zulassungsnummer51750, 61550 (Swissmedic).
PackungenHuminsulin Basal (NPH) 100 I.E./ml:
Patronen (3,0 ml) für 3,0 ml Pen: 5 (B)
Huminsulin KwikPen (3,0 ml): 5 (B)
ZulassungsinhaberinEli Lilly (Suisse) S.A. Vernier/Genève.
Stand der InformationSeptember 2021
|

