ZusammensetzungWirkstoffe
Isoleucin, Leucin, wasserfreies Lysin als Lysinhydrochlorid, Methionin, Phenylalanin, Threonin, Tryptophan, Valin, Arginin, Histidin als Histidinhydrochlorid Monohydrat, Alanin, Aspartinsäure, Glutaminsäure, Glycin, Prolin, Serin, Natriumhydroxid, Natriumchlorid, Natriumacetat als Natriumacetat-Trihydrat, Kaliumacetat, Magnesiumacetat als Magnesiumacetat-Tetrahydrat, wasserfreies Calciumchlorid als Calciumchlorid-Dihydrat, Glucose als Glucose-Monohydrat, wasserfreies Natriumdihydrogenphosphat als Natriumdihydrogenphosphat-Dihydrat, Zinkacetat als Zinkacetat-Dihydrat, Sojaöl, mittelkettige Triglyceride, Omega-3-Säurentriglyceride.
Hilfsstoffe
Citronensäure-Monohydrat, Eilecithin, Glycerol, Natriumoleat corresp. Natrium 4,5 mg/Liter, allrac-α-Tocopherol (E 307), Natriumhydroxid corresp. Natrium bis max. 6,9 mg/Liter (zur pH-Anpassung), Wasser für Injektionszwecke.
Indikationen/AnwendungsmöglichkeitenZufuhr von Energie, essentiellen Fettsäuren einschliesslich Omega-3- und Omega-6- Fettsäuren, Aminosäuren, Elektrolyten und Flüssigkeiten im Rahmen einer parenteralen Ernährung bei Patienten mit mittelschwerer bis schwerer Katabolie, wenn eine orale oder enterale Ernährung nicht möglich, unzureichend oder kontraindiziert ist.
Dosierung/AnwendungZur zentralvenösen Infusion.
Die Dosierung ist den individuellen Bedürfnissen der Patienten anzupassen.
Es wird empfohlen, Omegaflex plus kontinuierlich zu verabreichen. Eine stufenweise Steigerung der Infusionsrate in den ersten 30 Minuten auf die gewünschte Infusionsrate beugt möglichen Komplikationen vor.
Jugendliche ab 14 Jahren und Erwachsene
Die maximale Tagesdosis beträgt 40 ml/kg KG, entsprechend:
1,54 g Aminosäuren/kg KG und Tag,
4,8 g Glucose/kg KG und Tag,
1,6 g Fett/kg KG und Tag.
Die maximale Infusionsgeschwindigkeit beträgt 2,0 ml/kg KG und Stunde entsprechend:
0,08 g Aminosäuren/kg KG und Stunde,
0,24 g Glucose/kg KG und Stunde,
0,08 g Fett/kg KG und Stunde.
Für einen Patienten mit 70 kg KG entspricht dies einer Infusionsgeschwindigkeit von 140 ml pro Stunde. Es werden pro Stunde 5,4 g Aminosäuren, 16,8 g Glucose und 5,6 g Fett verabreicht.
Patienten mit Leberfunktionsstörungen
Bei Patienten mit Leberinsuffizienz sollten die Dosen individuell angepasst werden (Siehe auch “Warnhinweise und Vorsichtsmassnahmen”).
Patienten mit Nierenfunktionsstörungen
Bei Patienten mit Niereninsuffizienz sollten die Dosen individuell angepasst werden (Siehe auch “Warnhinweise und Vorsichtsmassnahmen”).
Kinder und Jugendliche
Neugeborene, Säuglinge und Kleinkinder im Alter von < 2 Jahre
Omegaflex plus darf nicht bei Neugeborenen, Säuglingen und Kleinkindern im Alter von < 2 Jahren angewendet werden (siehe “Kontraindikationen”).
Kinder im 3. bis 13. Lebensjahr:
Die angegebenen Dosierungsempfehlungen stellen orientierende Durchschnittswerte dar. Die Dosierung muss individuell nach Alter, Entwicklungsstand und Krankheit angepasst werden. Bei der Berechnung der Dosierung muss der Hydratationszustand des pädiatrischen Patienten berücksichtigt werden.
Bei Kindern kann es erforderlich sein, die Ernährungstherapie mit der Hälfte der angestrebten Dosis zu beginnen. Die Dosierung sollte schrittweise entsprechend der individuellen Umsatzkapazität bis zum Maximalwert gesteigert werden.
Tagesdosis im 3. bis 4. Lebensjahr
Die maximale Tagesdosis beträgt 40 ml/kg Körpergewicht entsprechend:
1,54 g Aminosäuren/kg Körpergewicht und Tag
4,8 g Glucose /kg Körpergewicht und Tag
1,6 g Fett /kg Körpergewicht und Tag.
Tagesdosis im 5. bis 13. Lebensjahr
Die maximale Tagesdosis beträgt 25 ml/kg Körpergewicht entsprechend:
0,96 g Aminosäuren /kg Körpergewicht und Tag
3,0 g Glucose /kg Körpergewicht und Tag
1,0 g Fett /kg Körpergewicht und Tag.
Die maximale Infusionsgeschwindigkeit beträgt 2,0 ml/kg KG und Stunde entsprechend:
0,08 g Aminosäuren /kg KG und Stunde,
0,24 g Glucose /kg KG und Stunde,
0,08 g Fett /kg KG und Stunde.
Infolge des unterschiedlichen individuellen Bedarfs von Kindern und Jugendlichen reicht die Gabe von Omegaflex plus bei manchen Patienten nicht aus, um den gesamten Energie- und Flüssigkeitsbedarf zu decken. In solchen Fällen müssen zusätzlich Kohlenhydrate und/oder Fette und/oder Flüssigkeit in geeigneter Form zugeführt werden.
Therapiedauer
Die Therapiedauer im Rahmen der genannten Indikationen ist nicht begrenzt.
Bei Anwendung von Omegaflex plus ist eine ausreichende Substitution von Spurenelementen und Vitaminen erforderlich.
Art der Anwendung
Intravenöse Anwendung.
Kontraindikationen·Überempfindlichkeit gegen die Wirkstoffe, gegenüber Ei-, Fisch-, Erdnuss oder Sojaprotein oder einen der Hilfsstoffe gemäss Zusammensetzung.
·Angeborene Aminosäurestoffwechselstörungen
·Schwere Hypertriglyzeridämie (≥1000 mg/dl oder 11,4 mmol/l)
·Schwere Gerinnungsstörung
·Hyperglykämie, die nicht auf Insulindosen von bis zu 6 Einheiten Insulin/Stunde anspricht
·Azidose
·Intrahepatische Cholestase
·Schwere Leberinsuffizienz
·Schwere Niereninsuffizienz, wenn keine Dialyseeinrichtungen vorhanden sind
·Verschlimmernde hämorrhagische Diathesen
·Akute thromboembolische Ereignisse, Fettembolie
Auf Grund seiner Zusammensetzung darf Omegaflex plus nicht bei Neugeborenen, Säuglingen und Kleinkindern im Alter von unter 2 Jahren angewendet werden.
Allgemeine Gegenanzeigen einer parenteralen Ernährung sind unter anderem:
·Instabile Kreislaufverhältnisse mit vitaler Bedrohung (Kollaps- und Schockzustände)
·Akute Phasen von Herzinfarkt und Schlaganfall
·Instabile Stoffwechsellage (z. B. schweres Postaggressionssyndrom, Koma unbekannter Ursache)
·Unzureichende zelluläre Sauerstoffversorgung
·Störungen des Elektrolyt- und Flüssigkeitshaushalts
·Akutes Lungenödem
·Dekompensierte Herzinsuffizienz
Warnhinweise und VorsichtsmassnahmenVorsicht ist bei erhöhter Serumosmolarität geboten.
Vor Beginn der Infusion sind Störungen des Flüssigkeits-, Elektrolyt- oder Säure-Basen-Haushalts zu korrigieren.
Eine zu schnelle Infusion kann zu Flüssigkeitsüberladung mit pathologischen Serumelektrolytkonzentrationen, Hyperhydratation und Lungenödem führen.
Jedes Anzeichen oder Symptom einer anaphylaktischen Reaktion (wie Fieber, Schüttelfrost, Hautausschlag oder Dyspnoe) sollte zu einer sofortigen Unterbrechung der Infusion führen.
Während der Infusion von Omegaflex plus ist die Serumtriglyceridkonzentration zu überwachen.
Abhängig von der Stoffwechsellage des Patienten kann gelegentlich eine Hypertriglyzeridämie auftreten. Wenn die Konzentration der Plasmatriglyceride während der Verabreichung von Fett auf mehr als 4,6 mmol/l (400 mg/dl) ansteigt, wird empfohlen, die Infusionsgeschwindigkeit zu reduzieren. Bei weiter ansteigenden Werten muss ein Abbruch der Infusion erwogen werden, da ab 11.4 mmol/l das Risiko einer Pankreatitis ansteigt.
Patienten mit Fettstoffwechselstörungen
Omegaflex plus sollte bei Patienten mit Fettstoffwechselstörungen mit erhöhten Serumtriglyceriden, z.B. Niereninsuffizienz, Diabetes mellitus, Pankreatitis, beeinträchtigter Leberfunktion, Hypothyreose (mit Hypertriglyzeridämie), Sepsis und metabolischem Syndrom (Kombination von Diabetes, hohem Blutdruck und Übergewicht), vorsichtig angewendet werden. Wenn Omegaflex plus an Patienten mit diesen Erkrankungen verabreicht wird, ist eine häufigere Überwachung der Serumtriglyceride notwendig, um die Triglyceridelimination und stabile Triglyceridspiegel unter 4,6 mmol/l (400 mg/dl) sicherzustellen.
Bei kombinierten Hyperlipidämien und beim metabolischen Syndrom reagieren die Triglyceridwerte auf Glucose, Fette und Überernährung. Die Dosis ist in diesen Fällen entsprechend anzupassen. Andere Fett- und Glucosequellen sowie Drogen und Arzneimittel, die den Stoffwechsel des Patienten beeinträchtigen, müssen bestimmt und überwacht werden.
Das Auftreten einer Hypertriglyzeridämie 12 Stunden nach Verabreichung von Lipiden ist ebenfalls ein Hinweis auf eine Fettstoffwechselstörung.
Wie bei allen kohlenhydrathaltigen Lösungen kann die Verabreichung von Omegaflex plus zu einer Hyperglykämie führen. Kontrollen des Blutzuckerspiegels sind daher erforderlich. Bei einem Blutzuckeranstieg ist die Infusionsgeschwindigkeit zu vermindern oder Insulin zu verabreichen. Erhält der Patient gleichzeitig andere intravenöse Glucoselösungen, muss die Menge der zusätzlich verabreichten Glucose berücksichtigt werden.
Eine Unterbrechung der Anwendung ist ebenfalls angezeigt, wenn der Blutzuckerspiegel während der Verabreichung auf über 14 mmol/l (250 mg/dl) steigt.
Das sogenannte Refeeding-Syndrom oder die Repletion von mangel- oder unterernährten Patienten kann eine Hypokaliämie, Hypophosphatämie und Hypomagnesiämie verursachen. Eine engmaschige Überwachung der Serumelektrolyte ist unbedingt erforderlich. Bei Abweichung der Elektrolyt-Konzentrationen von den Normwerten ist eine entsprechende Supplementierung erforderlich.
Kontrollen der Serumelektrolytwerte, des Wasserhaushalts, des Säuren-Basen-Gleichgewichts, des Blutbilds, des Gerinnungsstatus und der Leberfunktion sind notwendig.
Eine dem Bedarf entsprechende Substitution von Elektrolyten, Vitaminen und Spurenelementen ist eventuell erforderlich. Da Omegaflex plus Zink, Magnesium, Calcium und Phosphat enthält, ist bei gleichzeitiger Verabreichung von Lösungen, die diese Elemente ebenfalls enthalten, Vorsicht geboten.
Omegaflex plus ist ein komplex zusammengesetztes Präparat. Es wird daher grundsätzlich von der Zugabe anderer Lösungen abgeraten (sofern deren Kompatibilität nicht nachgewiesen ist – siehe “Sonstige Hinweise”).
Omegaflex plus sollte wegen der Gefahr einer Pseudoagglutination nicht zusammen mit Blut über das selbe Infusionssystem verabreicht werden.
Wie bei allen Lösungen zur intravenösen Anwendung, insbesondere Lösungen zur parenteralen Ernährung, sind bei der Infusion von Omegaflex plus streng aseptische Bedingungen einzuhalten.
Ältere Patienten
Die Dosierungen sind grundsätzlich dieselben wie bei Erwachsenen, jedoch ist bei Patienten mit anderen Erkrankungen wie Herz- oder Niereninsuffizienz, die häufig mit fortgeschrittenem Alter einhergehen, Vorsicht geboten.
Patienten mit Diabetes mellitus, beeinträchtigter Herz- oder Nierenfunktion
Wie alle grossvolumigen Infusionslösungen sollte Omegaflex plus bei Patienten mit eingeschränkter Herz- oder Nierenfunktion mit Vorsicht angewendet werden.
Es liegen nur begrenzte Erfahrungen zur Anwendung bei Patienten mit Diabetes mellitus oder Nierenversagen vor.
InteraktionenEinige Arzneimittel wie z.B. Insulin können das Lipasesystem des Körpers beeinflussen. Diese Wechselwirkung ist jedoch nur von untergeordneter klinischer Bedeutung.
Heparin verursacht in therapeutischen Dosen eine vorübergehende Freisetzung von Lipoproteinlipase in den Blutkreislauf. Dies kann anfänglich zu einer erhöhten Plasmalipolyse führen, gefolgt von einer vorübergehenden Senkung der Triglyceridclearance.
Sojaöl enthält von Natur aus Vitamin K1. Dies kann die therapeutische Wirkung von Cumarinderivaten beeinträchtigen. Daher sind Patienten, die mit diesen Arzneimitteln behandelt werden, sorgfältig zu überwachen.
Kaliumhaltige Lösungen wie Omegaflex plus sollten mit Vorsicht bei Patienten angewendet werden, die Arzneimittel erhalten, welche die Kaliumkonzentration erhöhen; wie z.B. kaliumsparende Diuretika (z.B. Amilorid, Spironolacton, Triamteren), ACE-Hemmern (Enalapril, Captopril), Angiotensin II-Rezeptor-Antagonisten (Losartan, Valsartan), Ciclosporin und Tacrolismus.
Die Gabe von Corticosteroiden und ACTH ist mit Flüssigkeits- und Natriumretention verbunden.
Die Wirksamkeit der Herzglykoside kann durch das in der Lösung enthaltene Kalium vermindert werden.
Schwangerschaft, StillzeitSchwangerschaft
Es liegen keine oder nur sehr begrenzte Erfahrungen mit der Anwendung von Omegaflex plus bei Schwangeren vor. Tierexperimentelle Studien sind ungenügend für die Beurteilung der Reproduktionstoxizität (siehe “Präklinische Daten”).
Während der Schwangerschaft kann eine parenterale Ernährung notwendig werden. Omegaflex plus sollte bei schwangeren Frauen nur nach sorgfältiger Abwägung angewendet werden.
Stillzeit
Bestandteile/Metabolite von Omegaflex plus werden in die Muttermilch ausgeschieden, doch sind bei therapeutischer Dosierung keine Auswirkungen auf das (den) gestillte (n) Neugeborene/Säugling zu erwarten. Dennoch wird nicht empfohlen, dass Mutter Ihr Kind stillen, wenn sie eine parenterale Ernährung erhalten.
Fertilität
Es liegen keine Daten zur Anwendung von Omegaflex plus vor.
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von MaschinenNicht zutreffend.
Unerwünschte WirkungenMögliche Frühreaktionen bei Applikation von Fettemulsionen sind: geringer Temperaturanstieg, Hitzegefühl, Kältegefühl, Schüttelfrost, Appetitlosigkeit, Übelkeit, Erbrechen, Atemnot, Kopf-, Rücken-, Knochen-, Brust- und Lendenschmerzen, Blutdruckabfall oder -anstieg (Hypotonie, Hypertonie), Überempfindlichkeitsreaktionen (z.B. anaphylaktoide Reaktionen, Hautausschlag).
Die unerwünschten Wirkungen sind nach MedDRA-Systemorganklassen und Häufigkeit gemäss folgender Konvention geordnet:
„sehr häufig“ (≥1/10)
„häufig“ (≥1/100, <1/10),
„gelegentlich“ (≥1/1‘000, <1/100)
„selten“ (≥1/10‘000, <1/1‘000)
„sehr selten“ (<1/10‘000)
„nicht bekannt“ (kann aus den verfügbaren Daten nicht abgeschätzt werden)
Die folgende Auflistung enthält eine Reihe systemischer Reaktionen, die im Zusammenhang mit der Anwendung von Omegaflex plus stehen können. Bei sachgemässer Anwendung, Einhaltung der Dosierung und Beachtung der Sicherheitsauflagen und -Vorschriften treten diese meistens selten auf (≥ 1/10’000 bis < 1/1’000).
Erkrankungen des Blut- und Lymphsystems
Selten Hyperkoagulation.
Nicht bekannt Leukopenie, Thrombocytopenie.
Stoffwechsel- und Ernährungsstörungen
Sehr selten Hyperlipämie, Hyperglykämie, metabolische Azidose. Die Häufigkeit dieser unerwünschten Wirkungen ist dosisabhängig und kann bei absoluter oder relativer Fettüberdosierung erhöht sein.
Erkrankungen des Nervensystems
Selten Kopfschmerzen, Schläfrigkeit.
Gefässerkrankungen
Selten Hypertonie oder Hypotonie, Hautrötungen (Flush)
Erkrankungen der Atemwege, des Brustraums und Mediastinums
Selten Dyspnoe, Zyanose.
Gastrointestinale Störungen
Gelegentlich Übelkeit, Erbrechen, Appetitlosigkeit
Leber- und Gallenerkrankungen
Nicht bekannt Cholestase.
Erkrankungen der Haut und des Unterhautzellgewebes
Selten Erythem, Schwitzen
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen
Selten Schmerzen in Rücken, Knochen, Brustkorb und Lumbalbereich
Allgemeine Störungen und Beschwerden am Verabreichungsort
Selten erhöhte Körpertemperatur, Kältegefühl, Schüttelfrost.
Sehr selten Fettüberladungssyndrom (siehe Beschreibung unten)
Bei Auftreten von Nebenwirkungen muss die Infusion beendet werden.
Bei Werten über 4,6 mmol/l (400 mg/dl) muss die Infusion mit einer reduzierten Dosierung fortgesetzt werden. Bei weiter ansteigenden Werten muss ein Abbruch der Infusion erwogen werden, da ab 11.4 mmol/l das Risiko einer Pankreatitis ansteigt.
Wenn die Infusion wiederaufgenommen wird, sollte der Patient besonders zu Beginn sorgfältig überwacht werden und die Serumtriglyceride sollten in kurzen Zeitabständen bestimmt werden.
Beschreibung spezifischer unerwünschter Wirkungen und Zusatzinformationen
Übelkeit, Erbrechen und Appetitlosigkeit sind Symptome, die oft mit Erkrankungen in Zusammenhang stehen, bei denen eine parenterale Ernährung durchgeführt wird, und können gleichzeitig mit der parenteralen Ernährung assoziiert sein.
Fettüberladungssyndrom
Bei Überdosierung kann die eingeschränkte Fähigkeit, Triglyceride abzubauen, zum Auftreten eines Fettüberladungssyndroms führen. Mögliche Anzeichen einer Stoffwechselüberlastung müssen beachtet werden. Die Ursache kann genetisch bedingt (individuell unterschiedlicher Metabolismus) oder die Folge einer Beeinträchtigung des Fettstoffwechsels durch andere gleichzeitige oder vorausgegangene Erkrankungen sein. Ein solches Syndrom kann selbst bei Einhaltung der empfohlenen Infusionsgeschwindigkeit bei schwerer Hypertriglyceridämie auftreten, oder durch eine plötzliche Veränderung des klinischen Zustandes des Patienten, wie z.B. bei Niereninsuffizienz oder Infektion, ausgelöst werden. Ein Fettüberlastungssyndrom ist durch folgende Symptome charakterisiert: Hyperlipidämie, Fieber, Fettinfiltration, Hepatomegalie mit oder ohne Ikterus, Splenomegalie, Anämie, Leukopenie, Thrombozytopenie, Gerinnungsstörungen, Hämolyse und Retikulozytose, anormale Leberfunktionswerte und Koma.
Die Symptome sind in der Regel nach Absetzen der Infusion der Fettemulsion reversibel.
Bei Anzeichen eines Fettüberladungssyndroms ist die Infusion von Omegaflex plus sofort zu beenden.
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von grosser Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdacht einer neuen oder schwerwiegenden Nebenwirkung über das Online-Portal ElViS (Electronic Vigilance System) anzuzeigen. Informationen dazu finden Sie unter www.swissmedic.ch.
ÜberdosierungAnzeichen und Symptome
Flüssigkeits- und Elektrolytüberdosierung:
Hyperhydration, Störungen des Elektrolythaushalts und Lungenödem.
Aminosäurenüberdosierung:
Renaler Aminosäurenverlust mit nachfolgenden Störungen des Aminosäurenhaushalts, Übelkeit, Erbrechen und Schüttelfrost.
Glucoseüberdosierung:
Hyperglykämie, Glucosurie, Dehydration, Hyperosmolarität, hyperglykämischhyperosmolares Koma.
Fettüberdosierung:
Siehe “Unerwünschte Wirkungen”.
Behandlung
Bei einer Überdosierung muss die Infusion sofort beendet werden. Weitere Therapeutische Massnahmen hängen von den jeweiligen Symptomen und deren Schweregrad ab. Bei Wiederaufnahme der Infusion nach Abklingen der Symptome wird empfohlen, die Infusionsrate unter häufiger Überwachung langsam zu erhöhen.
Eigenschaften/WirkungenATC-Code
B05BA10
Lösungen zur parenteralen Ernährung, Kombinationen.
Wirkungsmechanismus
Eine parenterale Ernährung dient zur Zufuhr aller notwendigen Nährstoffe für das Wachstum bzw. für die Regeneration von Geweben, als auch Energie zur Aufrechterhaltung aller Körperfunktionen zu liefern.
Fette sind aufgrund ihrer hohen Energiedichte effiziente Energielieferanten. Langkettige Triglyceride versorgen den Organismus mit essenziellen Fettsäuren für die Synthese von Zellbestandteilen. Für diese Zwecke enthält die Fettemulsion mittelkettige und langkettige Triglyceride (aus Sojaöl und Fischöl).
Der Anteil der langkettigen Triglyceride enthält Omega-6 und Omega-3-Triglyceride zur Bereitstellung von mehrfach ungesättigten Fettsäuren. Primär dienen diese der Prävention und Behandlung eines Mangels an essenziellen Fettsäuren und zusätzlich auch als Energielieferant.
Omegaflex plus enthält essentielle Omega-6 Fettsäuren, hauptsächlich in Form von Linolsäure, und Omega-3 Fettsäuren in Form von alpha-Linolensäure, Eicosapentaensäure und Docosahexaensäure. Das Verhältnis von Omega-6 zu Omega-3 Fettsäuren in Omegaflex plus beträgt etwa 2,5:1.
Pharmakodynamik
Keine Angaben
Klinische Wirksamkeit
Keine Angaben
PharmakokinetikAbsorption
Omegaflex plus wird intravenös infundiert. Somit sind alle Substrate für den Metabolismus sofort bioverfügbar.
Distribution
Die Dosis, Infusionsgeschwindigkeit, Stoffwechselsituation und individuelle Faktoren des Patienten (letzte Nahrungsaufnahme) bestimmen die maximal erreichten Triglyceridspiegel entscheidend. Bei bestimmungsgemässem Anwendung und Einhaltung der Dosierungsrichtlinien überschreiten die Triglyceridspiegel im Allgemeinen 4,6 mmol/l (400 mg/dl) nicht.
Mittelkettige Fettsäuren weisen eine geringe Affinität zu Albumin auf.
Es liegen keine Daten zum Transport der Bestandteile durch die Plazenta vor.
Metabolismus
Keine Angaben
Elimination
Sowohl Triglyceride aus Sojaöl als auch die mittelkettige Triglyceride werden vollständig zu CO2 und H2O abgebaut.
Eine renale Ausscheidung existiert praktisch nicht.
Präklinische DatenPräklinische Studien wurden mit Omegaflex plus nicht durchgeführt.
Bei Nährstoffmischungen, die zur Substitutionstherapie in der empfohlenen Dosierung verabreicht werden, sind keine toxischen Wirkungen zu erwarten.
Reproduktionstoxizität
In verschiedenen Pflanzenölen, besonders in Sojaöl, können Phytoöstrogene wie ß-Sitosterol enthalten sein. Bei subkutaner und intravaginaler Verabreichung von ß-Sitosterin wurde bei Ratten und Kaninchen eine Beeinträchtigung der Fertilität beobachtet. Nach Verabreichung von reinem ß-Sitosterol wurde eine Abnahme des Hodengewichts und eine Reduktion der Spermienkonzentration bei männlichen Ratten sowie eine geringere Schwangerschaftsrate bei weiblichen Kaninchen festgestellt. Nach dem gegenwärtigen Erkenntnisstand scheinen die bei Tieren beobachteten Wirkungen jedoch keine Relevanz für die klinische Anwendung zu haben.
Sonstige HinweiseInkompatibilitäten
Omegaflex plus ist ein komplex zusammengesetztes Präparat. Es wird daher grundsätzlich von der Zugabe von Zusätzen abgeraten. Es sind verschiedene Mischungen mit Zusätzen (z.B. Spurenelemente, Elektrolyte) unter bestimmten Bedingungen geprüft worden. Genauere Angaben dazu sind beim Hersteller zu erfragen.
Beeinflussung diagnostischer Methoden
Der Fettgehalt kann bestimmte Laborwertmessungen beeinflussen (z. B. Bilirubin, Lactatdehydrogenase, Sauerstoffsättigung), wenn Blutproben entnommen werden, bevor das Fett ausreichend aus dem Blut beseitigt wurde.
Haltbarkeit
Omegaflex plus darf nur bis zu dem auf dem Behälter mit “Exp” bezeichneten Verfalldatum verwendet werden.
Haltbarkeit nach Anbruch
Nach Entfernen der Schutzhülle und Mischen des Beutelinhalts
Die Stabilität der gebrauchsfertigen Mischung von Aminosäuren, Glucose und Fett wurde über 7 Tage bei 2-8 °C und zusätzliche 2 Tage bei 25 °C geprüft und nachgewiesen.
Nach Beimischung von kompatiblen Zusatzstoffen:
Aus mikrobiologischer Sicht sollte das Produkt nach Beimischung von Zusatzstoffen sofort verwendet werden. Wenn es nicht sofort nach der Beimischung von Zusatzstoffen verwendet wird, liegen die Aufbewahrungszeiten und –Bedingungen vor der Anwendung in der Verantwortung des Anwenders.
Nach Anbruch des Behältnisses (Durchstechen des Infusionsports)
Nach Anbruch des Behältnisses muss die Emulsion sofort verwendet werden.
Besondere Lagerungshinweise
Nicht über 25 °C lagern. Nicht einfrieren. Den Behälter im Umkarton aufbewahren, um den Inhalt vor Licht zu schützen.
Hinweise für die Handhabung
Keine besonderen Anforderungen für die Beseitigung.
Produkte für die parenterale Ernährung sollten vor der Anwendung visuell auf Beschädigung, Verfärbung und Instabilität der Emulsion geprüft werden.
Nur unbeschädigte Beutel verwenden; weder Schutzhülle noch Innenbeutel dürfen beschädigt sein. Nur verwenden, wenn die Peelnähte zwischen den Kammern intakt sind, die Aminosäuren- und Glucoselösungen klar und farblos bis schwach gelblich sind und die Emulsion eine milchig-weisse homogene Flüssigkeit ist. Nicht verwenden, wenn die Lösungen verfärbt sind oder Partikel enthalten.
Nicht verwenden, wenn die Emulsion Anzeichen einer Phasentrennung (Öltropfen, Ölschicht) aufweist.
Vor Öffnen der Schutzhülle die Farbe des Sauerstoffindikators kontrollieren (siehe Abbildung A):
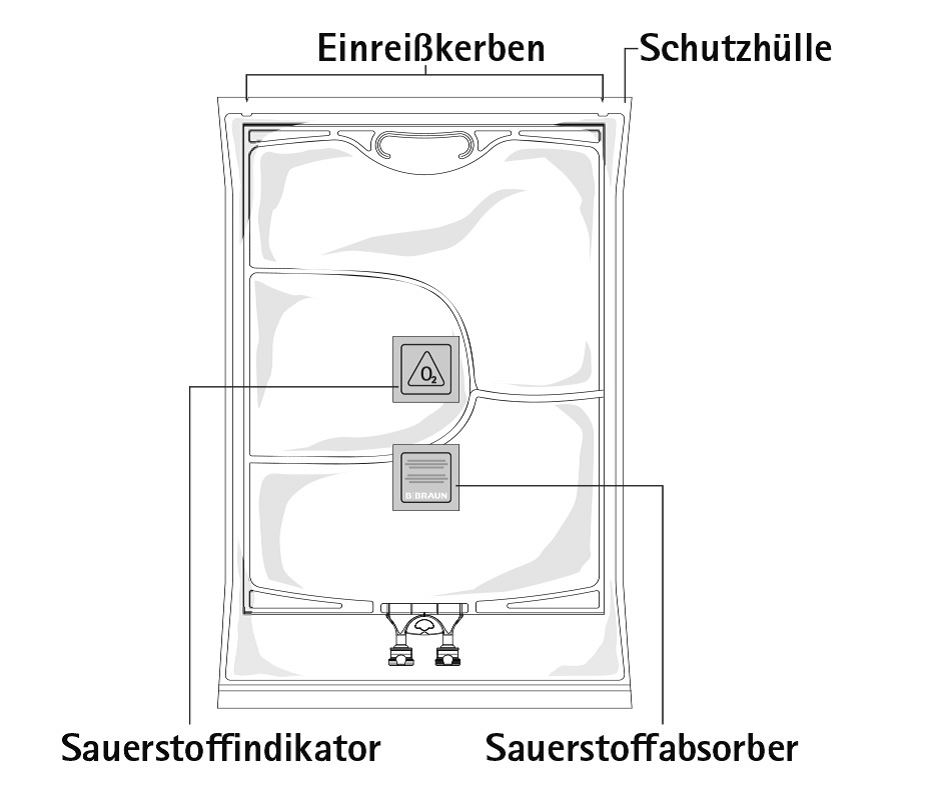
Abb. A
Nicht verwenden, wenn der Sauerstoffindikator rosa gefärbt ist. Nur verwenden, wenn der Sauerstoffindikator gelb gefärbt ist.
Herstellung der Mischemulsion
Die Regeln der aseptischen Handhabung müssen strikt eingehalten werden.
Zum Öffnen: Die Schutzhülle beginnend an den Einreiskerben aufreissen (Abb. 1). Den Beutel aus der Schutzhülle nehmen. Schutzhülle, Sauerstoffindikator und Sauerstoffabsorber verwerfen.
Den Innenbeutel visuell auf Undichtigkeiten prüfen. Undichte Beutel müssen verworfen werden, da die Sterilität nicht gewährleistet werden kann.
Um die Kammern der Reihe nach zu öffnen und ihren Inhalt zu mischen, den Beutel mit beiden Händen aufrollen; dabei mit dem Öffnen der Peelnaht beginnen, welche die obere Kammer (Glucose) und die untere Kammer (Aminosäuren) trennt (Abb. 2a). Danach weiterhin Druck ausüben, so dass sich die Peelnaht, welche die mittlere Kammer (Fette) und die untere Kammer trennt, öffnet (Abb. 2b).
Nach Entfernen des Aluminiumverschlusses (Abb. 3) können über den Medikationsport kompatible Zusatzstoffe hinzugefügt werden (Abb. 4).
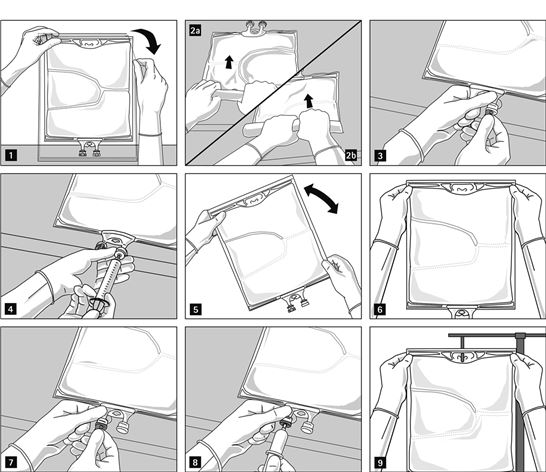
Den Inhalt des Beutels gründlich mischen (Abb. 5) und die Mischung visuell prüfen (Abb. 6). Es dürfen keine Anzeichen einer Phasentrennung der Emulsion erkennbar sein.
Die Mischung ist eine milchig-weisse homogene Öl-in-Wasser-Emulsion.
Vorbereitung zur Infusion
Die Emulsion sollte vor der Infusion stets auf Raumtemperatur gebracht werden.
Die Aluminiumfolie vom Infusionsport entfernen (Abb. 7) und das Infusionsbesteck befestigen (Abb. 8). Ein unbelüftetes Infusionsbesteck verwenden oder bei Verwendung eines belüfteten Infusionsbestecks das Entlüftungsventil schliessen. Den Beutel an einen Infusionsständer hängen (Abb. 9) und die Infusion entsprechend der Standardtechnik durchführen.
Nur zum Einmalgebrauch bestimmt. Das Behältnis und nicht verbrauchte Reste müssen nach der Verwendung verworfen werden.
Teilweise verbrauchte Behältnisse nicht wieder an ein Infusionssystem anschliessen.
Wenn Filter verwendet werden, müssen diese lipiddurchlässig sein (Porengrösse ≥ 1,2 μm).
Zulassungsnummer65816 (Swissmedic)
PackungenOmegaflex plus wird in flexiblen Mehrkammer-Polypropylenbeuteln geliefert:
5 x 1250 ml (B)
5 x 1875 ml (B)
ZulassungsinhaberinB. Braun Medical AG, Sempach
Stand der InformationJanuar 2023
|


