Eigenschaften/WirkungenATC-Code C03DA04
Wirkungsmechanismus
Siehe «Pharmakodynamik».
Pharmakodynamik
Eplerenon bindet relativ selektiv an rekombinante menschliche Mineralokortikoid- Rezeptoren verglichen mit seiner Bindungsaffinität zu rekombinanten menschlichen Glukokortikoid-, Progesteron- und Androgen-Rezeptoren. Eplerenon verhindert die Bindung von Aldosteron.
Klinische Wirksamkeit
Eplerenon wurde in der Eplerenone post-acute myocardial infarction heart failure efficacy and survival study (EPHESUS) untersucht. EPHESUS war eine doppelblinde, placebokontrollierte Multizenter-Studie an n=6632 Patienten (mittleres Follow-up 16 Monate) mit akutem Myokardinfarkt, linksventrikulärer Dysfunktion (gemessen als linksventrikuläre Ejektionsfraktion [LVEF] <40%), und klinischen Anzeichen einer Herzinsuffizienz. Die Patienten wurden 3 bis 14 Tage nach der Diagnose Myokardinfarkt randomisiert in die EPHESUS Studie aufgenommen. Die durchschnittliche Dauer bis zur Aufnahme betrug 7 Tage. Aufgrund des erhöhten kardiovaskulären Risikos assoziiert mit Diabetes, wurden Patienten mit Diabetes und einer linksventrikulären Dysfunktion in Abwesenheit von Symptomen einer Herzinsuffizienz in die Studie aufgenommen; 10% der Studienpopulation entsprachen diesem Kriterium. Zusätzlich zur Standardtherapie erhielten die Patienten entweder Eplerenon oder Placebo in einer Initialdosierung von 25 mg einmal täglich mit anschliessender Erhöhung auf die Erhaltungsdosis von 50 mg einmal täglich innerhalb von 4 Wochen bei Serumkaliumwerten <5.0 mEq/l. Während der Studie erhielten die Patienten zusätzlich eine Standardtherapie, bestehend aus Aspirin (92%), ACE-Inhibitor (90%), Betablockern (83%), Nitraten (72%), Schleifendiuretika (66%) oder HMG-CoA-Reduktase Inhibitoren (60%).
In der EPHESUS-Studie waren die co-primären Endpunkte Gesamtmortalität und der kombinierte Endpunkt aus kardiovaskulärer Mortalität oder kardiovaskulärer Hospitalisierung. Unter Eplerenon verstarben 14.4% der Patienten und unter Placebo 16.7% (alle Ursachen), während 26.7% der Patienten mit Eplerenon und 30.0% unter Placebo den kombinierten Studienendpunkt aus kardiovaskulärer Mortalität oder kardiovaskulärer Hospitalisierung erfüllten. Somit verringerte Eplerenon in der EPHESUS-Studie im Vergleich zu Placebo das Risiko der Gesamtsterblichkeit um 15% (absolute Risikoreduktion 2.3%, RR 0.85; 95% Konfidenzintervall, 0.75–0.96; p=0.008; NNT: 43), hauptsächlich durch die Reduktion der kardiovaskulären Mortalität. Das Risiko eines kardiovaskulären Todes bzw. einer kardiovaskulären Hospitalisierung wurde durch Eplerenon um 13% verringert (absolute Risikoreduktion 3.3%; RR 0.87; 95% Konfidenzintervall, 0.79–0.95; p=0.002; NNT: 31).
Die klinische Wirksamkeit einer Behandlung mit Eplerenon zeigte sich bei Patienten <75 Jahren. Der therapeutische Nutzen bei Patienten ≥75 Jahren ist unklar. Bei einem signifikant grösseren Anteil der mit Eplerenon behandelten Patienten (n=2372 Patienten, 75.3%) verbesserte sich verglichen mit Placebo (n=2242 Patienten, 71.3%) die NYHA-Klassifikation oder blieb unverändert (p<0.001).
Abbildung 1: Hazard Ratios aller Todesursachen geordnet nach Subgruppen
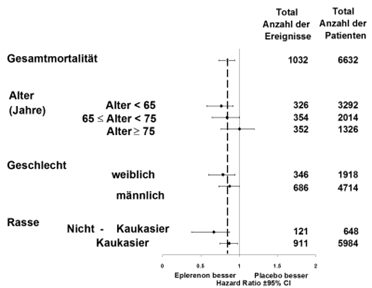



In Studie EMPHASIS-HF (Eplerenone in Mild Patients Hospitalization and Survival Study in Heart Failure) wurde Eplerenon zusätzlich zu einer Standardtherapie bei Patienten mit systolischer Herzinsuffizienz und milden Symptomen (NYHA-Funktionsklasse II) untersucht. Patienten der NYHA-Funktionsklassen- III und IV wurden in der Studie nicht untersucht.
In die Studie aufgenommen wurden Patienten im Alter von ≥55 Jahren mit einer linksventrikulären Ejektionsfraktion (LVEF) von ≤30% oder einer LVEF ≤35% und zusätzlich einer QRS-Dauer von >130 msec. Zusätzlich mussten die Studienteilnehmer entweder innerhalb der vorangegangenen 6 Monate aufgrund einer kardiovaskulären (KV) Ursache hospitalisiert worden sein oder einen BNP-Plasmaspiegel ≥250 pg/ml oder einen Pro-BNP-Spiegel von ≥500 pg/ml (Männer) bzw. ≥750 pg/ml (Frauen) aufweisen. Die Behandlung mit Eplerenon wurde mit einer Dosis von 25 mg einmal täglich begonnen, welche nach 4 Wochen auf 50 mg einmal täglich erhöht wurde, sofern die Serumkaliumwerte bei <5.0 mmol/l und die eGFR bei ≥50 ml/min lagen. Alternativ wurde, wenn die geschätzte glomeruläre Filtrationsrate bei 30-49 ml/min/1.73 m2 lag, die Behandlung mit Eplerenon mit einer Dosis von 25 mg jeden 2. Tag begonnen, welche auf 25 mg einmal täglich erhöht werden konnte.
Die häufigsten kardiovaskulären Begleitmedikationen zusätzlich zu Eplerenon oder Plazebo bei den insgesamt n=2737 Studienteilnehmern waren Diuretika (85%), ACE-Inhibitor (78%), Angiotensin-II-Rezeptor-Antagonisten (19%), Betablocker (87%), antithrombotisch wirksame Arzneimittel (88%), Lipidsenker (63%) und Digitalisalkaloide (27%). Die mittlere LVEF betrug 26% und die mittlere QRS-Dauer lag bei 122 msec. Die meisten Patienten (83.4%) waren innerhalb der letzten 6 Monate vor der Randomisierung aufgrund kardiovaskulärer Ursachen hospitalisiert worden, ca. 50% wegen Herzinsuffizienz. Etwa 20% der Patienten hatten implantierbare Defibrillatoren oder eine kardiale Resynchronisationsbehandlung.
Der primäre Endpunkt (kardiovaskuläre Todesfälle oder Hospitalisierung wegen Herzinsuffizienz) ereignete sich bei n=249 Patienten (18.3%) der Eplerenon-Gruppe und n=356 (25.9%) der Placebo-Gruppe (RR 0.63, 95% CI, 0.54-0.74; p<0.001). Das Ergebnis war in allen untersuchten Subgruppen konsistent.
Der sekundäre Endpunkt Gesamtmortalität ereignete sich bei n=171 Patienten (12.5%) der Eplerenon-Gruppe und n=213 Patienten (15.5%) der Placebo-Gruppe (RR 0.76; 95% CI, 0.62-0.93; p=0.008). Kardiovaskuläre Todesfälle wurden bei n=147 (10.8%) Patienten der Eplerenon-Gruppe und bei n=185 (13.5%) der Placebo-Gruppe berichtet (RR 0.76; 95% CI, 0.61-0.94; p=0.01).
Während der Studie wurde bei n=158 Patienten (11.8%) der Eplerenon-Gruppe und bei n=96 Patienten (7.2%) der Placebo-Gruppe über Hyperkaliämie (Serumkaliumwerte >5.5 mmol/l) berichtet (p<0.001). Eine Hypokaliämie, definiert als Serumkaliumwerte <4.0 mmol/l, ereignete sich seltener mit Eplerenon als mit Placebo (38.9% mit Eplerenon im Vergleich zu 48.4% mit Placebo, p<0.0001).
| 



