Eigenschaften/WirkungenATC-Code
A10AE
Wirkungsmechanismus
Suliqua
Suliqua kombiniert zwei blutzuckersenkende Wirkstoffe mit einander ergänzenden Wirkmechanismen: Insulin glargin, ein Basalinsulinanalogon (wirkt insbesondere auf den Nüchternplasmaglukose- [NPG-]Wert), und Lixisenatid, ein GLP-1-Rezeptoragonist (wirkt insbesondere auf die postprandialen Plasmaglukosewerte [PPG]). So wird bei Patienten mit Diabetes mellitus Typ 2 gleichzeitig die Verbesserung der Blutzuckerkontrolle und die Minimierung der Gewichtszunahme und des Hypoglykämierisikos angestrebt.
Insulin glargin
Die Hauptwirkung von Insulin, einschliesslich Insulin glargin, ist die Regulierung des Glukosestoffwechsels. Insulin und seine Analoga senken den Blutzuckerspiegel durch eine Stimulierung der peripheren Glukoseaufnahme, insbesondere durch die Skelettmuskulatur und das Fettgewebe, sowie durch eine Hemmung der Glukoneogenese in der Leber. Insulin hemmt die Lipolyse und die Proteolyse und fördert die Proteinsynthese.
Lixisenatid
Lixisenatid ist ein selektiver GLP-1-Rezeptor-Agonist. Der GLP-1-Rezeptor ist der Zielrezeptor für natives GLP-1, ein endogenes Inkretinhormon, das glukoseabhängig die Insulinsekretion von pankreatischen Betazellen steigert.
Die Wirkung von Lixisenatid wird durch eine spezifische Interaktion mit GLP-1-Rezeptoren vermittelt, was zu einer Zunahme der Bildung von intrazellulärem zyklischem Adenosinmonophosphat (cAMP) führt. Lixisenatid stimuliert die Insulinsekretion bei hohem Blutzuckerspiegel, jedoch nicht bei Normoglykämie. Auf diese Weise wird das Hypoglykämierisiko begrenzt. Gleichzeitig wird die Sekretion von Glukagon unterdrückt. Im Falle einer Hypoglykämie bleibt der Mechanismus der Gegenregulation, die Glukagonsekretion, erhalten.
Lixisenatid verzögert die Entleerung des Magens, sodass die mit der Nahrung aufgenommene Glukose langsamer in den Blutkreislauf gelangt. Diese Wirkung auf die Magenentleerung könnte auch zu einem Gewichtsverlust beitragen.
Pharmakodynamik
Suliqua
Die Kombination von Insulin glargin und Lixisenatid hat keinen Einfluss auf die pharmakodynamische Wirkung von Insulin glargin. Der Einfluss der Kombination von Insulin glargin und Lixisenatid auf die Pharmakodynamik von Lixisenatid wurde nicht in Phase-I-Studien untersucht.
Übereinstimmend mit einem relativ konstanten Konzentrations-Zeit-Profil über 24 Stunden ohne ausgeprägten Peak bei Gabe von Insulin glargin allein war das Glukoseutilisations-Zeit-Profil bei Gabe der Kombination von Insulin glargin und Lixisenatid ähnlich, ohne ausgeprägten Peak.
Die Resorptionsgeschwindigkeit von Insulinen, einschliesslich Suliqua, kann inter- und auch intraindividuell variieren.
Insulin glargin
In klinischen Studien zu Insulin glargin (100 Einheiten/ml) zeigte intravenös appliziertes Insulin glargin einen mit Humaninsulin vergleichbaren blutzuckersenkenden Effekt auf molarer Basis, d.h. wenn beide Insuline in gleicher Dosis gegeben wurden.
Lixisenatid
In einer 28-tägigen placebokontrollierten Studie bei Patienten mit Typ-2-Diabetes wurde die Wirkung von 5–20 µg Lixisenatid ein- oder zweimal täglich auf den Glykämieverlauf nach einer standardisierten Testmahlzeit zur Frühstückszeit untersucht. Lixisenatid in einer Dosierung von 10 oder 20 µg ein- oder zweimal täglich bewirkte eine bessere Blutzuckereinstellung mit sowohl postprandial als auch nüchtern niedrigerem Blutzuckerspiegel. In dieser Studie bewirkte Lixisenatid in der morgendlichen Dosierung von 20 µg einmal täglich eine Aufrechterhaltung der statistisch signifikanten Reduktion des postprandialen Blutzuckerspiegels nach dem Frühstück, Mittagessen und Abendessen.
Postprandiale Glukose
In einer Studie bei Typ-2-Diabetikern zur Beurteilung von Lixisenatid in Kombination mit Metformin über 4 Wochen und in Kombination mit Insulin glargin und zum Teil zusätzlich noch mit Metformin über 8 Wochen bewirkte eine Dosis von 20 µg Lixisenatid einmal täglich vor einer Testmahlzeit zum Frühstück eine Senkung der postprandialen Plasmaglukose (AUC 0:30–4:30 h). Der Anteil der Patienten mit einem postprandialen Blutzuckerspiegel unterhalb von 7,77 mmol/l betrug nach 28 Tagen 69,3 % und nach 56 Tagen 76,1 %.
Insulinsekretion
Eine Studie zu Lixisenatid als Monotherapie belegt, dass das Arzneimittel allein im Vergleich zu Placebo laut Messung der AUC bei Typ-2-Diabetikern die erste Phase der Insulinsekretion in glukoseabhängiger Weise um den Faktor 2,8 erhöht (90 %-KI: 2,5–3,1) und die Insulinsekretion der zweiten Phase um den Faktor 1,6 (90 %-KI: 1,4–1,7).
Magenentleerung
Nach einer standardisierten Testmahlzeit verzögert Lixisenatid die Magenentleerung und reduziert dadurch die postprandiale Glukoseresorption. Die verzögernde Wirkung auf die Magenentleerung wird über die gesamte Dauer einer 28-tägigen Lixisenatid-Monotherapie bei Typ-2-Diabetikern aufrechterhalten.
Glukagonsekretion
Für Lixisenatid allein wurde nach Verabreichung von 20 µg einmal täglich ein Rückgang des postprandialen Glukagonwerts bei Typ-2-Diabetikern nach einer Testmahlzeit im Vergleich zum Behandlungsbeginn nachgewiesen. Bei gesunden Probanden wurde mit einem hypoglykämischen Clamp-Test die Wirkung einer einmaligen Injektion von 20 µg Lixisenatid auf die Glukagonreaktion im Vergleich zu Placebo untersucht und festgestellt, dass die Gegenregulation mit Glukagon unter hypoglykämischen Bedingungen bei Vorliegen einer wirksamen Lixisenatid-Plasmakonzentration erhalten blieb.
Kardiale Elektrophysiologie (QTc)
Die Auswirkung von Lixisenatid auf die Repolarisation des Herzens wurde in einer QTc-Studie untersucht (mit dem 1,5-fachen der zugelassenen Erhaltungsdosis); die Studie ergab keine Hinweise auf relevante Auswirkungen von Lixisenatid auf die ventrikuläre Repolarisation.
Herzfrequenz
In den placebokontrollierten Phase-III-Studien zu Suliqua wurde keine Steigerung der durchschnittlichen Herzfrequenz festgestellt.
Klinische Wirksamkeit
Die Sicherheit und Wirksamkeit von Suliqua zur Blutzuckerkontrolle wurde in zwei randomisierten klinischen Studien bei Patienten mit Typ-2-Diabetes untersucht:
·Add-on-Therapie zu oralen Antidiabetika (OAD) [insulinnaive Patienten]
·Patienten, die zuvor mit Basalinsulin behandelt wurden
In jeder der wirkstoffkontrollierten Studien erzielte die Behandlung mit Suliqua klinisch und statistisch signifikante Verbesserungen des Hämoglobin-A1c- (HbA1c-)Werts.
Bei Erreichen niedrigerer HbA1c-Spiegel und einer stärkeren HbA1c-Senkung führte die Behandlung mit dem Kombinationsprodukt im Vergleich zu Insulin glargin allein nicht zu verstärkten Hypoglykämien (siehe «Unerwünschte Wirkungen»).
In der klinischen Studie zur Add-on-Therapie zu Metformin wurde die Behandlung mit 10 Dosisschritten begonnen. In der klinischen Studie zur Umstellung von einem Basalinsulin betrug die Anfangsdosis 20 oder 30 Dosisschritte, je nach vorheriger Insulindosis. In beiden Studien wurde die Dosis einmal wöchentlich auf Basis selbst gemessener Nüchternplasmaglukosewerte titriert.
·Add-on-Therapie zu oralen Antidiabetika (OAD) [insulinnaive Patienten]
Klinische Studie bei Patienten mit Typ-2-Diabetes, die mit OAD nicht ausreichend kontrolliert waren
Insgesamt 1170 Patienten mit Typ-2-Diabetes wurden in einer nicht-verblindeten, 30-wöchigen, aktiv kontrollierten Studie randomisiert, um die Wirksamkeit und Sicherheit von Suliqua im Vergleich zu den Einzelkomponenten, Insulin glargin (100 Einheiten/ml) und Lixisenatid, zu untersuchen.
Patienten mit Typ-2-Diabetes, die mit Metformin allein oder mit Metformin und einem zweiten OAD (Sulfonylharnstoff, Glinid, Natrium-Glukose-Cotransporter-2- (SGLT-2-)Inhibitor oder Dipeptidyl-Peptidase-4- (DPP-4-)Inhibitor) behandelt wurden und die mit dieser Behandlung nicht ausreichend kontrolliert waren (HbA1c-Werte zwischen 7,5 % und 10 % bei Patienten, die bisher mit Metformin allein behandelt wurden, und zwischen 7 % und 9 % bei Patienten, die bisher mit Metformin und einem weiteren oralen Antidiabetikum behandelt wurden), durchliefen eine 4-wöchige Run-in-Phase. Während dieser Run-in-Phase wurde die Metformin-Behandlung optimiert und alle anderen OAD abgesetzt. Am Ende der Run-in-Phase wurden Patienten, die noch immer nicht ausreichend kontrolliert waren (HbA1c zwischen 7 % und 10 %) entweder auf Suliqua oder Insulin glargin oder Lixisenatid randomisiert. Insgesamt 58 % der Patienten erhielten zum Zeitpunkt des Screenings ein zweites OAD.
Die Typ-2-Diabetes-Population wies die folgenden Charakteristika auf: Das Durchschnittsalter betrug 58,4 Jahre, 50,6 % der Patienten waren männlich, der durchschnittliche BMI-Ausgangswert betrug 31,7 kg/m2, und die durchschnittliche Diabetesdauer lag bei ca. 9 Jahren.
Nach 30 Wochen zeigte Suliqua eine statistisch signifikante Verbesserung des HbA1c-Werts (p-Wert < 0,0001) im Vergleich zu den Einzelkomponenten. In einer vorab spezifizierten Analyse dieses primären Endpunkts waren die beobachteten Unterschiede im Hinblick auf den HbA1c-Ausgangswert (< 8 % oder ≥8 %) oder die Anwendung von OAD bei Studienbeginn (Metformin allein oder Metformin mit einem zweiten OAD) konsistent.
Zu den weiteren Studienendpunkten siehe nachstehende Tabelle und Abbildung.
Ergebnisse nach 30 Wochen – Klinische Studie zur Add-on-Therapie zu Metformin (mITT-Population)
|
|
Suliqua
|
Insulin glargin
|
Lixisenatid
| |
Anzahl Teilnehmer (mITT)
|
468
|
466
|
233
| |
HbA1c (%)
| |
Ausgangswert (Mittelwert; nach der Run-in-Phase)
|
8,1
|
8,1
|
8,1
| |
Ende der Studie (Mittelwert)
|
6,5
|
6,8
|
7,3
| |
Veränderung zum Ausgangswert (Kleinste-Quadrate-Mittelwert)
|
-1,6
|
-1,3
|
-0,9
| |
Unterschied vs. Insulin glargin
|
-0,3
|
| |
[95 %-Konfidenzintervall]
|
[-0,4; -0,2]
|
| |
(p-Wert)
|
(< 0,0001)
|
| |
Unterschied vs. Lixisenatid
|
|
|
-0,8
| |
[95 %-Konfidenzintervall]
|
|
|
[-0,9; -0,7]
| |
(p-Wert)
|
|
|
(< 0,0001)
| |
Anzahl Patienten (%), die in Woche 30 einen HbA1c-Wert < 7 % erreichten
|
345 (74 %)
|
277 (59 %)
|
77 (33 %)
| |
Nüchternplasmaglukose (mmol/l)
| |
Ausgangswert (Mittelwert)
|
9,88
|
9,75
|
9,79
| |
Ende der Studie (Mittelwert)
|
6,32
|
6,53
|
8,27
| |
Veränderung zum Ausgangswert (Kleinste-Quadrate-Mittelwert)
|
-3,46
|
-3,27
|
-1,50
| |
Veränderung vs. Insulin glargin (Kleinste-Quadrate-Mittelwert)
|
-0,19
|
|
| |
[95 %-Kl]
|
[-0,420 bis
0,038]
|
|
| |
(p-Wert)
|
(0,1017)
|
|
| |
Veränderung vs. Lixisenatid (Kleinste-Quadrate-Mittelwert)
|
-1,96
|
|
| |
[95 %-Kl]
|
[-2,246 bis
-1,682]
|
|
| |
(p-Wert)
|
(< 0,0001)
|
|
|
|
|
Suliqua
|
Insulin glargin
|
Lixisenatid
| |
Anzahl Teilnehmer (mITT)
|
468
|
466
|
233
| |
PPG nach 2 Stunden (mmol/l)
| |
[Glykämieschwankung nach 2 Stunden* (mmol/l)]
| |
Veränderung zum Ausgangswert in Woche 30
|
-5,68
|
-3,31
|
-4,58
| |
(Kleinste-Quadrate-Mittelwert)
|
[-2,31]
|
[-0,18]
|
[-3,23]
| |
Durchschnittliches Körpergewicht (kg)
| |
Ausgangswert (Mittelwert)
|
89,4
|
89,8
|
90,8
| |
Veränderung zum Ausgangswert (Kleinste-Quadrate-Mittelwert)
|
-0,3
|
1,1
|
-2,3
| |
Unterschied vs. Insulin glargin
|
|
-1,4
|
| |
[95 %-Konfidenzintervall]
|
|
[-1,9 bis
-0,9]
|
| |
(p-Wert)
|
|
(< 0,0001)
|
| |
Unterschied vs Lixisenatid
[95 %-Konfidenzintervall]
|
|
|
2,01
[1,4 bis
2,6]
| |
Anzahl an Patienten (%), die in Woche 30 einen HbA1c-Wert < 7,0 % ohne Gewichtszunahme erreichten
|
202
(43,2 %)
|
117
(25,1 %)
|
65
(27,9 %)
| |
Prozentualer Unterschied vs. Insulin glargin
|
|
18,1
|
| |
[95 %-Konfidenzintervall]
|
|
[12,2 bis
24,0]
|
| |
(p-Wert)
|
|
(< 0,0001)
|
| |
Prozentualer Unterschied vs. Lixisenatid
|
|
|
15,2
| |
[95 %-Konfidenzintervall]
|
|
|
[8,1 bis
22,4]
| |
Tagesdosis Insulin glargin
| |
Veränderung der Insulindosis in Woche 30 (Kleinste-Quadrate-Mittelwert)
|
39,8
|
40,5
|
n.z.
|
* PPG (postprandiale Glukose) nach 2 Stunden abzüglich des Glukosewerts vor der Mahlzeit
Mittlerer HbA1c-Wert (%) zu Beginn des Screenings, zum Zeitpunkt der Randomisierung und zu allen weiteren festgelegten Zeitpunkten (Teilnehmer, die die Studie abgeschlossen haben) und in Woche 30 (LOCF*) – mITT-Population
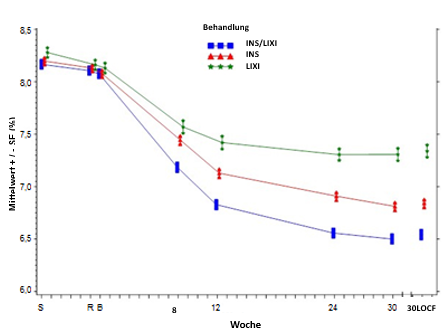
* LOCF = Last Observation Carried Forward (Fortschreibung des letzten gemessenen Werts)
Patienten in der Suliqua-Gruppe zeigten einen statistisch signifikanten Rückgang
in dem durch Plasmaglukoseselbstkontrolle ermittelten durchschnittlichen 7-Punkte-Profil von Studienbeginn bis Woche 30 (-3,35 mmol/l) im Vergleich zu Patienten in der Insulin-glargin-Gruppe
(-2,66 mmol/l; Unterschied -0,69 mmol/l) und Patienten in der Lixisenatid-Gruppe
(-1,95 mmol/l; Unterschied -1,40 mmol/l) (p < 0,0001 für beide Vergleiche).
Zu allen Zeitpunkten waren die durchschnittlichen 30-Wochen-Plasmaglukosewerte in der Suliqua-Gruppe niedriger als in der Insulin-glargin-Gruppe und der Lixisenatid-Gruppe, mit Ausnahme des Werts vor dem Frühstück, der in der Suliqua-Gruppe und der Insulin-glargin-Gruppe vergleichbar war.
·Patienten, die zuvor mit Basalinsulin behandelt wurden
Klinische Studie bei Patienten mit Typ-2-Diabetes, die durch ein Basalinsulin nicht ausreichend kontrolliert waren
Insgesamt 736 Patienten mit Typ-2-Diabetes nahmen an einer randomisierten, 30-wöchigen, aktiv kontrollierten, nicht-verblindeten, zweiarmigen multizentrischen Studie mit Parallelgruppendesign teil, in der die Wirksamkeit und Sicherheit von Suliqua im Vergleich zu Insulin glargin (100 Einheiten/ml) untersucht wurden.
Die gescreenten Patienten hatten Typ-2-Diabetes und wurden seit mindestens 6 Monaten mit einem Basalinsulin behandelt. Die Patienten erhielten eine stabile Tagesdosis zwischen 15 und 40 Einheiten allein oder in Kombination mit einem oder zwei OAD (Metformin oder ein Sulfonylharnstoff oder ein Glinid oder ein SGLT-2-Inhibitor oder ein DPP-4-Inhibitor). Sie hatten einen HbA1c-Wert zwischen 7,5 % und 10 % und einen Nüchternblutzuckerwert kleiner oder gleich 10,0 mmol/l bzw. 11,1 mmol/l, je nach vorhergehender Diabetesbehandlung.
Nach dem Screening traten die geeigneten Patienten (n = 1018) in eine 6-wöchige Run-in-Phase ein, in der sie entweder mit Insulin glargin weiterbehandelt oder, falls sie zuvor ein anderes Basalinsulin angewendet hatten, auf Insulin glargin umgestellt wurden. Die Insulindosis wurde unter weiterer Einnahme von Metformin (falls dies bisher eingenommen wurde) titriert/stabilisiert. Alle anderen OAD wurden abgesetzt.
Am Ende der Run-in-Phase wurden Patienten mit einem HbA1c-Wert zwischen 7 % und 10 %, einem Nüchternblutzuckerwert ≤7,77 mmol/l und einer Insulin-glargin-Tagesdosis zwischen 20 und 50 Einheiten auf entweder Suliqua (n = 367) oder Insulin glargin (n = 369) randomisiert.
Diese Typ-2-Diabetes-Population wies die folgenden Charakteristika auf: Das Durchschnittsalter betrug 60 Jahre, 46,7 % der Patienten waren männlich, der durchschnittliche BMI-Ausgangswert betrug rund 31 kg/m2 und die durchschnittliche Diabetesdauer betrug ca. 12 Jahre.
In Woche 30 zeigte sich unter Suliqua eine statistisch signifikante Verbesserung des HbA1c-Werts (p-Wert < 0,0001) im Vergleich zu Insulin glargin.
Zu den weiteren Studienendpunkten siehe nachstehende Tabelle und Abbildung.
Ergebnisse nach 30 Wochen – Klinische Studie zu Typ-2-Diabetes, unkontrolliert mit einem Basalinsulin (mITT-Population)
|
|
Suliqua
|
Insulin glargin
| |
Anzahl Teilnehmer (mITT)
|
366
|
365
| |
HbA1c (%)
| |
Beim Screening (Mittelwert)
|
8,5
|
8,5
| |
Ausgangswert (Mittelwert; nach der Run-in-Phase)
|
8,1
|
8,1
| |
Ende der Behandlung (Mittelwert)
|
6,9
|
7,5
| |
Veränderung zum Ausgangswert (Kleinste-Quadrate-Mittelwert)
|
-1,1
|
-0,6
| |
Unterschied vs. Insulin glargin
|
-0,5
| |
[95 %-Konfidenzintervall]
|
[-0,6; -0,4]
| |
(p-Wert)
|
(< 0,0001)
| |
Patienten [n (%)], die in Woche 30 einen HbA1c-Wert < 7 % erreichten
|
201 (54,9 %)
|
108 (29,6 %)
| |
Nüchternplasmaglukose (mmol/l)
| |
Ausgangswert (Mittelwert)
|
7,33
|
7,32
| |
Ende der Studie (Mittelwert)
|
6,78
|
6,69
| |
Veränderung zum Ausgangswert (Kleinste-Quadrate-Mittelwert)
|
-0,35
|
-0,46
| |
PPG nach 2 Stunden (mmol/l) [Glykämieschwankung nach 2 Stunden* (mmol/l)]
| |
Veränderung zum Ausgangswert in Woche 30 (Kleinste-Quadrate-Mittelwert)
|
-4,72
[-3,90]
|
-1,39
[-0,47]
| |
Durchschnittliches Körpergewicht (kg)
| |
Ausgangswert (Mittelwert)
|
87,8
|
87,1
| |
Veränderung zum Ausgangswert (Kleinste-Quadrate-Mittelwert)
|
-0,7
|
0,7
| |
Unterschied vs. Insulin glargin
|
-1,4
| |
[95 %-Konfidenzintervall]
|
[-1,8 bis -0,9]
| |
(p-Wert)
|
(< 0,0001)
|
|
|
Suliqua
|
Insulin glargin
| |
Anzahl Teilnehmer (mITT)
|
366
|
365
| |
Anzahl Patienten (%), die in Woche 30 einen HbA1c-Wert < 7,0 % ohne Gewichtszunahme erreichten
|
125
(34,2 %)
|
49
(13,4 %)
| |
Prozentualer Unterschied vs. Insulin glargin
|
20,8
| |
[95 %-Konfidenzintervall]
|
[15,0 bis 26,7]
| |
(p-Wert)
|
(< 0,0001)
| |
Tagesdosis Insulin glargin
| |
Ausgangswert (Mittelwert)
|
35,0
|
35,2
| |
Endpunkt (Mittelwert)
|
46,7
|
46,7
| |
Veränderung der Insulindosis in Woche 30 (Kleinste-Quadrate-Mittelwert)
|
10,6
|
10,9
|
* PPG (postprandiale Glukose) nach 2 Stunden abzüglich des Glukosewerts vor der Mahlzeit
Mittlerer HbA1c-Wert (%) zu Beginn des Screenings, bei der Randomisierung und zu allen weiteren festgelegten Zeitpunkten (Teilnehmer, die die Studie abgeschlossen haben) und in Woche 30 (LOCF*) – mITT-Population
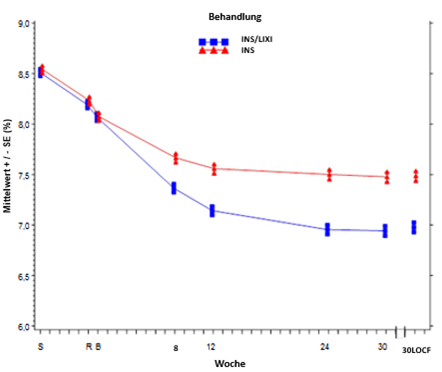
* LOCF = Last Observation Carried Forward (Fortschreibung des letzten gemessenen Werts)
Studien zu kardiovaskulären Endpunkten
Die kardiovaskuläre Sicherheit von Insulin glargin und Lixisenatid wurde in den klinischen Studien ORIGIN bzw. ELIXA nachgewiesen. Zu Suliqua wurde keine gesonderte Studie zu kardiovaskulären Endpunkten durchgeführt.
Insulin glargin
Die ORIGIN-Studie (Outcome Reduction with Initial Glargine Intervention) war eine nicht-verblindete, randomisierte Studie mit 12'537 Patienten mit erhöhtem kardiovaskulärem (KV) Risiko und Anomalie des Nüchternblutzuckers (NBZ), Glukoseintoleranz oder Diabetes mellitus Typ 2 in einem frühen Stadium. Ziel der Studie war der Vergleich von LANTUS mit der Standardtherapie im Hinblick auf den Zeitpunkt des ersten Auftretens eines schwerwiegenden kardiovaskulären Ereignisses (MACE; major adverse cardiovascular event). MACE war definiert als zusammengesetzte Grösse aus Tod kardiovaskulärer Ursache, nicht-tödlichem Myokardinfarkt und nicht-tödlichem Schlaganfall. Die mediane Nachbeobachtungsdauer betrug 6,2 Jahre. Die Häufigkeit von MACE war in der ORIGIN-Studie unter LANTUS vergleichbar wie unter Standardtherapie (Hazard Ratio [95 %-KI] für MACE: 1,02 [0,94; 1,11]).
Lixisenatid
Die ELIXA-Studie war eine randomisierte, doppelblinde, placebokontrollierte, multinationale Studie, in der kardiovaskuläre (KV) Endpunkte unter der Behandlung mit Lixisenatid bei Patienten mit Typ-2-Diabetes (n = 6068) und kurz zurückliegendem akuten Koronarsyndrom untersucht wurden. Der zusammengesetzte primäre Wirksamkeitsendpunkt war die Zeit bis zum ersten Auftreten eines der folgenden Ereignisse, validiert durch den Beurteilungsausschuss für kardiovaskuläre Ereignisse: Kardiovaskulärer Tod, nicht-tödlicher Myokardinfarkt, nicht-tödlicher Schlaganfall oder stationäre Behandlung wegen instabiler Angina pectoris. Einer der sekundären kardiovaskulären Endpunkte war eins der Ereignisse des primären Endpunkts oder stationäre Behandlung wegen Herzinsuffizienz oder koronarer Revaskularisierung. Die mediane Nachbeobachtungsdauer der Studie betrug 25,8 Monate in der Lixisenatid-Gruppe und 25,7 Monate in der Placebogruppe.
Die Inzidenz des primären Endpunkts war in der Lixisenatid-Gruppe und der Placebogruppe vergleichbar: Die Hazard Ratio (HR) für Lixisenatid vs. Placebo betrug 1,017 bei einem zweiseitigen 95 %-Konfidenzintervall (KI) von 0,886 bis 1,168. Vergleichbare Prozentwerte für die beiden Gruppen wurden auch bei den sekundären Endpunkten und für jede der einzelnen Komponenten der zusammengesetzten Endpunkte ermittelt. So betrug der Anteil der Patienten, die wegen Herzinsuffizienz stationär behandelt wurden, 4,0 % in der Lixisenatid-Gruppe und 4,2 % in der Placebogruppe (HR [95 %-Kl] = 0,96 [0,75; 1,23]).
|


