Eigenschaften/WirkungenATC-Code
M05BX05
Wirkungsmechanismus
Burosumab ist ein rekombinanter humaner monoklonaler IgG1 Antikörper gegen den Fibroblasten-Wachstumsfaktor 23 (FGF23), hergestellt mittels rekombinanter DNA Technologie. Burosumab bindet an den FGF23 und hemmt dessen Aktivität. Durch die Hemmung von FGF23 steigert Burosumab die tubuläre Rückresorption von Phosphat aus der Niere und erhöht die Serumkonzentration von 1,25-Dihydroxy-Vitamin D.
Pharmakodynamik
Siehe oben.
Klinische Wirksamkeit
Klinische Wirksamkeit bei Kindern mit XLH
Studie UX023-CL301
In der pädiatrischen Studie UX023-CL301 wurden 61 Patienten im Alter von 1 bis 12 Jahren (56% weiblich; 44% männlich, Alter bei der ersten Dosis: Mittelwert [SD]: 6.3 [3.31] Jahre) randomisiert einer Behandlung mit Burosumab (n = 29) oder einer aktiven Kontrolle (n = 32; orales Phosphatpräparat und aktives Vitamin D) zugewiesen. Beim Eintritt in die Studie mussten alle Patienten seit mindestens 6 Monaten mit einem oralen Phosphatpräparat und aktivem Vitamin D behandelt worden sein. Von allen Patienten lagen röntgenologische Nachweise einer XLHbedingten Knochenerkrankung (Rachitis-Severity-Score ≥2) vor. Die Behandlung mit Burosumab wurde mit einer Dosis von 0.8 mg/kg alle 2 Wochen eingeleitet und bei unzureichendem Ansprechen laut Nüchtern-Serumphosphatwert auf 1.2 mg/kg gesteigert. Patienten, die in die aktive Kontrollgruppe randomisiert wurden, erhielten mehrere tägliche Dosen eines oralen Phosphatpräparats und von aktivem Vitamin D.
Primärer Wirksamkeitsendpunkt war die Veränderung des Rachitis-Schweregrades in Woche 40 gemäss RGI-C-Score (Radiographic Global Impression of Change; radiographischer Gesamteindruck der Veränderung) im Vergleich zwischen der Burosumab-Gruppe und der aktiven Kontrollgruppe.
Der RGI-C ist eine relative Beurteilungsskala zum Vergleich der Rachitis vor und nach einer Behandlung mithilfe einer 7 Punkte umfassenden Ordinalskala, welche die Veränderung bei den gleichen Anomalien beurteilt, die anhand des (unten beschriebenen) RSS bewertet wurden. Die Punktbewertungen (Scores) reichen von -3 (schwere Verschlechterung der Rachitis) bis +3 (vollständige Heilung der Rachitis).
Der Schweregrad der pädiatrischen Rachitis wurde mithilfe des RSS bestimmt, einer Bewertungsmethode für Röntgenaufnahmen basierend auf dem Grad der Ausfransung oder Becherung der Metaphyse und inwieweit die Wachstumsfuge betroffen ist. In Studie UX023-CL301 wurde der RSS anhand einer vorgegebenen Skala bewertet, die spezifische Anomalien von Hand- und Kniegelenken berücksichtigte.
Alle Patienten durchliefen mindestens 64 Wochen der randomisierten Behandlung. Bei keinem der Patienten wurde die Dosis reduziert, und bei 8 (28%) der mit Burosumab behandelten Patienten wurde die Dosis auf 1.2 mg/kg erhöht.
Primäre Wirksamkeitsergebnisse
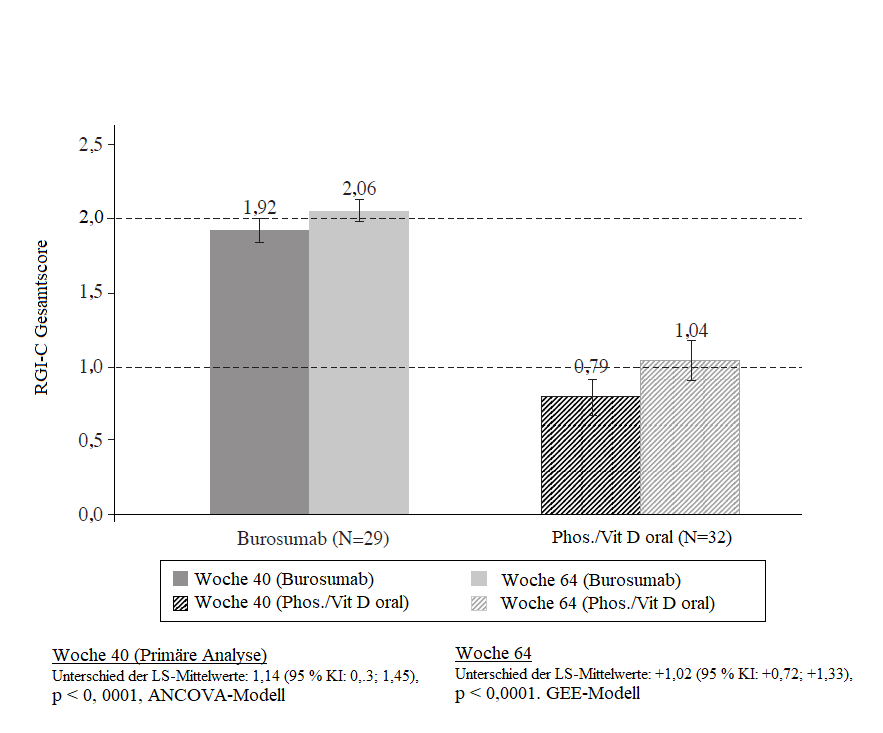
Bei der Behandlung mit Burosumab wurde im Vergleich zur aktiven Kontrolle eine bessere Heilung der Rachitis in Woche 40 beobachtet. Diese Wirkung hielt bis Woche 64 an, wie aus Abbildung 1 hervorgeht.
Abbildung 1: RGI-C-Gesamtscore (Mittelwert ± SE) – Primärer Wirksamkeitsendpunkt in Woche 40 und 64 (Gesamtgruppe)
Sekundäre Wirksamkeitsergebnisse
Die wichtigsten Ergebnisse der sekundären Wirksamkeitsendpunkte sind in Tabelle 6 dargestellt.
Tabelle 6 Ergebnisse der sekundären Wirksamkeitsendpunkte
|
Endpunkt
|
Woche
|
Aktive Kontrolle
LS Mittelwert (SE)
|
Burosumab
LS Mittelwert (SE)
|
Unterschied (Burosumab – aktive Kontrolle)
| |
Missbildung der unteren Gliedmassen; gemäss RGI-C
(GEE-Modell)
|
40
|
+0.22 (0.080)
|
+0.62 (0.153)
|
+0.40 [95%-KI: 0.07, 0.72] p = 0.0162
| |
64
|
+0.29 (0.119)
|
+1.25 (0.170)
|
+0.97 [95%-KI: +0.57, +1.37] p < 0.0001
| |
Grösse; Z-Score
|
Studienbeginn
|
-2.05 (0.87)
|
-2.32 (1.17)
|
| |
40a
|
+0.03 (0.031)
|
+0.16 (0.052)
|
+0.12 [95%-KI: 0.01, 0.24] p = 0.0408
| |
64b
|
+0.02 (0.035)
|
+0.17 (0.066)
|
+0.14 [95%-KI: 0.00, 0.29] p = 0.0490
| |
Rachitis-Schweregrad, RSS-Gesamtscore
|
Studienbeginn
|
3.19 (1.141)
|
3.17 (0.975)
|
| |
40a
|
-0.72 (0.162)
|
-2.08 (0.104)
|
-1.34 [95%-KI: -1.74, -0.94] p < 0.0001
| |
64b
|
-1.01 (0.151)
|
-2.23 (0.117)
|
-1.21 [95%-KI: -1.59, -0.83] p < 0.0001
| |
Alkalische Phosphatase im Serum (U/L)
|
Studienbeginn
|
523 (154)
|
511 (125)
|
| |
40a
|
489 (189)
|
381 (99)
|
-97 [95% KI: -138, -56]
p < 0.0001
| |
64b
|
495 (182)
|
337 (86)
|
-147 [95% KI: -192, -102]
p < 0.0001
| |
Sechs-Minuten-Gehtest (m)
|
Studienbeginn
|
450 (106)
|
385 (86)
|
| |
40a
|
+4 (14)
|
+47 (16)
|
+43 [95%-KI: -0.3, 87]; p = 0.0514
| |
64b
|
+29 (17)
|
+75 (13)
|
+46 [95%-KI: 2, 89];
p = 0.0399
|
a Veränderung zwischen Studienbeginn und Woche 40 laut ANCOVA-Modell.
b Veränderung zwischen Studienbeginn und Woche 64 laut GEE-Modell.
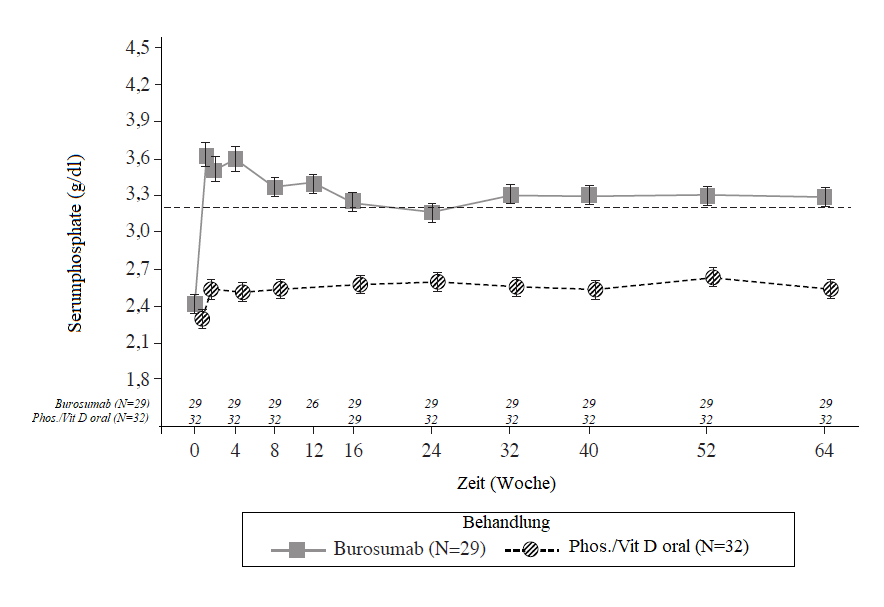
Serumphosphat
Bei jedem Studientermin, bei dem in beiden Gruppen die Serumphosphatwerte beurteilt wurden, waren die Veränderungen der Serumphosphatwerte gegenüber Studienbeginn in der Burosumab-Gruppe grösser als in der aktiven Kontrollgruppe (p < 0.0001; GEE-Modell) (Abbildung 2).
Abbildung 2: Serumphosphatkonzentration und Veränderung gegenüber Studienbeginn (mg/dl) (Mittelwert ± SE) nach Behandlungsgruppe (PD Analysegruppe)
Hinweis: Die gestrichelte Linie in der Abbildung zeigt die untere Grenze des Serumphosphat-Referenzbereichs von 3.2 mg/dl an (1.03 mmol/L).
Pädiatrische PROMIS-Fragebögen
In der Burosumab-Gruppe wurden in den Wochen 40 und 64 klinisch bedeutsame Verbesserungen in Bezug auf Schmerzbeeinträchtigung und Erschöpfung (erhoben für Patienten ≥ 5 Jahren) festgestellt, wobei zwischen den Behandlungsgruppen in Woche 40 ein statistisch signifikanter Unterschied zugunsten der Burosumab-Gruppe hinsichtlich der Schmerzbeeinträchtigung beobachtet wurde (p = 0.0212). In der aktiven Kontrollgruppe gab es in den Wochen 40 oder 64 keine klinisch bedeutsame Veränderung gegenüber den Ausgangswerten.
Studie UX023-CL201
In der pädiatrischen Studie UX023-CL201 wurden 52 Kinder im Alter von 5 bis 12 Jahren (mittleres Alter 8.5 Jahre; Standardabweichung (SD) 1.87) mit XLH über 64 Wochen behandelt. Bei fast allen Patienten lagen zu Studienbeginn röntgenologische Nachweise einer Rachitis vor, und sie waren zuvor über eine mittlere (SD) Zeitdauer von 7 (2.4) Jahren mit oralen Phosphatpräparaten und Vitamin D-Derivaten behandelt worden. Diese konventionelle Therapie wurde 2 bis 4 Wochen vor Einleitung der Burosumab-Behandlung abgesetzt. Die Burosumab-Dosis wurde an einen Zielwert für den Nüchtern-Serumphosphatwert von 3.50 bis 5.02 mg/dl (1.13 bis 1.62 mmol/l) angepasst. Von den 52 Patienten erhielten 26 Burosumab alle 4 Wochen (Q4W). Ebenfalls 26 der 52 Patienten erhielten Burosumab alle zwei Wochen (Q2W) in einer Durchschnittsdosis (Min., Max.) von 0.73 (0.3; 1.5), 0.98 (0.4; 2.0) und 1.04 (0.4; 2.0) mg/kg in Woche 16, 40 bzw. 64 und bis zu einer Maximaldosis von 2.0 mg/kg.
Burosumab erhöhte die Serumphosphat-Konzentration und den Quotienten aus maximaler tubulärer Rückresorption von Phosphat und glomerulärer Filtrationsrate (TmP/GFR-Quotienten). In der Patientengruppe, die Burosumab alle 2 Wochen erhielt, erhöhte sich die mittlere (SD) Serumphosphat-Konzentration von 2.38 (0.405) mg/dl (0.77 (0.13) mmol/l) zu Studienbeginn auf 3.30 (0.396) mg/dl (1.07 (0.13) mmol/l) in Woche 40 und blieb bis Woche 64 auf einem Wert von 3.35 (0.445) mg/dl (1.08 (0.14) mmol/l).
Aktivität der alkalischen Phosphatase
Die mittlere (SD) Gesamtaktivität der alkalischen Phosphatase im Serum betrug bei Ausgangswerterhebung 459 (105) E/l und sank auf 369 (76) E/l in Woche 64 (-19.6%; p <0.0001).
Der Gehalt an knochenspezifischer alkalischer Phosphatase im Serum betrug 165 (52) μg/l [Mittel (SD)] bei Ausgangswerterhebung und 115 (31) μg/l in Woche 64 (mittlere Veränderung: -28.5%).
Der Schweregrad der pädiatrischen Rachitis wurde in Studie UX023-CL201 mithilfe des RSS (siehe oben) bestimmt. In Studie UX023-CL201 wurde der RSS anhand einer vorgegebenen Skala bewertet, die spezifische Anomalien der Handgelenke und Knie berücksichtigte. Die Ergebnisse sind in Tabelle 7 zusammengefasst.
Als Ergänzung zur Beurteilung des RSS wurde die RGI-C Bewertungsskala verwendet. Die Ergebnisse sind in Tabelle 7 zusammengefasst.
Tabelle 7: Ansprechen der Rachitis bei Kindern von 5 bis 12 Jahren, die in Studie UX023-CL201 mit Burosumab behandelt wurden
|
Endpunkt
|
Dauer der Burosumab-Behandlung
(Woche)
|
Effektgrösse
| |
Alle 2 Wochen (N=26)
|
Alle 4 Wochen (N=26)
| |
RSS Gesamtscore
Mittelwert (SD) zu Studienbeginn
Veränderung des LS Mittelwertes (SE) des Gesamtscoresa gegenüber Baseline (ein reduzierter RSS-Score zeigt eine Besserung des Schweregrades der Rachitis)
|
|
|
| |
40
|
1.92 (1.2)
-1.06 (0.1) (p < 0.0001)
|
1.67 (1.0)
-0.73 (0.1) (p < 0.0001)
| |
64
|
-1.00 (0.1) (p < 0.0001)
|
-0.84 (0.1) (p < 0.0001)
| |
RGI-C Gesamtscore
LS Mittelwert (SE)a (positive weist auf Heilung hin)
|
40
|
+1.66 (0.1) (p < 0.0001)
|
+1.47 (0.1) (p < 0.0001)
| |
64
|
+1.56 (0.1) (p < 0.0001)
|
+1.58 (0.1) (p < 0.0001)
|
a Schätzungen des LS Mittelwerts und der p-Werte stammen von dem Gleichungsmodell für generalisierte Schätzungen, das den Ausgangs-RSS, Besuchstermine und Behandlungsregime sowie deren Interaktionen berücksichtigt.
Studie UX023-CL205
In der pädiatrischen Studie UX023-CL205 wurde Burosumab an 13 Kindern mit XLH im Alter von 1 bis 4 Jahren (mittleres Alter 2.9 Jahre; SD 1.1) über 40 Wochen untersucht. Bei allen Patienten lagen zu Studienbeginn röntgenologische Nachweise einer Rachitis vor, und zwölf Patienten waren für eine mittlere (SD) Zeitdauer von 16.7 (14.4) Monaten mit oralen Phosphatpräparaten und Vitamin D-Derivaten vorbehandelt worden. Diese konventionelle Therapie wurde 2 bis 6 Wochen vor Einleitung der Burosumab-Behandlung abgesetzt. Die Patienten erhielten Burosumab in einer Dosis von 0.8 mg/kg alle zwei Wochen.
In Studie UX023-CL205 stieg die mittlere (SD) Nüchtern-Serumphosphat-Konzentration von 2.51 (0.284) mg/dl (0.81 (0.092) mmol/l) zu Studienbeginn auf 3.47 (0.485) mg/dl (1.12 (0.158) mmol/l) in Woche 40.
Aktivität der alkalischen Phosphatase im Serum
Die mittlere (SD) Gesamtaktivität der alkalischen Phosphatase im Serum betrug 549 (193.8) E/l zu Studienbeginn und sank auf 335 (87.6) E/l in Woche 40 (mittlere Veränderung: -36.3%).
Rachitis-Severity-Score (RSS; Score zur Erfassung des Schweregrads der Rachitis)
Nach 40 Behandlungswochen mit Burosumab besserte sich der mittlere Gesamt-RSS von 2.92 (1.367) zu Studienbeginn auf 1.19 (0.522); dies entsprach einer Veränderung des angepassten Mittelwerts (SE) gegenüber dem Ausgangswert von -1.73 (0.132) (p < 0.0001).
Radiographic Global Impression of Change (RGI-C; Radiographischer Gesamteindruck der Veränderung)
Nach 40 Behandlungswochen mit Burosumab betrug der angepasste Mittelwert (SE) des RGI-C-Gesamtscores +2.33 (0.08) bei allen 13 Patienten (p < 0.0001), was eine Besserung der Rachitis belegte. Alle 13 Patienten wurden als RGI-C-Responder gemäss der Definition durch einen RGI-C-Gesamtscore ≥ +2.0 eingestuft.
Klinische Wirksamkeit bei Erwachsenen mit XLH
Studie UX023-CL303 ist eine randomisierte, doppelblinde, placebokontrollierte Studie an 134 erwachsenen XLH-Patienten. Die Studie umfasste eine 24-wöchige placebokontrollierte Behandlungsphase, gefolgt von einer 24-wöchigen offenen Phase, in der alle Patienten Burosumab erhielten. Burosumab wurde in einer Dosis von 1 mg/kg alle 4 Wochen verabreicht. Ein Patient in der Burosumab-Gruppe brach die Behandlung ab. Zu Studienbeginn lag das mittlere Alter der Patienten bei 40 Jahren (Spanne 19 bis 66 Jahre) und 35% waren männlich. Die mittlere (SE) Phosphatkonzentration im Serum zu Studienbeginn lag unterhalb der unteren Normgrenze bei 1.98 (0.314) mg/dl (0.64 (1.10) mmol/l).
In Studie UX023-CL304 wurde der Einfluss von Burosomab auf die durch die Hypophosphatämie bedingte Osteomalazie anhand der Untersuchung von Beckenkamm-Biopsien evaluiert. Es handelte sich um eine 48-wöchige, offene, einarmige Studie an 14 erwachsenen Patienten mit XLH. Die Patienten erhielten alle 4 Wochen 1.0 mg/kg Burosumab.
Serumphosphat
In Studie UX023-CL303 lag der Serumphosphatwert zu Studienbeginn bei 1.92 (0.32) mg/dl (0.62 (0.102) mmol/l) in der Placebo- und bei 2.03 (0.30) mg/dl (0.66 (0.098) mmol/l in der Burosumab-Gruppe. Im Verlauf der 24 Behandlungswochen betrug der mittlere (SD) Serumphosphatwert in der Mitte der Verabreichungsintervalle (2 Wochen nach Verabreichung) 2.08 (0.30) mg/dl (0.67 (0.09) mmol/l) in der Placebo- bzw. 3.24 (0.53) mg/dl (1.05 (0.17) mmol/l) in der Burosumab-Gruppe. Für den primären Wirksamkeitsendpunkt sind die Resultate in Tabelle 8 aufgeführt.
Tabelle 8: Anteil der erwachsenen Patienten, die in Studie UX023-CL303 (doppelblinde Phase) in der Mitte des Verabreichungsintervalls einen mittleren Serumphosphatwert über der LLN erreichten
|
|
Placebo
(N = 66)
|
Burosumab
(N = 68)
| |
In der Mitte der Verabreichungsintervalle bis Woche 24 ein mittleres Serumphosphat > LLN erreicht - n (%)
|
7.6% (5/66)
|
94.1% (64/68)
| |
95%-KI
|
(3.3, 16.5)
|
(85.8, 97.7)
| |
p-Werta
|
|
< 0.0001
|
Die 95%-KIs wurden mithilfe der Wilson-Score-Methode berechnet.
a Der P-Wert stammt aus einem Cochran-Mantel-Haenszel (CMH) Test auf Assoziation zwischen dem Erreichen des primären Endpunkts und der Behandlungsgruppe zur Adjustierung für die Stratifizierungen der Randomisierung.
Die drei wichtigsten sekundären, von den Patienten berichteten Endpunkte Steifigkeit, stärkster Schmerz (Worst Pain) und körperliche Funktion (Physical Function) wurden in Woche 24 ausgewertet und mit den Ausgangswerten verglichen. Die Ergebnisse sind in Tabelle 9 dargestellt.
Tabelle 9: Veränderung der von den Patienten berichteten Ergebnisse zwischen Studienbeginn und Woche 24 sowie Auswertung des Unterschieds in Woche 24
|
|
Placebo
(N = 66)
|
Burosumab
(N = 68)
| |
WOMAC-Steifigkeitsscore
(Abnahme bedeutet geringere Steifigkeit)
|
|
| |
Mittelwert (SD) zu Studienbeginn
|
61.36 (20.77)
|
64.71 (20.25)
| |
Mittelwert (SD) in Woche 24
|
60.38 (21.83)
|
53.73 (20.76)
| |
Veränderung des LS Mittelwertes (SE) zwischen Studienbeginn und Woche 24
|
+0.46 (3.14)
|
-7.85 (3.03)
| |
Unterschied im LS Mittelwert (SE) (Burosumab vs. Placebo)
|
-8.3 (3.25)
| |
p-Wert
|
0.0106
| |
WOMAC Physical Function-Score
(Abnahme bedeutet Besserung der körperlichen Funktionsfähigkeit)
|
|
| |
Mittelwert (SD) zu Studienbeginn
|
43.89 (19.94)
|
50.79 (19.66)
| |
Mittelwert (SD) in Woche 24
|
42.65 (22.76)
|
43.43 (19.51)
| |
Veränderung des LS Mittelwertes (SE) zwischen Studienbeginn und Woche 24
|
+1.79 (2.72)
|
-3.11 (2.55)
| |
Unterschied (SE) (Burosumab vs. Placebo)
|
-4.9 (2.48)
| |
p-Wert
|
0.0478
| |
BPI-SF Worst Pain-Score
(Abnahme bedeutet weniger Schmerz)
|
|
| |
Mittelwert (SD) zu Studienbeginn
|
6.54 (1.43)
|
6.81 (1.31)
| |
Mittelwert (SD) in Woche 24
|
6.09 (2.01)
|
5.82 (1.92)
| |
Veränderung des LS Mittelwertes (SE) zwischen Studienbeginn und Woche 24
|
-0.32 (0.22)
|
-0.79 (0.21)
| |
Unterschied (SE) (Burosumab vs. Placebo)
|
-0.5 (0.28)
| |
p-Werta
|
0.0919
| |
BPI-SF = Brief Pain Inventory (Schmerzfragebogen); GEE = generalized estimation equation (generalisierte Schätzgleichung); LS = least squares (kleinste Quadrate); WOMAC = Western Ontario and McMaster Universities osteoarthritis index (Arthroseindex der Universitäten Western Ontario und McMaster)
a Schätzungen der LS-Mittelwerte und der p-Werte in Woche 24 stammen von dem Gleichungsmodell für generalisierte Schätzungen, das die Veränderung seit Studienbeginn für den Endpunkt von Interesse als abhängige Variable, Region, Besuchstermin, Behandlungsregime, tatsächliche Stratifizierung bei Randomisierung (nicht bei der Auswertung des BPI Worst Pain-Scores) und die Interaktion zwischen Besuchstermin und Behandlungsregime als Festfaktoren sowie den Ausgangswert für den Endpunkt von Interesse als Kovariable mit einer zusammengesetzt-symmetrischen Kovarianzstruktur berücksichtigt.
|
Radiologische Beurteilung von Frakturen und Pseudofrakturen
In Studie UX023-CL303 wurde zu Studienbeginn ein Skelettröntgen durchgeführt, um osteomalaziebedingte Frakturen und Pseudofrakturen zu identifizieren. Zu Studienbeginn hatten 52% der Patienten entweder aktive (nicht verheilte) Frakturen (12%) oder aktive Pseudofrakturen (47%). In Woche 24 waren 36.9% der zu Studienbeginn aktiven Frakturen/Pseudofrakturen in der Burosumab-Gruppe vollständig abgeheilt, verglichen mit 9.9% in der Placebo-Gruppe.
Histomorphometrische Untersuchungen der Knochenstruktur bei Erwachsenen
Nach 48 Behandlungswochen in Studie UX023-CL304 wurde bei 10 Patienten anhand von Abnahmen des Osteoidvolumens/Knochenvolumens (OV/BV) von einem mittleren (SD) Score von 26.1% (12.4) bei Studienbeginn auf 11.2% (6.5), einer Reduktion um 57%, eine Heilung der Osteomalazie beobachtet.
| 

