Eigenschaften/WirkungenATC-Code
M03AX01
Wirkungsmechanismus / Pharmakodynamik
Clostridium botulinum Neurotoxin Typ A blockiert die periphere Freisetzung des Neurotransmitters Acetylcholin an präsynaptischen cholinergen Nervenenden neuromuskulärer Verbindungen durch Spaltung von SNAP 25, einem Protein, das für das erfolgreiche Andocken und die Freisetzung von Acetylcholin aus Bläschen in den Nervenendigungen von Bedeutung ist, was zur Denervierung des Muskels und einer schlaffen Lähmung führt.
Nach der Injektion kommt es zunächst zu einer schnellen Bindung des Toxins mit hoher Affinität an spezifische Rezeptoren an der Zelloberfläche. Daraufhin wird das Toxin durch rezeptorvermittelte Endozytose durch die Plasmamembran geschleust. Schliesslich wird das Toxin unter fortschreitender Hemmung der Acetylcholinfreisetzung ins Zytosol freigesetzt. Klinische Symptome treten innerhalb von 2 bis 3 Tagen auf, wobei die maximale Wirkung innerhalb von 4 Wochen nach der Injektion festzustellen ist. Ein Abflauen der Wirkung tritt normalerweise innerhalb von 3 bis 4 Monaten nach der Injektion auf, wenn die Nervenenden erneut aussprossen und sich wieder mit der Endplatte verbinden.
Klinische Wirksamkeit
Die Sicherheit und Wirksamkeit von Letybo wurden in 3 pivotalen, doppelblinden Phase-III-Studien (BLESS I, BLESS II und BLESS III) untersucht, in denen insgesamt 955 Patienten eine Behandlung mit Letybo und 317 Patienten eine Behandlung mit einem Placebo erhielten. Darüber hinaus liegen Daten von 854 Patienten vor, die im Rahmen einer nicht verblindeten Verlängerungsphase der Studien BLESS I und II weitere 1 bis 3 Behandlungen mit Letybo erhielten. Unterstützende Daten zu Glabellafalten stammen aus dem klinischen Entwicklungsprogramm in Korea, das eine Phase-III-Studie (HG-11-01) bei 137 Patienten und eine Post-Marketing-Studie (HG-13-02) bei 815 Patienten umfasste.
In den Studien BLESS I, BLESS II und BLESS III hatten alle Patienten bei maximalem Stirnrunzeln zu Studienbeginn mittelstarke (27 % der Patienten) oder starke (73 % der Patienten) Glabellafalten. Letybo reduzierte in einer Dosis von 20 Einheiten signifikant die Stärke der Glabellafalten bei maximalem Stirnrunzeln, gemessen anhand der Beurteilung der Stärke der Glabellafalten durch den Prüfarzt und den Patienten auf einer 4-Punkte-Skala zur Beurteilung von Gesichtsfalten (Facial Wrinkle Scale, FWS). Bei Anlegen eines Endpunkts, der eine Verbesserung auf der FWS um 2 Punkte erforderte, wurden statistisch signifikante Ansprechraten zugunsten von Letybo festgestellt. Hohe Ansprechraten zugunsten von Letybo wurden auch bei Anwendung der Definition eines klinisch bedeutsamen Ansprechens (Erreichen eines Scores von 0 oder 1 auf der FWS bzw. keine oder leichte Linien) nach Einstufung durch den Prüfarzt in Woche 4 beobachtet (siehe Tabelle 2).
Tabelle 2: Ansprechraten von der Baseline bis Woche 4 bei maximalem Stirnrunzeln auf der Grundlage der Skala zur Beurteilung von Gesichtsfalten (FWS) in den Studien BLESS I, BLESS II und BLESS III – Vollständige Analysegruppe
|
|
BLESS I
|
BLESS II
|
BLESS III
| |
Beurteilt von:
|
Letybo
(N = 529)
|
Placebo
(N = 175)
|
Letybo
(N = 160)
|
Placebo
(N = 53)
|
Letybo
(N = 266)
|
Placebo
(N = 89)
| |
Ansprechrate (n [%]): Reduzierung des FWS-Scores von mittelstark oder stark auf keine oder leicht (Verbesserung um ≥2 Punkte erforderlich)a
| |
Prüfarzt UND Patient
|
246 (46,5 %)*
|
0 (0 %)
|
78 (48,8 %)*
|
1 (1,9 %)
|
172 (64,7 %)*
|
0 (0,0 %)
| |
Prüfarzt
|
348 (65,8 %)*
|
1 (0,6 %)
|
120 (75,0 %)*
|
1 (1,9 %)
|
209 (78,6 %)*
|
1 (1,1 %)
| |
Patient
|
290 (54,8 %)*
|
0 (0 %)
|
83 (51,9 %)*
|
1 (1,9 %)
|
183 (68,8 %)*
|
0 (0,0 %)
| |
Ansprechrate (%): Reduzierung des FWS-Scores von mittelstark oder stark auf keine oder leichtb
| |
Prüfarzt
|
393 (74,3 %)*
|
3 (1,7 %)
|
136 (85,0%)*
|
2 (3,8 %)
|
218 (82,0 %)*
|
1 (1,1 %)
|
* p-Wert <0,001 im Cochran–Mantel–Haenszel-Test auf Vorhandensein eines Unterschieds zwischen Letybo und Placebo; N: Anzahl der randomisierten Patienten, n: Anzahl Responder
a Primärer Wirksamkeitsendpunkt
b Post-hoc-Analyse
Insgesamt 38,3 % der mit Letybo behandelten Studienteilnehmer wiesen in Woche 4 nach Einschätzung durch den Prüfarzt eine Verbesserung der Faltenstärke um 3 Punkte von anfangs starken Falten (FWS-Grad 3) zu keinen Falten (FWS-Grad 0) auf.
Die Verbesserung der Glabellafalten (basierend auf einer Verbesserung bzw. Reduzierung des FWS-Scores um ≥2 Punkte bei maximalem Stirnrunzeln, basierend auf der Beurteilung durch den Studienteilnehmer und den Prüfarzt) setzte innerhalb einer Woche nach der Injektion ein und erreichte eine maximale Wirkung in der zweiten Woche nach der Injektion. Die Wirkungsdauer beträgt zwischen 12 und 16 Wochen (siehe Abbildung 1).
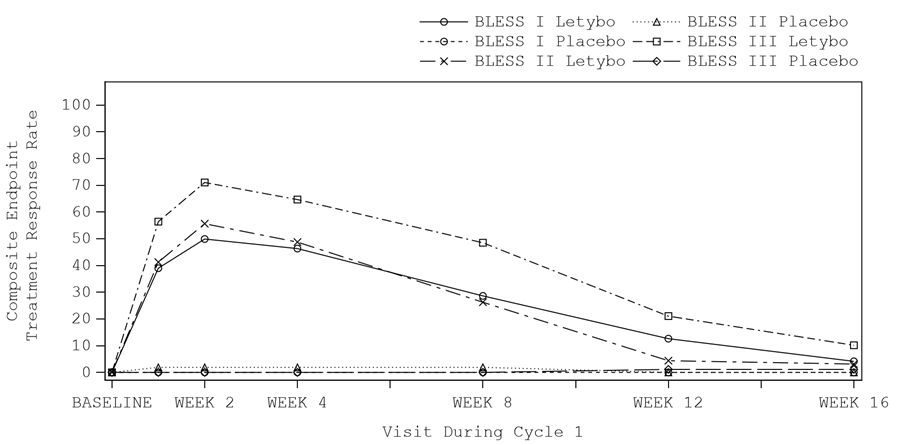
Abbildung 1: Zeitlicher Verlauf der Responderrate (Verbesserung um ≥2 Punkte auf der FWS sowohl bei Einschätzung durch den Studienteilnehmer als auch durch den Prüfarzt erforderlich) in Zyklus 1 bei Anwendung der Verum- versus der Placebo-Behandlung in den pivotalen BLESS-Studien
Es konnte gezeigt werden, dass die Responderrate mit Reduzierung des FWS-Scores in Ruhe um ≥1 Punkt(e) in der Letybo-Gruppe im Vergleich zur Placebo-Gruppe statistisch signifikant höher war: Vier Wochen nach der Injektion wiesen 63,1 %, 59,4 % und 61,3 % der mit Letybo behandelten Patienten sowie 15,4 %, 5,7 % und 9,0 % der mit Placebo behandelten Patienten in den Studien BLESS I, BLESS II bzw. BLESS III nach Einschätzung durch den Prüfarzt eine Verbesserung in Ruhe um ≥1 Punkt(e) auf der FWS auf (der p-Wert für Unterschiede zwischen den Behandlungen war in allen Studien <0,001).
Offene Langzeitdaten bei wiederholter Anwendung bestätigten, dass die Ansprechraten nach der zweiten, dritten und vierten Behandlung mit Letybo während des einjährigen Studienzeitraums hoch blieben, wenngleich in den Wiederholungszyklen bedingt durch das Studiendesign eine gewisse Tendenz in Richtung eines Nichtansprechens vorlag.
Gemäss der neu entwickelten modifizierten Skindex 16 Glabellar Line Quality of Life-Skala lagen zur Baseline bei mehr als 85 % der Patienten, die an der Studie teilnahmen, mittelstarke oder starke und bei etwa 15 % der Patienten leichte negative psychologische Auswirkungen der Glabellafalten vor.
Bei Patienten unter Behandlung mit Letybo wurde gegenüber denen in der Placebogruppe eine deutliche Verbesserung der psychologischen Auswirkungen, gemessen anhand der modifizierten Skindex 16 Glabellar Line Quality of Life-Skala, festgestellt.
Die Patienten berichteten über insgesamt positive ästhetische Ergebnisse und eine hohe Zufriedenheit mit dem Ergebnis.
Post-Marketing-Daten
Die Post-Marketing-Daten, einschliesslich der Daten aus einer Post-Marketing-Studie zu Glabellafalten (HG-13-02) bei 815 Patienten, stimmen mit den Daten aus den klinischen Studien überein.
Ältere Patienten
In den Studien BLESS I, BLESS II und BLESS III waren insgesamt 152/1’272 (11,91 %) der Patienten zum Screening-Zeitpunkt ≥65 Jahre alt. Kein Patient war älter als 75 Jahre. Die kombinierte Responderrate in Woche 4 (primärer Endpunkt) unter Behandlung mit Letybo betrug bei Kombination der Studien BLESS I, BLESS II und BLESS III bei Patienten ≥65 Jahren 46/118 (39,0 %) und war damit niedriger als bei Patienten <65 Jahren (450/839 bzw. 53,6 %). In den 3 Studien kombiniert gab es keine grossen Unterschiede in den Gesamtraten der Patienten mit TEAEs, die als mit der doppelblinden Letybo-Behandlung im Zusammenhang stehend eingestuft wurden (3,7 % bei Patienten <65 Jahren und 1,7 % bei den Patienten ≥65 Jahren, wenn medikationsbezogene TEAEs und/oder durch das Injektionsverfahren bedingte TEAEs berücksichtigt wurden).
|

