PharmakokinetikDie nachfolgend aufgeführte Pharmakokinetik von Aripiprazol nach der Anwendung von Abilify Asimtufii basiert auf der Verabreichung in den Glutealmuskel.
Abilify Asimtufii 960 mg/720 mg setzt im Vergleich mit Abilify Maintena 400 mg/300 mg Aripiprazol über einen Zeitraum von 2 Monaten frei. Abilify Asimtufii -Dosen von 960 mg und 720 mg führen bei Anwendung in den Glutealmuskel insgesamt zu Expositionsbereichen gegenüber Aripiprazol, die innerhalb des Expositionsbereichs liegen, wie sie bei Dosen von 300 mg bzw. 400 mg Abilify Maintena (einmal monatliche Dosisgabe) auftreten. Zusätzlich waren die unter Abilify Asimtufii 960 mg/720 mg beobachteten mittleren maximalen Plasmakonzentrationen (Cmax) sowie Plasmakonzentrationen von Aripiprazol am Ende des Dosierungsintervalls vergleichbar mit denen, die bei entsprechenden Dosen von Abilify Maintena 400 mg/300 mg beobachtet wurden (siehe Abschnitt «Klinische Wirksamkeit», Tabelle 2).
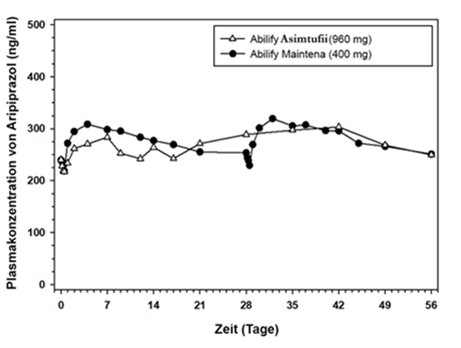
Die mittlere Plasmakonzentration von Aripiprazol im Vergleich zu den Zeitprofilen nach der 4. Anwendung von Abilify Asimtufii 960 mg (n = 102) oder der 7. und 8. Anwendung von Abilify Maintena 400 mg (n = 93) in den Glutealmuskel von Patienten mit Schizophrenie (und Bipolar-I-Störung) ist in Abbildung 2 zu sehen.
Abbildung 2: Mittlere Plasmakonzentration von Aripiprazol vs. Zeitprofil nach der 4. Anwendung von Abilify Asimtufii 960 mg oder der 7. und 8. Anwendung von Abilify Maintena 400 mg
Distribution
Die Resorption von Aripiprazol nach glutealer Injektion in den Blutkreislauf erfolgt langsam und anhaltend aufgrund der niedrigen Löslichkeit der Aripiprazol-Partikel. Das Freisetzungsprofil von Aripiprazol bei Abilify Asimtufii 960 mg/720 mg führt nach glutealen Injektionen 2 Monate lang zu anhaltenden Plasmakonzentrationen. Die Freisetzung des Wirkstoffs nach einer Einzeldosis von 780 mg von einmal alle 2 Monate injiziertem, gebrauchsfertigem und langwirksamem Aripiprazol beginnt an Tag 1 und hält bis zu 34 Wochen an. Für die Standarddosierung von 960 mg ist eine noch über 34 Wochen hinausgehende Nachweisdauer von Aripiprazol im Plasma wahrscheinlich.
Metabolismus
Aripiprazol wird überwiegend in der Leber hauptsächlich über drei Biotransformationswege metabolisiert: Dehydrierung, Hydroxylierung und N-Dealkylierung. Basierend auf in vitro-Studien sind die Enzyme CYP3A4 und CYP2D6 für die Dehydrierung und Hydroxylierung von Aripiprazol verantwortlich, die N-Dealkylierung wird durch CYP3A4 katalysiert. Aripiprazol macht den Hauptanteil des Arzneimittels im systemischen Kreislauf aus. Nach Verabreichung mehrerer Abilify Asimtufii 960 mg/720 mg-Dosen beträgt der Anteil von Dehydro-Aripiprazol, dem aktiven Metaboliten, annähernd 30 % der AUC von Aripiprazol im Plasma.
Elimination
Nach mehrmaliger Verabreichung von 400 mg oder 300 mg Abilify Maintena, beträgt die durchschnittliche terminale Eliminationshalbwertszeit von Aripiprazol 46,5 respektive 29,9 Tage, vermutlich aufgrund der resorptionsratenbegrenzten Kinetik.
Nach einmaliger oraler Gabe von [14C]-markiertem Aripiprazol, wurden etwa 27% der zugeführten Radioaktivität im Urin und etwa 60% in den Fäzes nachgewiesen. Weniger als 1% an unverändertem Aripiprazol wurde im Urin ausgeschieden und etwa 18% wurden unverändert in den Fäzes nachgewiesen.
Kinetik spezieller Patientengruppen
Geschlecht
Nach oraler Gabe von Aripiprazol gibt es keine Unterschiede in der Pharmakokinetik von Aripiprazol zwischen gesunden männlichen und weiblichen Probanden. Ebenso zeigten sich bei der pharmakokinetischen Populationsanalyse von Aripiprazol in klinischen Studien bei schizophrenen Patienten keine geschlechtsabhängigen Wirkungen.
Rauchen
Eine populationsspezifische Auswertung zur Pharmakokinetik von oral angewendetem Aripiprazol ergab keinen Hinweis auf klinisch signifikante Wirkungen hinsichtlich des Rauchens auf die Pharmakokinetik von Aripiprazol.
Ethnische Zugehörigkeit
Eine populationspharmakokinetische Untersuchung von Abilify Asimtufii lieferte keine Hinweise auf ethnisch bedingte Unterschiede in der Pharmakokinetik von Aripiprazol.
Leberfunktionsstörungen
Eine Einzeldosisstudie mit oraler Gabe von Aripiprazol bei Probanden mit verschiedengradiger Leberzirrhose (Child-Pugh-Klassen A, B und C) zeigte keine signifikante Wirkung hinsichtlich der Beeinträchtigung der Leberfunktion auf die Pharmakokinetik von Aripiprazol und Dehydro-Aripiprazol, aber die Studie umfasste nur 3 Patienten mit Leberzirrhose der Klasse C, was nicht ausreicht, um Schlüsse auf deren metabolische Kapazität zu ziehen.
Nierenfunktionsstörungen
In einer Einzeldosisstudie mit oraler Gabe von Aripiprazol wurde bezüglich der pharmakokinetischen Eigenschaften von Aripiprazol und Dehydro-Aripiprazol festgestellt, dass sie bei Patienten mit schweren Nierenerkrankungen im Vergleich zu denen von jungen gesunden Probanden ähnlich sind.
Ältere Patienten
Nach oraler Gabe von Aripiprazol gibt es keine Unterschiede in der Pharmakokinetik von Aripiprazol zwischen gesunden älteren und jüngeren erwachsenen Probanden. Ebenso zeigten sich bei der pharmakokinetischen Populationsanalyse von Aripiprazol bei schizophrenen Patienten keine altersabhängigen Wirkungen.
Genetische Polymorphismen
Langsame Metabolisierer für CYP2D6
Basierend auf einer pharmakokinetischen Populationsanalyse ist die Plasmakonzentration von Aripiprazol bei langsamen CYP2D6-Metabolisierern etwa 2-mal höher als bei normalen CYP2D6-Metabolisierern (für Dosierungsanweisungen siehe Dosierung / Anwendung).
| 
