Luveris® 75 IEWas ist Luveris und wann wird es angewendet?Luveris enthält luteinisierendes Hormon Lutropin alfa (r-hLH), welches mit dem natürlichen, im Menschen vorkommenden Hormon im Wesentlichen identisch ist, jedoch gentechnologisch hergestellt wird. Es gehört zu der Gruppe von Hormonen, die als Gonadotropine bezeichnet werden, welche u.a. die Funktionen der weiblichen Keimdrüsen (Eierstöcke) steuern und so an der normalen Kontrolle der Fortpflanzung beteiligt sind.
Die Verabreichung von Luveris erfolgt ausschliesslich auf ärztliche Verschreibung und unter strenger Überwachung durch Ihren Arzt bzw. Ihre Ärztin.
Luveris wird zur Behandlung von Frauen mit einem ein LH-Mangel, angewendet. Luveris wird zusammen mit einem anderen Hormon verabreicht, dem sogenannten follikelstimulierenden Hormon (FSH), um das Wachstum und die Entwicklung von Eizellen (Follikeln) herbeizuführen. Die Follikel sind Strukturen in den Eierstöcken, in denen die Eizellen heranreifen. Nach der Behandlung mit Luveris und FSH wird eine einzelne Dosis von humanem Choriongonadotropin (hCG) verabreicht, was zur Freisetzung einer Eizelle aus dem Follikel führt (Eisprung).
Was sollte dazu beachtet werden?Der Arzt bzw. die Ärztin wählt die für jede Patientin angemessene Behandlung aus. Befolgen Sie bitte gewissenhaft seine bzw. ihre Anweisungen und gehen Sie zu den Kontrolluntersuchungen.
Wann darf Luveris nicht angewendet werden?Luveris darf nicht angewendet werden,
·wenn Sie einen Gehirntumor (im Hypothalamus oder der Hirnanhangsdrüse) haben
·wenn Sie an vergrösserten Eierstöcken oder an Eierstockzysten (mit Flüssigkeit gefüllte Hohlräume im Gewebe der Eierstöcke) unbekannter Ursache leiden (ausgenommen gutartige mehrzystische Veränderungen der Eierstöcke)
·wenn Sie vaginale Blutungen unbekannter Ursache haben
·wenn Sie an Eierstock-, Gebärmutter- oder Brustkrebs erkrankt sind
·wenn Sie schwanger sind oder Ihr Kind stillen
·wenn Sie allergisch gegen luteinisierendes Hormon (LH) oder einen der sonstigen Inhaltsstoffe sind
Wann ist bei der Anwendung von Luveris Vorsicht geboten?Bevor mit der Behandlung begonnen wird, müssen die exakten Ursachen der Unfruchtbarkeit des Paares genau abgeklärt werden und Ursachen, die eine Schwangerschaft unmöglich machen wie z.B. Missbildungen der Geschlechtsorgane oder gutartige Tumore der Gebärmutter ausgeschlossen werden.
Ovarielles Überstimulationssyndrom (OHSS)
Auch wenn die strikte Einhaltung der empfohlenen Dosierung und der vorgeschriebenen Kontrolluntersuchungen das Risiko von Nebenwirkungen reduziert, darf das Risiko für das Entstehen eines Überstimulationssyndroms nicht ausser Acht gelassen werden. Dieses Syndrom äussert sich durch eine übermässige Vergrösserung der Eierstöcke und Symptome wie Unterleibsschmerzen, möglicherweise einhergehend mit Übelkeit, Erbrechen, Krankheitsgefühl, Atembeschwerden, Bauchschmerzen, Durchfall oder schneller Gewichtszunahme (siehe Welche Nebenwirkungen kann Luveris haben?).
Sehr selten sind Komplikationen wie Verdrehungen der Eierstöcke und Blutungen in den Bauchraum beobachtet worden.
Benachrichtigen Sie sofort Ihren Arzt bzw. Ihre Ärztin beim Auftreten der genannten Symptome
Wenn sich bei Ihnen die Entwicklung eines OHSS abzeichnet, sollte kein humanes Choriongonadotropin (hCG), ein weiteres Arzneimittel, welches auch eine wichtige Rolle bei der Fortpflanzung spielt, gegeben werden und Sie werden angewiesen für mindestens 4 Tage Geschlechtsverkehr zu vermeiden oder ein geeignetes Verhütungsmittel (Barrieremethoden) zu benutzen.
Das ovarielle Überstimulationssyndrom tritt in der Regel 1-2 Wochen nach der Verabreichung von hCG. Sein Schweregrad kann erheblich variieren.
Bei Frauen, die sich einer Behandlung zur Reifung mehrerer Follikel unterziehen, ist das Risiko eines ovariellen Überstimulationssyndroms grösser, kann jedoch durch Absaugen aller Follikel vor dem Eisprung reduziert werden.
Um das Risiko eines OHSS zu reduzieren, sollten Ultraschall- sowie Blutuntersuchungen (Estradiolbestimmung) durchgeführt werden.
Mehrlingsschwangerschaft
Das Risiko einer Mehrlingsschwangerschaft nach künstlicher Befruchtung hängt mit Ihrem Alter und der Anzahl transferierter Eizellen/Embryonen zusammen. Das Risiko einer Mehrlingsschwangerschaft bzw. Mehrlingsgeburt ist unter einer Behandlung zur Auslösung einesEisprunges höher als bei einer natürlichen Empfängnis. Das Risiko von Mehrlingsschwangerschaften kann durch die Einhaltung der empfohlenen Dosierung und des empfohlenen Therapieschemas verringert werden.
Ektope Schwangerschaft
Insbesondere bei Frauen mit einer früheren Eileitererkrankung, kann eine ektope Schwangerschaft auftreten, das heisst, der Embryo nistet sich ausserhalb der Gebärmutter ein.
Fehlgeburt
Bei der Anwendung von Verfahren zur künstlichen Befruchtung (IVF) oder der Stimulierung der Eierstöcke ist eine Fehlgeburt eher möglich als beim Durchschnitt der Frauen.
Missbildungen
Nach einer künstlichen Befruchtung (IVF) kann die Häufigkeit von Missbildungen etwas höher sein als nach einer natürlichen Empfängnis. Dies kann in Zusammenhang mit Risikofaktoren bei den Eltern wie das Alter der Mutter, die Erbveranlagung, die Anwendung der IVF und Mehrlingsschwangerschaften stehen.
Auftreten von Blutgerinnseln (thromboembolische Ereignisse)
Wenn Sie bekannte Risikofaktoren (Übergewicht, Rauchen, eigene oder Familienanamnese für solche Ereignisse) für das Auftreten von Blutgerinnseln in den grossen Blutgefässen (thromboembolische Ereignisse) haben, dann kann sich das Risiko während der Behandlung mit Luveris weiter erhöhen. Es ist jedoch anzumerken, dass eine Schwangerschaft selbst dieses Risiko ebenfalls erhöht (siehe Welche Nebenwirkungen kann Luveris haben?).
Tumore
Bei Frauen, die sich während mehreren Zyklen wegen Unfruchtbarkeit behandeln liessen, wurde über gutartige wie auch bösartige Tumoren der Eierstöcke oder anderer Fortpflanzungsorgane berichtet.
Porphyrie
Wenn Sie oder eines Ihrer Familienmitglieder an Porphyrie (eine Stoffwechselerkrankung, die von den Eltern auf die Kinder vererbt werden kann und bei der die Bildung des roten Blutfarbstoffes gestört ist) leiden, sollten Sie Ihren Arzt bzw. Ihre Ärztin vor Beginn der Behandlung informieren, da die Anwendung bestimmter Medikamente einen Anfall dieser Krankheit auslösen kann.
Wenn Sie bemerken, dass Ihre Haut verletzlich wird und schnell zur Blasenbildung neigt (besonders an Stellen, die häufig der Sonnenstrahlung ausgesetzt sind) und/oder Sie Bauch- oder Gliederschmerzen haben, informieren Sie bitte Ihren Arzt bzw. Ihre Ärztin. Er bzw. sie wird Ihnen gegebenenfalls empfehlen, die Behandlung abzusetzen.
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von Maschinen
Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und das Bedienen von Maschinen durchgeführt. Da nach der Anwendung von Luveris jedoch Schläfrigkeit und Schwindelgefühl auftreten kann, ist Vorsicht geboten, wenn Sie ein Fahrzeug lenken oder Maschinen bedienen.
Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro Dosis, d.h. es ist nahezu «natriumfrei».
Informieren Sie Ihren Arzt, Apotheker bzw. Ihre Ärztin, Apothekerin, wenn Sie
·an anderen Krankheiten leiden,
·Allergien haben oder
·andere Arzneimittel (auch selbst gekaufte!) einnehmen oder äusserlich anwenden!
Darf Luveris während einer Schwangerschaft oder in der Stillzeit angewendet werden?Sie dürfen Luveris nicht anwenden, wenn Sie schwanger sind oder Ihr Kind stillen.
Wie verwenden Sie Luveris?Ihr Arzt bzw. Ihre Ärztin passt die Behandlung mit Luveris individuell an und überwacht das Ansprechen. Deshalb dienen die nachfolgend aufgeführten Dosierungsangaben lediglich als Richtwerte. Befolgen Sie die Anweisungen Ihres Arztes bzw. Ihrer Ärztin genau.
Luveris wird unter die Haut (subkutan) gespritzt.
In der Regel wird Luveris für bis zu 3 Wochen lang gleichzeitig mit FSH täglich verabreicht. Bei Anwendung des üblichen Behandlungsschemas wird mit 75 IE (1 Durchstechflasche) Luveris zusammen mit 75 IE oder 150 IE FSH begonnen.
Je nach Ansprechen wird Ihr Arzt bzw. Ihre Ärztin die Dosis von Luveris auf bis zu 225 IE (3 Durchstechflaschen) und die Dosis von FSH um 37.5 – 75 IE in 7 bis 14-tägigen Intervallen erhöhen.
Wenn die gewünschte Reaktion erreicht ist, wird 24-48 Stunden nach den letzten Injektionen von Luveris und FSH einmalig ein anderes Hormon, humanes Choriongonadotropin (hCG) verabreicht. Sie sollten am Tag der Verabreichung von hCG und am darauffolgenden Tag Geschlechtsverkehr haben, alternativ kann eine intrauterine Insemination oder je nach Einschätzung Ihres Arztes/Ihrer Ärztin ein anderes Verfahren zur künstlichen Befruchtung durchgeführt werden.
Bei einer überschiessenden Reaktion ist die Behandlung zu beenden und kein hCG zu verabreichen (siehe Welche Nebenwirkungen kann Luveris haben?). Für den folgenden Zyklus wird Ihnen Ihr Arzt bzw. Ihre Ärztin eine niedrigere Dosis von FSH verschreiben als im vorherigen Zyklus.
Anwendung bei Kindern und Jugendlichen
Luveris darf bei Kindern und Jugendlichen nicht eingesetzt werden.
Anwendung bei älteren Patienten
Luveris darf bei älteren Patienten nicht eingesetzt werden.
Ändern Sie nicht von sich aus die verschriebene Dosierung. Wenn Sie glauben, das Arzneimittel wirke zu schwach oder zu stark, so sprechen Sie mit Ihrem Arzt oder Apotheker bzw. mit Ihrer Ärztin oder Apothekerin.
Anweisung für die Selbstanwendung
Wenn Sie die subkutanen Injektionen selbst anwenden möchten, ist eine Einführung in die praktische Durchführung durch Ihren Arzt bzw. Ihre Ärztin zwingend erforderlich, damit ein optimales Ansprechen auf Luveris gewährleistet ist und um Infektion vorzubeugen. Lesen Sie bitte die Anweisung am Ende dieser Packungsbeilage durch.
Wenn Sie eine grössere Menge von Luveris angewendet haben, als Sie sollten:
Die Auswirkungen einer Überdosierung von Luveris sind nicht bekannt, man kann aber annehmen, dass es zum Auftreten eines OHSS kommen kann. Dies wird jedoch erst dann eintreten, wenn hCG verabreicht wird (siehe Wann ist bei der Anwendung von Luveris Vorsicht geboten? und Welche Nebenwirkungen kann Luveris haben?).
Wenn Sie die Anwendung von Luveris vergessen haben:
Wenden Sie nicht die doppelte Dosis an, um vergessene Einzeldosen nachzuholen. Kontaktieren Sie bitte Ihren Arzt bzw. Ihre Ärztin.
Welche Nebenwirkungen kann Luveris haben?Folgende Nebenwirkungen können bei der Anwendung von Luveris zusammen mit FSH auftreten:
Häufig (betrifft 1 bis 10 von 100 Anwendern)
Infektionen des oberen Respirationstrakts, Kopfschmerzen, Schläfrigkeit, Schwindelgefühl, Bauchschmerzen, aufgeblähter Bauch, Übelkeit, Erbrechen, Durchfall, Beschwerden beim Wasserlösen, Unterleibsschmerzen, Brustschmerzen, Ovarialzysten, leichtes bis mässiges OHSS (siehe Warnhinweise und Vorsichtsmassnahmen), Reaktionen an der Injektionsstelle (Schmerzen, Rötung, Bluterguss, Schwellung und/oder Reizung), Schwächegefühl, Fieber.
Bei der Behandlung mit FSH und LH kann es, insbesondere wenn humanes Choriongonadotropin (hCG) verabreicht wurde, zu einem sogenannten ovariellen Überstimulationssyndrom (OHSS), kommen (siehe Wann ist bei der Anwendung von Luveris Vorsicht geboten?). Dieses Syndrom ist durch grosse Ovarialzysten charakterisiert. Die ersten Anzeichen einer ovariellen Überstimulation sind Unterleibsschmerzen, möglicherweise in Verbindung mit Übelkeit, Erbrechen, Krankheitsgefühl, Atembeschwerden, Bauchschmerzen, Durchfall und Gewichtszunahme. Sollten die o.g. Symptome auftreten, sollte so bald als möglich eine sorgfältige medizinische Untersuchung stattfinden.
Gelegentlich (betrifft 1 bis 10 von 1000 Anwendern)
Gelegentlich können grippeähnliche Symptome sowie ein schweres ovarielles Überstimulationssyndrom mit deutlich vergrösserten Ovarien, einer Flüssigkeitsansammlung im Bauch- oder Brustbereich auftreten.
Sehr selten (betrifft weniger als 1 von 10'000 Anwendern)
In sehr seltenen Fällen wurde über allergische Reaktionen berichtet, die Hautrötung, Hautausschlag, Schwellungen, Nesselsucht und Atembeschwerden verursachten. Diese Reaktionen können schwerwiegend sein. Wenn Sie diese Symptome beobachten, nehmen Sie unverzüglich mit Ihrem Arzt bzw. Ihrer Ärztin Kontakt auf. Schwerwiegende Komplikationen wie thromboembolische Ereignisse (Blutgerinnsel), gewöhnlich in Kombination mit einem OHSS, werden sehr selten beobachtet. Diese könnten Brustschmerzen, Atemlosigkeit, Hirnschlag oder einen Herzinfarkt zur Folge haben.
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt, Apotheker bzw. Ihre Ärztin, Apothekerin. Dies gilt insbesondere auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind.
Was ist ferner zu beachten?Das Arzneimittel darf nur bis zu dem auf dem Behälter mit «EXP» bezeichneten Datum verwendet werden.
Aufbrauchfrist nach Anbruch
Das Arzneimittel muss sofort nach der Auflösung des Pulvers angewendet werden.
Lagerungshinweis
Nicht über 25ºC lagern.
In der Originalverpackung aufbewahren.
Den Behälter im Umkarton aufbewahren, um den Inhalt vor Licht zu schützen.
Ausser Reichweite von Kindern aufbewahren.
Weitere Hinweise
Der Inhalt einer Durchstechflasche ist zum einmaligen Gebrauch bestimmt.
Sie dürfen das Arzneimittel nicht verwenden, wenn Sie sichtbare Anzeichen von Zersetzung bemerken wie Verfärbung des Pulvers oder Beschädigung der Behältnisse. Die Lösung darf nicht angewendet werden, wenn sie Partikel enthält, oder nicht klar ist.
Luveris darf, ausser mit Follitropin alfa, nicht mit anderen Arzneimitteln in einer Injektion gemischt werden. Allfällige nach Ende der Behandlung verbleibende Arzneimittel oder solche mit abgelaufenem Verfalldatum bitte zur fachgerechten Entsorgung Ihrer Verkaufsstelle (Arzt oder Apotheker bzw. Ärztin oder Apothekerin) übergeben.
Weitere Auskünfte erteilt Ihnen Ihr Arzt, Apotheker bzw. Ihre Ärztin, Apothekerin. Diese Personen verfügen über die ausführliche Fachinformation.
Was ist in Luveris enthalten?Pulver und Lösungsmittel zur Herstellung einer Injektionslösung. Subkutane (s.c.) Anwendung.
Wirkstoffe
Eine Durchstechflasche mit Pulver enthält 3.7 Mikrogramm Lutropin alfa (r-hLH aus gentechnisch veränderten Ovarialzellen des chinesischen Hamsters (CHO) hergestellt), entsprechend 75 IE (Internationale Einheiten).
Hilfsstoffe
Pulver: Saccharose, Natriummonohydrogenphosphat-Dihydrat, Natriumdihydrogenphosphat-Monohydrat, Polysorbat 20, Phosphorsäure, Natriumhydroxid, Methionin.
Lösungsmittel: 1 ml Wasser für Injektionszwecke.
Wo erhalten Sie Luveris? Welche Packungen sind erhältlich?In Apotheken gegen ärztliche Verschreibung, die nur zum einmaligen Bezug berechtigt.
Packungen mit 1 Durchstechflasche mit Pulver und 1 Durchstechflasche mit Lösungsmittel.
Zulassungsnummer55430 (Swissmedic)
ZulassungsinhaberinMerck (Schweiz) AG, Zug
Diese Packungsbeilage wurde im Dezember 2023 letztmals durch die Arzneimittelbehörde (Swissmedic) geprüft.Anweisungen zur Zubereitung und Verabreichung der Injektionslösung
1) Vorbereitungen vor der Injektion
·Waschen Sie sich die Hände. Es ist wichtig, dass Ihre Hände und die verwendeten Gegenstände, die Sie für die Injektion benötigen, so sauber wie möglich sind.
·Stellen Sie sich alles zusammen, was Sie brauchen und legen Sie alles auf eine saubere Fläche:
·eine Durchstechflasche mit Luveris
·eine Durchstechflasche mit Lösungsmittel
·zwei Alkoholtupfer
·eine Spritze
·eine Rekonstitutionsnadel zur Auflösung des Pulvers im Lösungsmittel
·eine feine Nadel für die subkutane Injektion
·einen Behälter zur sicheren Entsorgung von Glas und Nadeln
2) Vorbereitung des Lösungsmittels zur Rekonstitution
|
|
|
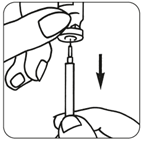
·Entfernen Sie die Schutzkappe von der Durchstechflasche mit dem Lösungsmittel.
·Befestigen Sie die Rekonstitutionsnadel an der Spritze und ziehen Sie etwas Luft in die Spritze auf, indem Sie den Spritzenkolben bis etwa zur 1-ml-Markierung herausziehen. Führen Sie anschliessend die Nadel in die Durchstechflasche ein und drücken Sie den Spritzenkolben herunter, um die Luft aus der Spritze auszustossen.
·Drehen Sie dann die Durchstechflasche um, und ziehen Sie behutsam die gesamte Lösungsmittelmenge in die Spritze auf.
·Legen Sie die Spritze vorsichtig auf die Arbeitsfläche und geben Sie acht, dass Sie die Nadel nicht berühren.
|
3) Vorbereitung der Injektionslösung
|
|
|
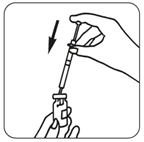
·Entfernen Sie die Schutzkappe von der Durchstechflasche mit Luveris.
·Nehmen Sie die Spritze mit dem Lösungsmittel auf und spritzen Sie das Lösungsmittel langsam in die Durchstechflasche mit Luveris (Pulver) ein.
·Schwenken Sie die Durchstechflasche behutsam, ohne dabei die Spritze zu entfernen. Nicht schütteln.
·Nachdem sich das Pulver aufgelöst hat, was in der Regel sofort eintritt, vergewissern Sie sich, dass die entstandene Lösung klar ist und keine Partikel enthält.
·Drehen Sie die Durchstechflasche um und ziehen Sie die Lösung wieder behutsam in die Spritze auf.
|
Es können bis zu 3 Durchstechflaschen Pulver in 1 ml Lösungsmittel aufgelöst werden.
4) Luftblasenkontrolle
|
|
|
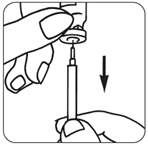
·Tauschen Sie die Nadel gegen die feine Nadel aus und entfernen Sie Luftblasen:
·Halten Sie die Spritze so, dass die Nadel nach oben zeigt, und klopfen Sie leicht mit den Fingern an die Spritze, bis sich die Luft an der Spitze ansammelt. Drücken Sie auf den Spritzenkolben, bis die Luftblasen verschwunden sind.
|
5) Injektion
|
|
|
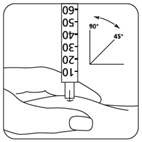
·Ihr Arzt bzw. Ihre Ärztin oder Ihr Pflegepersonal wird Ihnen den Injektionsbereich empfehlen (z.B. Bauch, vorderer Bereich der Oberschenkel).
·Desinfizieren Sie die Injektionsstelle mit einem Alkoholtupfer.
·Drücken Sie die Haut fest zusammen und stechen Sie die Nadel in einem 45-bis 90-Grad-Winkel mit einer schnelle, sicheren Bewegung in die Haut.
·Spritzen Sie die Lösung unter die Haut, wie man es Ihnen gezeigt hat.
·Spritzen Sie sich nicht direkt in eine Vene.
·Injizieren Sie die Lösung, indem Sie sanft auf den Spritzenkolben drücken. Nehmen Sie sich so viel Zeit, wie Sie benötigen, um die gesamte Lösung zu injizieren.
|
6) Nach der Injektion
·Ziehen Sie die Nadel sofort zurück und reiben Sie die Injektionsstelle kreisförmig mit dem Alkoholtupfer.
·Entsorgen Sie alle gebrauchten Gegenstände, Nadeln, leeren Glasbehältnisse und die Spritze in speziell dafür vorgesehene Behälter.
·Unverbrauchte Reste der Injektionslösung müssen verworfen werden.
Vorgehen, falls Ihnen Ihr Arzt oder Ihre Ärztin Luveris zusammen mit einem Follitropin alfa- Präparat verordnet hat:Sie können Luveris und Follitropin alfa zusammen mischen, anstatt jedes Präparat einzeln zu injizieren. Nachdem Sie das Pulver Luveris aufgelöst haben, ziehen Sie dazu die Lösung wieder in die Spritze auf und spritzen Sie sie in das Behältnis des Pulvers mit Follitropin alfa. Nachdem sich das Pulver aufgelöst hat, ziehen Sie die Lösung wieder in die Spritze auf. Prüfen Sie die Lösung wie zuvor auf Partikel, und benutzen Sie die Lösung nicht, wenn sie nicht klar ist.Nun ist die Mischinjektion bereit, dass Sie sie injizieren können.
|




