CompositionPrincipes actifs
Toxoïde diphtérique; toxoïde tétanique; toxoïde de la coqueluche (PT); hémagglutinine filamenteuse (HAF) de Bordetella pertussis; pertactine (PRN) de Bordetella pertussis; poliovirus inactivé de type 1 (souche Mahoney); poliovirus inactivé de type 2 (souche MEF-1); poliovirus inactivé de type 3 (souche Saukett).
Excipients
Hydroxyde d'aluminium hydraté, chlorure de sodium corresp. 1,8 mg de sodium, milieu 199, eau pour préparations injectables q.s. ad 0,5 mL.
Résidus
Sulfate de néomycine, sulfate de polymyxine B, polysorbate 80, formaldéhyde.
Indications/Possibilités d’emploiImmunisation de base
Infanrix DTPa-IPV est indiqué pour l'immunisation active contre la diphtérie, le tétanos, la coqueluche et la poliomyélite chez les enfants à partir de 2 mois.
Vaccinations de rappel
Infanrix DTPa-IPV convient pour la 4ème dose (1ère vaccination de rappel) chez les enfants dans leur 2ème année de vie qui ont reçu au préalable une immunisation de base avec un vaccin DTP et un vaccin polio.
Infanrix DTPa-IPV est indiqué pour la 5ème dose (= 2ème rappel) chez les enfants entre 4 et 7 ans (selon le plan de vaccination suisse).
Infanrix DTPa-IPV doit être administré selon les recommandations officielles de vaccination.
Posologie/Mode d’emploiPosologie usuelle
La dose entière recommandée de 0,5 mL doit être administrée.
Immunisation de base
Elle comporte trois vaccinations administrées à intervalles de 2 mois.
1ère dose à l'âge de 2 mois.
2ème dose à l'âge de 4 mois.
3ème dose à l'âge de 6 mois.
Vaccinations de rappel
La 4ème dose est administrée dans la 2ème année de vie (de préférence à l'âge de 15 à 18 mois), la 5ème dose à l'âge de 4 – 7 ans.
Mode d'administration
Infanrix DTPa-IPV doit être injecté par voie intramusculaire profonde. Chez les nourrissons, le site d'injection recommandé est la face antérolatérale de la cuisse. Chez les enfants plus âgés, l'injection doit être faite dans le muscle deltoïde.
Les vaccinations successives sont à effectuer de préférence dans le membre opposé.
Infanrix DTPa-IPV doit être administré avec prudence aux enfants présentant un trouble léger de la coagulation sanguine, car un saignement peut survenir chez ces personnes suite à une injection intramusculaire. Une pression constante (sans frotter) doit être exercée au site d'injection pendant au moins 2 minutes. Les enfants souffrant d'un trouble de la coagulation sanguine nécessitant un traitement par substitution, par ex. l'hémophilie, doivent recevoir la vaccination par voie intramusculaire en même temps ou juste après la substitution avec le facteur de coagulation correspondant. Les thrombocytopénies graves ≤ 50 000/µL représentent une contre-indication aux vaccinations intramusculaires. Dans ces cas, Infanrix DTPa-IPV doit être administré par voie sous-cutanée.
Contre-indicationsInfanrix DTPa-IPV ne doit pas être utilisé chez des enfants présentant une hypersensibilité connue à l'un des composants du vaccin (y compris hypersensibilité connue à la néomycine et à la polymyxine) ou chez des enfants qui ont présenté des signes d'hypersensibilité après une administration antérieure de vaccins contre la diphtérie, le tétanos, la coqueluche ou la polio.
Une vaccination par Infanrix DTPa-IPV est également contre-indiquée chez les sujets ayant présenté dans l'anamnèse vaccinale une encéphalopathie d'étiologie inconnue dans les 7 jours suivant une vaccination par un vaccin contre la coqueluche.
Comme pour les autres vaccins, la vaccination par Infanrix DTPa-IPV doit être différée chez les personnes atteintes d'affections fébriles, sévères, aiguës.
Une infection légère ne représente pas une contre-indication.
Mises en garde et précautionsInfanrix DTPa-IPV ne doit en aucun cas être administré par voie intravasculaire!
La vaccination doit être précédée d'un contrôle de l'anamnèse (principalement en ce qui concerne les vaccinations antérieures et d'éventuels effets secondaires) et d'un examen clinique.
Si la survenue de l'un des événements suivants est chronologiquement liée à l'administration d'une vaccination DTP, l'administration d'autres doses contenant des composants de la coqueluche devra être soigneusement évaluée:
·température ≥ 40,0°C dans les 48 heures, ne pouvant être attribuée à une autre cause;
·collapsus ou pseudo-état de choc (épisode d'hypotonie-hyporéactivité) dans les 48 heures;
·pleurs persistants, inconsolables, d'une durée supérieure à 3 heures, survenant dans les 48 heures après la vaccination;
·convulsions avec ou sans fièvre, survenant dans les 3 jours.
Comme pour toute vaccination, le rapport bénéfice-risque d'une vaccination par Infanrix DTPa-IPV ou d'un report de celle-ci chez un nourrisson ou un enfant souffrant d'une maladie neurologique sévère nouvelle ou évolutive, doit être évalué avec attention.
Dans certaines circonstances, p.ex. en cas d'incidence élevée de coqueluche, les bénéfices potentiels de la vaccination peuvent l'emporter sur les risques éventuels, surtout lorsque ces événements ne s'accompagnent pas de séquelles permanentes.
Des antécédents de convulsions fébriles ou des antécédents familiaux de crises convulsives ou de mort subite du nourrisson (SIDS) ne représentent pas une contre-indication à la vaccination par Infanrix DTPa-IPV.
Chez les enfants recevant un traitement immunosuppresseur (corticothérapie, chimiothérapie antimitotique, etc.), la vaccination par Infanrix DTPa-IPV doit être différée jusqu'à la fin du traitement.
Une infection à VIH ne représente pas une contre-indication à la vaccination par Infanrix DTPa-IPV. Il se peut chez ces patients qu'une réponse immunitaire adéquate ne soit pas obtenue après la vaccination par DTPa-IPV.
Comme pour tous les vaccins injectables, un traitement médical approprié doit toujours être à disposition pour le cas où surviendrait une réaction anaphylactique après la vaccination.
Infanrix DTPa-IPV doit être administré avec précaution chez des enfants présentant une thrombocytopénie ou un trouble de la coagulation en raison du risque d'hémorragie chez ces enfants après une administration intramusculaire.
Le risque potentiel d'apnées et la nécessité d'une surveillance respiratoire pendant 48 - 72 heures doivent être pris en considération dans le cadre de la vaccination de base des grands prématurés (nés avant la fin de la 28ème semaine de grossesse) et en particulier de ceux ayant des antécédents de signes d'immaturité pulmonaire. Le bénéfice de la vaccination étant élevé chez ces nourrissons, celle-ci ne doit pas leur être refusée ni être reportée.
Une syncope (évanouissement) peut survenir après toute vaccination, voire même avant, en particulier chez les adolescents, comme réaction psychogène à l'injection. Ceci peut s'accompagner de plusieurs signes neurologiques comme un trouble transitoire de la vision, des paresthésies et des mouvements tonico-cloniques des membres durant la phase de récupération. Il est important que des mesures soient mises en place afin d'éviter des blessures en cas d'évanouissement.
Ce médicament contient moins de 1 mmol de sodium (23 mg) par dose de vaccin, c.-à-d. qu'il est pratiquement «sans sodium».
InteractionsDans des études cliniques, Infanrix DTPa-IPV a été utilisé en même temps qu'un vaccin rougeole-oreillons-rubéole ou qu'un vaccin Hib. Les données disponibles ne suggèrent aucune interférence cliniquement significative dans la réponse immunitaire (anticorps) à chaque antigène.
Des études d'interaction avec d'autres vaccins, produits biologiques ou médicaments n'ont pas été effectuées. Infanrix DTPa-IPV étant un produit inactivé et conformément aux directives globalement applicables pour l'immunisation, il n'existe aucune raison théorique interdisant une administration d'Infanrix DTPa-IPV en même temps que d'autres vaccins ou immunoglobulines en utilisant des sites d'injection différents.
Comme avec d'autres vaccins, une réponse immunitaire adéquate peut ne pas être obtenue chez les patients traités par des immunodépresseurs ou présentant un déficit immunitaire.
Lorsque l'on vaccine un enfant, il est habituel d'effectuer simultanément plusieurs vaccinations. Dans ce cas, il faut toujours choisir des sites d'injection différents.
Grossesse, allaitementComme Infanrix DTPa-IPV n'est pas destiné à être employé chez les adultes, on ne dispose d'aucune donnée sur la sécurité du vaccin pendant la grossesse et l'allaitement.
Effet sur l’aptitude à la conduite et l’utilisation de machinesOn admet qu'Infanrix DTPa-IPV ne sera que rarement administré à des personnes qui conduisent des véhicules ou manipulent des machines. Il existe cependant de nombreux rapports de somnolence à la suite d'une vaccination. Cela peut affecter transitoirement l'aptitude à la conduite et à l'utilisation de machines.
Effets indésirablesEtudes cliniques
Le profil de sécurité suivant repose sur les données de plus de 2'200 personnes.
Les fréquences déterminées sont indiquées comme suit: «très fréquent» (≥1/10), «fréquent» (≥1/100 à <1/10), «occasionnel» (≥1/1000 à <1/100), «rare» (≥1/10 000 à < 1/1000), «très rare» (< 1/10 000).
Comme observé avec les vaccins DTPa et les vaccins contenant les composants DTPa, une augmentation de la réactogénicité locale et de la fièvre a été rapportée après la vaccination de rappel en comparaison à la vaccination de base.
Affections hématologiques et du système lymphatique
Rares: lymphadénopathie1.
Troubles du métabolisme et de la nutrition
Très fréquents: perte d'appétit (après vaccination de base: 10,8%; après vaccination de rappel: 14,8%).
Affections psychiatriques
Très fréquents: irritabilité (vaccination de base: 46,9%; vaccination de rappel: 20,1%), agitation (vaccination de base: 26,7%; vaccination de rappel: 21,5%), cris inhabituels (vaccination de base: 14,1%; vaccination de rappel: 12,6%).
Affections du système nerveux
Très fréquents: céphalées1 (enfants de 6 à 13 ans; vaccination de rappel: 25,0%), somnolence (vaccination de base: 32,7%; vaccination de rappel: 22,1%).
Affections respiratoires, thoraciques et médiastinales
Occasionnels: bronchite2, toux2.
Affections gastro-intestinales
Fréquents: nausées1, vomissements, diarrhée.
Occasionnels: douleurs abdominales.
Affections de la peau et du tissu sous-cutané
Occasionnels: dermatite allergique, éruption cutanée2,3.
Rares: urticaire, prurit.
Troubles généraux et anomalies au site d'administration
Très fréquents: douleurs (vaccination de base: 15,2%; vaccination de rappel: 46,4%), rougeur (vaccination de base: 40,1%; vaccination de rappel: 49,0%), tuméfaction locale au site d'injection (≤50 mm, vaccination de base: 23,7%; vaccination de rappel: 39,8%), fièvre (≥38,0°C, vaccination de base: 10,3%; rappel: 21,5%).
Fréquents: malaise1, gonflement du membre entier autour du site d'injection (> 50 mm)4, asthénie, réactions au site d'injection y compris induration, gonflement diffus du membre où l'injection a été faite, s'étendant parfois jusqu'à l'articulation la plus proche4, fièvre5 (> 39,5°C).
Effets indésirables identifiés après la mise sur le marché
Affections hématologiques et du système lymphatique
Thrombocytopénie6.
Affections du système immunitaire
Réactions allergiques, y compris réactions anaphylactiques2 et anaphylactoïdes.
Affections du système nerveux
Collapsus ou état ressemblant à un choc (épisode hypotonique-hyporéactif), convulsions avec ou sans fièvre dans les 2 à 3 jours suivant la vaccination.
Affections respiratoires, thoraciques et médiastinales
Apnée2.
Affections de la peau et du tissu sous-cutané
Prurit, œdème angioneurotique2.
Troubles généraux et anomalies au site d'administration
Gonflement de tout le membre4 où l'injection a été faite, vésicules au site d'injection.
1 Rapporté uniquement après la vaccination de rappel.
2 Rapporté avec des vaccins de GlaxoSmithKline contenant DTPa.
3 Rapporté occasionnellement après la vaccination de rappel.
4 Les enfants ayant reçu pour la vaccination de base des vaccins contenant une composante anticoquelucheuse acellulaire ont une probabilité plus élevée de développer un gonflement après la vaccination de rappel en comparaison avec les enfants ayant reçu une vaccination de base avec une composante anticoquelucheuse à germes entiers. Un gonflement localisé au site d'injection (> 50 mm) et un gonflement diffus peuvent se produire plus souvent (très fréquemment et fréquemment) si la dose de rappel est administrée à un âge de 4 à 6 ans.Des informations concernant les gonflements diffus du membre entier autour du site d'injection après la vaccination par Infanrix DTPa-IPV (définis comme un gonflement d'un diamètre > 50 mm avec gonflement diffus visible ou augmentation visible de la circonférence du membre en question) ont été recueillies dans deux études cliniques: Lors de l'administration d'Infanrix DTPa-IPV en tant que 4ème ou 5ème dose de vaccin DTPa à des enfants de 4 à 6 ans, un gonflement massif (> 50 mm) au site d'injection est survenu chez les sujets vaccinés avec une incidence respective de 13% et de 25%. Cette réaction s'est manifestée le plus souvent sous la forme de gonflements localisés massifs (diamètre > 50 mm) au site d'injection. Respectivement 3% et 6% des sujets vaccinés ont présenté des gonflements diffus de tout le membre ayant reçu le vaccin, s'étendant parfois jusqu'aux articulations les plus proches. Ces réactions ont généralement commencé dans les 48 heures suivant la vaccination et régressé sans séquelles en l'espace de 4 jours.
5 Rapporté fréquemment après la vaccination de rappel.
6 Rapporté après l'administration de vaccins antidiphtériques et antitétaniques.
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageDes cas de surdosage ont été rapportés dans le cadre de la surveillance post-commercialisation. Lorsque des effets indésirables ont été rapportés, ceux-ci n'étaient pas de nature particulière, mais semblables aux effets indésirables rapportés dans le cadre de l'utilisation normale d'un vaccin.
Propriétés/EffetsCode ATC
J07CA02 (vaccin bactérien et viral combiné)
Infanrix DTPa-IPV contient l'anatoxine diphtérique, l'anatoxine tétanique et trois antigènes purifiés de Bordetella pertussis [anatoxine pertussique (PT), hémagglutinine filamenteuse (HAF) et pertactine (la protéine membranaire externe pesant 69 kilodaltons (kDa) PRN)], qui sont adsorbés sur de l'hydroxyde d'aluminium. Il contient également trois types du virus de la poliomyélite inactivé (type 1: Mahoney; type 2: MEF-1; type 3: Saukett).
Les toxines de la diphtérie et du tétanos sont obtenues à partir de cultures de Corynebacterium diphtheriae et de Clostridium tetani, puis les toxines sont détoxifiées et purifiées. Les composants acellulaires du vaccin contre la coqueluche (PT, HAF et PRN) sont obtenus à partir de bactéries Bordetella pertussis à partir desquelles les antigènes PT, HAF et PRN sont extraits, purifiés et irréversiblement détoxifiés.
Les trois types du virus de la poliomyélite sont cultivés dans une lignée continue de cellules VERO, purifiés et inactivés par le formaldéhyde.
Les anatoxines diphtérique et tétanique et les composants du vaccin acellulaire contre la coqueluche sont adsorbés sur de l'hydroxyde d'aluminium. Le vaccin fini se présente dans une solution de NaCl.
Infanrix DTPa-IPV est conforme aux exigences de l'OMS en matière de fabrication de produits biologiques, de vaccins contre la diphtérie, le tétanos, la coqueluche et de vaccins inactivés contre la poliomyélite.
Mécanisme d'action
Non pertinent.
Pharmacodynamique
Réponse immunitaire au composant DTPa après l'immunisation de base et la 1ère vaccination de rappel (= 4ème dose) dans la 2ème année de vie
Un mois après une immunisation de base avec trois doses d'Infanrix DTPa-IPV (à l'âge de 2, 4 et 6 mois), plus de 99% des enfants présentaient des titres d'anticorps ≥ 0,1 UI/mL contre la diphtérie et le tétanos. Après l'administration d'une 1ère vaccination de rappel, le nombre d'enfants a augmenté à 99,5%.
Après 3 doses, 100% des enfants étaient séropositifs pour les trois composants de la coqueluche (PT, HAF, PRN) et les réponses immunitaires pour les trois composants se situaient à 98,4% (PT), 97,7% (HAF) et 97,3% (PRN).
Après la 1ère vaccination de rappel, des réponses immunitaires ont été observées chez 97,6%, 99% et 98,5% des enfants vaccinés pour les antigènes de la coqueluche. Tous étaient séropositifs un mois après la 4e dose.
Réponse immunitaire au composant DTPa après la 2ème vaccination de rappel
Un mois après une vaccination de rappel avec une dose d'Infanrix DTPa-IPV chez des enfants entre 5 et 6 ans, 100% des enfants présentaient des anticorps protecteurs ≥ 0,1 UI/mL contre la diphtérie et le tétanos. Les réponses immunitaires pour les trois composants de la coqueluche se situaient à 95,4% (PT), 100% (HAF) et 100% (PRN).
Réponse immunitaire au composant IPV après l'immunisation de base et la 1ère vaccination de rappel (= 4ème dose) dans la 2ème année de vie
Un mois après une immunisation de base avec trois doses d'Infanrix DTPa-IPV (à l'âge de 2, 4 et 6 mois), plus de 99,5% des enfants étaient séropositifs pour les 3 sérotypes (1, 2 et 3).
Après l'administration d'une vaccination de rappel dans la deuxième année de vie (13 - 24 mois), tous les enfants qui avaient reçu auparavant l'immunisation de base étaient séropositifs pour les trois types.
Réponse immunitaire du composant IPV après la 2ème vaccination de rappel
Un mois après une vaccination de rappel avec une dose d'Infanrix DTPa-IPV chez des enfants entre 5 et 6 ans, la réponse immunitaire se situait à 95,8% (sérotype 1), 95,7% (sérotype 2) et 91,3% (sérotype 3).
Aucun corrélat sérologique n'a été défini pour l'effet des antigènes coquelucheux. Les titres d'anticorps obtenus avec les trois composants anticoquelucheux ont été supérieurs dans tous les cas aux titres observés après la vaccination de base avec le vaccin combiné à composant anticoquelucheux acellulaire pour enfants (DTPa, Infanrix). L'efficacité de celui-ci a été démontrée dans une étude d'exposition en milieu familial. Sur la base de ces comparaisons, on peut supposer qu'Infanrix DTPa-IPV offre une protection contre la coqueluche, bien que le degré et la durée de l'effet du vaccin restent indéterminés.
Efficacité clinique
Voir sous «Pharmacodynamique».
PharmacocinétiqueL'évaluation des propriétés pharmacocinétiques n'est pas requise pour les vaccins.
Absorption
Non pertinent.
Distribution
Non pertinent.
Métabolisme
Non pertinent.
Élimination
Non pertinent.
Données précliniquesNon pertinent.
Remarques particulièresIncompatibilités
Infanrix DTPa-IPV ne doit pas être mélangé à d'autres vaccins dans la même seringue, à l'exception d'Hiberix.
Conservation
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur l'emballage.
Remarques particulières concernant le stockage
Conserver au réfrigérateur (2-8°C), à l'abri de la lumière dans l'emballage d'origine et hors de portée des enfants.
Ne pas congeler! Tout vaccin congelé doit être jeté.
Au cours du stockage, un dépôt blanc et un surnageant limpide peuvent être observés.
Remarques concernant la manipulation
Le vaccin doit être bien agité avant utilisation afin d'obtenir une suspension trouble blanche homogène. La suspension doit en outre être examinée pour détecter la présence de toute particule étrangère et/ou altération de l'aspect physique. En cas de modification, jeter le vaccin.
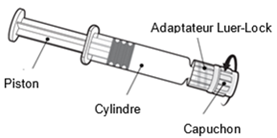
Mode d'emploi de la seringue préremplie:
|
|
|
Tenez la seringue par le cylindre, pas par le piston.
Dévissez le capuchon de la seringue en le tournant dans le sens inverse des aiguilles d'une montre.
| |
|
|
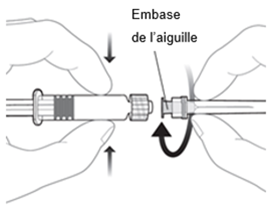
Pour fixer l'aiguille à la seringue, connectez l'embase de l'aiguille à l'adaptateur Luer-Lock et tournez l'aiguille d'un quart de tour dans le sens des aiguilles d'une montre jusqu'à ce que vous sentiez qu'elle s'enclenche.
Ne tirez pas le piston de la seringue hors du cylindre. Si cela se devait se produire, n'administrez pas le vaccin.
|
Les résidus de vaccin non utilisés et les déchets doivent être éliminés conformément aux exigences nationales.
Numéro d’autorisation00638 (Swissmedic)
PrésentationEmballage avec une seringue préremplie et une aiguille fournie séparément [B].
Titulaire de l’autorisationGlaxoSmithKline AG, 6340 Baar
Mise à jour de l’informationJuillet 2023
|


