CompositionPrincipe actif: Phospholipida e pulmone suis 80 mg/ml (soit 120 mg pro 1,5 ml).
Excipients: Natrii chloridum 9 mg/ml (soit 13,5 mg pro 1,5 ml), aqua ad suspensionem pro 1,5 ml.
Curosurf est un surfactant naturel préparé à partir de poumons de porc, contenant presque exclusivement des phospholipides dont environ 70% de phosphatidylcholine et près de 1% de protéines hydrophobes spécifiques à faible poids moléculaire (SP-B et SP-C).
Forme galénique et quantité de principe actif par unitéSuspension stérile avec 120 mg de surfactant par ampoule à 1,5 ml (80 mg/ml) pour l'instillation endotrachéopulmonaire.
Indications/Possibilités d’emploiTraitement de prématurés présentant un syndrome de détresse respiratoire (SDR) consécutif à une carence en surfactant ou présentant un risque élevé de développer un tel syndrome.
Posologie/Mode d’emploiProphylaxie et traitement
Une dose unique de 100-200 mg/kg de poids corporel (1,25-2,5 ml/kg) sera administrée par voie intratrachéale le plus rapidement possible après la naissance (de préférence dans les 15 premières minutes) en cas de risque élevé ou de signes d'un SDR consécutif à une carence en surfactant.
Il est possible d'administrer des doses supplémentaires de 100 mg/kg de poids corporel (1,25 ml/kg) dans l'intervalle de 6 à 12 heures après la première administration et de 12 heures après la seconde administration à des nouveaux-nés sous ventilation assistée présentant des signes persistants de SDR. La dose maximale s'élève à 300-400 mg/kg.
Curosurf ne doit être utilisé que dans un hôpital avec des médecins expérimentés dans le traitement, la réanimation et la stabilisation de prématurés.
Curosurf est administré par voie endotrachéopulmonaire aux nouveaux-nés dont la fréquence cardiaque et la concentration artérielle d'oxygène ou la saturation en oxygène sont continuellement surveillées, comme c'est normalement possible dans les services de néonatologie (voir sous «Mises en garde et précautions»).
Remarques concernant la manipulation
Préparation
Avant utilisation, l'ampoule doit être chauffée à température ambiante (15-25 °C) – p.ex. en la tenant dans la main pendant quelques minutes – et retournée plusieurs fois de haut en bas, avec précaution et sans l'agiter, pour obtenir une suspension uniforme.
Application
La suspension doit être extraite de l'ampoule en utilisant une seringue stérile à aiguille fine.
Pour extraire la suspension, veuillez vous conformer aux instructions suivantes:
1. Localisez l'encoche sur le capuchon en plastique de couleur (FLIP

UP).
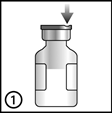
2. Soulevez l'encoche et tirez-la vers le haut.
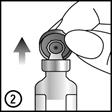
3. Tirez le capuchon en plastique avec le bouchon en aluminium vers le bas.
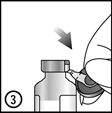
4. et 5. Enlevez la totalité de l'anneau en aluminium.
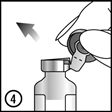
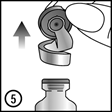
6. et 7. Enlevez le bouchon en caoutchouc pour extraire le contenu.
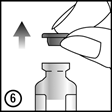
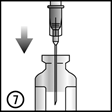
Curosurf peut être administré comme suit.
a) En séparant l'enfant du respirateur:
Après une interruption momentanée de la ventilation mécanique, Curosurf 1,25-2,5 ml/kg (100-200 mg/kg) est instillé en bolus via une sonde endotrachéale par voie intratrachéale en profondeur.
Après une brève ventilation manuelle au ballon pendant environ 1 minute, l'enfant est à nouveau branché au respirateur, avec dans un premier temps les mêmes paramètres de réglage que ceux qui étaient utilisés avant l'administration de Curosurf.
D'autres doses (1,25 ml/kg) peuvent être administrées de la même façon.
b) Sans séparer l'enfant du respirateur:
Curosurf 1,25-2,5 ml/kg (100-200 mg/kg) est instillé en une seule dose via la sonde endotrachéale à travers le port d'aspiration. D'autres doses (1,25 ml/kg) peuvent être administrées de la même façon.
c) Comme troisième option directement dans la salle d'accouchement, on administre Curosurf à travers la sonde endotrachéale avant que ne débute la ventilation manuelle au ballon. L'extubation et l'utilisation consécutive d'un CPAP est une option envisageable, soit dans la salle d'accouchement ou plus tard après le transfert dans le service de néonatologie (INtubation SURfactant Extubation – INSURE).
d) Administration moins invasive de surfactant avec un cathéter fin (Less Invasive Surfactant Administration (LISA))
Il est également possible, chez les prématurés qui respirent spontanément, d’administrer le Curosurf par la technique LISA à l'aide d'un cathéter fin. Les doses sont les mêmes que celles indiquées pour les modes d’emploi visés aux points a), b) et c). Un cathéter de petit diamètre est placé dans la trachée des nourrissons sous CPAP, assurant une respiration spontanée continue, avec une visualisation directe des cordes vocales par laryngoscopie. Le Curosurf est instillé par un seul bolus pendant 0,5-3 minutes. Après l'instillation du Curosurf, le tube est immédiatement retiré. Le traitement par CPAP doit être poursuivi pendant toute la procédure.
Des catheters fins portant le marquage CE et dédiés à cette utilisation doivent être choisis pour l’administration du surfactant.
Afin d'assurer la traçabilité des médicaments biotechnologiques, il convient de documenter pour chaque traitement le nom commercial et le numéro de lot.
Contre-indicationsHypersensibilité au principe actif ou à l'un des excipients.
Mises en garde et précautionsUn surfactant exogène, y compris Curosurf, peut provoquer une chute de la saturation en oxygène, une détérioration de la distensibilité pulmonaire, une bradycardie, une hypotension, et obstruer la sonde. C'est pourquoi Curosurf ne doit être utilisé qu'en clinique par des médecins qui sont formés et expérimentés dans le suivi et la réanimation de prématurés. Des installations de ventilation et de surveillance adéquates pour les prématurés atteints de SDR doivent être disponibles.
Avant le début du traitement avec Curosurf, il faut stabiliser les fonctions vitales du prématuré. Il est également recommandé de corriger l'acidose, l'hypotension, l'anémie, l'hypoglycémie et l'hypothermie.
Si un reflux apparaît, il faut interrompre l'administration de Curosurf et, si nécessaire, augmenter la pression de ventilation (PIP) jusqu'à ce que la sonde endotrachéale soit libérée.
Chez les nouveaux-nés dont la ventilation est soudain nettement entravée pendant ou juste après l'administration, on est éventuellement en présence d'un bouchon muqueux dans la sonde endotrachéale, notamment quand la sécrétion pulmonaire était déjà importante avant l'administration. L'aspiration des nouveaux-nés avant l'administration peut réduire la probabilité de la formation de bouchons muqueux. Si on soupçonne une obstruction de la sonde endotrachéale et que la sonde ne peut pas être libérée par aspiration, il faut immédiatement changer la sonde endotrachéale.
Toutefois, une aspiration des sécrétions trachéales pendant au moins 6 heures après l'administration n'est pas recommandée, sauf en cas de situation potentiellement mortelle.
Si des épisodes de bradycardie, d'hypotension ou de saturation en oxygène réduite surviennent (voir sous «Effets indésirables»), l'administration de Curosurf doit être interrompue et des mesures correspondantes pour normaliser la fréquence cardiaque doivent être envisagées et exécutées. Après sa stabilisation, le nouveau-né peut être traité sous surveillance des fonctions vitales.
Après l'administration de Curosurf, la distensibilité pulmonaire et l'approvisionnement en oxygène peuvent rapidement s'améliorer, si bien que le réglage de l'appareil respiratoire doit immédiatement être adapté.
L'amélioration de l'échange gazeux alvéolaire peut provoquer une augmentation subite de la concentration artérielle d'oxygène, ce qui peut exiger un réglage immédiat de la ventilation pour éviter une hyperoxie. Pour maintenir une concentration d'oxygène dans le sang adéquate, il est recommandé, en plus de l'analyse périodique des gaz du sang, de surveiller en continu la PaO2 transcutanée ou la saturation en oxygène.
nCPAP (nasal continuous positive airway pressure) peut être utilisé dans les services qui sont équipés de cette technique pour poursuivre le traitement.
Toutefois, il convient de ne pas cesser brusquement l'assistance respiratoire pour ne pas accroître le risque d'apnée.
Les enfants traités par un surfactant doivent être contrôlés soigneusement sur des signes d'infections. Lors de la survenue des premiers signes infectieux, les enfants doivent être traités immédiatement par une antibiothérapie spécifique.
En cas de réponse insuffisante au traitement avec Curosurf ou d'une rechute rapide, il faut envisager d'autres complications liées à l'immaturité comme un canal artériel ouvert ou d'autres maladies pulmonaires comme la pneumonie avant d'administrer la dose suivante.
La réponse au traitement avec un surfactant exogène peut ne pas être optimale chez les nouveaux-nés ayant souffert d'une rupture des membranes ancienne (il y a plus de 3 semaines), étant donné qu'ils peuvent être atteints d'une certaine hypoplasie pulmonaire.
Avant d'administrer un surfactant, on peut s'attendre à une baisse du degré de gravité du syndrome de détresse respiratoire. Toutefois, on ne peut pas s'attendre à éliminer totalement le risque de mortalité et de morbidité inhérent à la prématurité. Les enfants qui ont survécu grâce à l'application de Curosurf restent exposés à d'autres complications en rapport avec leur immaturité.
Après l'administration de Curosurf, un ralentissement passager de l'activité cérébro-corticale d'une durée de 2 à 10 minutes a été observée. Cela n'a cependant été observé que dans une seule étude et les répercussions ne sont pas claires.
L'utilisation de Curosurf chez des prématurés atteints d'hypotension sévère n'a pas été étudiée à ce jour.
Lorsque le Curosurf est administré avec la technique LISA, une augmentation de la fréquence de bradycardies, d'apnées et de réductions de la saturation en oxygène ont été signalées. Ces événements sont généralement de courte durée, sans conséquences pendant l'administration et faciles à gérer. Si ces événements deviennent graves, arrêtez le traitement par surfactant et traitez les complications.
InteractionsAucune étude d'interaction n'est disponible.
Grossesse, allaitementSans objet.
Effet sur l’aptitude à la conduite et l’utilisation de machinesSans objet.
Effets indésirablesLes effets indésirables qui ont été observés pendant le traitement dans le cadre d'études cliniques, associés à ceux de la phase post-marketing, sont classés ci-dessous selon le système de classes d'organe MedDRA avec indication des fréquences suivantes:
très fréquents (≥1/10), fréquents (≥1/100, <1/10), occasionnels (≥1/1'000, <1/100), rares (≥1/10'000, <1/1'000), très rares (<1/10'000), inconnus (ne peuvent pas être évalués sur la base des données disponibles).
Infections
Occasionnels: septicémie.
Système nerveux
Occasionnels: hémorragies intracrâniennes.
Troubles cardiaques
Rares: bradycardie.
Troubles vasculaires
Rares: hypotension.
Organes respiratoires
Occasionnels: pneumothorax.
Rares: dysplasie bronchopulmonaire, hémorragies pulmonaires.
Inconnus: hyperoxie, cyanose néonatale, apnée.
Investigations
Rares: saturation en oxygène réduite.
Inconnus: anormalités dans l'électroencéphalogramme.
Lésions, empoisonnements et complications en relation avec la procédure
Inconnus: complications liées à l'intubation endotrachéale.
L'apnée et la septicémie peuvent survenir comme conséquence de l'immaturité du nouveau-né.
L'apparition d'hémorragies intracrâniennes après l'administration de Curosurf a été imputée à une réduction de la pression artérielle moyenne et à des pics précoces dans la concentration artérielle d'oxygène (PaO2). Il est recommandé d'éviter les pics élevés de PaO2 en adaptant la ventilation mécanique immédiatement après l'instillation.
Les études cliniques menées à ce jour ont montré une incidence plus élevée de persistance du canal artériel ouvert chez les enfants traités par un surfactant.
La formation d'anticorps contre les composants protéiniques de Curosurf a été observée, mais il n'existe jusqu'ici aucun signe d'une pertinence clinique.
Les prématurés présentent une incidence relativement élevée d'hémorragies cérébrales, d'ischémie cérébrale, rapportée comme leucomalacie péri-ventriculaire, et d'anomalies hémodynamiques telles qu'un canal artériel ouvert ainsi que la persistance de la circulation fœtale. Ces nouveaux-nés présentent également un risque élevé de développer des infections comme la pneumonie et la bactériémie (ou septicémie). Des crises convulsives peuvent également apparaître durant la période périnatale. Les prématurés peuvent aussi fréquemment développer des troubles sanguins ou de l'équilibre électrolytique qui peuvent être aggravés par des maladies graves ou par la ventilation mécanique.
Pour compléter le tableau des complications qui peuvent survenir chez les prématurés, on citera les états suivants qui sont directement liés au degré de gravité de la maladie et à la ventilation mécanique nécessaire à la réoxygénation: pneumothorax, emphysème pulmonaire interstitiel et hémorragies pulmonaires.
L'utilisation de longue durée de concentrations d'oxygène élevées et la ventilation mécanique sont également associées à l'apparition de la dysplasie broncho-pulmonaire et de la rétinopathie du prématuré.
La technique LISA
Lors des essais cliniques, certains effets indésirables transitoires et légers, sans conséquences pendant l'administration, ont été plus fréquents dans les groupes LISA que dans les groupes contrôles du traitement standard; en particulier: désaturation en oxygène (57,4% groupe LISA vs 26,6 % groupe contrôle), apnée (21,8% vs 12,8%), bradycardie (11,9% vs 2,8%), écume à la bouche (21,8 vs 2,8%), toux (7,9 vs 0,9%), étouffement (6,9% vs 1,8%) et éternuements (5% vs 0). Cette différence entre les deux groupes pourrait être justifiée par l'utilisation moins fréquente de la sédation dans les groupes LISA par rapport au traitement standard.
La majorité de ces événements ont été facilement pris en charge.
Au cours d'un essai clinique comparatif spontané (NINSAPP), des cas d'entérocolite nécrosante nécessitant une intervention chirurgicale (8,4% dans le groupe avec la méthode LISA et 3,8% dans le groupe avec la méthode standard d'administration-intubation/MV) et de perforation interstitielle focale nécessitant une intervention chirurgicale (11,2% dans le groupe LISA et 10,6% dans le groupe standard) ont été signalés, sans différence statistiquement significative entre les groupes.
Ces événements pourraient représenter des complications de la prématurité ou des conséquences d'autres traitements utilisés chez ces bébés prématurés.
L’annonce d’effets secondaires préumé aprè l’autorisation est d’une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d’effet secondaire nouveau ou grave via le portail d’annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageAucun effet d'un surdosage de Curosurf n'est connu à ce jour. En cas de surdosage accidentel, la suspension devra être aspirée et le bébé sera mis sous surveillance toute particulière en ce qui concerne l'équilibre hydro-électrolytique.
Propriétés/EffetsCode ATC: R07AA02
Mécanisme d'action
Le surfactant pulmonaire est un mélange de substances contenant principalement des phospholipides et des protéines spécifiques, qui recouvre la surface interne des alvéoles et abaisse la tension superficielle dans les poumons. Cette activité diminuant la tension superficielle stabilise les alvéoles et prévient ainsi l'affaissement à la fin de la phase d'expiration, ce qui assure un échange gazeux adéquat pendant le cycle de respiration.
Un déficit en surfactant, de n'importe quelle origine, entraîne une insuffisance respiratoire sévère connue sous le nom de syndrome de détresse respiratoire (SDR) ou maladie des membranes hyalines (MMH) chez les prématurés. Le SDR est la principale cause de mortalité et de morbidité aiguës chez les prématurés et peut avoir des conséquences respiratoires et neurologiques.
Curosurf a été développé pour remplacer le surfactant pulmonaire endogène, en cas de déficience, par administration de surfactant exogène dans les voies respiratoires basses. Les propriétés tensioactives de Curosurf favorisent sa distribution uniforme dans les poumons et sa répartition à l'interface air-liquide des alvéoles.
Efficacité clinique
Chez les enfants présentant un SDR et un poids à la naissance compris entre 700 et 2000 g et lors d'un traitement instauré au plus tard 48 h après le diagnostic, l'efficacité thérapeutique de Curosurf est mise en évidence dans des études internationales d'envergure. Ainsi, des prématurés traités par Curosurf ont montré une amélioration marquée et rapide de l'échange gazeux et de l'oxygénation. La mortalité et l'incidence de complications pulmonaires sévères a régressé sous Curosurf.
PharmacocinétiqueAbsorption
L'absorption de Curosurf, après administration intratrachéale, est relativement lente chez le lapin nouveau-né (demi-vie alvéolaire: environ 65 heures). Aucune détermination n'a été faite chez l'homme.
Aucune donnée pharmacocinétique n'est disponible chez les enfants prématurés, du fait des barrières éthiques et techniques évidentes s'opposant à l'obtention de telles données.
Données précliniquesDes études de mutagénicité avec Curosurf ont donné des résultats négatifs, des études sur le potentiel carcinogène et la toxicité de reproduction n'ont pas été effectuées.
Remarques particulièresStabilité
Conserver fermé, au réfrigérateur entre 2 °C et 8 °C (jusqu'à l'emploi) et à l'abri de la lumière. Après ouverture, les quantités restantes doivent être éliminées. Les ampoules fermées et non utilisées qui ont été chauffées à température ambiante peuvent être replacées dans le réfrigérateur pour une utilisation en l'espace de 24 heures.
Le médicament ne doit pas être chauffé à température ambiante et remis au réfrigérateur plus d'une fois.
Remarques particulières concernant le stockage
Le médicament ne doit être utilisé au-delà de la date imprimée sur l'emballage avec la mention «EXP».
Numéro d’autorisation51886 (Swissmedic).
PrésentationAmpoule de 1,5 ml, pour une dose unique de 120 mg (80 mg/ml). [A]
Titulaire de l’autorisationChiesi SA, Villars-sur-Glâne.
Mise à jour de l’informationMai 2020.
|








