CompositionPrincipes actifs
Chlorhydrate de méthylphénidate.
Excipients
Noyau du comprimé: butylhydroxytoluène (E 321), acétate de cellulose, hypromellose, acide phosphorique concentré, poloxamère 188, macrogol 200 000 et 7 000 000, povidone K29-32, chlorure de sodium, acide stéarique, acide succinique, oxydes de fer noir et jaune (E 172).
Comprimés à libération prolongée à 27 mg et à 54 mg: oxyde de fer rouge (E 172).
Pelliculage: hypromellose, lactose monohydraté, dioxyde de titane (E 171), triacétine, cire de carnauba, macrogol 400.
Comprimé à libération prolongée à 18 mg: oxyde de fer jaune (E 172) et acide stéarique en plus.
Comprimé à libération prolongée à 27 mg: oxyde de fer noir (E 172) en plus.
Comprimé à libération prolongée à 54 mg: oxydes de fer rouge et jaune (E 172) en plus.
Encre d'impression: oxyde de fer noir (E 172), hypromellose, propylèneglycol.
Teneur totale en sodium:
Comprimé à libération prolongée à 18 mg: 7,08 mg; comprimé à libération prolongée à 27 mg: 7,08 mg; comprimé à libération prolongée à 36 mg: 14,16 mg; comprimé à libération prolongée à 54 mg: 14,16 mg.
Teneur en lactose:
Comprimé à libération prolongée à 18 mg: 6,5 mg; comprimé à libération prolongée à 27 mg: 4,9 mg; comprimé à libération prolongée à 36 mg: 16,7 mg; comprimé à libération prolongée à 54 mg: 7,6 mg.
Indications/Possibilités d’emploiConcerta est indiqué pour traiter un trouble déficitaire de l'attention/hyperactivité (TDAH) persistant depuis l'enfance dans le cadre d'une stratégie thérapeutique globale.
Le traitement doit être initié et surveillé exclusivement par un médecin spécialisé dans les troubles du comportement des enfants, des adolescents, ou des adultes.
L'efficacité de Concerta dans le traitement du TDAH a été documentée dans le traitement du TDAH dans des essais cliniques contrôlés chez des enfants et des adolescents âgés de 6 à 17 ans et des adultes âgés de 18 à 65 ans, qui remplissaient les critères DSM-IV du TDAH (voir «Mises en garde et précautions»).
Une partie des enfants chez lesquels un TDAH a été observé en conservent les symptômes à l'âge adulte. Les symptômes des adultes doivent donc avoir déjà commencé dans l'enfance lorsqu'un traitement est entamé.
L'utilisation de Concerta doit être limitée aux patients ayant besoin d'un médicament dont l'effet se prolonge de la prise matinale jusqu'au soir.
Concerta doit être utilisé dans le cadre d'un programme complet de traitement lorsque des mesures comportementales à elles seules n'ont pas suffi. Un programme thérapeutique complet pour traiter le TDAH peut comprendre des mesures psychologiques, pédagogiques et sociales.
Le diagnostic doit être posé selon les critères DSM actuels ou la classification ICD.
Un traitement par Concerta n'est pas indiqué chez tous les enfants et adolescents atteints de TDAH et la décision d'utiliser le médicament doit reposer sur une évaluation très soigneuse du degré de gravité des symptômes du patient. Les stimulants ne sont pas prévus pour être utilisés chez des patients qui montrent des symptômes secondaires dus à leur environnement et/ou d'autres troubles psychiatriques primaires, psychoses comprises. Des mesures pédagogiques adaptées sont essentielles et une prise en charge psychosociale est souvent bénéfique.
L'étiologie spécifique de ce syndrome est inconnue. Un diagnostic adéquat ne peut pas être posé par un seul test diagnostique. Il exige l'emploi de ressources médicales, psychologiques, pédagogiques et sociales spécifiques. L'apprentissage peut être entravé, mais pas obligatoirement. Le traitement par Concerta peut atténuer les principales manifestations du TDAH comme la distraction moyenne à forte, le relâchement rapide de l'attention, l'impulsivité, une activité motrice accrue (agitation) et un comportement anormal en société.
Posologie/Mode d’emploiExamens préconisés avant le début du traitement
Avant de commencer le traitement par Concerta, il est nécessaire d'effectuer et de documenter un examen cardiovasculaire, comprenant un examen physique, la tension artérielle et la fréquence cardiaque, ainsi qu'une anamnèse soigneuse et, le cas échéant, des examens cardiologiques complémentaires (voir «Mises en garde et précautions»). Comme il n'existe pas de données à long terme, des examens cardiovasculaires réguliers devraient être effectués en présence de facteurs de risque correspondants (voir «Mises en garde et précautions»).
Par ailleurs, il convient de mesurer le poids et la taille du patient avant le début du traitement et de les noter sur une courbe de croissance (voir «Mises en garde et précautions»).
Posologie usuelle
Enfants (dès 6 ans), adolescents et adultes
Le traitement ne doit être initié que par un médecin ayant de l'expérience dans le traitement des troubles de comportement chez les enfants, les adolescents et les adultes et doit être également surveillé par lui.
Concerta s'administre une fois par jour par voie orale. Comme l'effet dure pendant 12 heures après la prise, le médicament doit être pris une fois par jour le matin.
Schéma d'administration
Patients prenant le méthylphénidate pour la première fois
La dose initiale journalière recommandée de Concerta pour les patients qui ne prennent pas de méthylphénidate actuellement, ou à qui l'on administre d'autres stimulants que le méthylphénidate, est de 18 mg une fois par jour pour les enfants et adolescents et de 18 ou 36 mg une fois par jour pour les adultes.
Patients prenant actuellement du méthylphénidate
La dose recommandée de Concerta pour les patients prenant actuellement du méthylphénidate à libération immédiate trois fois par jour à des doses de 10 à 60 mg/jour est indiquée dans le tableau suivant:
Tableau 1: Changement de dose recommandé d'un schéma de méthylphénidate à Concerta
|
Dose journalière de méthylphénidate jusqu'à présent
|
Dose initiale recommandée de Concerta
| |
5 mg de méthylphénidate 3× par jour
|
18 mg 1× jour le matin
| |
10 mg de méthylphénidate 3× par jour
|
36 mg 1× jour le matin
| |
15 mg de méthylphénidate 3× par jour
|
54 mg 1× jour le matin
| |
20 mg de méthylphénidate 3× par jour
|
72 mg 1× jour le matin
|
Ajustement de la posologie/titration
La détermination de la posologie pour les patients prenant actuellement du méthylphénidate dans d'autres schémas posologiques doit se faire sur la base d'une évaluation clinique.
La dose peut être augmentée par paliers de 18 mg à intervalles hebdomadaires.
La dose journalière maximale de Concerta est de 54 mg chez les enfants et de 72 mg chez les adolescents et les adultes.
Réduction de la dose et arrêt
En cas de réactions paradoxales (aggravation des symptômes) ou d'autres effets indésirables, la posologie doit être réduite ou, si c'est nécessaire, le médicament doit être arrêté.
Durée du traitement et traitement à long terme
Si les symptômes ne s'améliorent pas après une augmentation de la dose pendant 1 mois, le médicament doit être arrêté.
Concerta doit être arrêté de temps en temps (mais au plus tard après 12 mois) pour vérifier l'état des patients sans prise de médicament, et le bénéfice du traitement à long terme doit être réévalué régulièrement.
Il n'existe pas d'analyses systématiques sur la base d'études contrôlées en ce qui concerne l'utilisation à long terme du méthylphénidate, surtout en ce qui concerne le potentiel de dépendance et d'autres effets indésirables (voir «Mises en garde et précautions» et «Effets indésirables»).
Passage de Concerta à un autre médicament à base de méthylphénidate à libération prolongée
D'autres médicaments à base de méthylphénidate à libération prolongée et avec des profils de libération différents peuvent présenter des profils d'efficacité et de tolérance différents de ceux de Concerta. Il est recommandé de ne procéder à une substitution que sous surveillance médicale additionnelle.
Patients âgés (>65 ans)
L'utilisation de Concerta chez les patients âgés de plus de 65 ans n'a pas été étudiée dans des études contrôlées.
Patients présentant des troubles de la fonction hépatique
Le méthylphénidate n'a pas été étudié chez les patients présentant une insuffisance hépatique.
Patients présentant des troubles de la fonction rénale
Le méthylphénidate n'a pas été étudié chez les patients présentant une insuffisance rénale.
Enfants (<6 ans)
L'utilisation de Concerta chez les patients de moins de 6 ans n'a pas été étudiée dans des études contrôlées. Concerta ne doit pas être utilisé chez les patients de moins de 6 ans.
Mode d'administration
Les comprimés à libération prolongée de Concerta doivent être avaler entiers avec du liquide. Ils ne doivent être ni machés, ni divisés, ni écrasés car le principe actif est contenu dans une enveloppe non absorbable, qui le libère de façon contrôlée et continue (voir «Mises en garde et précautions»). Concerta peut être pris avec ou sans nourriture (voir «Pharmacocinétique»).
Contre-indications·Anxiété et tension psychique marquées et agitation prononcée, car le méthylphénidate peut renforcer ces symptômes;
·diagnostic ou antécédents de dépression sévère, anorexie mentale, symptômes psychotiques, tendance suicidaire, manie, schizophrénie ou trouble de la personnalité borderline car le méthylphénidate peut aggraver ces états;
·abus d'alcool et de drogues;
·antécédents familiaux ou diagnostic de syndrome de Gilles de la Tourette;
·glaucome;
·chez les patients avec une augmentation de taille de la prostate et rétention urinaire;
·phéochromocytome;
·hyperthyroïdie;
·troubles du rythme cardiaque;
·présence de maladies cardio-vasculaires incluant hypertension sévère, insuffisance cardiaque, angine de poitrine, malformation cardiaque congénitale hémodynamiquement significative, cardiomyopathies, infarctus du myocarde, arythmies et canalopathies (affections provoquées par un dysfonctionnement des canaux ioniques) potentiellement fatales;
·maladie occlusive artérielle;
·affections cérébrovasculaires préexistantes, telles qu'anévrysmes cérébraux, anomalies vasculaires y compris vascularite et accident vasculaire cérébral;
·traitement par les inhibiteurs non sélectifs et irréversibles de la monoamine-oxydase (MAO) et pendant au moins 14 jours après l'arrêt d'un inhibiteur de la MAO, en raison du risque de survenue de poussée hypertensive (voir «Interactions»);
·hypersensibilité connue au principe actif ou à l'un des excipients mentionnés dans la composition.
Mises en garde et précautionsGénéralités
La décision, après anamnèse détaillée et examen complet, de prescrire Concerta dans les troubles hyperkinétiques devrait dépendre de l'évaluation du degré de sévérité des symptômes et de l'âge de l'enfant. La décision ne devrait pas être prise seulement en raison de l'existence d'un ou de plusieurs troubles comportementaux manifestes. Si les symptômes sont liés à des réactions de stress aiguës, Concerta n'est en général pas indiqué.
Utilisation à long terme (plus de 12 mois)
La sécurite et 'efficacité de l'utilisation à long terme du méthylphénidate n'ont pas été évaluées de façon systématique au cours d'études contrôlées. Il n'est pas nécessaire ni souhaitable, que le traitement par méthylphénidate soit indéfini. Chez les enfants et les adolescents le traitement est habituellement interrompu pendant ou après la puberté. Les patients traités par méthylphénidate à long terme (c-à-d. plus de 12 mois) doivent être surveillés continuellement et attentivement conformément aux recommandations décrites dans «Mises en garde et précautions» (voir ci-dessous), relatives à l'état cardiovasculaire, la croissance (enfants), le poids, l'appétit, le développement de nouveaux troubles psychiatriques ou l'aggravation de troubles psychiatriques préexistants. Les troubles psychiatriques devant faire l'objet d'une surveillance sont décrits ci-dessous et incluent (mais de manière non limitative): tics moteurs ou verbaux, comportement agressif ou hostile, agitation, anxiété, dépression, psychose, manie, délire, irritabilité, manque de spontanéité, retrait et persévération excessive.
Lorsque le méthylphénidate est prescrit sur une longue période (plus de 12 mois), il convient de réévaluer régulièrement le bénéfice à long terme du médicament pour chaque patient en prévoyant des périodes sans traitement afin d'évaluer le comportement du patient sans traitement médicamenteux. Il est recommandé d'interrompre le traitement par méthylphénidate au moins une fois par an afin d'évaluer l'état du patient (pour les enfants de préférence pendant les vacances scolaires). Une amélioration peut se maintenir éventuellement à l'arrêt temporaire ou définitif du médicament.
Patients âgés
Le méthylphénidate ne doit pas être utilisé chez les patients âgés. La sécurité et l'efficacité du méthylphénidate n'ont pas été établies dans ce groupe d'âge. Concerta n'a pas été étudié pour le TDAH chez les patients âgés de plus de 65 ans.
Patients de moins de 6 ans
Concerta ne doit pas être utilisé chez les patients de moins de 6 ans. Il n'existe pas de données suffisantes sur l'efficacité et la sécurité et sur la posologie chez l'enfant de moins de 6 ans.
Anomalies cardiaques structurelles, autres maladies cardiaques sévères et mort subite
Des cas de mort subite ont été rapportés chez des patients traités par des stimulants du SNC, y compris le méthylphénidate, aux doses usuelles et ayant des anomalies cardiaques structurelles ou d'autres problèmes cardiaques sévères. De tels événements ont également été observés dans des cas isolés chez des patients porteurs supposés de maladies cardiovasculaires préexistantes. En conséquence, le méthylphénidate ne sera pas administré chez les patients ayant des anomalies cardiaques structurelles ou des antécédents de maladies cardiovasculaires (p.ex. cardiomyopathie, des anomalies graves du rythme cardiaque ou d'autres problèmes cardiaques sévères) parce qu'ils pourraient les exposer à une vulnérabilité accrue vis-à-vis des effets sympathomimétiques des stimulants.
Maladies cardiaques – adultes
Des cas de mort subite, d'accident vasculaire cérébral et d'infarctus du myocarde ont été rapportés chez des adultes prenant des médicaments stimulants aux doses habituelles pour le TDAH. Bien que le rôle des stimulants dans ces cas soit inconnu, les adultes sont plus susceptibles que les enfants de présenter des anomalies cardiaques structurelles graves, une cardiomyopathie, des anomalies graves du rythme cardiaque, une maladie coronarienne ou d'autres problèmes cardiaques graves. Les adultes présentant de telles anomalies ne devraient généralement pas être traités par des stimulants.
Mésusage et événements cardiovasculaires
Le mésusage des stimulants du système nerveux central peut être associé à une mort subite ou à d'autres événements indésirables cardiovasculaires sévères.
Statut cardiovasculaire avant et pendant le traitement
Pour identifier l'existence de maladies cardiaques, on devrait effectuer chez les patients qu'on prévoit de traiter par le méthylphénidate, une anamnèse soigneuse (y compris l'anamnèse familiale de décès subits ou d'arythmies ventriculaires) et un examen physique. Si les premiers résultats ou les données anamnestiques indiquent une maladie de ce type, d'autres examens cardiologiques (par ex. électrocardiogramme, échocardiogramme) doivent être faits.
La prudence est donc recommandée en cas de traitement de patients dont l'état général pourrait être affecté par une augmentation de la pression artérielle ou du pouls (voir «Contre-indications»). Le statut cardiovasculaire doit être surveillé soigneusement. La pression artérielle et la fréquence cardiaque doivent être vérifiées et documentées par écrit à chaque ajustement de la dose et en cas de besoin clinique, puis à des intervalles appropriés (mais au moins tous les 6 mois).
Si pendant un traitement par le méthylphénidate des symptômes comme palpitations, douleurs thoraciques à l'effort, syncopes, dyspnée ou d'autres symptômes laissant supposer une maladie cardiaque apparaissent, un examen cardiologique doit être effectué immédiatement.
Le méthylphénidate doit être arrêté chez les patients présentant des enregistrements répétés de tachycardie, d'arythmie ou de pression artérielle systolique élevée (>95ème percentile). Une consultation chez un cardiologue est indiquée.
L'administration de méthylphénidate est contre-indiquée dans certains cas de troubles cardiovasculaires préexistants sous réserve de l'obtention d'un avis de cardiologue (voir «Contre-indications»).
L'analyse des données issues des études cliniques avec le méthylphénidate chez l'enfant ou l'adolescent atteint de TDAH a montré que les patients traités par méthylphénidate développent fréquemment des modifications de la pression artérielle systolique et diastolique de plus de 10 mmHg par rapport à la valeur initiale et par comparaison au groupe contrôle. Des augmentations des valeurs des pressions artérielles diastolique et systolique ont également été observées dans des données d'essai clinique obtenues auprès de patients adultes atteints de TDAH. De plus, des études cliniques chez des enfants traités par méthylphénidate ont montré une augmentation du pouls au repos de 2 à 6 battements par minute en moyenne pendant la journée par comparaison avec le placebo.
Les conséquences cliniques, à court et à long terme, de ces effets cardiovasculaires chez l'enfant et l'adolescent ne sont pas connues. La possibilité de complications cliniques résultant des effets observés lors des études cliniques ne peut être exclue, notamment lorsque le traitement pris pendant l'enfance/l'adolescence se poursuit à l'âge adulte.
Agonistes alpha-2 centraux
La prudence est de mise lors de l'utilisation concomitante d'agonistes alpha-2 centraux tels que la clonidine car des effets indésirables graves, y compris des morts subites, ont été rapportés (voir «Interactions»).
Anesthésiques halogénés
Si une intervention chirurgicale est prévue, le méthylphénidate ne doit pas être pris le jour de l'intervention, car il existe alors un risque d'augmentation soudaine de la pression artérielle et de la fréquence cardiaque au cours de l'intervention (vois «Interactions»).
Affections cérébrovasculaires
Des affections cérébrovasculaires telles que vascularite/artérite cérébrale, occlusion cérébrovasculaire et hémorragie cérébrale ont été rapportées lors de l'utilisation de Concerta (voir «Effets indésirables»). Un diagnostic précoce sur la base d'indices forts peut permettre l'arrêt immédiat de Concerta et est essentiel pour un traitement précoce. Les indices forts sont des symptômes neurologiques nouveaux indiquant une ischémie ou une hémorragie cérébrale, tels que des céphalées sévères, un engourdissement, une faiblesse (unilatérale), une paralysie, des troubles de la coordination, de la vision, de la parole, du langage ou de la mémoire.
Les patients présentant des facteurs de risque supplémentaires (tels que des antécédents de maladie cardiovasculaire, une médication concomitante augmentant la pression artérielle) devront être surveillés à chaque visite après l'initiation du traitement par méthylphénidate à la recherche de signes et symptômes neurologiques.
Le traitement par Concerta n'est pas recommandé chez les patients présentant des affections cérébrovasculaires préexistantes (p.ex. anévrysme, malformations/anomalies vasculaires) (voir «Contre-indications»).
Convulsions
Concerta doit être utilisé avec prudence chez les patients atteints d'épilepsie. Il existe des indices cliniques selon lesquels le méthylphénidate peut abaisser le seuil de convulsions chez les patients ayant des antécédents de crises épileptiques ou présentant des anomalies de l'EEG sans crises épileptiques ou dans des cas très rares chez des patients sans antécédents de crises épileptiques et sans indications dans l'EEG. En cas d'apparition de convulsions ou d'augmentation de la fréquence des convulsions, le méthylphénidate doit être arrêté.
Troubles de la vision
Dans de rares cas, des symptômes de troubles de la vision sont survenus. On a rapporté alors des troubles de l'accommodation et une vision floue.
Syndrome sérotoninergique
Un syndrome sérotoninergique a été rapporté après l'administration concomitante de méthylphénidate avec des médicaments sérotoninergiques. Si l'utilisation concomitante de méthylphénidate avec un médicament sérotoninergique est justifiée, la reconnaissance rapide des symptômes du syndrome sérotoninergique est importante. Ces symptômes peuvent inclure des modifications de l'état mental (p.ex. agitation, hallucinations, coma), une instabilité autonome (p.ex. tachycardie, pression artérielle labile, hyperthermie), des anomalies neuromusculaires (p.ex. hyperréflexie, trouble de coordination, rigidité) et/ou des symptômes gastro-intestinaux (p.ex. nausée, vomissement, diarrhée). En cas de suspicion d'un syndrome sérotoninergique, le traitement par méthylphénidate doit être arrêté le plus rapidement possible (voir «Interactions»).
Dépendance et mésusage médicamenteux
Le risque de mésusage ou d'abus de méthylphénidate doit être étroitement surveillé.
Le méthylphénidate doit être administré avec précaution chez les patients ayant une dépendance connue aux drogues et/ou à l'alcool en raison du risque d'abus et de mésusage.
L'abus chronique peut entraîner une accoutumance marquée et une dépendance psychique avec divers degrés de comportement anormal. Des épisodes manifestement psychotiques peuvent se produire, surtout lors d'usage abusif par voie parentérale.
L'âge du patient, la présence de facteurs de risque d'assuétude (tels qu'un trouble oppositionnel avec provocation, un trouble des conduites ou un trouble bipolaire) ainsi qu'un abus de substances antérieur ou actuel par le patient doivent être pris en compte avant de décider l'initiation d'un traitement d'un TDAH. Il est recommandé d'être prudent chez les patients présentant une instabilité émotionnelle, comme chez ceux ayant des antécédents de dépendance aux drogues ou à l'alcool, en raison d'une augmentation possible des doses par les patients.
Pour les patients présentant un risque élevé de mésusage, l'utilisation du méthylphénidate ou d'autres stimulants peut ne pas être appropriée et un traitement sans stimulants devra alors être envisagé.
Arrêt
En cas de l'arrêt du médicament, une surveillance étroite est nécessaire car des manifestations de sevrage ainsi qu'un démasquage de dépressions ou de l'hyperactivité chronique peuvent survenir. En particulier lors de l'arrêt après une utilisation abusive, une surveillance très étroite est nécessaire, car des dépressions sévères peuvent survenir. En outre, même en cas d'utilisation thérapeutique, certains patients peuvent avoir besoin d'un suivi à long terme et/ou d'un traitement ultérieur des symptômes démasqués du trouble sous-jacent.
Affections psychiatriques
Les troubles psychiatriques concomitants sont fréquents dans le TDAH et doivent être pris en compte lors de la prescription de stimulants. Avant le début du traitement par méthylphénidate, le patient doit être examiné afin de détecter tout trouble psychiatrique existant; de plus, les antécédents familiaux en termes de troubles psychiatriques doivent être renseignés. En cas d'apparition de symptômes psychiatriques ou d'exacerbation de troubles psychiatriques préexistants, le traitement par méthylphénidate ne doit pas être poursuivi à moins que les bénéfices attendus soient supérieurs aux risques chez le patient.
La survenue ou l'aggravation de troubles psychiatriques doit être surveillée à chaque ajustement de la posologie, puis au moins tous les 6 mois et à chaque visite; l'arrêt du traitement peut alors être envisagé.
Symptômes psychotiques ou maniaques
L'administration de méthylphénidate à des patients présentant des troubles psychotiques peut exacerber les symptômes de troubles du comportement ou de troubles de la pensée.
Des symptômes psychotiques liés au traitement (hallucinations visuelles/tactiles/auditives et idées délirantes) ou une manie peuvent survenir après administration de méthylphénidate aux doses usuelles chez des patients sans antécédents de maladie psychotique ou de manie (voir «Effets indésirables»). En cas d'apparition de symptômes maniaques ou psychotiques, il convient de considérer un lien causal possible avec le méthylphénidate et un arrêt du traitement pourra être envisagé.
Troubles bipolaires
La plus grande prudence est requise en cas d'administration de stimulants pour traiter le TDAH chez des patients pouvant présenter un trouble bipolaire associé, mais se trouvant à ce moment-là en euthymie ou en intervalle d'entretien, car un épisode maniaque pourrait être déclenché. Avant de commencer un traitement par les stimulants, il faut vérifier très soigneusement chez les patients présentant des symptômes dépressifs associés s'il n'existe pas chez eux un risque de trouble bipolaire. Ceci implique le relevé d'une anamnèse psychiatrique détaillée, y compris une anamnèse familiale des suicides, troubles bipolaires et dépressions. Une surveillance étroite et continue est nécessaire chez ces patients (voir ci-dessus sous «Affections psychiatriques»). L'apparition de symptômes doit être surveillée à chaque adaptation posologique, puis au moins tous les 6 mois et à chaque visite.
Dépressions sévères
Concerta ne doit pas être utilisé pour traiter des dépressions sévères.
Agressivité ou comportement hostile
Chez les patients commençant un traitement par Concerta, il faut faire attention à l'apparition ou l'aggravation de comportements agressifs ou d'hostilité. Une surveillance attentive est nécessaire, au début du traitement, à chaque ajustement de doses, puis au moins tous les 6 mois et à chaque visite. L'agressivité est souvent liée au TDAH; cependant l'apparition inattendue ou l'aggravation de l'agressivité pendant le traitement par Concerta ont été rapportées. Le médecin devra évaluer la nécessité d'ajuster le schéma thérapeutique chez les patients présentant un changement dans leur comportement en gardant à l'esprit qu'une augmentation ou une diminution progressive de la posologie peut être appropriée. Un arrêt du traitement peut être envisagé (voir «Effets indésirables»).
Tendances suicidaires
Les patients ayant des idées ou un comportement suicidaire au cours du traitement du TDAH doivent être immédiatement examinés par leur médecin. L'aggravation d'une affection psychiatrique sous-jacente devra être prise en considération et un possible lien de causalité avec le traitement par méthylphénidate devra être envisagé. Le traitement d'une affection psychiatrique sous-jacente pourra être nécessaire et il conviendra alors d'envisager l'arrêt du traitement par méthylphénidate.
Tics
Les stimulants à effet sur le système nerveux central, méthylphénidate compris, ont été mis en relation avec le déclenchement ou l'aggravation de tics moteurs ou verbaux. Une aggravation du syndrome de Gilles de la Tourette a également été rapportée (voir «Effets indésirables»). Une évaluation des antécédents familiaux ainsi qu'un examen clinique à la recherche de tics ou du syndrome de Gilles de la Tourette devront être réalisés avant l'administration de stimulants. Pendant le traitement par le méthylphénidate, les patients doivent être surveillés en ce qui concerne la survenue de tics ou d'un syndrome de Gilles de la Tourette lors de chaque adaptation posologique, puis au moins tous le 6 mois ou à chaque visite; le traitement doit être interrompu en cas de nécessité clinique.
Anxiété, tension psychique ou agitation
Des cas d'anxiété, d'agitation et de tension psychique ont été rapportés chez les patients traités par méthylphénidate (voir «Effets indésirables»). Le méthylphénidate est également associé à une aggravation de symptômes préexistants d'anxiété, de tension psychique ou d'agitation. L'anxiété a conduit à l'arrêt du traitement par méthylphénidate chez certains patients. Une évaluation clinique de l'anxiété, de la tension psychique ou de l'agitation devra être réalisée avant l'administration de méthylphénidate. Une surveillance régulière de la survenue ou de l'aggravation de ces symptômes au cours du traitement devra être réalisée en évaluant les patients à chaque adaptation posologique, puis au moins tous les 6 mois ou à chaque visite.
Croissance chez les enfants
Une prise de poids médiocre et un retard de croissance ont été rapportés lors du traitement à long terme d'enfants par le méthylphénidate. Des études de suivi chez des enfants âgés de 7 à 10 ans suggèrent que les enfants prenant constamment du méthylphénidate (p.ex. 7 jours par semaine pendant 1 an) peuvent présenter un ralentissement transitoire de la vitesse de croissance (en moyenne, réduction de la croissance en taille de 2 cm et réduction de la prise de poids de 2,7 kg sur 3 ans). Des données de suivi à l'âge de 25 ans montrent que les patients traités de manière durable présentent systématiquement une réduction de la taille de 3,3 cm et un poids augmenté de 7,4 kg par rapport au groupe non traité. D'autres études à long terme n'ont toutefois montré aucun effet significatif du méthylphénidate sur la taille et le poids.
Pour cette raison, les enfants et les adolescents ayant besoin d'un traitement à long terme devraient faire l'objet d'une surveillance très stricte (au moins tous les 6 mois) en ce qui concerne leur taille, leur poids et leur appétit et documentés au moins tous les 6 mois sur une courbe de croissance. Le traitement devrait être interrompu chez les patients dont la croissance ou la prise de poids ne correspondent pas aux attentes.
Poids corporel
Concerta peut diminuer l'appétit et le poids. Une diminution du poids a également été rapportée avec le traitement par méthylphénidate chez les adultes (voir «Effets indésirables»). Chez les adultes, le poids doit donc également faire l'objet d'une surveillance régulière.
Possibilité d'obstruction gastro-intestinale
Comme les comprimés à libération prolongée de Concerta ne se déforment pas et ne changent pas significativement de forme même dans le tractus gastro-intestinal, Concerta ne devrait normalement pas être administré à des patients ayant une sténose ou un rétrécissement gastro-intestinal sévère préexistant (pathologique ou iatrogène), une dysphagie ou des difficultés marquées à avaler des comprimés. Des cas rares de symptômes obstructifs ont été rapportés chez des patients ayant un rétrécissement gastro-intestinal connu associé à la prise de médicaments non déformables à libération prolongée.
Patients ayant des troubles de la déglutition
Afin de garantir la libération prolongée du principe actif du comprimé à libération prolongée, Concerta ne doit être prescrit qu'à des patients pouvant avaler le comprimé à libération prolongée entier (voir «Possibilité d'obstruction gastro-intestinale»). Les patients doivent être informés que les comprimés à libération prolongée de Concerta doivent être avalés entiers (non divisés) avec du liquide. Les comprimés à libération prolongée ne doivent être ni machés, ni divisés, ni écrasés.
Élimination de l'enveloppe du comprimé
Le principe actif est contenu dans une enveloppe non absorbable destinée à libérer le principe actif de façon continue. L'enveloppe du comprimé non absorbable est éliminée de l'organisme avec les autres composants insolubles du noyau du comprimé; les patients ne doivent pas s'inquiéter s'ils découvrent dans leur selles un objet ressemblant à un comprimé.
Examen hématologique-clinique et autres paramètres de laboratoire
La sécurité du traitement à long terme par méthylphénidate n'est pas totalement connue. Pendant un traitement à long terme, des examens hématologiques réguliers sont recommandés (hémogramme différentiel complet et numération des plaquettes). En cas de leucopénie, thrombocytopénie, anémie ou autres modifications incluant celles indiquant des troubles rénaux ou hépatiques sévères, l'arrêt du traitement devra être envisagé (voir «Effets indésirables»).
Priapisme
En relation avec le traitement par des médicaments contenant du méthylphénidate, des cas isolés d'érection pénienne douloureuse de longue durée (priapisme) ayant nécessité une intervention médicale immédiate, ou parfois même chirurgicale, ont été rapportés aussi bien chez des adultes que chez des enfants et des adolescents (voir «Effets indésirables»). Les cas de priapisme n'ont pour la plupart d'entre eux pas été observés au début du traitement, mais sont survenus après que le médicament a été pris pendant un certain temps déjà, souvent à la suite d'une augmentation des doses. Un priapisme a également été observé au cours de périodes sans traitement par méthylphénidate (pause thérapeutique ou arrêt du traitement). Les patients qui développent des érections douloureuses anormalement prolongées (plus de 2 heures) ou fréquentes doivent immédiatement consulter un médecin. Le personnel médical doit explicitement informer les patients et leurs parents sur ce problème et sur son caractère d'urgence.
Fatigue
Concerta ne doit pas être utilisé pour la prévention ou le traitement d'états de fatigue normaux.
Insuffisance rénale ou hépatique
Il n'existe pas d'expérience sur l'utilisation de méthylphénidate chez des patients présentant une insuffisance rénale ou hépatique.
Lactose
Ce médicament contient du lactose. Les patients présentant une intolérance au galactose, un déficit total en lactase ou un syndrome de malabsorption du glucose et du galactose (maladies héréditaires rares) ne devraient pas prendre ce médicament.
Sodium
Ce médicament contient moins de 1 mmol de sodium (23 mg) par comprimé à libération prolongée, c.-à-d. qu'il est essentiellement «sans sodium».
Choix de la forme pharmaceutique de méthylphénidate
Le choix de la forme pharmaceutique du médicament contenant du méthylphénidate devra être effectué par le médecin spécialiste au cas par cas; ce choix dépendra de la durée d'action souhaitée.
Dépistage des drogues
Ce médicament contenant du méthylphénidate peut donner des résultats faussement positifs lors de la recherche d'amphétamines, notamment avec les méthodes d'immunodosage. Les sportifs de haut niveau doivent être conscients que ce médicament peut entraîner une réaction positive aux contrôles anti-dopage.
InteractionsInfluence d'autres substances sur la pharmacocinétique du méthylphénidate
Le cytochrome P450 n'intervient pas de façon cliniquement significative dans le métabolisme du méthylphénidate. Une modification significative de la pharmacocinétique du méthylphénidate par l'administration d'inducteurs ou d'inhibiteurs du cytochrome P450 n'est pas attendue. Inversement, les énantiomères D et L du méthylphénidate n'inhibent pas de façon significative les cytochromes P450 1A2, 2C8, 2C9, 2C19, 2D6, 2E1 ou 3A.
Influence du méthylphénidate sur la pharmacocinétique d'autres substances
L'effet du méthylphénidate sur les concentrations plasmatiques de médicaments administrés de façon concomitante n'est pas connu. Par conséquent, la prudence est recommandée lors de l'association de méthylphénidate avec d'autres médicaments, notamment avec les médicaments à faible marge thérapeutique.
Autres interactions
Des rapports indiquent que le méthylphénidate peut inhiber le métabolisme d'anticoagulants de type coumarine, d'anticonvulsivants (p.ex. phénobarbital, phénytoïne, primidone) et de certains antidépresseurs (antidépresseurs tricycliques et inhibiteurs sélectifs de la recapture de la sérotonine). Lors de l'instauration ou de l'arrêt d'un traitement par le méthylphénidate, il peut s'avérer nécessaire d'ajuster la dose de ce médicament administré de façon concomitante et de déterminer les concentrations plasmatiques du principe actif (ou les temps de coagulation dans le cas de la coumarine).
Influence du méthylphénidate sur la pharmacodynamique d'autres substances
Utilisation concomitante contre-indiquée
Inhibiteurs de la monoamine-oxydase (MAO)En raison de la possibilité de poussée hypertensive, le méthylphénidate est contre-indiqué chez les patients traités par des inhibiteurs non sélectifs et irréversibles de la MAO (traitement actuel ou durant les deux semaines précédentes) (voir «Contre-indications»).
Anesthésiques halogénés
Il existe un risque d'augmentation soudaine de la pression artérielle et de la fréquence cardiaque lors d'interventions chirurgicales. Le méthylphénidate ne doit pas être pris le jour de l'intervention lorsqu'une intervention est prévue.
Agonistes alpha-2 centraux (p.ex. clonidine)
Des effets indésirables graves (y compris la mort subite) ont été rapportés en cas d'utilisation simultanée de clonidine et de méthylphénidate. La sécurité de l'utilisation à long terme de méthylphénidate en association avec la clonidine ou d'autres agonistes alpha-2 centraux n'a pas été étudiée systématiquement jusqu'à présent.
Utilisation concomitante non recommandée
Alcool
L'alcool peut renforcer les effets indésirables sur le système nerveux central des psychotropes, y compris Concerta. Les données in vitro indiquent que des concentrations d'alcool supérieures à 10% augmentent la libération cumulée de méthylphénidate des comprimés de Concerta. La pertinence clinique de ce résultat sur l'exposition au méthylphénidate après la prise orale de Concerta avec de l'alcool est inconnue. Il est donc conseillé de s'abstenir de consommer de l'alcool pendant le traitement par Concerta.
Médicaments sérotoninergiques
La survenue d'un syndrome sérotoninergique a été rapportée après l'utilisation concomitante de méthylphénidate et d'autres médicaments sérotoninergiques.
Les médicaments sérotoninergiques comprennent par exemple les triptans, les inhibiteurs sélectifs de la recapture de la sérotonine (ISRS), les inhibiteurs de la recapture de la sérotonine-noradrénaline (IRSN), le lithium, le fentanyl et ses analogues, le tramadol, le dextrométhorphane, le tapentadol, la péthidine, la méthadone, ou le millepertuis (Hypericum perforatum) tout comme les principes actifs inhibant le métabolisme de la sérotonine (y compris les inhibiteurs de la MAO comme p.ex. le bleu de méthylène), la substance antibiotique linézolide et les précurseurs de la sérotonine comme par exemple les compléments alimentaires contenant du tryptophane.
L'administration concomitante de Concerta et d'un de ces médicaments sérotoninergiques n'est pas recommandée car elle peut provoquer le développement d'un syndrome sérotoninergique.
Le syndrome sérotoninergique est un état potentiellement fatal. Les symptômes peuvent par exemple comprendre des modifications de l'état mental, une instabilité du système nerveux autonome, des symptômes neuromusculaires, des convulsions, des tremblements et/ou des symptômes gastro-intestinaux. Dans sa forme la plus sévère, le syndrome sérotoninergique peut ressembler à un syndrome malin des neuroleptiques.
Si l'utilisation concomitante de méthylphénidate avec un médicament sérotoninergique est justifiée, l'identification rapide des symptômes du syndrome sérotoninergique est importante (voir «Mises en garde et précautions»).
En cas de suspicion d'un syndrome sérotoninergique, le méthylphénidate doit être immédiatement arrêté et un traitement approprié doit être instauré.
Autres Interactions
Antihypertenseurs
Concerta peut diminuer l'effet hypotenseur des antihypertenseurs.
Médicaments augmentant la pression artérielle
La prudence est recommandée chez les patients traités par méthylphénidate et recevant un autre médicament pouvant augmenter la pression artérielle (voir «Mises en garde et précautions» - «Statut cardiovasculaire avant et pendant le traitement» et «Affections cérébrovasculaires»).
Substances dopaminergiques incluant les antipsychotiques
Comme l'un des principaux effets du méthylphénidate est d'augmenter les taux extracellulaires de dopamine, Concerta peut être associé à des interactions pharmacodynamiques lorsqu'il est administré avec des agonistes dopaminergiques directs ou indirects (y compris des substances dopaminergiques et des antidépresseurs tricycliques), ou alors avec des antagonistes dopaminergiques (y compris des antipsychotiques).
La prudence est recommandée chez les patients traités par Concerta ainsi que par un antipsychotique, car des symptômes extrapyramidaux pourraient survenir lors de l'administration concomitante de ces médicaments ou lors de l'ajustement de la posologie de l'un de ces médicaments ou des deux médicaments.
Grossesse, allaitementGrossesse
Concerta ne doit pas être utilisé pendant la grossesse sauf si c'est absolument nécessaire.
Les résultats d'une étude de cohorte portant sur au total d'environ 3400 femmes exposées au cours du premier trimestre de la grossesse ne montrent pas d'augmentation du risque global d'anomalies congénitales. Par rapport aux grossesses non exposées, une faible augmentation de la fréquence de malformations cardiaques a été observée (risque relatif ajusté combiné, 1,3; IC à 95%: 1,0-1,6), correspondant à trois enfants supplémentaires nés avec des malformations cardiaques pour 1000 femmes exposées au méthylphénidate pendant le premier trimestre de grossesse.
Des cas de toxicité cardiorespiratoire néonatale, notamment des tachycardies et des détresses respiratoires fœtales, ont été rapportés dans le cadre des notifications spontanées.
Les études expérimentales animales ont montré une toxicité pour la reproduction (voir «Données précliniques»).
Allaitement
Le méthylphénidate a été mis en évidence dans le lait maternel. Sur la base d'échantillons de lait maternel de cinq mères, les concentrations de méthylphénidate présentes dans le lait maternel ont entraîné des doses correspondant à 0,16 à 0,7% de la dose maternelle corrigée en fonction du poids chez le nourrisson et un rapport de la quantité dans le lait maternel sur la quantité dans le plasma maternel de 1,1, à 2,7. Par mesure de précaution, on devrait conseiller aux mères qui allaitent de ne pas prendre Concerta.
Fertilité
Les études expérimentales animales n'ont pas montré d'effet sur la fertilité (voir «Données précliniques»).
Effet sur l’aptitude à la conduite et l’utilisation de machinesIl est connu que Concerta peut occasionner des vertiges. La prudence est donc recommandée lors de la conduite, de l'utilisation de machines ou d'autres activités potentiellement dangereuses. Les patients devraient être avertis en conséquence jusqu'à ce qu'ils soient suffisamment sûrs que Concerta n'a pas d'influence négative sur leur aptitude à exercer ces activités.
Effets indésirablesDans les paragraphes suivants, la fréquence est indiquée comme suit: très fréquent (≥1/10), fréquent (<1/10 et ≥1/100), occasionnel (<1/100 et ≥1/1000), rare (<1/1000 et ≥10 000), très rare (<1/10 000), fréquence inconnue (ne peut être estimée sur la base des données disponibles).
Des effets indésirables considérés comme des effets de classe ont été observés lors de l'emploi de médicaments contenant du méthylphénidate.
Les effets indésirables observés le plus fréquemment sont:
Infections et infestations: rhinopharyngite.
Troubles du métabolisme et de la nutrition: anorexie, diminution de l'appétit, diminution modérée de la prise de poids et de la croissance en taille en cas d'utilisation prolongée chez l'enfant.
Affections psychiatriques: insomnie, nervosité, anorexie, labilité affective, agression, agitation, anxiété, dépression, irritabilité, comportement anormal.
Affections du système nerveux: céphalées, vertiges, dyskinésie, hyperactivité psychomotrice, somnolence.
Affections cardiaques: arythmie, tachycardie, palpitations.
Affections vasculaires: hypertension.
Affections respiratoires, thoraciques et médiastinales: toux, douleurs pharyngées et laryngées.
Affections gastro-intestinales: douleurs abdominales, diarrhée, nausées, troubles gastriques et vomissements, sécheresse buccale.
Affections de la peau et du tissu sous-cutané: alopécie, prurit, éruption cutanée, urticaire.
Affections musculosquelettiques et du tissu conjonctif: arthralgie.
Troubles généraux et anomalies au site d'administration: pyrexie, retard de croissance lors d'une utilisation prolongée chez l'enfant.
Investigations: modifications de la pression artérielle et de la fréquence cardiaque (le plus souvent une élévation), perte de poids.
Indépendamment de leur fréquence, il faut informer aussi les patients des effets indésirables suivants, cliniquement significatifs ou sévères, survenant avec les médicaments contenant du méthylphénidate:
Affections psychiatriques: suicide, tentative de suicide, idées suicidaires, comportement répétitif, hallucinations tactiles.
Affections du système nerveux: mouvements choréo-athétosiques, tics ou aggravation de tics existants, troubles nerveux réversibles, migraine, syndrome malin des neuroleptiques.
Affections oculaires: troubles de l'accommodation.
Affections cardiaques: mort subite cardiaque, infarctus du myocarde.
Affections vasculaires: troubles ou hémorragie cérébrovasculaires, vascularite, syndrome de Raynaud, sensation de froid périphérique (mains ou pieds froids).
Affections gastro-intestinales: insuffisance hépatique.
Affections de la peau et du tissu sous-cutané: dermatite exfoliative, syndrome de Steven-Johnson, érythème polymorphe, exanthème médicamenteux.
Troubles du rein et des voies urinaires: hématurie.
Affections des organes de reproduction et du sein: gynécomastie.
En outre, des effets indésirables ont été rapportés en relation avec l'utilisation de Concerta:
Données provenant des études cliniques
Les effets indésirables figurant ci-dessous ont été rapportés dans le cadre d'études faites soit chez l'enfant ou l'adolescent, soit chez l'adulte et peuvent s'appliquer aux deux populations de patients.
Patients pédiatriques
La sécurité de Concerta a été étudiée dans quatre études cliniques en double-aveugle, contrôlées par placebo sur 639 patients pédiatriques (enfants et adolescents) atteints de TDAH. Les informations de ce paragraphe sont tirées de données regroupées.
Dans le tableau 2 sont listés les effets indésirables qui ont été signalés dans ces études chez ≥1% des patients pédiatriques traités par Concerta (enfants et adolescents).
Tableau 2: Effets indésirables signalés dans quatre études cliniques en double-aveugle contrôlées par un placebo chez ≥1% des patients pédiatriques traités par Concerta (enfants et adolescents)
|
Système/classe d'organe
Événement indésirable
|
Concerta
(n = 321)
%
|
Placebo
(n = 318)
%
| |
Infections et infestations
| |
Rhinopharyngite
|
2,8
|
2,2
| |
Affections psychiatriques
| |
Insomnie*
|
2,8
|
0,3
| |
Affections du système nerveux
| |
Vertiges
|
1,9
|
0
| |
Affections respiratoires, thoraciques et médiastinales
| |
Toux
|
1,9
|
0,9
| |
Douleurs pharyngo-laryngées
|
1,2
|
0,9
| |
Affections gastro-intestinales
| |
Douleurs épigastriques
|
6,2
|
3,8
| |
Vomissements
|
2,8
|
1,6
| |
Troubles généraux et anomalies au site d'administration
| |
Pyrexie (fièvre)
|
2,2
|
0,9
|
* Comprend les troubles du sommeil au début du traitement (Concerta = 0,6%) et l'insomnie au cours du traitement (Concerta = 2,2%).
La plupart des effets indésirables avaient un degré de gravité léger à moyen.
Patients adultes
La sécurité de Concerta a été étudiée sur 905 patients adultes atteints de TDAH qui avaient pris part à trois études cliniques en double-aveugle, contrôlées par un placebo. Les informations de ce paragraphe viennent de données regroupées.
Les effets indésirables qui ont été signalés dans ces études par ≥1% des patients Concerta sont présentés dans le tableau 3.
Tableau 3: effets indésirables indiqués par ≥1% des patients adultes sous Concerta dans 3 études cliniques en double-aveugle, contrôlées par un placebo.
|
Système/classe d'organe
Événement indésirable
|
Concerta
(n = 596)
%
|
Placebo
(n = 309)
%
| |
Infections et infestations
| |
Infection du tractus respiratoire supérieur
|
1,7
|
1,0
| |
Sinusite
|
1,3
|
1,0
| |
Troubles du métabolisme et de la nutrition
| |
Diminution de l'appétit
|
24,8
|
6,1
| |
Perte de l'appétit
|
4,2
|
1,3
| |
Affections psychiatriques
| |
Insomnie
|
13,3
|
7,8
| |
Anxiété
|
8,4
|
2,9
| |
Troubles du début du sommeil
|
5,7
|
2,6
| |
Humeur dépressive
|
4,4
|
2,6
| |
Excitation
|
4,0
|
0
| |
Agitation
|
3,2
|
0,6
| |
Nervosité
|
2,3
|
0,6
| |
Bruxisme
|
1,5
|
0,6
| |
Dépression
|
1,5
|
0,6
| |
Faiblesse affective
|
1,3
|
0,6
| |
Diminution de la libido
|
1,3
|
0,6
| |
Attaques de panique
|
1,3
|
0,3
| |
Tension
|
1,3
|
0,3
| |
Agressivité
|
1,2
|
0,6
| |
Confusion
|
1,0
|
0,3
| |
Affections du système nerveux
| |
Céphalées
|
24,2
|
18,8
| |
Sensations de vertiges
|
7,4
|
5,5
| |
Tremblements
|
3,4
|
0,6
| |
Paresthésies
|
1,2
|
0
| |
Céphalées de tension
|
1,0
|
0,3
| |
Affections oculaires
| |
Trouble de l'accommodation
|
1,3
|
0
| |
Vision floue
|
1,3
|
1,0
| |
Affections de l'oreille et du labyrinthe
| |
Vertige
|
2,0
|
0,3
| |
Affections cardiaques
| |
Tachycardie
|
6,0
|
0
| |
Palpitations
|
4,5
|
0,6
| |
Affections vasculaires
| |
Hypertension
|
2,2
|
1,6
| |
Bouffées de chaleur
|
1,3
|
0,6
| |
Affections respiratoires, thoraciques et médiastinales
| |
Douleurs oro-pharyngo-laryngées
|
1,5
|
1,3
| |
Toux
|
1,2
|
1,0
| |
Dyspnée
|
1,2
|
0,6
| |
Affections gastro-intestinales
| |
Sécheresse de la bouche
|
15,1
|
3,6
| |
Nausée
|
14,3
|
4,9
| |
Dyspepsie
|
2,0
|
1,9
| |
Vomissements
|
1,8
|
0,6
| |
Constipation
|
1,5
|
0,6
| |
Affections de la peau et du tissu sous-cutané
| |
Transpiration excessive
|
5,7
|
1,3
| |
Affections musculosquelettiques et du tissu conjonctif
| |
Tension musculaire
|
1,3
|
0
| |
Crampes musculaires
|
1,0
|
0,3
| |
Affections des organes de reproduction et du sein
| |
Dysfonction érectile
|
1,0
|
0,3
| |
Troubles généraux et anomalies au site d'administration
| |
Irritabilité
|
5,2
|
2,9
| |
Fatigue
|
4,7
|
4,2
| |
Soif
|
1,8
|
0,6
| |
Asthénie
|
1,2
|
0
| |
Investigations
| |
Perte de poids
|
8,7
|
3,6
| |
Augmentation de la fréquence cardiaque
|
3,0
|
1,9
| |
Augmentation de la pression artérielle
|
2,5
|
1,9
| |
Augmentation de l'alanine aminotransférase
|
1,0
|
0
|
La plupart des effets indésirables avaient un degré de gravité léger à moyen.
Données d'études ouvertes – Effets indésirables signalés avec une fréquence ≥1%
La sécurité de Concerta a été étudiée dans douze études cliniques ouvertes sur 3782 patients pédiatriques et adultes atteints de TDAH. Les informations de ce paragraphe se basent sur des données regroupées.
Dans le tableau 4 sont listés les effets indésirables du médicament qui ont été indiqués dans ces études par ≥1% des patients traités par Concerta et qui n'ont pas été cités dans les tableaux 2 et 3.
Tableau 4: effets indésirables du médicament indiqués par ≥1% des patients traités par Concerta dans douze études ouvertes
|
Classification par discipline médicale
Événement indésirable
|
Concerta
(n = 3782)
%
| |
Affections psychiatriques
| |
Tics
|
2,0
| |
Fluctuations d'humeur
|
1,1
| |
Affections du système nerveux
| |
Somnolence
|
1,0
| |
Affections gastro-intestinales
| |
Diarrhée
|
2,4
| |
Symptômes abdominaux
|
1,3
| |
Douleurs abdominales
|
1,2
| |
Affections de la peau et du tissu sous-cutané
| |
Exanthème
|
1,3
| |
Troubles généraux et anomalies au site d'administration
| |
Nervosité («remue sans cesse»)
|
1,4
|
La majorité des effets indésirables étaient d'une sévérité légère à modérée.
Données d'études en double-aveugle et d'études ouvertes – Effets indésirables signalés avec une fréquence < 1%
Les autres effets indésirables du médicament apparus dans les études cliniques en double-aveugle et dans les études ouvertes avec une fréquence < 1% chez les patients pédiatriques et adultes traités par Concerta sont listés ci-dessous.
Affections hématologiques et du système lymphatique
Leucopénie.
Affections psychiatriques
Colère, troubles du sommeil, hypervigilance, tristesse, fluctuations d'humeur.
Affections du système nerveux
Hyperactivité psychomotrice, sédation, léthargie.
Affections oculaires
Yeux secs.
Affections de la peau et du tissu sous-cutané
Exanthème maculaire.
Investigations
Souffle cardiaque.
La plupart des effets indésirables avaient un degré de gravité léger à moyen.
Effets indésirables identifiés après la mise sur le marché
Ci-dessous sont listés les effets indésirables qui ont été identifiés en tant que tels après la mise sur le marché de Concerta. Les effets indésirables sont rangés par classe de système d'organes de la classification MedDRA et par fréquence selon la convention suivante:
«très fréquent» (≥1/10),
«fréquent» (≥1/100 à <1/10),
«occasionnel» (≥1/1000 à <1/100),
«rare» (≥1/10 000 à <1/1000),
«très rare» (<1/10 000), cas isolés compris,
«fréquence inconnue» (ne peut être estimée sur la base des données disponibles).
Affections hématologiques et du système lymphatique
Très rare: leucopénie, pancytopénie, thrombopénie, purpura thrombocytopénique.
Affections du système immunitaire
Rare: réactions d'hypersensibilité comme angio-œdème, réactions anaphylactiques, gonflement auriculaire, troubles bulleux et desquamation, urticaire, prurit, éruption cutanée, exanthème.
Affections psychiatriques
Très rare: confusion, désorientation, hallucinations, hallucinations auditives, hallucinations visuelles, manie, nervosité, agitation, psychose induite par les médicaments, logorrhée, troubles de la libido.
Affections su système nerveux
Très rare: convulsions, crises d'épilepsie (Grand Mal), dyskinésie, affections cérébrovasculaires (y compris vascularite/artérite cérébrale, hémorragie cérébrale, occlusion cérébrovasculaire).
Affections oculaires
Très rare: diplopie, mydriase, vision trouble, troubles de la vision.
Affections cardiaques
Très rare: palpitations, angine de poitrine, bradycardie, extrasystoles, tachycardie supraventriculaire, extrasystoles ventriculaires.
Affections vasculaires
Très rare: syndrome de Raynaud.
Affections respiratoires, thoraciques et médiastinales
Fréquence inconnue: épistaxis.
Affections hépatobiliaires
Très rare: élévation de la phosphatase alcaline dans le sang, augmentation de la concentration de bilirubine, troubles de la fonction hépatique allant de l'augmentation des transaminases jusqu'à un coma hépatique, insuffisance hépatique aiguë.
Affections de la peau et du tissu sous-cutané
Très rare: chute de cheveux, érythème, transpiration excessive.
Affections musculosquelettiques et du tissu conjonctif
Très rare: arthralgie, myalgie, spasmes musculaires.
Affections des organes de reproduction et du sein
Rare: gynécomastie.
Très rare: priapisme.
Troubles généraux et anomalies au site d'administration
Rare: diminution de la réponse thérapeutique.
Très rare: douleurs dans la cage thoracique, troubles thoraciques, diminution de l'efficacité du médicament, hyperpyrexie.
Investigations
Rare: perte de poids.
Très rare: diminution du compte de thrombocytes, compte de leucocytes anormal.
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageLors du traitement de patients présentant un surdosage, il faut également tenir compte de la fraction à libération retardée de la formulation de méthylphénidate.
Signes et symptômes
Parmi les signes et symptômes d'un surdosage de Concerta résultant principalement d'une hyperstimulation du système nerveux central et sympathique, on trouve: vomissements, agitation, secousses musculaires, convulsions, grand mal, confusion, hallucinations (auditives et/ou visuelles), transpiration excessive, céphalées, pyrexie, tachycardie, palpitations, augmentation de la fréquence cardiaque, arythmies sinusales, hypertension, mydriase, sécheresse de la bouche et rhabdomyolyse.
Traitement
Le traitement consiste à prendre les mesures de soutien adéquates, en empêchant le patient de se blesser et le protégeant de tout stimulus extérieur qui viendrait aggraver l'hyperstimulation existante. L'efficacité du charbon actif n'a pas été démontrée. Des soins intensifs sont indispensables pour le maintien des fonctions circulatoire et respiratoire. Pour réduire une pyrexie éventuelle, il peut s'avérer nécessaire de rafraîchir le patient par des mesures externes.
L'efficacité de la dialyse péritonéale et de l'hémodialyse n'a pas été établie lors de surdosage de Concerta.
Au cours du traitement de patients surdosés, il faut tenir compte de la libération retardée du méthylphénidate à partir de la formulation de Concerta.
Propriétés/EffetsCode ATC
N06BA04
Mécanisme d'action/Pharmacodynamique
Le chlorhydrate de méthylphénidate est un stimulant du système nerveux central. Son mode d'action thérapeutique sur le TDAH n'est pas connu. On suppose que le méthylphénidate bloque la recapture de la noradrénaline et de la dopamine dans les neurones présynaptiques et renforce la libération de ces monoamines dans l'espace extra-neuronique. Le méthylphénidate est un mélange racémique des isomères d et l, l'isomère d étant plus actif du point de vue pharmacologique que l'isomère l.
Efficacité clinique
Études cliniques
L'efficacité de Concerta dans le traitement du TDAH a été démontrée dans 4 études randomisées, en double aveugle, contrôlées contre placebo menées chez des enfants et des adolescents et dans 2 études en double aveugle, contrôlées contre placebo menées chez des adultes qui présentaient les critères d'un TDAH selon le DSM-IV.
Adultes
Deux études en double aveugle, contrôlées contre placebo, menées chez 627 adultes âgés de 18 à 65 ans ont été réalisées. En ce qui concerne les études contrôlées, il s'agissait d'une étude de titration de la dose avec groupes parallèles, multicentrique, de 7 semaines (étude 02-159) et d'une étude à dose fixe avec groupes parallèles, multicentrique, de 5 semaines (étude 3002), dans lesquelles Concerta utilisé une fois par jour (36 à 108 mg/jour ou 18, 36 et 72 mg/jour) a été comparé avec un placebo.
Dans l'étude 02-159, la variation du critère d'évaluation principal, l'échelle AISR (Adult ADHD Investigator Rating Scale; échelle destinée à l'évaluation du TDAH par l'investigateur chez l'adulte), a été évaluée à la fin de la semaine 7 chez des adultes âgés de 18 à 65 ans atteints de TDAH. Cette étude a comparé Concerta à des doses comprises entre 36 mg/jour et 108 mg/jour, et un placebo. Sur les 226 patients inclus dans cette étude de 7 semaines, 110 ont été randomisés dans le groupe traité par Concerta et 116 dans le groupe placebo. La dose initiale était de 36 mg/jour, mais la dose a été augmentée par paliers de 18 mg/jour (36 à 108 mg/jour), en fonction de la survenue de certains critères d'amélioration en présence d'une tolérance acceptable. Lors de l'évaluation par l'investigateur au cours du dernier rendez-vous de l'étude, une réponse significativement meilleure au score moyen de la variation (moyenne des moindres carrés, SEM) de l'échelle AISR a été observée pour les adultes qui avaient pris Concerta, par rapport aux adultes qui avaient pris le placebo.
L'étude 3002 était une étude dose-réponse multicentrique, en double aveugle, randomisée, contrôlée contre placebo, avec groupes parallèles (durée de 5 semaines) et 3 groupes à dose fixe (18, 36 et 72 mg). Les patients chez qui un TDAH avait été diagnostiqué ont été randomisés pour recevoir soit Concerta à des doses de 18 mg (n=101), 36 mg (n=102), ou 72 mg/jour (n=102), soit un placebo (n=96). Après 5 semaines, les patients adultes des trois groupes qui avaient reçu Concerta ont présenté une réponse significativement meilleure au score global de l'échelle CAARS-SS (Conners' Adult ADHD Rating Scale – Self Report – Short Form (échelle de Conners pour l'évaluation du TDAH chez les adultes)), par rapport aux patients qui avaient pris le placebo.
Adolescents
Une étude randomisée, en double aveugle, multicentrique, contrôlée contre placebo (étude 01-146) menée chez 177 patients âgés de 13 à 18 ans atteints de TDAH a évalué dans quelle mesure des améliorations peuvent être observées après un traitement par Concerta à des doses allant jusqu'à 72 mg/jour (1,4 mg/kg/jour), en comparaison avec un placebo. Sur 220 patients ayant été inclus dans la phase de titration ouverte de 4 semaines, 177 patients sont passés à une dose individualisée (au maximum 72 mg/jour), selon que certains critères d'amélioration de l'échelle d'évaluation du TDAH étaient ou non satisfaits et qu'une tolérance acceptable était constatée lors de l'évaluation globale de l'efficacité. Les patients qui remplissaient ces critères ont ensuite été randomisés pour recevoir leur dose individualisée de Concerta (18-72 mg/jour, n=87) ou le placebo (n=90) durant une phase en double aveugle de deux semaines. À la fin de cette phase, les scores moyens de l'évaluation par l'investigateur obtenus sur l'échelle de l'évaluation du TDAH présentaient des résultats significativement meilleurs pour les adolescents qui avaient pris Concerta que pour ceux qui avaient pris le placebo.
Enfants
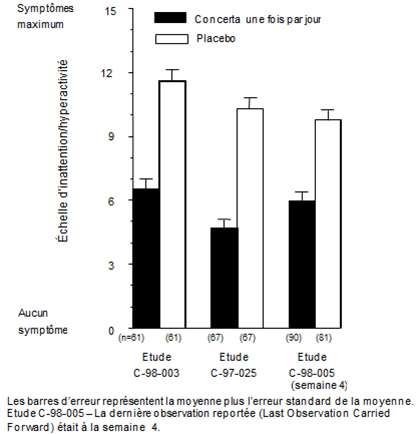
Trois études en double aveugle, contrôlées contre principe actif et placebo, ont été réalisées chez 416 enfants âgés de 6 à 12 ans. Dans les études contrôlées, Concerta utilisé une fois par jour (18, 36 ou 54 mg), le méthylphénidate utilisé trois fois par jour sur une période de 12 heures (dose journalière totale: 15, 30 ou 45 mg) et un placebo ont été comparés dans deux études croisées monocentriques de 3 semaines (études C-98-003 et C-97-025) et dans une étude comparative en groupes parallèles, multicentrique, de 4 semaines (étude C-98-005). Les trois études étaient conçues de façon à démontrer une supériorité de Concerta par rapport au placebo.
Dans les études C-98-003, C-97-025 et C-98-005, les symptômes de TDAH ont été évalués par les enseignants à l'aide de l'échelle de Conners pour l'inattention/hyperactivité avec agression (IOWA). Dans les trois études contrôlées, les enfants qui avaient reçu Concerta présentaient unanimement un classement significativement meilleur au niveau de la sous-échelle inattention/hyperactivité en comparaison avec le placebo. Les valeurs pour Concerta et le placebo des trois études sont illustrées dans la figure 1.
Figure 1. Evaluation moyenne de l'inattention/hyperactivité des enfants par leur enseignant au moyen de l'échelle de Conners pour l'IOWA lors de l'utilisation de Concerta.
PharmacocinétiqueAbsorption
Le méthylphénidate est absorbé rapidement. Après administration orale de Concerta à des adultes, les concentrations plasmatiques augmentent rapidement et atteignent le premier maximum au bout de 1 à 2 heures, pour continuer à augmenter légèrement ensuite pendant plusieurs heures. Au bout de 6 à 8 heures, la concentration plasmatique atteint son pic, à partir duquel une lente diminution du taux plasmatique de méthylphénidate s'amorce. Administré une fois par jour, Concerta réduit par sa libération continue du principe actif les fluctuations entre concentrations hautes et basses, comme elles se manifestent en cas d'administration de méthylphénidate trois fois par jour, ce qui se retrouve dans les profils des concentrations plasmatiques moyennes en fonction du temps. La biodisponibilité relative de Concerta administré une fois par jour et du méthylphénidate administré 3 fois par jour est comparable.
Les moyennes des paramètres pharmacocinétiques de 36 adultes après administration de Concerta (18 mg une fois par jour) et du chlorhydrate de méthylphénidate (5 mg 3 fois par jour) étaient comparables en termes de Cmax (ng/ml), Tmax (h), AUCinf (ng h/ml) et demi-vie (h).
On n'a constaté aucune différence entre les paramètres pharmacocinétiques de Concerta après administration une fois et plusieurs fois par jour, ce qui laisse supposer qu'il n'y a aucune accumulation significative de substance active dans le corps. L'aire sous la courbe (AUC) tout comme la demi-vie t½ montrent, après administration plusieurs fois par jour, des valeurs semblables à celles obtenues après la première dose de Concerta.
Concerta est presque complètement résorbé, comme avec le méthylphénidate non retardé. En raison du métabolisme de premier passage, la disponibilité systémique du méthylphénidate varie individuellement de 11 à 51%.
Proportionnalité de la dose
Après administration de Concerta en doses uniques de 18, 36 et 54 mg/jour à des adultes en bonne santé, les valeurs Cmax et AUC(0-inf) du d-méthylphénidate étaient proportionnelles à la dose, tandis que Cmax et AUC(0-inf) du l-méthylphénidate ne l'étaient pas. Lors de l'administration de Concerta, les concentrations plasmatiques de l'isomère l, pharmacologiquement moins actif, atteignaient à peu près 1/40ème de celles de l'isomère d actif. Ceci est dû à l'effet de premier passage énantiomère-sélectif.
Des doses uniques ou répétées une fois par jour de 54 à 144 mg/jour de Concerta ont provoqué sur des adultes sains des augmentations linéaires et proportionnelles à la dose de la Cmax et de l'AUCinf du méthylphénidate global (MPH) et de son métabolite le plus important: l'acide (alpha)-phénylpipéridine-acétique. La clairance de la dose unique et à l'état d'équilibre (jour 4) et les paramètres de demi-vie étaient semblables, ce qui indique que le méthylphénidate ne dépend pas du temps dans la pharmacocinétique. La relation entre le métabolite (l'acide [alpha]-phénylpipéridineacétique) et la substance de départ (MPH) était constante à des posologies de 54 à 144 mg/jour autant après une dose unique qu'après des doses répétées.
Dans une étude à doses répétées chez des patients adolescents atteints de TDAH âgés de 13 à 16 ans, recevant des doses de Concerta entre 18 et 72 mg/jour, l'augmentation de la Cmax et l'AUCTAU du d-méthylphénidate et/ou du méthylphénidate total était proportionnelle à la dose.
Distribution
Les concentrations plasmatiques de méthylphénidate chutent biexponentiellement après administration orale. La demi-vie du méthylphénidate chez les adultes après administration de Concerta était d'environ 3,5 heures.
Métabolisme
Chez l'homme, le méthylphénidate est d'abord métabolisé par scission du groupe ester en acide (alpha)-phénylpipéridineacétique (PPAA), qui n'a qu'un faible effet pharmacologique, sinon aucun. Le métabolisme de Concerta administré une fois par jour, déterminé par la dégradation en PPAA, est semblable à celui du méthylphénidate administré trois fois par jour. Le métabolisme d'une dose unique de Concerta par jour montre des valeurs semblables à celui de plusieurs doses répétées par jour.
Élimination
Après administration orale de méthylphénidate avec marquage radioactif à des personnes, on a pu déceler environ 90% de la radioactivité dans l'urine. Le métabolite le plus important dans l'urine était le PPAA; il correspondait à environ 80% de la dose.
Effet de la nourriture prise simultanément
On n'a constaté aucune différence ni dans les paramètres pharmacocinétiques, ni dans les paramètres pharmacodynamiques, quand Concerta était pris après un petit-déjeuner riche en graisses. Il n'y a aucune indication que la biodisponibilité puisse être influencée par la prise concomitante de nourriture.
Cinétique pour certains groupes de patients
Sexe: chez les adultes sains à qui Concerta a été administré, les valeurs moyennes corrigées en fonction de la dose pour AUC(0-inf) étaient de 36,7 ng·h/ml pour les hommes et de 37,1 ng·h/ml pour les femmes. Aucune différence n'a pu être constatée entre les deux groupes.
Ethnie: chez les adultes à qui Concerta a été administré, les valeurs moyennes corrigées en fonction de la dose pour AUC(0-inf) étaient cohérentes dans les divers groupes ethniques; mais il se peut également qu'on n'ait pas pu démontrer de différences ethniques en raison des chiffres de population trop faibles.
Age: la pharmacocinétique de Concerta n'a pas été étudiée chez les enfants de moins de 6 ans.
Troubles de la fonction hépatique
Il n'existe pas d'expérience sur l'utilisation de Concerta chez des patients présentant une insuffisance hépatique.
Troubles de la fonction rénale
Il n'existe pas d'expérience sur l'utilisation de Concerta chez des patients présentant une insuffisance rénale. Après administration orale de méthylphénidate avec marquage radioactif à des personnes, celui-ci a été en grande partie métabolisé et environ 80% de la radioactivité ont été éliminés par les reins sous forme de PPAA. Comme la clairance rénale n'a pas une grande importance pour la clairance du méthylphénidate, on suppose qu'une insuffisance rénale n'a qu'un effet limité sur la pharmacocinétique de Concerta.
Données précliniquesAucun effet toxique n'a été observé chez les chiens dans deux études de 30 jours distinctes, au cours desquelles Concerta était donné en doses orales de 72 mg/jour (jusqu'à 8,6 mg/kg/jour) pour l'une et de 144 mg/jour (jusqu'à 22 mg/kg/jour) pour la seconde.
Génotoxicité
Dans le test in-vitro d'Ames (Reverse Mutation Assay) et dans l'essai in vitro Mouse Lymphoma Cell Forward Mutation Assay, aucun effet mutagène du méthylphénidate n'a été décelable. L'échange de chromatides sœurs (sister chromatid exchange) et les transformations chromosomiques (chromosome aberrations) ont montré dans un test in-vitro sur des cultures cellulaires d'ovules du hamster chinois des valeurs plus élevées, même si ce n'était qu'après des doses cytotoxiques élevées. Le méthylphénidate s'est révélé négatif invivo dans le test des micronoyaux de la moelle épinière des souris.
Carcinogénicité
Dans une étude de carcinogénicité à vie sur des souris, le chlorhydrate de méthylphénidate administré à une posologie d'environ 60 mg/kg/jour a entraîné une augmentation des adénomes hépatocellulaires et, mais seulement chez les mâles, des hépatoblastomes. Cette dose est en mg/kg nettement plus élevée que la posologie recommandée pour les humains. L'administration unique en bolus d'une telle dose a entraîné chez les souris une exposition systémique au méthylphénidate plus élevée. Dans l'ensemble on n'a constaté aucune augmentation de tumeurs hépatiques malignes. La race de souris utilisée est sujette au développement de tumeurs hépatiques et la force probante de ces résultats pour les humains n'est pas certaine.
Dans une étude à vie d'objectif semblable sur des rats et avec une posologie allant jusqu'à 45 mg/kg/jour, on n'a trouvé aucune indication de carcinogénicité.
Dans une étude de 24 semaines sur la souche de souris transgénique p53±, aucun indice de carcinogénicité n'a été mis en évidence à des posologies allant jusqu'à 74 mg/kg/jour de chlorhydrate de méthylphénidate.
Toxicité pour la reproduction
A des dosages de 200 mg/kg/jour, des effets tératogènes du chlorhydrate de méthylphénidate ont été détectés chez les lapines. Ce dosage correspond à environ 100 fois la dose maximale journalière en mg/kg recommandée chez les humains.
Chez les rats, aucun effet tératogène n'a été observé à des dosages de chlorhydrate de méthylphénidate allant jusqu'à 30 mg/kg/jour. Cela correspond, sur la base des données pharmacologiques, à environ 7 fois l'exposition systémique au méthylphénidate rapportée dans les études sur des volontaires et des patients avec la posologie maximale recommandée de Concerta.
Dans une étude de reproduction continue pendant 18 semaines sur des souris, le chlorhydrate de méthylphénidate, administré à des doses allant jusqu'à 160 mg/kg/jour, n'a montré aucune diminution de la fertilité.
Remarques particulièresStabilité
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur l'emballage.
Remarques particulières concernant le stockage
Conserver à température ambiante (15–25 °C).
Conserver le récipient bien fermé.
Conserver hors de portée des enfants.
Numéro d’autorisation56249 (Swissmedic).
PrésentationConcerta comprimés à libération prolongée 18 mg: 30. (A+)
Concerta comprimés à libération prolongée 18 mg: 60 (2 × 30). (A+)
Concerta comprimés à libération prolongée 27 mg: 30. (A+)
Concerta comprimés à libération prolongée 27 mg: 60 (2 × 30). (A+)
Concerta comprimés à libération prolongée 36 mg: 30. (A+)
Concerta comprimés à libération prolongée 36 mg: 60 (2 × 30). (A+)
Concerta comprimés à libération prolongée 54 mg: 30. (A+)
Concerta comprimés à libération prolongée 54 mg: 60 (2 × 30). (A+)
Titulaire de l’autorisationJanssen-Cilag AG, Zug, ZG.
Mise à jour de l’informationDécembre 2023.
|

