Propriétés/EffetsCode ATC
C03DA04
Mécanisme d'action
Voir «Pharmacodynamique».
Pharmacodynamique
L'éplérénone présente une sélectivité relative dans sa fixation aux récepteurs minéralocorticoïdes humains recombinants en comparaison de sa fixation aux récepteurs humains recombinants aux glucocorticoïdes, à la progestérone et aux androgènes. L'éplérénone empêche la fixation de l'aldostérone.
Efficacité clinique
L'éplérénone a été évaluée dans l'étude «Eplerenone Post-Acute Myocardial Infarction Heart Failure Efficacy and Survival Study» (EPHESUS). EPHESUS est une étude multicentrique, en double aveugle et contrôlée par placebo, menée chez n=6632 patients (moyenne du suivi: 16 mois) ayant eu un infarctus du myocarde aigu, présentant une dysfonction ventriculaire gauche (avec une fraction d'éjection ventriculaire gauche [FEVG] ≤40%) et des signes cliniques d'insuffisance cardiaque. L'inclusion des patients après randomisation dans l'étude EPHESUS a eu lieu dans les 3 à 14 jours suivant la pose du diagnostic d'infarctus du myocarde. La durée moyenne jusqu'à l'inclusion était de 7 jours. En raison du risque cardiovasculaire accru associé au diabète, les patients diabétiques présentant une dysfonction ventriculaire gauche et sans symptômes d'insuffisance cardiaque ont été inclus dans l'étude; 10% de la population de l'étude remplissait ce critère. En plus d'un traitement standard, les patients ont reçu de l'éplérénone ou un placebo à une dose initiale de 25 mg une fois par jour, avec augmentation de la posologie en l'espace de 4 semaines jusqu'à la dose d'entretien de 50 mg une fois par jour si la kaliémie était <5.0 mEq/l. Pendant l'étude, les patients ont reçu un traitement standard comportant de l'aspirine (92%), des inhibiteurs de l'ECA (90%), des bêtabloquants (83%), des dérivés nitrés (72%), des diurétiques de l'anse (66%) ou des inhibiteurs de la HMG-CoA réductase (60%).
Dans l'étude EPHESUS, les critères primaires d'évaluation étaient la mortalité toutes causes confondues et un critère combiné de mortalité cardiovasculaire ou d'hospitalisation d'origine cardiovasculaire. 14.4% des patients recevant l'éplérénone et 16.7% des patients recevant le placebo sont décédés (toutes causes confondues), alors que 26.7% des patients recevant l'éplérénone et 30.0% des patients recevant le placebo ont présenté le critère combiné de mortalité cardiovasculaire ou d'hospitalisation d'origine cardiovasculaire. Ainsi, dans l'étude EPHESUS, l'éplérénone a réduit le risque de mortalité toutes causes confondues de 15% (réduction du risque absolu 2.3%, RR 0.85; intervalle de confiance à 95%, 0.75-0.96; p=0.008; NNT: 43) en comparaison du placebo, essentiellement en réduisant la mortalité cardiovasculaire. Le risque de mortalité cardiovasculaire ou d'hospitalisation d'origine cardiovasculaire a été réduit de 13% avec l'éplérénone (réduction du risque absolu 3.3%; RR 0.87; intervalle de confiance à 95%, 0.79-0.95; p=0.002; NNT: 31).
L'efficacité clinique d'un traitement par éplérénone a été démontrée essentiellement lorsque les patients étaient <75 ans. Les bénéfices du traitement chez les patients ≥75 ans sont incertains. La classification fonctionnelle de NYHA s'est améliorée ou est restée stable (p<0.001) pour une proportion significativement plus élevée de patients traités par éplérénone (n=2'372 patients, 75.3%) par rapport au groupe placebo (n=2242 patients, 71.3%).
Figure 1: Rapport des risques pour toutes les causes de mortalité par sous-groupe
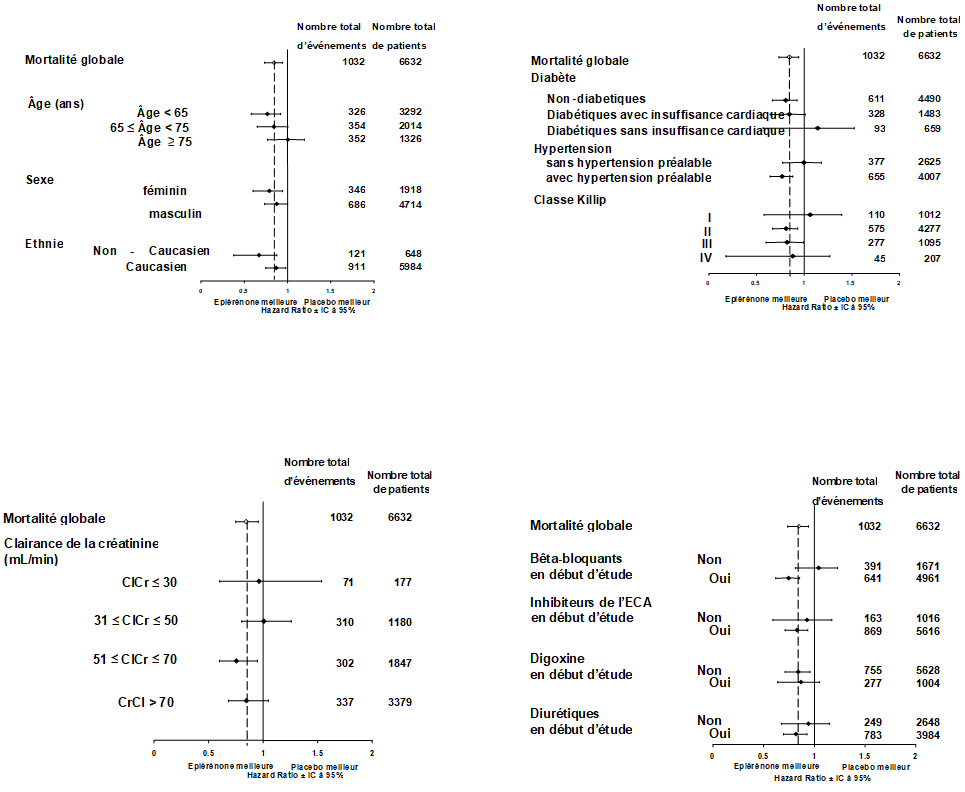
Dans l'étude EMPHASIS-HF (Eplerenone in Mild Patients Hospitalization and Survival Study in Heart Failure), l'éplérénone a été évaluée en complément à un traitement standard chez des patients présentant une insuffisance cardiaque systolique et des symptômes légers (classe fonctionnelle II selon la NYHA). Aucun patient des classes fonctionnelles III et IV selon la NYHA n'a été évalué dans l'étude.
Les patients inclus dans l'étude avaient ≥55 ans et présentaient une fraction d'éjection ventriculaire gauche (FEVG) ≤30% ou une FEVG ≤35% et en plus une durée du QRS >130 msec. En outre, les participants à l'étude devaient soit avoir été hospitalisés dans les 6 mois précédents pour une cause cardiovasculaire (CV), soit présenter un taux plasmatique de BNP ≥250 pg/ml ou un taux de pro-BNP ≥500 pg/ml (hommes) ou ≥750 pg/ml (femmes). Le traitement par l'éplérénone a été commencé à la posologie de 25 mg une fois par jour, posologie qui a été augmentée à 50 mg une fois par jour après 4 semaines dans la mesure où les taux sériques de potassium étaient <5.0 mmol/l et le TFGe ≥50 ml/min. Comme alternative, si le taux de filtration glomérulaire estimé était compris entre 30 et 49 ml/min/1.73 m2, le traitement par l'éplérénone a été commencé à la posologie de 25 mg tous les 2 jours, posologie qui a pu être augmentée à 25 mg une fois par jour.
Les médicaments cardiovasculaires les plus fréquemment associés à l'éplérénone ou au placebo chez l'ensemble des n=2737 participants à l'étude ont été des diurétiques (85%), des inhibiteurs de l'ECA (78%), des antagonistes des récepteurs de l'angiotensine II (19%), des bêtabloquants (87%), des médicaments antithrombotiques (88%), des hypolipémiants (63%) et des alcaloïdes de la digitale (27%). La FEVG moyenne était de 26% et la durée moyenne du QRS était d'environ 122 msec. La plupart des patients (83.4%) avaient été hospitalisés pour des causes cardiovasculaires dans les 6 derniers mois précédant la randomisation et env. 50% pour une insuffisance cardiaque. Environ 20% des patients étaient pourvus d'un défibrillateur implanté ou bénéficiaient d'un traitement de resynchronisation cardiaque.
Le critère d'évaluation principal (décès d'origine cardiovasculaire ou hospitalisation pour insuffisance cardiaque) a été observé chez n=249 patients (18.3%) du groupe éplérénone et chez n=356 patients (25.9%) du groupe placebo (RR 0.63, IC à 95%, 0.54-0.74; p<0.001). Ce résultat a été cohérent dans tous les sous-groupes étudiés.
Le critère d'évaluation secondaire, à savoir la mortalité toutes causes confondues, a été observé chez n=171 patients (12.5%) du groupe éplérénone et chez n=213 patients (15.5%) du groupe placebo (RR 0.76; IC à 95%, 0.62-0.93; p=0.008). Un décès d'origine cardiovasculaire a été rapporté chez n=147 patients (10.8%) du groupe éplérénone et chez n=185 patients (13.5%) du groupe placebo (RR 0.76; IC à 95%, 0.61-0.94; p=0.01).
Une hyperkaliémie (taux sérique de potassium >5.5 mmol/l) a été rapportée au cours de l'étude chez n=158 patients (11.8%) du groupe éplérénone et chez n=96 patients (7.2%) du groupe placebo (p<0.001). Une hypokaliémie, définie comme un taux sérique de potassium <4.0 mmol/l, est survenue plus rarement avec l'éplérénone qu'avec le placebo (38.9% avec l'éplérénone en comparaison de 48.4% avec le placebo, p<0.0001).
| 
