Propriétés/EffetsCode ATC
N04BC09
Mécanisme d'action
La rotigotine est un agoniste dopaminergique D3/D2/D1 de type non ergoline destiné au traitement symptomatique de la maladie de Parkinson idiopathique et du syndrome des jambes sans repos idiopathique.
Conformément à l'activité fonctionnelle au niveau des différents sous-types de récepteurs et de leur répartition dans le cerveau, la rotigotine est décrite comme un agoniste des récepteurs D2 et D3, ayant également une efficacité au niveau des récepteurs D1, D4 et D5. Au niveau des récepteurs non dopaminergiques, la rotigotine montre un antagonisme au niveau des récepteurs alpha2B et un agonisme au niveau du récepteur 5HT-1A, par contre aucune activité au niveau des récepteurs 5HT2B.
On suppose que l'effet bénéfique de la rotigotine sur la maladie de Parkinson est lié à l'activation des récepteurs D3, D2 et D1 au niveau du noyau caudé et du putamen dans le cerveau.
Le mécanisme d'action précis de la rotigotine dans le traitement du SJSR n'est pas connu. On suppose que la rotigotine exerce principalement son effet par le biais des récepteurs dopaminergiques.
Pharmacodynamique
N'est pas applicable.
Efficacité clinique
Études cliniques relatives au syndrome des jambes sans repos
L'efficacité de Neupro a été évaluée au cours de 5 études contrôlées versus placebo sur plus de 1'400 patients souffrant du syndrome des jambes sans repos (SJSR). Son efficacité a été démontrée au cours d'études contrôlées chez des patients traités jusqu'à 29 semaines. L'effet s'est maintenu sur une période de 6 mois.
Les critères principaux d'efficacité ont été les changements par rapport aux valeurs initiales sur l'échelle IRLS (International Restless Legs Syndrom) et de l'item n° 1 de la CGI (gravité de la maladie). Pour les deux critères principaux, des différences statistiquement significatives ont été observées pour les doses de 1 mg/24 h, de 2 mg/24 h et de 3 mg/24 h comparé au placebo. Après un traitement d'entretien de 6 mois chez des patients souffrant de SJSR modéré à sévère, le score IRLS initial a été amélioré de 30,7 à 20,7 dans le groupe placebo et de 30,2 à 13,8 dans le groupe Neupro. La différence moyenne ajustée a été de –6,5 points (IC 95% –8,7; –4,4, p <0,0001).
Le taux de répondeurs sur l'item 1 de la CGI (fortement amélioré, très fortement amélioré) ont été de 43,0% et 67,5% respectivement pour le placebo et Neupro (différence 24,5% IC 95%; 14,2%; 34,8%, p <0,0001).
Dans une étude contrôlée versus placebo d'une durée de 7 semaines, les paramètres polysomnographiques ont été étudiés. Neupro a significativement réduit l'indice des mouvements périodiques des membres (PLMI: Periodic Limb Movement Index) de 50,9 à 7,7 contre 37,4 à 32,7 dans le groupe placebo (p <0,0001).
Études cliniques relatives à la maladie de Parkinson
L'efficacité de Neupro dans le traitement symptomatique de la maladie de Parkinson idiopathique a été évaluée dans le cadre de quatre études menées en groupes parallèles, randomisées en double aveugle et contrôlées contre placebo. D'autres travaux ont porté sur l'efficacité de la rigotine concernant certains aspects spécifiques de la maladie de Parkinson.
Deux études pivots ont porté sur l'efficacité de Neupro en monothérapie dans le traitement symptomatique de la maladie de Parkinson idiopathique au stade précoce. Les patients inclus dans ces études ne recevaient aucun traitement par un agoniste de la dopamine et la durée d'un éventuel traitement antérieur par la Levodopa était au moins inférieure à 6 mois avant l'inclusion dans l'étude.
L'évaluation primaire du résultat s'est faite sur la base du score des deux composantes Activités de la vie quotidienne (ADL, partie II) et Motricité (partie III) de l'échelle UPDRS «Unified Parkinson's Disease Rating Scale».
L'efficacité a été déterminée par la réponse des patients au traitement, mesurée à l'amélioration du taux de répondeurs et de la somme absolue en nombre de points des scores ADL et Examen moteur combinés (parties II + III de l'échelle UPDRS).
Dans l'une des études en double aveugle, 177 patients ont reçu de la rotigotine et 96 ont reçu un placebo. Partant d'une dose initiale de 2 mg/24 h, la dose individuelle optimale de rotigotine ou de placebo a été obtenue au terme d'une augmentation par paliers hebdomadaires de 2 mg/24 h jusqu'à une dose maximale de 6 mg/24 h. Les patients de chaque groupe de traitement ont continué de recevoir leur dose optimale pendant 6 mois.
À la fin du traitement d'entretien, 91% des sujets du groupe rotigotine avaient pour dose optimale la dose maximale autorisée dans cette étude, à savoir 6 mg/24 h. Une amélioration de 20% a été observée chez 48% des sujets recevant de la rotigotine et chez 19% des sujets recevant un placebo (différence: 29%, IC95% 18% – 39%, p <0,0001). L'amélioration moyenne du score UPDRS (parties II + III) par la rotigotine était de –3,98 points (valeur initiale: 29,9 points), tandis qu'on observait une péjoration de 1,31 point (valeur initiale: 30,0 points) dans le groupe traité par placebo. La différence, de 5,28 points, était statistiquement significative (p <0,0001).
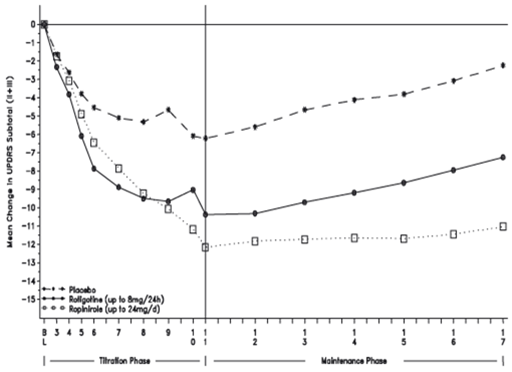
Dans une seconde étude en double aveugle, 213 patients ont reçu de la rotigotine, 227 ont reçu du ropinirole et 117 un placebo. Partant d'une dose initiale de 2 mg/24 h, la dose individuelle optimale de rotigotine a été obtenue au terme d'une augmentation de 2 mg/24 h par paliers hebdomadaires sur 4 semaines jusqu'à une dose maximale de 8 mg/24 h. Chez les patients du groupe ropinirole, la dose optimale (au maximum 24 mg/jour) a été atteinte en 13 semaines. Les patients de chaque groupe de traitement ont ensuite été maintenus sous ce traitement d'entretien pendant 6 mois.
À la fin du traitement d'entretien (étude n° 17 dans le graphique ci-dessous), la dose optimale correspondait à la dose maximale autorisée, à savoir 8 mg/24 h, chez 92% des sujets du groupe rotigotine. Une amélioration de 20% a été observée chez 52% des sujets recevant de la rotigotine, 68% des sujets recevant du ropinirole et 30% des sujets sous placebo (différence rotigotine vs placebo: 21,7%, IC95% 11,1% – 32,4%; différence ropinirole vs placebo: 38,4%, IC95% 28,1% – 48,6%; différence ropinirole vs rotigotine: 16,6%, IC95% 7,6% – 25,7%). L'amélioration moyenne du score UPDRS (parties II+III) était de 6,83 points pour le bras rotigotine (valeur initiale: 33,2 points), de 10,78 points pour le bras ropinirole (valeur initiale: 32,2 points) et de 2,33 points pour le bras placebo (valeur initiale: 31,3 points). Toutes les différences entre traitements actifs et placebo étaient statistiquement significatives. Cette étude n'a pas permis de démontrer la non-infériorité de la rigotine par rapport au ropinirole.
Une étude ouverte multicentrique et multinationale effectuée ultérieurement a porté sur la tolérance d'un changement de traitement consistant à remplacer pendant la nuit le ropinirole, le pramipexole ou la cabergoline par un patch de rotigotine. L'efficacité de cette substitution sur les symptômes de la maladie de Parkinson idiopathique faisait également l'objet de ce travail. 116 patients traités jusqu'ici par voie orale ont reçu une dose de rigotine pouvant atteindre 8 mg/24 h. Parmi eux, 47 étaient traités au ropinirole à une dose de 9 mg par jour maximum, 47 au pramipexole à 2 mg par jour maximum et 22 à la cabergoline à 3 mg par jour maximum. La substitution à la rigotine s'est révélée réalisable, la posologie n'ayant dû être légèrement ajustée (2 mg/24 h en moyenne) que chez 2 des patients traités au ropinirole, 5 des patients traités au pramipexole et 4 des patients traités à la cabergoline. Des améliorations du score UPDRS, parties I à IV, ont été observées. Il n'y avait pas de modification du profil de sécurité par rapport aux études antérieures.
Deux études pivot supplémentaires ont été réalisées chez des patients sous traitement concomitant par la lévodopa. Le critère principal d'évaluation du résultat était la réduction du temps «off» (en heures). L'efficacité a été déterminée par la réponse du sujet au traitement en termes de répondeur et d'amélioration absolue du temps «off».
Lors d'une étude en double aveugle, 113 patients ont reçu de la rotigotine à une dose maximale de 8 mg/24 h, 109 patients ont reçu de la rotigotine à une dose maximale de 12 mg/24 h et 119 patients ont reçu un placebo.
La dose optimale de rotigotine ou de placebo a été obtenue par une augmentation hebdomadaire de 2 mg/24 h en débutant à 4 mg/24 h.
Les patients de chaque groupe de traitement ont été maintenus à leur dose optimale pendant 6 mois. À la fin du traitement d'entretien, on a constaté une amélioration d'au moins 30% chez 57% et 55% des sujets traités à la rotigotine aux doses respectives de 8 mg/24 h et 12 mg/24 h et chez 34% des sujets recevant un placebo (différence: 22% et 21% respectivement, IC95% 10% – 35% et 8% – 33% respectivement, p <0,001 pour les deux groupes rotigotine). Avec la rotigotine, les réductions moyennes du temps «off» ont été respectivement de 2,7 et 2,1 heures, tandis que dans le groupe placebo il a été observé une réduction de 0,9 heures. Les différences étaient statistiquement significatives (p <0,001 et p= 0,003 respectivement).
Au cours d'une seconde étude en double aveugle, 201 patients ont reçu de la rotigotine, 200 ont reçu du pramipexole et 100 patients ont reçu un placebo. La dose optimale de rotigotine a été obtenue par une augmentation hebdomadaire de 2 mg/24 h en débutant à 4 mg/24 h jusqu'à une dose maximale de 16 mg/24 h. Les patients du groupe pramipexole ont reçu 0,375 mg la première semaine, 0,75 mg la deuxième semaine et la dose a ensuite été augmentée de 0,75 mg par semaine jusqu'à la dose individuelle optimale, avec un maximum de 4,5 mg/jour. Les patients de chaque groupe de traitement ont été maintenus à leur dose optimale pendant 4 mois.
À la fin du traitement d'entretien, on a constaté une amélioration d'au moins 30% de la période «off» absolue chez 60% des sujets traités par la rotigotine, chez 67% des sujets traités par pramipexole et chez 35% des sujets recevant un placebo (différence rotigotine versus placebo: 25%, IC95% 13%; 36%, différence pramipexole versus placebo: 32%, IC95% 21%; 43%, différence pramipexole versus rotigotine: 7%, IC95% –2%; 17%). La non-infériorité par rapport au pramipexole n'a ainsi pas été mise en évidence.
La réduction moyenne du temps «off» a été de 2,5 heures dans le groupe rotigotine, de 2,8 heures dans le groupe pramipexole et de 0,9 heures dans le groupe placebo. Toutes les différences entre traitements actifs et placebo ont été statistiquement significatives.
Une autre étude multinationale a été menée en double aveugle sur 287 patients atteints de la maladie de Parkinson au stade précoce ou au stade avancé accompagnée d'un contrôle insuffisant de la mobilité matinale. 81,5% des patients ont été en outre traités par la lévodopa. 190 patients ont reçu de la rotigotine et 97 un placebo. Les patients ont été titrés sur une période de 8 semaines en commençant par une dose de 2 mg/24 h par paliers de 2 mg/24 h par semaine à la dose optimale de rotigotine ou de placebo jusqu'à la dose maximale de 16 mg/24 h et ces doses d'entretien ont été maintenues pendant 4 semaines. Les paramètres cibles co-primaires étaient la mobilité matinale, mesurée par la Unified Parkinson's Disease Rating Scale (UPDRS III) et les troubles du sommeil nocturne, mesurés par la Parkinson's Disease Sleep Scale (PDSS-2) modifiée. À la fin de la phase d'entretien, la valeur UPDRS III des patients traités par la rotigotine (initialement 29,6) s'était améliorée de 7,0 points et la valeur des patients du groupe placebo (initialement 32,0) s'était améliorée de 3,9 points. L'augmentation de la valeur totale de la PDSS-2 dans le groupe rotigotine était de 5,9 points (initialement 19,3) et de 1,9 points dans le groupe placebo (initialement 20,5). Les différences de traitements pour les variables co-primaires étaient statistiquement significatives (p= 0,0002 et p <0,0001).
|

