CompositionPrincipes actifs
Gestodène, éthinylestradiol.
Excipients
Calcium édétate de sodium (contient 0.02 mg de sodium), lactose monohydraté 36.87 mg, amidon de maïs, povidone K25, stéarate de magnésium, saccharose 19.63 mg, povidone, macrogol 6000, carbonate de calcium, talc, cire montan.
Indications/Possibilités d’emploiContraception hormonale.
La décision de prescrire Femadiol-Mepha 20 doit être prise en tenant compte des facteurs de risque de la patiente, notamment ses facteurs de risque de thromboembolie veineuse (TEV), ainsi que du risque de TEV associé à Femadiol-Mepha 20 en comparaison aux autres CHC (Contraceptifs Hormonaux Combinés) (voir rubriques «Contre-indications» et «Mises en garde et précautions»).
Posologie/Mode d’emploiLes CHC tels que Femadiol-Mepha 20 ne devraient être prescrits que par des médecins ayant l'expérience de ces traitements et qui sont en mesure, d'une part, de fournir aux patientes toutes les explications requises sur les avantages et inconvénients de toutes les méthodes contraceptives disponibles et, d'autre part, de procéder à un examen général et gynécologique.
La prescription d'un CHC doit en principe se faire conformément aux dernières recommandations de la Société Suisse de Gynécologie et d'Obstétrique (SSGO).
Les dragées doivent être prises dans l'ordre indiqué sur la plaquette, si possible à la même heure de la journée et de préférence avec du liquide. Une dragée par jour est prise pendant 21 jours successifs. Il s'ensuit une pause de 7 jours sans prise de dragée avant de commencer la prochaine plaquette. Il se produit habituellement pendant cette pause une hémorragie de privation qui apparaît normalement 2 à 3 jours après la prise de la dernière dragée et peut encore persister alors que la prochaine plaquette est déjà commencée.
Début de la prise
Femmes n'ayant pas utilisé de contraceptifs hormonaux le mois précédent
Il faut commencer la prise des dragées le 1er jour du cycle (= 1er jour des règles). Il est aussi possible de commencer du 2e au 5e jour, mais il est alors recommandé d'utiliser d'autres méthodes contraceptives non hormonales en complément (p.ex. des préservatifs, mais pas la méthode d'abstinence périodique d'Ogino-Knaus ou la méthode des températures) pendant les 7 premiers jours de la prise de dragées lors du 1er cycle.
Remplacement d'un autre contraceptif oral combiné (COC), anneau vaginal ou patch transdermique
La prise de Femadiol-Mepha 20 se fait de préférence le lendemain de la prise de la dernière dragée active du COC précédent, au plus tard cependant le lendemain du dernier jour de l'intervalle habituel sans dragée ou de la phase placebo. Lors du remplacement d'un anneau vaginal ou d'un patch transdermique, la prise de Femadiol-Mepha 20 commence de préférence le jour du retrait du dernier anneau ou du dernier patch, ou au plus tard au moment où l'application suivante aurait été prévue.
Remplacement d'une préparation progestative seule (minipilule, injection, implant, dispositif intra-utérin délivrant un progestatif [DIU])
Le remplacement de la minipilule peut se faire un jour quelconque, celui d'un implant ou d'un DIU délivrant un progestatif au plus tôt le jour du retrait et celui d'une préparation injectable au moment où la prochaine injection devrait être faite. Dans tous ces cas, il faut utiliser d'autres méthodes contraceptives non hormonales pendant les 7 premiers jours de la prise des dragées.
Après un avortement dans le 1er trimestre de la grossesse
La prise de Femadiol-Mepha 20 peut être immédiate. Le recours à d'autres méthodes contraceptives est alors inutile.
Après un avortement au 2e trimestre de grossesse ou un accouchement
La décision quant à la (re)prise d'un CHC tel que Femadiol-Mepha 20 après un avortement au 2e trimestre de grossesse ou un accouchement doit tenir compte du risque accru d'accidents thromboemboliques veineux pendant la période puerpérale (jusqu'à 12 semaines après l'accouchement ou l'avortement; cf. «Mises en garde et précautions»).
Dans tous les cas, après un accouchement ou un avortement au 2e trimestre de grossesse, la prise de Femadiol-Mepha 20 doit débuter au plus tôt entre le 21e et le 28e jour. Si le traitement débute plus tard, il est recommandé d'appliquer des méthodes contraceptives supplémentaires non hormonales durant les 7 premiers jours de la prise. Si des rapports sexuels ont eu lieu entre-temps, il convient d'exclure l'éventualité d'une grossesse ou d'attendre les premières règles avant de débuter le traitement.
Conduite à tenir en cas d'oubli de dragée(s)
Si la patiente s'aperçoit dans un intervalle de 12 heures qu'elle a oublié de prendre une dragée à l'heure habituelle, elle devra prendre celle-ci immédiatement. Les dragées suivantes seront à nouveau prises à l'heure habituelle. La protection contraceptive n'est alors pas compromise.
Si plus de 12 heures se sont écoulées depuis l'heure habituelle de la prise, il se peut que la protection contraceptive soit réduite. Les deux règles de base suivantes s'appliquent en cas d'oubli de dragée(s):
1.La prise ne doit jamais être interrompue plus de 7 jours.
2.Une prise régulière pendant au moins 7 jours est nécessaire pour réprimer efficacement l'axe hypothalamo-hypophyso-ovarien.
Il en résulte la conduite à tenir suivante, en fonction de la semaine de prise:
1re semaine de prise
La patiente doit prendre la dragée oubliée dès qu'elle s'en aperçoit – même si cela implique la prise de 2 dragées le même jour. Les dragées suivantes devront à nouveau être prises à l'heure habituelle. Pendant les 7 jours suivants, la patiente devra utiliser une autre méthode contraceptive non hormonale. Si la patiente a eu des rapports sexuels pendant les 7 jours précédents, il faudra tenir compte de l'éventualité d'une grossesse. Plus le nombre de dragées oubliées est grand et plus cet oubli est proche de l'intervalle sans dragée, plus le risque de grossesse est élevé.
2e semaine de prise
La patiente devra prendre la dragée oubliée dès qu'elle s'en aperçoit, même si cela implique la prise de 2 dragées le même jour. Les dragées suivantes devront être prises à l'heure habituelle. À condition que la prise ait été régulière les 7 jours précédents, aucune autre mesure contraceptive n'est nécessaire. Si cela n'a pas été le cas ou si plusieurs dragées ont été oubliées, la patiente devra utiliser d'autres méthodes contraceptives non hormonales pendant les 7 jours suivants.
3e semaine de prise
Étant donné la proximité de l'intervalle sans dragée, le risque de grossesse est accru. Lorsque la patiente utilise une des possibilités de prise suivantes, il ne lui est pas nécessaire d'utiliser d'autres méthodes contraceptives, pour autant qu'elle ait pris régulièrement les dragées pendant les 7 jours précédents. Dans le cas contraire, il lui faudra suivre la première des deux possibilités et utiliser une méthode contraceptive non hormonale pendant les 7 jours suivants.
a.La patiente doit prendre la dragée oubliée dès qu'elle s'en aperçoit – même si cela implique la prise de 2 dragées le même jour. Les dragées suivantes devront être prises à l'heure habituelle. Il faut commencer la prise des dragées de la plaquette suivante immédiatement après la fin de cette plaquette, sans respecter l'intervalle sans dragée. Il est improbable qu'une hémorragie de privation apparaisse avant la fin de la 2e plaquette, mais la survenue de petites pertes sanglantes ou de saignements intermenstruels peut être plus fréquente.
b.La patiente interrompt la prise des dragées de la plaquette actuelle. La plaquette suivante doit être commencée après une pause de 7 jours au maximum (le jour de l'oubli de la dragée compris).
Si l'hémorragie de privation ne se produit pas pendant le prochain intervalle sans dragée, il faut envisager l'éventualité d'une grossesse.
Conduite à tenir en cas de troubles gastro-intestinaux
En cas de troubles gastro-intestinaux sévères, – quelle que soit leur cause (c.-à-d. aussi en cas de diarrhée d'origine médicamenteuse, etc.) – l'absorption peut être incomplète et des méthodes de contraception supplémentaires doivent être utilisées.
En cas de vomissements dans les 3 à 4 heures suivant la prise d'une dragée il faut observer les règles de base de la rubrique «Conduite à tenir en cas d'oubli de dragée(s)». Afin que le schéma habituel de prise puisse être conservé, la patiente devra prendre la dragée supplémentaire d'une plaquette de réserve.
Décalage de la menstruation
Report de la menstruation (allongement du cycle)
La prise doit être poursuivie par la plaquette suivante sans respecter l'intervalle entre les 2 plaquettes. La patiente peut ainsi retarder la menstruation aussi longtemps qu'elle le désire (au maximum jusqu'à la fin de la deuxième plaquette). Pendant cette période, de petites pertes sanglantes ou des saignements intermenstruels peuvent se produire. La prise régulière de Femadiol-Mepha 20 sera alors poursuivie après la pause habituelle de 7 jours.
Avance de la menstruation
Le début de la menstruation peut être avancé à un autre jour de la semaine, en raccourcissant à volonté l'intervalle sans dragée. Plus l'intervalle est court, plus la survenue d'une hémorragie de privation est improbable et plus de petites pertes sanglantes ou des saignements intermenstruels sont fréquents pendant la prise de la plaquette suivante (comme lors du report de la menstruation).
Conduite à tenir en cas d'irrégularités menstruelles
Des saignements irréguliers (petites pertes sanglantes ou saignements intermenstruels) peuvent se produire avec tous les CHC, en particulier pendant les premiers mois de la prise. En cas de saignements irréguliers, un bilan diagnostique n'est judicieux qu'après une phase d'adaptation d'environ 3 cycles.
Si les irrégularités menstruelles persistent ou si elles surviennent pour la première fois après des cycles auparavant réguliers, il faut aussi envisager des causes d'origine non hormonale. Des mesures diagnostiques adéquates permettant d'exclure une grossesse ou une affection maligne sont par conséquent indiquées. Ces mesures peuvent inclure un curetage.
L'hémorragie de privation peut faire défaut pendant l'intervalle sans dragée. Une grossesse est improbable si le CHC a été pris conformément aux instructions posologiques. Toutefois avant de poursuivre la prise, il faudra exclure une grossesse si le CHC n'a pas été pris selon les instructions avant la première hémorragie de privation manquante ou en cas d'absence de deux hémorragies de privation.
Instructions posologiques particulières
Enfants et adolescents
Femadiol-Mepha 20 n'est indiqué qu'après la ménarche. L'efficacité et la sécurité de Femadiol-Mepha 20 ont été examinées chez des femmes âgées de 18 ans et plus. Chez les adolescentes, si indiqué, la posologie recommandée est la même que chez les adultes.
Patientes âgées
Femadiol-Mepha 20 n'est pas indiqué après la ménopause.
Patients présentant des troubles de la fonction rénale
Femadiol-Mepha 20 n'a pas été étudié chez les femmes atteintes d'insuffisance rénale.
Patients présentant des troubles de la fonction hépatique
Femadiol-Mepha 20 ne doit pas être utilisé chez les femmes avec une insuffisance hépatique.
Contre-indications·Présence ou risque de thromboembolie veineuse (TEV)
·Thromboembolie veineuse (patiente traitée par des anticoagulants) ou antécédents de TEV (p.ex. thrombose veineuse profonde ou embolie pulmonaire);
·Facteurs de risque majeurs de thromboembolie veineuse tels que prédisposition connue, héréditaire ou acquise, telle qu'une résistance à la protéine C activée (PCa) (y compris une mutation du facteur V de Leiden), un déficit en antithrombine III, un déficit en protéine C, un déficit en protéine S;
·Présence simultanée de multiples facteurs de risque de thromboembolie veineuse, selon la rubrique «Mises en garde et précautions».
·Présence ou risque de thromboembolie artérielle (TEA)
·Thromboembolie artérielle, antécédents de TEA ou prodromes de TEA (p.ex. angine de poitrine, infarctus du myocarde, accident ischémique transitoire, accident vasculaire cérébral);
·Facteurs de risque majeurs de TEA comme
·diabète avec complications vasculaires
·hypertension artérielle sévère
·dyslipoprotéinémie sévère
·antécédents de migraine avec signes neurologiques focaux
·prédisposition héréditaire ou acquise à la TEA, telle qu'une hyperhomocystéinémie ou la présence d'anticorps anti-phospholipides (anticorps anti-cardiolipine, anticoagulant lupique);
·Présence simultanée de multiples facteurs de risque de TEA, selon la rubrique «Mises en garde et précautions».
·Affection hépatique sévère ou antécédent d'affection hépatique sévère, en l'absence de normalisation des tests fonctionnels hépatiques;
·Utilisation concomitante avec l'association des principes actifs ombitasvir/paritaprévir/ritonavir avec ou sans dasabuvir, glécaprévir/pibrentasvir et sofosbuvir/velpatasvir/voxilaprévir (médicament pour le traitement de l'hépatite C) (voir «Mises en garde et précautions» et «Interactions»);
·Tumeur hépatique (bénigne ou maligne) ou antécédent de tumeur hépatique;
·Existence ou suspicion d'une pathologie maligne dépendante des hormones sexuelles au niveau de l'appareil génital et du sein;
·Saignements vaginaux d'origine inconnue;
·Grossesse confirmée ou suspicion de grossesse;
·Hypersensibilité aux principes actifs ou à l'un des excipients de Femadiol-Mepha 20.
Mises en garde et précautionsLe risque de thromboembolie veineuse (TEV) et de thromboembolie artérielle (TEA) est augmenté chez les femmes utilisant un CHC par rapport à celles qui n'en utilisent pas. Les mises en garde et précautions décrites ci-après doivent être prises en considération avant toute prescription (cf. «Risque de thromboembolie veineuse [TEV]» et «Risque de thromboembolie artérielle [TEA]»). Il est en outre important d'informer la patiente des risques d'accidents thromboemboliques veineux et artériels, des facteurs connus de risques vasculaires et en particulier des symptômes de TEV et de TEA ainsi que des mesures à prendre en présence de ces symptômes et de suspicion de thrombose (cf. «Les symptômes d'une TEV [thrombose veineuse profonde et embolie pulmonaire]» et «Les symptômes d'une TEA»).
Avant de prescrire un CHC tel que Femadiol-Mepha 20, les bénéfices associés à son utilisation doivent être évalués par rapport aux maladies/risques détaillés ci-dessous. Le degré de gravité de chaque facteur individuel ainsi que la présence concomitante de plusieurs facteurs de risque doivent être pris en compte et discutés avec la patiente (cf. également «Contre-indications»). La patiente doit en outre être invitée à lire attentivement la notice d'emballage et à suivre les conseils qui y figurent.
Examen médical
Avant le début ou le renouvellement de la prise d'un CHC tel que Femadiol-Mepha 20, il est nécessaire de procéder à une anamnèse personnelle et familiale minutieuse ainsi qu'à un examen général et gynécologique approfondi en prenant en compte les «Contre-indications» et les «Mises en garde et précautions» afin de dépister les affections nécessitant un traitement ainsi que les états à risque, et de pouvoir exclure l'éventualité d'une grossesse. Ces examens comprennent généralement une mesure de la tension artérielle, un examen des seins, de l'abdomen, des organes pelviens (avec frottis cytologique du col) et les examens de laboratoire appropriés.
Les examens doivent être répétés à intervalle régulier pendant la durée d'utilisation des CHC. Le type et la fréquence d'examen doivent toutefois être déterminés individuellement et se référer aux directives de la Société suisse de gynécologie et d'obstétrique (SSGO). Les contre-indications (p.ex. accident ischémique transitoire) et les facteurs de risque (p.ex. anamnèse familiale de thrombose veineuse ou artérielle; voir «Facteurs de risque de TEV» et «Facteurs de risque de TEA») peuvent apparaître pour la première fois en cours d'utilisation d'un CHC et doivent dès lors être recherchés lors de chaque contrôle.
Motifs imposant l'arrêt immédiat de la prise du médicament
La patiente doit être informée qu'en cas d'apparition de l'une des contre-indications précitées ou de l'une des situations suivantes, il lui faut consulter au plus vite un médecin, qui décidera de la poursuite ou de l'arrêt de la prise du CHC:
·céphalées apparaissant pour la première fois en présentant un caractère de migraine ou se manifestant de façon répétée avec une intensité inhabituelle;
·troubles soudains de la vision, de l'audition, du langage ou autres troubles sensoriels;
·dès les premiers signes d'événements thromboemboliques (voir «Symptômes de TEV [thrombose veineuse profonde et embolie pulmonaire]» et «Symptômes de TEA»);
·4 semaines au moins avant une intervention chirurgicale programmée et pendant une immobilisation (p.ex. à la suite d'un accident ou d'une opération);
·augmentation cliniquement pertinente de la tension artérielle (lors de mesures répétées);
·apparition d'un ictère, d'une hépatite, d'un prurit généralisé;
·fortes douleurs épigastriques ou hépatomégalie;
·états dépressifs sévères;
·grossesse ou suspicion de grossesse.
Risque de thromboembolie veineuse (TEV)
Le risque de TEV est augmenté chez les femmes utilisant un CHC par rapport à celles qui n'en utilisent pas. Les CHC contenant du lévonorgestrel, du norgestimate ou de la noréthistérone sont associés au risque de TEV le plus faible. Le risque de TEV associé aux autres CHC, tels que Femadiol-Mepha 20, peut être jusqu'à deux fois plus élevé.
La décision de prendre le médicament doit être prise uniquement après un entretien approfondi avec la patiente, afin de s'assurer qu'elle comprend:
·Le risque de TEV associé à la prise de Femadiol-Mepha 20.
·Comment ses facteurs de risque personnels préexistants influent sur ce risque?
·Le risque plus élevé de développer une TEV pendant la première année d'utilisation (et en particulier pendant les 3 premiers mois).
·Les données disponibles indiquent que le risque de TEV est accru aussi bien lors de la première utilisation d'un CHC que lors de la réutilisation du même ou d'un autre CHC après une interruption d'au moins 4 semaines ou plus.
·Femadiol-Mepha 20 est un médicament. En cas d'accident ou d'intervention chirurgicale, la patiente doit informer les médecins traitants qu'elle prend Femadiol-Mepha 20.
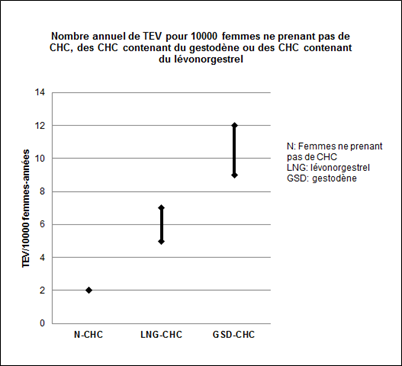
Environ 2 femmes sur 10'000 n'utilisant pas de CHC et qui ne sont pas enceintes développeront une TEV au cours d'une année. Le risque peut toutefois être considérablement plus élevé, selon les facteurs de risque individuels (voir ci-dessous).
À partir des données épidémiologiques, il est possible d'estimer que 9 à 12 femmes sur 10'000 utilisant un CHC contenant du gestodène développeront une TEV au cours d'une année. En comparaison, ce nombre est estimé à 5 à 7 par année pour 10'000 femmes utilisant un CHC contenant du lévonorgestrel.
Dans les deux cas, le nombre de TEV par année est inférieur à celui attendu pendant la grossesse ou en période post-partum.
La TEV peut être fatale dans 1 à 2% des cas.
Très rarement, chez des utilisatrices de CHC, des cas de thrombose veineuse ont été signalés en dehors des membres, p.ex. thromboses des veines sinusales ou thromboses des veines hépatiques, mésentériques, rénales ou rétiniennes.
Facteurs de risque de TEV
Le risque de complications thromboemboliques veineuses chez les utilisatrices de CHC peut être considérablement accru si d'autres facteurs de risque sont présents, surtout s'ils sont multiples (voir le tableau ci-dessous). Lors de l'évaluation du rapport bénéfices/risques, il est important de prendre en considération l'augmentation particulière du risque d'accident thromboembolique veineux en présence de plusieurs facteurs de risques concomitants, augmentation qui peut être supérieure à la seule somme des risques pris individuellement. Dans ce cas, le risque global de TEV doit être pris en compte. Femadiol-Mepha 20 est contre-indiqué chez les femmes présentant simultanément de multiples facteurs de risque qui les exposent globalement à un risque élevé de thrombose veineuse.
Tableau: Facteurs de risque de TEV
|
Facteur de risque
|
Commentaire
| |
Obésité (indice de masse corporelle supérieur à 30 kg/m²)
|
L'augmentation de l'IMC accroît considérablement le risque.
Il est particulièrement important d'en prendre compte si d'autres facteurs de risque sont présents.
| |
Immobilisation prolongée, intervention chirurgicale majeure, toute intervention chirurgicale sur les jambes ou la hanche, neurochirurgie ou traumatisme majeur
|
Dans ces situations, il est conseillé de suspendre la prise des dragées (au moins quatre semaines à l'avance en cas de chirurgie programmée) et de ne reprendre le CHC que deux semaines au moins après la complète remobilisation. Une autre méthode de contraception doit être utilisée afin d'éviter une grossesse non désirée.
Un traitement anti-thrombotique devra être envisagé si Femadiol-Mepha 20 n'a pas été interrompu à l'avance.
| |
Antécédents familiaux (chaque thromboembolie veineuse survenue dans la fratrie ou chez un parent, en particulier à un âge relativement jeune, c.-à-d. avant 50 ans)
|
En cas de prédisposition héréditaire suspectée, la femme devra être adressée à un spécialiste pour avis avant toute décision concernant la prise de Femadiol-Mepha 20.
Si une thrombophilie est détectée, la prise de CHC comme Femadiol-Mepha 20 est contre-indiquée.
| |
Autres affections médicales associées à un risque accru de TEV
|
Lupus érythémateux disséminé, syndrome hémolytique et urémique, maladies inflammatoires chroniques intestinales (maladie de Crohn ou rectocolite hémorragique), drépanocytose, affections malignes.
| |
Âge
|
En particulier au-delà de 35 ans
|
Remarque: l'immobilisation temporaire, y compris les trajets aériens >4 heures, peut également constituer un facteur de risque de TEV, en particulier chez les femmes présentant d'autres facteurs de risque.
Il n'existe aucun consensus quant au rôle éventuel joué par les varices et les thrombophlébites superficielles dans l'apparition ou la progression d'une thrombose veineuse.
Le risque accru de thromboembolie pendant la période puerpérale doit être pris en compte. Certaines données indiquent en effet que le risque peut être encore augmenté jusqu'à 12 semaines après l'accouchement.
Symptômes de TEV (thrombose veineuse profonde et embolie pulmonaire)
La patiente doit être informée qu'en cas d'apparition d'un ou de plusieurs de ces symptômes, elle doit consulter un médecin en urgence et indiquer au personnel médical qu'elle prend Femadiol-Mepha 20.
·Les symptômes de thrombose veineuse profonde des membres inférieurs peuvent inclure:
·gonflement unilatéral d'une jambe ou le long d'une veine de la jambe;
·sensation de tension ou douleur à une jambe, même si elle n'est ressentie qu'en position debout ou en marchant;
·sensation de chaleur, rougeur ou changement de la coloration cutanée de la jambe affectée.
·Les symptômes de l'embolie pulmonaire peuvent inclure:
·difficulté respiratoire subite et inexpliquée, respiration rapide ou détresse respiratoire, intolérance à l'effort;
·toux d'apparition soudaine, éventuellement accompagnée d'expectorations sanglantes;
·douleur aiguë et soudaine dans la poitrine pouvant s'amplifier à la respiration profonde;
·obnubilation sévère, vertiges ou sensation d'angoisse;
·tachycardie ou arythmie.
Certains de ces symptômes (p.ex. «essoufflement» ou «toux») ne sont pas spécifiques et peuvent être interprétés à tort comme des signes d'événements fréquents ou moins sévères (infections respiratoires, p. ex.).
Risque de thromboembolie artérielle (TEA)
Des études épidémiologiques ont montré une association entre l'utilisation de contraceptifs hormonaux et l'augmentation du risque de thromboembolie artérielle (infarctus du myocarde, accident cérébrovasculaire ou accident ischémique transitoire). Avant de décider de prescrire Femadiol-Mepha 20, la patiente doit être informée de ce risque et, surtout, du fait que des facteurs de risque individuels préexistants sont susceptibles d'aggraver ce risque.
De très rares cas de thromboses dans d'autres vaisseaux sanguins (tels que les artères hépatiques, mésentériques, rénales ou rétiniennes) ont été observés chez les utilisatrices de CHC.
Facteurs de risque de TEA
Le risque de complications thromboemboliques artérielles ou d'accident cérébrovasculaire chez les utilisatrices de CHC augmente avec la présence de facteurs de risque (voir tableau). Lors de l'évaluation du rapport bénéfices/risques, il est important de prendre en considération l'augmentation particulière du risque d'accident thromboembolique artériel en présence de plusieurs facteurs de risques concomitants, augmentation qui peut être supérieure à la seule somme des risques pris individuellement. Dans ce cas, le risque global de TEA doit être pris en compte. Femadiol-Mepha 20 est contre-indiqué chez les femmes présentant un facteur de risque sévère ou de multiples facteurs de risque de TEA qui les exposent à un risque élevé de thrombose artérielle.
Tableau: Facteurs de risque de TEA
|
Facteur de risque
|
Commentaire
| |
Âge
|
En particulier au-delà de 35 ans
| |
Tabagisme
|
Il doit être conseillé aux femmes de ne pas fumer si elles souhaitent utiliser un CHC comme Femadiol-Mepha 20. Une méthode de contraception différente doit être fortement conseillée aux femmes de plus de 35 ans qui continuent de fumer.
| |
Hypertension artérielle
|
| |
Diabète
|
L'utilisation de CHC est contre-indiquée chez les femmes diabétiques qui présentent déjà des complications vasculaires.
| |
Dyslipoprotéinémie
|
| |
Valvulopathie cardiaque
|
| |
Fibrillation auriculaire
|
| |
Obésité (indice de masse corporelle supérieur à 30 kg/m2)
|
L'augmentation de l'IMC accroît considérablement le risque.
Il est particulièrement important d'en tenir compte si d'autres facteurs de risque sont présents.
| |
Antécédents familiaux (thromboembolie artérielle survenue dans la fratrie ou chez un parent, en particulier à un âge relativement jeune, c.-à-d. avant 50 ans).
|
En cas de prédisposition héréditaire suspectée, la femme devra être adressée à un spécialiste pour avis avant toute décision concernant la prise de Femadiol-Mepha 20.
Si l'examen révèle une thrombophilie, la prise de CHC comme Femadiol-Mepha 20 est contre-indiquée.
| |
Migraine
|
L'accroissement de la fréquence ou de la sévérité des migraines lors de la prise de Femadiol-Mepha 20 peut être le prodrome d'un événement cérébrovasculaire et constituer un motif d'arrêt immédiat de Femadiol-Mepha 20.
| |
Autres affections médicales associées à un risque accru de TEA.
|
Hyperhomocystéinémie, lupus érythémateux disséminé, drépanocytose, affections malignes.
|
Symptômes de TEA
Les femmes doivent être informées qu'en cas d'apparition d'un ou de plusieurs de ces symptômes, elles doivent consulter un médecin en urgence et indiquer au personnel médical qu'elles prennent Femadiol-Mepha 20.
·Les symptômes d'un accident cérébrovasculaire peuvent inclure:
·perte soudaine de sensibilité ou de force au niveau du visage, d'un bras ou d'une jambe, touchant notamment une moitié du corps;
·confusion soudaine;
·élocution incompréhensible ou difficulté de compréhension;
·troubles subits de la vision d'un ou des deux yeux;
·troubles subits de la marche;
·vertiges;
·troubles de l'équilibre ou de la coordination;
·céphalées soudaines et sévères, ou de durée inhabituelle, de cause inconnue;
·perte de connaissance ou évanouissement avec ou sans épisode convulsif.
·Les symptômes de l'infarctus du myocarde peuvent inclure:
·douleurs, malaise, sensation de pression, sensation de pesanteur, sensation de serrement ou de tension dans la poitrine, le bras ou derrière le sternum;
·douleurs irradiant dans le dos, la mâchoire, le cou, le bras ou l'estomac;
·sensation de réplétion, troubles gastriques ou effort de vomissement;
·sueurs, nausées, vomissements ou vertiges;
·sensation de grande faiblesse, d'angoisse ou essoufflement;
·tachycardie ou arythmies.
·L'occlusion d'un vaisseau peut engendrer d'autres symptômes:
·douleur soudaine, tuméfaction ou cyanose discrète d'une extrémité;
·abdomen aigu.
Suspicion de prédisposition héréditaire ou acquise aux complications thromboemboliques
En cas de suspicion de prédisposition héréditaire ou acquise aux complications thromboemboliques, un examen de la coagulation sanguine doit être effectué par un spécialiste, qui peut le cas échéant demander une analyse de certains paramètres hémostatiques.
Maladies tumorales
Un risque augmenté de cancer du col de l'utérus a été rapporté lors d'une utilisation au long cours des CHC (>5 ans) dans quelques études épidémiologiques. Néanmoins, ceci est toujours en discussion de façon controversée dans la mesure où ce résultat est influencé par d'autres facteurs, comme une infection par des papillomavirus humains (HPV) (facteur de risque le plus puissant), par la fréquence de la participation au screening du col de l'utérus ou par le comportement sexuel.
Une métaanalyse de 54 études épidémiologiques a montré que le risque relatif (RR) qu'un cancer du sein soit diagnostiqué, est légèrement augmenté chez les femmes utilisant un CHC (RR = 1.24). Cette augmentation du risque diminue d'une manière continue après l'arrêt des CHC et n'est plus détectable au bout de 10 ans. Les cancers du sein étant rares avant l'âge de 40 ans, le nombre supplémentaire de cancers du sein diagnostiqués chez les femmes qui utilisent, ou ont utilisé jusqu'à récemment, un CHC est faible par rapport au risque total de cancer du sein. Ces études ne donnent pas d'indications sur un lien de causalité. L'augmentation du risque observée peut être due aussi bien à un dépistage plus précoce chez les utilisatrices de CHC qu'aux effets biologiques des CHC ou aux deux facteurs. Les cancers du sein ont été, au moment où le diagnostic a été posé, tendanciellement moins évolués chez les femmes ayant utilisé un CHC que chez celles qui n'avaient jamais utilisé de CHC.
Dans de rares cas, on a observé à la suite de l'utilisation de principes actifs hormonaux tels que ceux contenus dans Femadiol-Mepha 20, des altérations hépatiques bénignes, plus rarement malignes, dont les complications possibles peuvent être à l'origine d'hémorragies intra-abdominales mettant en jeu le pronostic vital. Si des douleurs épigastriques intenses, une hépatomégalie ou des signes en faveur d'une hémorragie intra-abdominale apparaissent, il faut inclure l'éventualité d'une tumeur hépatique dans le diagnostic différentiel.
Troubles dépressifs
Les dépressions ou humeurs dépressives sont des effets indésirables potentiels connus survenant lors de l'utilisation d'hormones sexuelles, y compris les contraceptifs hormonaux (voir également rubrique «Effets indésirables»). Ces troubles peuvent apparaître peu de temps après le début du traitement. Une dépression peut avoir une évolution grave et représente un facteur de risque de suicide ou de comportement suicidaire. Les utilisatrices de contraceptifs hormonaux doivent donc être informées des symptômes possibles des troubles dépressifs. Il est vivement conseillé d'aviser les utilisatrices de s'adresser immédiatement à un médecin si elles remarquent des variations d'humeur ou autres symptômes de dépression lors de l'utilisation du contraceptif. Les patientes présentant des antécédents de dépression sévère doivent être attentivement surveillées. Si des états dépressifs sévères réapparaissent lors de l'utilisation de Femadiol-Mepha 20, la prise du médicament doit être arrêtée.
Autres précautions
Les femmes prenant un contraceptif hormonal ne doivent pas être traitées simultanément par des préparations à base de millepertuis (Hypericum), car celui-ci peut diminuer l'action contraceptive. Des saignements intermenstruels et des cas isolés de grossesses non désirées ont été rapportés (voir aussi «Interactions»).
Chez les femmes atteintes d'hypertriglycéridémie ou ayant des antécédents familiaux d'hypertriglycéridémie, l'utilisation de CHC peut augmenter le risque de pancréatite.
Bien qu'une légère augmentation de la tension artérielle pendant la prise de CHC ait été assez fréquemment rapportée, des valeurs élevées cliniquement significatives sont rares. Si la prise du CHC conduit à une augmentation cliniquement significative de la tension artérielle (confirmée par des mesures répétées), la prise du CHC devra être arrêtée. Dans les cas où l'indication semble justifiée, on pourra envisager la reprise d'un CHC, pour autant que la tension artérielle se soit normalisée (sous traitement).
La prise de CHC peut entraîner une diminution de la tolérance au glucose. Les femmes diabétiques et celles ayant une tolérance au glucose réduite doivent donc toutes être attentivement surveillées, particulièrement au cours des premiers mois, lors de la prise d'un CHC. Sauf exception, il n'existe toutefois aucune raison de modifier le traitement antidiabétique.
Des troubles aigus ou chroniques de la fonction hépatique peuvent imposer un arrêt du CHC, jusqu'à ce que les valeurs hépatiques se soient normalisées. La récidive d'un ictère cholestatique apparu pour la première fois pendant une grossesse ou lors d'une prise antérieure d'hormones stéroïdiennes sexuelles, doit faire arrêter la prise du CHC.
Chez les patientes atteintes d'hépatite C et utilisant un CHC à base d'éthinylestradiol, une augmentation significativement plus fréquente de l'ALT (y compris les cas d'une augmentation de plus du quintuple, dans des cas isolés de plus de 20 fois la limite supérieure de la normale), que chez les patientes uniquement traitées par des principes antiviraux a été observée sous l'utilisation de l'association des principes actifs ombitasvir/paritaprévir/ritonavir avec ou sans dasabuvir (voir «Interactions»). Des augmentations de l'ALT similaires ont également été observées sous les médicaments anti-VHC qui contenaient du glécaprévir/pibrentasvir ou du sofosbuvir/velpatasvir/voxilaprévir. Par conséquent, Femadiol-Mepha 20 doit être arrêté avant l'instauration d'un traitement par ces associations de principes actifs. À condition que les paramètres hépatiques soient normaux, la prise de Femadiol-Mepha 20 peut être reprise au plus tôt 2 semaines, mieux encore 4 semaines, après l'arrêt des associations de principes actifs ombitasvir/paritaprévir/ritonavir avec ou sans dasabuvir, glécaprévir/pibrentasvir ou sofosbuvir/velpatasvir/voxilaprévir. Ce faisant, il faut tenir compte du fait que l'efficacité du CHC peut encore être entravée en cas d'intervalle de moins de 4 semaines en raison des propriétés inductrices des enzymes du ritonavir et, par conséquent, une méthode barrière supplémentaire doit être utilisée (voir rubrique «Interactions/Inducteurs enzymatiques»).
Les estrogènes peuvent augmenter la lithogénicité de la vésicule biliaire. Des cas de cholélithiase et d'autres affections de la vésicule biliaire (p.ex. cholécystite) ont été rapportés chez des femmes sous contraceptifs hormonaux.
Chez les femmes atteintes d'un angioœdème héréditaire et/ou acquis, des estrogènes exogènes peuvent induire ou aggraver les symptômes.
Les affections suivantes peuvent survenir ou être aggravées pendant la grossesse ou l'utilisation d'un CHC, même si les données actuellement disponibles ne permettent pas d'imputer une relation de causalité claire avec l'utilisation d'un CHC: ictère et/ou prurit cholestatique; cholélithiase; porphyrie; lupus érythémateux disséminé; syndrome hémolytique et urémique; chorée mineure; herpes gestationis; surdité due à une otosclérose. La prise de CHC a en outre été associée à des cas de maladie de Crohn et de colite ulcéreuse.
Chez les femmes prédisposées, l'utilisation de CHC peut occasionnellement provoquer un chloasma, qui est encore renforcé par une exposition intense aux rayons solaires. Les femmes présentant une tendance au chloasma ne devraient donc pas s'exposer à des rayonnements UV importants.
Il faut informer les patientes que le CHC n'offre aucune protection contre les infections à VIH (SIDA) et autres maladies sexuellement transmissibles.
La prise régulière d'acide folique avant et pendant une grossesse contribue à prévenir les défauts de fermeture du tube neural (Spina bifida, anencéphalie). Hormis une alimentation riche en acide folique, une supplémentation continue de 0.4 mg par jour (p.ex. par une préparation polyvitaminée) est dès lors recommandée pour toutes les femmes à l'arrêt de la contraception hormonale s'il y a souhait ou possibilité de grossesse.
Femadiol-Mepha 20 contient du lactose et du saccharose. Les patients présentant une intolérance au fructose et au galactose, un déficit total en lactase, un syndrome de malabsorption du glucose et du galactose ou une insuffisance en sucrase et isomaltase (maladies héréditaires rares) ne doivent pas prendre ce médicament.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dragée, c.-à-d. qu'il est essentiellement «sans sodium».
InteractionsAfin de connaître les éventuelles interactions, il est recommandé de consulter également l'information professionnelle des médicaments co-administrés.
Influence d'autres substances sur la pharmacocinétique des contraceptifs hormonaux
Inducteurs enzymatiques
Des interactions peuvent survenir entre contraceptifs hormonaux et médicaments induisant les enzymes microsomales, ce qui peut conduire à une augmentation de la clairance des hormones sexuelles, à une diminution de l'effet contraceptif et à des saignements intermenstruels. Ceci vaut par exemple pour les barbituriques, le bosentan, la carbamazépine, le felbamate, le modafinil, l'oxcarbazépine, la phénytoïne, la primidone, la rifabutine, la rifampicine et le topiramate ainsi que pour les médicaments contenant du millepertuis (Hypericum perforatum).
Une induction enzymatique peut déjà être observée après quelques jours seulement. L'induction enzymatique maximale est généralement atteinte au bout de 2 à 3 semaines et peut persister pendant 4 semaines ou plus après l'arrêt de ces médicaments. Les femmes traitées sur une courte période par un de ces médicaments doivent provisoirement utiliser une méthode de contraception non hormonale en complément au CHC ou choisir une autre méthode contraceptive. Une méthode de contraception mécanique doit être poursuivie pendant toute la prise concomitante des médicaments et encore pendant 28 jours après l'arrêt du traitement. Lorsque la prise concomitante d'un inducteur enzymatique dure au-delà de la fin de l'emballage du CHC, il faut passer immédiatement à l'emballage suivant, donc sauter l'intervalle habituel sans prise de comprimés. Dans ce cas, il ne faut pas s'attendre à l'hémorragie de privation avant la fin du deuxième emballage. En l'absence d'hémorragie de privation pendant l'intervalle sans prise de comprimés à la fin du deuxième emballage, il est impératif d'exclure toute grossesse avant de poursuivre avec un nouvel emballage.
En cas de traitement de longue durée avec des médicaments qui entraînent une induction enzymatique hépatique, il convient d'utiliser des méthodes contraceptives non hormonales fiables.
On sait en outre que différents inhibiteurs de la protéase du VIH/VHC et inhibiteurs non nucléosidiques de la transcriptase inverse peuvent entraîner une baisse ou une augmentation des concentrations plasmatiques en estrogènes et progestatifs. Ces modifications peuvent être cliniquement significatives dans certains cas.
Les inhibiteurs des protéases en particulier, tels que le ritonavir ou le nelfinavir (y compris leurs associations) sont connus comme étant des inhibiteurs puissants du CYP3A4, mais en cas de co-administration avec des hormones stéroïdiennes, ils peuvent entraîner une induction enzymatique et provoquer une baisse des concentrations plasmatiques en estrogènes et progestatifs.
Inhibiteurs enzymatiques
Les inhibiteurs forts et modérés du CYP3A comme les antifongiques azolés (p.ex. itraconazole, voriconazole, fluconazole), les macrolides (clarithromycine, érythromycine), diltiazem, vérapamil et le jus de pamplemousse peuvent augmenter les taux plasmatiques des estrogènes et/ou des progestatifs et entraîner des effets indésirables plus nombreux.
Lorsqu'elles étaient administrées en même temps qu'un contraceptif hormonal combiné contenant 0.035 mg d'éthinylestradiol, des doses d'étoricoxib comprises entre 60 et 120 mg/jour ont entraîné une multiplication des concentrations plasmatiques d'éthinylestradiol par un facteur situé entre 1.4 et 1.6. La pertinence clinique de ces modifications n'est pas connue.
Les inhibiteurs de l'HMG-CoA-réductase atorvastatine et rosuvastatine sont eux aussi susceptibles d'augmenter les concentrations plasmatiques des hormones sexuelles (augmentation d'environ 20 à 30% de l'AUC des composantes œstrogénique et progestative) et, dans certaines circonstances, d'accroître ainsi la survenue des effets indésirables.
Interférence avec le métabolisme entéro-hépatique
En cas de prise simultanée et sur une courte durée (jusqu'à 10 jours) d'antibiotiques qui n'interagissent pas avec le système enzymatique du CYP3A4, aucune interaction pharmacocinétique n'est à prévoir. Il est cependant nécessaire d'avertir la patiente que dans certains cas, la maladie (p.ex. maladie vénérienne) contre laquelle l'antibiotique est utilisé peut nécessiter en complément l'utilisation d'une méthode contraceptive mécanique.
En cas de co-médication de longue durée avec des antibiotiques (p.ex. en cas d'ostéomyélite ou de borréliose), les données d'interaction actuellement disponibles sont insuffisantes. Pour exclure avec certitude toute grossesse, il est dans de tels cas recommandé d'utiliser en complément une méthode contraceptive mécanique pendant la durée de l'antibiothérapie et pendant les 7 jours qui suivent la fin de ce traitement.
En cas d'apparition de diarrhées et/ou de vomissements sous traitement antibiotique, se référer aux indications dans le paragraphe «Conduite à tenir lors de troubles gastro-intestinaux» dans la rubrique «Posologie/Mode d'emploi».
Influence des contraceptifs hormonaux sur la pharmacocinétique d'autres médicaments
Les contraceptifs hormonaux peuvent, par différents mécanismes d'interaction, influer également sur la pharmacocinétique de certains autres médicaments: ils peuvent inhiber les enzymes hépatiques microsomaux ou induire la conjugaison hépatique, en particulier la glucuroconjugaison. Les concentrations plasmatiques ou tissulaires d'autres médicaments peuvent par conséquent être augmentées (p.ex. la cyclosporine) ou diminuées (p.ex. la lamotrigine, voir ci-dessous). Par ailleurs, l'effet pharmacologique des groupes médicamenteux suivants peut également être influencé: Analgésiques, antidépresseurs, antidiabétiques, antimalariques, certaines benzodiazépines, certains bêta-bloquants, corticostéroïdes et anticoagulants oraux. Les modifications des taux plasmatiques résultant de ces interactions ne sont pas toujours cliniquement pertinentes.
In vitro, l'éthinylestradiol a révélé une inhibition des CYP1A1, CYP1A2, CYP2C19, CYP3A4/5 et CYP2C8. Dans des études cliniques, l'utilisation d'un contraceptif contenant de l'éthinylestradiol a entraîné une augmentation modérée (p.ex. mélatonine et tizanidine) ou légère (p.ex. théophylline) des concentrations plasmatiques de substrats du CYP1A2, ainsi qu'une augmentation uniquement minime ou absente des concentrations plasmatiques de substrats du CYP3A4 (p.ex. midazolam).
Lamotrigine
Une étude sur l'interaction avec la lamotrigine, un antiépileptique, et un contraceptif oral combiné (0.03 mg d'éthinylestradiol/0.15 mg de lévonorgestrel) a montré une hausse significative de la clairance de la lamotrigine et une diminution significative des taux plasmatiques de lamotrigine lorsque ces médicaments sont administrés en même temps. Une telle diminution des concentrations plasmatiques peut s'accompagner d'une réduction du contrôle des crises. On ignore cependant dans quelle mesure ces résultats sont transposables à d'autres contraceptifs combinés contenant un autre composant progestatif et/ou une autre dose d'estrogène. Mais on peut partir du principe que ces préparations présentent un profil d'interactions comparable.
Lors du commencement de la prise de Femadiol-Mepha 20, chez une patiente prenant de la lamotrigine, une adaptation de la dose de lamotrigine peut donc être nécessaire, et les concentrations de lamotrigine devraient être surveillées étroitement au début du traitement. En l'occurrence, il peut y avoir une hausse significative du taux de lamotrigine (selon les cas jusqu'à un niveau toxique) lors de l'arrêt de la prise du contraceptif hormonal (ainsi dans certains cas pendant la période de 7 jours sans prise).
Interactions au mécanisme inconnu
Dans des études cliniques, une augmentation de l'ALT significativement plus fréquente (y compris les cas d'une augmentation de plus du quintuple, dans des cas isolés de plus de 20 fois la limite supérieure de la normale [LSN]), que chez les patientes uniquement traitées par des principes antiviraux a été observée sous l'utilisation concomitante d'un CHC contenant de l'éthinylestradiol et de l'association des principes actifs ombitasvir/paritaprévir/ritonavir avec ou sans dasabuvir utilisée dans le traitement des infections à VIH. Des augmentations de l'ALT similaires ont également été observées sous les médicaments anti-VHC qui contenaient du glécaprévir/pibrentasvir ou du sofosbuvir/velpatasvir/voxilaprévir. Par conséquent, Femadiol-Mepha 20 doit être arrêté avant l'instauration d'un traitement par une telle association antivirale (voir également «Contre-indications» et «Mises en garde et précautions»).
Grossesse, allaitementGrossesse
La prise de Femadiol-Mepha 20 est contre-indiquée pendant la grossesse. Il faut donc exclure toute grossesse avant le début de la prise. Si une grossesse survient ou est suspectée lors de la prise de Femadiol-Mepha 20, la prise du médicament doit être arrêtée immédiatement et le médecin consulté.
Des études expérimentales animales suggèrent des risques pour le fœtus (voir aussi «Données précliniques»). La plupart des études épidémiologiques réalisées jusqu'ici n'ont toutefois montré aucun indice en faveur d'un effet embryotoxique ou tératogène lors de la prise accidentelle de CHC pendant la grossesse.
Allaitement
Le médicament ne doit pas être pris pendant l'allaitement, car il peut réduire la production de lait et modifier sa qualité; d'autre part, de faibles concentrations du principe actif peuvent être mesurées dans le lait. Des méthodes de contraception non hormonales devront si possible être utilisées jusqu'à ce que la mère ait complètement cessé d'allaiter.
Concernant le risque d'événements thromboemboliques chez la mère pendant la période puerpérale, voir la rubrique «Mises en garde et précautions».
Effet sur l’aptitude à la conduite et l’utilisation de machinesAucune étude n'a été menée en lien avec une influence possible sur l'aptitude à la conduite et l'utilisation de machines.
Effets indésirablesLes effets indésirables les plus graves en rapport avec la prise de CHC sont décrits dans la rubrique «Mises en garde et précautions» (voir la rubrique). Les effets indésirables sérieux incluent en particulier des thromboembolies artérielles et veineuses.
Les effets indésirables suivants peuvent survenir lors de la prise de CHC. Les fréquences sont définies comme suit: fréquents (≥1/100 à <1/10); occasionnels (≥1/1'000 à <1/100); rares (≥1/10'000 à <1/1'000); fréquence intéterminée (la fréquence exacte ne peut être estimée essentiellement sur la base des rapports spontanés issus de la surveillance postcommercialisation).
Infections et infestations
Fréquence inconnue: candidose vulvovaginale.
Affections du système immunitaire
Rares: réactions d'hypersensibilité.
Fréquence inconnue: œdème de Quincke.
Troubles du métabolisme et de la nutrition
Fréquents: prise pondérale.
Occasionnels: rétention liquidienne, changement dans l'appétit.
Rares: perte pondérale.
Affections psychiatriques
Fréquents: humeur dépressive, modification de l'humeur.
Occasionnels: diminution de la libido.
Rares: augmentation de la libido.
Affections du système nerveux
Fréquents: céphalées, vertiges.
Occasionnels: migraine.
Affections oculaires
Rares: mauvaise tolérance des lentilles de contact.
Affections cardiaques/Affections vasculaires
Rares: thromboembolie veineuse (p.ex. thrombose veineuse profonde, embolie pulmonaire), thromboembolie artérielle (p.ex. accident ischémique transitoire, accident vasculaire cérébral, infarctus du myocarde), augmentation de la tension.
Affections gastro-intestinales
Fréquents: nausées.
Occasionnels: vomissements, diarrhées.
Affections hépatobiliaires
Rares: cholélithiase, ictère cholestatique, tumeurs hépatiques.
Affections de la peau et du tissu sous-cutané
Occasionnels: érythème, urticaire, prurit généralisé.
Rares: chloasma, érythème noueux, érythème polymorphe, acné, alopécie.
Affections des organes de reproduction et du sein
Fréquents: douleurs du bas-ventre, sensation de tension ou douleurs dans les seins, saignements intermenstruels.
Occasionnels: aménorrhée, augmentation du volume du sein.
Rares: galactorrhée, sécrétions vaginales respectivement modifications des sécrétions vaginales.
Fréquence inconnue: vaginite, cervicite.
Troubles généraux et anomalies au site d'administration
Occasionnels: œdème.
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageOn ne dispose d'aucune déclaration sur des conséquences sévères d'un surdosage. Les symptômes d'un surdosage sont nausées, vomissements et saignements vaginaux. Ces derniers peuvent également survenir chez les jeunes filles avant la ménarche suite à la prise accidentelle du médicament.
Il n'existe pas d'antidote spécifique. Un traitement symptomatique est éventuellement requis.
Propriétés/EffetsCode ATC
G03AA10
Mécanisme d'action
Comme pour tous les contraceptifs hormonaux combinés (CHC), l'action contraceptive de Femadiol-Mepha 20 repose sur différents facteurs dont les plus importants sont le blocage de l'ovulation et la modification de la glaire cervicale. En outre, l'endomètre offre des conditions défavorables à une nidation en raison des altérations morphologiques et enzymatiques qu'il subit. Enfin, du fait des modifications hormonales induites par le CHC, les cycles deviennent plus réguliers et les saignements moins abondants. Pour autant qu'ils soient pris correctement, les contraceptifs hormonaux combinés présentent un taux d'échec inférieur à 1% par an.
Pharmacodynamique
Voir rubrique «Mécanisme d'action».
Efficacité clinique
Voir rubrique «Mécanisme d'action».
PharmacocinétiqueGestodène
Absorption
Après administration orale, le gestodène est résorbé rapidement et complètement. Des concentrations sériques maximales de 3.5 ng/ml sont atteintes environ 1 heure après l'administration d'une dose unique.
La biodisponibilité est d'environ 99%.
Distribution
Le gestodène est lié aussi bien à l'albumine sérique qu'à la sex hormone binding globulin (SHBG). Seuls 0.6-2% de la concentration sérique totale sont sous forme de stéroïde libre, 50–85% sont liés spécifiquement et avec une forte affinité pour la SHBG. L'augmentation de la concentration de SHBG induite par l'éthinylestradiol influe sur la liaison relative aux protéines sériques, entraînant une augmentation de la liaison à la SHBG et une diminution de la liaison à l'albumine et de la fraction libre. Le volume de distribution du gestodène est de 0.7 l/kg.
Métabolisme
Le gestodène est complètement métabolisé dans le foie, par réduction du groupement cétonique 3 et de la double liaison Δ-4, ainsi que par un certain nombre d'étapes d'hydroxylation. Aucune interaction avec l'éthinylestradiol administré simultanément n'a été constatée.
Élimination
Les concentrations sériques de gestodène diminuent biphasique, avec une demi-vie terminale de 12–22 heures. La clearance plasmatique totale est de 0.8 ml/min/kg. Les métabolites sont éliminés dans un rapport de 6:4 dans les urines et dans la bile, leur demi-vie est d'environ 24 heures.
Conditions à l'état d'équilibre
La pharmacocinétique du gestodène est influencée par les taux de SHBG qui sont multipliés par deux par l'éthinylestradiol. Lors d'une prise quotidienne, les taux sériques de gestodène quadruplent à peu près, l'état d'équilibre étant atteint dans la deuxième moitié du cycle d'administration.
Éthinylestradiol
Absorption
Après administration orale, l'éthinylestradiol est résorbé rapidement et complètement. Des concentrations sériques maximales d'environ 65 pg/ml sont atteintes 1.7 heures après l'administration d'une dose unique.
Suite à une métabolisation présystémique (effet de premier passage), la biodisponibilité absolue est d'environ 45% avec une grande variabilité interindividuelle de 20–65%.
Distribution
L'éthinylestradiol est très fortement mais non spécifiquement lié à l'albumine sérique (environ 98%) et induit une augmentation des concentrations sériques de SHBG. Le volume de distribution est d'environ 2.8–8.6 l/kg.
Métabolisme
L'éthinylestradiol fait l'objet d'un métabolisme présystémique aussi bien dans la muqueuse de l'intestin grêle que dans le foie. Il subit une conjugaison dans la muqueuse de l'intestin grêle et est dégradé dans le foie par un métabolisme de phase-I (principaux métabolites: 2-hydroxyéthinylestradiol et 2-méthoxyéthinylestradiol) et une conjugaison. Le cytochrome 3A4 est fortement impliqué dans le métabolisme.
Élimination
Les taux sériques d'éthinylestradiol diminuent en deux phases, avec une demi-vie d'environ 1 heure, respectivement de 10–20 heures. La clairance est de 2.3-7 ml/min/kg environ. L'éthinylestradiol est éliminé seulement sous forme de ses métabolites par voie biliaire et par voie rénale dans un rapport de 6:4. Les conjugués d'acide glucuronique et de sulfate de l'éthinylestradiol ainsi que les métabolites de phase I sont soumis à un cycle entéro-hépatique. La demi-vie d'élimination des métabolites est d'environ 24 heures.
Conditions à l'état d'équilibre
Lors d'une prise quotidienne, les taux sériques d'éthinylestradiol atteignent leur état d'équilibre au bout d'une semaine environ.
Cinétique pour certains groupes de patients
On ne dispose pas de données sur la pharmacocinétique chez des femmes atteintes d'insuffisance rénale ou hépatique
Données précliniquesLes études précliniques effectuées avec les contraceptifs oraux combinés sur la toxicité après administration répétée, la génotoxicité et le potentiel carcinogène n'ont montré aucun indice clair de risques particuliers pour l'être humain, même si un risque accru de carcinome hépatique a pu être mis en évidence dans des études épidémiologiques. Celui-ci a été observé principalement lors de l'administration au long cours (>6 ans) chez des femmes ne souffrant pas de cirrhose hépatique ainsi que HBV et HCV négatives.
Chez les animaux d'expérience, l'éthinylestradiol a déjà présenté un effet embryolétal à une posologie relativement faible, lequel est considéré comme spécifique à l'espèce; des malformations du tractus urogénital et une féminisation des fœtus de sexe masculin ont été observées. L'extrapolation à l'homme de ces résultats expérimentaux chez l'animal, est contestée.
Les études toxicologiques de reproduction chez le rat, la souris et le lapin n'ont montré aucun indice d'action tératogène. Voir la rubrique «Grossesse, Allaitement» pour les risques chez l'être humain.
Remarques particulièresInfluence sur les méthodes de diagnostic
Les stéroïdes contraceptifs peuvent perturber les résultats de certains tests de laboratoire, tels que les paramètres biochimiques du foie, de la thyroïde, de la fonction surrénalienne et rénale, les taux plasmatiques des protéines (porteuses) et des fractions lipidiques/lipoprotéiniques, les paramètres du métabolisme glucidique, de la coagulation sanguine et de la fibrinolyse. Ces modifications restent en général dans les limites de la normale.
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Remarques particulières concernant le stockage
Conserver dans l'emballage d'origine. Ne pas conserver au-dessus de 25°C. Conserver hors de portée des enfants.
Numéro d’autorisation58323 (Swissmedic).
PrésentationFemadiol-Mepha 20 dragées: 1 x 21, 3 x 21, 6 x 21 (B)
Titulaire de l’autorisationMepha Pharma AG, Basel.
Mise à jour de l’informationAoût 2021.
Numéro de version interne: 9.1
|

