CompositionPrincipes actifs
Eligard 7,5 mg
Acétate de leuproréline
Eligard 22,5 mg
Acétate de leuproréline
Eligard 45 mg
Acétate de leuproréline
Excipients
Eligard 7,5 mg
Poly(DL-lactide-co-glycolide) 50/50, N-méthyl-2-pyrrolidone.
Eligard 22,5 mg
Poly(DL-lactide-co-glycolide) 75/25, N-méthyl-2-pyrrolidone.
Eligard 45 mg
Poly(DL-lactide-co-glycolide) 85/15, N-méthyl-2-pyrrolidone.
Indications/Possibilités d’emploiCarcinome prostatique: traitement palliatif symptomatique du carcinome prostatique hormonodépendant à un stade avancé.
Posologie/Mode d’emploiEligard 7,5 mg / 22,5 mg / 45 mg est administré une fois tous les 1, 3 et 6 mois respectivement sous forme d’injection sous-cutanée. La suspension injectée forme un dépôt solide de principe actif et permet ainsi une libération continue d’acétate de leuproréline pendant 1, 3 ou 6 mois.
Généralement, le traitement du carcinome prostatique au stade avancé requiert un traitement à long terme ne devant pas être interrompu en cas de rémission ou d’amélioration des symptômes.
L’administration d’Eligard doit uniquement être réalisée sous la supervision d’un médecin expérimenté en oncologie, tel qu’un urologue.
Il convient de contrôler la réponse au traitement par Eligard au moyen de paramètres cliniques et de la détermination de la valeur sérique de l’antigène prostatique spécifique (APS).
Des études cliniques ont montré que le taux de testostérone augmentait pendant les 3 premiers jours de traitement chez la plupart des patients non orchidectomisés et qu’il baissait en 3 à 4 semaines pour atteindre des concentrations inférieures à celles observées après une castration iatrogène. Après avoir atteint un taux similaire à celui observé après une castration, le taux de testostérone se maintenait à ce niveau tout au long de la poursuite du traitement. Si le patient ne répond pas de manière optimale au traitement, il est recommandé de vérifier si le taux de testostérone sérique a atteint le niveau de celui observé après une castration ou s’il se maintient à ce niveau.
Chez les patients non orchidectomisés atteints d’un carcinome de la prostate métastatique résistant à la castration, recevant un analogue de la GnRH (comme la leuproréline) et éligibles à un traitement par un inhibiteur de la biosynthèse des androgènes ou par un inhibiteur du récepteur des androgènes, il est possible de poursuivre le traitement par un analogue de la GnRH.
Administration
Les contenus des deux seringues préremplies stériles doivent être mélangés juste avant l’administration sous-cutanée d’Eligard. Il convient d’éviter absolument toute injection accidentelle par voie intra-artérielle ou intraveineuse.
Préparation de la solution/suspension prête à l’emploi: se reporter aux rubriques «Remarques particulières», «Remarques concernant la préparation de la suspension injectable».
Il convient de changer à chaque fois de site d’injection.
Instructions posologiques particulières
Enfants et adolescents
Il n’existe aucune donnée concernant l’utilisation de ce médicament chez l’enfant et l’adolescent de moins de 18 ans.
Patients âgés
Aucune adaptation posologique n’est nécessaire en fonction de l’âge.
Insuffisance hépatique ou rénale
Aucune étude clinique n’a été menée chez des patients souffrant d’insuffisance hépatique ou rénale.
Contre-indications·Patients orchidectomisés (les analogues de la GnRH n’ont pas induit de baisse du taux de testostérone sérique en cas de castration chirurgicale).
·Traitement unique de patients atteints d’un carcinome prostatique avec compression médullaire ou présentant des signes de métastases dans la moelle épinière (voir «Mises en garde et précautions»).
·Femmes et enfants.
·Hypersensibilité à la gonadoréline (GnRH), aux analogues de la GnRH, à l’acétate de leuproréline ou à l’un des excipients de la préparation.
Mises en garde et précautionsHypertension intracrânienne idiopathique
Des cas d’hypertension intracrânienne idiopathique (Pseudotumor cerebri) ont été rapportés chez des patients recevant de la leuproréline. Les patients doivent être informés des signes et symptômes d’une hypertension intracrânienne idiopathique, notamment des céphalées intenses ou récurrentes, des troubles de la vision et des acouphènes. En cas de survenue d’une hypertension intracrânienne idiopathique, il convient d’envisager l’interruption du traitement par la leuproréline.
Réactions indésirables cutanées graves
Des réactions indésirables cutanées graves (SCAR), dont le syndrome de Stevens-Johnson (SSJ) et la nécrolyse épidermique toxique (NET), qui peuvent engager le pronostic vital ou être mortelles, ont été rapportées en lien avec le traitement par la leuproréline. Au moment de la prescription, les patients doivent être informés des signes et des symptômes de ces réactions, et faire l’objet d’une surveillance étroite pour détecter d’éventuelles réactions indésirables cutanées graves. En cas de survenue de signes et de symptômes de telles réactions, le traitement par la leuproréline doit immédiatement être arrêté et un autre traitement doit être envisagé, le cas échéant.
Effets cardiovasculaires
Plusieurs études épidémiologiques à grande échelle portant sur des patients présentant un carcinome prostatique ont montré un risque accru de développement d’infarctus du myocarde et d’accident vasculaire cérébral en cas d’utilisation d’agonistes de la GnRH. Il convient d’évaluer minutieusement ce risque en tenant compte de l’existence d’éventuels autres facteurs de risque cardiovasculaire (hypertension, diabète, hypercholestérolémie) lors de l’élaboration du schéma thérapeutique pour un patient souffrant de carcinome prostatique. Chez les patients traités par des agonistes de la GnRH, il convient de contrôler régulièrement la pression artérielle ainsi que les taux de glycémie et de lipides sériques et de surveiller l’absence de symptômes évocateurs de maladies cardiovasculaires. Les facteurs de risque existants doivent être traités conformément aux directives concernées. Un sevrage androgénique peut allonger l’intervalle QT.
Chez les patients ayant des antécédents d’allongement de l’intervalle QT, chez ceux présentant des facteurs de risque d’allongement de l’intervalle QT, ainsi que chez les patients prenant simultanément d’autres médicaments pouvant allonger l’intervalle QT (voir «Interactions»), le médecin traitant doit évaluer soigneusement le rapport bénéfice-risque avant de commencer le traitement par Eligard en tenant compte de l’apparition éventuelle de torsades de pointes.
Apoplexie hypophysaire
Pendant la période de surveillance du marché, de rares cas d’apoplexie hypophysaire (syndrome clinique secondaire à un infarctus de l’hypophyse) ont été rapportés suite à l’administration d’agonistes de l’hormone de libération des gonadotrophines hypophysaires (GnRH). Dans la majorité de ces cas, le patient présentait un adénome hypophysaire. La plupart des cas sont survenus dans les 2 semaines suivant l’administration de la première dose, et, pour certains cas, dans la première heure. Une apoplexie hypophysaire peut se manifester par des céphalées soudaines, des vomissements, des altérations visuelles, une ophtalmoplégie, un état mental altéré et, occasionnellement, par un collapsus cardiovasculaire. Une prise en charge médicale immédiate est nécessaire.
Il convient donc de ne pas administrer d’agonistes de la GnRH en cas d’adénome hypophysaire connu.
Évolution du taux de testostérone et complications au début du traitement
Comme d’autres analogues de la GnRH, Eligard entraîne une hausse temporaire des concentrations sériques de testostérone, de dihydrotestostérone et des phosphatases acides pendant la première semaine de traitement, entraînant ainsi une exacerbation des symptômes ou l’apparition de nouveaux symptômes, y compris de douleurs osseuses, d’une neuropathie, d’hématurie ou d’obstruction urétérale ou vésicale (voir «Effets indésirables»). Ces symptômes disparaissent à la poursuite du traitement.
L’administration concomitante d’anti-androgènes appropriés peut être envisagée 3 jours avant le début du traitement et poursuivie pendant 2 à 3 semaines afin d’atténuer les éventuelles conséquences d’une augmentation initiale du taux de testostérone et d’une exacerbation des symptômes cliniques. Un certain pourcentage de patients a développé des tumeurs non hormonodépendantes. L’absence d’amélioration clinique malgré une suppression adaptée de la testostérone est un signe que le patient ne peut pas bénéficier d’un traitement par Eligard. Après une castration chirurgicale, Eligard n’entraîne pas de diminution supplémentaire du taux de testostérone sérique chez les hommes. Il convient de décider de la poursuite du traitement en accord avec les directives thérapeutiques actuelles.
Densité osseuse/risque de fracture
Une diminution de la densité osseuse (DMO) a été rapportée dans la littérature médicale chez les hommes ayant subi une orchidectomie ou ayant été traités par des analogues de la GnRH. Le risque de diminution de la DMO est particulièrement accru en présence d’autres facteurs de risque d’ostéoporose, tels qu’un âge avancé, une consommation excessive de nicotine et d’alcool, un surpoids ou un manque d’exercice physique.
Le risque de fractures liées à l’ostéoporose augmente significativement sous traitement anti-androgène. Il n’existe qu’un nombre limité de données à ce sujet. Dans différentes études, des fractures ostéoporotiques ont été observées chez 5 % des patients après 22 mois de traitement pharmacologique par suppression androgénique et chez 4 % des patients après 5 à 10 ans de traitement.
Modifications métaboliques
Une hyperglycémie ainsi qu֦’une augmentation du risque de développer un diabète sucré ont été observées chez des hommes traités par des agonistes de la GnRH. Une hyperglycémie peut être un signe de développement d’un diabète sucré ou d’aggravation du contrôle glycémique chez des patients diabétiques. Il convient de contrôler régulièrement la glycémie et/ou l’hémoglobine glyquée (HbA1c) des patients traités par des agonistes de la GnRH et, le cas échéant, de les prendre en charge en respectant les pratiques cliniques standard. Les modifications métaboliques potentielles liées aux agonistes de la GnRH peuvent également inclure la stéatose hépatique non alcoolique.
Convulsions
Des cas de convulsions ont été rapportés après commercialisation chez des patients traités par acétate de leuproréline, avec et sans prédisposition. Ces convulsions doivent être contrôlées conformément aux pratiques cliniques standard.
Autres mesures de précaution
Des cas d’obstruction urétérale et de compression médullaire pouvant entraîner une paralysie avec ou sans complications fatales ont été rapportés en lien avec des analogues de la GnRH. En cas de développement d’une compression médullaire ou de troubles de la fonction rénale, il convient d’instaurer un traitement standard de ces complications. Les patients présentant des métastases vertébrales et/ou cérébrales ou une obstruction au niveau des voies urinaires doivent être étroitement surveillés pendant les premières semaines de traitement, si possible dans le cadre d’une hospitalisation.
Mises en garde spéciales
Une mauvaise préparation (reconstitution) du produit peut entraîner un manque d’efficacité clinique. Les instructions de manipulation sont décrites dans la rubrique «Remarques particulières». Si elle est trop serrée pendant la reconstitution, l’embase de l’aiguille de sécurité peut se fissurer, ce qui peut entraîner une fuite du médicament pendant l’injection ainsi qu’un potentiel manque d’efficacité du fait d’un sous-dosage. En cas de soupçon d’erreur de manipulation d’Eligard, il convient de contrôler le taux de testostérone. Ce contrôle doit être adapté à chaque patient (voir la rubrique «Évolution du taux de testostérone et complications au début du traitement»).
InteractionsAucune étude pharmacocinétique d’interaction médicamenteuse n’a été effectuée avec Eligard. Il n’existe à ce jour aucun compte rendu concernant des interactions éventuelles entre l’acétate de leuproréline et d’autres médicaments.
Le sevrage androgénique pouvant entraîner un allongement de l’intervalle QT ainsi que l’apparition de torsades de pointes, l’administration concomitante d’Eligard et d’autres médicaments qui peuvent provoquer un allongement de l’intervalle QT ou des torsades de pointes, tels que des antiarythmiques de classe IA (par ex. quinidine, disopyramide) ou de classe III (par ex. amiodarone, sotalol, dofétilide, ibutilide), la méthadone, la moxifoxacine, les antipsychotiques, etc. doit être soigneusement évaluée. Voir «Mises en garde et précautions».
Grossesse, AllaitementSans objet du fait qu’Eligard est contre-indiqué chez les femmes.
Effet sur l’aptitude à la conduite et l’utilisation de machinesAucune étude spécifique n’a été menée au sujet des effets d’Eligard sur l’aptitude à la conduite et l’utilisation de machines. L’aptitude à la conduite et l’utilisation de machines peuvent toutefois être altérées par la fatigue, les vertiges et les troubles visuels qui ont été observés au cours du traitement ou qui sont des conséquences de la maladie sous-jacente.
Effets indésirablesLes effets indésirables observés sous Eligard sont principalement dus à l’effet pharmacologique spécifique de l’acétate de leuproréline, à savoir l’augmentation ou la réduction des concentrations de certaines hormones. Les effets indésirables les plus fréquemment décrits sont: bouffées de chaleur, malaise et fatigue ainsi qu’une irritation locale momentanée au site d’injection. Près de 58 % des patients ont souffert de bouffées de chaleur légères à modérées.
Les effets indésirables sont répartis selon les catégories de fréquence suivantes: très fréquents (≥1/10), fréquents (≥1/100 à <1/10), occasionnels (≥1/1 000 à <1/100), rares (≥1/10 000 à <1/1 000) très rares (<1/10 000) ou «fréquence inconnue» (principalement sur la base de déclarations spontanées effectuées au cours de la période de surveillance du marché, la fréquence exacte ne pouvant donc pas être estimée). Les effets indésirables suivants ont été observés pendant les essais cliniques:
Infections et infestations
Fréquents: rhinopharyngite.
Occasionnels: infection urinaire, infection cutanée locale.
Affections hématologiques et du système lymphatique
Fréquents: altérations hématologiques, allongement du temps de coagulation, anémie.
Occasionnels: allongement du temps de prothrombine.
Affections endocriniennes
Fréquence inconnue: apoplexie pituitaire (voir «Mises en garde et précautions»).
Troubles du métabolisme et de la nutrition
Occasionnels: prise de poids, aggravation d’un diabète sucré, augmentation du taux de triglycérides sériques.
Affections psychiatriques
Occasionnels: rêves anormaux, dépression, perte de libido.
Affections du système nerveux
Fréquents: hypoesthésie.
Occasionnels: vertiges, céphalées, insomnie, troubles de l’odorat et du goût.
Rares: mouvements anormaux et involontaires, amnésie.
Fréquence inconnue: hypertension intracrânienne idiopathique (Pseudotumor cerebri).
Affections oculaires
Fréquence inconnue: troubles de la vision.
Affections cardiovasculaires
Très fréquents: bouffées de chaleur.
Occasionnels: hypotension, hypertension.
Rares: palpitations, syncope et collapsus, embolie pulmonaire.
Fréquence inconnue: allongement de l’intervalle QT.
Affections respiratoires, thoraciques et médiastinales
Occasionnels: rhinorrhée, dyspnée.
Fréquence inconnue: pneumopathie interstitielle.
Affections gastro-intestinales
Fréquents: nausées, diarrhée, gastro-entérite/colite.
Occasionnels: constipation, sécheresse buccale, dyspepsie, vomissements.
Rares: flatulences, éructations.
Affections hépatobiliaires
Occasionnels: augmentation de l’alanine aminotransférase.
Affections de la peau et du tissu sous-cutané
Très fréquents: ecchymoses, érythème.
Fréquents: prurit.
Occasionnels: peau froide et moite.
Rares: alopécie, éruption cutanée, rash.
Fréquence inconnue: syndrome de Stevens-Johnson/nécrolyse épidermique toxique (SSJ/NET), éruption cutanée toxique, érythème multiforme.
Affections musculo-squelettiques et systémiques
Fréquents: augmentation de la créatinine phosphokinase sanguine, raideur musculaire, arthralgies, douleurs dans les extrémités, myalgies.
Rares: douleurs dorsales, crampes musculaires.
Affections du rein et des voies urinaires
Fréquents: miction difficile, fréquence de miction diminuée, dysurie, nycturie, oligurie.
Occasionnels: spasmes de la vessie, hématurie, augmentation de la fréquence des mictions, rétention urinaire.
Affections des organes de reproduction et du sein
Fréquents: sensibilité mammaire, gynécomastie, atrophie testiculaire, douleurs testiculaires, infertilité, dysfonction érectile, réduction de la taille du pénis.
Occasionnels: impuissance, troubles testiculaires.
Rares: douleurs dans la poitrine.
Troubles généraux et anomalies au site d’administration
Très fréquents: fatigue; au site d’injection: brûlures et paresthésies.
Fréquents: malaise, sueurs nocturnes, sensation de faiblesse; au site d’injection: picotements, douleurs et hématome.
Occasionnels: léthargie, transpiration accrue, douleurs, fièvre; au site d’injection: prurit, induration.
Rares: œdème périphérique; au site d’injection: ulcération.
Très rares: au site d’injection: nécrose.
D’autres événements indésirables ont été décrits dans le cadre d’un traitement par l’acétate de leuproréline, notamment une leucopénie, une thrombocytopénie, des altérations de la tolérance au glucose, une faiblesse musculaire, des frissons, une sensibilité cutanée, une atrophie musculaire (en cas d’utilisation prolongée) et des convulsions. Dans de rares cas, des réactions anaphylactiques/anaphylactoïdes ont été rapportées après une administration d’analogues de la GnRH.
L’annonce d’effets secondaires présumés après l’autorisation est d’une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d’effet secondaire nouveau ou grave via le portail d’annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageEligard ne présente aucun risque d’abus et un surdosage volontaire est peu probable. Dans la pratique clinique, aucun cas d’abus ou de surdosage d’acétate de leuproréline n’a été observé. Si une exposition excessive se produisait, il conviendrait de surveiller étroitement le patient et d’instaurer un traitement symptomatique.
Propriétés/EffetsCode ATC
L02AE02
Groupe pharmacothérapeutique: traitement endocrinien, analogue de la GnRH.
Mécanisme d’action
L’acétate de leuproréline est un nonapeptide de synthèse et un analogue de l’hormone naturelle de libération des gonadotrophines hypophysaires (GnRH) qui, en cas de prise prolongée, inhibe la sécrétion des gonadotrophines hypophysaires et réprime la formation des stéroïdes testiculaires chez les individus masculins. Cet effet est réversible après l’arrêt du traitement. Toutefois, cet analogue est plus puissant que l’hormone naturelle et le temps nécessaire pour restaurer le taux de testostérone peut varier selon les patients.
Pharmacodynamique
L’administration d’acétate de leuproréline entraîne une élévation initiale des taux circulants d’hormone lutéinisante (LH) et d’hormone de stimulation folliculaire (FSH), responsables chez les individus masculins d’une augmentation temporaire du taux sérique de stéroïdes gonadiques, de testostérone et de dihydrotestostérone. Une administration continue d’acétate de leuproréline entraîne une réduction des taux de LH et de FSH. Chez l’homme, le taux de testostérone diminue jusqu’à atteindre des valeurs inférieures au seuil de castration (≤ 50 ng/dL). Ces changements apparaissent 3 à 5 semaines après le début du traitement par Eligard 7,5 mg / 22,5 mg / 45 mg. Après 6 mois, les taux moyens de testostérone s’élevaient à 6,1 (± 0,4) ng/dL, 10,1 (± 0,7) ng/dL ou 10,4 (± 0,53) ng/dL, et étaient comparables aux taux observés après une orchidectomie bilatérale.
Efficacité clinique
Tous les patients, sauf un, traités par une dose totale de 45 mg de leuproréline, ont atteint les taux de castration en 4 à 6 semaines. Chez la grande majorité des patients, le taux de testostérone est tombé en dessous de 20 ng/dL, même si le bénéfice clinique d’un taux aussi faible n’a pas encore été établi. Des études à long terme ont montré que, lors d’un traitement continu, le taux de testostérone restait inférieur au seuil de castration pendant une période allant jusqu’à sept ans (et probablement indéfiniment).
Bien que la taille de la tumeur n’ait pas été mesurée directement lors des études cliniques, la réponse de la tumeur au traitement par Eligard a été indirectement démontrée par une réduction du taux moyen d’APS de 94 %, 98 % ou 97 % respectivement après 6 mois.
PharmacocinétiqueAbsorption
Chez les patients atteints d’un carcinome prostatique au stade avancé, les concentrations moyennes de leuproréline sérique s’élevaient à 25,3 ng/mL, 127 ng/mL ou 82 ng/mL (Cmax), 5, 4,6 ou 4,4 heures respectivement après la première injection. Après l’augmentation initiale qui suit chaque injection (plateau de 2 à 28 jours, 3 à 84 jours ou 3 à 168 jours après chaque injection), les concentrations sériques sont restées relativement constantes (0,2 à 2 ng/mL). Il n’existe aucun signe d’accumulation significative lors de l’administration de doses répétées.
Distribution
Le volume moyen de distribution de la leuproréline à l’état d’équilibre après une injection par voie intraveineuse en bolus chez des volontaires masculins sains s’élevait à 27 L. In vitro, la liaison aux protéines plasmatiques humaines atteignait 43 % à 49 %.
Métabolisme
La métabolisation de la leuproréline n’a pas été étudiée.
Élimination
Aucune étude sur l’élimination du principe actif n’a été réalisée avec Eligard. Une injection intraveineuse en bolus de 1 mg d’acétate de leuproréline chez des volontaires masculins sains a entraîné une clairance systémique moyenne de 8,34 L/h, avec une demi-vie d’élimination d’environ 3 heures sur la base d’un modèle à deux chambres.
Cinétique pour certains groupes de patients
Aucune étude sur l’excrétion du principe actif n’a été réalisée avec Eligard.
Données précliniquesLes études précliniques réalisées sur l’acétate de leuproréline ont montré, chez les deux sexes, que la substance avait les effets attendus sur le système reproducteur compte tenu des propriétés pharmacologiques de celle-ci. Ces effets se sont révélés réversibles après l’interruption du traitement et une période de régénération. L’acétate de leuproréline n’a montré aucun effet tératogène. Une embryotoxicité/létalité a été observée chez des lapins en lien avec les propriétés pharmacologiques de l’acétate de leuproréline sur le système reproducteur.
Des études de cancérogénicité ont été réalisées pendant 24 mois sur des rats et des souris. Chez le rat, des adénomes hypophysaires dose-dépendants ont été observés après une injection sous-cutanée de 0,6 à 4 mg/kg/jour. Comme cet effet n’a pas été observé chez la souris, l’effet observé chez le rat est considéré comme spécifique à l’espèce et n’est pas considéré comme pertinent pour l’être humain.
L’acétate de leuproréline ne s’est pas révélé mutagène dans une série de tests réalisés in vitro et in vivo.
Remarques particulièresIncompatibilités
La leuproréline contenue dans la seringue B doit uniquement être mélangée avec le solvant de la seringue A. Elle ne doit pas être mélangée avec d’autres médicaments.
Influence sur les méthodes de diagnostic
Aucune donnée disponible.
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur l’emballage.
Eligard doit être conservé au réfrigérateur (à 2-8 °C) dans son emballage d’origine et hors de portée des enfants. Lorsque le produit est sorti du réfrigérateur, il peut être conservé à température ambiante (à une température ne dépassant pas 25 °C) pendant 4 semaines maximum. Après ouverture du plateau thermo, la poudre et le solvant pour suspension injectable doivent être immédiatement utilisés pour reconstituer le médicament et administrés au patient. La stabilité physico-chimique a été prouvée pendant 30 minutes à 25 °C. La viscosité de la suspension augmente avec le temps.
Remarques particulières concernant le stockage
Tenir hors de la vue et de la portée des enfants.
Après ouverture du plateau thermo, le produit doit être utilisé immédiatement.
Conserver dans l’emballage d’origine, au réfrigérateur (2-8 °C).
Remarques concernant la préparation de la suspension injectable
Les deux seringues préremplies stériles doivent être mélangées juste avant l’injection sous-cutanée. Le produit doit avoir atteint la température ambiante avant l’injection et doit donc être sorti du réfrigérateur environ 30 minutes avant utilisation.
Commencer par préparer le patient pour l’injection. Préparer ensuite la suspension injectable en suivant les instructions ci-après:
Remarques concernant la manipulation
1re étape: Avant de l’utiliser, laisser la préparation se réchauffer à la température ambiante.
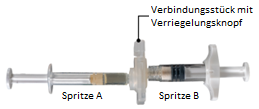
Sur un plan de travail propre, ouvrir le plateau en retirant le film depuis un coin et en sortir le contenu. Jeter le sachet de dessiccant. Retirer le système de seringues préconnectées (Figure 1.1) du plateau. Ouvrir l’emballage de l’aiguille de sécurité (pour Eligard 7,5 mg/22,5 mg: Figure 1.2; pour Eligard 45 mg: Figure 1.3) en décollant la languette en papier. Remarque: les seringues A et B doivent être décalées l’une par rapport à l’autre lorsqu’elles sont connectées au raccord.
|
Figure 1.1
Contenu du plateau: système de seringues préconnectées
|
|
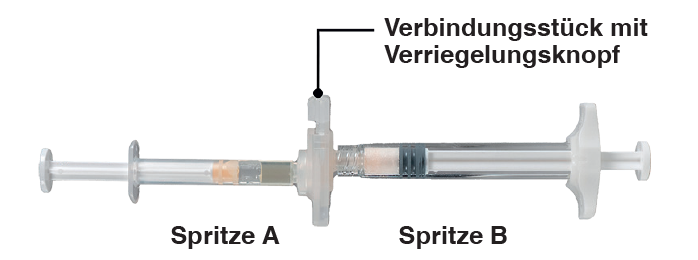
Figure 1.1
Contenu du plateau: système de seringues préconnectées
|
| |
Eligard 7,5 mg / 22,5 mg
|
Eligard 45 mg
|
|
Figure 1.2
Sous le plateau: aiguille de sécurité avec capuchon
| |
|

| |
Eligard 7,5 mg / 22,5 mg
| |
Figure 1.3
Sous le plateau: aiguille de sécurité avec capuchon
| |
Eligard 45 mg
|
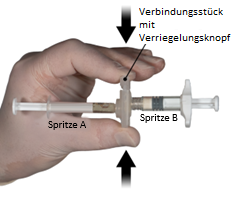
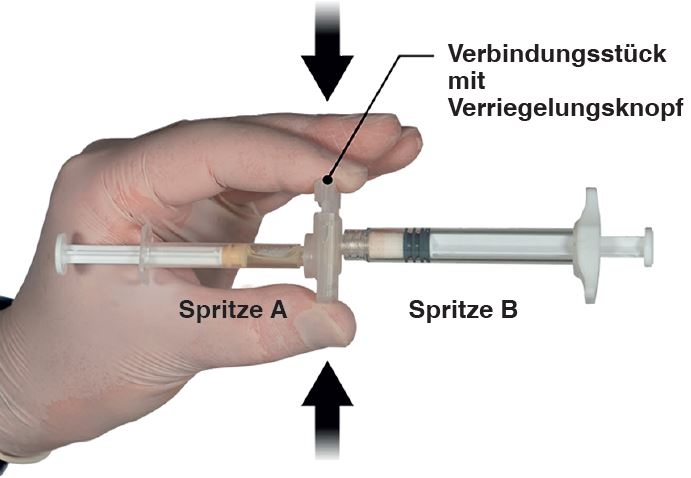
2e étape: Saisir le bouton de verrouillage du raccord entre le pouce et l’un des autres doigts et appuyer (Fig. 2) jusqu’à entendre un bruit d’encliquetage. Les deux seringues sont maintenant alignées. Il n’est pas nécessaire d’orienter particulièrement le système de seringues pour activer le raccord. Ne pas plier le système de seringues (cela pourrait entraîner une fuite de liquide, car les seringues risquent d'être partiellement dévissées).
|
Figure 2
|
Figure 2
| |
|
|
|
| |
Eligard 7,5 mg / 22,5 mg
|
Eligard 45 mg
|
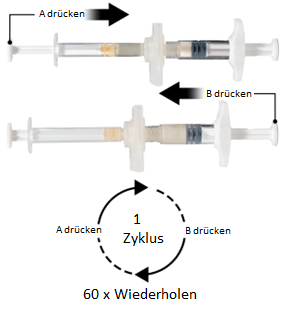
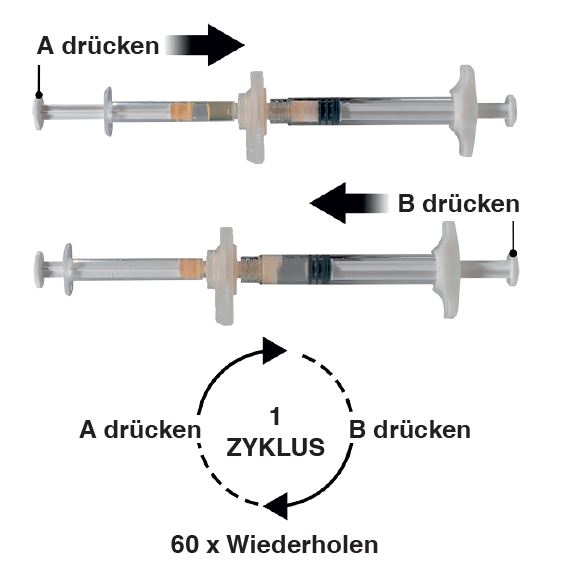
3e étape: Tenir les seringues à l’horizontale et faire passer le contenu liquide de la seringue A dans la seringue B contenant la poudre d’acétate de leuproréline. Mélanger soigneusement le produit pendant 60 cycles en faisant passer avec précaution le contenu d’une seringue à l’autre tout en les maintenant en position horizontale (un cycle correspondant à une pression sur le piston de la seringue A et à une pression sur le piston de la seringue B) afin d’obtenir une solution homogène et visqueuse (Fig. 3). Ne pas plier le système de seringues (cela pourrait entraîner une fuite de liquide, car les seringues risquent d'être partiellement dévissées).
|
Figure 3
|
Figure 3
| |
|
|
|
| |
Eligard 7,5 mg / 22,5 mg
|
Eligard 45 mg
|
Lorsqu’elle est bien mélangée, la solution est visqueuse et incolore à blanche ou brunâtre (il est possible d’observer des nuances blanches à jaune pâle).
Important: une fois la solution mélangée, passer immédiatement à la prochaine étape, car la viscosité de la solution augmente avec le temps. Ne pas remettre le produit préparé au réfrigérateur.
Remarque: la préparation doit être mélangée comme décrit ici. Secouer la préparation NE permet PAS d’obtenir un mélange utilisable.
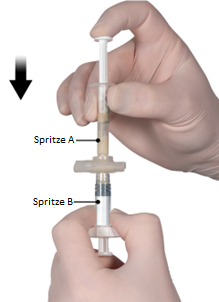
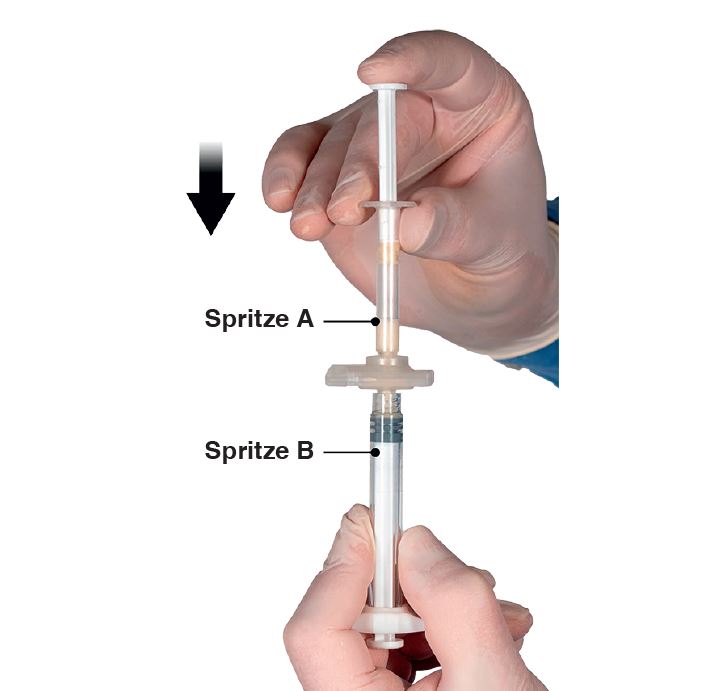
4e étape: Après avoir mélangé la solution, tenir les seringues à la verticale (seringue B en bas). Les seringues doivent être vissées fermement l’une avec l’autre. En appuyant sur le piston de la seringue A et en tirant légèrement sur le piston de la seringue B, faire passer la totalité du mélange dans la seringue B, qui est plus courte et plus large (Figure 4).
|
Figure 4
|
Figure 4
| |
|
| |
|
|
|
| |
Eligard 7,5 mg / 22,5 mg
|
Eligard 45 mg
|
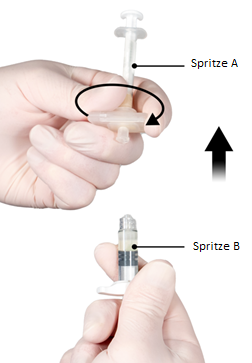
5e étape: Après s’être assuré que le piston de la seringue A est complètement enfoncé, tenir le raccord et dévisser la seringue B. La seringue A reste connectée au raccord (Fig. 5). Aucun liquide ne doit s’échapper; si tel n’est pas le cas, l’aiguille ne pourra pas être correctement vissée.
Remarque: il pourra rester une grosse bulle d’air ou plusieurs petites bulles d’air dans la préparation. Ceci n’est pas un problème.
Pendant cette phase, ne pas essayer de pousser les bulles d’air hors de la seringue B, car cela pourrait entraîner une perte de produit.
|
Figure 5
|
Figure 5
| |
|
|
|
| |
Eligard 7,5 mg / 22,5 mg
|
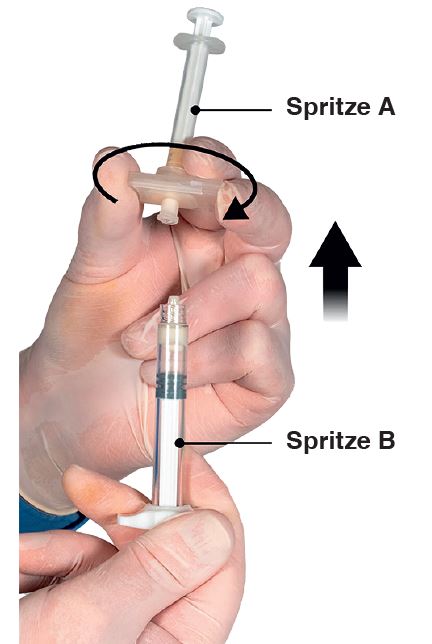
Eligard 45 mg
|
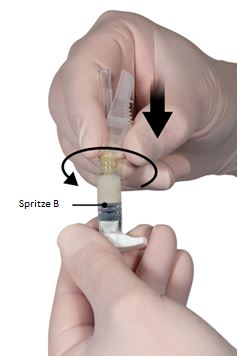
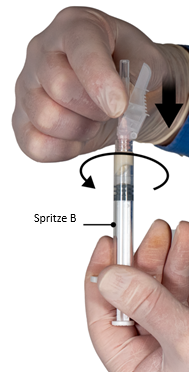
6e étape: Tenir la seringue B à la verticale et retenir le piston blanc afin d’éviter toute perte de produit. Enfin, placer l’aiguille de sécurité sur la seringue B en tenant l’aiguille et en tournant délicatement la seringue d’environ trois quarts de tour dans le sens des aiguilles d’une montre jusqu’à ce que l’aiguille soit bien positionnée (Figure 6).
Ne pas trop tourner la seringue, car cela pourrait fissurer l’embase de l’aiguille et entraîner ainsi une fuite de produit pendant l’injection.
Si l’embase de l’aiguille se brise, semble endommagée ou fuit, ne pas utiliser le produit. L’aiguille défectueuse ne doit pas être remplacée, et le produit utilisé ne doit pas être injecté. La totalité du produit doit être éliminée de manière sécurisée. Si l’embase de l’aiguille est endommagée, utiliser un nouveau produit.
|
Figure 6
| |
|
|
|
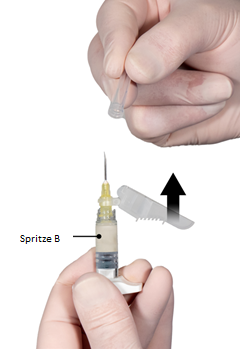
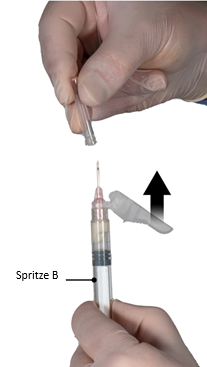
7e étape: Avant l’injection, pousser le dispositif de protection rabattable de l’aiguille et retirer le capuchon de protection de l’aiguille (Figure 7).
Important: Avant l’injection, vérifier que le dispositif de protection de l’aiguille de sécurité n’est pas engagé (voir actionnement du dispositif de protection à la 9e étape). Si l’embase de l’aiguille semble être endommagée ou si du liquide fuit, ne pas utiliser le produit. L’aiguille endommagée ne doit pas être remplacée, et le médicament ne doit pas être injecté. Si l’embase de l’aiguille est endommagée, utiliser un nouveau kit Eligard.
|
Figure 7
| |
|
|
|
8e étape: Avant utilisation, pousser les grosses bulles d’air hors de l’aiguille B. Administrer le produit par voie sous-cutanée tout en maintenant le dispositif de protection écarté de l’aiguille.
Procédure d’administration:
|
·Choisir un site d’injection sur le ventre, la partie supérieure des fesses ou à un autre endroit où la quantité de tissu sous-cutané est suffisante mais qui ne présente pas de pigmentation excessive, ni de nodule, de lésion ou poils et qui n’a pas été utilisé récemment.
·Nettoyer la zone autour du site d’injection avec un tampon d’alcool (non fourni).
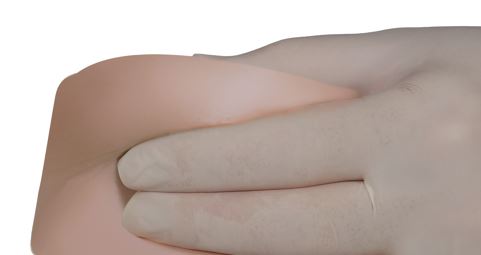
·Saisir la zone de la peau autour du site d’injection entre le pouce et l’index et la pincer.
|
Figure 8
|
| |
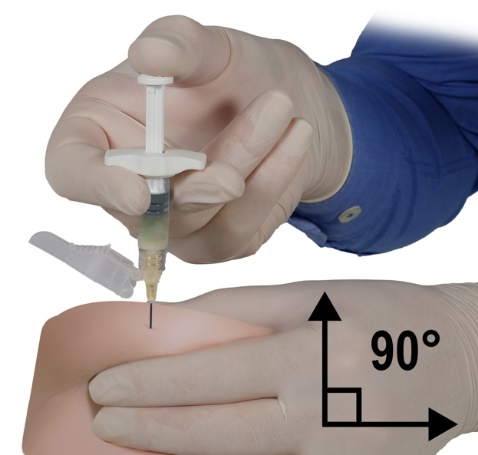
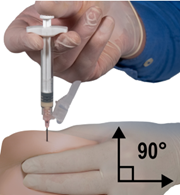
·En utilisant la main dominante, insérer l’aiguille par un geste rapide, à un angle de 90° par rapport à la surface de la peau. La profondeur d’insertion dépend de la quantité de tissu sous-cutané, de sa densité ainsi que de la longueur de l’aiguille. Après insertion de l’aiguille, relâcher la peau.
·Injecter le médicament en appliquant une pression lente et régulière et appuyer sur le piston jusqu’à ce que la seringue soit vide. Avant de retirer l’aiguille, s’assurer que la totalité du produit contenu dans la seringue B a été injectée.
·Tout en maintenant la pression sur le piston, retirer rapidement l’aiguille selon le même angle de 90° que celui utilisé pour l’insertion.
|
|
|
|
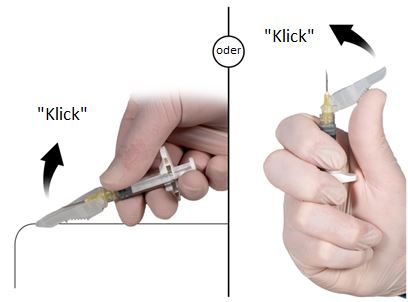
9e étape: Après l’administration du produit, fermer le dispositif de protection de l’une des façons suivantes:
1.Fermeture sur une surface plane
Presser le dispositif de protection avec le levier contre une surface plane (Figure 9a) afin de recouvrir l’aiguille, puis fermer le dispositif de protection.
Un «clic» sonore et tactile indique que le dispositif de protection a bien été fermé. Lorsqu’il est bien fermé, le dispositif de protection recouvre complètement l’aiguille.
2.Fermeture avec le pouce
Placer le pouce sur le dispositif de protection (Figure 9b), recouvrir l’aiguille avec le dispositif de protection, puis fermer le dispositif de protection. Un «clic» sonore et tactile indique que le dispositif de protection a bien été fermé. Lorsqu’il est bien fermé, le dispositif de protection recouvre complètement l’aiguille.
|
Figure 9a
Fermeture sur une surface plane
|
Figure 9b
Fermeture avec le pouce
| |
|
| |
Eligard 7,5 mg / 22,5 mg
|
|
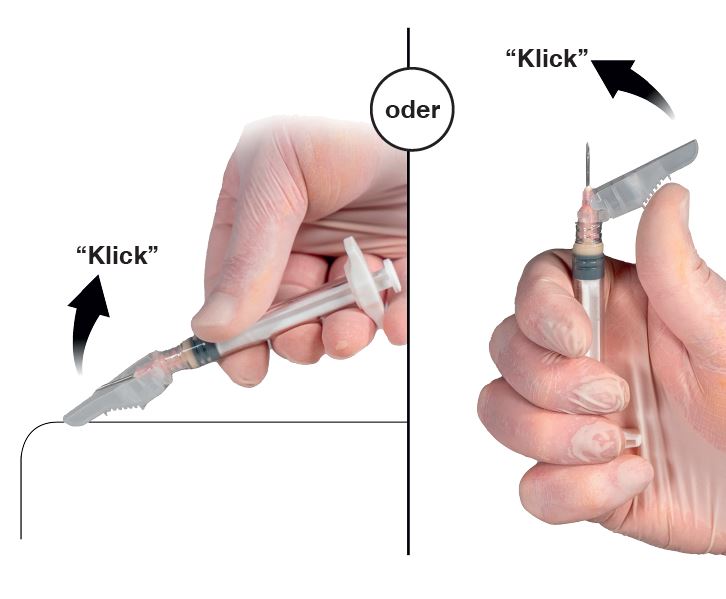
Figure 9a
Fermeture sur une surface plane
|
Figure 9b
Fermeture avec le pouce
| |
|
| |
Eligard 45 mg
|
10e étape: Une fois le dispositif de protection fermé, jeter immédiatement l’aiguille et la seringue dans un conteneur pour seringues adapté.
Numéro d’autorisation56852, 56892, 58431 (Swissmedic)
PrésentationEligard 7,5 mg et 22,5 mg sont fournis dans les emballages suivants:
·Emballage contenant un plateau thermoformé et une aiguille stérile de 20G dans une boîte en carton. Le plateau contient un système de seringues préconnectées et un sachet de dessicant.
Eligard 45 mg
·Emballage contenant un plateau thermoformé et une aiguille stérile de 18G dans une boîte en carton. Le plateau contient un système de seringues préconnectées et un sachet de dessicant.
Titulaire de l’autorisationRecordati AG, 6340 Baar
Mise à jour de l’informationMars 2025
|




















