CompositionPrincipes actifs
Triptoréline, sous forme d'embonate de triptoréline.
Excipients
Polymère D, L lactide-co-glycolide, Mannitol, Carmellose sodique*, Polysorbate 80.
Solvant: Eau pour préparations injectables.
* la quantité de sodium apportée par la carmellose sodique correspond à 2.3 mg par dose.
Indications/Possibilités d’emploiCancer de la prostate hormono-dépendant au stade avancé.
Cancer de la prostate hormono-dépendant localisé à haut risque ou localement avancé traité en association à une radiothérapie (voir «Efficacité clinique»).
Puberté précoce centrale (central precocious puberty, CPP) chez les enfants de 2 ans et plus avec un début de la CPP avant 8 ans chez les filles et 9 ans chez les garçons.
Posologie/Mode d’emploiLa préparation Pamorelin LA 22,5 mg ne doit être utilisée que par les médecins ou le personnel médical.
Mode d'administration
La préparation Pamorelin LA 22,5 mg doit être injectée par voie intramusculaire.
Du fait que Pamorelin LA 22,5 mg est une suspension de microgranules, toute injection intravasculaire doit absolument être évitée. Le site d'injection doit changer périodiquement.
Pour la préparation de la suspension injectable prête à l'emploi, se reporter à la rubrique «Remarques particulières», paragraphe «Mode de préparation».
Posologie usuelle
La posologie usuelle pour toutes les indications est d'une injection intramusculaire de Pamorelin LA 22,5 mg toutes les 24 semaines sous contrôle médical.
Cancer de la prostate
L'efficacité du traitement peut être contrôlée par dosage des taux sériques de la testostérone et de l'antigène spécifique de la prostate (PSA) et appréciation subjective (amélioration des symptômes tels que troubles mictionnels, douleurs cancéreuses, etc.). La testostérone peut être dosée immédiatement avant ou après l'injection.
Puberté précoce centrale
Le traitement des enfants par Pamorelin LA 22,5 mg doit se faire sous la surveillance générale d'un endocrino-pédiatre, d'un pédiatre ou d'un endocrinologue ayant une expertise dans le traitement de la puberté précoce centrale.
Afin d'assurer la surveillance du traitement, des dosages hormonaux adaptés doivent être réalisés entre 1 et 2 mois après l'injection de la première dose, puis à la discrétion du médecin traitant. La taille de l'enfant doit être mesurée tous les 3 à 6 mois. Il faut également procéder à une surveillance régulière de l'âge osseux.
Le traitement doit être arrêté chez les filles avant l'âge de 11 ans et chez les garçons avant l'âge de 12 ans.
Instructions posologiques particulières
Enfants et adolescents
La sécurité et l'efficacité de Pamorelin LA 22,5 mg n'ont pas été étudiées chez les enfants de moins de 2 ans. Une utilisation dans cette classe d'âge n'est donc pas recommandée.
Patients âgés
Une adaptation de la dose en fonction de l'âge n'est pas nécessaire.
Patients présentant des troubles de la fonction rénale
Aucune adaptation de la posologie n'est requise pour les patients souffrant d'une fonction rénale limitée.
Patients présentant des troubles de la fonction hépatique
Aucune adaptation de la posologie n'est requise pour les patients souffrant d'une fonction hépatique limitée.
Contre-indicationsContre-indications générales
Grossesse et l'allaitement (voir «Grossesse et Allaitement»).
Hypersensibilité à la triptoréline, à d'autres analogues de la GnRH, ou à l'un des excipients selon la composition.
Cancer de la prostate
Pamorelin LA 22,5 mg ne doit pas être administré s'il y a des indices en faveur du fait que la tumeur n'est pas hormonodépendante ou après castration chirurgicale.
Pamorelin LA 22,5 mg est contre-indiqué chez les patients ayant une compression médullaire provoquée par des métastases de leur carcinome prostatique.
Mises en garde et précautionsMises en garde générales
Réactions d'hypersensibilité:
Peu après l'injection de Pamorelin LA 22,5 mg ont été observées quelques rares réactions allergiques. De rares cas de choc anaphylactique et d'œdème angioneurotique ont été décrits après administration de triptoréline.
Apoplexie hypophysaire:
De rares cas d'apoplexie hypophysaire (syndrome clinique résultant d'un infarcissement hypophysaire) ont été décrits chez les hommes traités avec des agonistes de la GnRH. Un adénome hypophysaire a été diagnostiqué dans la plupart de ces cas. La plupart des cas se sont produits dans les 2 semaines, certains dans l'heure ayant suivi la première injection. L'apoplexie hypophysaire s'est manifestée par céphalées soudaines, vomissements, troubles visuels, ophtalmoplégie, altération de l'état mental et parfois collapsus cardiovasculaire.
Une intervention médicale immédiate est indispensable.
Il ne faut donc pas administrer d'agoniste de la GnRH en cas d'adénome hypophysaire connu.
Troubles de l'humeur/Dépression:
Des troubles de l'humeur allant jusqu'à des dépressions (dont certaines sévères) ont été rapportés sous traitement par triptoréline. De rares cas d'idées suicidaires ou de tentatives de suicide ont également été rapportés sous traitement par d'autres analogues de la GnRH. Les patients souffrant de dépression (même dans leur anamnèse) doivent donc être étroitement surveillés pendant la prise de Pamorelin LA 22,5 mg. Les patients ou les parents et personnes qui s'occupent des enfants doivent être avertis du risque d'apparition de tels symptômes (et de la possibilité d'une aggravation d'une dépression préexistante).
Convulsions:
Des cas de convulsions ont été rapportés sous traitement par des analogues de la GnRH, en particulier chez les femmes et les enfants. Certains de ces patients présentaient des facteurs de risque de convulsions (comme des antécédents d'épilepsie, des tumeurs intracrâniennes ou un traitement concomitant avec des médicaments connus pour présenter un risque de réactions sous forme de convulsions). Mais des cas de convulsions chez des patients ne présentant aucun facteur de risque de ce type ont également été déclarés.
Patients sous anticoagulants:
Une prudence particulière est de mise chez les patients traités par anticoagulants en raison du risque d'hématome au site d'injection.
Autres précautions
Paresthésies et migraines sévères sont rares. Dans les cas graves ou récidivants, interrompre le traitement.
Une augmentation des lymphocytes a été rapportée chez des patients traités par des analogues de la GnRH.
Mises en garde dans le traitement du cancer de la prostate
Symptômes et complications du cancer de la prostate: Comme les autres agonistes de la GnRH, la triptoréline provoque une ascension passagère du taux de testostérone circulante au cours de la première semaine après la première injection de la forme à libération retardée du principe actif. Ce qui est également possible si l'intervalle entre 2 injections est > 24 semaines. Contrairement à la chute du taux de testostérone suite à une orchidectomie, un faible pourcentage de patients (<5%) peut présenter une aggravation passagère des signes et symptômes de carcinome prostatique en raison de l'ascension initiale du taux de testostérone circulante. Ce qui se manifeste la plupart du temps par une aggravation des douleurs cancéreuses, principalement par une neuropathie, une hématurie et des douleurs osseuses pouvant être maîtrisées par un traitement symptomatique. Des cas isolés peuvent présenter une aggravation de leurs symptômes, soit une obstruction de l'urètre ou du sphincter vésical, ou une compression médullaire par métastases, pouvant s'accompagner de paralysies avec ou sans issue fatale.
Si une compression médullaire ou une insuffisance rénale se déclare, il s'agit de mettre en route un traitement standard de ces complications et d'envisager à l'extrême une orchidectomie en urgence. Un contrôle consciencieux est donc indispensable pendant les premières semaines de traitement, spécialement chez les patients souffrant de métastases vertébrales et/ou d'obstructions des voies urinaires.
Pendant la phase initiale du traitement, envisager l'administration concomitante d'un antiandrogène pour compenser l'ascension initiale du taux sérique de testostérone et prévenir l'aggravation de la symptomatologie clinique.
Ostéoporose / densité osseuse:
L'administration d'analogues de la GnRH synthétiques dans le traitement du carcinome prostatique peut provoquer une fonte osseuse pouvant aller jusqu'à l'ostéoporose et augmenter ainsi le risque de fractures. La conséquence peut être un faux diagnostic de métastases osseuses. Une attention particulière est nécessaire pour les patients présentant des facteurs de risques additionnels d'ostéoporose (comme un abus chronique d'alcool, le tabagisme, la malnutrition, des anamnèses familiales positives d'ostéoporose ou un traitement de longue durée par des médicaments réduisant la densité osseuse tels que les corticoïdes ou les anticonvulsifs).
Risque de diabètes / risque cardiovasculaire:
Des études épidémiologiques ont mis en évidence des changements métaboliques (par exemple une perturbation de la tolérance au glucose, une stéatose hépatique) et un risque accru de diabète sucré et / ou des maladies cardiovasculaires chez les hommes traités avec des agonistes de la GnRH. Néanmoins, les données prospectives n'ont pas confirmé le lien entre le traitement par les analogues de la GnRH et l'augmentation de la mortalité cardiovasculaire. Il est conseillé, avant de commencer le traitement par la triptoréline, d'évaluer le risque de maladies métaboliques ou cardiovasculaires et de surveiller les patients au cours de la thérapie.
Effet sur l'intervalle QT/QTc:
La privation d'androgène à long terme peut prolonger l'intervalle QT. Il est donc conseillé de surveiller les patients ayant un syndrome d'allongement de l'intervalle QT, des troubles électrolytiques ou une insuffisance cardiaque. L'utilisation concomitante de triptoréline avec des médicaments connus pour allonger l'intervalle QT ou capables d'induire des torsades de pointes tels que les antiarythmiques de classe IA (ex. quinidine, disopyramide) ou de classe III (ex. amiodarone, sotalol) doit être évaluée avec précaution.
Risque d'anémie:
En raison de la privation androgénique, le traitement par les analogues de la GnRH peut augmenter le risque d'anémie. Ce risque doit être évalué chez les patients traités et faire l'objet d'une surveillance appropriée.
Mises en gardes dans le traitement de la puberté précoce centrale
Le diagnostic de CPP doit être confirmé avant l'instauration du traitement par des dosages hormonaux adaptés (p.ex. un test de stimulation GnRH) et la présence avérée des symptômes cliniques correspondants.
Les pseudo-pubertés précoces (hyperplasie ou tumeur des glandes surrénales ou des gonades) et les pubertés précoces indépendantes des gonadotrophines (testotoxicose, hyperplasie familiale des cellules de Leydig) devront être exclues.
Il faut en outre exclure l'existence d'une tumeur intracrânienne. Aucune donnée n'est disponible concernant une utilisation de Pamorelin 22,5 mg chez des patients pédiatriques présentant une tumeur intracrânienne. Il faut donc procéder dans ce cas à une évaluation individuelle approfondie du rapport bénéfice-risque.
Chez les filles, il convient de confirmer que la patiente n'est pas enceinte avant de prescrire de la triptoréline.
Au cours du premier mois de traitement chez les filles, la stimulation ovarienne initiale suivie par la suppression des taux des œstrogènes induits par le traitement, peuvent conduire à des saignements vaginaux d'intensité légère ou modérée. Les parents doivent être informés de la survenue possible de tels saignements. Le médecin devra être consulté si les saignements persistent.
Hypertension intracrânienne idiopathique:
Une hypertension intracrânienne idiopathique (pseudotumeur cérébrale) a été rapportée chez des patients pédiatriques recevant la triptoréline. Les patients doivent être avertis des signes et symptômes d'hypertension intracrânienne idiopathique, qui consistent en des maux de tête sévères ou récurrents, des troubles de la vision, des douleurs derrière l'œil, des étourdissements, des nausées et des acouphènes. En cas d'hypertension intracrânienne idiopathique, l'arrêt de la triptoréline doit être envisagé.
Epiphysiolyse:
Une épiphysiolyse de la hanche peut se produire après l'arrêt du traitement. Il se pourrait que ce soit consécutif à l'affaiblissement du cartilage de conjugaison en raison des faibles concentrations en œstrogène pendant le traitement et à l'augmentation de la vitesse de croissance qui se produit après l'arrêt du traitement et qui faciliterait le déplacement des épiphyses.
Densité osseuse:
Le traitement par les agonistes de la GnRH peut entraîner une diminution de la densité minérale osseuse (DMO). Toutefois, après l'arrêt du traitement, le bilan ultérieur de la masse osseuse est préservé et le pic de croissance de la masse osseuse à la fin de la puberté ne semble pas être affecté par le traitement. Il n'existe cependant aucune donnée à long terme sur l'évolution de la densité minérale osseuse après l'arrêt d'un traitement par triptoréline chez les enfants.
Autres précautions chez les enfants
A l'arrêt du traitement, le développement pubertaire reprend.
Les données relatives à la fertilité des patientes traitées par les analogues de la GnRH pendant l'enfance sont encore limitées. Chez la plupart des filles, la ménarche survient environ 1 an après la fin du traitement.
Excipients pharmaceutiques revêtant un intérêt particulier
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c.-à-d. qu'il est essentiellement «sans sodium».
InteractionsInteractions pharmacodynamiques
Quand la triptoréline est coadministrée avec des médicaments affectant la sécrétion hypophysaire de gonadotrophines, une attention particulière doit être donnée et il est recommandé de superviser l'état hormonal du patient.
Interactions pharmacocinétiques
Les cytochromes P450 (CYP) sont peu probablement impliqués dans le métabolisme et l'élimination de la triptoréline. De plus, des données in vitro ont montré que la triptoréline n'est pas un inhibiteur ou un inducteur de CYP, ni un substrat ou inhibiteur de P-glycoprotéine (Pgp). Par conséquent, les interactions pharmacocinétiques avec la triptoréline sont peu probables.
Grossesse, allaitementGrossesse
Aucune étude n'a été réalisée chez les femmes enceintes La triptoréline est contre-indiquée pendant la grossesse, car l'utilisation des agonistes de la GnRH est associée à un risque d'avortement et d'anomalies fœtales.
Allaitement
On ignore si la triptoréline passe dans le lait maternel ou pourrait influer sur la production de lait maternel. La triptoréline est contre-indiquée pendant l'allaitement.
Effet sur l’aptitude à la conduite et l’utilisation de machinesAucune étude n'a été effectuée à ce sujet. Cependant, plusieurs effets indésirables tels qu'apathie, crises épileptiques et anomalies visuelles peuvent atténuer les réflexes et diminuer l'aptitude à la conduite, à l'utilisation d'outils ou de machines.
Effets indésirablesGénéralités
Quelques rares réactions allergiques ont été constatées peu après l'injection de Pamorelin LA 22,5 mg, qui ont régressé sous traitement conventionnel.
Les effets indésirables les plus fréquents observés sous traitement par la triptoréline ont été attribuables à ses effets physiologiques prévus: ascension initiale du taux de testostérone, suivie d'une suppression quasi-totale de la testostérone.
Cancer de la prostate
Une aggravation des douleurs cancéreuses peut survenir pendant 7 à 10 jours après la première injection, du fait de l'augmentation passagère du taux de testostérone (voir «Mises en garde et précautions»). Ces douleurs régressent habituellement dès que le carcinome répond au traitement. Un traitement temporaire par un antiandrogène peut être envisagé.
Les effets observés le plus fréquemment étaient les bouffées de chaleur (70%), les douleurs osseuses (26%) et la diminution du volume des organes génitaux (12%).
Les effets indésirables suivants ont été signalés lors des essais cliniques ou de la pharmacovigilance. En fonction de leur incidence ces effets indésirables sont classés comme suit: très fréquents (≥1/10); fréquents (≥1/100, <1/10); occasionnels (≥1/1'000, <1/100); rares (≥1/10'000, <1/1'000); très rares (<1/10'000), inconnus (reposant principalement sur des annonces spontanées provenant de la surveillance du marché, la fréquence précise ne pouvant être indiquée)
Infections
Occasionnel: infections urinaires.
Néoplasmes
Fréquent: flambée de la tumeur.
Circulation sanguine et lymphatique
Occasionnel: thrombocytose.
Rare: lymphadénopathie.
Inconnu: anémie
Système immunitaire
Occasionnel: réactions d'hypersensibilité (voir aussi «Mises en garde et précautions»).
Troubles endocriniens
Pendant la phase post-marketing, de rares cas d'apoplexie hypophysaire ont été décrits (voir «Mises en garde et précautions»).
Troubles du métabolisme et de la nutrition
Fréquent: ascension de la phosphatase alcaline, hyperuricémie, anorexie.
Occasionnel: hyperglycémie, ascension de l'azote uréique, diabète, augmentation de l'azote non protéique, prise de poids.
Troubles psychiatriques
Fréquent: changements d'humeur, dépression, baisse de la libido.
Occasionnel: nervosité, amnésie, euphorie.
Système nerveux
Fréquent: céphalées, vertiges, insomnie.
Occasionnel: paresthésies, somnolence, pertes de connaissance.
Rare: migraine, dysgueusie, compression médullaire, hypoesthésies.
Inconnu : convulsions.
Troubles oculaires
Fréquent: douleurs visuelles, conjonctivite.
Rare: troubles visuels, perturbations du champ visuel, papille de stase.
Oreille
Occasionnel: acouphènes.
Troubles cardiaques
Rare: ischémie myocardique.
Inconnu : allongement de l'intervalle QT.
Troubles vasculaires
Très fréquent: bouffées de chaleur (70%).
Fréquent: hypertension.
Occasionnel: hypotension, thrombose veineuse profonde, embolie pulmonaire.
Organes respiratoires
Fréquent: toux, dyspnée, pharyngite.
Occasionnel: rhinite.
Troubles gastro-intestinaux
Fréquent: douleurs abdominales, nausée, constipation, diarrhée, dyspepsie.
Occasionnel: vomissement, ténesme, reflux gastro-oesophagien.
Troubles hépato-biliaires
Fréquent: anomalies des fonctions hépatiques.
Occasionnel: hépatite cholestatique.
Troubles cutanés et tissus sous-cutanés
Fréquent: exanthème.
Occasionnel: transpiration plus abondante, alopécie, prurit anal, eczéma, éruption bulleuse.
Rare: urticaire, réactions de photosensibilisation.
Troubles musculosquelettiques
Très fréquent: douleurs osseuses (26%).
Fréquent: dorsalgies, douleurs dans les jambes, arthralgies, myalgies, crampes musculaires des membres inférieurs.
Occasionnel: arthrose, faiblesse musculaire.
Rare: fractures pathologiques.
Troubles rénaux et urinaires
Fréquent: dysurie, rétention urinaire.
Occasionnel: pollakiurie, nycturie, troubles fonctionnels de l'urètre, incontinence urinaire, douleurs rénales, hématurie, anomalies de la fonction rénale.
Organes de reproduction et seins
Très fréquent: diminution de volume des organes génitaux (12%).
Fréquent: impuissance, gynécomastie, douleurs de la glande mammaire.
Occasionnel: troubles prostatiques, troubles testiculaires, inflammation de la glande mammaire.
Troubles généraux et accidents liés au site d'administration
Fréquent: douleurs, fatigue, douleurs thoraciques, asthénie, douleurs au site d'injection, œdèmes périphérique.
Occasionnel: malaise, inflammations et autres réactions au site d'injection.
Rare: douleurs périnéales.
Sécurité dans la population pédiatrique (Puberté précoce centrale)
Les effets indésirables suivants ont été signalés lors de l'utilisation de préparations à base de triptoréline au cours d'essais cliniques ou de la pharmacovigilance. En fonction de leur incidence les effets indésirables sont classés comme suit: très fréquents (≥1/10); fréquents (≥1/100, <1/10); occasionnels (≥1/1'000, <1/100); rares (≥1/10'000, <1/1'000); très rares (<1/10'000), inconnu (reposant principalement sur des annonces spontanées provenant de la surveillance du marché, la fréquence précise ne pouvant être indiquée).
Système immunitaire
Fréquent: réactions d'hypersensibilité (voir aussi «Mises en garde et précautions»)
Inconnu: choc anaphylactique, œdème angioneurotique
Troubles endocriniens
Inconnu: augmentation de la prolactinémie
Troubles du métabolisme et de la nutrition
Fréquent: prise de poids
Occasionnel: obésité.
Troubles psychiatriques
Occasionnel:changements d'humeur.
Inconnu: dépression, nervosité, labilité émotionnelle
Système nerveux
Fréquent: céphalées
Inconnu: convulsions, hypertension intracrânienne idiopathique (pseudotumeur cérébrale)
Troubles oculaires
Occasionnel: troubles visuels.
Inconnu : perturbations du champ visuel.
Troubles vasculaires
Fréquent: bouffées de chaleur.
Inconnu: hypertension
Organes respiratoires
Occasionnel: épistaxis
Troubles gastro-intestinaux.
Fréquent: douleurs abdominales
Occasionnel: nausée, constipation, vomissement
Troubles cutanés et tissus sous-cutanés
Fréquent: acné
Occasionnel: prurit, urticaire, éruption cutanée
Troubles musculosquelettiques
Occasionnel: douleur à la nuque
Inconnu : myalgie
Organes de reproduction et seins
Très fréquent: saignements vaginaux (incluant hémorragie vaginale, saignement de retrait, hémorragie utérine, pertes vaginales, saignements vaginaux, y compris spotting).
Occasionnel: Douleurs mammaires.
Troubles généraux et accidents liés au site d'administration
Fréquent: réaction au site d'injection (incluant douleur au site d'injection douleurs, érythème et inflammation).
Inconnu: malaise.
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageLes caractéristiques pharmacologiques de triptoréline rendent tout surdosage accidentel ou intentionnel improbable. L'expérimentation animale montre qu'aucun autre effet que l'effet thérapeutique prévu sur la concentration des hormones sexuelles et le système reproducteur ne se produit, même à des doses plus élevées de triptoréline.
Traitement
Un éventuel surdosage doit bénéficier d'un traitement symptomatique.
Propriétés/EffetsCode ATC
L02AE04
Mécanisme d'action
Le remplacement de l'acide aminé glycine par le D-tryptophane en position 6 de la gonadoréline donne un agoniste dont l'activité biologique est plus puissante que celle de l'hormone naturelle Gonadotropine-Releasing-Hormone (GnRH). Cette augmentation de l'effet peut être attribuée à une affinité renforcée pour les récepteurs hypophysaires et à une inactivation plus lente dans le tissu cible.
Pharmacodynamique
Lors de l'administration unique et intermittente de GnRH, la libération de LH et de FSH par l'hypophyse est stimulée. En cas de dosage continu par contre, comme cela se produit lors de la libération retardée après l'injection de Pamorelin LA 22,5 mg, un effet «paradoxal» peut être observé: les taux plasmatiques de LH, FSH, testostérone et œstrogènes/progestérone descendent au niveau de la castration en l'espace de quelques 2-4 semaines, après une augmentation passagère enregistrée au début du traitement. Ce qui provoque une atrophie des organes sexuels accessoires. Ces effets sont généralement réversibles après la fin de ce traitement médicamenteux.
Chez les enfants avec puberté précoce, l'inhibition de l'hyperactivité gonadotrope hypophysaire conduit à une baisse des taux de LH selon le test de stimulation de GnRH (ou agoniste de la GnRH) et à la suppression de la sécrétion d'oestradiol et de testostérone chez les filles et les garçons, respectivement. On peut s'attendre, après l'arrêt du traitement par triptoréline, à ce que les processus de maturation physiologiques reprennent dès que les gonadotrophines ont à nouveau atteint des taux du stade prépubère.
Les dérivés embonate et acétate de triptoréline sont équivalents en matière de pharmacodynamique et de toxicité et sont interchangeables.
Efficacité clinique
Cancer de la prostate
Pamorelin LA 22,5 mg a fait l'objet d'une étude clinique de type ouvert, non contrôlée, conduite chez 120 patients masculins d'Afrique du Sud atteints d'un carcinome prostatique à un stade avancé, dont 64% de Caucasiens, 23% de Noirs et 13% d'autres ethnies. Leur âge allait de 51 à 96 ans (moyenne d'âge 71 ans).
Ces patients ont reçu Pamorelin LA 22,5 mg (n = 120) tous les 168 jours avec un total de 2 doses (durée maximale de traitement: 336 jours). Les critères primaires d'efficacité étaient l'atteinte du niveau de castration après 29 jours et son maintien du 57e au 337e jour.
Les taux sériques de testostérone correspondant au niveau de castration (≤1,735 nmol/l) ont été atteints le 29e jour chez 117 des 120 patients (97,5%) traités par Pamorelin LA 22,5 mg.
Les taux sériques de testostérone correspondant au niveau de castration ont été maintenus du 57e au 337e jour chez 93% des patients traités par Pamorelin LA 22,5 mg.
Lors d'un essai clinique randomisé de phase III, (EORTC 22961) incluant 970 patients atteints de cancer de la prostate localement avancé (principalement T2c-T4, avec des patients T1c à T2b avec un envahissement ganglionnaire régional) et traités par radiothérapie, 483 patients ont été traités par une suppression androgénique courte (6 mois) associée et 487 patients par une suppression androgénique longue (3 ans) associée. Globalement, la mortalité totale à 5 ans était de 19% dans le groupe «traitement hormonal court» et de 15% dans le groupe «traitement hormonal long», soit un risque relatif de 1,42. La mortalité à 5 ans spécifiquement liée au cancer de la prostate était 5% dans le groupe «traitement hormonal court» et de 3% dans le groupe «traitement hormonal long», soit un risque relatif de 1,71.
Puberté précoce centrale:
Lors d'une étude clinique non comparative, 44 enfants atteints de puberté précoce centrale (39 filles et 5 garçons) ont reçu 2 injections intramusculaires de Pamorelin LA 22,5 mg à un intervalle de 6 mois et ont fait l'objet d'une surveillance pendant 12 mois (48 semaines). La suppression des concentrations de LH stimulée à des taux prépubères a été atteinte chez 93% et 98% des sujets aux 6ème et 12ème mois respectivement.
Par la suite, une régression ou une stabilisation des caractéristiques sexuels secondaires est constatée ainsi qu'un ralentissement de la maturation osseuse accélérée et de la croissance. Après 6 mois de traitement, plus de 90% des filles, et 3 des 5 garçons atteignent des taux de LH correspondant à un niveau prépubertaire. Vu le nombre très limité de garçons inclus dans l'étude, il n'est pas possible d'exclure d'éventuelles différences dans la réponse au traitement en fonction du sexe.
PharmacocinétiqueAbsorption
Après une injection intramusculaire unique de Pamorelin LA 22,5 mg chez des patients atteints de carcinome prostatique, le tmax était de 3 (2-12) heures et la Cmax (0-169 jours) de 40,0 (22,2-76,8) ng/ml.
Aucune accumulation cliniquement significative n'a été observée à la suite de la deuxième injection.
Distribution
Après une administration intraveineuse en bolus, la distribution de la triptoréline correspond à un modèle à 3 compartiments avec des demi-vies de 6 minutes, 45 minutes et 3 heures. Le volume de distribution correspond approximativement à 30 litres à l'état d'équilibre. Dans des concentrations cliniquement relevantes la triptoréline ne se lie pas aux protéines plasmatiques.
Métabolisme
Aucun métabolite de la triptoréline n'a été découvert chez l'être humain. Mais les données pharmacocinétiques humaines montrent que les fragments C-terminaux produits par destruction tissulaire sont soit entièrement détruits dans les tissus, soit rapidement définitivement détruits dans le plasma soit éliminés par les reins. L'implication des enzymes CYP450 dans le métabolisme est peu probable.
Élimination
La triptoréline est éliminée par le foie et les reins. Après injection i.v. de 0,5 mg de triptoréline, 42% de cette dose ont été éliminés dans les urines sous forme de triptoréline non métabolisée.
La clearance totale de la triptoréline est d'environ 200 ml/min et sa demi-vie terminale de 2,8 heures.
Cinétique pour certains groupes de patients
Enfants et adolescents
Il n'existe que des données pharmacocinétiques limitées chez les patients pédiatriques. La Cmax et le Tmax ne diffèrent pas de manière significative de ceux des adultes.
Patients âgés
L'influence de l'âge sur la pharmacocinétique de la triptoréline n'a pas été systématiquement étudiée. Les données pharmacocinétiques recueillies sur de jeunes volontaires de sexe masculin âgés de 20 à 22 ans ayant une clairance de la créatinine supraphysiologique (env. 150 ml/min) indiquent cependant que la triptoréline est éliminée deux fois plus vite chez les jeunes, ce qui est imputable au fait que la clairance de la créatinine diminue avec l'âge.
Troubles de la fonction rénale
En cas d'insuffisance rénale, la clairance de la triptoréline diminue proportionnellement à celle de la créatinine. Ainsi, chez les patients adultes atteints d'insuffisance rénale modérée (clairance de la créatinine moyenne de 40 ml/min), l'AUC était environ le double de celle de patients ayant une fonction rénale normale, et chez les patients atteints d'insuffisance rénale sévère (clairance de la créatinine moyenne de 8,9 ml/min), elle était environ 2,5 fois plus élevée.
La demi-vie était de 6,7 heures chez les patients ayant une insuffisance rénale modérée et de 7,8 heures chez les patients souffrant d'insuffisance rénale grave.
Troubles de la fonction hépatique
Chez les patients adultes ayant une fonction hépatique limitée, l'AUC de la triptoréline était environ 3,7 fois plus élevée que chez des sujets sains et la demi-vie de triptoréline était de 7,65 heures. La part de triptoréline non métabolisée éliminée par les urines s'est accrue à 62% chez ces patients.
Données précliniquesLa toxicité aiguë de la triptoréline est faible. Les effets observés sont essentiellement liés à une exacerbation de l'effet pharmacologique de la triptoréline.
Après administration chez le rat par voie sous-cutanée de 10 µg/kg du jour 6 à 15 de la gestation (comparativement à la dose clinique de 3,75 mg toutes les 4 semaines chez l'être humain), la triptoréline n'a eu aucun effet embryotoxique, tératogène ni foetotoxique. Cependant, une diminution de la prise pondérale maternelle et une augmentation de la résorption ont été observées à 100 µg/kg.
Toxicité en cas d'administration répétée
Aucune étude sur la fertilité chez le rat mâle n'a été effectuée; lors d'études de toxicologie chronique, la triptoréline induit à doses cliniques des changements macro- et microscopiques sur l'appareil reproducteur chez les rats et les chiens mâles. Ces effets sont considérés comme reflétant la suppression de la fonction gonadique due à l'activité pharmacologique du principe actif. Ces lésions ont partiellement régressé lors de la phase de récupération.
Mutagénicité
La triptoréline n'est pas mutagène, pas plus in vitro qu'in vivo.
Carcinogénicité
Une étude de carcinogenèse de 23 mois chez le rat a montré à chaque palier posologique une manifestation de presque 100% de tumeurs hypophysaires bénignes ayant entraîné la mort prématurée. Cette incidence accrue de tumeurs hypophysaires bénignes chez le rat est un effet fréquent du traitement par agonistes de la GnRH. L'importance clinique de cette observation n'est pas connue.
Administrée à des souris à des doses allant jusqu'à 6'000 µg/kg, la triptoréline n'a fait preuve d'aucun effet oncogène après 18 mois de traitement.
Toxicité sur la reproduction
A une dose 8 fois supérieure à celle recommandée chez l'être humain (par rapport à la surface corporelle), l'expérimentation animale a montré une toxicité chez le rat pour l'organogenèse (toxicité maternelle et embryotoxicité). Des cas isolés d'hydro-uretère ont été constatés chez des jeunes rats exposés in utero à des doses élevées de triptoréline.
Dans le cadre de la procréation médicalement assistée, la triptoréline a souvent été utilisée dans des études contrôlées pour la suppression des gonadotrophines et œstrogènes endogènes.
Remarques particulièresIncompatibilités
En l'absence d'études de compatibilité, ce médicament ne doit pas être mélangé avec d'autres médicaments.
Influence sur les méthodes de diagnostic
La triptoréline à doses thérapeutiques provoque une suppression du système hypophyso-gonadique. La fonction normale est d'habitude rétablie après l'arrêt du traitement. Les résultats des tests fonctionnels diagnostiques hypophyso-gonadiques effectués pendant le traitement ou 4 à 12 semaines après interruption des agonistes de la GnRH pourraient donc être erronés.
Conservation
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur l'emballage.
Conservation après ouverture
Pour des raisons microbiologiques, la suspension doit être injectée immédiatement après sa reconstitution.
Remarques particulières concernant le stockage
Ne pas conserver au-dessus de 25°C.
Ne pas congeler.
Conserver dans l'emballage d'origine.
Conserver le récipient fermé.
Conserver hors de portée des enfants.
Remarques concernant la manipulation
La préparation de la suspension pour injection doit se faire immédiatement avant l'injection.
Voir le mode d'emploi illustré en fin de document.
Numéro d’autorisation61238 (Swissmedic)
PrésentationPamorelin LA 22,5 mg est délivré en 2 présentations:
·1 flacon avec poudre pour 22,5 mg de triptoréline,
·1 seringue pré-remplie contenant 2 ml de solvant,
·1 adaptateur de flacon et 1 aiguille (A)
ou
·1 flacon avec poudre pour 22,5 mg de triptoréline,
·1 ampoule contenant 2 ml de solvant,
·1 seringue et 2 aiguilles. (A)
Titulaire de l’autorisationDebiopharm Research & Manufacturing SA, 1920 Martigny
Mise à jour de l’informationAvril 2025
02-010626/12
Instructions pour la préparation de la suspension
Instructions générales et recommandations
Le produit est une suspension de microparticules:
·Le produit est une suspension de microparticules qui peuvent sédimenter dans le diluant. Le produit devrait être d'apparence homogène, épaisse et laiteuse. Si le produit sédimente dans le flacon, agiter-le à nouveau:
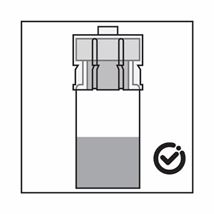
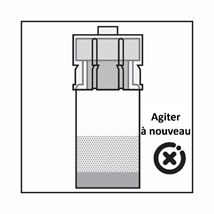
·Si les particules sédimentent dans la seringue, cela entraîne un blocage de l'aiguille lors de l'administration. Il est très important d'injecter le produit dans les 2 minutes suivant la reconstitution dans le flacon.
·Si le produit sédimente dans la seringue, reprendre un peu d'air dans la seringue, puis agiter à nouveau, et expulser l'air (sans amorcer l'aiguille) avant de l'administrer.
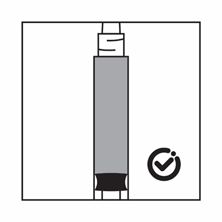
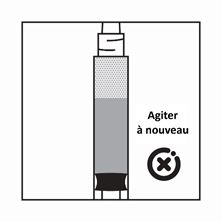
Instructions pour la préparation de la suspension de Pamorelin LA 22,5 mg dans la présentation avec seringue pré-remplie de solvant
|
1
|
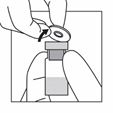
Prendre le flacon contenant la poudre.
Enlever le couvercle plastique du flacon.
|
|
| |
2
|
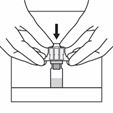
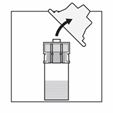
Retirer le film protecteur du système d'adaptation.
Ne pas retirer l'adaptateur de flacon du blister. Déposer le flacon sur une surface plate et dure. Centrer l'adaptateur de flacon sur le bouchon du flacon et appuyer jusqu'à ce qu'un déclic se fasse entendre.
Retirer et éliminer le blister.
|
|
|
| |
3
|
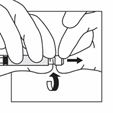
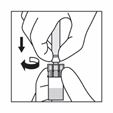
Prendre la seringue, la tenir par le connecteur (rotatif) plastique entre l'index et le pouce d'une main puis dévisser son capuchon de l'autre main.
En tenant toujours la seringue par le connecteur rotatif, l'attacher verticalement à l'adaptateur en opérant un demi-tour dans le sens des aiguilles d'une montre (seulement jusqu'à ce qu'une résistance soit ressentie).
Attention un serrage excessif peut entraîner une déconnexion et des fuites.
|
|
|
| |
4
|
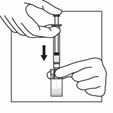
En tenant bien le flacon au niveau de l'adaptateur d'une main, pousser le piston de la seringue de l'autre main puis injecter lentement tout le contenu de la seringue dans le flacon.
A ce stade préparer le patient pour l'injection. Les étapes suivantes doivent être réalisées sans interruption.
|
|
| |
5
|
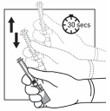
Tenir tout le dispositif (seringue + adaptateur + flacon) fermement dans la main puis agiter le vigoureusement de haut en bas pendant 30 secondes.
Vérifier l'apparence de la suspension en regardant par le fond du flacon. La suspension devrait être d'apparence homogène, épaisse et laiteuse.
Agiter le dispositif de nouveau en cas de sédimentation.
Si une partie de la suspension remonte dans la seringue pendant l'agitation, pousser le piston pour remettre la suspension dans le flacon et agiter à nouveau avant de passer à l'étape suivante.
Le produit doit maintenant être injecté dans les 2 minutes.
|
|
| |
6
|
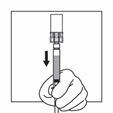
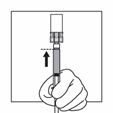
Tourner immédiatement le dispositif de sorte à ce que le flacon soit en haut et la seringue en bas et tirer doucement sur la tige du piston afin d'aspirer tout le contenu du flacon dans la seringue.
|
|
|
| |
7
|
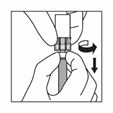
Une fois tout le contenu aspiré dans la seringue, chasser l'air de la seringue dans le flacon. S'arrêter quand la suspension arrive à la base de la tête de la seringue.
|
|
| |
|
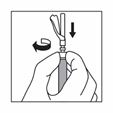
Déconnecter la seringue de l'adaptateur en tenant la seringue d'une main et de l'autre main tourner l'adaptateur dans le sens inverse des aiguilles d'une montre.
En tenant la seringue par le connecteur rotatif, attacher l'aiguille pour injection.
S'assurer que le produit est homogène, épais, laiteux et qu'il n'y a pas de sédimentation avant l'injection.
|
|
|
| |
8
|
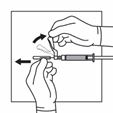
Déplacez la gaine de sécurité en arrière de l'aiguille et vers le corps de la seringue. La gaine de sécurité reste dans la position où elle a été mise.
Retirer la protection transparente de l'aiguille.
|
|

| |
|
Ne pas amorcer l'aiguille avec la suspension.
La seringue contenant la suspension est maintenant prête à être administrée. La suspension doit être administrée immédiatement (moins de 2 minutes après reconstitution) pour éviter un épaississement excessif de la suspension.
|
|
| |
9
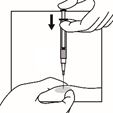
|
Injecter la suspension relativement rapidement et sans interruption par voie intramusculaire. Veiller à ce que toute la quantité de produit soit injectée dans les 10 secondes sans interruption.
Les sites d'injection doivent être alternés.
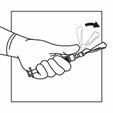
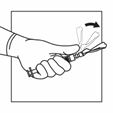
Activer le système de sécurité de l'aiguille d'injection en centrant votre pouce ou votre index sur la zone texturée de la gaine de sécurité et en le poussant vers l'avant sur l'aiguille jusqu'à ce que vous entendiez ou sentiez qu'il se verrouille. Effectuer l'opération avec une seule main et activer le mécanisme loin de vous et des autres. Jeter immédiatement la seringue dans un conteneur pour objets tranchants après une seule utilisation.
|
|
|
|
Jeter les aiguilles dans un conteneur prévu à cet effet.
A usage unique seulement. Toute suspension non utilisée doit être éliminée.
Instructions pour la préparation de la suspension de Pamorelin LA 22,5 mg dans la présentation avec ampoule de solvant
|
1. Préparation de l'injection
2 aiguilles sont fournies dans le set:
·L'aiguille de reconstitution sans système de sécurité
·L'aiguille d'injection avec système de sécurité
·Tapoter la solution se trouvant éventuellement dans le sommet de l'ampoule pour la faire couler dans le réservoir principal de l'ampoule de solvant.
·Tourner l'aiguille sans système de sécurité sur la seringue (ne pas encore enlever la protection d'aiguille!).
·Casser l'ampoule de solvant (point contre soi).
|
| |
·Retirer la protection de l'aiguille de reconstitution et aspirer tout le solvant dans la seringue (fig. A).
·Mettre de côté la seringue contenant le solvant.
·Prendre le flacon contenant la poudre.
·Enlever le couvercle plastique du flacon.
|
|
| |
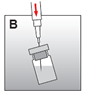
·Reprendre la seringue contenant le solvant et enfoncer l'aiguille dans le bouchon caoutchouc du flacon et injecter lentement le solvant de manière à ce qu'il coule largement sur la paroi du flacon (fig. B).
·A ce stade préparer le patient pour l'injection. Les étapes suivantes doivent être complétées sans interruption.
|
|
| |
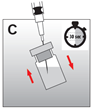
·Retirer l'aiguille en dessus du niveau du liquide et agiter vigoureusement le flacon pendant 30 secondes. La suspension doit avoir un aspect laiteux et homogène (fig. C). Vérifier qu'il ne reste pas de poudre dans le flacon, et si nécessaire continuer la mise en suspension jusqu'à disparition complète de la poudre.
Attention: le mélange ne doit pas se faire par aspirations et vidanges répétées avec la seringue!
·Le produit doit maintenant être injecté dans les 2 minutes.
|
|
| |
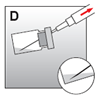
·Aspirer ensuite la totalité de la suspension pour injection dans la seringue (fig. D).
|
|
| |
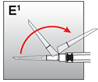
·Enlever l'aiguille de reconstitution. Tourner fermement l'aiguille à injection avec système de sécurité sur la seringue (à fond). Ne saisir que la gaine de couleur.
·Déplacez la gaine de sécurité en arrière de l'aiguille et vers le corps de la seringue (fig. E1). La gaine de sécurité reste dans la position où elle a été mise.
·Retirer la protection de l'aiguille d'injection.
·Puis administrer immédiatement l'entièreté de la seringue.
·Ne pas amorcer l'aiguille avec la suspension (fig. E2).
|
|

|
| |
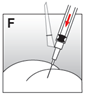
2. Injection
·Injecter la suspension pour injection relativement rapidement et sans interruption par voie intramusculaire (fig. F).
|
|
| |
3. Après usage
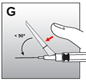
·Activer le système de sécurité de l'aiguille d'injection selon l'une des méthodes suivantes:
·presser d’une main sur la sécurité vers l’avant pour recouvrir l’aiguille et refermer la sécurité (fig. G). Toujours garder l’index ou le pouce derrière la pointe de l’aiguille.
Ou
·Appuyer la sécurité dirigée vers le bas sur une surface plane, p.ex. la table, pour recouvrir l'aiguille et refermer la sécurité (fig. H).
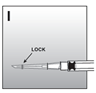
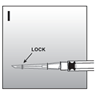
·La sécurité de l'aiguille pour injection est refermée dès que la pointe de l'aiguille est complètement recouverte (fig. I).
S'en assurer par des signes audibles, perceptibles et/ou optiques.
·Jeter les aiguilles dans un conteneur prévu à cet effet.
·A usage unique seulement. Toute suspension non utilisée doit être éliminée.
|
|

Ou
|
|
|
|






























