CompositionPrincipes actifs
Étonogestrel.
Excipients
Sulfate de baryum, stéarate de magnésium, copolymère éthylène-acétate de vinyle pro praeparatione.
Indications/Possibilités d’emploiContraception hormonale.
Posologie/Mode d’emploiAvant l'implantation ou le retrait de l'implant, il faut lire soigneusement et suivre les instructions de la rubrique «Remarques particulières/Remarques concernant la manipulation/Mise en place d'Implanon NXT ou Retrait d'Implanon NXT». L'implantation comme le retrait d'Implanon NXT doivent toujours être effectués par un médecin familiarisé avec la technique d'implantation et de retrait d'Implanon NXT et dans le strict respect des techniques d'asepsie habituelles.
N'essayez pas d'effectuer l'intervention si vous n'êtes pas certain des étapes nécessaires à l'implantation et au retrait en toute sécurité de l'implant.
Important: avant l'utilisation d'Implanon NXT, une grossesse doit être exclue.
Implanon NXT est un contraceptif hormonal d'effet prolongé. L'implant est inséré par voie sous-cutanée à l'aide d'un applicateur. Il faut informer l'utilisatrice que l'implant peut lui être retiré à tout moment si elle le souhaite. Il faut systématiquement retirer Implanon NXT au plus tard au bout de 3 ans, car une efficacité contraceptive suffisante n'est pas prouvée lors d'utilisation prolongée. Chez les femmes de poids corporel important, le remplacement de l'implant devrait toutefois être envisagé avant ce délai (voir «Mises en garde et précautions»).
Si, après le retrait, on remplace Implanon NXT immédiatement par un nouvel implant, la protection contraceptive n'est pas interrompue. Si l'utilisatrice ne souhaite plus employer Implanon NXT, mais n'envisage pas de grossesse, il faut lui recommander une autre méthode de contraception.
Si les recommandations concernant le moment de l'implantation indiquées ci-après sont respectées, aucune mesure contraceptive supplémentaire n'est nécessaire. Si, au contraire, l'implantation a lieu à une date postérieure à ce qui est indiqué dans les recommandations correspondantes (voir ci-dessous), il faut demander à l'utilisatrice d'utiliser un contraceptif barrière supplémentaire durant les 7 premiers jours après insertion de l'implant. Si un rapport sexuel a déjà eu lieu, une grossesse doit être exclue avant l'insertion d'Implanon NXT.
Moment de l'implantation
·Pas d'utilisation antérieure de contraceptifs hormonaux (au cours du mois écoulé): L'implantation d'Implanon NXT devrait être effectuée entre le jour 1 et le jour 5 du cycle naturel de la femme (même si les saignements continuent), le jour 1 étant le premier jour de ses règles.
·Remplacement d'un contraceptif hormonal combiné (contraceptif oral combiné (COC), anneau vaginal ou dispositif transdermique): Implanon NXT devrait être implanté de préférence le lendemain de la prise du dernier comprimé actif du COC précédent ou le jour du retrait de l'anneau vaginal ou du dispositif transdermique, et en tout cas au plus tard le lendemain de la période habituellement sans prise de comprimé, sans anneau ou sans dispositif transdermique ou de la phase sous placebo.
·Remplacement d'une préparation uniquement progestative (pilule progestative, produit injectable, implant) ou d'un dispositif intra-utérin (DIU) libérant une hormone:Pilule progestative: l'implantation d'Implanon NXT peut avoir lieu à n'importe quel jour du mois. L'implant devrait être mis en place dans les 24 heures suivant la prise du dernier comprimé.Contraceptif injectable: l'implant devrait être mis en place à la date qui était prévue pour l'injection suivante.Implant ou DIU: Implanon NXT doit être mis en place le jour du retrait de l'implant ou du DIU utilisé jusque-là.
·Après un avortement survenu pendant le premier trimestre de la grossesse:Implanon NXT devrait être implanté dans les 5 jours. En cas d'implantation plus tardive, une méthode de contraception barrière supplémentaire doit être utilisée durant les 7 premiers jours.
·Après un accouchement ou après un avortement survenu pendant le deuxième trimestre de la grossesse:
·Implanon NXT devrait être implanté 21 à 28 jours après l'accouchement ou après l'avortement survenu pendant le deuxième trimestre de la grossesse. Si l'implantation est effectuée à une date ultérieure, il faut demander à la femme d'utiliser une méthode de contraception barrière supplémentaire pendant les 7 jours suivant l'implantation. S'il y a déjà eu un rapport sexuel, il faut exclure une grossesse avant l'implantation ou bien attendre les premières règles spontanées de la femme pour effectuer l'implantation. Pour les femmes qui allaitent, voir la rubrique «Grossesse, Allaitement».
Instructions posologiques particulières
Patientes présentant des troubles de la fonction hépatique
Implanon NXT ne doit pas être utilisé par les femmes souffrant d'insuffisance hépatique.
Patientes présentant des troubles de la fonction rénale
Implanon NXT n'a pas été étudié chez des femmes souffrant d'insuffisance rénale et il est impossible de formuler des recommandations posologiques.
Enfants et adolescentes
L'efficacité et la sécurité d'Implanon NXT ont été étudiées chez des femmes adultes. Si Implanon NXT est indiqué chez des adolescentes, la posologie recommandée est la même que chez l'adulte.
Patientes âgées
Il n'y a pas d'indication après la ménopause.
Contre-indicationsLes contraceptifs contenant des progestatifs ne doivent pas être utilisés dans les situations suivantes:
·maladies thromboemboliques veineuses ou artérielles aiguës (p.ex. thrombose veineuse profonde, embolie pulmonaire, infarctus du myocarde, AVC);
·présence confirmée ou suspectée de tumeurs sensibles aux hormones sexuelles;
·hémorragies vaginales d'origine indéterminée;
·maladie hépatique grave, présente ou passée, tant que subsistent des paramètres anormaux de la fonction hépatique;
·tumeurs hépatiques bénignes ou malignes, présentes ou passées;
·hypersensibilité à l'un des composants d'Implanon NXT.
Si l'une de ces situations ou maladies survient pour la première fois après l'implantation d'Implanon NXT, il faut immédiatement retirer l'implant.
Mises en garde et précautionsAvant d'utiliser Implanon NXT, il faut s'assurer que la femme n'est pas enceinte.
Avant l'utilisation du premier implant Implanon NXT ou des implants suivants, les antécédents médicaux complets (y compris les antécédents familiaux) et un examen gynécologique et général comportant une mesure de la pression artérielle devraient être pratiqués, en tenant tout particulièrement compte des contre-indications et des précautions. L'utilisatrice devrait être également instruite à lire attentivement la notice et à respecter les conseils qu'elle contient.
Avant l'utilisation, le médecin doit discuter avec l'utilisatrice des avantages et inconvénients d'Implanon NXT comparativement à d'autres méthodes contraceptives.
Trois mois après l'implantation d'Implanon NXT, il faut pratiquer un premier examen de contrôle comprenant une mesure de la pression artérielle et interroger l'utilisatrice sur les effets indésirables ou troubles éventuellement survenus. Pour fixer la fréquence et la nature des examens de contrôle réguliers suivants, le médecin doit tenir compte de la situation individuelle et médicale.
Il faut signaler à l'utilisatrice le fait qu'Implanon NXT ne protège ni contre une infection par le VIH (sida), ni contre les autres maladies sexuellement transmissibles.
Situations dans lesquelles il faut immédiatement retirer Implanon NXT
Il faut immédiatement retirer Implanon NXT quand il existe l'une des contre-indications susmentionnées et dans les situations suivantes:
·survenue d'un ictère, d'une hépatite ou d'un prurit généralisé,
·apparition pour la première fois ou augmentation de la fréquence ou de l'intensité de maux de tête de type migraineux ou de maux de tête inhabituellement intenses,
·signes d'une maladie thromboembolique (y compris infarctus du myocarde ou AVC),
·troubles aigus de la vision, de l'ouïe ou de la parole ou autres déficits sensoriels ou symptômes évoquant une ischémie cérébrale,
·augmentation importante de la pression artérielle,
·immobilisation prolongée (p.ex. après des accidents ou des interventions chirurgicales majeures),
·états dépressifs graves,
·accroissement de crises d'épilepsie,
·croissance objectivée de tumeurs préexistantes, induite par le traitement.
En présence de l'une des situations décrites ci-après, il faut mettre en balance, au cas par cas, le bénéfice de l'emploi d'un contraceptif hormonal et les risques possibles et en discuter avec la femme, avant qu'elle ne prenne sa décision quant à l'utilisation d'Implanon NXT. Il faut lui demander de consulter son médecin si l'un des phénomènes mentionnés ci-après apparaît pour la première fois ou s'aggrave. Le médecin devrait alors déterminer s'il convient ou non de poursuivre l'utilisation d'Implanon NXT.
Événements thromboemboliques
Implanon NXT devrait être utilisé avec prudence chez les femmes qui ont des antécédents de thrombophlébite ou de maladies thromboemboliques. Des études épidémiologiques montrent une augmentation du risque de maladies thromboemboliques veineuses et artérielles (p.ex. thrombose veineuse profonde, embolie pulmonaire, infarctus du myocarde ou accident vasculaire cérébral) en cas d'utilisation de contraceptifs hormonaux combinés (CHC).
Les fumeuses utilisant un CHC présentent un risque accru de thromboembolies artérielles et veineuses. Ce risque augmente avec l'âge et avec la consommation de cigarettes. Les femmes à partir de 35 ans ne doivent donc pas fumer si elles utilisent une contraception hormonale. De même, une obésité (IMC >30 kg/m2) et des antécédents familiaux positifs entraînent un risque accru de complications thromboemboliques.
On ignore la signification clinique de ces résultats d'étude pour l'étonogestrel utilisé seul à titre contraceptif, sans association avec un estrogène. Après la commercialisation, on a rapporté chez des femmes porteuses d'implants à l'étonogestrel des cas sévères de complications thromboemboliques veineuses et artérielles, dont des thromboses veineuses profondes, des embolies pulmonaires (parfois létales), des infarctus du myocarde et des accidents vasculaires cérébraux.
À l'apparition de symptômes éventuels d'une complication thromboembolique, les mesures correspondantes de diagnostic et de traitement doivent être instaurées.
Les premiers signes d'une complication thromboembolique veineuse peuvent être de fortes douleurs ou le gonflement d'une jambe, des douleurs lancinantes inhabituelles et inexpliquées en respirant ou en toussant, un souffle court, des douleurs thoraciques ou une sensation d'oppression thoracique.
Les premiers signes d'une complication thromboembolique artérielle peuvent être l'apparition soudaine de fortes douleurs thoraciques irradiant éventuellement dans le bras (gauche), une soudaine détresse respiratoire, une extrême sensation de faiblesse, une première survenue de migraine ou toute autre survenue inhabituelle de maux de tête sévères et prolongés, un soudain engourdissement ou manque de force au niveau du visage, d'un bras ou d'une jambe (surtout dans une moitié du corps), des troubles moteurs, une perte soudaine, partielle ou totale, de la vision, une diplopie, un langage inarticulé ou une aphasie, des vertiges, une perte de conscience avec ou sans crise de convulsions focales, une nette augmentation de la pression artérielle.
Dans le cas d'une thrombose confirmée, l'implant doit être retiré et une méthode de contraception non hormonale être envisagée à la place. De même, en cas d'immobilisation prolongée, motivée par une opération ou une maladie, il faut retirer l'implant et respecter un délai d'au moins 2 semaines après la mobilisation complète de la patiente avant de réinstaurer une contraception hormonale. Les femmes qui ont des antécédents de maladies thromboemboliques doivent être informées du risque éventuellement accru de récidive de celles-ci.
Pour l'évaluation du rapport bénéfices-risques vasculaires, il faut songer qu'un traitement approprié de maladies préexistantes permet de réduire le risque de thromboses qui leur est associé et qu'une grossesse s'accompagne d'un risque plus élevé que l'utilisation d'Implanon NXT.
Cancers
Le risque de carcinome mammaire augmente avec l'âge. Pendant l'utilisation de contraceptifs hormonaux (combinés) (CHC), le risque de diagnostic d'un carcinome mammaire est légèrement augmenté, mais il diminue continuellement au cours des 10 ans suivant l'arrêt de l'utilisation de ces produits. Ce risque ne dépend pas de la durée d'utilisation, mais de l'âge de l'utilisatrice. Le nombre attendu de cas de carcinome mammaire diagnostiqués pour 10 000 femmes qui utilisent des CHC (jusqu'à 10 ans après l'arrêt de l'utilisation), comparé au nombre de cas chez les femmes qui n'ont jamais utilisé de CHC pendant la même période, a été calculé dans les diverses tranches d'âge. Le tableau ci-dessous indique les résultats:
|
Tranche d'âge
|
Cas attendus chez les utilisatrices de CHC
|
Cas attendus chez les non-utilisatrices
| |
16-19 ans
|
4,5
|
4
| |
20-24 ans
|
17,5
|
16
| |
25-29 ans
|
48,7
|
44
| |
30-34 ans
|
110
|
100
| |
35-39 ans
|
180
|
160
| |
40-44 ans
|
260
|
230
|
Le risque pour les femmes utilisant des produits contenant uniquement un progestatif est probablement comparable au risque pour les utilisatrices de CHC. Les données disponibles concernant les produits contenant uniquement un progestatif sont toutefois insuffisantes pour que l'on puisse fournir des estimations chiffrées à ce propos. Les carcinomes mammaires avaient tendance à être moins évolués au moment du diagnostic chez les femmes qui utilisaient un CHC que chez les femmes qui n'avaient jamais utilisé de CHC. L'augmentation du risque chez les utilisatrices de CHC pourrait s'expliquer par un diagnostic précoce, par des effets biologiques des CHC ou par une combinaison des deux facteurs. Tant qu'un effet biologique ne peut pas être exclu, une analyse du rapport bénéfice/risque individuelle devrait être effectuée chez les femmes qui ont des antécédents de carcinome mammaire ou chez lesquelles un tel carcinome est diagnostiqué pendant l'utilisation d'Implanon NXT.
Après l'utilisation de principes actifs hormonaux tels que celui qui est contenu dans Implanon NXT, on a observé, dans de rares cas, des tumeurs hépatiques bénignes et, plus rarement encore, des tumeurs malignes qui ont, exceptionnellement, provoqué des hémorragies intra-abdominales mettant la vie de la patiente en danger. En conséquence, s'il apparaît de vives douleurs dans le haut de l'abdomen, une augmentation du volume du foie ou des signes d'hémorragie intra-abdominale, la possibilité d'une tumeur du foie devrait être envisagée lors du diagnostic différentiel.
Défaut de localisation de l'implant/rupture de l'implant/rejet de l'implant
Des cas d'expulsion de l'implant ou de migration dans le bras à distance du point d'insertion ont été rapportés. Ils peuvent être liés à une insertion profonde (voir aussi «Remarques particulières», paragraphe Mise en place d'Implanon NXT) ou à une action externe (p.ex. manipulation au niveau de l'implant ou sports de contact). L'implant a migré dans le bras de la patiente dans la plupart des cas rapportés, mais il est parvenu jusqu'à la paroi thoracique dans de rares cas. De rares cas de migration de l'implant dans les vaisseaux sanguins du bras, voire dans l'artère pulmonaire, ont été rapportés depuis la mise sur le marché.
Dans les quelques cas où l'implant a été retrouvé dans l'artère pulmonaire, des douleurs thoraciques et/ou des symptômes respiratoires (tels que toux, dyspnée ou hémoptysies) ont été rapportés; d'autres cas sont cependant restés asymptomatiques.
Si l'implant a migré dans le bras à partir de son point d'insertion, il peut être plus difficile à localiser et son retrait peut nécessiter un geste chirurgical (éventuellement au bloc opératoire; voir aussi «Remarques particulières», paragraphe Retrait d'Implanon NXT). Une localisation intravasculaire de l'implant nécessite une intervention endovasculaire ou chirurgicale pour le retrait.
Si, à un moment quelconque, l'implant n'est plus palpable, il devrait être localisé et il est conseillé de le retirer rapidement. Si l'implant n'est pas retiré, la contraception et le risque d'effets indésirables d'origine progestative peuvent persister plus longtemps que ne le souhaite la patiente.
Des cas d'implants pliés et/ou cassés dans le bras des patientes et dans certains cas, de migration d'un fragment cassé à l'intérieur du bras ont été rapportés. Des actions extérieures (p.ex. une pression ou des coups) sur le bras pourraient représenter un facteur de risque de pliage ou de rupture de l'implant. Selon les données in vitro, une telle détérioration de l'implant peut entraîner une légère augmentation du taux de libération d'étonogestrel, sans toutefois que des répercussions cliniques significatives soient à craindre. Lors du retrait d'un implant cassé, il importe de vérifier que tous les fragments ont été extraits (voir «Remarques particulières», paragraphe Retrait d'Implanon NXT).
Un rejet de l'implant est possible, surtout quand l'implantation n'a pas été effectuée selon les instructions («Remarques particulières», paragraphe Mise en place d'Implanon NXT) ou en raison d'une inflammation locale.
Développement d'un follicule/risque de grossesse extra-utérine
Comme avec tous les contraceptifs hormonaux faiblement dosés, un follicule peut se développer et parfois devenir plus gros que lors d'un cycle normal. En général, ces follicules hypertrophiques disparaissent spontanément. Ils sont souvent asymptomatiques, mais s'accompagnent parfois de légères douleurs abdominales et exigent rarement une intervention chirurgicale.
Le risque de grossesse ectopique est plus élevé avec les produits classiques contenant uniquement un progestatif qu'avec les CHC, phénomène qui a été mis en rapport avec les ovulations fréquentes et le ralentissement du péristaltisme tubaire lors de l'utilisation de progestatifs purs. Même si Implanon NXT inhibe presque totalement l'ovulation, il faut toujours évoquer l'éventualité d'une grossesse ectopique lors du diagnostic différentiel quand une femme se plaint d'une aménorrhée ou de douleurs pelviennes persistantes pendant l'utilisation d'Implanon NXT.
Troubles dépressifs
Les dépressions et humeurs dépressives sont connues comme étant des effets indésirables potentiels lors de l'utilisation d'hormones sexuelles, y compris de contraceptifs hormonaux (voir aussi la rubrique «Effets indésirables»). De tels troubles peuvent survenir peu de temps après le début du traitement. Une dépression peut être grave et représente un facteur de risque de suicide ou de comportement suicidaire. Les utilisatrices de contraceptifs hormonaux doivent donc être informées des symptômes possibles de troubles dépressifs. Il faut impérativement conseiller à l'utilisatrice de s'adresser immédiatement à un médecin si elle remarque des fluctuations d'humeur ou d'autres symptômes de dépression lorsqu'elle utilise un contraceptif. Les utilisatrices ayant des antécédents de dépression sévère doivent être surveillées attentivement. En cas de réapparition d'états dépressifs graves au cours de l'utilisation de Implanon NXT, le traitement doit être interrompu.
Changements du profil de saignements
Pendant l'utilisation d'Implanon NXT, on peut noter des changements du profil de saignements. Une augmentation de la fréquence ou de la durée des saignements est observée chez 1 femme sur 5 environ. D'autres femmes n'ont qu'occasionnellement ou plus du tout de saignements (dans le cadre des études, le taux d'aménorrhée se situait autour de 20%). Le profil individuel de saignements au cours des trois premiers mois de traitement est généralement prédictif de l'évolution de la menstruation par la suite avec Implanon NXT. Le médecin peut améliorer l'acceptabilité de la modification du profil de saignements en informant les patientes, en les conseillant et en leur recommandant d'utiliser un calendrier des saignements. L'évaluation des saignements vaginaux devrait être effectuée sur une base ad hoc et en même temps inclure des examens permettant d'exclure l'éventualité de maladies gynécologiques ou d'une grossesse.
Autres précautions
·Le traitement par des progestatifs peut induire une rétention liquidienne et une prise de poids. Il faut soigneusement surveiller les patientes atteintes de maladies préexistantes qui risqueraient de s'aggraver de ce fait (p.ex. asthme, migraine, troubles de la fonction cardiaque ou rénale, épilepsie).
·Il peut être nécessaire de retirer l'implant s'il apparaît des perturbations aiguës ou chroniques de la fonction hépatique. L'utilisatrice devrait être adressée à un spécialiste.
·L'utilisation d'Implanon NXT devrait être interrompue si la pression artérielle est en permanence augmentée ou en cas d'hypertension importante, réfractaire au traitement antihypertenseur.
·Quand des femmes diabétiques commencent à utiliser Implanon NXT, elles devraient être surveillées attentivement, car il semble qu'Implanon NXT influence la tolérance au glucose.
·Certains progestatifs peuvent élever le taux de LDL et rendre plus difficile le contrôle d'une hyperlipidémie. Les femmes présentant une hyperlipidémie préexistante devraient donc être surveillées attentivement.
·Les maladies suivantes ont été observées aussi bien pendant la grossesse que pendant l'utilisation de stéroïdes sexuels, sans que la relation avec l'utilisation de progestatifs soit formellement établie: ictère et/ou prurit associé à une cholestase, cholélithiase; porphyrie; lupus érythémateux disséminé; syndrome hémolytique et urémique; chorée de Sydenham; herpès gestationnel; perte de l'audition due à une otospongiose; induction ou aggravation d'un angio-œdème.
·On peut parfois observer un chloasma, surtout chez les femmes qui ont des antécédents de chloasma pendant la grossesse. Pendant l'utilisation d'Implanon NXT, les femmes sujettes au chloasma devraient éviter de s'exposer à la lumière du soleil et à tout autre rayonnement ultraviolet.
·L'effet contraceptif d'Implanon NXT dépend de la concentration plasmatique d'étonogestrel, laquelle est inversement proportionnelle au poids corporel et diminue au fil du temps. L'expérience clinique acquise chez des femmes de poids corporel important (plus de 80 kilos) est limitée. Il n'est pas exclu que la fiabilité contraceptive soit diminuée chez ces femmes pendant la troisième année d'utilisation.
InteractionsNote: Les informations professionnelles des médicaments utilisés simultanément devraient être consultées afin d'exclure des interactions éventuelles.
Effet d'autres médicaments sur la pharmacocinétique d'Implanon NXT
La littérature décrit les interactions suivantes (essentiellement avec des contraceptifs hormonaux combinés mais aussi, très rarement, avec des contraceptifs purement progestatifs):
Inducteurs enzymatiques
Les interactions entre les contraceptifs hormonaux et les médicaments induisant les enzymes microsomales (notamment les enzymes du cytochrome P450) et pouvant donc conduire à une augmentation de la clairance des hormones sexuelles, peuvent entraîner une diminution de l'effet contraceptif d'Implanon NXT ainsi que des troubles hémorragiques. Ceci vaut par exemple pour les barbituriques, le bosentan, la carbamazépine, le felbamate, le modafinil, l'oxcarbazépine, la phénytoïne, la primidone, la rifabutine, la rifampicine, le topiramate ainsi que pour les médicaments contenant du millepertuis (Hypericum perforatum).
Une induction enzymatique peut se produire déjà après quelques jours de traitement. L'induction enzymatique maximale est en général observée après 2 à 3 semaines et peut persister pendant au moins 4 semaines ou plus après l'arrêt de ces médicaments.
Les femmes traitées pendant une courte durée par un de ces médicaments, devraient être averties que l'efficacité d'Implanon NXT peut être réduite. S'il est décidé de poursuivre la contraception avec Implanon NXT, l'utilisatrice devrait être invitée à utiliser temporairement une méthode de contraception non hormonale supplémentaire. La méthode barrière devrait être utilisée pendant l'utilisation concomitante des médicaments et encore pendant 28 jours après l'arrêt du traitement.
En cas de traitement de longue durée par des médicaments qui entraînent une induction enzymatique hépatique, des méthodes contraceptives alternatives (non hormonales) devraient être utilisées.
On sait en outre que divers inhibiteurs des protéases du VIH/VHC (p.ex. nelfinavir, bocéprévir, télaprévir) et de la transcriptase inverse non nucléosidique (p.ex. éfavirenz, névirapine) ainsi que leurs combinaisons peuvent entraîner une baisse ou une élévation des concentrations plasmatiques des progestatifs. Ces changements peuvent avoir un effet clinique dans quelques cas. Par exemple, une étude publiée sur le traitement par de l'éfavirenz de patientes positives au VIH comparées à des femmes sans traitement antirétroviral a mis en évidence une Cmax de l'étonogestrel plus basse de 54% et une AUC diminuée de 63%.
Les inhibiteurs de protéase tels que le ritonavir ou le nelfinavir (y compris leurs combinaisons) sont des inhibiteurs puissants du CYP3A4 notoires, mais ils peuvent avoir un effet inducteur enzymatique s'ils sont co-administrés avec des hormones stéroïdiennes et peuvent ainsi réduire le taux plasmatique de progestatifs.
Inhibiteurs enzymatiques
Les inhibiteurs puissants et modérés du CYP3A comme les antifongiques azolés (itraconazole, voriconazole, posaconazole, fluconazole), les macrolides (clarithromycine, érythromycine), le diltiazem, le vérapamil et le jus de pamplemousse peuvent augmenter les taux plasmatiques des progestatifs comme l'étonogestrel et entraîner des effets indésirables plus nombreux.
Effet des contraceptifs hormonaux sur la pharmacocinétique d'autres médicaments
Les contraceptifs hormonaux peuvent, par différents mécanismes d'interaction, influer également sur la pharmacocinétique de certains autres médicaments. Ils peuvent inhiber les enzymes hépatiques microsomaux ou induire la conjugaison hépatique, en particulier la glucuroconjugaison. Les concentrations plasmatiques et tissulaires d'autres médicaments peuvent par conséquent être soit augmentées (p.ex. la ciclosporine) soit diminuées (p.ex. la lamotrigine, voir ci-dessous). Par ailleurs, l'effet pharmacologique des groupes médicamenteux suivants peut également être influencé: analgésiques, antidépresseurs, antidiabétiques, antimalariques, certaines benzodiazépines, certains bêtabloquants, corticostéroïdes, anticoagulants oraux et théophylline. C'est pourquoi, en cas d'utilisation de tels médicaments, il faut étroitement surveiller la patiente. Cependant, les modifications des taux plasmatiques résultant de ces interactions ne sont pas toujours cliniquement pertinentes.
Une étude d'interactions avec la lamotrigine, un anti-épileptique, et un contraceptif oral combiné (30 μg d'éthinylestradiol/150 μg de lévonorgestrel) a mis en évidence une augmentation cliniquement significative de la clairance de la lamotrigine avec une diminution significative des taux plasmatiques de lamotrigine lors de l'administration simultanée de ces médicaments. Une telle diminution des concentrations plasmatiques peut se manifester par un moins bon contrôle des crises épileptiques. On ne sait pas dans quelle mesure ces résultats peuvent être appliqués à une préparation uniquement progestative sous-cutanée comme Implanon NXT.
Grossesse, allaitementGrossesse
Ce médicament est contre-indiqué chez les femmes enceintes. Avant de commencer à l'utiliser, il faut donc s'assurer que la femme n'est pas enceinte. Si une grossesse débute ou est suspectée, il faut immédiatement retirer Implanon NXT. Des expérimentations animales ont montré que les doses très fortes de produits contenant des progestatifs exerçaient un effet virilisant sur les fœtus de sexe féminin (voir «Données précliniques»). Des études épidémiologiques de grande ampleur n'ont indiqué ni augmentation du risque d'anomalie à la naissance chez les enfants dont la mère avait utilisé des CHC avant la grossesse, ni effets tératogènes dans les cas où des femmes, ignorant qu'elles étaient enceintes, avaient utilisé des contraceptifs purement progestatifs. Bien que cela vaille sans doute pour tous les CHC, on ignore s'il en va de même pour Implanon NXT.
Les données de pharmacovigilance concernant divers contraceptifs combinés contenant de l'étonogestrel ou du désogestrel (l'étonogestrel est un métabolite du désogestrel) n'ont pas non plus montré d'augmentation du risque.
Allaitement
Comme d'autres produits contraceptifs contenant uniquement un progestatif, Implanon NXT n'a pas d'effet défavorable sur la quantité et la qualité (protéines, lactose ou concentrations de lipides) du lait maternel. Toutefois, de petites quantités d'étonogestrel sont sécrétées dans ce dernier. Sur la base d'une absorption moyenne de lait de 150 ml/kg par jour, la quantité moyenne d'étonogestrel absorbée par le nouveau-né – après un mois de libération d'étonogestrel – est d'environ 27 ng/kg par jour, ce qui représente à peu près 0,2% de la dose quotidienne absolue absorbée par la mère (2,2% quand le calcul est effectué par kilo de poids). Le taux d'étonogestrel dans le lait maternel diminue avec le temps. Il existe des données recueillies à long terme auprès de 38 enfants dont la mère avait reçu un implant entre la quatrième et la huitième semaine après la naissance. Ces enfants ont été allaités pendant une durée moyenne de 14 mois et suivis pendant 36 mois. Leur croissance et leur développement physique et psychique ont été observés et comparés à ceux de nourrissons dont la mère avait utilisé un DIU (n=33). Cette étude n'a pas montré de différence entre les deux groupes. Néanmoins, le développement et la croissance de l'enfant devraient être soigneusement surveillés. À la lumière des données disponibles, Implanon NXT peut être utilisé pendant l'allaitement, mais il faut respecter un délai d'au moins 4 semaines entre l'accouchement et l'implantation.
Effet sur l’aptitude à la conduite et l’utilisation de machinesÉtant donné le profil pharmacodynamique d'Implanon NXT, on suppose que ce produit n'a aucune influence ou une influence négligeable sur l'aptitude à la conduite ou l'utilisation de machines.
Effets indésirablesLes effets indésirables les plus graves en rapport avec la prise de contraceptives hormonaux sont décrits dans la rubrique «Mises en garde et précautions».
Les effets indésirables les plus fréquents observés lors d'études cliniques avec Implanon NXT ont été les suivants: maux de tête, acné, vaginite, prise de poids, ainsi que sensation de tension et douleurs mammaires. Dans les études cliniques, la raison la plus fréquente d'arrêt du traitement était les modifications des saignements (environ 11%).
L'implantation ou le retrait de l'implant peuvent causer des hématomes, un prurit, une légère irritation locale ou des douleurs. Des paresthésies peuvent survenir au point d'implantation. Une cicatrice, un abcès ou une fibrose peuvent aussi se former.
Des réactions vasovagales (par ex. hypotension, vertiges ou syncopes) liées à l'insertion ou au retrait de l'implant ont été rapportées.
Des cas de migration ou d'expulsion de l'implant ont été rapportés (voir «Mises en garde et précautions»).
Les effets indésirables observés pendant les études cliniques et/ou au cours de la surveillance post-commercialisation durant l'utilisation d'Implanon NXT sont énumérés ci-dessous par classe de système d'organes et fréquence. Les catégories de fréquence sont définies comme suit: très fréquents (≥1/10); fréquents (≥1/100, <1/10); occasionnels (≥1/1000, <1/100); rares (≥10 000, <1/1000); fréquence inconnue (indications principalement basées sur des signalements spontanés après la mise sur le marché, estimation exacte de la fréquence impossible).
Infections et infestations
Occasionnels: Pharyngite, rhinite, infections urinaires.
Affections du système immunitaire
Occasionnels: Réactions d'hypersensibilité.
Fréquence inconnue: Réactions anaphylactiques, angio-œdème (y compris aggravation d'un angio-œdème héréditaire).
Troubles du métabolisme et de la nutrition
Très fréquents: Prise de poids (14%).
Fréquents: Modification de l'appétit, perte de poids.
Affections psychiatriques
Fréquents: Fluctuations de l'humeur, diminution de la libido, humeur dépressive, nervosité.
Occasionnels: Anxiété, insomnie, somnolence.
Affections du système nerveux
Très fréquents: Maux de tête (25%).
Fréquents: Vertiges.
Occasionnels: Migraine.
Fréquence inconnue: Hypertension intracrânienne idiopathique.
Affections vasculaires
Fréquents: Bouffées de chaleur.
Rares: Augmentation de la pression artérielle cliniquement significative.
Affections gastro-intestinales
Fréquents: Douleurs abdominales, nausées, flatulences.
Occasionnels: Vomissements, constipation, diarrhée.
Affection de la peau et du tissu sous-cutané
Très fréquents: Acné (14%)
Fréquents: Alopécie.
Occasionnels: Hypertrichose, éruption cutanée, prurit.
Fréquence inconnue: Séborrhée, urticaire.
Affections musculosquelettiques et du tissu conjonctif
Occasionnels: Douleurs dorsales, arthralgies, myalgies et douleurs musculosquelettiques.
Affections du rein et des voies urinaires
Occasionnels: Dysurie.
Affections des organes de reproduction et du sein
Très fréquents: Changements du profil de saignements utérins, vaginite (15%), douleurs et sensibilité mammaires (13%).
Fréquents: Dysménorrhée, aménorrhée, kystes de l'ovaire.
Occasionnels: Leucorrhée, gêne vulvovaginale, galactorrhée, augmentation du volume mammaire, prurit génital.
Fréquence inconnue: Grossesse ectopique.
Troubles généraux et anomalies au site d'administration
Fréquents: Douleurs et autres réactions au site d'implantation (p.ex. érythème, gonflement, prurit, légère irritation, hématome; voir «Propriétés/Effets»), fatigue, symptômes de type grippal, douleurs.
Occasionnels: Fièvre, œdèmes.
On a rapporté par ailleurs les effets indésirables suivants en rapport avec l'utilisation d'autres contraceptifs hormonaux (voir «Mises en garde et précautions»): maladies thromboemboliques veineuses et artérielles, hypertension artérielle, tumeurs hormono-dépendantes (p.ex. tumeurs du foie ou cancer du sein) et chloasma.
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageIl n'y a pas d'informations concernant les effets d'un surdosage en étonogestrel, mais, en raison de la forme pharmaceutique, un surdosage est peu probable.
D'une manière générale, on n'a pas encore signalé d'effets néfastes graves en cas de surdosage en contraceptifs hormonaux.
Avant de poser un nouvel implant, il faut toujours retirer l'ancien.
Propriétés/EffetsCode ATC
G03AC08
Mécanisme d'action
Implanon NXT est un implant contenant de l'étonogestrel destiné à une utilisation sous-cutanée. L'étonogestrel (= 3-cétodésogestrel) est le métabolite biologiquement actif du désogestrel, un progestatif fréquemment utilisé dans les contraceptifs oraux. Sur le plan structurel, il s'agit d'un dérivé de la 19-nortestostérone doté d'une haute affinité de liaison pour les récepteurs des progestatifs des organes cibles.
À la différence des contraceptifs purement progestatifs classiques, l'étonogestrel exerce son effet contraceptif essentiellement en inhibant l'ovulation sans bloquer totalement l'activité ovarienne. On n'a jamais observé d'ovulations pendant les deux premières années d'utilisation; pendant la troisième année, des ovulations ont été observées chez 4,3% des utilisatrices. L'étonogestrel provoque non seulement une inhibition de l'ovulation, mais aussi une diminution de l'épaisseur de l'endomètre et une augmentation de la viscosité de la glaire cervicale, ce qui empêche le passage des spermatozoïdes.
Pharmacodynamique
Aucune information.
Efficacité clinique
Dans les études cliniques réalisées auprès de femmes âgées de 18 à 40 ans avec une exposition de 36 555 cycles au total, aucune grossesse n'a été observée. En revanche, il existe des rapports de grossesses non désirées dans le cadre de la surveillance post-commercialisation. Bien qu'il n'y ait pas eu de comparaison directe, il semble que l'effet contraceptif d'Implanon NXT soit au moins comparable à celui des contraceptifs oraux combinés.
Cette grande fiabilité contraceptive tient entre autres au fait que l'effet contraceptif d'Implanon NXT ne dépend pas de l'utilisatrice.
L'effet contraceptif de l'étonogestrel est réversible, ce qui se traduit par une normalisation rapide du cycle menstruel (généralement en l'espace d'un mois) après le retrait de l'implant.
Sécurité clinique
Lors d'une étude clinique dans laquelle les médecins investigateurs devaient évaluer le site d'implantation après la mise en place d'Implanon NXT, des réactions au site d'implantation ont été décrites chez 8,6% des femmes. Parmi ces réactions, la plus fréquente était l'érythème apparaissant sur le site d'implantation pendant ou peu de temps après l'insertion chez 3,3% des femmes. Des hématomes (3,0%), des ecchymoses (2,0%), des douleurs (1,0%) et des gonflements (0,7%) ont également été rapportés.
L'effet de l'étonogestrel sur la densité osseuse (n=44) a été comparé à celui d'un DIU non hormonal (n=29) pendant deux ans.
Aucun effet indésirable sur la densité osseuse n'a été observé.
On n'a pas constaté d'effets cliniquement notables sur le métabolisme lipidique.
Les contraceptifs contenant des progestatifs peuvent avoir un effet néfaste sur la résistance à l'insuline et sur la tolérance au glucose (voir «Mises en garde et précautions»).
Les études cliniques ont par ailleurs montré que les symptômes de dysménorrhée étaient souvent atténués chez les femmes utilisant Implanon NXT.
PharmacocinétiqueAbsorption
Après l'insertion de l'implant, l'étonogestrel est rapidement absorbé. Des concentrations plasmatiques inhibant l'ovulation sont atteintes en l'espace d'un jour. La biodisponibilité absolue de l'étonogestrel est d'environ 95%. Les concentrations plasmatiques maximales (qui sont comprises entre 472 et 1270 pg/ml) sont atteintes en l'espace de 1 à 13 jours.
La libération du principe actif à partir de l'implant diminue au fil du temps. Pendant les semaines 5 et 6, elle est d'environ 60-70 µg d'étonogestrel par jour; elle diminue ensuite à environ 35-45 µg à la fin de la première année, puis à environ 30-40 µg à la fin de la deuxième année et enfin à environ 25-30 µg d'étonogestrel par jour à la fin de la troisième année.
C'est pourquoi les concentrations plasmatiques diminuent rapidement pendant les premiers mois. À la fin de la première année, la concentration moyenne est d'environ 200 pg/ml (150-261 pg/ml); elle diminue lentement à 156 pg/ml (111-202 pg/ml) à la fin de la troisième année. Les concentrations plasmatiques d'étonogestrel dépendent du poids. La variabilité observée peut donc être imputée, au moins en partie, à des différences de poids corporel.
Distribution
L'étonogestrel est lié aux protéines plasmatiques à hauteur de 95,5-99%, cette liaison se faisant essentiellement à l'albumine mais aussi, dans une moindre mesure, à la SHBG. Le volume de distribution est d'environ 220 l. Chez les femmes qui allaitent, le rapport concentration d'étonogestrel dans le lait/concentration sérique était de 0,44-0,50 (voir «Grossesse, Allaitement»).
Métabolisme
L'étonogestrel est hydroxylé par le système des enzymes microsomiales hépatiques, puis réduit et conjugué en sulfates et glucuronides. L'hydroxylation est catalysée par l'isoenzyme CYP3A4.
Élimination
Après l'administration intraveineuse d'étonogestrel, la demi-vie d'élimination est en moyenne d'environ 25 heures. La clairance plasmatique est d'environ 7,5 l/heure. Ces deux paramètres restent constants pendant les 3 ans d'utilisation d'Implanon NXT.
L'excrétion de l'étonogestrel et de ses métabolites, sous forme de stéroïdes libres ou de conjugués, se fait dans les urines et dans les selles (dans la proportion de 1,5:1).
Cinétique pour certains groupes de patientes
Il n'existe pas de données concernant la pharmacocinétique chez les femmes souffrant d'insuffisance hépatique ou rénale.
Données précliniquesLes études précliniques menées avec l'étonogestrel sur la toxicité en administration répétée, la génotoxicité et le potentiel cancérogène n'ont pas révélé clairement de risque particulier pour l'être humain. Dans les expérimentations animales, des substances de type progestatif ont eu un effet embryolétal et, à fortes doses, un effet virilisant sur les fœtus femelles. Les études visant à évaluer la toxicité de l'étonogestrel sur la reproduction chez le rat et le lapin n'ont montré aucun signe d'effet tératogène.
Remarques particulièresInfluence sur les méthodes de diagnostic
Des rapports concernant des CHC ont montré que les stéroïdes contraceptifs pouvaient modifier les résultats de certains examens de laboratoire, notamment: paramètres biochimiques de la fonction hépatique, thyroïdienne, surrénalienne et rénale, taux plasmatiques de protéines (de transport) (par exemple globuline fixant les corticoïdes) et lipides/fractions des lipoprotéines, paramètres du métabolisme glucidique et paramètres de la coagulation et de la fibrinolyse. En général, ces modifications restent comprises dans la fourchette de la normale. On ignore si les produits contenant uniquement un progestatif induisent aussi ces modifications.
Imagerie par résonance magnétique (IRM)
Implanon NXT est sans danger pour l'IRM.
Stabilité
Le médicament ne doit pas être implanté au-delà de la date figurant après la mention «EXP» sur l'emballage.
Remarques particulières concernant le stockage
Conserver à 2-30 °C dans l'emballage original.
Conserver hors de portée des enfants.
Remarques concernant la manipulation
L'implantation comme le retrait ou le remplacement d'Implanon NXT doivent être effectués uniquement par un médecin familiarisé avec ces techniques. L'intervention doit avoir lieu dans des conditions d'asepsie et au moyen de l'applicateur fourni. Celui-ci contient l'implant dans une aiguille.
Les médecins qui n'ont encore jamais implanté Implanon NXT doivent d'abord suivre une formation organisée par le distributeur. Les médecins qui n'ont que peu d'expérience de l'implantation sous-cutanée doivent apprendre la technique nécessaire sous la direction d'un confrère expérimenté.
Le succès de la mise en place et du retrait d'Implanon NXT repose sur une insertion sous-cutanée de l'implant, effectuée correctement et avec précaution, conformément aux instructions figurant ci-dessous.
En cas de question ou de doute ainsi que de difficultés lors de l'implantation, de la localisation ou du retrait de l'implant, veuillez-vous adresser à la filiale locale du titulaire de l'autorisation. Ceci s'applique en particulier si vous n'êtes pas (encore) familiarisé avec la technique.
On a signalé quelques cas dans lesquels Implanon NXT n'avait pas été implanté au moment opportun (le bon jour), n'avait pas été correctement implanté ou ne l'avait pas été du tout, ce qui a provoqué, entre autres, des grossesses non désirées. On peut minimiser le risque de tels incidents en respectant strictement les instructions ci-dessous de Mise en place d'Implanon NXT ainsi que les informations sous «Posologie/Mode d'emploi», Moment de l'implantation. Immédiatement après l'implantation, aussi bien le/la médecin que l'utilisatrice devraient vérifier la localisation correcte de l'implant par palpation. Si l'implant n'est pas palpable ou s'il n'est pas sûr qu'il ait été inséré, suivre les instructions données ci-dessous au point Si l'implant n'est pas palpable après l'insertion.
Mise en place d'Implanon NXT
Pour garantir que l'implant est inséré directement sous la peau, le/la médecin devrait être positionné(e) de manière à voir l'avancement de l'aiguille en observant l'applicateur par le côté et non par le dessus du bras. Par le côté, le point d'insertion et le mouvement de l'aiguille directement sous la peau sont clairement visibles.
L'implant devrait être inséré en sous-cutané directement sous la peau au niveau de la face interne du bras non dominant. Un implant inséré plus profondément que le plan dermique (appelé «insertion profonde» ci-après) peut ne pas être palpable et sa localisation et/ou son retrait peuvent être difficiles (voir «Mises en garde et précautions»).
Si l'implant a été placé profondément, des vaisseaux ou nerfs de la patiente peuvent être lésés. Des insertions profondes ou incorrectes ont été associées à des paresthésies (dues à des lésions nerveuses) et à des migrations de l'implant (lors d'une mise en place dans un fascia ou un muscle). Dans de rares cas, l'implant a été inséré dans un vaisseau.
|
|
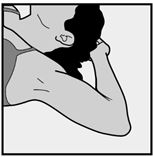
Priez l'utilisatrice de s'allonger sur le dos, de plier son bras non dominant au niveau du coude et de tourner celui-ci vers l'extérieur, de façon à ce que sa main se trouve sous sa tête (ou aussi près que possible) (Fig. 1).
|
Fig. 1
|
| |
|

|
Déterminez le site d'insertion. Il doit se situer sur la face interne du haut du bras non dominant, au niveau du triceps, environ 8 à 10 cm au-dessus de l'épicondyle médial de l'humérus et 3 à 5 cm derrière (resp. sous) le sillon entre le biceps et le triceps (Fig. 2a, 2b et 2c). Le choix de cette localisation permet d'éviter les gros vaisseaux et nerfs qui se situent à l'intérieur et autour du sillon. S'il n'est pas possible d'insérer l'implant à cet endroit (p.ex. chez les femmes ayant des bras fins), il devrait être implanté aussi loin que possible derrière le sillon.
| |
|
Marquez deux points à l'aide d'un marqueur chirurgical: d'abord le point d'insertion et ensuite un deuxième point proximal à 5 cm du premier (en direction de l'épaule) (Fig. 2a et b). La deuxième marque (dite «marque repère») indiquera par la suite la direction d'insertion.
|
Fig. 2a
|
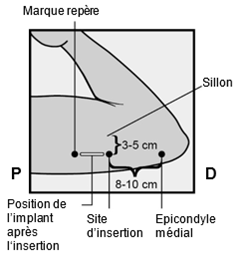
P, proximal (en direction de l'épaule);
D, distal (en direction du coude)
| |
|
|
Fig. 2b
|
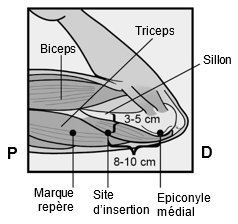
| |
|
|
Fig. 2c
|
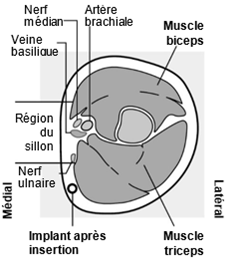
Coupe transversale du haut du bras gauche,
vue du coude
Médial (face interne du bras)
Latéral (face externe du bras)
| |
|
Une fois que vous avez marqué le bras, assurez-vous encore une fois que le site se trouve au bon endroit sur la face interne du bras.
Nettoyez la peau du site d'insertion jusqu'à la marque repère avec une solution antiseptique.
Anesthésiez la zone d'insertion (par exemple avec un spray anesthésiant ou avec 2 ml d'une solution de lidocaïne à 1% directement sous la peau, le long du canal d'implantation prévu).
Retirez l'applicateur stérile – qui contient l'implant dans une aiguille – de son emballage thermoformé. Avant l'utilisation, effectuer un contrôle visuel pour vérifier que l'emballage n'est pas endommagé (par ex. déchiré, percé, etc.). Si l'emballage présente des dommages visibles susceptibles de compromettre la stérilité, l'applicateur ne doit pas être utilisé.
| |
|
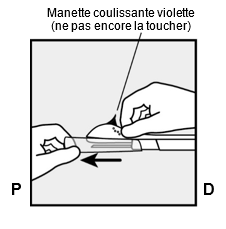
Tenez l'applicateur au-dessus de l'aiguille, au niveau de la zone à surface structurée, et retirez le capuchon protecteur transparent de l'aiguille en le tirant horizontalement dans le sens de la flèche (Fig. 3). Si le capuchon ne peut pas être retiré aisément, l'applicateur ne devrait pas être utilisé. Vous devriez voir l'implant (de couleur blanche) en regardant dans la pointe de l'aiguille. Ne touchez en aucun cas la manette coulissante violette avant d'avoir entièrement placé l'aiguille en position sous-cutanée: cela provoquerait une rétraction de l'aiguille et une libération prématurée de l'implant.
Si la manette coulissante violette est libérée prématurément, recommencez la procédure d'insertion avec un nouvel applicateur.
|
Fig. 3
|
| |
|
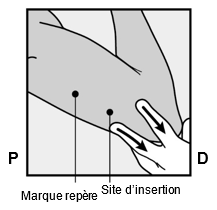
De votre main libre, tendez la peau autour du site d'insertion en direction du coude (Fig. 4).
L'implant devrait être inséré en sous-cutané directement sous la peau (voir «Mises en garde et précautions»). Pour garantir que l'implant est inséré directement sous la peau, vous devriez vous positionner de manière à voir l'avancement de l'aiguille en observant l'applicateur par le côté et non par le dessus du bras (voir Fig. 6).
|
Fig. 4
|
| |
|
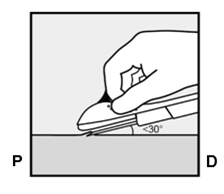
Avec la pointe de l'aiguille, transpercez la peau selon un angle aigu de moins de 30° (Fig. 5a).
|
Fig. 5a
|
| |
|

|
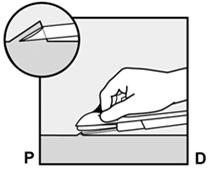
Introduisez l'aiguille jusqu'à ce que le biseau (ouverture biseautée de la pointe) se trouve juste sous la peau (et pas plus loin) (Fig. 5b). Si vous avez introduit l'aiguille au-delà du biseau, retirez-la à nouveau jusqu'à ce que seul le biseau soit encore sous la peau.
|
Fig. 5b
|
| |
|
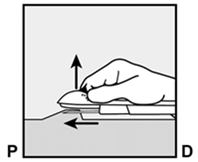
Amenez l'applicateur en position presque horizontale. Pour faciliter le positionnement sous-cutané, soulevez la peau avec la pointe de l'aiguille pendant que vous poussez l'aiguille sur toute sa longueur (Fig. 6). Vous sentirez éventuellement une légère résistance, mais vous ne devez pas exercer trop de force. Si l'aiguille n'a pas été introduite sur toute sa longueur, l'implant ne sera pas correctement placé.
Si la pointe de l'aiguille dépasse de la peau avant l'insertion complète de l'aiguille, l'aiguille devrait être retirée et remise en position sous-cutanée avant de pouvoir achever l'insertion.
|
Fig. 6
|
| |
|
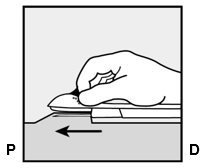
Maintenez l'applicateur dans cette position avec son aiguille entièrement insérée (Fig. 7). Si nécessaire, vous pouvez stabiliser l'applicateur avec votre main libre.
|
Fig. 7
|
| |
|
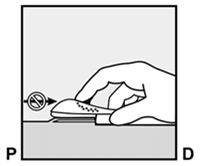
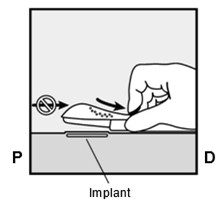
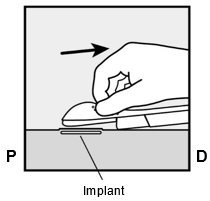
Déverrouillez maintenant la manette coulissante violette en la pressant légèrement vers le bas (Fig. 8a). Faites glisser la partie coulissante en arrière jusqu'à la butée sans toutefois bouger l'applicateur (
|

, Fig. 8b). L'implant est à présent dans sa position d'insertion sous-cutanée, tandis que l'aiguille est verrouillée à l'intérieur de l'applicateur. L'applicateur peut alors être retiré (Fig. 8c).
|
Fig. 8a
|
| |
|
|
Fig. 8b
|
| |
|
|
Fig. 8c
|
| |
|
Si l'applicateur n'est pas maintenu dans la même position lors de cette étape ou si la manette coulissante violette n'est pas entièrement tirée en arrière jusqu'à la butée, l'implant ne sera pas inséré correctement.
Si l'implant dépasse du site d'insertion, retirez l'implant et effectuez une nouvelle intervention au même site d'insertion avec un nouvel applicateur. Ne repoussez en aucun cas un implant éventuellement saillant dans l'incision.
| |
|
Appliquez un petit pansement adhésif sur le site d'insertion.
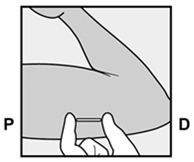
Contrôlez toujours immédiatement par palpation la présence de l'implant dans le bras de l'utilisatrice. En palpant les deux extrémités de l'implant, espacées de 4 cm, vous devriez être en mesure de confirmer la présence du bâtonnet (Fig. 9). Voir aussi Si l'implant n'est pas palpable après l'insertion.
|
Fig. 9
|
| |
|
Priez l'utilisatrice de palper l'implant.
Posez un bandage compressif afin de prévenir la formation d'un hématome. L'utilisatrice pourra retirer le bandage compressif au bout de 24 h et le petit pansement adhésif au bout de 3 à 5 jours.
L'emballage d'Implanon NXT contient une carte d'utilisatrice indiquant le numéro du lot. Notez sur cette carte la date et la localisation (bras droit ou gauche) d'insertion d'Implanon NXT ainsi que la date prévue (au plus tard) pour le retrait de l'implant. Remettez la carte à l'utilisatrice pour qu'elle la conserve. Les étiquettes autocollantes également contenues dans l'emballage facilitent la documentation du numéro de lot dans le dossier de la patiente.
L'applicateur est destiné à un usage unique et doit être éliminé ensuite correctement en accord avec les réglementations applicables.
| |
|
Si l'implant n'est pas palpable après l'insertion:
Si l'implant n'est pas palpable ou si vous avez des doutes quant à sa présence, il est possible qu'il n'ait pas été inséré ou qu'il l'ait été (trop) profondément:
·Contrôlez l'applicateur. L'aiguille doit être entièrement rétractée et seule la pointe violette de l'obturateur doit être visible.
·Utilisez d'autres méthodes pour confirmer la présence de l'implant. Les méthodes appropriées pour la localisation englobent l'échographie avec traducteur linéaire à haute fréquence (10 MHz ou supérieure), la radiographie bidimensionnelle, la tomodensitométrie (TDM) et l'imagerie par résonance magnétique (IRM). Si les méthodes d'imagerie échouent, il est recommandé de vérifier le taux sanguin d'étonogestrel chez la patiente afin de vérifier la présence de l'implant. Vous pouvez demander plus de détails à la filiale locale du titulaire de l'autorisation.
·Jusqu'à ce que la présence de l'implant soit confirmée, il est nécessaire d'utiliser une méthode de contraception non hormonale.
·Les implants implantés trop profondément devraient être localisés et retirés aussi rapidement que possible afin d'éviter une migration (voir «Mises en garde et précautions»).
|
Retrait d'Implanon NXT
Le retrait de l'implant devrait être effectué dans des conditions d'asepsie par un médecin familiarisé avec ces techniques. Une petite incision dans la peau est nécessaire pour retirer l'implant.
Avant de retirer l'implant, il convient de vérifier sa localisation exacte par palpation. Si l'implant n'est pas palpable, vérifiez à l'aide de la carte d'utilisatrice ou du dossier de la patiente dans quel bras se trouve l'implant. Si l'implant n'est pas palpable, cela signifie probablement qu'il est inséré plus profondément ou qu'il a migré. Si l'implant a migré vers l'intérieur du bras, il peut être difficile de le localiser et son retrait peut nécessiter une petite intervention chirurgicale avec une incision plus étendue, voire une opération au bloc opératoire (voir aussi ci-dessous Localisation et retrait d'un implant non palpable).
Tenez compte du fait qu'il peut se trouver à proximité de vaisseaux et de nerfs. Le retrait d'un implant non palpable devrait par conséquent être effectué exclusivement par un(e) médecin familiarisé(e) avec la localisation et le retrait d'implants insérés profondément ainsi qu'avec l'anatomie du bras. Si l'implant ne peut pas être palpé: voir Localisation et retrait d'un implant non palpable.
Retrait d'un implant palpable
|
|

|
La patiente doit être allongée sur le dos. Son bras devrait être plié au niveau du coude et sa main positionnée sous sa tête (ou aussi près que possible) (Fig. 1).
Localisez l'implant par palpation. Pressez l'extrémité de l'implant la plus proche de l'épaule (Fig. 10) vers le bas afin de le stabiliser; un renflement indiquant la pointe de l'implant la plus proche du coude devrait apparaître. Si la pointe ne se soulève pas, le retrait de l'implant peut s'avérer plus difficile et devrait être effectué exclusivement par un(e) médecin(e) familier(ère) du retrait d'implants insérés plus profondément.
Marquez l'extrémité distale (à savoir la plus proche du coude), p.ex. avec un marqueur chirurgical.
Nettoyez le site avec une solution antiseptique.
|
Fig. 10
|
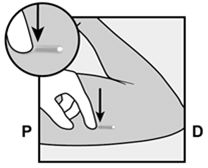
P, proximal (en direction de l'épaule);
D, distal (en direction du coude)
| |
|
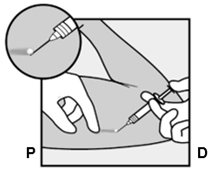
Effectuez une anesthésie locale, p.ex. avec 0,5 à 1 ml de solution de lidocaïne à 1%, au site prévu pour l'incision (Fig. 11). L'anesthésique doit être injecté directement sous l'implant pour que celui-ci reste le plus près possible de la surface de la peau. Une injection de l'anesthésique local au-dessus de l'implant peut compliquer le retrait.
|
Fig. 11
|
| |
|
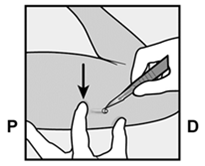
Immobilisez l'implant pendant l'intervention en poussant son extrémité la plus proche de l'épaule vers le bas (Fig. 12). Pratiquez une incision longitudinale de 2 mm en direction du coude, parallèlement à l'implant, en partant de la pointe de l'implant la plus proche du coude. Veillez à ne pas inciser la pointe de l'implant.
|
Fig. 12
|
| |
|
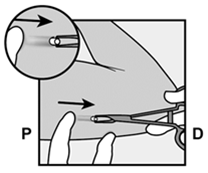
La pointe de l'implant doit maintenant dépasser de l'incision. Si ça n'est pas le cas, poussez doucement l'implant vers l'incision jusqu'à ce que son extrémité devienne visible. Saisissez l'implant à l'aide d'une pince et retirez-le (Fig. 13).
|
Fig. 13
|
| |
|
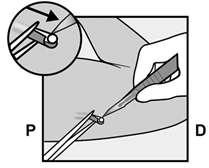
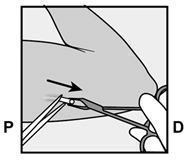
Retirez avec précaution les éventuels tissus adhérents de la pointe de l'implant par dissection mousse. Si la pointe de l'implant ne peut être dégagée en dépit de la dissection mousse, incisez l'enveloppe tissulaire et retirez l'implant à l'aide d'une pince (Fig. 14 et 15).
|
Fig. 14
|
| |
|
|
Fig. 15
|
| |
|

|
Si l'implant n'est pas encore visible, introduisez une pince en surface (de préférence une pince Mosquito courbe, la pointe dirigée vers le haut) dans l'incision (Fig. 16). Saisissez prudemment l'implant, puis faites passer cette pince dans l'autre main (Fig. 17). À l'aide d'une deuxième pince, dégagez avec précaution le tissu entourant l'implant et saisissez l'implant (Fig. 18). L'implant peut alors être retiré. S'il est impossible de saisir l'implant, arrêtez l'intervention et adressez la patiente à un(e) médecin familiarisé(e) avec les retraits d'implants compliqués ou consultez la filiale locale du titulaire de l'autorisation.
| |
|
Fig. 16
|
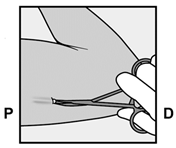
|
Fig. 17
|
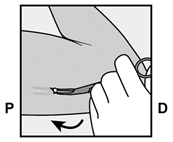
|
Fig. 18
|
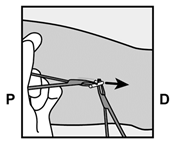
| |
|
Des cas d'implants cassés dans le bras des patientes ont été rapportés. Dans certains cas, une difficulté de retrait de l'implant cassé a été signalée.
Assurez-vous, en mesurant sa longueur, que vous avez retiré la totalité de l'implant, d'une longueur de 4 cm. Si une partie seulement de l'implant a été retirée (c'est-à-dire si l'élément obtenu mesure moins de 4 cm), l'incision doit, le cas échéant, être agrandie pour retirer également la partie de l'implant restée sous la peau. Il peut être nécessaire d'utiliser une méthode d'imagerie pour trouver la partie restante.
Après avoir retiré l'implant, appliquez un pansement adhésif stérile sur le site d'incision.
Posez un bandage compressif pour prévenir la formation d'hématomes. L'utilisatrice pourra retirer le bandage compressif au bout de 24 h et le pansement au bout de 3 à 5 jours.
|
Localisation et retrait d'un implant non palpable
Des cas de migration de l'implant ont été rapportés occasionnellement. Il s'agissait la plupart du temps d'un petit déplacement par rapport à la position initiale (voir «Mises en garde et précautions»). Un implant inséré (trop) profondément ou qui a migré peut ne pas être palpable et il faut alors utiliser, pour le localiser, les méthodes d'imagerie citées ci-dessous.
Un implant non palpable devrait toujours être localisé avant de tenter de le retirer. Les méthodes appropriées pour la localisation englobent l'échographie avec traducteur linéaire à haute fréquence (10 MHz ou supérieure), la radiographie bidimensionnelle, la tomodensitométrie ou l'IRM. Dès que l'implant a été localisé dans le bras, il devrait être retiré si nécessaire sous contrôle échographique par un(e) médecin familiarisé(e) avec la localisation et le retrait d'implants insérés profondément ainsi qu'avec l'anatomie du bras.
Si l'implant est introuvable dans le bras malgré des tentatives exhaustives de localisation, un examen du thorax par imagerie devrait être envisagé, car de rares cas de migration dans les vaisseaux pulmonaires ont été rapportés. Si l'implant est retrouvé dans le thorax, une intervention chirurgicale ou endovasculaire peut être nécessaire pour le retirer. Il faut alors faire appel à un spécialiste connaissant bien l'anatomie thoracique.
Si l'implant ne peut pas être localisé par les méthodes d'imagerie citées, le taux d'étonogestrel dans le sang peut être déterminé afin de confirmer la présence de l'implant.
Le retrait d'implants insérés profondément doit être effectué avec une prudence particulière afin d'éviter de léser des structures nerveuses ou vasculaires profondes. Les implants non palpables et insérés profondément devraient être retirés par des médecins familiarisés avec l'anatomie du bras et le retrait d'implants insérés profondément.
Il est vivement déconseillé de procéder à une intervention chirurgicale exploratrice sans connaissance de la position précise de l'implant.
Remplacement d'Implanon NXT
Si la patiente souhaite poursuivre l'utilisation d'Implanon NXT, un nouvel implant peut être mis en place immédiatement après le retrait de l'ancien implant. La technique de remplacement correspond pour l'essentiel à celle décrite sous Mise en place d'Implanon NXT.
Le nouvel implant peut être inséré dans le même bras, à travers l'incision pratiquée pour son retrait, dans la mesure où celle-ci se trouve au bon emplacement, c-à-d. 8 à 10 cm au-dessus de l'épicondyle médial de l'humérus et 3 à 5 cm derrière (sous) le sillon (voir le paragraphe Mise en place d'Implanon NXT). Dans ce cas, anesthésiez le site d'insertion le long du canal d'insertion prévu (p.ex. avec 2 ml d'une solution de lidocaïne à 1%) directement sous la peau, en commençant au niveau de l'incision. Suivez ensuite les instructions pour la mise en place de l'implant.
Numéro d’autorisation61298 (Swissmedic).
PrésentationEmballage de 1 implant, contenu dans la canule d'un applicateur à usage unique (B).
Titulaire de l’autorisationOrganon GmbH, Lucerne
Mise à jour de l’informationJanvier 2024
S-CCDS-OG8415-IPTx-072023-IIH/RCN-100003125-CH
|




























