CompositionPrincipes actifs
Midazolamum (ut Midazolami hydrochloridum).
Excipients
Natrii chloridum corresp. Natrium 3.16 mg/ml, Acidum hydrochloridum, Natrii hydroxidum ad pH, Aqua ad iniectabile.
Indications/Possibilités d’emploiTraitement d'urgence des crises convulsives aiguës prolongées chez les enfants à partir de 6 mois, les adolescents et les adultes.
Buccolam ne doit être administré par des parents/des soignants que si un diagnostic d'épilepsie a été posé chez le patient.
Posologie/Mode d’emploiPosologie usuelle
À partir de 6 mois
Les soignants ne doivent administrer qu'une seule dose de midazolam. Si la crise convulsive n'a pas cessé dans les 10 minutes suivant l'administration de midazolam, le médecin d'urgence doit être appelé immédiatement et la seringue préremplie vide doit être remise au médecin ou au personnel médical à titre d'information sur la dose reçue par le patient.
|
Tranche d'âge
|
Dose
|
Couleur de l'étiquette
| |
>6 mois à <1 an
|
2.5 mg
|
Jaune
| |
1 an à <5 ans
|
5 mg
|
Bleu
| |
5 ans à <10 ans
|
7.5 mg
|
Mauve
| |
À partir de 10 ans et adultes
|
10 mg
|
Orange
|
En cas de réponse insuffisante ou de réapparition des crises convulsives après réponse initiale, une seconde dose ou une dose répétée ne doit pas être administrée avant 30 minutes après la première utilisation en raison du risque dépression respiratoire, et uniquement sur avis médical préalable.
Chez les patients présentant un risque accru de dépression respiratoire déclenchée par les benzodiazépines, l'utilisation de Buccolam doit être considérée sous avis médical professionnel avant l'instauration du traitement par Buccolam. Cette utilisation peut être effectuée durant une phase exempte de crises.
Instructions posologiques particulières
Patients présentant des troubles de la fonction hépatique
L'insuffisance hépatique entraîne une diminution de la clairance du midazolam avec pour conséquence un allongement de la période de demi-vie terminale. Les effets cliniques peuvent donc être plus puissants et plus prolongés. De ce fait, une surveillance étroite des effets cliniques et des signes vitaux est recommandée après l'administration de midazolam aux patients présentant une insuffisance hépatique (voir «Mises en garde et précautions»).
Buccolam est contre-indiqué chez les patients atteints d'insuffisance hépatique sévère (voir «Contre-indications»).
Patients présentant des troubles de la fonction rénale
Aucune adaptation posologique n'est nécessaire; toutefois, Buccolam doit être utilisé avec prudence chez les patients présentant une insuffisance rénale chronique car l'élimination du midazolam peut être retardée et ses effets peuvent être prolongés (voir «Mises en garde et précautions»).
Enfants et adolescents
L'innocuité et l'efficacité du midazolam chez les enfants âgés de 0 à 6 mois n'ont pas été établies. Aucune étude n'est disponible.
Patients âgés
Les personnes âgées sont plus sensibles aux effets des benzodiazépines. Buccolam doit être utilisé avec prudence chez les patients à partir de 60 ans et chez les patients plus âgés.
Mode d'emploi
Buccolam est destiné à une administration buccale. La totalité de la solution doit être administrée lentement dans l'espace entre la gencive et la joue. L'application laryngotrachéale doit être évitée afin de prévenir une aspiration accidentelle de la solution. Si nécessaire (pour des volumes plus importants et/ou des patients plus petits), environ la moitié de la dose devrait être administrée lentement d'un côté de la cavité buccale, puis la seconde moitié de l'autre côté.
Mesures de précaution à prendre avant/pendant la manipulation ou avant/pendant l'administration du médicament
Aucune aiguille ne doit être fixée sur la seringue préremplie et celle-ci ne doit pas être reliée à une ligne de perfusion ou tout autre dispositif destiné à l'administration parentérale.
Buccolam ne doit pas être administré par voie intraveineuse.
Afin d'éviter tout risque d'étouffement, retirer le capuchon de la seringue préremplie avant utilisation.
Pour des instructions détaillées sur la façon d'administrer le médicament, voir rubrique «Remarque particulières – Instructions pour la manipulation».
Contre-indications·Hypersensibilité au principe actif, aux benzodiazépines ou à l'un des excipients (voir rubrique «Composition»).
·Myasthénie grave,
·Insuffisance respiratoire sévère,
·Syndrome d'apnée du sommeil,
·Insuffisance hépatique sévère.
Mises en garde et précautionsUne prudence particulière s'impose lors de l'administration de midazolam chez les patients à risque:
·patients de plus de 60 ans
·patients souffrant d'affection chronique ou présentant un état général fragilisé, p. ex.
·patients atteints d'insuffisance respiratoire chronique
·patients atteints d'insuffisance rénale chronique, de troubles de la fonction hépatique ou d'insuffisance cardiaque
·enfants présentant une faiblesse circulatoire
Ces patients à risque nécessitent éventuellement des doses plus faibles.
Le midazolam doit être utilisé avec prudence chez les patients présentant une insuffisance respiratoire, car le midazolam peut exacerber la dépression respiratoire.
L'administration concomitante de midazolam avec d'autres médicaments sédatifs / hypnotiques et dépresseurs du SNC, y compris l'alcool, peut entraîner une sédation profonde, une dépression respiratoire, le coma et la mort. Il devrait être limité à la dose la plus faible possible et les patients doivent être surveillés pour les signes et les symptômes de la dépression respiratoire et de la sédation.
En raison du rapport métabolite/molécule mère plus élevé chez les enfants les plus jeunes, un risque de dépression respiratoire différée due aux concentrations actives élevées du métabolite ne peut pas être exclu chez les nourrissons entre 3 et 6 mois. De ce fait, l'administration de Buccolam chez les nourrissons de 3 à 6 mois ne doit être faite que sous surveillance médicale dans un établissement disposant d'un équipement de réanimation et permettant la surveillance de la fonction respiratoire, et dans lequel un équipement d'assistance respiratoire est également disponible en cas de besoin.
Le midazolam doit être utilisé avec prudence chez les patients présentant une insuffisance rénale chronique ou une insuffisance hépatique ou cardiaque. Le midazolam peut s'accumuler chez les patients présentant une insuffisance rénale ou une insuffisance hépatique chronique, tandis que sa clairance peut être diminuée chez les patients présentant une insuffisance cardiaque.
Les patients affaiblis sont plus sensibles aux effets des benzodiazépines sur le système nerveux central et des doses plus faibles peuvent éventuellement s'avérer nécessaires.
L'administration de midazolam doit être évitée chez les patients ayant des antécédents d'alcoolisme ou de toxicomanie.
Le midazolam peut provoquer une amnésie antérograde.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c.-à-d. qu'il est essentiellement «sans sodium».
InteractionsLe midazolam est métabolisé par le CYP3A4. Les inhibiteurs et les inducteurs du CYP3A4 ont la capacité respectivement d'augmenter ou de diminuer les concentrations plasmatiques et de ce fait les effets du midazolam, ce qui nécessite en conséquence des adaptations de la dose. Les interactions pharmacocinétiques des inhibiteurs ou des inducteurs du CYP3A4 sont plus prononcées avec l'administration orale du midazolam qu'avec l'administration buccale ou parentérale, car les enzymes CYP3A4 sont également présentes dans les voies digestives supérieures. Après une administration buccale, seule la clairance systémique est affectée. Après l'administration d'une dose unique de midazolam par voie buccale, l'inhibition du CYP3A4 n'a qu'un retentissement mineur sur l'effet clinique maximal tandis que la durée de l'effet peut être prolongée. C'est pourquoi une surveillance étroite des effets cliniques et des signes vitaux est recommandée en cas d'administration de midazolam (même après un usage unique) conjointement avec un inhibiteur du CYP3A4.
Anesthésiques et analgosédatifs: Le fentanyl peut diminuer la clairance du midazolam.
Anti-épileptiques: L'administration conjointe avec du midazolam peut majorer la sédation ou la dépression respiratoire ou cardiovasculaire. Le midazolam peut interagir avec d'autres médicaments métabolisés dans le foie, par ex. la phénytoïne, et entraîner une potentialisation des effets.
Pour les patients traités par carbamazépine, les doses recommandées n'agissent pas suffisamment.
Un traitement simultané avec des médicaments alternatifs comme par ex. le diazépam par voie rectale n'est pas recommandé en raison de l'action sédative supplémentaire.
Inhibiteurs calciques: Le diltiazem et le vérapamil diminuent de manière avérée la clairance du midazolam et des autres benzodiazépines et peuvent potentialiser leurs effets.
Agents dopaminergiques: Le midazolam peut entraîner une inhibition de la lévopoda.
Myorelaxants: par ex. le baclofène. Le midazolam peut entraîner une potentialisation des myorelaxants, avec une majoration des effets dépresseurs du SNC.
Nabilone: L'administration conjointe avec du midazolam peut majorer la sédation ou la dépression respiratoire et cardiovasculaire.
Médicaments anti-ulcéreux: La cimétidine, la ranitidine et l'oméprazole diminuent de manière avérée la clairance du midazolam et des autres benzodiazépines et peuvent potentialiser leurs effets.
Xanthines: Les xanthines accélèrent le métabolisme du midazolam et des autres benzodiazépines.
Médicaments inhibiteurs du CYP3A4
Après administration de midazolam par voie buccale, les interactions médicamenteuses sont vraisemblablement similaires à celles observées avec le midazolam administré par voie intraveineuse plutôt que par voie orale.
Aliments
Jus de pamplemousse: il diminue la clairance du midazolam et potentialise son action.
Antifongiques azolés
Le kétoconazole a multiplié par 5 les concentrations plasmatiques de midazolam administré par voie intraveineuse tandis que la demi-vie terminale a été multipliée par 3 environ.
Le voriconazole a multiplié par 3 l'exposition par rapport au midazolam administré par voie intraveineuse tandis que la demi-vie d'élimination a été multipliée par 3 environ.
Le fluconazole et l'itraconazole ont multiplié par 2 à 3 les concentrations plasmatiques de midazolam administré par voie intraveineuse, la demi-vie terminale a été multipliée par 2.4 pour l'itraconazole et par 1.5 pour le fluconazole.
Le posaconazole a multiplié par 2 environ les concentrations plasmatiques de midazolam administré par voie intraveineuse.
Antibiotiques macrolides
L'érythromycine a multiplié par 1.6 à 2 environ les concentrations plasmatiques de midazolam administré par voie intraveineuse et par 1.5 à 1.8 sa demi-vie terminale.
La clarithromycine a multiplié par jusqu'à 2.5 les concentrations plasmatiques de midazolam administré par voie intraveineuse et par 1.5 à 2 sa demi-vie terminale.
Inhibiteurs de la protéase du VIH
Le saquinavir et autres inhibiteurs de la protéase du VIH: L'association avec des inhibiteurs de la protéase peut entraîner une augmentation importante de la concentration de midazolam. Après administration concomitante avec le lopinavir amplifié par le ritonavir, les concentrations plasmatiques de midazolam administré par voie intraveineuse ont été multipliées par 5.4, avec une augmentation similaire de la demi-vie terminale.
Inhibiteurs calciques
Diltiazem: Une dose unique de diltiazem a augmenté de 25% environ les concentrations plasmatiques de midazolam administré par voie intraveineuse et prolongé de 43% la demi-vie terminale.
Autres médicaments
L'atorvastatine a multiplié par 1.4 les concentrations plasmatiques de midazolam administré par voie intraveineuse comparativement au groupe témoin.
Médicaments inducteurs du CYP3A4
La rifampicine (600 mg une fois par jour pendant 7 jours) a diminué d'environ 60% les concentrations plasmatiques de midazolam administré par voie intraveineuse. La demi-vie terminale a diminué d'environ 50-60%.
Médicaments à base de plantes
Le millepertuis a diminué d'environ 20-40% les concentrations plasmatiques de midazolam, avec une réduction d'environ 15-17% de la demi-vie terminale. L'effet inducteur sur le CYP3A4 peut varier en fonction de l'extrait de millepertuis utilisé.
Interactions médicamenteuses pharmacodynamiques
La co-administration de midazolam avec d'autres agents sédatifs/hypnotiques et dépresseurs du SNC, dont l'alcool, peut conduire à la sédation profonde, la dépression respiratoire, le coma et la mort (voir «Mises en garde et précautions»).
Ces médicaments incluent par exemple les opiacés (utilisés comme analgésiques, antitussifs ou dans le cadre de traitements substitutifs), les antipsychotiques, les autres benzodiazépines utilisées comme anxiolytiques ou hypnotiques, les barbituriques, le propofol, la kétamine, l'étomidate, les antidépresseurs sédatifs, les anti-histaminiques H1 de première génération et les antihypertenseurs centraux.
L'alcool (y compris les médicaments contenant de l'alcool) peut renforcer de façon importante l'effet sédatif du midazolam. La consommation d'alcool doit être strictement évitée en cas d'administration de midazolam (voir «Mises en garde et précautions»).
Le midazolam diminue la concentration alvéolaire minimale (CAM) d'anesthésiques inhalés.
L'effet des inhibiteurs du CYP3A4 peut être plus important chez les nourrissons du fait qu'une partie de la dose administrée par voie buccale est vraisemblablement avalée et absorbée au niveau du tractus gastro-intestinal.
Grossesse, allaitementGrossesse
Les données sont insuffisantes pour évaluer l'innocuité du midazolam pendant la grossesse. Les études expérimentales chez l'animal n'ont pas mis en évidence d'effet tératogène, mais une fœtotoxicité a été observée, comme avec les autres benzodiazépines. Il n'existe pas de données sur l'utilisation du midazolam pendant les deux premiers trimestres de la grossesse.
Après l'administration de doses élevées de midazolam au cours du dernier trimestre de la grossesse ou pendant l'accouchement, des effets indésirables maternels ou fœtaux ont été rapportés (risque d'aspiration des liquides et du contenu stomacal pendant le travail chez la mère, irrégularités de la fréquence cardiaque chez le fœtus, hypotonie, faiblesse de la succion, hypothermie et dépression respiratoire chez le nouveau-né).
Le midazolam ne peut être administré pendant la grossesse sauf en cas de nécessité absolue. En cas d'administration de midazolam pendant le troisième trimestre de la grossesse, le risque pour le nouveau-né doit être pris en compte.
Allaitement
Le midazolam passe en faibles quantités (0.6%) dans le lait maternel. L'allaitement ne doit donc pas être nécessairement arrêté après l'administration d'une dose unique de midazolam.
Fertilité
Les études effectuées chez l'animal n'ont pas mis en évidence une diminution de la fertilité (voir «Données précliniques»).
Effet sur l’aptitude à la conduite et l’utilisation de machinesLe midazolam a une influence importante sur l'aptitude à la conduite ou l'utilisation de machines.
La sédation, l'amnésie, la diminution de l'attention et l'altération des fonctions musculaires peuvent affecter l'aptitude à conduire un véhicule (y compris une bicyclette) et à utiliser des machines. Le patient doit être averti qu'après avoir pris du midazolam, il ne doit pas conduire un véhicule, ni utiliser des machines tant qu'il n'a pas complètement récupéré.
Effets indésirablesSelon des études cliniques publiées, le midazolam a été administré par voie buccale à 443 enfants présentant des crises convulsives. Dans la plupart des études, le nombre d'effets secondaires n'était pas indiqué, néanmoins il était mentionné qu'aucun évènement grave n'avait été rapporté ou qu'aucune différence n'avait été constatée par rapport au traitement de comparaison, le diazépam administré (par exemple par voie rectale ou intraveineuse). Une dépression respiratoire survient avec une fréquence allant jusqu'à 5%; cependant il n'existe pas seulement un rapport avec l'administration de benzodiazépines, mais il s'agit également d'une complication connue des crises convulsives. Un épisode de prurit a été jugé comme étant éventuellement imputable à l'administration de midazolam par voie buccale.
Le tableau suivant présente les effets indésirables survenus après l'administration de midazolam par voie buccale dans le cadre d'études cliniques et après la mise sur le marché.
Les effets indésirables sont rangés par classe de système d'organes de la classification MedDRA et par fréquence selon la convention suivante:
Fréquent: ≥1/100, <1/10
Occasionnel: ≥1/1000, <1/100
Très rare: <1/10'000
Fréquence inconnue: ne peut être estimée sur la base des données disponibles
Au sein de chaque groupe de fréquence, les effets indésirables d'un système organe-classe sont présentés par ordre décroissant de gravité:
|
Classe de systèmes d'organes
|
Fréquence: Effets indésirables médicamenteux
| |
Affections du système immunitaire
|
Fréquence inconnue: Réaction anaphylactique*
| |
Affections du système nerveux
|
Fréquent: Sédation, somnolence, diminution du niveau de conscience, dépression respiratoire
| |
Affections gastro-intestinales
|
Fréquent: Nausées et vomissements
| |
Affections de la peau et du tissu sous-cutané
|
Occasionnel: Prurit, éruption cutanée et urticaire
Fréquence inconnue: Angioedème*
|
* Effet indésirable rapporté dans le cadre de la surveillance après la mise sur le marché
Les effets indésirables suivants, susceptibles d'être pertinents pour l'administration par voie buccale, ont été rapportés (très rarement) après l'injection de midazolam chez des enfants ou des adultes:
|
Classe de systèmes d'organes
|
Fréquence: Effets indésirables médicamenteux - Tous les effets surviennent très rarement
| |
Affections psychiatriques
|
Agressivité, agitation, accès de colère, état confusionnel, humeur euphorique, hallucinations, hostilité, troubles du mouvement, violences physiques
| |
Affections du système nerveux
|
Amnésie antérograde, ataxie, vertiges, céphalées, crise convulsive, réactions paradoxales
| |
Affections cardiaques
|
Bradycardie, arrêt cardiaque, hypotension, vasodilatation
| |
Affections respiratoires, thoraciques et médiastinales
|
Apnée, dyspnée, laryngospasme, arrêt respiratoire
| |
Affections gastro-intestinales
|
Constipation, sécheresse buccale
| |
Troubles généraux et anomalies au site d'administration
|
Fatigue, hoquet
|
Description d'effets indésirables sélectionnés
Un risque accru de chutes et fractures est connu chez les personnes âgées traitées par benzodiazépines.
Des évènements potentiellement fatals sont susceptibles de survenir avec une plus haute probabilité chez les patients présentant une insuffisance respiratoire préexistante ou une insuffisance cardiaque, notamment en cas d'administration de doses élevées (voir «Mises en garde et précautions»).
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageUn surdosage de midazolam ne devrait pas entraîner de manifestations engageant le pronostic vital, sauf si le patient souffre d'une insuffisance respiratoire ou cardiaque préexistante ou en cas d'association avec d'autres dépresseurs du SNC (y compris l'alcool).
Pour le traitement du surdosage de tout médicament, il convient de tenir compte de la possibilité d'une intoxication multiple.
En cas de surdosage de midazolam administré par voie orale, il faut induire des vomissements (dans l'heure qui suit) si le patient est conscient, ou pratiquer un lavage d'estomac en veillant à la protection des voies respiratoires si le patient est inconscient. Si un lavage gastrique n'est pas pertinent, il convient d'administrer du charbon actif pour diminuer l'absorption. Les fonctions respiratoire et cardiovasculaire doivent en particulier être étroitement surveillées dans un service de soins intensifs.
Un surdosage de benzodiazépines entraîne en général à des degrés divers une dépression du système nerveux central allant de la somnolence jusqu'au coma. Dans les cas bénins, les symptômes sont la somnolence, la confusion mentale et la léthargie. Dans les cas les plus graves, les symptômes peuvent être l'ataxie, l'hypotonie, l'hypotension et la dépression respiratoire, plus rarement le coma, et très rarement le décès.
Le flumazénil peut être administré à titre d'antidote.
Propriétés/EffetsCode ATC
N05CD08
Mécanisme d'action
Le midazolam est un dérivé du groupe des imidazobenzodiazépines. La base libre est une substance lipophile faiblement soluble dans l'eau. La base azotée en position 2 de la structure en anneau de l'imidazobenzodiazépine permet au midazolam de former le sel chlorhydrate avec les acides. Ceci donne une solution stable adaptée à l'administration buccale.
Pharmacodynamique
L'action pharmacologique du midazolam est caractérisée par une durée courte en raison d'un métabolisme rapide. Le midazolam possède un effet anti-convulsivant. Il exerce en outre une action sédative et inductrice du sommeil de forte intensité ainsi qu'une action anxiolytique et myorelaxante.
Efficacité clinique
Dans quatre études contrôlées versus diazépam administré par voie rectale et une étude versus diazépam par voie intraveineuse, menées chez 688 enfants au total, une disparition des signes visibles des crises convulsives a été observée dans les 10 minutes suivant l'administration chez 65% à 78% des enfants qui ont reçu du midazolam par voie buccale. En outre, dans deux des études, une disparition des signes visibles des convulsions dans les 10 minutes sans récidive dans l'heure suivant l'administration, a été observée chez 56% à 70% des enfants. La fréquence et la sévérité des effets médicamenteux indésirables rapportés pour le midazolam administré par voie buccale dans les études cliniques publiées étaient comparables aux effets médicamenteux indésirables rapportés dans le groupe témoin qui avait reçu du diazépam par voie rectale.
L'autorisation de l'utilisation de Buccolam chez l'adulte repose sur l'extrapolation des résultats d'efficacité et de sécurité pédiatriques à l'adulte (voir «Pharmacocinétique»).
PharmacocinétiqueAbsorption
Sur la base d'études de pharmacocinétique de population, les paramètres pharmacocinétiques simulés pour les posologies recommandées sont représentés dans le tableau ci-dessous:
|
Dose
|
Âge
|
Paramètre
|
Valeur moyenne
|
Déviation standard
| |
*2.5 mg
|
3 mois <1 an
|
AUC0-inf (ng.h/ml)
|
168
|
98
| |
|
|
Cmax (ng/ml)
|
104
|
46
| |
5 mg
|
1 an <5 ans
|
AUC0-inf (ng.h/ml)
|
242
|
116
| |
|
|
Cmax (ng/ml)
|
148
|
62
| |
7.5 mg
|
5 ans <10 ans
|
AUC0-inf (ng.h/ml)
|
254
|
136
| |
|
|
Cmax (ng/ml)
|
140
|
60
| |
10 mg
|
10 ans <18 ans
|
AUC0-inf (ng.h/ml)
|
189
|
96
| |
|
|
Cmax (ng/ml)
|
87
|
44
| |
**10 mg
|
>18 ans
|
AUC0-inf (ng.h/ml)
|
259
|
62
| |
|
|
Cmax (ng/ml)
|
71
|
29
|
* Buccolam n'est pas indiqué pour les enfants âgés de 3 à 6 mois.
** Les paramètres pharmacocinétiques simulés chez les adultes ont été déterminés sur la base de données issues d'une étude de biodisponibilité réalisée sur des adultes sains. Aucun sujet de plus de 68 ans ni obèse n'a été inclus dans l'étude.
Après administration buccale, le midazolam est absorbé rapidement. La concentration plasmatique maximale est atteinte en 30 minutes. Chez l'adulte, la biodisponibilité absolue de midazolam administré par voie buccale est d'environ 75%. La biodisponibilité du midazolam administré par voie buccale a été évaluée à 87% chez des enfants présentant un paludisme sévère et des convulsions.
Distribution
Le midazolam est très lipophile et fortement distribué. Le volume de distribution à l'état d'équilibre après administration buccale est évalué à 5.3 l/kg.
La liaison du midazolam aux protéines plasmatiques est d'environ 96-98%. La majeure partie de la liaison aux protéines plasmatiques concerne l'albumine. Le midazolam passe lentement et en quantités non significatives dans le liquide céphalo-rachidien. Il a été démontré que chez l'être humain, le midazolam traverse lentement le placenta et pénètre dans la circulation fœtale. De faibles quantités de midazolam sont retrouvées dans le lait maternel.
Métabolisme
Le midazolam est presque entièrement éliminé par biotransformation. La fraction de la dose éliminée par le foie est évaluée à 30-60%. Le midazolam est hydroxylé par l'isoenzyme 3A4 du cytochrome P450 et le principal métabolite urinaire et plasmatique est l'alpha-hydroxy-midazolam. Après administration par voie buccale, le quotient AUC (aire sous la courbe) alpha-hydroxy-midazolam/midazolam est de 0.46 chez les enfants et 0.28 chez les adultes.
Une étude pharmacocinétique de population a montré des taux de métabolites plus élevés chez les patients pédiatriques plus jeunes que chez les patients pédiatriques plus âgés, ce qui permet de conclure que ces taux sont probablement plus importants chez les enfants que chez les adultes.
Élimination
Chez l'enfant la clairance plasmatique du midazolam administré par voie buccale est de 30 ml/kg/min. Les demi-vies d'élimination initiale et terminale sont respectivement de 27 et de 204 minutes. Le midazolam est éliminé principalement par voie rénale (60-80% de la dose injectée) et il est retrouvé sous forme d'alpha-hydroxy-midazolam glucuroconjugué. Moins de 1% de la dose administrée est retrouvé dans les urines sous forme inchangée.
Cinétique pour certains groupes de patients
Patients âgés
L'exposition au midazolam après utilisation dans la cavité buccale chez des sujets adultes sains entre 60 et 68 ans (n = 4) n'a montré aucune différence pertinente par rapport à des adultes sains plus jeunes. L'exposition après utilisation dans la cavité buccale chez des adultes de plus de 68 ans n'est pas connue. Elle peut cependant être accrue, étant donné que la demi-vie d'élimination peut être jusqu'à quatre fois plus longue après l'administration par voie intraveineuse.
Patients obèses
La demi-vie moyenne du midazolam après utilisation dans la cavité buccale chez les adultes ayant un IMC entre 30 et 34 (n = 6) n'a montré aucune différence pertinente par rapport aux adultes ayant un IMC entre 25 et 30 (8.4 heures contre 5.5 heures). La demi-vie moyenne n'est pas connue chez les adultes ayant un IMC de plus de 34. Elle peut cependant être accrue, étant donné que la demi-vie moyenne est plus longue chez les patients obèses que chez les patients non obèses (5.9 heures contre 2.3 heures). Cela est dû à une augmentation d'environ 50% du volume de distribution corrigé pour le poids corporel total. La clairance n'est pas significativement différente chez les patients obèses et non obèses.
Patients avec troubles de la fonction hépatique
Chez les patients cirrhotiques, la demi-vie d'élimination peut être plus longue et la clairance plus faible que chez les volontaires sains (voir «Mises en garde et précautions»).
Patients avec troubles de la fonction rénale
La demi-vie d'élimination chez les patients présentant une insuffisance rénale chronique est comparable à celle des volontaires sains.
Chez les patients en état critique, la demi-vie d'élimination du midazolam est prolongée jusqu'à six fois.
Patients avec insuffisance cardiaque
La demi-vie d'élimination est plus longue chez les patients présentant une insuffisance cardiaque décompensée que chez les volontaires sains (voir «Mises en garde et précautions»).
Exposition après une seconde dose au cours de la même crise convulsive
Les données d'exposition simulées montrent que l'AUC totale est à peu près doublée lorsqu'une seconde dose est administrée resp. 10, 30 et 60 minutes après la première dose.
Une seconde dose administrée 10 minutes après la première dose entraîne une multiplication significative par 1.7 à 1.9 de la Cmax moyenne. En cas d'administration après 30 et 60 minutes, une élimination significative du midazolam survient déjà, et de ce fait l'augmentation moyenne de la Cmax est moins prononcée: multiplication par 1.3 à 1.6, respectivement de 1.2 à 1.5 (voir «Posologie/Mode d'emploi»).
Données précliniquesDans une étude de fertilité menée chez le rat, aucun effet négatif sur la fertilité n'a été observé chez des animaux auxquels on a administré jusqu'à dix fois la dose clinique.
Il n'existe pas de données précliniques pertinentes pour le médecin prescripteur autres que celles qui figurent déjà dans les autres rubriques.
Remarques particulièresIncompatibilités
Sans objet.
Influence sur les méthodes de diagnostic
Sans objet.
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Remarques particulières concernant le stockage
Conserver la seringue préremplie pour application dans la cavité buccale dans le tube de protection en plastique et à température ambiante (15-25°C).
Ne pas conserver au réfrigérateur ni congeler.
Conserver hors de portée des enfants.
Remarques concernant la manipulation
Buccolam ne doit pas être administré par voie intraveineuse.
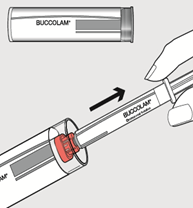
Étape 1
|
|
|
Retirer le capuchon. Sortir la seringue préremplie du tube.
|
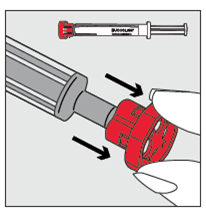
Étape 2
|
|
|
Retirer le capuchon rouge de l'embout de la seringue préremplie et vérifier que la totalité du capuchon, constitué de l'embout interne transparent et du capuchon rouge, a été enlevée (voir figure 1 ci-dessous), puis jeter l'embout. Il faut s'assurer que l'embout interne transparent n'est pas resté fixé sur la seringue, comme le montre la figure 2 ci-dessous. Si l'embout interne transparent est resté fixé sur l'extrémité de la seringue, il doit être retiré manuellement avant l'administration du médicament. Sinon, il risque de pénétrer dans la bouche du patient pendant l'application et d'être inhalé ou avalé (pour de plus amples informations, voir la rubrique «Instructions complémentaires pour une utilisation correcte de Buccolam en seringues pour administration buccale»).
| |
|

| |
Figure 1: CORRECT L'embout interne transparent est retiré
| |
|

| |
Figure 2: INCORRECT L'embout interne transparent reste fixé à l'extrémité de la seringue
|
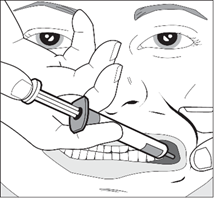
Étape 3
|
|
|
Saisir délicatement la joue du patient avec le pouce et l'index et l'étirer. Introduire l'extrémité de la seringue dans la partie arrière de l'espace entre la joue et la gencive de la mâchoire inférieure.
|
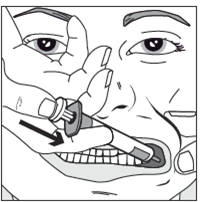
Étape 4
|
|
|
Enfoncer lentement le piston de la seringue jusqu'à la butée.
Administrer lentement la quantité totale de solution dans l'espace entre la gencive et la joue (cavité buccale).
Selon la prescription du médecin (pour des volumes plus importants et/ou des patients plus petits), environ la moitié de la dose peut être administrée lentement d'un côté de la cavité buccale, puis la seconde moitié de l'autre côté.
|
Instructions complémentaires pour une utilisation correcte de Buccolam en seringues pour administration buccale
L'embout interne blanc transparent inséré dans le capuchon rouge des seringues préremplies Buccolam peut parfois rester fixé à l'extrémité de la seringue après que le capuchon rouge a été détaché (voir figure 2 ci-dessus). Si cela se produit, l'embout interne transparent peut tomber dans la bouche du patient et pourrait être aspiré ou avalé. Si l'embout interne est aspiré, il y a un risque d'étouffement. Les parents et les tuteurs doivent être informés de ce risque et de la nécessité d'un contrôle approprié avant l'utilisation du produit.
Si l'on craint que l'embout interne est tombé dans la bouche du patient, il faut immédiatement vérifier qu'il n'est pas resté inséré dans le capuchon rouge. Si ce n'est pas le cas, ne pas essayer de le chercher avec un doigt dans la bouche ou de retirer le capuchon de la bouche. Tournez plutôt le patient sur le côté (position latérale de sécurité) et veiller à ce qu'il recrache le capuchon dès que la crise convulsive est terminée.
Numéro d’autorisation62556 (Swissmedic).
Présentation2.5 mg dans 0.5 ml de solution, boîte de 2 (actuellement indisponible dans le commerce) et 4 seringues préremplies (B)
5 mg dans 1 ml de solution, boîte de 2 (actuellement indisponible dans le commerce) et 4 seringues préremplies (B)
7.5 mg dans 1.5 ml de solution, boîte de 2 (actuellement indisponible dans le commerce) et 4 seringues préremplies (B)
10 mg dans 2 ml de solution, boîte de 2 (actuellement indisponible dans le commerce) et 4 seringues préremplies (B)
Titulaire de l’autorisationNeuraxpharm Switzerland AG, Cham
Mise à jour de l’informationDécembre 2024
Interne Versionsnummer: 4.0
|






