Propriétés/EffetsCode ATC
A10AD06
Mécanisme d'action
L'insuline dégludec et l'insuline asparte se lient spécifiquement au récepteur de l'insuline humaine et ont donc les mêmes effets pharmacologiques que l'insuline humaine.
L'effet hypoglycémiant de l'insuline est dû à la liaison de l'insuline aux récepteurs de l'insuline des cellules musculaires et adipeuses, facilitant ainsi l'absorption du glucose, et à l'inhibition simultanée de la production hépatique de glucose.
Pharmacodynamique
L'effet pharmacodynamique de Ryzodeg est spécifique pour chaque composant (figure 1) et le profil d'action qui en résulte reflète les deux composants, l'insuline asparte d'action rapide et l'insuline basale dégludec.
Le composant basal à longue durée d'action de Ryzodeg (insuline dégludec) forme des multihexamères solubles après injection sous-cutanée, ce qui entraîne un dépôt à partir duquel l'insuline dégludec est lentement absorbée en continu dans la circulation, avec pour résultat un effet hypoglycémiant stable et plat. Cet effet est maintenu dans l'association avec l'insuline asparte et n'interfère pas avec les monomères d'insuline asparte d'action rapide.
Après l'administration de Ryzodeg, l'entrée en action est très rapide et couvre les repas. La composante basale présente un profil plat, stable et de longue durée d'action, ce qui permet une couverture continue du besoin basal d'insuline. La durée d'action d'une dose unique de Ryzodeg est supérieure à 24 heures.

Figure 1: Taux de perfusion moyen de Ryzodeg après l'administration d'une dose unique de 0,8 U/kg chez des diabétiques de type 1.
L'effet hypoglycémiant général et l'effet hypoglycémiant maximum de Ryzodeg augmentent linéairement avec la dose. L'état équilibre est atteint 2 à 3 jours après la première dose administrée.
Il n'y a pas de différence au niveau de l'effet pharmacodynamique de Ryzodeg entre les sujets âgés et les sujets plus jeunes.
Efficacité clinique
Sept études cliniques «treat-to-target» multinationales, randomisées, contrôlées, en mode ouvert d'une durée comprise entre 26 semaines et 52 semaines ont été menées. Dans le cadre de celles-ci, un total de 1761 sujets atteints de diabète (1 étude avec 362 sujets avec un diabète de type 1 et 6 études avec 1399 sujets avec un diabète de type 2) ont été traités par Ryzodeg.
Ryzodeg, administré une fois par jour a été comparé à l'insuline glargine (IGlar) (une fois par jour) dans le cadre de deux études portant sur le diabète de type 2 (tableau 1).
Ryzodeg, administré deux fois par jour a été comparé à l'insuline asparte biphasique 30 (IAspB 30) administrée deux fois par jour dans le cadre de deux études portant sur le diabète de type 2 et dans le cadre d'une étude portant également sur le diabète de type 2, Ryzodeg a été comparé à l'insuline dégludec (IDeg) administrée une fois par jour et à l'insuline asparte (IAsp) administrée 2 à 4 fois par jour (tableau 2).
Dans une étude sur le diabète sucré de type 2, Ryzodeg, administré une fois par jour, a été comparé à l'insuline glargine (IGlar) administrée une fois par jour avec l'IAsp administrée une fois par jour. Après 26 semaines de traitement, la dose de Ryzodeg a été divisée en deux doses quotidiennes (tableau 3). Les antidiabétiques oraux (OAD) ont été autorisés dans toutes les études sur le diabète sucré de type 2.
Ryzodeg administré une fois par jour en association avec de l'insuline asparte (IAsp) a également été comparé à l'insuline détémir (IDet) administrée une ou deux fois par jour en association avec de l'IAsp dans le diabète de type 1 (tableau 4).
La non-infériorité de la variation de l'HbA1c de référence jusqu'à la fin de l'étude a été confirmée dans 6 des 7 études par rapport à tous les comparateurs utilisant le principe du traitement par rapport à la cible, tandis que la non-infériorité dans une étude (comparaison de Ryzodeg administré deux fois par jour avec IDeg une fois par jour avec l'insuline IAsp administrée 2 à 4 fois par jour) chez des diabétiques du type 2 n'était pas confirmée (tableau 2).
En association avec un ADO, Ryzodeg une fois par jour permet, aussi bien chez les diabétiques de type 2 n'ayant jamais été traités à l'insuline que chez ceux l'ayant déjà été, un contrôle glycémique similaire à celui de l'insuline glargine. Ryzodeg a conduit à un meilleur contrôle glycémique prandial, avec un plus faible taux d'hypoglycémies nocturnes (définies comme les épisodes survenant entre minuit et 6 h du matin avec un taux de glucose plasmatique confirmé <3,1 mmol/l ou les situations où le patient avait besoin de l'aide d'une tierce personne) (tableau 1) par comparaison avec l'insuline glargine.
Il a été démontré que le contrôle de la glycémie (HbA1c) avec Ryzodeg administré 2 fois par jour est similaire à celui obtenu avec BIAsp 30 administré 2 fois par jour. Ryzodeg a permis d'obtenir une meilleure glycémie à jeun et les patients ont atteint la valeur-cible d'un taux plasmatique de 5 mmol/l plus rapidement qu'avec le BIAsp 30. Ryzodeg a conduit à un plus faible taux total d'hypolycémies et d'hypoglycémies nocturnes (tableau 2).
Ryzodeg, administré deux fois par jour, a été comparé à l'insuline IDeg administrée une fois par jour avec l'insuline IAsp (2 à 4 injections par jour) chez des patients atteints de diabète sucré de type 2 traités avec de l'insuline basale et nécessitant une intensification thérapeutique avec de l'insuline prandiale. Les deux traitements ont amélioré le contrôle de la glycémie, mais le traitement par Ryzodeg n'a pas atteint la limite de non-infériorité prédéfinie de 0,4% par rapport à l'IDeg plus IAsp en ce qui concerne le paramètre principal de modification de l'HbA1c à la semaine 26 (Tableau 2). Il n'y avait aucune différence statistiquement significative entre les deux groupes de traitement.
Dans une étude menée auprès de patients atteints de diabète sucré de type 2 traités avec l'insuline basale et nécessitant une intensification du traitement avec l'insuline prandiale, Ryzodeg a été comparé à l'insuline IGlar administrée une fois par jour avec l'insuline IAsp administrée une fois par jour pendant 26 semaines. Après 26 semaines, la dose de Ryzodeg dans le groupe Ryzodeg a été divisée en deux doses quotidiennes. Dans le groupe IGlar, des doses supplémentaires d'IAsp auraient pu être administrées pendant d'autres repas (jusqu'à trois fois par jour). Ryzodeg, administré une fois par jour, a obtenu un contrôle glycémique similaire (HbA1c) comparé à l'insuline IGlar administrée une fois par jour avec l'insuline IAsp administrée une fois par jour après 26 semaines. Ryzodeg, administré une ou deux fois par jour, a obtenu un contrôle glycémique similaire (HbA1c) une fois par jour avec l'insuline IAsp administrée une à trois fois par jour après 38 semaines par rapport à l'IGlar administrée une fois par jour avec l'IAsp. Ryzodeg a montré un taux plus faible d'hypoglycémie nocturne pendant les 26 et 38 semaines (tableau 3).
Chez les patients ayant un diabète de type 1, il a été démontré que le traitement par Ryzodeg une fois par jour en association avec l'insuline asparte pour les autres repas procure un contrôle de la glycémie (HbA1c et glycémie à jeun) similaire, avec un taux d'hypoglycémies nocturnes plus faible comparativement à un schéma basal/bolus avec l'insuline détémir en association à l'insuline asparte à tous les repas (tableau 4).
Tableau 1: Résultat de deux études de 26 semaines portant sur le diabète de type 2
|
|
Ryzodeg
(une fois par jour)1
Patients n'ayant jamais été traités à l'insuline
|
IGlar
(une fois par jour)1
Patients n'ayant jamais été traités à l'insuline
|
Ryzodeg
(une fois par jour)2 Patients prenant de l'insuline
|
IGlar
(une fois par jour)2
Patients prenant de l'insuline
| |
N
|
266
|
263
|
230
|
233
| |
Valeur HbA1c moyenne (%)
| |
Fin de l'étude
Modification moyenne par rapport à la valeur initiale
|
7,2
-1,65
|
7,2
-1,72
|
7,3
-0,98
|
7,4
-1,00
| |
|
Différence:
0,03 [-0,14; 0,20]
|
Différence:
-0,03 [-0,20; 0,14]
| |
Glycémie à jeun (GAJ) (mmol/l)
| |
Fin de l'étude
Modification moyenne par rapport à la valeur initiale
|
6,8
-3,32
|
6,3
-4,02
|
6,3
-1,68
|
6,0
-1,88
| |
|
Différence:
0,51 [0,09; 0,93]
|
Différence:
0,33 [-0,11; 0,77]
| |
Glycémie (plasma) 90 minutes après les repas, à la fin de l'étude (en mmol/l)
| |
Après le petit-déjeuner
Modification moyenne par rapport à la valeur initiale
|
1,9
-1,5
|
3,4
-0,3
|
|
| |
Après le repas du soir
Modification moyenne par rapport à la valeur initiale
|
|
|
1,2
-1,5
|
2,6
-0,6
| |
Taux d'hypoglycémies (par patient-année d'exposition)
| |
Sévères
|
0,01
|
0,01
|
0,00
|
0,04
| |
Confirmées3
|
4,23
|
1,85
|
4,31
|
3,20
| |
|
Ratio:
2,17 [1,59; 2,94]
|
Ratio:
1,43 [1,07; 1,92]
| |
Nocturnes confirmées3
|
0,19
|
0,46
|
0,82
|
1,01
| |
|
Ratio:
0,29 [0,13;0,65]
|
Ratio:
0,80 [0,49;1,30]
|
1 Administration une fois par jour + metformine
2 Administration une fois par jour + metformine ± pioglitazone ± inhibiteur de la DPP-4
3 L'hypoglycémie confirmée a été définie comme des épisodes confirmés par un taux de glucose plasmatique <3,1 mmol / l ou par le patient nécessitant une aide extérieure. L'hypoglycémie nocturne confirmée était définie comme des épisodes survenus entre minuit et 6h00.
IGlar = insuline glargine
Tableau 2: Résultat de trois études de 26 semaines portant sur le diabète de type 2
|
|
Ryzodeg
(deux fois par jour)1
Patients prenant de l'insuline
|
BIAsp 30
(deux fois par jour)1
Patients prenant de l'insuline
|
Ryzodeg
(deux fois par jour)2
Patients prenant de l'insuline
|
BIAsp 30
(deux fois par jour)2
Patients prenant de l'insuline
|
Ryzodeg (deux fois par jour)3 Patients prenant de l'insuline
|
IDeg (une fois fois par jour) + IAsp4
Patients prenant de l'insuline
| |
N
|
224
|
222
|
280
|
142
|
138
|
136
| |
Valeur HbA1c moyenne (%)
| |
Fin de l'étude
Modification moyenne par rapport à la valeur initiale
|
7,1
-1,28
|
7,1
-1,30
|
7,1
-1,38
|
7,0
-1,42
|
7,0
-1,31
|
6,8
-1,50
| |
|
Différence:
-0,03 [-0,18; 0,13]
|
Différence:
0,05 [-0,10; 0,20]
|
Différence:
0,18 [-0,04; 0,41]
| |
Glycémie à jeun (GAJ) (mmol/l)
| |
Fin de l'étude
Modification moyenne par rapport à la valeur initiale
|
5,8
-3,09
|
6,8
-1,76
|
5,4
-2,55
|
6,5
-1,47
|
6,8
-2,25
|
7,1
-1,78
| |
|
Différence:
-1,14 [-1,53; -0,76]
|
Différence:
-1,06 [-1,43; -0,70]
|
Différence:
-0,31 [-0,97; 0,34]
| |
Taux d'hypoglycémies (par patient-année d'exposition)
| |
Sévères
|
0,09
|
0,25
|
0,05
|
0,03
|
0,47
|
0,24
| |
Confirmées5
|
9,72
|
13,96
|
9,56
|
9,52
|
11,55
|
13,62
| |
|
Ratio:
0,68 [0,52; 0,89]
|
Ratio:
1,00 [0,76; 1,32]
|
Ratio:
0,81 [0,61; 1,07]
| |
Nocturnes confirmées5
|
0,74
|
2,53
|
1,11
|
1,55
|
1,23
|
1,55
| |
|
Ratio:
0,27 [0,18; 0,41]
|
Ratio:
0,67 [0,43; 1,06]
|
Ratio:
0,80 [0,50; 1,29]
| |
Dose totale d'insuline (unités)
| |
Fin de l'étude
|
|
106,7
|
130,6
| |
Ratio:
0,81 [0,69; 0,95]
|
1 Administration deux fois par jour ± metformine ± pioglitazone ± inhibiteur de la DPP-4
2 Administration deux fois par jour ± metformine
3 Administration deux fois par jour ± metformine ± sécrétagogue d'insuline ± inhibiteur DPP-4 ± inhibiteur α-glucosidase
4 Administration une fois par jour + insuline asparte 2 à 4 fois par jour sous forme d'insuline prandiale ± metformine ± sécrétagogue d'insuline ± inhibiteur de DPP-4 ± inhibiteur de α-glucosidase
5 L'hypoglycémie confirmée a été définie comme des épisodes confirmés par un taux de glucose plasmatique <3,1 mmol / l ou par le patient nécessitant une aide extérieure. L'hypoglycémie nocturne confirmée était définie comme des épisodes survenus entre minuit et 6h00.
Tableau 3: Résultat d'une étude de 38 semaines portant sur le diabète de type 2
|
|
Ryzodeg
(une fois par jour)1
Après 26 semaines
|
IGlar (une fois par jour) +
IAsp (une fois par jour)1
Après 26 semaines
|
Ryzodeg
(une fois par jour/deux fois par jour)2
Après 38 semaines
|
IGlar (une fois par jour) +
IAsp (une à trois fois par jour)3
Après 38 semaines
| |
N
|
267
|
265
|
267
|
265
| |
Valeur HbA1c moyenne (%)
|
|
| |
Fin de l'étude
Modification moyenne par rapport à la valeur initiale
|
7,1
-1,1
|
7,1
-1,1
|
7,0
-1,2
|
6,9
-1,2
| |
|
Différence:
0,07 [-0,06; 0,21]
|
Différence:
0,09 [-0,04; 0,22]
| |
Glycémie à jeun (GAJ) (mmol/l)
|
|
| |
Fin de l'étude
Modification moyenne par rapport à la valeur initiale
|
6,7
-2.3
|
6.5
-2,3
|
6,3
-2,7
|
6,5
-2,3
| |
|
Différence:
0,04 [-0,34; 0,42]
|
Différence:
-0,24 [-0,60; 0,13]
| |
Taux d'hypoglycémies (par patient-année d'exposition)
| |
Sévères ou confirmées4
|
2,58
|
2,96
|
2,87
|
3,43
| |
|
Ratio:
0,90 [0,67; 1,22]
|
Ratio:
0,86 [0,65; 1,14]
| |
Nocturnes sévères ou confirmées4
|
0,48
|
0,93
|
0,60
|
1,01
| |
|
Ratio:
0,55 [0,34; 0,90]
|
Ratio:
0,61 [0,40; 0,93]
| |
Dose totale d'insuline (unités)
| |
Fin de l'étude
|
70,9
|
79,4
|
83,4
|
89,3
| |
|
Ratio:
0,88 [0,81; 0,95]
|
Ratio:
0,91 [0,83; 0,99]
|
1 Administration une fois par jour ± ADOs
2 Administration une fois ou deux fois par jour ± ADOs
3 Une fois par jour insuline glargine + insuline asparte 1 à 3 fois par jour ± ADOs
4 L'hypoglycémie confirmée a été définie comme des épisodes confirmés par un taux de glucose plasmatique <3,1 mmol / l ou par le patient nécessitant une aide extérieure. L'hypoglycémie nocturne confirmée était définie comme des épisodes survenus entre minuit et 6h00.
Remarque: Les ADOs peuvent contenir toute combinaison de metformine, d'inhibiteurs de la DPP-4, d'inhibiteurs de la glucosidase α ou d'inhibiteurs de la SGLT2.
Tableau 4: Résultat d'une étude de 26 semaines portant sur le diabète de type 1
|
|
Ryzodeg
(une fois par jour)1
|
IDet
(une/deux fois par jour)2
| |
N
|
366
|
182
| |
Valeur HbA1c moyenne (%)
| |
Fin de l'étude
Modification moyenne par rapport à la valeur initiale
|
7,6
-0,73
|
7,6
-0,68
| |
|
Différence:
-0,05 [-0,18; 0,08]
| |
Glycémie à jeun (GAJ) (mmol/l)
| |
Fin de l'étude
Modification moyenne par rapport à la valeur initiale
|
8,7
-1,61
|
8,6
-2,41
| |
|
Différence:
0,23 [-0,46; 0,91]
| |
Taux d'hypoglycémies (par patient-année d'exposition)
| |
Sévères
|
0,33
|
0,42
| |
Confirmées3
|
39,2
|
44,3
| |
|
Ratio:
0,91 [0,76; 1,09]
| |
Nocturnes confirmées3
|
3,71
|
5,72
| |
|
Ratio:
0,63 [0,49; 0,81]
|
1 Administration une fois par jour + insuline asparte pour couvrir les besoins en insuline liés aux repas
2 Administration une ou deux fois par jour + insuline asparte pour couvrir les besoins en insuline liés aux repas
3 L'hypoglycémie confirmée a été définie comme des épisodes confirmés par un taux de glucose plasmatique <3,1 mmol/l ou par le patient nécessitant une aide extérieure. L'hypoglycémie nocturne confirmée était définie comme des épisodes survenus entre minuit et 6h00.
Évaluation cardiovasculaire
DEVOTE est un essai clinique randomisé en double aveugle comparant la sécurité cardiovasculaire de l'insuline dégludec à celle de l'insuline glargine (100 unités/ml) chez 7637 patients atteints de diabète sucré de type 2 et présentant un risque élevé de manifestations cardiovasculaires. La durée de l'étude était «événementielle», c'est-à-dire jusqu'à ce que les événements ≥633 soient atteints. La durée médiane du traitement était de 1,83 an, la durée d'observation médiane étant de 1,99 an.
L'analyse primaire couvrait la période allant de la randomisation à la première occurrence d'un événement cardiovasculaire indésirable grave (MACE). MACE comportait trois volets: «décès d'origine cardiovasculaire», «crise cardiaque non mortelle» ou «accident vasculaire cérébral non mortel».
Afin d'écarter une augmentation de plus de 30% du risque cardiovasculaire relatif, l'étude a été conçue comme une étude de non-infériorité. La limite supérieure de l'intervalle de confiance (IC) à 95% pour MACE-HR était inférieure à ce seuil prédéfini de 1,3, ce qui démontre l'innocuité cardiovasculaire de l'insuline dégludec par rapport à l'insuline glargine (figure 2).
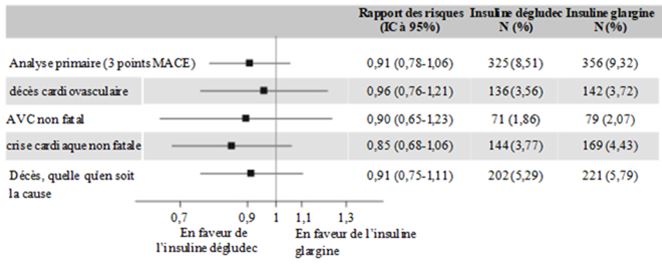
N: nombre de patients ayant eu un premier événement confirmé par l'EAC au cours de l'étude.
%: pourcentage de patients ayant présenté le premier événement confirmé par l'EAC par rapport au nombre de patients randomisés.
EAC: Event Adjudication Commitee.
IC: intervalle de confiance
Figure 2: Diagramme de l'analyse des paramètres combinés MACE à 3 composants et des paramètres cardiovasculaires individuels dans DEVOTE.
L'amélioration de l'HbA1c obtenue avec l'insuline dégludec et l'insuline glargine était également comparable (tableau 5).
Le traitement à l'insuline dégludec a entraîné une réduction du taux d'événements hypoglycémiques sévères et de la proportion de patients présentant au moins une hypoglycémie grave par rapport au traitement avec l'insuline glargine (tableau 4).
Tableau 5: Résultats de DEVOTE
|
|
Insuline dégludec1
|
Insuline glargine1
| |
N
|
3818
|
3819
| |
Valeur HbA1c moyenne (%)
| |
Valeur initiale
|
8.44
|
8.41
| |
Après 2 années de traitement
|
7.50
|
7.47
| |
|
Différence:
0.008 [-0.05; 0.07]IC à 95%
| |
Hypoglycémies (par 100 années-patients d'observation)
| |
Sévères
|
3.70
|
6.25
| |
|
Hazard-Ratio:
0.60 [0.48; 0.76]IC à 95%
| |
Proportion de patients ayant eu une hypoglycémie (pourcentage de patients)
| |
Sévère
|
4.9
|
6.6
| |
|
Rapport des risques:
0.73 [0.60; 0.89]IC à 95%
|
Sécurité et efficacité en pédiatrie
La sécurité et l'efficacité de Ryzodeg ont été étudiées chez des enfants et des adolescents ayant un diabète sucré de type 1 au cours d'une étude clinique randomisée et contrôlée sur une période de 16 semaines (n=362). Les patients du groupe de traitement traité par Ryzodeg étaient 40 enfants âgés de 2 à 5 ans, 61 enfants âgés de 6 à 11 ans et 80 adolescents âgés de 12 à 17 ans. L'administration de Ryzodeg une fois par jour au moment du repas principal en association avec de l'insuline asparte administrée au moment des autres repas a montré une réduction similaire du taux d'HbA1c à la semaine 16 et aucune différence entre la glycémie à jeun et la glycémie mesurée par rapport à l'insuline détémir, administrée une ou deux fois par jour, en association avec de l'insuline asparte administrée au moment des repas. À la semaine 16, la dose quotidienne moyenne d'insuline totale était de 0,88 unité/kg dans le groupe traité avec Ryzodeg contre 1,01 unité/kg dans le groupe traité avec l'insuline détémir. Les taux (d'événements par année-patient d'exposition) d'hypoglycémie confirmée (définition ISPAD [International Society for Child and Adolescent Diabetology] 2009: 46,23 vs 49,55) et d'hypoglycémie confirmée nocturne (5,77 vs 5,40) étaient comparables pour Ryzodeg et l'insuline détémir. Cependant, le taux d'hypoglycémie sévère (0,26 contre 0,07) était numériquement plus élevé chez les patients traités avec Ryzodeg (RC 3,2 [0.88; 11.66]IC à 95%).
Données à long terme
Il n'y a pas de développement cliniquement significatif d'anticorps dirigés contre l'insuline après un traitement à long terme avec Ryzodeg.
Informations complémentaires
Fertilité
Les essais chez l'animal sur la reproduction sous insuline dégludec n'ont pas révélé d'effets négatifs sur la capacité de reproduction.
|


