Propriétés/EffetsCode ATC
C09CA07
Mécanisme d’action
Le telmisartan est un bloqueur efficace par voie orale et spécifique du récepteur de l'angiotensine II (type AT1). Le telmisartan déplace avec une très forte affinité l'angiotensine II de son site de fixation sur le récepteur AT1, responsable des effets connus de l'angiotensine II. Le telmisartan n'a aucun effet agoniste partiel sur le récepteur AT1. Il ne présente aucune affinité notable pour d'autres récepteurs. Il n'inhibe pas la rénine plasmatique humaine et ne bloque pas les canaux ioniques. Le telmisartan n'inhibe pas l'enzyme de conversion de l'angiotensine (kininase II), enzyme également responsable de la dégradation de la bradykinine.
Au cours des essais cliniques, l'incidence de la toux sèche a été nettement moindre chez les patients traités par telmisartan que chez les patients traités par d'autres inhibiteurs de l'ECA. L'incidence de la toux sèche chez les patients traités par telmisartan a été comparable à celle du groupe placebo.
Pharmacodynamique
Traitement de l’hypertension artérielle légère à modérée
Chez l'homme, une dose de 80 mg de telmisartan inhibe presque totalement les augmentations de la pression artérielle engendrée par l'angiotensine II. L'effet inhibiteur se maintient 24 heures et reste mesurable 48 heures après la prise.
Après la première prise, l'effet antihypertenseur se manifeste progressivement au cours des 3 premières heures. En général, la réduction maximale de la pression artérielle est obtenue 4 à 8 semaines après le début du traitement et persiste en cas de traitement au long cours.
Les mesures de la pression artérielle effectuées sur une longue période ont montré que l'effet antihypertenseur est constant au cours des 24 heures suivant l'administration, y compris pendant les 4 dernières heures qui précèdent l'administration suivante. Les rapports pic/vallée mesurés au cours des études cliniques contrôlées contre placebo, uniformément supérieurs à 80% après administration de 40 mg et 80 mg de telmisartan, le confirment.
Chez les patients souffrant d'hypertension artérielle, Telmisartan Spirig HC abaisse la pression artérielle systolique et diastolique sans effet sur la fréquence du pouls. Après interruption du traitement par Telmisartan Spirig HC, la pression artérielle revient progressivement en l'espace de quelques jours à sa valeur initiale. Il n'existe aucun indice de réaction excessive de la pression artérielle après interruption du traitement (rebond).
Dans des études cliniques incluant des patients présentant une hypertension artérielle et une hypertrophie cardiaque gauche, il a été démontré que le traitement par telmisartan est associé à une diminution statistiquement significative de la masse ventriculaire gauche et de l’index de masse ventriculaire gauche.
Réduction du risque d’infarctus du myocarde et d’accident vasculaire cérébral chez des patients présentant un risque cardiovasculaire élevé et/ou un diabète sucré de type 2
Efficacité clinique
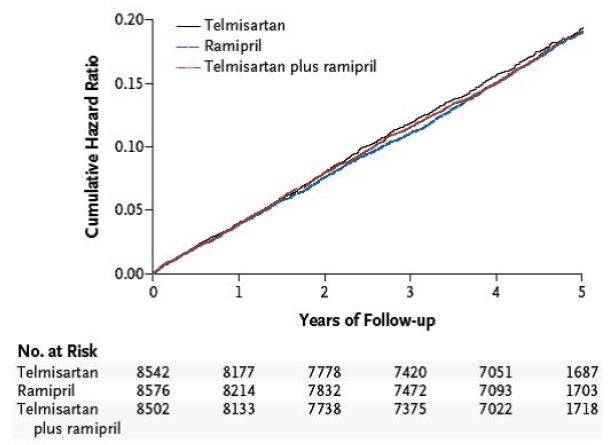
Dans l'étude ONTARGET, une étude clinique comparative, randomisée, en double aveugle, versus l'inhibiteur de l'ECA ramipril, le bloqueur du récepteur de l'angiotensine II telmisartan s'est avéré aussi efficace que le ramipril pour réduire le critère d'évaluation composite primaire (mortalité cardiovasculaire, infarctus du myocarde aigu, accident vasculaire cérébral et hospitalisation pour insuffisance cardiaque) et plusieurs critères d'évaluation secondaires prédéfinis, tout en présentant une meilleure tolérance et une meilleure observance au traitement.
Dans la population globale des patients testés dans l'étude ONTARGET, l'association des deux médicaments n'a pas entraîné de diminution supplémentaire des événements cardiovasculaires, mais le profil d'effets secondaires s'est modifié de manière défavorable, ce qui explique pourquoi l'utilisation d'une association de telmisartan et de ramipril n'est pas recommandée dans cette population.
Dans cette étude incluant à l'échelle mondiale 25'620 patients présentant un risque cardiovasculaire élevé et une tension artérielle normale ou bien contrôlée ont été évalués pendant une période de suivi de 56 mois en moyenne.
Les patients présentant une intolérance aux inhibiteurs de l'ECA ont été exclus de l'étude pendant la phase de screening et une «phase de run-in en simple aveugle» de 28 jours, puis les patients restants ont été randomisés dans l'un des trois bras thérapeutiques suivants:
·8576 patients ont reçu 10 mg de ramipril
·8542 patients ont reçu 80 mg de telmisartan
·8502 patients ont reçu le traitement combiné
La population examinée se composait de 73% d'hommes et 83% des patients étaient hypertendus. Une grande partie des patients avaient déjà été traités avant le début de l'étude par des antiagrégants plaquettaires (80%), des statines (62%), des bêtabloquants (57%), des diurétiques (28%), des bloqueurs du calcium (33%)
Le faible taux de «cas perdus de vue au cours du suivi» (0.19% = 48 patients sur 25'620) montre la qualité élevée des résultats de l'étude.
L’étude TRANSCEND réalisée parallèlement a évalué la réduction du risque du même critère composite primaire, provoquée par 80 mg de telmisartan versus un traitement standard qui pouvait être adapté au cours de l’étude, chez 5 926 patients à risque qui ne se différenciaient de la population de l’étude ONTARGET que par une intolérance à un inhibiteur de l’ECA et une proportion élevée de femmes de 43%.
L’analyse a montré que l’utilisation de telmisartan permettait, malgré un traitement standard optimisé, une réduction du risque de 8% concernant les critères évalués.
Survenue du critère primaire (cumulatif)
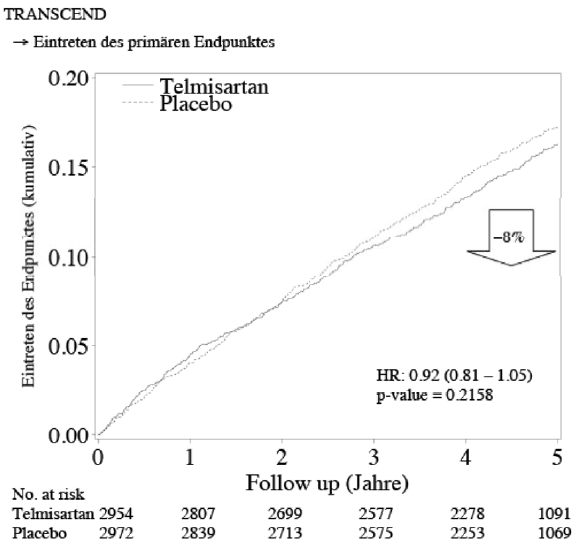
T: telmisartan / Pl: placebo
| 

