CompositionPrincipes actifs
Chlorhydrate de lévométhadone.
Excipients
4-hydroxybenzoate de méthyle (E 218) (1,50 mg par ml solution), chlorhydrate de bétaïne; glycérol 85% (E 422), eau purifiée.
Indications/Possibilités d’emploiEn cas de douleurs aiguës et prolongées d'intensité moyenne à forte ou en cas d'efficacité insuffisante d'analgésiques non opioïdes et/ou d'opioïdes faibles, par exemple en cas de:
·fortes douleurs, coliques néphrétiques et hépatiques, douleurs postopératoires;
·fortes douleurs dues à un ulcère malin.
Traitement de substitution par voie orale en cas de dépendance aux opioïdes, dans le cadre d'une prise en charge médicale, sociale et psychologique.
Posologie/Mode d’emploiSur la base de la masse (mg), la lévométhadone est environ deux fois plus efficace que la méthadone (racémate de lévométhadone et de dextrométhadone). Lors du passage d'un traitement par un racémate de méthadone à un traitement par la lévométhadone, la dose administrée jusqu'à présent doit donc être réduite de moitié.
Traitement des douleurs
Objectifs du traitement et interruption du traitement
Avant de commencer le traitement par L-Polamidon, il convient de convenir avec le patient d'une stratégie de traitement comprenant la durée et les objectifs du traitement, conformément aux directives relatives au traitement de la douleur. Pendant le traitement, un contact régulier entre le médecin et le patient doit être maintenu afin d'évaluer la nécessité de poursuivre le traitement, d'envisager l'arrêt du médicament et, le cas échéant, d'adapter la posologie. Lorsqu'un patient n'a plus besoin du traitement par L-Polamidon, il peut être conseillé de réduire progressivement la dose afin d'éviter les symptômes de sevrage (voir la rubrique «Mises en garde et précautions»). En cas de contrôle insuffisant de la douleur, il convient d'envisager la possibilité d'une accoutumance (tolérance) et d'une progression de la maladie sous-jacente (voir «Mises en garde et précautions»).
Adultes et adolescents de plus de 16 ans
En tant qu'analgésique, L-Polamidon doit être utilisé à la plus petite dose efficace afin d'éviter une dépendance et le développement d'une tolérance. Une adaptation de la dose doit être effectuée chez les patients jeunes et âgés (à partir de 65 ans) ainsi qu'en cas d'administration concomitante de médicaments qui exercent une action inhibitrice sur le système nerveux central. En fonction de la situation individuelle, des doses plus élevées que les doses maximales habituelles peuvent être nécessaires.
Dose unitaire: 1,25-7,5 mg (0,25-1,5 ml de solution buvable), jusqu'à trois fois par jour si nécessaire.
Dose unitaire maximale: 10 mg (2 ml de solution buvable).
Dose journalière maximale habituelle: 30 mg (6 ml de solution buvable).
Passage d'autres opioïdes puissants à L-Polamidon
Les recommandations disponibles dans les guides cliniques en ce qui concerne le passage d'un traitement par un opioïde administré par voie orale ou parentérale à un traitement par L-Polamidon ne peuvent servir que de points de repère étant donné que leur dosage relatif peut varier d'un patient à un autre. En principe, les besoins en L-Polamidon d'un patient sur 24 heures doivent être définis à un niveau plutôt plus bas. En règle générale, on commence par la moitié de la dose journalière estimée, puis on augmente la dose au cas par cas et sous surveillance médicale.
Traitement de substitution en cas de dépendance aux opioïdes
Adultes et adolescents de plus de 16 ans
L'expérience montre que ces patients ont besoin d'une surveillance et d'un soutien attentifs. Pour des raisons de sécurité, il est recommandé d'administrer le médicament chaque jour sous surveillance au cabinet médical et de ne délivrer L-Polamidon si possible que sous une forme prête à boire et pour une courte durée.
De plus, il convient d'attirer l'attention sur les risques liés à l'association avec d'autres drogues et/ou de l'alcool.
Afin d'évaluer les interactions possibles et la posologie nécessaire de L-Polamidon, la consommation supplémentaire d'autres substances psychotropes doit être abordée avec le patient au début et au cours du traitement de substitution. L'attention du patient doit être attirée sur les dangers d'une telle consommation (voir également «Interactions»).
En particulier pendant les cinq premiers jours de la phase d'induction du traitement, la prise de L-Polamidon doit être étroitement contrôlée ou avoir lieu sous surveillance visuelle. Commencer le traitement au début de la semaine évite d'avoir à interrompre la surveillance pendant le week-end au cours de la phase d'induction du traitement.
Instauration du traitement chez les patients dépendants aux opioïdes non préalablement traités
Commencer la substitution par L-Polamidon à la dose suivante:
·10 mg (2 ml de solution buvable) une fois par jour,
·en cas de tolérance élevée, 15 mg (3 ml de solution buvable) une fois par jour,
·en cas de tolérance incertaine, 5-7,5 mg (1-1,5 ml de solution buvable) une fois par jour.
En cas de suspicion d'une tolérance élevée aux opioïdes ou d'un métabolisme rapide, le patient peut être convoqué une nouvelle fois quatre heures après; en présence de symptômes de sevrage clairs, il est alors possible d'administrer une dose supplémentaire jusqu'à 10 mg (soit 2 ml de solution buvable).
L'augmentation quotidienne de la dose ne doit pas être supérieure à 2,5-5 mg (0,5-1 ml de solution buvable). Les principaux symptômes pour une augmentation de dose sont les symptômes de sevrage objectifs et subjectifs et la consommation supplémentaire d'opioïdes. En cas de signes d'intoxication, la dose doit immédiatement être réduite.
La dose journalière, qui doit être déterminée en se basant sur les paramètres cliniques, est au moins de 30-40 mg (6-8 ml de solution buvable) une fois par jour, sachant qu'il est possible que des posologies plus faibles soient suffisantes ou que des doses élevées supérieures à 60 mg (supérieures à 12 ml de solution buvable) une fois par jour soient nécessaires.
Instauration du traitement chez les patients dépendants aux opioïdes qui ont déjà été traités au préalable
Le passage d'un traitement de substitution en cours à L-Polamidon doit avoir lieu du jour au lendemain.
En traitement de substitution, la lévométhadone est en moyenne environ 12-16 fois plus efficace que la morphine, sachant que la posologie nécessaire doit toujours être déterminée au cas par cas en se basant sur les paramètres cliniques, en partant de la plus petite dose efficace et en tenant compte des symptômes de sevrage et d'intoxication.
La longue demi-vie de la lévométhadone, variable selon le nombre de doses, doit également être prise en considération.
En cas d'ajustement dans une faible plage de doses, il convient de passer à une dose de lévométhadone correspondant à la moitié de la dose calculée, et d'augmenter la dose au cas par cas.
En cas de besoin et de bonne tolérance du traitement, la dose doit être augmentée progressivement jusqu'à ce que la dose journalière optimale soit atteinte.
Lors du passage d'un traitement par la buprénorphine ou la diamorphine à L-Polamidon, la posologie adéquate doit être déterminée en se basant sur les paramètres cliniques.
Poursuite du traitement
Une fois l'état psychique et physique du patient stabilisé, le traitement doit être poursuivi en conservant la posologie adaptée, qui pourra être ajustée en fonction du tableau clinique.
En cas d'interruption du traitement pendant une journée, aucune adaptation de la dose n'est nécessaire. En revanche, en cas d'interruption des prises pendant une plus longue période, la dose suivante doit être réduite proportionnellement, de manière à revenir à une dose initiale de 15 mg (3 ml de solution buvable) après cinq jours d'interruption. La dose doit ensuite être augmentée progressivement jusqu'à l'atteinte de la dose journalière optimale, comme lors de l'instauration du traitement sans traitement préalable.
Si l'arrêt du traitement de substitution est prévu, la dose doit être réduite progressivement sur plusieurs semaines, voire sur plusieurs mois, selon l'état du/de la patient(e) et l'apparition d'éventuels symptômes de sevrage. La dose journalière de L-Polamidon peut être réduite de 2,5 mg (0,5 ml de solution buvable) par semaine. En cas de doses quotidiennes inférieures à 10-15 mg (2-3 ml de solution buvable), des réductions de dose hebdomadaires inférieures sont recommandées. Les réductions de la dose ne doivent intervenir que lorsque les éventuels troubles apparus à la suite de la réduction précédente ont disparu (voir également «Mises en garde et précautions»).
Instructions spéciales pour la posologie
Enfants et adolescents de moins de 16 ans
Traitement des douleurs
Faute d'expérience, l'utilisation de L-Polamidon pour traiter la douleur chez l'enfant et l'adolescent de moins de 16 ans est déconseillée.
Traitement de substitution en cas de dépendance aux opioïdes
On ne dispose d'aucune donnée sur l'innocuité et l'efficacité de L-Polamidon pour le traitement de substitution chez l'enfant et l'adolescent de moins de 16 ans dépendants aux opioïdes.
L'âge du patient ne doit toutefois pas constituer un critère d'exclusion pour l'instauration d'un traitement de substitution. Le traitement de substitution doit être mis en place conformément aux recommandations pour l'adulte, en augmentant la dose progressivement et avec prudence, et en gardant le patient sous étroite surveillance.
Patients âgés
Chez les patients âgés (à partir de 65 ans), il convient généralement d'opter pour une posologie plus faible (voir «Pharmacocinétique»).
Patients présentant des troubles de la fonction hépatique ou de la fonction rénale
Chez les patients atteints d'insuffisance hépatique ou rénale, il convient généralement d'opter pour une posologie plus faible (voir «Pharmacocinétique»).
Mode d'administration
La solution buvable ne doit être utilisée que par voie orale. En général, la solution est prise dans au moins 100 ml d'eau ou de jus de fruit (p.ex. jus d'orange, sirop de framboise).
Le prélèvement de la dose individuelle du flacon de 100 ml se fait de façon volumétrique par l'insert conique de Luer, à l'aide d'une seringue à usage unique graduée adaptée, telle qu'on en trouve dans le commerce.
Dans le flacon en verre de 500 ml, le prélèvement peut se faire en pharmacie via un dispositif de distribution calibré disponible dans le commerce par exemple.
Autres remarques relatives à la remise et aux préparations, voir «Remarques particulières».
Contre-indications·Hypersensibilité à la lévométhadone ou à l'un des excipients conformément à la composition
·Dépression respiratoire significative.
·Asthme bronchique aigu ou sévère dans un contexte sans surveillance médicale ou sans équipement de réanimation.
·Obstruction ou paralysie abdominale aiguë.
·Insuffisance hépatique sévère ou cirrhose du foie avec insuffisance rénale concomitante.
·Prise d'inhibiteurs de la monoamine oxydase de manière concomitante ou dans les deux semaines suivant leur arrêt (voir «Interactions»).
·Utilisation concomitante d'antagonistes ou agonistes partiels des récepteurs opioïdes µ (p.ex. buprénorphine), sauf pour le traitement d'un surdosage.
·L-Polamidon ne doit pas être utilisé pendant la grossesse et la période d'allaitement pour le traitement de la douleur (voir «Grossesse, Allaitement»).
Mises en garde et précautionsIl convient de noter que sur la base de la masse (mg), la lévométhadone est environ deux fois plus efficace que la méthadone (racémate de lévométhadone et de dextrométhadone).
Une indication stricte et une surveillance médicale particulière sont nécessaires dans les cas suivants:
·tableaux cliniques pour lesquels il convient de prévenir une dépression du centre respiratoire,
·altération modérée à sévère du centre respiratoire et de la fonction respiratoire.
·asthme bronchique, broncho-pneumopathie chronique obstructive, cœur pulmonaire, réserve respiratoire fortement diminuée, p.ex. en cas d'obésité grave, atteinte préexistante de la fonction respiratoire, hypoxie ou hypercapnie, syndrome obstructif des apnées du sommeil (SAOS),
·états de conscience réduits, p.ex. après intoxication alcoolique aiguë,
·hypertension intracrânienne, p.ex. après un traumatisme crânien, augmentation de la pression du liquide céphalorachidien du fait de la propriété des opioïdes.
·hypotension en cas d'hypovolémie,
·bradycardie,
·phéochromocytome,
·hypertrophie de la prostate avec formation d'urine résiduelle,
·pancréatite,
·affections des voies biliaires,
·affections intestinales inflammatoires,
·hypothyroïdie,
·grossesse et allaitement pendant le traitement de substitution (voir «Contre-indications» et «Grossesse, Allaitement»).
Il est recommandé de réduire la posologie chez les patients atteints de maladies rénales (taux de filtration glomérulaire < 90 ml/min/1,73 m2) ou de maladies hépatiques chroniques sévères (à partir du stade C selon l'échelle de Child-Pugh [10-15 points]), chez les patients âgés (à partir de 65 ans) ou encore chez les patients présentant un état général réduit (voir «Pharmacocinétique»).
Développement d'une tolérance, dépendance aux médicaments et potentiel d'abus
La lévométhadone est un analgésique opioïde et présente elle-même un fort potentiel de dépendance. Elle a une longue demi-vie et peut donc s'accumuler. Une dose unique qui soulage les symptômes peut entraîner, en cas de prise quotidienne répétée, une accumulation et éventuellement entraîner la mort.
Comme pour les autres opioïdes, une accoutumance et une dépendance physique et/ou psychique peuvent se développer en cas d'utilisation répétée de lévométhadone. Lors du traitement de douleurs, la prise répétée de L-Polamidon peut entraîner un trouble lié à l'utilisation d'opioïdes (TUO). Une dose élevée et un traitement prolongé avec des opioïdes peuvent augmenter le risque de développer un trouble lié à l'utilisation d'opioïdes. Avant le début du traitement par L-Polamidon et pendant le traitement, il convient de convenir avec le patient d'objectifs de traitement et d'un plan d'arrêt du médicament (voir «Posologie/Mode d'emploi»). Avant et pendant le traitement, le patient doit en outre être informé des risques et des signes d'un trouble lié à l'utilisation des opioïdes. Les patients doivent être informés de consulter leur médecin si ces signes apparaissent. L'abus ou la mauvaise utilisation intentionnelle de L-Polamidon peut entraîner un surdosage et/ou la mort. Le risque de développer un trouble lié à l'utilisation d'opioïdes est plus élevé chez les patients ayant des antécédents personnels ou familiaux (parents ou frères et sœurs) de troubles liés à l'utilisation de substances (y compris les troubles liés à la consommation d'alcool), chez les fumeurs ou chez les patients ayant des antécédents d'autres maladies mentales (par ex. dépression majeure, anxiété et troubles de la personnalité). Les patients doivent être surveillés afin de détecter tout signe de comportement addictif (drug-seeking behavior) (p.ex. demande trop précoce d'ordonnances de renouvellement). Cela inclut la vérification de la prise simultanée d'opioïdes et de médicaments psychoactifs (comme les benzodiazépines). Pour les patients présentant des signes et des symptômes de troubles liés à l'utilisation d'opioïdes, il convient d'envisager la consultation d'un spécialiste des addictions.
Dépression respiratoire
Comme pour tous les autres opioïdes, l'utilisation de L-Polamidon est associée à un risque de dépression respiratoire cliniquement pertinente. La dépression respiratoire, si elle n'est pas reconnue et traitée immédiatement, peut entraîner un arrêt respiratoire et la mort. Le traitement d'une dépression respiratoire comprend, selon l'état clinique du patient, une surveillance étroite, des mesures de soutien et l'administration d'antagonistes des opioïdes. Une dépression respiratoire grave, potentiellement mortelle ou fatale, peut survenir à tout moment du traitement, le risque étant maximal au début du traitement ou après une augmentation de dose.
Chez les patients présentant une prédisposition atopique, une exacerbation d'un asthme déjà existant, des éruptions cutanées et des modifications de la formule sanguine (éosinophilie) peuvent survenir.
Troubles respiratoires liés au sommeil
Les opioïdes peuvent provoquer des troubles respiratoires liés au sommeil, y compris l'apnée centrale du sommeil (ACS) et l'hypoxémie liée au sommeil. L'utilisation d'opioïdes s'accompagne d'une augmentation dose-dépendante du risque d'apnée centrale du sommeil. Chez les patients souffrant d'apnée centrale du sommeil, une réduction de la dose totale d'opioïdes doit être envisagée.
Utilisation simultanée avec des substances à action dépressive centrale
L'utilisation simultanée d'opioïdes avec des benzodiazépines ou d'autres substances à action dépressive centrale peut renforcer la sédation, et entraîner la dépression respiratoire, le coma et la mort. En raison de ces risques, les opioïdes et les benzodiazépines ou d'autres médicaments à action dépressive centrale ne doivent être administrés de manière concomitante qu'aux patients pour lesquels aucune autre option de traitement n'est envisageable. S'il est décidé de prescrire du L-Polamidon en association avec des benzodiazépines ou d'autres médicaments à action dépressive centrale, il convient de choisir la dose efficace la plus faible et une durée minimale d'utilisation simultanée. Les signes et symptômes de dépression respiratoire et de sédation doivent être surveillés étroitement. (voir «Interactions»)
Exposition accidentelle
Les patients et les personnes qui s'en occupent doivent être informés que L-Polamidon contient une substance active en quantité susceptible d'entraîner la mort, en particulier chez les enfants. Les patients et les personnes qui s'en occupent doivent être informés de la nécessité de conserver toutes les doses unitaires hors de portée des enfants et d'éliminer correctement les doses unitaires entamées ou non utilisées.
Syndrome de sevrage néonatal aux opioïdes
L'utilisation prolongée de L-Polamidon pendant la grossesse peut entraîner un syndrome de sevrage néonatal aux opioïdes, qui peut potentiellement mettre la vie en danger lorsqu'il n'est pas identifié et traité en temps opportuns. Le traitement doit être effectué selon les protocoles développés par des experts en néonatologie. Si l'utilisation d'opioïdes chez une femme enceinte est nécessaire pendant une période prolongée, informez la patiente du risque de syndrome de sevrage néonatal aux opioïdes et assurez-vous que le traitement adéquat est disponible le cas échéant.
Insuffisance surrénalienne
Les opioïdes peuvent provoquer une insuffisance surrénalienne réversible qui nécessite une surveillance et un traitement de substitution par glucocorticoïdes. Les symptômes de l'insuffisance surrénalienne peuvent notamment comprendre les suivants: nausée, vomissement, perte d'appétit, fatigue, faiblesse, vertige ou tension artérielle basse.
Diminution des hormones sexuelles et augmentation de la prolactine
L'utilisation à long terme d' opioïdes peut être associée à une baisse des taux d'hormones sexuelles et à une augmentation des taux de prolactine. Les symptômes incluent une baisse de la libido, l'impuissance ou l'aménorrhée.
Hypoglycémie
Des cas d'hypoglycémie ont été observés en lien avec un surdosage ou une augmentation de la dose de méthadone. En cas d'augmentation de la dose, une surveillance régulière de la glycémie est recommandée.
Spasme du sphincter d'Oddi/pancréatite
Les opioïdes peuvent entraîner un dysfonctionnement et un spasme du sphincter d'Oddi, ce qui augmente la pression intrabiliaire et accorît le risque de symptômes des voies biliaires et de pancréatite.
Troubles du rythme cardiaque
Un allongement de l'intervalle QT à l'ECG et des arythmies ventriculaires pouvant mettre en jeu le pronostic vital (torsades de pointes) ont été observés dans de rares cas avec de la méthadone à doses élevées (racémate de lévométhadone et de dextrométhadone). Les patients doivent avoir pour instruction de contacter immédiatement leur médecin en cas d'apparition de syncopes, d'épisodes de vertiges inhabituels ou de palpitations.
Dans les situations suivantes, le risque de troubles du rythme cardiaque est accru et le bénéfice thérapeutique doit être évalué soigneusement:
·Prolongation congénitale de l'intervalle QT, arythmies ventriculaires significatives, bradycardie cliniquement significative, insuffisance cardiaque cliniquement significative avec réduction de la fraction d'éjection ventriculaire gauche.
·Troubles électrolytiques (hypokaliémie, hypomagnésémie) et situations qui favorisent ces troubles (p.ex. vomissements ou diarrhées persistants, traitement diurétique).
·Utilisation concomitante d'antiarythmiques de classe IA et III et autres médicaments prolongeant l'intervalle QT (voir «Interactions»).
·Utilisation concomitante de médicaments qui peuvent inhiber le métabolisme de la lévométhadone (voir «Interactions»).
Dans ces situations, il convient de procéder à un examen clinique et si possible à un ECG avant et deux semaines après le début du traitement par L-Polamidon, en cas d'augmentation de la dose et une fois par an. En cas de symptômes d'origine inconnue, la possibilité d'une cause cardiaque doit être envisagée. Si d'autres médicaments doivent être modifiés, il convient de tenir compte des éventuelles interactions pouvant influer sur l'intervalle QT.
Potentiel d'abus
L-Polamidon est exclusivement destiné à une administration par voie orale. L'administration abusive par voie intraveineuse de L-Polamidon peut entraîner des effets indésirables sévères, éventuellement d'issue fatale, tels que septicémie, inflammations des veines ou embolies pulmonaires.
Contrôle antidopage
L'utilisation de L-Polamidon peut induire une réaction positive lors de contrôles antidopage. De plus, l'utilisation de L-Polamidon comme produit dopant peut entraîner des risques pour la santé.
Traitement de la douleur
Hyperalgésie
L'hyperalgésie induite par les opioïdes (HIO) se présente lorsqu'un analgésique opioïde provoque paradoxalement une augmentation de la douleur ou une augmentation de la sensibilité à la douleur. Cet état diffère de la tolérance, dans laquelle des doses plus élevées d'opioïdes sont nécessaires pour maintenir un effet donné. Les symptômes de l'HIO comprennent notamment une augmentation de la douleur en cas d'augmentation de la dose d'opioïdes, une diminution de la douleur en cas de diminution de la dose d'opioïdes ou une douleur en cas de stimuli normalement non douloureux (allodynie). Si l'on soupçonne une HIO chez un patient, il convient d'envisager une réduction de la dose d'opioïdes ou une rotation des opioïdes.
Traitement de substitution en cas de dépendance aux opioïdes
Risques particuliers chez les patients sous traitement de substitution
La prise de doses élevées de L-Polamidon par des personnes intolérantes aux opioïdes est dangereuse pour la santé et peut entraîner la mort par arrêt respiratoire (voir également «Surdosage»).
Il convient d'expliquer au patient qu'en raison d'une potentialisation de la dépression respiratoire, la consommation concomitante d'opioïdes illégaux, de benzodiazépines, d'alcool ou d'autres substances ou médicaments déprimant le système nerveux central peut entraîner la mort par paralysie respiratoire (voir «Interactions»). Disposer d'informations sur tous les psychotropes consommés actuellement et dans le passé et sur l'ensemble des médicaments pris par le patient est essentiel pour pouvoir évaluer les interactions potentielles.
En cas de traitement de substitution, il convient de surveiller particulièrement l'apparition de symptômes suggérant un surdosage et de symptômes de sevrage. Les patients doivent donc faire l'objet d'une surveillance médicale étroite et la posologie doit être ajustée en conséquence s'il y a lieu (voir «Posologie/mode d'emploi»). Le patient ne peut renoncer à la consommation supplémentaire d'opioïdes qu'en l'absence de symptômes de sevrage.
Lors de l'arrêt du traitement de substitution, il est indiqué de réduire lentement la dose sur plusieurs semaines, voire sur plusieurs mois (voir «Posologie/mode d'emploi»). Le patient doit être informé de la perte de tolérance et du risque accru de surdosage en cas de reprise de la consommation d'opioïdes.
Traitement de la douleur et traitement de substitution concomitants
En principe, la douleur doit être traitée conformément au schéma de l'Organisation mondiale de la Santé (OMS). En raison de la tolérance croisée à l'action analgésique des opioïdes, ces derniers doivent généralement être administrés à une posologie élevée pour obtenir une absence de douleurs. La posologie du traitement de substitution doit être conservée, sans être réduite.
Les troubles addictifs peuvent favoriser une hyperalgésie.
InteractionsInteractions pharmacodynamiques
L'utilisation concomitante d'autres médicaments affectant le SNC, tels que d'autres opioïdes, des sédatifs tels que les benzodiazépines ou les hypnotiques, les anesthésiques généraux, les phénothiazines, les tranquillisants, les relaxants de la musculature squelettique, les anti-histaminiques sédatifs, les gabapentinoïdes (gabapentine et prégabaline) et l'alcool, peut produire des effets dépresseurs effets additifs, entraînant une dépression respiratoire, une hypotension, une forte sédation ou un coma, parfois fatal (voir «Mises en garde et précautions»).
L-Polamidon n'est pas indiqué en association avec des IMAO ou dans un intervalle de 14 jours après l'arrêt d'un tel traitement (voir également «Contre-indications»).
En cas de prise concomitante de médicaments prolongeant l'intervalle QTc, le risque d'arythmie est accru (voir «Mises en garde et précautions» et «Propriétés/Effets»):
antiarythmiques des classes IA (par ex. quinidine, disopyramide, procaïnamide) et III (p.ex. amiodarone, sotalol), certains neuroleptiques (p.ex. phénothiazine, thioridazine), certains antidépresseurs, certains antimicrobiens (moxifloxacine, sparfloxacine, érythromycine i.v., pentamidine, antipaludéens, en particulier halofantrine), certains antihistaminiques (mizolastine), autres (cisapride, vincamine i.v.)(voir aussi «Mises en garde et précautions»).
L'utilisation concomitante d'agonistes partiels des récepteurs opioïdes µ (p.ex. buprénorphine) peut réduire l'efficacité de la lévométhadone et éventuellement entraîner des manifestations de sevrage. La buprénorphine doit être administrée au plus tôt 20 heures après l'arrêt de L-Polamidon.
L'effet antihypertensif éventuel de la lévométhadone peut être renforcé par des antihypenseurs tels que la clonidine, l'urapidil et la prazosine.
Un syndrome sérotoninergique peut survenir en cas d'administration simultanée d'opioïdes avec des inhibiteurs de la monoamine oxydase (IMAO) et des agents sérotoninergiques, tels que les inhibiteurs sélectifs de la recapture de la sérotonine (ISRS), les inhibiteurs de la recapture de la sérotonine et de la norépinéphrine (IRSN) et les antidépresseurs tricycliques. Les symptômes d'un syndrome sérotoninergique peuvent inclure des modifications de l'état de conscience, une instabilité autonome, des anomalies neuromusculaires et/ou des symptômes gastro-intestinaux.
Interactions pharmacocinétiques
Il convient de surveiller attentivement les patients en cas d'administration concomitante de lévométhadone et d'autres médicaments ou substances qui sont métabolisés par des enzymes hépatiques ou peuvent influer sur la liaison protéique (la lévométhadone se lie principalement à l'alpha-glycoprotéine acide et à l'albumine, voir «Pharmacocinétique») ainsi qu'après l'arrêt de ces médicaments ou substances, afin de détecter les symptômes cliniques de surdosage, de sous-dosage ou de sevrage. Un ajustement posologique correspondant est recommandé.
La concentration plasmatique de la lévométhadone peut être accrue et la durée d'action prolongée par des médicaments ou substances inhibant la dégradation enzymatique de la lévométhadone dans le foie (système des cytochromes P450), p.ex.:
·la cimétidine,
·les antifongiques azolés (p.ex. fluconazole, itraconazole, voriconazole),
·les macrolides (p.ex. érythromycine, clarithromycine),
·les antiarythmiques (via CYP3A4: amiodarone, lidocaïne; via CP2D6: flécaïnide, propafénone),
·les antidépresseurs de la classe des inhibiteurs de la recapture de la sérotonine, p.ex. sertraline, fluvoxamine, fluoxétine et paroxétine,
·la ciprofloxacine,
·l'amitriptyline,
·le cannabidiol.
Chez l'homme, la lévométhadone est N-déméthylée par plusieurs isoenzymes CYP, les enzymes CYP3A4, CYP2B6, CYP2C19 et CYP2D6 jouant un rôle important. La concentration plasmatique de la lévométhadone peut être réduite et la durée d'action raccourcie par des médicaments ou substances stimulant la dégradation enzymatique de la lévométhadone dans le foie (inducteurs enzymatiques). Aussi peut-on s'attendre à des manifestations de sevrage lors de l'utilisation concomitante de lévométhadone et de:
·carbamazépine,
·phénobarbital,
·phénytoïne,
·rifampicine,
·millepertuis,
·acide fusidique,
·spironolactone,
·névirapine,
·éfavirenz,
·inhibiteurs de protéase du VIH (fosamprénavir, ritonavir, nelfinavir),
·contraceptifs (œstrogènes),
·métamizole.
Dans le cadre de l'administration concomitante de méthadone (en tant que racémate de méthadone) et d'antirétroviraux, il été décrit que la concentration plasmatique des antirétroviraux était soit réduite (didanosine et stavudine), soit augmentée (zidovudine), sans changement de la concentration plasmatique de méthadone. Ces patients doivent faire l'objet d'une surveillance étroite pour obtenir la réponse clinique adéquate au traitement par la lévométhadone et détecter les signes de toxicité du médicament.
Grossesse, allaitementGrossesse
Des études expérimentales chez l'animal avec la méthadone (racémate de lévométhadone et de dextrométhadone) ont montré une toxicité sur la reproduction (voir «Données précliniques»).
La méthadone et la lévométhadone passent la barrière placentaire.
Les études épidémiologiques sur le risque de malformations cardiaques et d'autres malformations congénitales chez les enfants exposés à la méthadone dans l'utérus sont contradictoires et insuffisantes pour établir un lien de cause à effet entre la prise de méthadone pendant la grossesse et le risque de malformations cardiaques et d'autres malformations congénitales.
L'utilisation prolongée de L-Polamidon pendant la grossesse peut entraîner un syndrome de sevrage néonatal aux opioïdes, qui peut potentiellement mettre la vie en danger lorsqu'il n'est pas identifié et traité en temps opportuns. Le traitement doit être effectué selon les protocoles développés par des experts en néonatologie. Si l'utilisation d'opioïdes chez une femme enceinte est nécessaire pendant une période prolongée, informez la patiente du risque de syndrome de sevrage néonatal aux opioïdes et assurez-vous que le traitement approprié est disponible, le cas échéant (voir aussi «Mises en garde et précautions»).
Traitement de la douleur
L-Polamidon ne doit pas être utilisé pendant la grossesse pour le traitement de la douleur (voir «Contre-indications»).
Traitement de substitution en cas de dépendance aux opioïdes
Chez les femmes enceintes dépendantes aux opioïdes, l'instauration ou la poursuite d'un traitement de substitution est recommandée. Une substitution adaptée pour éviter des symptômes de sevrage limite l'ampleur des dommages pour le fœtus.
Du fait des modifications physiologiques pendant la grossesse (voir «Pharmacocinétique»), il peut être nécessaire d'augmenter la dose ou de fractionner la dose journalière.
Allaitement
La lévométhadone est excrétée en faibles quantités dans le lait maternel.
En ce qui concerne la méthadone (racémate de lévométhadone et de dextrométhadone), des effets indésirables, notamment une dépression respiratoire et des troubles de la conscience pouvant être fatals, ont été rapportés chez les nourrissons qui ont ingéré de la méthadone dans le lait maternel. Les facteurs observés susceptibles d'y avoir contribué sont l'utilisation de substances à effet dépresseur sur le SNC, la constitution génétique et le surdosage.
Traitement de la douleur
L-Polamidon ne doit pas être utilisé pendant la période d'allaitement pour le traitement de la douleur (voir «Contre-indications»).
Traitement de substitution en cas de dépendance aux opioïdes
Pendant le traitement par la lévométhadone, il convient d'éviter d'allaiter. Si la mère a été traitée avec de la lévométhadone jusqu'à la fin de sa grossesse, l'allaitement peut être envisagé pour atténuer un syndrome de sevrage néonatal. Pour décider si l'allaitement peut être recommandé sous lévométhadone, il convient de demander conseil à un spécialiste clinique. Par ailleurs, il faut savoir si la femme prend une dose d'entretien de lévométhadone stable et si elle continue de consommer une substance illégale. Si l'allaitement est envisagé, la dose de lévométhadone définie doit être aussi faible que possible. Les médecins prescripteurs doivent demander à la femme allaitante de surveiller toute sédation et tout problème respiratoire chez son enfant et, le cas échéant, de consulter un médecin sans attendre. Bien que la quantité de lévométhadone qui passe dans le lait maternel ne suffise pas pour réprimer complètement les manifestations de sevrage chez les nourrissons allaités, elle peut atténuer la sévérité d'un syndrome de sevrage néonatal. S'il est nécessaire d'arrêter l'allaitement, il convient de le faire progressivement, car un sevrage soudain pourrait aggraver les symptômes de sevrage du nourrisson.
Effet sur l’aptitude à la conduite et l’utilisation de machinesL-Polamidon a une influence importante sur l'aptitude à la conduite ou l'utilisation de machines, particulièrement en début de traitement, après augmentation du dosage ou passage à L-Polamidon, ou en cas d'association avec l'alcool ou des substances à effet dépresseur sur le SNC. De ce fait, les patients doivent demander l'avis de leur médecin avant de conduire ou d'utiliser des machines.
Effets indésirablesLes fréquences sont classées comme suit: «fréquents» (≥1/100, <1/10), «occasionnels» (≥1/1'000, <1/100), «rares» (≥1/10'000, <1/1'000), «très rares» (<1/10'000), «fréquence inconnue» (fréquence non estimable sur la base des données disponibles).
Affections hématologiques et du système lymphatique
Rare: lors d'une utilisation de longue durée, lymphocytose, hyperalbuminémie, hyperglobulinémie.
Affections du système immunitaire
Fréquence inconnue: réactions d'hypersensibilité pouvant aller jusqu'au choc.
Troubles du métabolisme et de la nutrition
Fréquence inconnue: perte d'appétit, hypoglycémie.
Affections psychiatriques
Occasionnel: agitation, dysphorie, euphorie.
Fréquence inconnue: confusion, désorientation, insomnie, dépendance aux médicaments.
Affections du système nerveux
Occasionnel: somnolence, sédation, nervosité, vertiges.
Fréquence inconnue: étourdissements, céphalées, convulsions.
Affections oculaires
Fréquence inconnue: troubles de la vision, myosis.
Affections cardiaques
Occasionnel: hypotension.
Rare: prolongation de l'intervalle QT à l'ECG / arythmies ventriculaires (syncopes), torsades de pointes (voir «Mises en garde et précautions»).
Fréquence inconnue: insuffisance cardiovasculaire, palpitations, bradycardie, arrêt cardiaque.
Affections vasculaires
Fréquence inconnue: hypotension orthostatique.
Choc, saignements diffus (hémorragies).
Affections respiratoires, thoraciques et médiastinales
Occasionnel: dépression respiratoire, œdème pulmonaire non cardiogénique chez des patients traités en soins intensifs.
Fréquence inconnue: arrêt respiratoire, syndrome d'apnée centrale du sommeil.
Affections gastro-intestinales
Fréquent: nausées, vomissements, constipation.
Fréquence inconnue: sécheresse buccale, pancréatite.
Affections hépatobiliaires
Occasionnel: spasmes du sphincter d'Oddi, coliques hépatiques.
Affections de la peau et du tissu sous-cutané
Occasionnel: hyperhydrose.
Fréquence inconnue: urticaire, rash, prurit.
Affections du rein et des voies urinaires
Occasionnel: rétention urinaire.
Fréquence inconnue: diminution du volume urinaire.
Affections des organes de reproduction et du sein
Fréquent: diminution de la libido, troubles érectiles en cas d'utilisation prolongée.
Très rare: hyperprolactinémie.
Troubles généraux
Fréquence inconnue: Fatigue, accès de faiblesse, œdèmes, flush.
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageComme pour tous les opioïdes, il existe un risque élevé d'intoxication et de surdosage chez les personnes non habituées aux opioïdes.
Signes et symptômes
Les symptômes aigus sont notamment: myosis, dépression respiratoire, somnolence pouvant évoluer vers un état de stupeur ou un coma. D'autres symptômes possibles sont les nausées, les vomissements, l'hypotension, la bradycardie, le prolongement de l'intervalle QT, les arythmies, la diminution du tonus musculaire et l'atonie intestinale. Des cas d'hypoglycémie ont été rapportés. Les cas de surdosage sévère peuvent entraîner un arrêt respiratoire, un œdème pulmonaire non cardiogénique, une insuffisance circulatoire, voire le décès.
Une leucoencéphalopathie toxique a été observée en cas de surdosage des opioïdes.
Traitement de substitution en cas de dépendance aux opioïdes
Dans le cadre d'un traitement de substitution, des intoxications mixtes, notamment par benzodiazépines, alcool et cocaïne, peuvent survenir et masquer les symptômes typiques d'une intoxication due à la lévométhadone. Pour cette raison, il convient de surveiller les symptômes au moment du diagnostic.
Traitement
Il convient de surveiller la respiration et l'état de conscience; en cas de dépression respiratoire ou du SNC cliniquement significative: pratiquer la respiration artificielle, stabiliser la circulation et administrer la naloxone.
Posologie: 0,4-2 mg de naloxone par voie intraveineuse (chez l'enfant: 0,01-0,1 mg/kg de poids corporel).
Si nécessaire, répéter l'opération toutes les deux à trois minutes à deux ou trois reprises ou administrer une perfusion continue (voir information professionnelle correspondante). Dans le cadre du traitement de substitution, une application intramusculaire ou intranasale peut s'avérer nécessaire en raison de veines en mauvais état ou bouchées.
La durée d'action de la naloxone est relativement courte (demi-vie plasmatique: t½ de la naloxone = 1-1,5 heure, t½ de la lévométhadone = 16-53 heures); la dépression respiratoire peut être durable. Par conséquent, le patient doit être surveillé de manière prolongée même après administration de naloxone, et des administrations répétées de naloxone peuvent être nécessaires.
La naloxone doit être utilisée avec précaution chez les personnes susceptibles de prendre des opioïdes depuis longtemps (tolérance). La suppression soudaine ou totale de l'effet des opioïdes peut entraîner un syndrome de sevrage aigu. Une dose initiale de 0,04 mg de naloxone est recommandée.
Dans des cas spécifiques, on peut envisager après la prise une désintoxication primaire avec du charbon actif.
Propriétés/EffetsCode ATC
N02AC06
Mécanisme d'action
La lévométhadone est l'énantiomère R(–) actif de la méthadone.
La lévométhadone appartient au groupe des analgésiques très puissants de type morphinique. La méthadone se lie sélectivement aux récepteurs opioïdes (notamment agoniste des récepteurs μ) dans le cerveau.
Pharmacodynamique
La lévométhadone régule la conduction de la douleur et la perception de la douleur en stimulant le système endogène inhibiteur de la douleur. Les effets centraux sont en outre la sédation, la dépression respiratoire, l'inhibition du centre de la toux, le rétrécissement des pupilles, les vomissements et l'antidiurèse. En périphérie, le tonus des muscles lisses est accru, ce qui inhibe la vidange de l'estomac, de la vésicule biliaire et de la vessie et ralentit le transit intestinal.
En tant qu'agoniste des opioïdes, la lévométhadone produit des effets de type morphinique qui répriment les symptômes de sevrage lors du traitement de personnes dépendantes aux opioïdes. La prise par voie orale prévient en outre une augmentation rapide de la concentration dans le cerveau et diminue ainsi l'effet euphorisant.
La lévométhadone bloque 3,5 fois moins que la dextrométhadone les canaux potassiques hERG pour le cœur humain (hERG = human ether-a-go-go related gene) qui sont responsables de la repolarisation des cellules du muscle cardiaque.
Comme d'autres opioïdes, la lévométhadone réduit la motilité gastro-intestinale et augmente le tonus des muscles lisses, notamment dans la région de l'estomac et au niveau du sphincter d'Oddi.
Efficacité clinique
Après une administration de lévométhadone par voie orale, l'effet analgésique atteint son niveau maximal après 1-2 heure(s). La durée d'analgésie de 4-6 heures est, malgré une demi-vie plus longue, aussi longue que celle de la morphine. En cas d'administration orale prolongée, la durée d'action peut monter jusqu'à 22-48 heures.
PharmacocinétiqueAbsorption
Après administration par voie orale, la lévométhadone est rapidement et presque entièrement absorbée et peut être mise en évidence dans le plasma environ une demi-heure après. Des pics plasmatiques maximaux sont trouvés en l'espace de trois heures en cas d'administration par voie orale. La biodisponibilité absolue moyenne est de l'ordre d'au moins 80%.
Après une administration unique de 5 mg de L-Polamidon à des adultes en bonne santé, la concentration plasmatique maximale moyenne de lévométhadone s'est élevée à 8,8 ng/ml.
Distribution
La lévométhadone a un grand volume de distribution et la liaison aux protéines plasmatiques est d'environ 85%. La substance est liée à différentes protéines tissulaires, en particulier dans le cerveau. Ceci explique les effets cumulatifs et l'élimination lente de la méthadone. Il convient d'ajuster soigneusement la dose en cas d'administration répétée.
La lévométhadone passe la barrière placentaire et passe dans le lait maternel.
Métabolisme
La lévométhadone est principalement dégradée dans le foie via le système enzymatique des cytochromes P450 (principalement via les enzymes CYP2B6, mais aussi via CYP3A4) principalement en deux métabolites inactifs: 2-éthylidène-1,5-diméthyl-3,3-diphénylpyrrolidine (EDDP) et 2-éthyl-5-méthyl-3,3-diphénylpyrrolidine (EMDP). Les enzymes CYP2D6 et CYP2C19 participent au processus dans une moindre mesure.
Élimination
La lévométhadone et ses métabolites sont principalement éliminés dans l'urine et les selles. L'élimination de la méthadone dans l'urine est dépendante du pH: plus le pH urinaire est faible, plus la clairance est importante.
La demi-vie terminale de la lévométhadone est soumise à de fortes fluctuations individuelles et est de 16-53 heures.
Cinétique pour certains groupes de patients
Patients âgés
La demi-vie terminale peut être prolongée chez les patients âgés (à partir de 65 ans).
Grossesse
Au fil de la grossesse, la résorption gastro-intestinale peut être réduite et la distribution et la clairance (par induction de l'isoenzyme CYP3A4) de la lévométhadone peuvent être accrues.
Polymorphismes génétiques
Chez les métabolisateurs lents du CYP2B6 (7-8% des individus de race blanche), des concentrations plasmatiques supérieures de lévométhadone et un risque accru d'effets indésirables sont possibles.
Troubles de la fonction hépatique
Etant donné que la lévométhadone est métabolisée dans le foie, il y a un risque de concentrations plasmatiques de lévométhadone accrues chez les patients souffrant de maladies hépatiques chroniques sévères.
Troubles de la fonction rénale
En présence d'une insuffisance rénale, la lévométhadone est davantage éliminée dans la bile. Il n'a pas été observé de concentration plasmatique accrue en cas d'anurie. Le risque d'accumulation apparaît donc faible. Du fait des données limitées, on ne peut cependant exclure le risque de concentrations plasmatiques de lévométhadone accrues en cas de troubles de la fonction rénale.
La lévométhadone n'est que très faiblement dialysable. Selon les modèles effectués, environ 12 ng/ml de méthadone (en se référant au racémate de lévométhadone et de dextrométhadone) sont éliminés de la circulation systémique pendant une hémodialyse de quatre heures.
Données précliniquesSur le plan préclinique, la lévométhadone n'a pas été suffisamment étudiée. Toutefois, pour évaluer la sécurité préclinique, les connaissances relatives à la méthadone (racémate de lévométhadone et de dextrométhadone) peuvent être utilisées.
Mutagénicité et carcinogénicité
Les études in vitro et in vivo sur la génotoxicité de la méthadone ont en partie donné des résultats contradictoires avec des signes de faible potentiel clastogène. Selon l'état actuel des connaissances, il est impossible d'en déduire un risque pour l'homme. Les études à long terme chez la souris et le rat avec la méthadone n'ont fait apparaître aucune propriété cancérigène.
Toxicologie sur la reproduction
La progéniture de rongeurs mâles traités par la méthadone (jusqu'à 38 mg/kg/jour) quelques jours avant l'accouplement a présenté une mortalité néonatale accrue atteignant 74%. Dans les études d'embryotoxicité chez le rat et le lapin, la méthadone n'était pas tératogène. L'administration de méthadone à des animaux de laboratoire pendant la gestation ou la lactation a toutefois entraîné une exencéphalie (hamster et souris), des effets embryotoxiques et une mortalité néonatale accrue ainsi qu'un retard de développement postnatal physique et neurologique chez les jeunes animaux. Les résultats étaient en corrélation avec l'apparition d'une toxicité maternelle.
Remarques particulièresStabilité
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Stabilité après ouverture
Après ouverture du flacon, la solution se conserve pendant 3 mois.
Pour les préparations prêtes à l'emploi, la stabilité a été contrôlée et mise en évidence comme suit:
·mélange avec sirop de framboise: jusqu'à 7 jours au réfrigérateur (2-8°C) ou à température ambiante;
·mélange avec jus d'orange: jusqu'à 2 jours au réfrigérateur (2-8°C) ou à température ambiante.
Remarques particulières concernant le stockage
Ne pas conserver au-dessus de 30°C.
Conserver le récipient dans son carton pour le protéger de la lumière.
Tenir hors de portée des enfants.
Remarques concernant la manipulation
L-Polamidon, solution buvable 1 x 100 ml et 3 x 100 ml
Une seringue de dosage disponible dans le commerce avec un raccord Luer sans aiguille (non incluse dans l'emballage) est nécessaire pour le prélèvement de la solution. Procéder de la façon suivante:
|
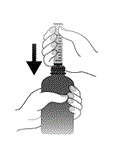
1.
|
Placez la seringue sur le cône Luer de la bouteille.
|
|
| |
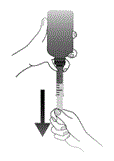
2.
|
Retournez le flacon avec la seringue à l'envers et prélevez la quantité de solution souhaitée.
|
|
| |
3.
|
Replacez le flacon avec la seringue à l'endroit et remettez le surplus de solution prélevée dans le flacon. Retirez la seringue de la bouteille.
|
|

|
L-Polamidon, solution buvable 500 ml
Un dispositif de distribution calibré disponible dans le commerce avec un filetage rond GL25 conforme à la norme DIN 168 est nécessaire pour le prélèvement de la solution.
En cas de remise, L-Polamidon est versé par portions, en fonction de la dose journalière, dans des contenants étiquetés et garantissant la sécurité des enfants.
Numéro d’autorisation65042 (Swissmedic)
PrésentationL-Polamidon, solution buvable 5 mg/ml 1 x 100 ml (A+)
L-Polamidon, solution buvable 5 mg/ml 3 x 100 ml (A+)
L-Polamidon, solution buvable 5 mg/ml 1 x 500 ml (A+)
Titulaire de l’autorisationSandoz Pharmaceuticals SA, Risch; domicile: Rotkreuz
Mise à jour de l’informationMars 2024
|



