Propriétés/EffetsCode ATC
A10BJ05
Mécanisme d'action
Le dulaglutide est un agoniste du récepteur du GLP-1 (Glucagon-like peptide-1) à action prolongée. La molécule comprend deux peptides identiques liés par des ponts disulfures, chacune contenant une séquence analogue à celle du GLP-1 humain modifiée, liée de manière covalente par un petit pont peptidique à la chaîne lourde (fragment Fc) d'une immunoglobuline humaine G4 (IgG4) modifiée. La partie du dulaglutide analogue du GLP-1 présente une homologie d'environ 90 % avec le GLP-1 natif humain. Le GLP-1 natif a une demi-vie de 1,5 à 2 minutes du fait de sa dégradation par la DPP-4 et de la clairance rénale. Contrairement au GLP-1 natif, le dulaglutide est protégé de la dégradation par la DPP-4 et sa grande taille ralentit son absorption et réduit sa clairance rénale. Ces caractéristiques structurelles donnent lieu à une formulation soluble à la demi-vie prolongée de 4,7 jours, ce qui permet une administration sous-cutanée hebdomadaire. De plus, la molécule de dulaglutide a été conçue pour empêcher la réponse immunitaire dépendante du récepteur Fcγ et réduire son potentiel immunogène.
Le dulaglutide présente plusieurs propriétés anti-hyperglycémiantes du GLP-1. En présence de concentrations élevées de glucose, le dulaglutide augmente l'AMP cyclique (AMPc) intracellulaire dans les cellules bêta du pancréas, ce qui entraîne la sécrétion d'insuline. Le dulaglutide inhibe la sécrétion de glucagon, qui est élevée chez les patients diabétiques de type 2. Des concentrations de glucagon plus faibles entraînent une diminution de la production de glucose hépatique. Le dulaglutide ralentit également la vidange gastrique.
Pharmacodynamique
Chez les patients atteints de diabète de type 2, le dulaglutide améliore le contrôle glycémique grâce aux effets prolongés de la diminution des concentrations de glucose à jeun, avant et après les repas dès la première administration du médicament; l'effet est maintenu pendant l'intervalle d'injection hebdomadaire.
Une étude pharmacodynamique avec Trulicity a permis d'observer, chez des patients atteints de diabète de type 2, un rétablissement de la première phase de la sécrétion d'insuline à un niveau dépassant ceux observés chez des sujets sains sous placebo et une amélioration de la deuxième phase de la sécrétion d'insuline en réponse à l'administration d'un bolus intraveineux de glucose.
Conformément à son profil pharmacocinétique, le dulaglutide a un profil pharmacodynamique adapté à une administration hebdomadaire (voir «Pharmacocinétique»).
Efficacité clinique
Contrôle glycémique
La tolérance et l'efficacité du dulaglutide ont été étudiées dans dix études contrôlées et randomisées de phase 3 incluant 8035 patients adultes atteints de diabète de type 2. Parmi eux, 1644 patients avaient 65 ans et plus, et parmi ces patients 174 avaient 75 ans et plus. Ces études ont inclus 5650 patients traités par le dulaglutide, dont 1558 traités par le dulaglutide 0,75 mg une fois par semaine, 2862 patients traités par le dulaglutide 1,5 mg une fois par semaine, 616 patients traités par le dulaglutide 3 mg une fois par semaine et 614 patients traités par le dulaglutide 4,5 mg une fois par semaine. Dans toutes les études, le dulaglutide a entrainé des améliorations cliniquement significatives du contrôle glycémique, mesurées par le taux d'hémoglobine glyquée A1c (HbA1c).
Monothérapie
Une monothérapie avec le dulaglutide a été comparée à la metformine dans une étude avec comparateur actif d'une durée de 52 semaines. Au bout de 26 semaines, le dulaglutide a été supérieur à la metformine (1500-2000 mg/jour) dans la réduction de l'HbA1c (valeur moyenne initiale 7,6 %). Un pourcentage significativement plus élevé de patients sous dulaglutide a atteint la valeur cible d'HbA1c de <7,0 % et de ≤6,5 % en comparaison avec la metformine au bout de 26 semaines. Ces effets se sont maintenus jusqu'à la 52e semaine. Le taux d'hypoglycémies symptomatiques documentées a été de 0,62 épisode/patient/an sous dulaglutide 1,5 mg, de 0,15 épisode/patient/an sous dulaglutide 0,75 mg et de 0,09 épisode/patient/an sous metformine. Des hypoglycémies sévères n'ont pas été constatées.
Tableau 1: Résultats d'une étude contrôlée de 52 semaines en monothérapie versus comparateur actif, comparant deux dosages de dulaglutide à la metformine
|
|
HbA1c
à l'inclusion
|
Changement moyen de l'HbA1c
|
Patients atteignant une valeur cible d'HbA1c
|
Changement de la glycémie à jeun
|
Changement du poids corporel
| |
|
(%)
|
(%)
|
<7,0 % (%)
|
≤6,5 % (%)
|
(mmol/l)
|
(kg)
| |
26 semaines
| |
Dulaglutide 1,5 mg 1 fois par semaine
(n=269)
|
7,63
|
-0,78††
|
61,5
|
46,0
|
-1,61
|
-2,29
| |
Dulaglutide 0,75 mg 1 fois par semaine
(n=270)
|
7,58
|
-0,71††
|
62,6
|
40,0
|
-1,46
|
-1,36
| |
Metformine 1500-2000 mg/jour
(n=268)
|
7,60
|
-0,56
|
53,6
|
29,8
|
-1,34
|
-2,22
| |
52 semaines
| |
Dulaglutide 1,5 mg 1 fois par semaine
(n=269)
|
7,63
|
-0,70††
|
60,0
|
42,3
|
-1,56
|
-1,93
| |
Dulaglutide 0,75 mg 1 fois par semaine
(n=270)
|
7,58
|
-0,55†
|
53,2
|
34,7
|
-1,00
|
-1,09
| |
Metformine 1500-2000 mg/jour
(n=268)
|
7,60
|
-0,51
|
48,3
|
28,3
|
-1,15
|
-2,20
|
†† Valeur p unilatérale ajustée pour tests multiples < 0,025, pour la supériorité du dulaglutide comparé à la metformine, évaluée seulement pour l'HbA1c.
† Valeur p unilatérale ajustée pour tests multiples < 0,025, pour la non-infériorité du dulaglutide comparé à la metformine, évaluée seulement pour l'HbA1c.
Association avec la metformine
La sécurité et l'efficacité du dulaglutide ont été examinées dans une étude contrôlée avec placebo et comparateur actif (sitagliptine 100 mg, une fois par jour), d'une durée de 104 semaines, en association avec la metformine. Au bout de 26 semaines, le traitement par le dulaglutide a entrainé une plus forte réduction de l'HbA1c que le placebo. Au bout de 52 semaines, la baisse de l'HbA1c sous dulaglutide était également supérieure à celle induite par la sitagliptine, avec une proportion significativement plus élevée de patients atteignant les valeurs cibles d'HbA1c < 7,0 % et ≤6,5 %. Le traitement par le dulaglutide a en outre induit une réduction significativement plus importante du glucose plasmatique à jeun mesuré et du poids corporel, par rapport à la sitagliptine. Ces effets se sont maintenus jusqu'à la fin de l'étude (104 semaines). Le taux d'hypoglycémies symptomatiques documentées sous dulaglutide 1,5 mg, dulaglutide 0,75 mg et sitagliptine s'est élevé respectivement à 0,19, 0,18 et 0,17 épisode/patient/an. Aucune hypoglycémie sévère n'a été rapportée sous dulaglutide.
Tableau 2: Résultats d'une étude contrôlée versus placebo et comparateur actif de 104 semaines comparant deux dosages de dulaglutide à la sitagliptine
|
|
HbA1c
à l'inclusion
|
Changement moyen de l'HbA1c
|
Patients atteignant une valeur cible d'HbA1c
|
Changement de la glycémie à jeun
|
Changement du poids corporel
| |
|
(%)
|
(%)
|
<7,0 % (%)
|
≤6,5 % (%)
|
(mmol/l)
|
(kg)
| |
26 semaines
| |
Dulaglutide 1,5 mg 1 fois par semaine
(n = 304)
|
8,12
|
-1,22‡‡
|
60,9
|
46,.7
|
-2,38
|
-3,18
| |
Dulaglutide 0,75 mg 1 fois par semaine
(n=302)
|
8,19
|
-1,01‡‡
|
55,2
|
31,0
|
-1,97
|
-2,63
| |
Placebo (n= 177)
|
8,10
|
0,03
|
21,0
|
12,5
|
-0,49
|
-1,47
| |
Sitagliptine 100 mg 1 fois par jour
(n = 315)
|
8,09
|
-0,61
|
37,8
|
21,8
|
-0,97
|
-1,46
| |
52 semaines
| |
Dulaglutide 1,5 mg 1 fois par semaine
(n = 304)
|
8,12
|
-1,10††
|
57,6
|
41,7
|
-2,38
|
-3,03
| |
Dulaglutide 0,75 mg 1 fois par semaine
(n=302)
|
8,19
|
-0,87††
|
48,8
|
29,0
|
-1,63
|
-2,60
| |
Sitagliptine 100 mg 1 fois par jour
(n = 315)
|
8.,09
|
-0,39
|
33,0
|
19,2
|
-0,90
|
-1,53
| |
104 semaines
| |
Dulaglutide 1,5 mg 1 fois par semaine
(n = 304)
|
8,12
|
-0,99††
|
54,3
|
39,1
|
-1,99
|
-2,88
| |
Dulaglutide 0,75 mg 1 fois par semaine
(n=302)
|
8,19
|
-0,71††
|
44,8
|
24,2
|
-1,39
|
-2,39
| |
Sitagliptine 100 mg 1 fois par jour
(n = 315)
|
8,09
|
-0,32
|
31,1
|
14,1
|
-0,47
|
-1,75
|
†† Valeur p unilatérale ajustée pour tests multiples < 0,025, pour la supériorité du dulaglutide comparé à la sitagliptine, évaluée seulement pour l'HbA1c, aux semaines 52 et 104.
‡‡ Valeur p unilatérale ajustée pour tests multiples < 0,001, pour la supériorité du dulaglutide comparé au placebo, évaluée seulement pour l'HbA1c.
Association avec la metformine et une sulfonylurée
Dans une étude avec comparateur actif d'une durée de 78 semaines, le dulaglutide a été comparé à l'insuline glargine, tous deux en association avec la metformine et une sulfonylurée (glimépiride). Au bout de 52 semaines, le dulaglutide a été supérieur à l'insuline glargine pour abaisser l'HbA1c; cette supériorité s'est maintenue jusqu'à la fin des 78 semaines. Cet effet s'est accompagné d'un pourcentage significativement plus élevé de patients qui atteignaient des valeurs cibles d'HbA1c < 7,0 % et ≤6,5 % au bout de 52 (contrôle principal) et 78 semaines (contrôle final).
Durant les 52 premières semaines, les patients sous dulaglutide ont perdu en moyenne 1,87 kg alors que les patients sous insuline glargine ont gagné 1,44 kg; cet effet s'est maintenu jusqu'à la 78e semaine. Le taux d'hypoglycémies symptomatiques documentées a été de 1,67 épisode/patient/an sous dulaglutide 1,5 mg, de 1,67 sous dulaglutide 0,75 mg et de 3,02 épisodes/patient/an sous insuline glargine. Deux cas d'hypoglycémies sévères ont été observés sous dulaglutide 1,5 mg, aucun cas sous dulaglutide 0,75 mg et deux cas sous insuline glargine. Les taux (épisodes/patient/an) d'hypoglycémies nocturnes ont été de 1,8 sous insuline glargine, de 0,59 sous dulaglutide 0,75 mg et de 0,74 sous dulaglutide 1,5 mg.
Tableau 3: Résultats d'une étude contrôlée de 78 semaines avec comparateur actif comparant deux dosages de dulaglutide à l'insuline glargine
|
|
HbA1c
à l'inclusion
|
Changement moyen de l'HbA1c
|
Patients atteignant une valeur cible d'HbA1c
|
Changement de la glycémie à jeun
|
Changement du poids corporel
| |
|
(%)
|
(%)
|
<7,0 % (%)
|
≤6,5 % (%)
|
(mmol/l)
|
(kg)
| |
52 semaines
| |
Dulaglutide 1,5 mg 1 fois par semaine
(n = 273)
|
8,18
|
-1,08††
|
53,2
|
27,0
|
-1,50
|
-1,87
| |
Dulaglutide 0,75 mg 1 fois par semaine
(n=272)
|
8,13
|
-0,76†
|
37,1
|
22,5
|
-0,87
|
-1,33
| |
Insuline glargine+ 1 fois par jour
(n = 262)
|
8,10
|
-0,63
|
30,9
|
13,5
|
-1,76
|
1,44
| |
78 semaines
| |
Dulaglutide 1,5 mg 1 fois par semaine
(n = 273)
|
8,18
|
-0,90††
|
49,0
|
28,1
|
-1,10
|
-1,96
| |
Dulaglutide 0,75 mg 1 fois par semaine
(n=272)
|
8,13
|
-0,62†
|
34,1
|
22,1
|
-0,58
|
-1,54
| |
Insuline glargine+
1 fois par jour
(n = 262)
|
8,10
|
-0,59
|
30,5
|
16,6
|
-1,58
|
1,28
|
†† Valeur p unilatérale ajustée pour tests multiples < 0,025, pour la supériorité du dulaglutide comparé à l'insuline glargine, évaluée seulement pour l'HbA1c.
† Valeur p unilatérale ajustée pour tests multiples < 0,025, pour la non-infériorité du dulaglutide comparé à l'insuline glargine, évaluée seulement pour l'HbA1c.
+ Les doses d'insuline glargine ont été ajustées en utilisant un algorithme avec une glycémie à jeun cible < 5,6 mmol/l.
Association avec une sulfonylurée
La sécurité et l'efficacité du dulaglutide en association avec la sulfonylurée glimépiride ont été étudiées dans une étude contrôlée avec placebo d'une durée de 24 semaines. Le traitement par le dulaglutide 1,5 mg a entraîné une réduction statistiquement significative de l'HbA1c par rapport au placebo au bout de 24 semaines (différence HbA1c LSM [95% CI] de-1,27 [-1,57, -0,97]). Avec le dulaglutide 1,5 mg, le pourcentage de patients ayant atteint les taux cibles d'HbA1c < 7,0 % et ≤6,5 % au bout de 24 semaines a été significativement plus élevé qu'avec le placebo.
Les taux d'hypoglycémie symptomatique documentée avec le dulaglutide 1,5 mg et avec placebo ont été respectivement de 0,90 et 0,04 épisode/patient/an. Aucun cas d'hypoglycémie sévère n'a été observé avec le duaglutide ni avec le placebo.
Tableau 4: Résultats d'une étude de 24 semaines contrôlée versus placebo comparant le dulaglutide en association avec le glimépiride
|
|
HbA1c à l'inclusion
|
Changement moyen de l'HbA1c
|
Patients atteignant une valeur cible d'HbA1c
|
Changement de la glycémie à jeun
|
Changement du poids corporel
| |
|
(%)
|
(%)
|
<7,0 % (%)
|
≤6,5 % (%)
|
(mmol/l)
|
(kg)
| |
24 semaines
| |
Dulaglutide 1,5 mg une fois par semaine (n=239)
|
8,39
|
-1,38‡‡
|
55,3‡‡
|
40,0**
|
-1,70‡‡
|
-0,91
| |
Placebo (n=60)
|
8,39
|
-0,11
|
18,9
|
9,4
|
0,16
|
-0,24
|
‡‡ p < 0,001 pour la supériorité du dulaglutide comparé au placebo, avec une erreur globale de type I contrôlée
** p < 0,001 pour la comparaison du groupe dulaglutide au placebo
Association avec un inhibiteur du SGLT-2 avec ou sans metformine
Une étude de 24 semaines à trois bras contrôlée par placebo a évalué l'efficacité du dulaglutide (1,5 mg et 0,75 mg une fois par semaine) chez des patients déjà traités avec un inhibiteur du SGLT-2 (avec ou sans metformine) et n'ayant pas un contrôle adéquat de la glycémie (HbA1c ≥7,0% - ≤9,5 %). Le critère d'évaluation principal était la diminution du taux d'HbA1c entre le début de l'étude et la semaine 24 (ΔHbA1c). Comparé au contrôle placebo, l'effet hypoglycémiant (ΔHbA1c) était statistiquement significativement supérieur dans les deux bras du dulaglutide (différence moyenne [IC à 95 %] pour 1,5 mg -0,82 % [-1,00, -0,64] et 0,75 mg -0,69% [-0,86, -0,51]). De plus, dans les deux bras du dulaglutide (1,5 mg et 0,75 mg), une proportion significativement supérieure au contrôle placebo a atteint la valeur cible de HbA1c <7,0% (71,5% et 61,8% contre 32,5%, p <0,001).
Association avec la metformine et la pioglitazone
Dans une étude contrôlée avec placebo et comparateur actif (exénatide deux fois par jour), tous deux en association avec la metformine et la pioglitazone, le dulaglutide a démontré sa supériorité pour améliorer l'HbA1c par rapport au placebo au bout de 26 semaines. En outre, le dulaglutide a entraîné une réduction de l'HbA1c supérieure à celle induite par l'exénatide au bout de 26 et 52 semaines. Cet effet s'est accompagné d'une baisse significativement plus importante de la glycémie à jeun et un pourcentage plus important de patients ont atteint des valeurs cibles d'HbA1c < 7,0 % et ≤ à 6,5 % au bout de 26 et 52 semaines. La perte de poids a été comparable sous dulaglutide et sous exénatide. Les taux d'hypoglycémie symptomatique documentés avec le dulaglutide 1,5 mg et 0,75 mg et l'exénatide deux fois par jour ont été respectivement de 0,19, 0,14 et 0,75 épisode/patient/an. Aucun cas d'hypoglycémie sévère n'a été observé sous dulaglutide et deux cas d'hypoglycémie sévère ont été observés avec l'exénatide deux fois par jour.
Tableau 5: Résultats d'une étude contrôlée de 52 semaines avec comparateur actif comparant deux dosages de dulaglutide à l'exénatide
|
|
HbA1c
à l'inclusion
|
Changement moyen de l'HbA1c
|
Patients atteignant une valeur cible d'HbA1c
|
Changement de la glycémie à jeun
|
Changement du poids corporel
| |
|
(%)
|
(%)
|
<7,0 % (%)
|
≤6,5 % (%)
|
(mmol/l)
|
(kg)
| |
26 semaines
| |
Dulaglutide 1,5 mg 1 fois par semaine
(n = 279)
|
8,10
|
-1,51‡‡,††
|
78,2
|
62,7
|
-2,36
|
-1,30
| |
Dulaglutide 0,75 mg 1 fois par semaine
(n=280)
|
8,05
|
-1,30‡‡,††
|
65.8
|
53,2
|
-1,90
|
0,20
| |
Placebo (n = 141)
|
8,06
|
-0,46
|
42,9
|
24,4
|
-0.26
|
1,24
| |
Exénatide+ 10 µg 2 fois par jour
(n = 276)
|
8,07
|
-0,99
|
52,3
|
38,0
|
-1,35
|
-1,07
| |
52 semaines
| |
Dulaglutide 1.5 mg 1 fois par semaine
(n = 279)
|
8,10
|
-1,36††
|
70,8
|
57,2
|
-2,04
|
-1,10
| |
Dulaglutide 0.75 mg 1 fois par semaine
(n=280)
|
8,05
|
-1,07††
|
59,1
|
48,3
|
-1,58
|
0,44
| |
Exénatide+ 10 µg 2 fois par jour
(n = 276)
|
8,07
|
-0,80
|
49,2
|
34,6
|
-1,03
|
-0,80
|
†† Valeur p unilatérale ajustée pour tests multiples < 0,025, pour la supériorité du dulaglutide comparé l'exénatide, évaluée seulement pour l'HbA1c
‡‡ Valeur p unilatérale ajustée pour tests multiples < 0,001, pour la supériorité du dulaglutide comparé au placebo, évaluée seulement pour l'HbA1c
+ Dosage de l'exénatide: 5 µg 2 fois par jour pendant les 4 premières semaines, puis 10 µg 2 fois par jour
En association avec l'insuline basale titrée, avec ou sans metformine
Dans une étude contrôlée avec placebo de 28 semaines, le dulaglutide 1,5 mg a été comparé au placebo en association avec de l'insuline glargine basale titrée (88 % avec et 12 % sans metformine) pour étudier l'effet sur le contrôle glycémique et la sécurité. Pour optimiser la dose d'insuline glargine, les deux groupes étaient titrés pour cibler une glycémie à jeun < 5,6 mmol/l. La dose moyenne initiale d'insuline glargine était de 37 unités/jour pour les patients recevant le placebo et de 41 unités/jour pour les patients recevant le dulaglutide 1,5 mg. Les doses initiales d'insuline glargine chez les patients ayant une HbA1c < 8,0 % étaient réduites de 20 %. A la fin des 28 semaines de traitement, la dose était de 65 unités/jour pour les patients recevant le placebo et de 51 unités/jour pour les patients recevant le dulaglutide 1,5 mg. A la 28e semaine, le traitement par Trulicity 1,5 mg une fois par semaine a entraîné une réduction statistiquement significative de l'HbA1c par rapport au placebo (différence HbA1c LSM [95% CI] de -0,77 [-0,97, -0,56]) et à un pourcentage significativement plus élevé de patients ayant atteint les taux cibles d'HbA1c < 7.0 % et ≤6.5 %.
Les taux d'hypoglycémie symptomatique documentée ont été de 3,38 épisodes/patient/an avec le dulaglutide 1,5 mg comparé à 4,38 épisodes/patient/an avec le placebo. Une hypoglycémie sévère a été rapportée chez un patient avec le dulaglutide 1,5 mg en association à l'insuline glargine, et aucune n'a été rapportée avec le placebo.
Tableau 6: Résultats d'une étude de 28 semaines comparant le dulaglutide au placebo en association avec de l'insuline glargine titrée
|
|
HbA1c
à l'inclusion
|
Changement moyen de l'HbA1c
|
Patients atteignant une valeur cible d'HbA1c
|
Changement de la glycémie à jeun
|
Changement du poids corporel
| |
|
(%)
|
(%)
|
<7,0 % (%)
|
≤6,5 % (%)
|
(mmol/l)
|
(kg)
| |
28 semaines
| |
Dulaglutide 1,5 mg une fois par semaine (n=150)
|
8,41
|
-1,44‡‡
|
66,7‡‡
|
50,0**
|
-2,48‡‡
|
-1,91‡‡
| |
Placebo une fois par semaine (n=150)
|
8,32
|
-0,67
|
33,3
|
16,7
|
-1,55
|
0,50
|
‡‡ p < 0,001 pour la supériorité du dulaglutide comparé au placebo, avec une erreur globale de type I contrôlée
** p < 0,001 pour la comparaison du groupe dulaglutide au placebo
Association avec l'insuline prandiale, avec ou sans metformine
Dans cette étude, des patients traités par 1 ou 2 injections quotidiennes d'insuline avant l'entrée dans l'étude ont arrêté leur traitement d'insuline préalable et ont été randomisés pour recevoir soit le dulaglutide une fois par semaine 1,5 mg ou 0,75 mg, soit de l'insuline glargine une fois par jour, en association avec de l'insuline prandiale lispro trois fois par jour, avec ou sans metformine. Au bout de 26 semaines, la baisse d'HbA1c sous dulaglutide a été supérieure à celle observée sous l'insuline glargine. Cet effet était maintenu à la fin des 52 semaines de l'étude. Cet effet s'est accompagné d'une perte de poids significative par rapport à l'insuline glargine, avec laquelle une prise pondérale a été observée au cours de l'étude. De même, un pourcentage plus important de patients ont atteint des valeurs cibles d'HbA1c < 7,0 % et ≤6,5 % au bout de 26 semaines et <7,0 % au bout de 52 semaines dans le groupe dulaglutide que dans le groupe insuline glargine. Le taux d'hypoglycémies symptomatiques documentées a été de 31,06 épisodes/patient/an sous dulaglutide 1,5 mg, de 35,66 épisodes/patient/an sous dulaglutide 0,75 mg et de 40,95 épisodes/patient/an sous insuline glargine. Sous dulaglutide 1,5 mg, 10 patients ont rapporté des hypoglycémies sévères, sous dulaglutide il y a eu 7 patients et 15 sous insuline glargine.
Les taux (épisodes/patient/an) d'hypoglycémies nocturnes ont été de 7,99 sous insuline glargine, de 3,94 sous dulaglutide 0,75 mg et de 3,61 sous dulaglutide 1,5 mg.
Tableau 7: Résultats d'une étude contrôlée de 52 semaines avec comparateur actif comparant deux dosages de dulaglutide à l'insuline glargine
|
|
HbA1c
à l'inclusion
|
Changement moyen de l'HbA1c
|
Patients atteignant une valeur cible d'HbA1c
|
Changement de la glycémie à jeun
|
Changement du poids corporel
| |
|
(%)
|
(%)
|
<7,0 % (%)
|
≤6,5 % (%)
|
(mmol/l)
|
(kg)
| |
26 semaines
| |
Dulaglutide 1,5 mg 1 fois par semaine
(n = 295)
|
8,46
|
-1,64††
|
67,6
|
48,0
|
-0,27
|
-0,87
| |
Dulaglutide 0,75 mg 1 fois par semaine
(n=293)
|
8,40
|
-1,59††
|
69,0
|
43,0
|
0,22
|
0,18
| |
Insuline glargine+
1 fois par jour
(n = 296)
|
8,53
|
-1,41
|
56,8
|
37,5
|
-1,58
|
2,33
| |
52 semaines
| |
Dulaglutide 1,5 mg 1 fois par semaine
(n = 295)
|
8,46
|
-1,48††
|
58,5
|
36,7
|
0,08
|
-0,35
| |
Dulaglutide 0,75 mg 1 fois par semaine
(n=293)
|
8,40
|
-1,42††
|
56,3
|
34,7
|
0,41
|
0,86
| |
Insuline glargine+
1 fois par jour
(n = 296)
|
8,53
|
-1,23
|
49,3
|
30,4
|
-1,01
|
2,89
|
†† Valeur p unilatérale ajustée pour tests multiples < 0,025, pour la supériorité du dulaglutide comparé l'insuline glargine, évaluée seulement pour l'HbA1c
+ Les doses d'insuline glargine ont été ajustées en utilisant un algorithme avec une valeur cible de glycémie à jeun de 4,0-5,5 mmol/l.
Étude d'outcome cardiovasculaire
L'étude à long terme sur l'outcome cardiovasculaire sous dulaglutide était une étude clinique en double aveugle, contrôlée avec placebo. Des patients atteints de diabète de type 2 ont reçu, en plus du traitement standard pour leur diabète de type 2, un traitement de dulaglutide 1,5 mg (4949) ou un placebo (4952). La durée médiane d'observation de l'étude a été de 5,4 ans.
L'âge moyen était de 66,2 ans, l'IMC moyen s'est élevé à 32,3 kg / m² et 46,3% des patients étaient de sexe féminin.
L'étude a inclus des patients dans les trois catégories de risque suivantes: 2892 (29,2%) patients ≥50 ans souffrant d'affection cardiovasculaire avérée (par ex. infarctus du myocarde), 2965 (29,9%) patients ≥55 ans présentant une affection cardiovasculaire subclinique (par ex. mise en évidence d'une ischémie cardiaque ou >50% de sténose coronarienne) et 3725 (37,6%) patients ≥60 ans qui présentaient ≥2 facteurs de risque cardiovasculaire (par ex. tabagisme ou hypertension artérielle).
La valeur initiale moyenne de l'HbA1c s'est élevée à 7,2%. La majorité des patients avaient une valeur initiale d'HbA1c située entre 6,0% et 8,9% (du 10e au 90e percentile). La durée moyenne du diabète était de 10,5 ans. Le bras de traitement avec le dulaglutide incluait des patients ≥65 ans (n = 2619; 52,9%) et ≥75 ans (n = 484; 9,7%) et des patients atteints d'insuffisance rénale légère (n = 2435; 50,2%), modérée (n = 1031; 21,3%) ou sévère (n = 50; 1,1%).
Le critère primaire a été le temps écoulé entre la randomisation et la première survenue d'un évènement cardiovasculaire sévère (MACE): mort cardiovasculaire, infarctus du myocarde non mortel ou accident vasculaire cérébral non mortel. Le statut au moment del'objectif primaire ou le statut vital à la fin de l'étude a été disponible pour 99,7% des participants qui avaient été randomisés pour recevoir le dulaglutide ou le placebo. Le dulaglutide était supérieur au placebo dans la prévention des MACE (Figure 1). Les patients traités avec le dulaglutide avaient un taux de MACE plus bas que ceux traités avec le placebo [HR: 0,88; IC à 95% (0,79, 0,99]). Chacune des composantes du MACE a contribué à la réduction du MACE, comme cela est illustré dans la Figure 2. L'efficacité du dulaglutide a été cohérente sur divers sous-groupes, notamment ceux formés en fonction de l'HbA1c de départ, du sexe, de la durée du diabète, de l'âge et de l'eGFR.
L'analyse par sous-groupes en fonction des catégories de risque cardiovasculaire a donné les résultats suivants: les patients ≥50 ans atteints d'une affection cardiovasculaire avérée [18,3% des patients sous dulaglutide avec MACE vs. 20,7% des patients sous placebo, HR: 0,87; IC à 95% (0,74, 1,03)], patients ≥55 ans présentant une affection cardiovasculaire subclinique [10,2% vs. 12,3%, HR: 0,81; IC à 95% (0,65, 1,01)] et patients ≥60 ans qui présentaient ≥2 facteurs de risque cardiovasculaire [8,9% vs. 9,1%, HR: 0,96; IC à 95% CI (0,78, 1,19).
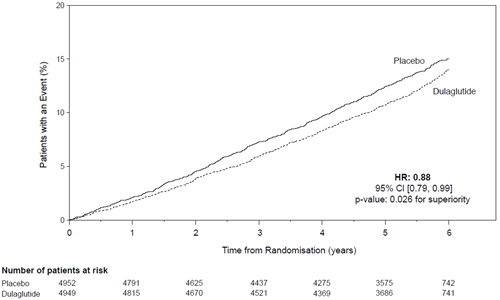
Figure 1: Diagramme selon Kaplan-Meier du temps écoulé jusqu'à la première survenue de l'objectif combiné: de mort CV, d'infarctus du myocarde non mortel ou d'accident vasculaire cérébral non mortel, dans l'étude à long terme sur l'outcome cardiovasculaire sous dulaglutide.
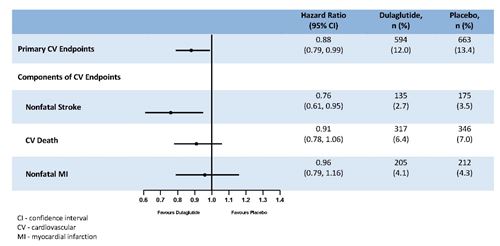
Figure 2: Représentation selon Forest de l'analyse du critère cardiovasculaire principal et de ses composantes individuelles: mort cardiovasculaire, infarctus du myocarde non mortel et accident vasculaire cérébral non mortel.
Sous dulaglutide vs. placebo ajoutés au traitement standard, une diminution significative et persistante de la valeur d'HbA1c entre le début de l'étude et le mois 60 a été observée (-0,29% vs. 0,22%; différence estimée entre les traitements – 0,51% [-0,57; -0,45]; p <0,001). Il y a eu significativement moins de patients dans le groupe dulaglutide qui ont nécessité une intervention glycémique additionnelle, par rapport au groupe sous placebo (dulaglutide: 2086 [42,2%]; placebo: 2825 [57,0%]; p <0,001).
Pression artérielle
L'effet du dulaglutide sur la pression artérielle, mesurée dans le cadre d'une surveillance ambulatoire de la pression artérielle, a été évalué dans une étude de 755 patients atteints de diabète de type 2. Le traitement avec le dulaglutide a entraîné 16 semaines après le début du traitement une réduction de la pression artérielle systolique par rapport au placebo (dose de 1,5 mg: -2,8 mmHg [97,3 %, CI -4,6, -1,0]; dose de 0,75 mg: (-1,1 mmHg [97,3 %, CI -2,8, 0,7]).
Aucune différence n'a été observée sur la pression artérielle diastolique. Des résultats similaires pour la pression artérielle systolique et diastolique ont été obtenus au bout de 26 semaines, au temps d'évaluation final de l'étude.
Traitement d'association du dulaglutide 4,5 mg, 3 mg et 1,5 mg avec la metformine
La sécurité d'emploi et l'efficacité de l'association du dulaglutide 3 mg et 4,5 mg une fois par semaine avec la metformine, en comparaison avec l'association de dulaglutide 1,5 mg une fois par semaine avec la metformine, ont été examinées dans une étude portant sur 52 semaines. Le dulaglutide 3 mg et 4,5 mg se sont avérés supérieurs au dulaglutide 1,5 mg à la semaine 36, en termes de réduction de l'HbA1c et du poids corporel. Un pourcentage plus élevé de patients a atteint les objectifs d'HbA1c de <7,0 % ou de ≤6,5 % au bout de 36 semaines avec le dulaglutide 3 mg et le dulaglutide 4,5 mg. Une réduction du poids corporel de ≥5 % par rapport à la valeur initiale a été obtenue respectivement par 31 %, 40 % et 49 % des patients sous dulaglutide 1,5 mg, 3 mg et 4,5 mg. Ces effets se sont maintenus sur 52 semaines.
Tableau 8: Résultats d'une étude avec contrôle actif comparant trois dosages de dulaglutide
|
|
HbA1c à l'inclusion
|
Changement moyen de l'HbA1c
|
Pourcentage de patients atteignant la valeur cible d'HbA1c
|
Changement de la glycémie à jeun
|
Changement du poids corporel
| |
(%)
|
(%)
|
<7,0 % (%)
|
≤6,5 % (%)
|
(mmol/l)
|
(kg)
| |
36 semaines
| |
Dulaglutide 1,5 mg 1x par semaine
(n = 612)
|
8,64
|
-1,53
|
57,0
|
38,1
|
-2,45
|
-3,1
| |
Dulaglutide 3 mg 1x par semaine
(n = 616)
|
8,63
|
-1,71#
|
64,7#
|
48,4‡‡
|
-2,66
|
-4,0#
| |
Dulaglutide 4,5 mg 1x par semaine
(n = 614)
|
8,64
|
-1,87##
|
71,5#
|
51,7‡‡
|
-2,90#
|
-4,7##
| |
52 semaines
| |
Dulaglutide 1.5 mg 1x par semaine
(n = 612)
|
8,64
|
-1,52
|
58,6
|
40,4
|
-2,39
|
-3,5
| |
Dulaglutide 3 mg 1x par semaine
(n = 616)
|
8,63
|
-1,71‡
|
65,4‡
|
49,2‡
|
-2,70‡
|
-4,3‡
| |
Dulaglutide 4,5 mg 1x par semaine
(n = 614)
|
8,64
|
-1,83‡‡
|
71,7‡‡
|
51,3‡‡
|
-2,92‡‡
|
-5,0‡‡
|
# p < 0,05, ## p < 0,001 pour la supériorité par rapport au dulaglutide 1,5 mg, valeurs de p ajustées avec le contrôle de l'erreur systématique de type 1
‡ p < 0,05, ‡‡ p < 0,001 par rapport au dulaglutide 1,5 mg
Les résultats visent l'effet sous traitement (l'analyse se base sur des modèles mixtes pour mesures répétées ou sur une régression logistique longitudinale).
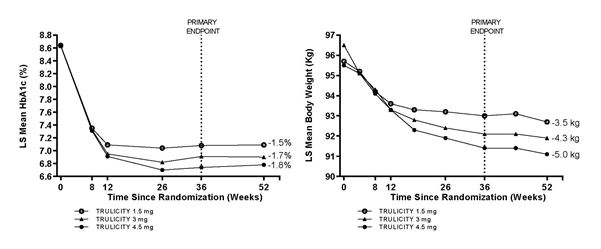
Figure 3. Variation moyenne de l'HbA1c (%) et du poids corporel (kg) entre la valeur initiale et la valeur à la semaine 52.
Les taux d'hypoglycémies symptomatiques documentées sous dulaglutide 1,5 mg, 3 mg et 4,5 mg ont été respectivement de 0,07, 0,05 et 0,07 épisode/patient/an. Un patient a rapporté une hypoglycémie sévère sous dulaglutide 1,5 mg, aucun patient sous dulaglutide 3 mg et un patient sous dulaglutide 4,5 mg.
Utilisation chez des patients atteints d'insuffisance rénale
Dans une étude de 52 semaines, le dulaglutide 1,5 mg et 0,75 mg ont été comparés à l'insuline glargine titrée en association avec l'insuline lispro prandiale pour étudier l'effet anti-hyperglycémiant chez des patients atteints de diabète de type 2 et d'insuffisance rénale chronique modérée à sévère (eGFR [selon CKD-EPI] < 60 et ≥15 ml/min/1,73m2). A l'inclusion, le eGFR global moyen était de 38 ml/min/1,73m2; 30 % des participants à l'étude avaient un eGFR < 30 ml/min/1,73m2. Le critère d'évaluation principal était le changement du taux d'HbA1c de l'inclusion jusqu'à la semaine 26, pour lequel les deux groupes dulaglutide (1,5 mg et 0,75 mg) étaient non-inférieurs par rapport au groupe insuline glargine (différence pour le changement de HbA1c [95 % CI]: -0,05 % [-0,26 %, 0,15 %] pour 1,5 mg et 0,02 % [-0,18 %, 0,22 %] pour 0,75 mg). Ceci a été confirmé par les résultats à 52 semaines de traitement.
Utilisation dans la population pédiatrique
La sécurité et l'efficacité du dulaglutide une fois par semaine (QW) ont été étudiées sur un total de 52 semaines dans une étude randomisée à 3 bras (1 [placebo]: 1 [dulaglutide 0,75 mg QW]: 1 [dulaglutide 1,5 mg QW]) portant sur un total de 154 enfants et adolescents âgés de 10 à 18 ans. Les participants à l'étude pouvaient recevoir, en plus du régime et de l'exercice physique, un prétraitement de metformine et/ou d'insuline basale. Le critère principal d'efficacité (changement de HbA1c) a été déterminé sur la période de la phase en double aveugle jusqu'à la semaine 26. Ensuite, les participants à l'étude pouvaient continuer à prendre pour 26 autres semaines un traitement ouvert de dulaglutide 0,75 mg QW. Le dulaglutide s'est avéré supérieur au contrôle de placebo en ce qui concerne le critère principal.
Il n'a pas été observé de différences statistiquement significatives ou pertinentes sur le plan clinique entre le dulaglutide et le placebo en termes de variation de l'IMC par rapport à la valeur initiale jusqu'à la semaine 26.
Tableau 9: Résultats d'une étude de 52 semaines destinée à comparer deux dosages de dulaglutide avec un placebo chez des patients pédiatriques qui étaient traités avec un régime alimentsaire et de l'exercice physique seuls, avec ou sans metformine et/ou insuline basale
|
|
HbA1c à l'inclusion
|
Changement moyen de l'HbA1c
|
Pourcentage de patients atteignant la valeur cible d'HbA1c
|
Changement de la glycémie à jeun
| |
|
(%)
|
(%)
|
<7,0 % (%)
|
≤6,5 % (%)
|
(mmol/l)
| |
26 semaines
| |
Dulaglutide combinéa (n = 103)
|
8,0
|
-0,7##
|
56,5##
|
46,7‡‡
|
-1,0#
| |
Dulaglutide 0,75 mg une fois par semaine (n = 51)
|
7,9
|
-0,5#
|
60,0##
|
48,9‡
|
-0,5#
| |
Dulaglutide 1,5 mg une fois par semaine (n = 52)
|
8,2
|
-1,0##
|
53,2##
|
44,7‡‡
|
-1,5#
| |
Placebo une fois par semaine (n = 51)
|
8,1
|
0,5
|
18,4
|
13,2
|
1,0
| |
52 semaines
| |
Dulaglutide combiné (n = 103)
|
8,0
|
-0,4
|
59,5
|
45,2
|
-0,63
| |
Dulaglutide 0,75 mg une fois par semaine (n = 51)
|
7,9
|
-0,2
|
65,0
|
55,0
|
-0,21
| |
Dulaglutide 1,5 mg une fois par semaine (n = 52)
|
8,2
|
-0,6
|
54,6
|
36,4
|
-0,95
| |
Placebo/dulaglutide 0,75 mg une fois par semaineb (n = 51)
|
8,1
|
-0,1
|
50,0
|
29,4
|
0,24
|
# p < 0,05, ## p < 0,001 pour la supériorité par rapport au placebo, valeurs p ajustées avec un contrôle général d'erreurs de type I.
‡ p < 0,05, ‡‡ p < 0,001 pour la supériorité par rapport au placebo
a Résultats combinés pour Trulicity 0,75 mg et 1,5 mg. La comparaison des deux doses combinées et individuelles était préspécifiée avec un contrôle général d'erreurs de type 1.
b Les patients qui, dans la phase initiale de 26 semaines en double aveugle, avaient été assignés à un traitement avec le placebo, ont commencé le traitement avec le dulaglutide 0,75 mg une fois par semaine dans la phase ouverte subséquente de 26 semaines.
|



