CompositionPrincipe actif
Paliperidonum (ut Paliperdoni palmitas).
Excipients
Polysorbatum 20, macrogolum 4000, acidum citricum monohydricum, natrii dihydrogenophosphas monohydricus, natrii hydroxidum, aqua ad injectabilie.
1 seringue préremplie à 175 mg contient 3.59 mg sodium.
1 seringue préremplie à 263 mg contient 5.40 mg sodium.
1 seringue préremplie à 350 mg contient 7.18 mg sodium.
1 seringue préremplie à 525 mg contient 10.78 mg sodium.
Indications/Possibilités d’emploiTrevicta, une forme galénique injectable trimestrielle de palmitate de palipéridone, est indiqué dans le traitement de la schizophrénie chez les patients adultes traités depuis au moins quatre mois de manière appropriée avec la forme galénique injectable mensuelle de palmitate de palipéridone.
Posologie/Mode d’emploiTrevicta ne doit être administré que lorsque le patient concerné a été traité de manière appropriée durant au moins quatre mois avec la forme injectable mensuelle de palmitate de palipéridone à libération prolongée. On recommande, pour la détermination d'une dose d'entretien unitaire, de donner les deux dernières injections mensuelles à libération prolongée aux mêmes doses que la première injection de Trevicta.
Posologie usuelle
Il faut commencer l'utilisation de Trevicta au moment prévu pour l'injection de la dose mensuelle suivante de palmitate de palipéridone. La dose de Trevicta se détermine d'après la dose précédente de palmitate de palipéridone mensuel injectée (voir tableau 1). Trevicta peut être administré jusqu'à 7 jours avant ou après le jour du mois prévu pour l'injection mensuelle suivante de palmitate de palipéridone.
Tableau 1: Conversion de la dernière dose mensuelle à libération prolongée de palmitate de palipéridone injectée à la dose trimestrielle à libération prolongée de suspension injectable de palmitate de palipéridone (Trevicta) par le facteur de multiplication 3,5
|
Si la dernière dose de l'injection mensuelle de palmitate de palipéridone était de:
|
Trevicta doit être commencé à la dose suivante:
| |
50 mg
|
175 mg
| |
75 mg
|
263 mg
| |
100 mg
|
350 mg
| |
150 mg
|
525 mg
|
Aucune étude n'a été menée pour convertir la dose mensuelle de 25 mg de l'injection de palmitate de palipéridone.
Après la dose initiale, Trevicta sera administré à intervalles de 3 mois. En cas de besoin, il est possible de procéder à une adaptation de la dose par paliers de 175 mg à 525 mg tous les 3 mois en fonction de la tolérance et/ou de l'efficacité chez le patient. Compte tenu de la longue durée d'action de Trevicta, la réaction du patient à un changement de dose peut n'apparaître qu'après plusieurs mois (voir «Pharmacocinétique»).
Omission d'une ou de plusieurs doses
Fenêtre posologique: Il faut dans toute la mesure du possible éviter l'omission de doses de Trevicta. Dans certains cas exceptionnels, on peut administrer l'injection jusqu'à 2 semaines avant ou après le jour de la prochaine dose trimestrielle.
Dose omise sur une période de plus de 3,5 mois et jusqu'à 4 mois: Si plus de 3,5 mois (jusqu'à 4 mois) se sont écoulés depuis la dernière injection de Trevicta, il faut injecter dès que possible une dose correspondant à la dernière administrée. Les injections suivantes devront à nouveau être administrées tous les 3 mois.
Dose omise sur une période de plus de 4 mois et jusqu'à 9 mois: Si plus de 4 mois (jusqu'à 9 mois) se sont écoulés depuis la dernière injection de Trevicta, on N'injectera PAS la dose suivante de Trevicta. On recommencera dans ce cas le traitement en se conformant au plan de traitement figurant dans le tableau 2.
Tableau 2: Réintroduction du traitement après l'omission de Trevicta sur une période de plus de 4 mois et jusqu'à 9 mois
|
Dernière dose trimestrielle de suspension injectable à libération prolongée de Trevicta
|
Administrer deux doses d'injection à libération prolongée de palmitate de palipéridone mensuel à une semaine d'intervalle (dans le muscle deltoïde)
|
Administrer ensuite la dose trimestrielle de suspension injectable à libération prolongée de Trevicta (dans le muscle deltoïdea ou dans le muscle fessier)
| |
|
Jour 1
|
Jour 8
|
1 mois après le jour 8
| |
175 mg
|
50 mg
|
50 mg
|
175 mg
| |
263 mg
|
75 mg
|
75 mg
|
263 mg
| |
350 mg
|
100 mg
|
100 mg
|
350 mg
| |
525 mg
|
100 mg
|
100 mg
|
525 mg
|
a Voir chapitre: «Remarques concernant l'utilisation» pour le choix de l'aiguille pour injection dans le muscle deltoïde en fonction du poids corporel.
Dose omise sur une période supérieure à 9 mois: Si plus de 9 mois se sont écoulés depuis la dernière injection de Trevicta, il convient de recommencer depuis le début le traitement par palmitate de palipéridone sous forme d'injections mensuelles de palmitate de palipéridone, selon les instructions figurant dans l'information professionnelle de cette préparation. L'utilisation de Trevicta ne pourra reprendre qu'une fois que le patient concerné aura été traité de façon adéquate avec l'injection mensuelle à libération prolongée de palmitate de palipéridone durant au moins quatre mois.
Passage d'un autre antipsychotique à Trevicta
'Trevicta ne doit être administré que lorsque le patient concerné a été traité de façon adéquate durant au moins quatre mois avec l'injection à libération prolongée de palmitate de palipéridone mensuel (voir «Indications/Possibilités d'emploi» et «Posologie/Mode d'emploi»).
Après l'arrêt de Trevicta, il convient de tenir compte de la libération prolongée du principe actif. Comme on le conseille aussi pour les autres antipsychotiques, il convient de réévaluer régulièrement l'indication à un traitement médicamenteux continu contre les éventuels symptômes extrapyramidaux (SEP).
Substitution de Trevicta par l'injection à libération prolongée mensuelle de palmitate de palipéridone
Pour le passage de Trevicta à l'injection mensuelle de palmitate de palipéridone, on administrera au moment prévu pour la prochaine injection de Trevicta une dose 3,5 fois inférieure de la suspension injectable mensuelle de palmitate de palipéridone (voir tableau 3). On poursuivra ensuite les injections à libération prolongée mensuelle de palmitate de palipéridone à intervalles d'un mois.
Tableau 3: Conversion de la dernière dose de suspension injectable à libération prolongée trimestrielle de palmitate de palipéridone (Trevicta) à l'injection à libération prolongée mensuelle de palmitate de palipéridone par le facteur de multiplication 3,5
|
Si la dernière dose de Trevicta était de:
|
l'injection mensuelle de palmitate de palipéridone sera administrée à la dose suivante:
| |
175 mg
|
50 mg
| |
263 mg
|
75 mg
| |
350 mg
|
100 mg
| |
525 mg
|
150 mg
|
On peut renoncer à la dose d'introduction telle qu'elle est décrite dans l'information professionnelle pour les injections à libération prolongée mensuelle de palmitate de palipéridone.
Substitution de Trevicta par les comprimés oraux à libération prolongée de palipéridone
Pour la substitution de Trevicta par les comprimés oraux à libération prolongée de palipéridone, on commencera les prises des doses journalières de comprimés à libération prolongée de palipéridone 3 mois après la dernière dose de Trevicta et on procédera à la substitution durant les mois suivants (voir tableau 4). Le tableau 4 présente un plan de conversion de dose pour atteindre une exposition de palipéridone avec les comprimés à libération prolongée une fois par jour comparable à celle obtenue sous des doses stables de Trevicta.
Tableau 4. Schéma à suivre pour la substitution de Trevicta par les comprimés à libération prolongée de palipéridone une fois par jour, afin d'atteindre une exposition comparable de palipéridone*
|
|
Semaines écoulées depuis la dernière dose de Trevicta
| |
≥3 mois jusqu'à ≤18 semaines
|
>18 semaines jusqu'à ≤24 semaines
|
>24 semaines
| |
Dernière dose de Trevicta
|
Dose journalière des comprimés oraux à libération prolongée de palipéridone
| |
175 mg
|
3 mg
|
3 mg
|
3 mg
| |
263 mg
|
3 mg
|
3 mg
|
6 mg
| |
350 mg
|
3 mg
|
6 mg
|
9 mg
| |
525 mg
|
6 mg
|
9 mg
|
12 mg
|
* Les doses des comprimés oraux à libération prolongée de palipéridone doivent être déterminées individuellement en fonction du motif du changement, de la réponse au traitement antérieur par palipéridone, de la sévérité des symptômes psychotiques et/ou de la tolérance.
Instructions posologiques particulières
Patients présentant des troubles de la fonction hépatique
Trevicta n'a pas été étudié chez les patients atteints d'insuffisance hépatique. D'après une étude réalisée avec la palipéridone orale, aucun ajustement posologique n'est nécessaire chez les patients présentant une insuffisance hépatique légère à modérée. La palipéridone n'a pas été évaluée chez les patients avec insuffisance hépatique sévère (voir «Pharmacocinétique»).
Patients présentant des troubles de la fonction rénale
Trevicta n'a pas fait l'objet d'études systématiques chez des patients atteints d'insuffisance rénale (voir «Pharmacocinétique»). Chez les patients avec insuffisance rénale légère (clairance de la créatinine ≥50 à <80 ml/min), on procède à un ajustement posologique lors de l'introduction du traitement injectable à libération prolongée de palmitate de palipéridone mensuel; il n'est pas nécessaire d'ajuster la dose de Trevicta. Comme cela a été décrit ci-dessus dans le chapitre «Posologie usuelle», le passage à Trevicta s'effectue avec une dose qui équivaut à 3,5 fois la dernière dose stabilisée de l'injection à libération prolongée de palmitate de palipéridone mensuel administrée. La dose maximale recommandée de Trevicta chez les patients avec insuffisance rénale légère est de 350 mg.
Trevicta n'est pas recommandé chez les patients avec insuffisance rénale modérée ou sévère (clairance de la créatinine <50 ml/min).
Patients âgés
Pour les patients âgés avec fonction rénale normale, on recommande en général les mêmes doses de Trevicta que pour les adultes plus jeunes avec fonction rénale normale. La fonction rénale pouvant être altérée chez les patients âgés, on se référera au chapitre «Patients présentant des troubles de la fonction rénale» ci-dessus pour les recommandations posologiques chez ces patients.
Enfants et adolescents
La sécurité et l'efficacité de Trevicta n'ont pas été étudiées chez les patients de moins de 18 ans.
Autres groupes de patients
Aucun ajustement de la dose de Trevicta n'est recommandé en fonction du sexe, de l'origine ethnique ou de la consommation de tabac. (Pour les femmes enceintes ou qui allaitent, voir «Grossesse, Allaitement».)
Mode d'administration
Avant leur administration, les médicaments parentéraux doivent être soumis à un contrôle visuel visant à chercher des corps étrangers ou une coloration. Il est important d'agiter vigoureusement la seringue pendant au moins 15 secondes dans les 5 minutes précédant l'injection de Trevicta au patient, afin d'assurer l'homogénéité de la suspension (voir «Remarques particulières»).
Trevicta est destiné uniquement à l'administration intramusculaire. Ne pas administrer par voie intravasale ou sous-cutanée. Éviter toute injection accidentelle dans un vaisseau sanguin. Les injections ne doivent être effectuées que par un professionnel médical. La dose doit être administrée sous la forme d'injections uniques; la dose ne doit pas être répartie sur plusieurs injections. L'injection doit être faite lentement par voie intramusculaire profonde dans le muscle deltoïde ou dans le muscle fessier.
Trevicta ne doit être administré qu'avec les aiguilles à paroi fine fournies avec les emballages de Trevicta. Les aiguilles de l'emballage contenant l'injection de palmitate de palipéridone mensuel ou les autres aiguilles disponibles sur le marché ne doivent pas être utilisées pour les injections de Trevicta.
La taille de l'aiguille recommandée pour l'injection de Trevicta dans le muscle deltoïde dépend du poids du patient. Pour les patients ≥90 kg (≥200 lbs), on recommande une aiguille à paroi fine de 1,5 pouce (3,81 cm) de long et un diamètre extérieur de 22 Gauge. Pour les patients <90 kg (<200 lbs), on recommande une aiguille à paroi fine de 1 pouce (2,54 cm) de long et un diamètre extérieur de 22 Gauge. Injecter au milieu du muscle deltoïde. Les injections dans le muscle deltoïde doivent se faire alternativement dans les deux muscles deltoïdes.
Pour l'administration de Trevicta dans le muscle fessier, on recommande le recours, indépendamment du poids corporel, à une aiguille à paroi fine de 1,5 pouce (3,81 cm) et un diamètre extérieur de 22 Gauge. L'injection est à faire dans le quadrant supéro-externe du muscle fessier. Les injections doivent se faire alternativement dans une fesse puis dans l'autre.
Comme la palipéridone est le métabolite actif de la rispéridone, la prudence est de mise lors de l'administration de Trevicta avec de la rispéridone ou avec de la palipéridone par voie orale sur une période prolongée. Les données de sécurité d'une administration simultanée de Trevicta avec d'autres antipsychotiques sont limitées.
Administration incomplète: Pour éviter des administrations incomplètes de Trevicta, il faut agiter vigoureusement la seringue prête à l'emploi pendant au moins 15 secondes, afin d'assurer l'homogénéité de la suspension [voir «Remarques particulières»]. Si la totalité de la dose n'est pas administrée, ne pas réinjecter le volume restant et ne pas administrer de nouvelle dose. Surveiller par contre étroitement le patient jusqu'à la prochaine dose trimestrielle de Trevicta prévue et le traiter en conséquence.
Contre-indicationsTrevicta est contre-indiqué chez les patients présentant une hypersensibilité connue à la palipéridone ou à un autre composant de la formulation. Comme la palipéridone est un métabolite actif de la rispéridone, Trevicta est contre-indiqué chez les patients avec hypersensibilité connue à la rispéridone.
Mises en garde et précautionsDans les études cliniques, la palipéridone était détectable dans le plasma jusqu'à 18 mois après une dose unique de Trevicta. La libération prolongée de la palipéridone après l'administration de Trevicta doit être prise en compte lors des réflexions thérapeutiques, en particulier en ce qui concerne les effets indésirables, les interactions pharmacocinétiques et pharmacodynamiques, ainsi que de la grossesse ou l'allaitement.
Syndrome malin des neuroleptiques
Des cas de syndrome malin des neuroleptiques (SMN) ont été rapportés en association avec les antipsychotiques, y compris la palipéridone. Le tableau se caractérise par une hyperthermie, une rigidité musculaire, une instabilité autonome, des troubles de la conscience et l'augmentation du taux de créatine phosphokinase sérique. D'autres signes cliniques peuvent être une myoglobinurie (rhabdomyolyse) et une insuffisance rénale aiguë. En présence d'indices cliniques de SMN chez un patient, il faut arrêter tous les antipsychotiques, y compris Trevicta. On tiendra dans ce cas compte de la longue durée d'action de Trevicta.
Dyskinésie tardive/Symptômes extrapyramidaux
Les médicaments ayant des propriétés antidopaminergiques sont associés à l'induction d'une dyskinésie tardive qui peut se manifester par des mouvements rythmiques involontaires, surtout de la langue et/ou du visage. En présence de symptômes d'une dyskinésie tardive, il faut envisager l'interruption de la prise de tous les antipsychotiques, y compris Trevicta. On tiendra dans ce cas compte de la longue durée d'action de Trevicta.
Symptômes extrapyramidaux et psychostimulants
La prudence est recommandée chez les patients recevant simultanément des psychostimulants (p.ex. du méthylphénidate) et de la palipéridone, car des symptômes extrapyramidaux sont susceptibles de survenir lors de l'ajustement posologique de l'un des médicaments ou des deux médicaments. Il convient d'envisager l'arrêt progressif de l'un des traitements ou des deux traitements (voir «Interactions»).
Intervalle QT
Comme avec d'autres antipsychotiques, la prudence est de rigueur lorsque Trevicta est prescrit chez des patients présentant des antécédents de troubles du rythme cardiaque, un syndrome du QT long congénital, ainsi qu'en cas d'utilisation simultanée avec d'autres médicaments susceptibles de prolonger l'intervalle QT.
Réactions d'hypersensibilité
De très rares cas de réactions anaphylactiques sont survenus à la suite de l'injection mensuelle de palmitate de palipéridone pendant la surveillance post-commercialisation chez des patients ayant préalablement bien toléré la rispéridone ou la palipéridone administrées par voie orale (voir «Posologie/Mode d'emploi» et «Effets indésirables»).
L'apparition de réactions d'hypersensibilité impose l'arrêt de l'utilisation de Trevicta; des mesures de soutien générales doivent être instaurées en fonction de l'indication clinique et le patient doit être surveillé jusqu'à la disparition des symptômes (voir «Contre-indications» et «Effets indésirables»).
Hyperglycémie et diabète sucré
Il existe des rapports sur la survenue d'hyperglycémies, d'un diabète sucré ou d'une aggravation d'un diabète préexistant sous traitement par médicaments antipsychotiques. L'évaluation de la relation entre l'utilisation d'antipsychotiques atypiques et des anomalies du glucose est compliquée par la possibilité d'une élévation du risque de fond de diabète sucré chez les patients schizophrènes et par l'incidence croissante du diabète sucré dans la population générale. Étant donné ces facteurs de confusion, la relation entre l'utilisation d'antipsychotiques atypiques et la survenue d'effets indésirables liés à une hyperglycémie n'est pas complètement élucidée. Tous les patients sous antipsychotiques atypiques, y compris Trevicta, doivent être surveillés à la recherche de symptômes d'hyperglycémie ou de diabète (voir «Effets indésirables»).
Prise de poids
Une prise de poids a été rapportée lors de l'utilisation d'antipsychotiques atypiques. Il convient de surveiller le poids corporel à intervalles réguliers.
Hypotension orthostatique
En raison de son activité α-bloquante, la palipéridone peut induire une hypotension orthostatique chez certains patients. Trevicta doit être utilisé avec prudence chez les patients présentant une maladie cardiovasculaire connue (par ex. insuffisance cardiaque, infarctus du myocarde ou ischémie, troubles de la conduction), une maladie cérébrovasculaire ou un état prédisposant à une hypotension (par ex. déshydratation, hypovolémie et traitement par antihypertenseurs).
Crises convulsives
Comme d'autres antipsychotiques, Trevicta doit être utilisé avec prudence chez les patients présentant des antécédents de crises convulsives ou d'autres états susceptibles de s'accompagner d'une diminution du seuil épileptogène.
Patients âgés atteints de démence
L'utilisation de Trevicta chez les patients âgés présentant une démence n'a pas été étudiée.
Mortalité globale
Dans une méta-analyse portant sur 17 études cliniques contrôlées, des patients âgés atteints de démence et traités par d'autres antipsychotiques atypiques, incluant la rispéridone, l'aripiprazole, l'olanzapine et la quétiapine, ont présenté une augmentation du risque de mortalité comparé au groupe placebo. Chez les patients traités par la rispéridone, la mortalité était de 4% contre 3,1% avec le placebo.
Effets indésirables cérébrovasculaires
Au cours d'études cliniques contrôlées par placebo chez des patients âgés atteints de démence et traités par certains antipsychotiques atypiques, dont la rispéridone, l'aripiprazole et l'olanzapine, le risque d'effets indésirables cérébrovasculaires (accident vasculaire cérébral et attaque ischémique transitoire), dont certains avec issue fatale, était augmenté par rapport au placebo.
Leucopénie, neutropénie et agranulocytose
Des cas de leucopénie, de neutropénie et d'agranulocytose ont été observés lors de l'utilisation d'antipsychotiques, y compris de la palipéridone. De très rares cas d'agranulocytose ont été observés dans le cadre de la surveillance post-commercialisation (chez moins de 1 sur 10'000 patients).
Pendant les premiers mois de traitement, il convient de surveiller les patients avec des antécédents de diminution cliniquement significative du nombre de leucocytes (LEU) ou de leucopénie/neutropénie d'origine médicamenteuse. Au premier signe de chute cliniquement significative de la numération leucocytaire et en l'absence d'autres facteurs causals, on doit envisager l'interruption du traitement par Trevicta.
Chez les patients avec neutropénie cliniquement significative, l'apparition de fièvre ou d'autres signes d'infection doit être soigneusement surveillée et il faut immédiatement instaurer un traitement si des symptômes de ce type apparaissent. Chez les patients présentant une neutropénie sévère (nombre absolu de neutrophiles <1× 109/l), le traitement par Trevicta doit être interrompu et le nombre de leucocytes surveillé jusqu'à sa normalisation complète.
On tiendra dans ce cas compte de la longue durée d'action de Trevicta.
Thromboembolie veineuse
Des cas de thromboembolies veineuses (TEV) ont été rapportés en lien avec l'utilisation d'antipsychotiques. Comme les patients traités par des antipsychotiques présentent souvent des facteurs de risque acquis de TEV, tout facteur de risque potentiel de TEV doit être identifié avant et pendant le traitement par Trevicta et des mesures préventives doivent être mises en œuvre.
Maladie de Parkinson et démence à corps de Lewy
Les antipsychotiques, dont Trevicta, ne doivent être prescrits aux patients atteints d'une maladie de Parkinson ou d'une démence à corps de Lewy (dementia with Lewy bodies, DLB) qu'après une évaluation médicale du rapport bénéfice-risque, car ces deux groupes de patients présentent un risque accru de syndrome malin des neuroleptiques et une sensibilité accrue aux antipsychotiques. Une telle augmentation de la sensibilité peut se manifester par exemple par un état confusionnel, une somnolence, des troubles de l'équilibre avec chutes fréquentes, ainsi que par des symptômes extrapyramidaux.
Priapisme
Selon certains rapports, les médicaments ayant des effets α-bloquants adrénergiques peuvent provoquer un priapisme. Depuis la commercialisation de la palipéridone, des cas de priapisme ont été rapportés (voir «Effets indésirables»).
Régulation de la température corporelle
Une association entre les antipsychotiques et la capacité de l'organisme à réduire la température centrale du corps a été décrite. La prudence est donc recommandée lors de la prescription de Trevicta à des patients exposés à des situations liées à une augmentation de la température centrale, par ex. lors d'un exercice physique intense, d'une exposition à une température extrêmement élevée, d'un traitement concomitant par des médicaments à action anticholinergique ou de déshydratation.
Effet antiémétique
Un effet antiémétique a été observé dans les études précliniques avec la palipéridone. Cet effet, lorsqu'il survient chez l'homme, peut masquer les signes d'un surdosage de certaines substances ou maladies telles qu'une obstruction intestinale, un syndrome de Reye et une tumeur cérébrale.
Administration
Éviter toute injection accidentelle de Trevicta dans un vaisseau sanguin.
Syndrome de l'iris hypotonique peropératoire
Des cas de syndrome d'iris hypotonique peropératoire (SIHP) ont été observés lors d'opérations de la cataracte chez des patients traités par des médicaments dotés d'un effet antagoniste sur les récepteurs α1a-adrénergiques, tel que Trevicta (voir «Effets indésirables»).
Le SIHP peut augmenter le risque de complications oculaires pendant et après l'intervention. Avant l'intervention, le chirurgien ophtalmologue doit être informé de la prise actuelle ou antérieure de médicaments dotés d'un effet antagoniste sur les récepteurs α1a-adrénergiques. Le bénéfice potentiel de l'interruption du traitement par les α-bloquants avant l'opération de la cataracte n'a pas été étudié et doit être évalué par rapport au risque d'une interruption du traitement antipsychotique.
Sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par seringue préremplie, c.-à-d. qu'il est essentiellement «sans sodium».
InteractionsLa prudence est recommandée lors de la prescription simultanée de Trevicta avec des médicaments connus pour allonger l'intervalle QT.
Le palmitate de palipéridone étant hydrolysé en palipéridone (voir «Pharmacocinétique»), il faut tenir compte des résultats des études réalisées avec la palipéridone orale lors de l'évaluation du potentiel d'interactions entre principes actifs.
Effets de Trevicta sur d'autres médicaments
Aucune interaction pharmacocinétique cliniquement significative entre la palipéridone et les médicaments métabolisés par les isoenzymes du cytochrome P450 n'est escomptée. Des études in vitro réalisées sur des microsomes hépatiques humains ont montré que la palipéridone n'inhibait pas sensiblement le métabolisme des principes actifs métabolisés par les isoenzymes du cytochrome P450, incluant les CYP1A2, CYP2A6, CYP2C8/9/10, CYP2D6, CYP2E1, CYP3A4, et CYP3A5. On admet donc que la palipéridone ne devrait pas inhiber de manière cliniquement significative la clairance des médicaments métabolisés par ces voies métaboliques. Par ailleurs, la palipéridone n'a probablement pas de propriétés d'induction enzymatique.
À fortes concentrations, la palipéridone exerce une légère action inhibitrice sur la glycoprotéine P (P-gp). Aucune donnée in vivo n'est disponible et la pertinence clinique n'est pas connue.
Compte tenu des effets primaires de la palipéridone sur le SNC (voir «Effets indésirables»), il faut faire preuve de prudence lors de l'utilisation de Trevicta en association avec d'autres médicaments agissant sur le SNC ou l'alcool. La palipéridone peut diminuer l'effet de la lévodopa et d'autres agonistes dopaminergiques.
Compte tenu de son potentiel d'induction d'une hypotension orthostatique (voir «Mises en garde et précautions: hypotension orthostatique»), il se peut que des effets additifs soient observés lors de l'administration de Trevicta avec d'autres médicaments présentant ce même potentiel.
L'administration concomitante de comprimés à libération prolongée de palipéridone à l'état d'équilibre (12 mg une fois par jour) et de comprimés à libération prolongée de divalproate de sodium (de 500 mg à 2000 mg une fois par jour) n'a pas affecté la pharmacocinétique à l'état d'équilibre du valproate.
Une interaction pharmacocinétique entre Trevicta et le lithium est peu probable.
Effets d'autres médicaments sur Trevicta
La palipéridone ne représente pas un substrat des CYP1A2, CYP2A6, CYP2C9, CYP2C19 et CYP3A5. Des interactions avec des inhibiteurs ou des inducteurs de ces isoenzymes sont donc improbables. Les études in vitro indiquent une faible implication du CYP2D6 et du CYP3A4 dans la dégradation de la palipéridone. Par contre, aucun examen in vitro ou in vivo n'indique que ces isoenzymes jouent un rôle important dans la dégradation de la palipéridone. Des études in vitro ont montré que la palipéridone était un substrat de la glycoprotéine-P (P-gp).
La palipéridone est métabolisée dans une faible mesure par le CYP2D6 (voir «Pharmacocinétique: métabolisme et élimination»). Dans une étude d'interactions, dans laquelle des volontaires sains ont reçu de la palipéridone orale associée avec de la paroxétine, un puissant inhibiteur du CYP2D6, aucun effet cliniquement significatif n'a été observé sur la pharmacocinétique de la palipéridone.
L'administration simultanée de palipéridone orale à libération prolongée une fois par jour et de 200 mg de carbamazépine deux fois par jour a entraîné une diminution d'environ 37% de la Cmax moyenne et de l'AUC de la palipéridone à l'état d'équilibre. Cette diminution est due, pour une large part, à une augmentation de 35% de la clairance rénale de la palipéridone résultant probablement de l'induction de la P-gp rénale par la carbamazépine. La diminution mineure de la quantité de principe actif inchangé excrétée dans l'urine suggère que l'administration simultanée de carbamazépine n'a que peu d'effets sur le métabolisme par le CYP ou sur la biodisponibilité de la palipéridone. Au début d'un traitement par la carbamazépine, la posologie de Trevicta devra être réévaluée et éventuellement augmentée. Inversement, à l'arrêt d'un traitement par la carbamazépine, la posologie de Trevicta devra être réévaluée et diminuée si nécessaire. On tiendra dans ce cas compte de la longue durée d'action de Trevicta.
La palipéridone, sous forme cationique à pH physiologique, est principalement excrétée par les reins sous forme inchangée et ce, environ pour moitié par filtration et pour moitié par sécrétion active. L'administration simultanée de triméthoprime, une substance connue pour son inhibition du transport cationique rénal actif de médicaments, n'a pas eu d'effets sur la pharmacocinétique de la palipéridone.
L'administration concomitante d'une dose unique d'un comprimé à libération prolongée de 12 mg de palipéridone et de comprimés à libération prolongée de divalproate de sodium (deux comprimés à 500 mg une fois par jour) a entraîné une élévation d'env. 50% de la Cmax et de l'AUC de la palipéridone, probablement à la suite d'une augmentation de l'absorption par la muqueuse buccale. Aucun effet sur la clairance systémique n'ayant été observé, aucune interaction cliniquement significative entre les comprimés à libération prolongée de divalproate de sodium et l'injection intramusculaire de Trevicta n'est attendue. Cette interaction n'a cependant pas été étudiée jusqu'ici avec Trevicta.
Une interaction pharmacocinétique entre Trevicta et le lithium est peu probable.
Utilisation simultanée de Trevicta en association avec la rispéridone ou la palipéridone orale
Comme la palipéridone est le métabolite actif principal de la rispéridone, la prudence est de mise lors de l'administration simultanée de Trevicta avec la rispéridone ou la palipéridone orale durant des périodes prolongées. Les données de sécurité d'une administration simultanée de Trevicta avec d'autres antipsychotiques sont limitées.
Utilisation simultanée de Trevicta et de psychostimulants
L'utilisation de psychostimulants (p.ex. méthylphénidate) en combinaison avec la palipéridone peut, en cas de modification de l'un des traitements ou des deux traitements, entraîner l'apparition de symptômes extrapyramidaux (voir «Mises en garde et précautions»).
Grossesse, allaitementGrossesse
La sécurité d'emploi du palmitate de palipéridone injecté par voie intramusculaire ou de la palipéridone administrée par voie orale pour l'utilisation pendant la grossesse n'a pas été étudiée.
Une étude de cohorte rétrospective d'observation, basée sur une banque de données américaine comportant des prestations de soins de santé remboursées, avait comparé le risque de malformations congénitales chez les enfants nés vivants chez des femmes ayant utilisé des antipsychotiques ou non au cours du premier trimestre de la grossesse. Lors de cette étude, une évaluation concrète de la palipéridone, le métabolite actif de la rispéridone, n'avait pas été effectuée. Après ajustement prenant en compte les variantes confondantes dans la banque de données, le risque de malformations congénitales en cas d'utilisation de rispéridone était augmenté par rapport à la non-utilisation de rispéridone (risque relatif = 1,26, IC 95%: 1,02-1,56). Aucun mécanisme biologique susceptible d'expliquer cette constatation n'avait pu être identifié et, lors des études précliniques, aucun effet tératogène n'avait été observé. En se fondant sur les résultats de cette unique étude d'observation, aucune relation causale entre l'exposition in utero à la rispéridone et les malformations congénitales n'a été mise en évidence.
Les nouveau-nés dont les mères ont reçu des antipsychotiques (dont la palipéridone) pendant le troisième trimestre de la grossesse présentent un risque de symptômes extrapyramidaux et/ou de symptômes de sevrage après la naissance. Ces symptômes chez les nouveau-nés peuvent être variables et comprendre une agitation, une hypertension, une hypotension, des tremblements, une somnolence, des difficultés respiratoires ou des problèmes d'alimentation. Ces complications peuvent avoir un degré de sévérité variable. Dans certains cas, ils ont été autolimitants; dans d'autres cas, les nouveau-nés ont nécessité une surveillance en service de soins intensifs ou une hospitalisation prolongée.
Comme la palipéridone reste détectable dans le plasma jusqu'à 18 mois après une dose unique de Trevicta, il convient de tenir compte de la longue durée d'action de Trevicta lors des réflexions. Une exposition maternelle à Trevicta avant et pendant la grossesse peut induire des effets indésirables chez le nouveau-né.
Les études sur des modèles animaux n'ont pas mis en évidence d'effets tératogènes, mais d'autres types d'effets toxiques pour la reproduction ont été constatés. Chez des animaux de laboratoire ayant reçu des doses élevées de palipéridone, une légère augmentation du nombre de morts fœtales a été observée (voir «Données précliniques»).
Trevicta ne doit pas être administré pendant la grossesse, sauf en cas de nécessité absolue. L'influence de Trevicta sur le déroulement de l'accouchement et de la naissance chez l'humain n'est pas connue.
Allaitement
Les expérimentations animales réalisées avec la palipéridone et les études menées chez l'humain avec la rispéridone ont montré que la palipéridone est excrétée dans le lait. Trevicta ne devrait pas être utilisé pendant l'allaitement.
Comme la palipéridone reste détectable dans le plasma jusqu'à 18 mois après une dose unique de Trevicta, il convient de tenir compte de la longue durée d'action de Trevicta lors des réflexions; l'administration de Trevicta même longtemps avant l'allaitement peut ainsi représenter un risque pour le nourrisson.
Effet sur l’aptitude à la conduite et l’utilisation de machinesTrevicta peut avoir une influence sur les activités nécessitant une vigilance intellectuelle et entraîner des effets sur la vision (voir «Effets indésirables»). Il faut donc avertir les patients de ne pas conduire de véhicule et de ne pas utiliser de machines tant qu'ils ne connaissent pas leur capacité de réaction individuelle.
Effets indésirablesLes effets indésirables sont présentés dans la section qui suit. Les effets indésirables sont des événements indésirables pour lesquels un lien plausible avec l'utilisation du palmitate de palipéridone est supposé sur la base d'une évaluation approfondie des informations disponibles au sujet de l'événement indésirable. Dans des cas isolés, un lien causal avec le palmitate de palipéridone ne peut pas être établi de manière fiable. En outre, comme les études cliniques sont exécutées dans des conditions variées, la fréquence des effets indésirables qui ont été observés au cours des études cliniques avec un médicament ne peut pas être directement comparée à la fréquence observée au cours des études cliniques menées avec un autre médicament, et elle ne correspond pas forcément à la fréquence de leur survenue observée en pratique clinique.
La palipéridone est le métabolite actif de la rispéridone. Les profils des effets secondaires des deux substances (y compris formulations orales et injectables) ont de ce fait une importance réciproque.
Résumé du profil de sécurité
La sécurité de la suspension injectable à libération prolongée de palmitate de palipéridone (injection mensuelle, injection trimestrielle et injection semestrielle (cette dernière n'est pas autorisée en Suisse)) a été évaluée dans des études cliniques chez 7565 patients atteints de schizophrénie et de trouble schizoaffectif.
La sécurité des comprimés à libération prolongée de palipéridone a été évaluée dans des études cliniques chez 2159 patients atteints de schizophrénie, de trouble schizoaffectif et de trouble bipolaire I.
La sécurité de la rispéridone (toutes les formulations) a été évaluée dans des études cliniques chez 12 195 patients atteints de schizophrénie, de trouble schizoaffectif, de trouble bipolaire, de trouble du spectre autistique, de troubles du comportement, chez des patients présentant un handicap mental léger à modéré, une démence, des troubles du comportement social, une démence de type Alzheimer, une maladie d'Alzheimer avec psychose ou des psychoses chroniques.
Les effets indésirables les plus fréquents (≥5%) rapportés au cours des études cliniques ont été: insomnie (12.0%), réactions au site d'injection (9.6%), prise de poids (9.6%), infections des voies respiratoires supérieures (9.4%), céphalées (8.8%), anxiété (7.4%), akathisie (6.7%) et parkinsonisme (6.1%).
Tous les effets indésirables qui sont survenus avec la palipéridone et/ou la rispéridone sont mentionnés ci-dessous. Ils sont classés par groupes de fréquence, les données relatives aux fréquences se rapportant uniquement aux études cliniques menées avec la suspension injectable à libération prolongée de palmitate de palipéridone (injection mensuelle, injection trimestrielle et injection semestrielle (cette dernière n'est pas autorisée en Suisse). Les effets secondaires rapportés pour le palmitate de palipéridone non pas lors des études cliniques, mais après l'autorisation de mise sur le marché, sont mentionnés dans la catégorie de fréquence fréquence inconnue. Il en est de même pour tous les effets indésirables observés pour la rispéridone (toutes les formes pharmaceutiques) ou la palipéridone orale dans les études cliniques ou après l'autorisation de mise sur le marché.
Les indications de fréquence utilisées sont les suivantes: Très fréquents (≥1/10), fréquents (<1/10, ≥1/100 ), occasionnels (<1/100, ≥1/1000 ), rares (<1/1000, ≥1/10 000 ), très rares (<1/10 000) et «fréquence inconnue» (les données cliniques disponibles ne permettent pas d'estimer la fréquence de l'effet indésirable).
Infections et infestations
Fréquents: infections des voies respiratoires supérieures, infections des voies urinaires, grippe.
Occasionnels: pneumonie, bronchite, infections des voies respiratoires, sinusite, cystite, otite, infection oculaire, amygdalite, onychomycose, cellulite, acrodermatite, abcès sous-cutané.
Affections hématologiques et du système lymphatique
Occasionnels: diminution du nombre de leucocytes, anémie, neutropénie, thrombocytopénie, augmentation du nombre de granulocytes éosinophiles.
Fréquence inconnuea: agranulocytose, baisse de l'hématocrite.
Affections du système immunitaire
Occasionnels: réactions d'hypersensibilité.
Fréquence inconnuea: réaction anaphylactique.
Affections endocriniennes
Fréquents: hyperprolactinémieb.
Rares: sécrétion inadéquate de l'hormone antidiurétique, glucosurie.
Troubles du métabolisme et de la nutrition
Fréquents: hyperglycémie, prise de poids, perte de poids, diminution de l'appétit, augmentation des triglycérides.
Occasionnels: diabèted, hyperinsulinémie, augmentation de l'appétit, anorexie, augmentation de la cholestérolémie, polydipsie.
Rares: acidocétose diabétique, hypoglycémie.
Fréquence inconnuea: intoxication à l'eau.
Affections psychiatriques
Très fréquents: insomniee.
Fréquents: agitation, dépression, anxiété.
Occasionnels: troubles du sommeil, manie, diminution de la libido, confusion, nervosité, cauchemars, anorgasmie.
Rares: catatonie, somnambulisme, perte d'affectivité.
Fréquence inconnuea: trouble alimentaire lié au sommeil (prise alimentaire incontrôlée lors du somnambulisme).
Affections du système nerveux
Très fréquents: céphalées.
Fréquents: parkinsonismec, akathisiec, somnolence, dystoniec, vertiges, dyskinésiec, tremblements.
Occasionnels: dyskinésie tardive, convulsionse, syncope, hyperactivité psychomotrice, vertige postural, troubles de l'attention, dysarthrie, dysgueusie, hypoesthésie, paresthésie, ischémie cérébrovasculaire.
Rares: syndrome malin des neuroleptiques, absence de réponse à la stimulation, perte de conscience, diminution du degré de conscience, troubles de l'équilibre, troubles de la coordination, tremblements au niveau de la tête.
Fréquence inconnuea: coma diabétique.
Affections oculaires
Occasionnels: vision floue, conjonctivite, sécheresse oculaire.
Rares: glaucome, trouble de la motricité oculaire, révulsion oculaire, photophobie, sécrétion lacrymale accrue, hyperémie oculaire.
Fréquence inconnuea: syndrome de l'iris hypotonique peropératoire.
Affections de l'oreille et du labyrinthe
Occasionnels: vertiges, acouphènes, otalgie.
Affections cardiaques
Fréquents: bradycardie, tachycardie.
Occasionnels: bloc auriculo-ventriculaire, trouble de la conduction, fibrillation auriculaire, allongement de l'intervalle QT à l'électrocardiogramme, syndrome de tachycardie orthostatique posturale, anomalies à l'électrocardiogramme, palpitations.
Rares: arythmies sinusales.
Affections vasculaires
Fréquents: hypertension.
Occasionnels: hypotension, hypotension orthostatique, embolie pulmonaire.
Rares: thrombose veineuse profonde, flush.
Fréquence inconnuea: ischémie.
Affections respiratoires, thoraciques et médiastinales
Fréquents: toux, nez bouché.
Occasionnels: dyspnée, stase pulmonaire, respiration haletante, douleurs pharyngolaryngées, épistaxis, stase dans les voies respiratoires.
Rares: syndrome d'apnée du sommeil, râle pulmonaire.
Fréquence inconnuea: hyperventilation, pneumonie d'aspiration, dysphonie.
Affections gastro-intestinales
Fréquents: douleur abdominale, vomissements, nausées, constipation, diarrhée, dyspepsie, douleurs dentaires.
Occasionnels: troubles abdominaux, gastro-entérite, dysphagie, sécheresse buccale, flatulence, gonflement de la langue.
Rares: pancréatite, obstruction intestinale, incontinence fécale, fécalome, chéilite.
Fréquence inconnuea: iléus.
Affections hépatobiliaires
Fréquents: augmentation des transaminases.
Occasionnels: augmentation des taux de gamma-glutamyl-transférase, augmentation des enzymes hépatiques.
Fréquence inconnuea: ictère.
Affections de la peau et du tissu sous-cutané
Fréquents: éruption cutanée.
Occasionnels: urticaire, prurit, alopécie, eczéma, sécheresse cutanée, érythème, acné.
Rares: exanthème médicamenteux, hyperkératose, dermatite séborrhéique, pellicules.
Fréquence inconnuea: syndrome de Stevens-Johnson/nécrolyse épidermique toxique, angio-œdème, modification de la couleur de la peau.
Affections musculosquelettiques et du tissu conjonctif
Fréquents: douleurs musculosquelettiques, dorsalgies, arthralgie.
Occasionnels: augmentation des taux de créatine phosphokinase, crampes musculaires, raideur articulaire, faiblesse musculaire, gonflement des articulations,.
Rares: rhabdomyolyse.
Fréquence inconnuea: posture anormale, douleurs de la nuque.
Affections du rein et des voies urinaires
Occasionnels: incontinence urinaire, pollakiurie, dysurie.
Rares: rétention urinaire.
Affections gravidiques, puerpérales et périnatales
Très rares: symptômes extrapyramidaux moteurs et/ou phénomènes de sevrage chez le nouveau-né (cf. «Grossesse, Allaitement»).
Affections des organes de reproduction et du sein
Fréquents: aménorrhée, galactorrhée, troubles menstruelse.
Occasionnels: dysfonction érectile, troubles de l'éjaculation, gynécomastie, dysfonction sexuelle, troubles mammaires, douleur mammaires, écoulement vaginal, augmentation du volume mammaire,.
Rares: priapisme, gonflement mammaire, écoulement mammaire.
Fréquence inconnuea: retard de règles.
Troubles généraux et anomalies au site d'administration
Fréquents: pyrexie, asthénie, fatigue, réactions au site d'injection.
Occasionnels: œdème facial, œdèmee, démarche anormale, augmentation de la température corporelle, douleur thoracique, symptômes thoraciques, sensation de maladie, induration, frissons.
Rares: hypothermie, , soif, syndrome de sevrage médicamenteux, abcès au site d'injection, cellulite au site d'injection, kyste au site d'injection, hématome au site d'injection.
Fréquence inconnuea: température corporelle diminuée, nécrose au site d'injection, ulcère au site d'injection.
Lésions, intoxications et complications liées aux procédures
Occasionnels: chute.
a La fréquence des effets indésirables est qualifiée comme «inconnue» car ils n'ont pas été observés lors d'essais cliniques portant sur le palmitate de palipéridone. Ils proviennent soit de rapports spontanés post-commercialisation et la fréquence ne peut être déterminée, soit de données issues d'essais cliniques et/ou de rapports post-commercialisation portant sur la rispéridone (quelle que soit la formulation) ou la palipéridone orale.
b Une hyperprolactinémie peut dans certains cas provoquer une gynécomastie, des troubles menstruels, une aménorrhée et une galactorrhée. Se référer à «Hyperprolactinémie» ci-dessous.
c Se référer à « Symptômes extrapyramidaux » ci-dessous.
d Dans les études contrôlées contre placebo, un diabète a été rapporté chez 0,32% des patients traités par Xeplion, comparé à un taux de 0,39% dans le groupe placebo. L'incidence totale dans toutes les études cliniques a été de 0,47% chez tous les patients traités par Xeplion.
e L'effet indésirable insomnie inclut troubles de l'endormissement et réveils nocturnes; les convulsions incluent: crises de grand mal; les œdèmes incluent: œdèmes généralisés, œdèmes périphériques, œdèmes prenant le godet («pitting edema»); les troubles menstruels incluent: irrégularité menstruelle, oligoménorrhée.
Description de certains effets indésirables et informations complémentaires
Suspension injectable à libération prolongée de palmitate de palipéridone, injection mensuelle
La sécurité de la suspension injectable à libération prolongée de palmitate de palipéridone (injection mensuelle) a été évaluée dans des études cliniques chez 4484 patients atteints de schizophrénie ou de trouble schizoaffectif. Les effets indésirables médicamenteux les plus fréquents (≥5%) ont été: insomnie (14,4%), céphalées (9,9%), infection des voies aériennes supérieures (7,3%), états anxieux (7,0%), réactions au site d'injection (7,0%), prise de poids (6,4%), parkinsonisme (6,2%) et akathisie (6,5%).
Les effets indésirables suivant ont été signalés plus fréquemment avec la suspension injectable à libération prolongée de palmitate de palipéridone (injection mensuelle) que dans les données de sécurité groupées pour l'injection mensuelle, l'injection trimestrielle et l'injection semestrielle (cette dernière n'est pas autorisée en Suisse), telles que décrites dans la liste des effets indésirables ci-dessus:
Très fréquents: bouche sèche, prurit.
Occasionnels: trouble de l'équilibre, hyperhémie oculaire, arythmie sinusale, incontinence fécale.
Suspension injectable à libération prolongée de palmitate de palipéridone, injection trimestrielle
La sécurité de la suspension injectable à libération prolongée de palmitate de palipéridone (injection trimestrielle) a été évaluée dans des études cliniques chez 1191 patients atteints de schizophrénie ou de trouble schizoaffectif. Les effets indésirables médicamenteux les plus fréquents (≥5%) ont été: prise de poids (13,5%), infection des voies aériennes supérieures (10,7%), états anxieux (7,6%), céphalées (6,7%), insomnie (6,0%) et réactions au site d'injection (5,3%).
Les effets indésirables suivant ont été signalés plus fréquemment avec la suspension injectable à libération prolongée de palmitate de palipéridone (injection trimestrielle) que dans les données de sécurité groupées pour l'injection mensuelle, l'injection trimestrielle et l'injection semestrielle (cette dernière n'est pas autorisée en Suisse), telles que décrites dans la liste des effets indésirables ci-dessus:
Très fréquents: infection des voies aériennes supérieures, prise de poids.
Fréquents: douleur pharyngolaryngée.
Occasionnels: glucose dans les urines, acidocétose diabétique, augmentation de la sécrétion lacrymale, chéilite.
Suspension injectable à libération prolongée de palmitate de palipéridone, injection semestrielle (non autorisée en Suisse)
La sécurité de la suspension injectable à libération prolongée de palmitate de palipéridone (injection semestrielle, non autorisée en Suisse) a été évaluée dans des études cliniques chez 478 patients atteints de schizophrénie ou de trouble schizoaffectif. Les effets indésirables médicamenteux les plus fréquents (≥5%) ont été: infection des voies aériennes supérieures (11,5%), réactions au site d'injection (10,7%), prise de poids (9,0%), céphalées (6,7%) et parkinsonisme (5,0%).
Les effets indésirables suivant ont été signalés plus fréquemment avec la suspension injectable à libération prolongée de palmitate de palipéridone (injection semestrielle, non autorisée en Suisse) que dans les données de sécurité groupées pour l'injection mensuelle, l'injection trimestrielle et l'injection semestrielle telles que décrites dans la liste des effets indésirables ci-dessus:
Très fréquents: urticaire, réactions au site d'injection.
Fréquents: anémie, diabète, gastroentérite, taux de créatine phosphokinase augmenté.
Occasionnels: tremblement de la tête, occlusion intestinale, dermite séborrhéique, priapisme.
Effets de classe
Allongements du QT, arythmies ventriculaires (fibrillation ventriculaire, tachycardie ventriculaire), cas de mort subite, arrêt cardiaque et torsades de pointes sont possibles sous traitement par des antipsychotiques. Des cas de thromboembolie veineuse, y compris embolie pulmonaire et thrombose veineuse profonde affectant la jambe, ont été rapportés sous antipsychotiques (cf. «Mises en garde et précautions»).
Symptômes extrapyramidaux (SEP).
Les données de la phase en double aveugle contrôlée par placebo de l'étude au long cours sur la prévention des récidives (voir «Propriétés/Effets: Efficacité clinique») ont montré que l'incidence des EI liés aux SEP dans le groupe Trevicta était plus élevée (13 patients [8,1%]) que dans le groupe placebo (5 patients [3,4%]).
Les symptômes extrapyramidaux (SEP) incluaient une analyse poolée des termes suivants: parkinsonisme (inclus trouble extrapyramidal, symptômes extrapyramidaux, phénomène on-off, maladie de Parkinson, crise parkinsonienne, hypersécrétion salivaire, raideur musculo-squelettique, parkinsonisme, salivation, phénomène de la roue dentée, bradykinésie, hypokinésie, faciès figé, tension musculaire, akinésie, rigidité de la nuque, rigidité musculaire, démarche parkinsonienne, réflexe palpébral anormal et tremblement parkinsonien de repos), akathisie (inclus akathisie, impatience, hyperkinésie et syndrome des jambes sans repos), dyskinésie (dyskinésie, chorée, trouble du mouvement, contractions musculaires, choréoathétose, athétose et myoclonie), dystonie (inclus dystonie, spasme cervical, emprosthotonos, crise oculogyre, dystonie oromandibulaire, rire sardonique, tétanie, hypertonie, torticolis, contractions musculaires involontaires, contracture musculaire, blépharospasme, crises oculogyres, paralysie de la langue, spasme facial, laryngospasme, myotonie, opisthotonus, spasme oropharyngé, pleurothotonus, spasme de la langue et trismus) et tremblement.
Dystonie
Effet de classe: des symptômes d'une dystonie (une contraction anormalement prolongée de groupes musculaires) peuvent survenir chez des patients y étant sensibles pendant les premiers jours du traitement et en cas de fortes doses de médicaments antipsychotiques. Un risque accru de dystonie aiguë est notamment observé chez les hommes et les patients jeunes.
Prise de poids
Dans une étude randomisée à long terme, évaluant l'arrêt du traitement, des augmentations anormales ≥7% du poids corporel depuis la phase en double aveugle jusqu'à la fin de l'étude ont été rapportées chez 10% des sujets du groupe Trevicta et 1% des sujets du groupe placebo. A l'inverse, des diminutions anormales du poids corporel (≥7%) depuis la phase en double aveugle jusqu'à la fin de l'étude ont été rapportées chez 1% des sujets du groupe Trevicta et 8% des sujets du groupe placebo. Les variations moyennes du poids corporel depuis la phase en double aveugle jusqu'à la fin de l'étude ont été, respectivement, de +0,94 kg et -1,28 kg pour les groupes Trevicta et placebo.
Hyperprolactinémie
Une hyperprolactinémie peut dans certains cas provoquer une gynécomastie, des troubles menstruels, une aménorrhée et une galactorrhée.
Durant la phase en double aveugle contrôlée par placebo de l'étude au long cours sur la prévention des récidives, on a observé des augmentations des taux de prolactine dépassant les intervalles de référence (>13,13 ng/ml chez les hommes et >26,72 ng/ml chez les femmes) chez une proportion plus élevée des patients du groupe Trevicta par rapport au groupe placebo (9% vs 3% et 5% vs 1%). Dans le groupe Trevicta, le changement moyen entre le début et la fin de la phase en double aveugle était de +2,90 ng/ml chez les hommes (vs -10,26 ng/ml dans le groupe placebo) et de +7,48 ng/ml chez les femmes (vs -32,93 ng/ml dans le groupe placebo). Une femme (2,4%) du groupe Trevicta a développé un effet indésirable sous la forme d'une aménorrhée, tandis que les femmes du groupe placebo n'ont pas présenté d'effets indésirables potentiellement en rapport avec la prolactine. Chez les hommes des deux groupes, aucun effet indésirable potentiellement en rapport avec la prolactine n'a été rapporté.
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageSignes et symptômes
En général, les caractéristiques et symptômes cliniques on peut s'attendre sont ceux résultant d'une exacerbation des effets pharmacologiques connus de la palipéridone, c.-à-d. obnubilation et sédation, tachycardie et hypotension, prolongement de l'intervalle QT et symptômes extrapyramidaux. Des tachycardies en torsades de pointes et une fibrillation ventriculaire ont été rapportées en rapport avec un surdosage de palipéridone orale. En cas de surdosage aigu, il faut envisager la possibilité d'une intoxication par plusieurs médicaments.
Traitement
Lorsque l'on évalue les besoins thérapeutiques et le rétablissement, il faut prendre en considération le fait qu'il s'agit avec Trevicta d'une forme à libération prolongée [effet dépôt] et le fait que la palipéridone a une longue demi-vie apparente. Il n'existe pas d'antidote spécifique de la palipéridone. Des mesures générales de soutien des fonctions vitales doivent être mises en œuvre. Il faut libérer les voies aériennes et les garder dégagées, assurer une oxygénation et une ventilation adéquates. Il faut immédiatement instaurer un monitoragecardiovasculaire, y compris une surveillance par ECG continu, pour détecter d'éventuelles arythmies. Une hypotension et une insuffisance cardio-circulatoire doivent être traitées par des mesures appropriées telles qu'une administration intraveineuse de solutés et/ou l'administration d'agents sympathomimétiques. En cas de symptômes extrapyramidaux sévères, il convient d'administrer des anticholinergiques. Le patient doit faire l'objet d'une surveillance étroite jusqu'à son rétablissement.
Propriétés/EffetsCode ATC
N05AX13
Trevicta contient un mélange racémique de palipéridone (+) et (-).
Mécanisme d'action / Pharmacodynamique
Le palmitate de palipéridone, le principe actif de Trevicta, est un agent psychotrope qui appartient à la classe chimique des dérivés du benzisoxazole (antipsychotique neuroleptique atypique). Trevicta contient un mélange racémique de palipéridone (+) et (-).
Le palmitate de palipéridone est hydrolysé en palipéridone (voir «Données précliniques»). La palipéridone est un antagoniste des récepteurs dopaminergiques D2 à action centrale qui a une activité antagoniste marquée sur les récepteurs sérotoninergiques 5-HT2A. La palipéridone exerce en outre un effet antagoniste sur les récepteurs adrénergiques α1 et α2 et sur les récepteurs histaminergiques H1. Elle n'a pas d'affinité pour les récepteurs cholinergiques muscariniques ou pour les récepteurs adrénergiques β1 et β2. L'activité pharmacologique des énantiomères (+) et (-) de la palipéridone est qualitativement et quantitativement similaire.
Tout comme le mécanisme d'action des autres médicaments efficaces dans le traitement de la schizophrénie, celui de la palipéridone est inconnu. Il a néanmoins été avancé que l'effet thérapeutique de la palipéridone dans la schizophrénie pourrait être médié par un effet antagoniste s'exerçant à la fois sur les récepteurs dopaminergiques de type 2 (D2) et sur les récepteurs sérotoninergiques de type 2 (5-HT2A). Certains des autres effets de la palipéridone pourraient s'expliquer par une action antagoniste sur des récepteurs autres que les récepteurs D2 et 5-HT2A.
Efficacité clinique
L'efficacité de Trevicta dans le traitement de la schizophrénie a été examinée dans le cadre d'une étude au long cours en double aveugle et contrôlée par placebo sur la prévention des récidives ou avec un sevrage randomisé, ainsi que d'une étude en double aveugle au long cours de non-infériorité avec contrôle actif chez des patients ayant été traités de manière adéquate pendant au moins 4 mois par des injections à libération prolongée mensuelle de palmitate de palipéridone.
Étude de prévention des récidives ou avec sevrage randomisé
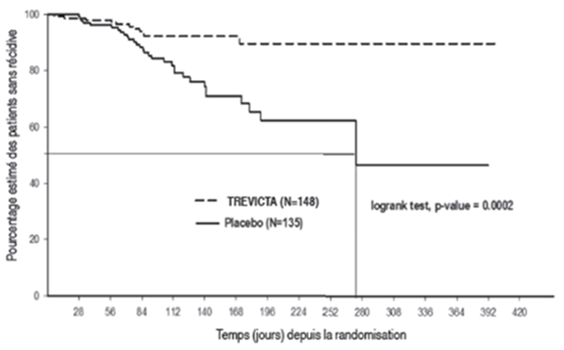
Dans l'étude de sevrage randomisée au long cours, 506 patients adultes répondant aux critères DSM IV pour la schizophrénie ont été inclus dans la phase de transition ouverte et ont reçu durant 17 semaines des doses flexibles de palmitate de palipéridone sous forme d'injection mensuelle à libération prolongée dans le muscle deltoïde ou fessier (50–150 mg) (des ajustements de la posologie ont eu lieu aux semaines 5 et 9). Au total, 379 patients ont ensuite reçu dans la phase de stabilisation ouverte une dose unique de Trevicta, soit dans le muscle deltoïde soit dans le muscle fessier (la dose correspondait à 3,5 fois la dernière dose d'injection mensuelle de palmitate de palipéridone). Les patients qui étaient considérés comme cliniquement stables à la fin de la phase de stabilisation de 12 semaines ont été randomisés à un rapport de 1:1 dans une phase en double aveugle de durée variable pour recevoir soit Trevicta soit un placebo (la dose de Trevicta correspondait à la dernière dose administrée dans le cadre de la phase de stabilisation; cette dose est restée identique pendant toute la durée de la phase en double aveugle). Durant cette phase, 305 patients avec symptomatologie stable ont été randomisés pour la poursuite du traitement par Trevicta (n = 160) ou placebo (n = 145) jusqu'à la survenue d'une récidive, jusqu'à un abandon prématuré ou jusqu'à la fin de l'étude. Le critère d'efficacité primaire était le délai jusqu'à l'apparition de la première récidive. Une analyse intermédiaire programmée, réalisée après que 283 patients ont été randomisés et que 42 événements de récidive ont été documentés, a montré un délai statistiquement significativement plus long (p <0,001) jusqu'à la survenue d'une récidive chez les patients sous Trevicta versus placebo. Un événement de récidive est survenu chez 23% des patients du groupe placebo et chez 7,4% des patients sous Trevicta. L'étude a été interrompue en raison de ces événements d'efficacité. Le hazard ratio était de 3,45 (IC 95%: 1,73; 6,88), autrement ditt une diminution de 71% du risque de récidive sous Trevicta versus placebo a été atteinte. La figure 1 représente une courbe de Kaplan-Meier de la période allant jusqu'à la survenue d'une récidive dans les groupes de traitement. Le graphique représente en outre la période jusqu'à la survenue d'une récidive dans le groupe placebo, qui était significativement plus courte (médiane de 274 jours) que dans le groupe Trevicta (une évaluation de la médiane n'était pas possible en raison du faible pourcentage de patients avec récidive [7,4%]).
Figure 1: Courbe de Kaplan-Meier de la période jusqu'à la survenue d'une récidive – analyse intermédiaire
Étude de non-infériorité
Dans l'étude de non-infériorité, 1429 patients souffrant d'une maladie aiguë (valeur initiale du score global PANSS moyen: 85,7) ont été inclus dans la phase ouverte et traités pendant 17 semaines par injections à libération prolongée mensuelles de palmitate de palipéridone. La dose pouvait être adaptée aux semaines 5 et 9 (c.-à-d. 50 mg, 75 mg, 100 mg ou 150 mg) et les injections pouvaient se faire au niveau du muscle deltoïde ou du muscle fessier. Des patients qui remplissaient les critères de randomisation aux semaines 14 et 17, 1016 ont été randomisés dans un rapport de 1:1 pour soit poursuivre les injections mensuelles de palmitate de palipéridone, soit passer à Trevicta à des doses de 3,5 fois la dose mensuelle injectée de palmitate de palipéridone aux semaines 9 et 13. La durée du traitement était de 48 semaines dans les deux groupes. Les patients ont reçu Trevicta une fois tous les 3 mois et des injections de placebo les autres mois pour assurer le caractère aveugle du traitement.
Le critère d'évaluation primaire de l'étude était le pourcentage de patients sans récidive à la fin de la phase en double aveugle de 48 semaines, partant de la valeur estimée sur la courbe de Kaplan-Meier après 48 semaines (Trevicta: 91,2%, de l'injection à libération prolongée mensuelle de palmitate de palipéridone: 90,0%). La durée d'exposition moyenne (SD) pendant la phase en double aveugle était de 295 (88) jours sous Trevicta et de 287 (96) jours dans le groupe sous palmitate de palipéridone en injection mensuelle. Compte tenu de la faible proportion de patients avec récidive, il n'a été possible d'évaluer la durée médiane jusqu'à la survenue d'une récidive dans aucun des deux groupes. La différence (IC 95%) entre les groupes de traitement était de 1,2% (-2,7%, 5,1%), si bien que le critère de non-infériorité fixé préalablement et basé sur un seuil de -15% était rempli. Trevicta n'était par conséquent pas inférieur au traitement par palmitate de palipéridone sous forme d'injection mensuelle à libération mensuelle. Les améliorations fonctionnelles mesurées par l'échelle PSP (échelle d'appréciation des fonctions personnelles et sociales) et observées pendant la phase de stabilisation ouverte sont restées présentes dans les deux groupes au cours de la phase en double aveugle.
Figure 2: La courbe de Kaplan-Meier de la durée jusqu'à la survenue d'une récidive sous Trevicta versus injection mensuelle de palmitate de palipéridone

Les résultats de l'efficacité étaient consistants dans tous les sous-groupes du collectif (sexe, âge et appartenance ethnique) dans les deux études.
PharmacocinétiqueAbsorption
En raison de sa solubilité extrêmement faible, le palmitate de palipéridone dans sa galénique d'injection trimestrielle à libération prolongée se dissout lentement après injection intramusculaire, avant d'être hydrolysé en palipéridone et absorbé dans la circulation sanguine. La libération du principe actif débute déjà le 1er jour et se poursuit jusqu'à 18 mois.
Les données mentionnées dans ce paragraphe sont basées sur une analyse pharmacocinétique de population. Après une dose intramusculaire unique de Trevicta, les taux plasmatiques de palipéridone augmentent progressivement jusqu'à la concentration maximale avec une Tmax médiane de 30-33 jours. Après l'injection intramusculaire de doses de Trevicta comprises entre 175 et 525 mg dans le muscle deltoïde, on a observé en moyenne une Cmax supérieure de 11 à 12% à celle obtenue après une injection dans le muscle fessier. Le profil de libération et le schéma posologique de Trevicta entraîne le maintien des concentrations thérapeutiques. L'exposition totale à la palipéridone après l'injection de Trevicta était dose-proportionnelle sur une plage de doses allant de 175 à 525 mg et environ dose-proportionnelle pour la Cmax. Le rapport moyen des valeurs maximales et minimales à l'état d'équilibre après une dose de Trevicta était de 1,6 après une injection dans le muscle fessier et de 1,7 après une injection dans le muscle deltoïde.
Distribution
Le volume de distribution apparent de la palipéridone après l'administration de Trevicta est de 1960 litres.
La liaison de la palipéridone racémique aux protéines plasmatiques est de 74%.
Après l'administration de Trevicta, il se produit une interconversion des énantiomères (+) et (-) de la palipéridone et le rapport AUC(+)/(-) est d'environ 1,7 à 1,8.
Métabolisme
Dans une étude menée avec la 14C-palipéridone à libération immédiate, on a retrouvé 59% de la dose sous forme inchangée dans l'urine après une dose orale unique de 1 mg de 14C-palipéridone à libération immédiate, ce qui signifie que la palipéridone ne semble pas être métabolisée dans le foie de manière extensive. Environ 80% de la radioactivité administrée a été retrouvée dans les urines et 11% dans les selles. Quatre voies métaboliques ont été identifiées in vivo, aucune d'entre elles ne comptant pour plus de 10% de la dose: déalkylation, hydroxylation, déshydrogénation et dissociation du benzisoxazole. Bien que les études in vitro suggèrent une participation possible du CYP2D6 et du CYP3A4 au métabolisme de la palipéridone, il n'y a pas de données in vivo qui indiquent un rôle significatif de ces deux isoenzymes dans le métabolisme de la palipéridone. Des analyses pharmacocinétiques de populations n'ont pas montré de différence manifeste entre les métaboliseurs extensifs et les métaboliseurs lents des substrats du CYP2D6 par rapport à la clairance apparente de la palipéridone après la prise de palipéridone orale. Des études in vitro réalisées sur des microsomes hépatiques humains ont montré que la palipéridone n'inhibait pas sensiblement le métabolisme des principes actifs métabolisés par les isoenzymes du cytochrome P450, incluant les CYP1A2, CYP2A6, CYP2C8/9/10, CYP2D6, CYP2E1, CYP3A4, et CYP3A5.
Les études effectuées in vitro ont montré que la palipéridone est un substrat de la P-gp et un léger inhibiteur de la P-gp à fortes concentrations. Aucune donnée in vivo n'est disponible et la pertinence clinique n'est pas connue.
D'après l'analyse pharmacocinétique de population, la demi-vie apparente médiane de la palipéridone après l'administration de Trevicta à des doses de 175 à 525 mg était de 84 à 95 jours après injection dans le muscle deltoïde et de 118 à 139 jours après injection dans le muscle fessier.
Suspension injectable à libération prolongée de palmitate de palipéridone trimestriel versus autres formulations de palipéridone
Trevicta est destiné à un traitement de palipéridone tous les 3 mois, alors que le palmitate de palipéridone injectable mensuel doit être administré tous les mois. Lorsque Trevicta est donné à des doses 3,5 fois supérieures à la dose correspondante injectable de palmitate de palipéridone mensuel, il en résulte une exposition à la palipéridone comparable à celle qui suit une dose mensuelle correspondante de palmitate de palipéridone mensuel ou d'une dose correspondante sous la forme de comprimés à libération prolongée de palmitate de palipéridone une fois par jour. La plage d'exposition lors de l'administration de Trevicta se situe à l'intérieur des plages d'exposition obtenues avec les comprimés à libération prolongée de palmitate de palipéridone aux doses autorisées.
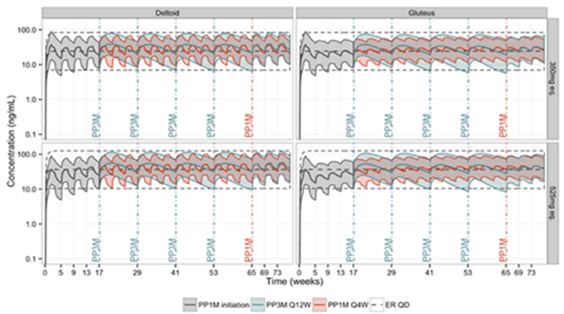
La figure 3 montre les profils pharmacocinétiques médians pronostiqués pour une population donnée de la palipéridone après l'administration de Trevicta aux doses de 350 mg et de 525 mg versus injections mensuelles de 100 mg et 150 mg de palmitate de palipéridone mensuel et prise de comprimés retard à libération prolongée (8 mg ou 12 mg). Un traitement d'au moins 4 mois par des injections de palmitate de palipéridone mensuel avant l'introduction de Trevicta a permis de maintenir l'exposition plasmatique à la palipéridone à l'état d'équilibre.
Figure 3: Concentrations plasmatiques de palipéridone pronostiquées au cours du temps après administration de Trevicta (PP3M) en groupes de doses de 350 mg et 525 mg par rapport à l'administration mensuelle d'injections de palmitate de palipéridone mensuel (PP1M) aux doses de 100 mg ou 150 mg. Les lignes en pointillé montrent les concentrations de palipéridone pronostiquées après prise de comprimés à libération prolongée de palipéridone 8 mg et 12 mg
Élimination
Voir Métabolisme.
Cinétique pour certains groupes de patients
Troubles de la fonction hépatique
La palipéridone n'est pas métabolisée de façon extensive dans le foie. Trevicta n'a certes pas été étudié chez des patients avec insuffisance hépatique, mais aucune adaptation des doses n'est nécessaire chez les patients en insuffisance hépatique légère ou modérée. Dans une étude avec la palipéridone orale sur des sujets présentant une insuffisance hépatique moyenne (classe Child-Pugh B), les concentrations plasmatiques de la palipéridone libre étaient similaires à celles obtenues sur les volontaires sains. La palipéridone n'a pas été évaluée chez les patients avec insuffisance hépatique sévère.
Troubles de la fonction rénale
Trevicta n'a pas été étudié de façon systématique chez les patients atteints d'insuffisance hépatique. La disponibilité d'une dose orale unique de type comprimé à libération prolongée à 3 mg de palipéridone a été étudiée chez des patients avec différents degrés d'insuffisance rénale. L'élimination de la palipéridone diminue lorsque la clairance rénale estimée de la créatinine baisse. Chez les sujets insuffisants rénaux participant à l'étude, la clairance totale de la palipéridone était inférieure de 32% en cas d'insuffisance rénale légère (CrCl = 50 à <80 ml/min), de 64% en cas d'insuffisance rénale modérée (CrCl = 30 à <50 ml/min) et de 71% en cas d'insuffisance rénale sévère (CrCl = 10 à <30 ml/min). Cela correspond à une exposition (AUCinf) en moyenne 1,5, 2,6 et 4,8 fois supérieure à celle observée chez les sujets sains. Sur la base d'un petit nombre d'observations avec Trevicta chez des sujets avec insuffisance rénale légère et de simulations pharmacocinétiques, on conseille chez les patients atteints d'une insuffisance rénale légère une réduction des doses d'induction et d'entretien d'injection de palmitate de palipéridone mensuel. Ces patients peuvent être passés sous Trevicta à la dose correspondante calculée par le facteur de multiplication 3,5. Aucune réduction supplémentaire des doses n'est nécessaire après l'introduction de Trevicta (voir «Posologie/Mode d'emploi»).
Patients âgés
Il n'est pas recommandé d'ajuster la dose sur la seule base de l'âge. Une adaptation de la dose peut néanmoins être nécessaire en raison d'une diminution de la clairance rénale en fonction de l'âge (voir «Troubles de la fonction rénale» et «Posologie/Mode d'emploi»).
Origine ethnique
Une analyse pharmacocinétique de population sur des données provenant d'études réalisées avec la palipéridone orale n'a montré aucune différence liée à l'origine ethnique en ce qui concerne la pharmacocinétique de la palipéridone après l'utilisation de Trevicta.
Sexe
Aucune différence significative n'a été mise en évidence entre les hommes et les femmes.
Tabagisme
Les études in vitro avec des enzymes hépatiques humaines permettent de conclure que la palipéridone n'est pas un substrat du CYP1A2; le tabagisme ne devrait donc avoir aucune influence sur la pharmacocinétique de la palipéridone. En corrélation avec ces résultats obtenus in vitro, une analyse pharmacocinétique de population n'a pas montré de différence entre les fumeurs et les non-fumeurs.
Indice de masse corporelle (IMC)/Poids corporel
Aucune adaptation des doses en fonction de l'IMC n'est nécessaire. Une Cmax plus basse a été observée chez les patients en surpoids et chez les patients obèses. À l'état d'équilibre apparent sous Trevicta, les concentrations minimales étaient comparables chez les patients de poids normal, chez les patients en surpoids et chez les patients obèses.
Données précliniquesToxicité à long terme (ou toxicité en cas d'administration répétée)
Comme avec d'autres antagonistes du récepteur dopaminergique D2, on a mesuré des augmentations de la prolactinémie après des doses répétées dans le cadre des études de toxicité lors d'injections intramusculaires de palmitate de palipéridone et d'administration orale de palipéridone.
Aucun effet sur la croissance, la maturation sexuelle et les performances de reproduction n'a été constaté dans une étude de toxicité de 7 semaines chez de jeunes rats avec des doses de palipéridone orale de 0,16, 0,63 et 2,5 mg/kg/jour. Des doses orales allant jusqu'à 2,5 mg/kg/jour n'ont pas affecté le développement comportemental neurologique chez les animaux femelles ou mâles; un effet sur l'apprentissage et la mémoire a néanmoins été mis en évidence chez les rats femelles avec 2,5 mg/kg/jour. Cet effet du traitement n'était plus présent après l'arrêt du traitement. La marge de sécurité basée sur la Cmax et l'AUC était chez les rats mâles sous 2,5 mg/kg/jour de 9 ou 2 fois et de 2, et 0,6 fois chez les rats femelles sous 0,63 mg/kg/jour par rapport à la dose maximale journalière de 12 mg chez l'homme.
Dans une étude sur 40 semaines chez de jeunes chiens recevant de la rispéridone orale (qui est essentiellement métabolisée en palipéridone) aux doses de 0,31, 1,25 et 5 mg/kg/jours, aucune influence sur la maturation sexuelle n'a été constatée sous des doses de 0,31 et 1,25 mg/kg/jour. Un effet sur la croissance des os longs a été observé avec des doses de 1,25 et 5 mg/kg/jour, alors que cet effet était absent sous 0,31 mg/kg/jour.
Mutagénicité
Le test de mutation inverse (test d'Ames), le test du lymphome de souris, ainsi que le test du micronoyau chez le rat n'ont pas mis en évidence de potentiel mutagène. Le palmitate de palipéridone n'a pas eu de propriétés génotoxiques au test de mutation inverse d'Ames ni au test du lymphome de souris.
Cancérogénicité
Le potentiel cancérigène du palmitate de palipéridone injecté par voie intramusculaire a été évalué chez le rat. Une augmentation statistiquement significative de l'incidence des adénocarcinomes mammaires a été constatée chez les rats femelles à des doses de 10, 30 et 60 mg/kg/mois. Des rats mâles ont présenté une augmentation statistiquement significative de l'incidence des adénomes et des carcinomes mammaires à des doses de 30 et 60 mg/kg/mois. Cela correspond à des expositions de l'ordre de 0,6 et 1,2 fois l'AUC chez l'homme sous la dose journalière maximale recommandée de 525 mg.
Le potentiel carcinogène de la palipéridone orale, un métabolite actif de la rispéridone, a été évalué sur la base d'études menées avec la rispéridone chez la souris et le rat. Les souris ont été traitées par la rispéridone pendant 18 mois et les rats pendant 25 mois, à des doses allant jusqu'à 10 mg/kg/jour. Une augmentation statistiquement significative de la fréquence des adénomes de l'hypophyse, des adénomes du pancréas endocrine et des adénocarcinomes mammaires a été observée. Une augmentation de la fréquence des tumeurs mammaires, hypophysaires et du pancréas endocrine a été observée après l'administration chronique d'autres antipsychotiques à des rongeurs. On suppose que cette augmentation est due à l'antagonisme dopaminergique D2 prolongé. La pertinence de l'observation de tumeurs chez les rongeurs pour le risque chez l'homme est inconnue.
Toxicité sur la reproduction
Développement fœtaux-embryonnaire
Les études sur le développement embryonnaire et fœtal n'ont montré aucun effet tératogène après administration orale d'une dose atteignant jusqu'à 10 mg/kg/jour de palipéridone chez le rat et jusqu'à 5 mg/kg/jour chez le lapin. Le nombre de fœtus de lapin survivants a été plus faible à une dose de 5 mg/kg/jour et cette dose a également induit une toxicité maternelle. Après administration intramusculaire de palmitate de palipéridone à des rattes portantes, aucune embryotoxicité ou tératogénicité n'ont été observées jusqu'à la dose maximale (160 mg/kg) correspondant à 2,2 fois le niveau d'exposition chez l'humain à la dose maximale recommandée de 525 mg.
Fertilité
Bien qu'un traitement par la palipéridone orale ait entraîné des effets médiés par la prolactine et le SNC, aucun effet sur la fertilité de rats mâles et femelles n'a été observé. Le nombre d'embryons vivants a diminué sous doses toxiques pour la mère de 2,5 mg/kg/jour. Chez le chien, une diminution de la motilité des spermatozoïdes et de la concentration plasmatique de testostérone a été décrite pour la rispéridone orale après l'administration de doses équivalentes à la dose maximale recommandée de rispéridone chez l'humain. Chez le rat femelle (mais non chez le rat mâle), une altération du comportement d'accouplement a été constatée sous rispéridone, tandis qu'aucun effet sur la fertilité n'a été observé.
Remarques particulièresIncompatibilités
Trevicta ne doit pas être mélangé avec d'autres produits ou solvants et doit être injecté par voie intramusculaire, directement depuis la seringue dans laquelle il est conditionné.
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur l'emballage.
Remarques particulières concernant le stockage
Ne pas conserver au-dessus de 30 °C.
Conserver hors de portée des enfants.
Numéro d’autorisation66054 (Swissmedic).
PrésentationKit constitué d'une seringue préremplie (copolymère d'oléfine cyclique), contenant une suspension de 175 mg (0,875 ml), 263 mg (1,315 ml), 350 mg (1,75 ml) ou 525 mg (2,625 ml) de palipéridone (sous forme de 273 mg, 410 mg, 546 mg ou 819 mg de palmitate de palipéridone), un bouchon-piston et un capuchon de seringue (caoutchouc bromobutyle), une valve antiretour et 2 types de seringues du commerce: une aiguille à paroi fine de sécurité 22G d'une longueur de 1,5 pouce (3,81 cm) et une aiguille à paroi fine de sécurité 22G d'une longueur de 1 pouce (2,54 cm). [B]
Titulaire de l’autorisationJanssen-Cilag AG, Zoug, ZG.
Mise à jour de l’informationMars 2023
Remarques concernant l'utilisation, la manipulation et l'élimination
Trevicta
Suspension injectable à libération prolongée pour injection intramusculaire

Uniquement destiné à l'injection intramusculaire. Ne pas l'administrer d'une autre manière.
Important
Trevicta doit être administré sous forme d'injection unique par un/une professionnel/le de santé. Ne pas répartir la dose sur plusieurs injections.
Trevicta est destiné uniquement à l'administration intramusculaire. Injecter lentement et profondément dans le muscle en évitant toute injection dans un vaisseau sanguin.
Lire tout le mode d'emploi avant l'utilisation.
Posologie
Ce médicament doit être injecté une seule fois tous les 3 mois.
Préparation
Retirer l'étiquette à languette de la seringue et l'intégrer au dossier du patient.
Trevicta doit être agité plus longtemps et plus vigoureusement que le palmitate de palipéridone en injection à libération prolongée mensuelle. Agiter vigoureusement en tenant l'embout de la seringue vers le haut pendant au moins 15 secondes dans les 5 minutes précédant l'injection (voir Étape 2).
Choix de l'aiguille à paroi fine de sécurité
Trevicta est administré au moyen d'aiguilles à paroi fine de sécurité spéciales. Seules les aiguilles contenues dans le kit Trevicta doivent être utilisées.
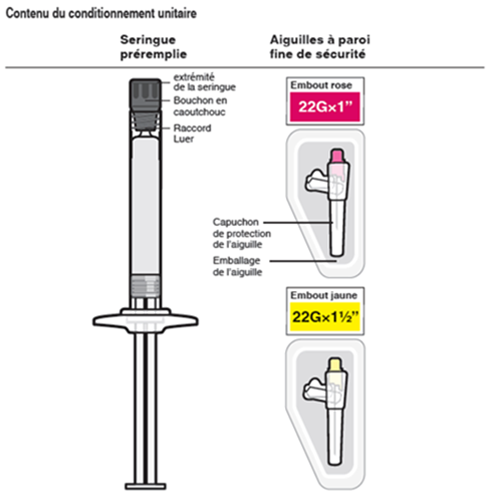
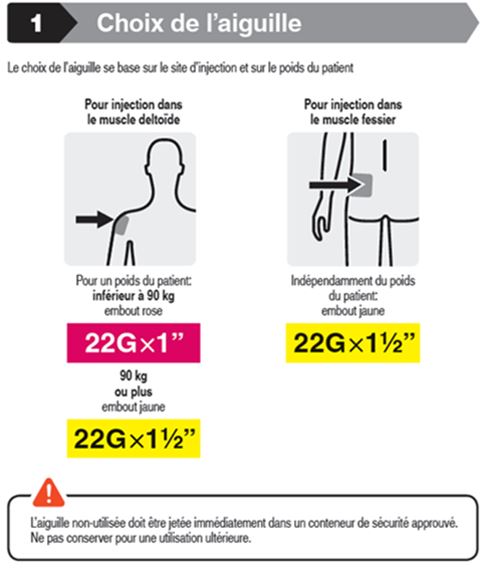
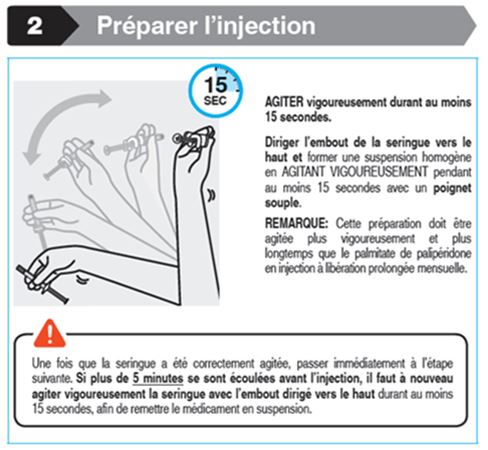
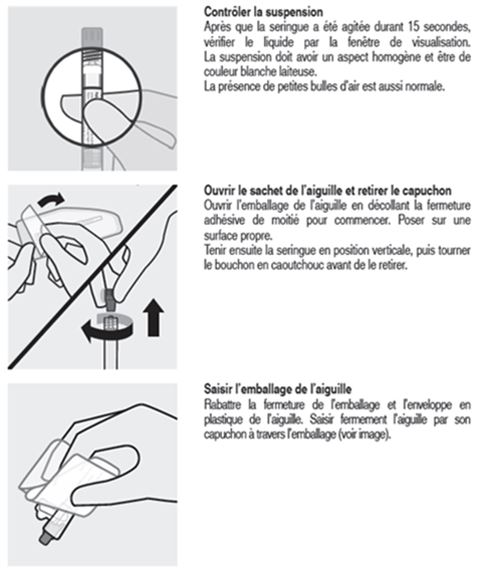

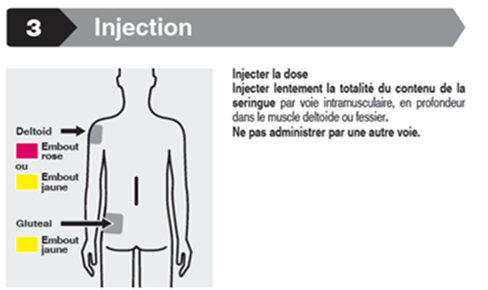

|











