PharmacocinétiqueAbsorption
En raison de sa solubilité extrêmement faible, le palmitate de palipéridone dans sa galénique d'injection trimestrielle à libération prolongée se dissout lentement après injection intramusculaire, avant d'être hydrolysé en palipéridone et absorbé dans la circulation sanguine. La libération du principe actif débute déjà le 1er jour et se poursuit jusqu'à 18 mois.
Les données mentionnées dans ce paragraphe sont basées sur une analyse pharmacocinétique de population. Après une dose intramusculaire unique de Trevicta, les taux plasmatiques de palipéridone augmentent progressivement jusqu'à la concentration maximale avec une Tmax médiane de 30-33 jours. Après l'injection intramusculaire de doses de Trevicta comprises entre 175 et 525 mg dans le muscle deltoïde, on a observé en moyenne une Cmax supérieure de 11 à 12% à celle obtenue après une injection dans le muscle fessier. Le profil de libération et le schéma posologique de Trevicta entraîne le maintien des concentrations thérapeutiques. L'exposition totale à la palipéridone après l'injection de Trevicta était dose-proportionnelle sur une plage de doses allant de 175 à 525 mg et environ dose-proportionnelle pour la Cmax. Le rapport moyen des valeurs maximales et minimales à l'état d'équilibre après une dose de Trevicta était de 1,6 après une injection dans le muscle fessier et de 1,7 après une injection dans le muscle deltoïde.
Distribution
Le volume de distribution apparent de la palipéridone après l'administration de Trevicta est de 1960 litres.
La liaison de la palipéridone racémique aux protéines plasmatiques est de 74%.
Après l'administration de Trevicta, il se produit une interconversion des énantiomères (+) et (-) de la palipéridone et le rapport AUC(+)/(-) est d'environ 1,7 à 1,8.
Métabolisme
Dans une étude menée avec la 14C-palipéridone à libération immédiate, on a retrouvé 59% de la dose sous forme inchangée dans l'urine après une dose orale unique de 1 mg de 14C-palipéridone à libération immédiate, ce qui signifie que la palipéridone ne semble pas être métabolisée dans le foie de manière extensive. Environ 80% de la radioactivité administrée a été retrouvée dans les urines et 11% dans les selles. Quatre voies métaboliques ont été identifiées in vivo, aucune d'entre elles ne comptant pour plus de 10% de la dose: déalkylation, hydroxylation, déshydrogénation et dissociation du benzisoxazole. Bien que les études in vitro suggèrent une participation possible du CYP2D6 et du CYP3A4 au métabolisme de la palipéridone, il n'y a pas de données in vivo qui indiquent un rôle significatif de ces deux isoenzymes dans le métabolisme de la palipéridone. Des analyses pharmacocinétiques de populations n'ont pas montré de différence manifeste entre les métaboliseurs extensifs et les métaboliseurs lents des substrats du CYP2D6 par rapport à la clairance apparente de la palipéridone après la prise de palipéridone orale. Des études in vitro réalisées sur des microsomes hépatiques humains ont montré que la palipéridone n'inhibait pas sensiblement le métabolisme des principes actifs métabolisés par les isoenzymes du cytochrome P450, incluant les CYP1A2, CYP2A6, CYP2C8/9/10, CYP2D6, CYP2E1, CYP3A4, et CYP3A5.
Les études effectuées in vitro ont montré que la palipéridone est un substrat de la P-gp et un léger inhibiteur de la P-gp à fortes concentrations. Aucune donnée in vivo n'est disponible et la pertinence clinique n'est pas connue.
D'après l'analyse pharmacocinétique de population, la demi-vie apparente médiane de la palipéridone après l'administration de Trevicta à des doses de 175 à 525 mg était de 84 à 95 jours après injection dans le muscle deltoïde et de 118 à 139 jours après injection dans le muscle fessier.
Suspension injectable à libération prolongée de palmitate de palipéridone trimestriel versus autres formulations de palipéridone
Trevicta est destiné à un traitement de palipéridone tous les 3 mois, alors que le palmitate de palipéridone injectable mensuel doit être administré tous les mois. Lorsque Trevicta est donné à des doses 3,5 fois supérieures à la dose correspondante injectable de palmitate de palipéridone mensuel, il en résulte une exposition à la palipéridone comparable à celle qui suit une dose mensuelle correspondante de palmitate de palipéridone mensuel ou d'une dose correspondante sous la forme de comprimés à libération prolongée de palmitate de palipéridone une fois par jour. La plage d'exposition lors de l'administration de Trevicta se situe à l'intérieur des plages d'exposition obtenues avec les comprimés à libération prolongée de palmitate de palipéridone aux doses autorisées.
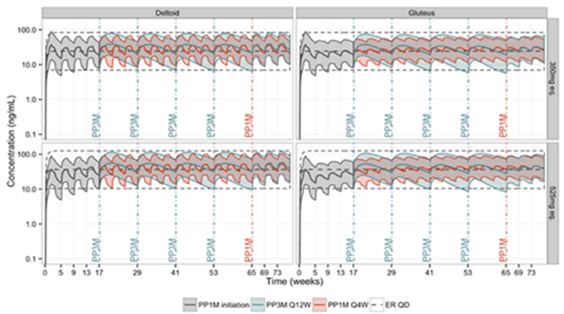
La figure 3 montre les profils pharmacocinétiques médians pronostiqués pour une population donnée de la palipéridone après l'administration de Trevicta aux doses de 350 mg et de 525 mg versus injections mensuelles de 100 mg et 150 mg de palmitate de palipéridone mensuel et prise de comprimés retard à libération prolongée (8 mg ou 12 mg). Un traitement d'au moins 4 mois par des injections de palmitate de palipéridone mensuel avant l'introduction de Trevicta a permis de maintenir l'exposition plasmatique à la palipéridone à l'état d'équilibre.
Figure 3: Concentrations plasmatiques de palipéridone pronostiquées au cours du temps après administration de Trevicta (PP3M) en groupes de doses de 350 mg et 525 mg par rapport à l'administration mensuelle d'injections de palmitate de palipéridone mensuel (PP1M) aux doses de 100 mg ou 150 mg. Les lignes en pointillé montrent les concentrations de palipéridone pronostiquées après prise de comprimés à libération prolongée de palipéridone 8 mg et 12 mg
Élimination
Voir Métabolisme.
Cinétique pour certains groupes de patients
Troubles de la fonction hépatique
La palipéridone n'est pas métabolisée de façon extensive dans le foie. Trevicta n'a certes pas été étudié chez des patients avec insuffisance hépatique, mais aucune adaptation des doses n'est nécessaire chez les patients en insuffisance hépatique légère ou modérée. Dans une étude avec la palipéridone orale sur des sujets présentant une insuffisance hépatique moyenne (classe Child-Pugh B), les concentrations plasmatiques de la palipéridone libre étaient similaires à celles obtenues sur les volontaires sains. La palipéridone n'a pas été évaluée chez les patients avec insuffisance hépatique sévère.
Troubles de la fonction rénale
Trevicta n'a pas été étudié de façon systématique chez les patients atteints d'insuffisance hépatique. La disponibilité d'une dose orale unique de type comprimé à libération prolongée à 3 mg de palipéridone a été étudiée chez des patients avec différents degrés d'insuffisance rénale. L'élimination de la palipéridone diminue lorsque la clairance rénale estimée de la créatinine baisse. Chez les sujets insuffisants rénaux participant à l'étude, la clairance totale de la palipéridone était inférieure de 32% en cas d'insuffisance rénale légère (CrCl = 50 à <80 ml/min), de 64% en cas d'insuffisance rénale modérée (CrCl = 30 à <50 ml/min) et de 71% en cas d'insuffisance rénale sévère (CrCl = 10 à <30 ml/min). Cela correspond à une exposition (AUCinf) en moyenne 1,5, 2,6 et 4,8 fois supérieure à celle observée chez les sujets sains. Sur la base d'un petit nombre d'observations avec Trevicta chez des sujets avec insuffisance rénale légère et de simulations pharmacocinétiques, on conseille chez les patients atteints d'une insuffisance rénale légère une réduction des doses d'induction et d'entretien d'injection de palmitate de palipéridone mensuel. Ces patients peuvent être passés sous Trevicta à la dose correspondante calculée par le facteur de multiplication 3,5. Aucune réduction supplémentaire des doses n'est nécessaire après l'introduction de Trevicta (voir «Posologie/Mode d'emploi»).
Patients âgés
Il n'est pas recommandé d'ajuster la dose sur la seule base de l'âge. Une adaptation de la dose peut néanmoins être nécessaire en raison d'une diminution de la clairance rénale en fonction de l'âge (voir «Troubles de la fonction rénale» et «Posologie/Mode d'emploi»).
Origine ethnique
Une analyse pharmacocinétique de population sur des données provenant d'études réalisées avec la palipéridone orale n'a montré aucune différence liée à l'origine ethnique en ce qui concerne la pharmacocinétique de la palipéridone après l'utilisation de Trevicta.
Sexe
Aucune différence significative n'a été mise en évidence entre les hommes et les femmes.
Tabagisme
Les études in vitro avec des enzymes hépatiques humaines permettent de conclure que la palipéridone n'est pas un substrat du CYP1A2; le tabagisme ne devrait donc avoir aucune influence sur la pharmacocinétique de la palipéridone. En corrélation avec ces résultats obtenus in vitro, une analyse pharmacocinétique de population n'a pas montré de différence entre les fumeurs et les non-fumeurs.
Indice de masse corporelle (IMC)/Poids corporel
Aucune adaptation des doses en fonction de l'IMC n'est nécessaire. Une Cmax plus basse a été observée chez les patients en surpoids et chez les patients obèses. À l'état d'équilibre apparent sous Trevicta, les concentrations minimales étaient comparables chez les patients de poids normal, chez les patients en surpoids et chez les patients obèses.
| 