CompositionPrincipe actif: Etanerceptum.
Excipients:
Solution injectable Erelzi et Erelzi SensoReady
Acidum citricum anhydricum, natrii citras dihydricus, natrii chloridum, saccharum, lysini hydrochloridum, aqua ad iniectabilia q.s. ad solutionem.
Forme galénique et quantité de principe actif par unitéSolution injectable Erelzi
Seringue pré-remplie à 25 mg/0,5 ml ou 50 mg/1 ml d'étanercept.
Erelzi SensoReady
Stylo pré-rempli à 50 mg/1 ml d'étanercept.
Indications/Possibilités d’emploiPolyarthrite rhumatoïde
Erelzi est indiqué pour le traitement de la polyarthrite rhumatoïde (PR) active (chez l'adulte) lorsqu'un traitement standard antérieur par antirhumatismaux de fond (DMARD) a été insuffisant. Erelzi peut être utilisé en association avec le méthotrexate chez les patients ne répondant pas suffisamment au méthotrexate seul.
Erelzi est également indiqué dans le traitement de la polyarthrite rhumatoïde sévère, active et évolutive de l'adulte non précédemment traité par le méthotrexate. On a montré par radiographie que chez ces patients, Erelzi ralentit la progression des dommages structuraux associés à la maladie.
Arthrite juvénile idiopathique
Erelzi est indiqué dans le traitement de la polyarthrite (facteur rhumatoïde positif ou négatif) et de l'oligoarthrite extensive (extended) de l'enfant et de l'adolescent (à partir de 2 ans), en cas de réponse inadéquate ou d'intolérance avérée au méthotrexate.
Traitement du rhumatisme psoriasique (arthritis psoriatica) de l'adolescent à partir de 12 ans, en cas de réponse inadéquate ou d'intolérance avérée au méthotrexate.
Traitement de l'arthrite associée à une enthésite chez l'adolescent à partir de 12 ans, en cas de réponse inadéquate ou d'intolérance au traitement conventionnel.
L'étanercept n'a pas été étudié chez l'enfant de moins de 2 ans. L'étanercept en association avec méthotrexate a été étudié chez l'enfant; mais non en association avec d'autres traitements de fond DMARD.
Rhumatisme psoriasique
Traitement du rhumatisme psoriasique actif et progressif chez l'adulte lorsque la réponse à un traitement antérieur par antirhumatismaux de fond a été insuffisante. Erelzi améliore les capacités fonctionnelles chez les patients atteints de rhumatisme psoriasique, et ralentit la progression des dommages structuraux articulaires périphériques tels que mesurés par la radiographie chez les patients ayant des formes polyarticulaires symétriques de la maladie.
Spondylarthrite ankylosante
Erelzi est indiqué pour la réduction des signes et symptômes et pour l'amélioration des capacités fonctionnelles chez les patients adultes atteints de spondylarthrite ankylosante sévère et active, en cas de réponse inadéquate au traitement conventionnel.
Psoriasis en plaques
Traitement du psoriasis en plaques modéré à sévère de l'adulte.
Psoriasis en plaques chez l'enfant et l'adolescent
Traitement du psoriasis en plaques chronique sévère de l'enfant et de l'adolescent à partir de 6 ans, en cas de réponse insuffisante ou d'intolérance à un autre traitement systémique ou à une photothérapie.
Posologie/Mode d’emploiErelzi ne doit être prescrit que par des médecins ayant l'expérience de la prise en charge des patients atteints de polyarthrite rhumatoïde active et réfractaire, d'arthrite juvénile idiopathique active polyarticulaire, de rhumatisme psoriasique, de spondylarthrite ankylosante, de psoriasis en plaques ou de psoriasis en plaques de l'enfant et de l'adolescent.
Erelzi SensoReady, solution injectable en stylo pré-rempli est disponible au dosage de 50 mg. Erelzi, solution pour injection en seringue pré-remplie est disponible aux dosages de 25 mg et 50 mg.
Des remarques détaillées concernant le mode d'emploi figurent dans la notice d'emballage sous «Instructions pour l'administration d'une injection».
Afin d'assurer la traçabilité des médicaments biotechnologiques, il convient de documenter pour chaque traitement le nom commercial et le numéro de lot.
Adultes
Polyarthrite rhumatoïde
La dose recommandée est de 25 mg administrés deux fois par semaine en injection sous-cutanée, à intervalles de 72 à 96 h.
Toutefois, l'efficacité et la sécurité d'emploi d'une administration de 50 mg une fois par semaine ont été démontrées (voir «Propriétés/Effets»).
Un traitement antérieur par méthotrexate, glucocorticoïdes, salicylés, AINS ou antalgiques peut être poursuivi pendant le traitement par Erelzi. Aucune étude n'a été menée sur l'association d'Erelzi à d'autres traitements de fond (DMARD) que le méthotrexate, ni sur l'emploi de plus fortes doses d'étanercept.
Rhumatisme psoriasique et spondylarthrite ankylosante
La dose recommandée est 25 mg d'Erelzi administrés deux fois par semaine (avec un intervalle de 3 à 4 jours) ou de 50 mg administré une fois par semaine.
Psoriasis en plaques
Dans le psoriasis en plaques, la dose recommandée d'Erelzi est de 50 mg par semaine (administrés en deux injections de 25 mg chacune, avec un intervalle de 3 à 4 jours ou en injection unique de 50 mg) jusqu'à l'obtention de la rémission, au maximum jusqu'à 24 semaines.
Toutefois, une administration de 50 mg deux fois par semaine peut être utilisée jusqu'à 12 semaines, suivie, si nécessaire, par l'administration d'une dose de 25 mg deux fois par semaine ou de 50 mg une fois par semaine.
Un traitement continu au-delà de 24 semaines peut être approprié pour les patients adultes qui, selon l'évaluation du médecin, répondent bien à Erelzi, mais sont susceptibles de récidiver peu de temps après l'arrêt d'Erelzi (voir «Propriétés/Effets, Essais cliniques»).
Si la reprise du traitement par Erelzi est indiquée chez des patients ayant répondu au traitement initial, le même schéma de durée de traitement décrit doit être suivi. La dose doit être de 25 mg administrés deux fois par semaine ou de 50 mg une fois par semaine.
Enfants et adolescents
Chez les patients pédiatriques, le dosage se base sur le poids corporel. Erelzi est disponible en unidoses fixes de 25 mg et 50 mg pour le traitement d'enfants et d'adolescents d'un poids corporel de ≥62,5 kg. Les patients d'un poids corporel inférieur à 62,5 kg doivent recevoir un autre produit contenant l'étanercept dosé de manière appropriée sur une base en mg/kg de poids corporel. Les patients dont le poids corporel est égal ou supérieur à 62,5 kg peuvent être traités avec la dose unique fixe d'Erelzi solution injectable en seringue pré-remplie ou solution injectable en stylo pré-rempli.
Arthrite juvénile idiopathique
0,4 mg/kg de PC (et au maximum 25 mg par injection) deux fois par semaine en injection sous-cutanée, à intervalles de 72 à 96 h ou 0,8 mg/kg de PC (et au maximum 50 mg par injection) une fois par semaine. L'arrêt du traitement doit être envisagé chez les patients qui n'ont pas répondu au traitement après 4 mois.
Aucune étude clinique formelle n'a été menée chez les enfants âgés de 2−3 ans. Des données limitées de registre (les expériences dans ce groupe d'âge des 2−3 ans se basent sur 47 patients) suggèrent que le profil de sécurité chez les enfants âgés de 2−3 ans est comparable à celui des adultes et des enfants de plus de 4 ans à une dose de 0,8 mg/kg de PC une fois par semaine («Propriétés/Effets»).
Psoriasis en plaques chez l'enfant et l'adolescent (à partir de 6 ans)
0,8 mg/kg de poids corporel (jusqu'à au maximum 50 mg par dose) une fois par semaine pendant une période allant jusqu'à 24 semaines. Après 12 semaines, le traitement doit être interrompu chez les patients ne présentant pas de réponse au traitement.
Si la reprise du traitement par étanercept est indiquée, le schéma de durée de traitement décrit ci-dessus doit être appliqué. La dose doit être de 0,8 mg/kg de poids corporel (jusqu'à une dose maximale de 50 mg) une fois par semaine.
Un traitement antérieur par glucocorticoïdes, AINS ou antalgiques peut être poursuivi pendant le traitement par Erelzi. Étanercept en association avec méthotrexate a été étudié chez l'enfant présentant une AJI, mais non en association avec d'autres DMARD. L'emploi de doses élevées d'étanercept n'a pas été étudié.
Sujets âgés
Aucun ajustement posologique n'est nécessaire.
Insuffisants rénaux et hépatiques: Aucun ajustement posologique n'est nécessaire.
Contre-indicationsHypersensibilité à la substance active ou à l'un des excipients.
Septicémie ou risque de septicémie.
Un traitement par Erelzi ne devrait pas être initié chez les patients ayant des infections actives, y compris des infections chroniques ou localisées.
Mises en garde et précautionsInfections
Avant, pendant et après un traitement par Erelzi, les patients devraient être examinés quant à l'apparition d'une infection, en tenant compte de la demi-vie d'élimination moyenne de l'étanercept de 70 h environ (de 7 à 300 h).
Des infections graves, septicémies, tuberculoses, et infections opportunistes (infections fongiques invasives, listériose et légionellose comprises), ont été rapportées avec étanercept (voir «Effets indésirables»). Ces infections étaient dues à des bactéries, des mycobactéries, des champignons, des virus et des parasites (protozoaires compris). Dans certains cas, des infections fongiques particulières et d'autres infections opportunistes n'ont pas été diagnostiquées, ce qui s'est traduit par un retard d'initiation du traitement approprié et parfois au décès. Lors de l'évaluation du risque d'infection chez un patient, son exposition à des facteurs de risque spécifiquement associés à certaines infections opportunistes (par exemple une exposition à des mycoses endémiques) doit être prise en compte.
Une surveillance attentive doit être exercée chez les patients traités par Erelzi développant une nouvelle infection. Le traitement par Erelzi sera interrompu si le patient développe une infection grave ou une septicémie. Il ne faut pas instaurer de traitement par Erelzi chez les patients présentant une infection évolutive y compris les infections chroniques ou localisées. Il ne faut utiliser Erelzi que sous surveillance médicale soigneuse chez les patients ayant des antécédents d'infections récurrentes ou ayant des affections prédisposant au risque infectieux, comme un diabète sévère ou mal équilibré.
Tuberculose
Des cas de tuberculose active comprenant des tuberculoses miliaires et des tuberculoses avec localisation extra-pulmonaire ont été rapportés chez des patients traités par étanercept.
Avant de débuter un traitement par Erelzi, une recherche de tuberculose active ou inactive («latente») doit être effectuée chez tous les patients. Cette recherche doit comprendre un entretien médical détaillé portant sur les antécédents personnels de tuberculose ou sur d'éventuels contacts antérieurs avec un patient tuberculeux, et sur un traitement immunosuppresseur ancien et/ou en cours. Des tests de dépistage appropriés, par exemple un test dermique à la tuberculine et une radiographie pulmonaire, devront être effectués chez tous les patients. Il est rappelé aux prescripteurs que le test dermique à la tuberculine peut s'avérer faussement négatif, en particulier chez un patient gravement malade ou immunodéprimé.
Si une tuberculose active est diagnostiquée, le traitement par Erelzi ne doit pas être instauré. En cas de diagnostic d'une tuberculose inactive («latente»), un traitement antituberculeux doit être mis en oeuvre avant d'initier Erelzi. Dans un tel cas, le rapport bénéfice/risque du traitement par Erelzi doit être soigneusement évalué.
Tous les patients devront être informés de la nécessité de consulter un médecin si des signes ou des symptômes évoquant une tuberculose (par exemple, toux persistante, amaigrissement/perte de poids, fébricule) apparaissent pendant ou après le traitement par Erelzi.
Réactivation de l'hépatite B
Une réactivation de l'hépatite B a été rapportée chez des patients ayant des antécédents d'infections par le virus de l'hépatite B (VHB) qui ont reçu de manière concomitante un antagoniste du TNF y compris étanercept. Les patients à risque d'infection par le VHB devront faire l'objet d'un dépistage d'infection préalable à VHB avant l'initiation d'un traitement par Erelzi. Des précautions devront être prises lors de l'administration d'Erelzi à des patients ayant des antécédents d'infections par le VHB. Chez ces patients, il faudra surveiller attentivement les signes et les symptômes d'une infection active par le VHB et, si nécessaire, un traitement approprié devra être initié.
Aggravation d'hépatite C
Des cas d'aggravation d'hépatite C ont été rapportés chez les patients recevant étanercept.
Administration concomitante d'Erelzi et de l'anakinra
L'administration concomitante d'étanercept et de l'anakinra a été associée à une augmentation du risque d'infections graves et de neutropénies comparativement à étanercept lorsqu'il est administré seul. Cette association n'a pas démontré un bénéfice clinique supérieur. Par conséquent l'association d'Erelzi et de l'anakinra n'est pas recommandée (voir «Effets indésirables» et «Interactions»).
Insuffisance cardiaque congestive
Les médecins devront utiliser Erelzi avec précaution chez les patients présentant une insuffisance cardiaque congestive (ICC). Après commercialisation, des cas d'aggravation d'ICC ont été rapportés, avec ou sans facteur favorisant identifiable, chez des patients sous étanercept. Par ailleurs, quelques rares (<0,1%) apparitions d'une nouvelle insuffisance cardiaque congestive ont été signalées, y compris insuffisance cardiaque congestive chez des patients sans antécédent connu de pathologie cardiovasculaire. Certains de ces patients étaient âgés de moins de 50 ans. Deux importantes études cliniques ayant pour objectif d'étudier l'efficacité de l'étanercept dans le traitement de l'ICC, ont été interrompues de façon prématurée pour cause de manque d'efficacité. Bien que non concluantes, les données de l'une de ces études montrent une tendance possible à la dégradation de l'ICC chez les patients ayant été assignés au groupe d'étanercept.
Par ailleurs, une étude clinique avec Infliximab (un anticorps monoclonal se fixant au TNF alpha) en tant que traitement de l'insuffisance cardiaque a été prématurément interrompue, car on a constaté une hausse de la mortalité chez les patients traités. C'est la raison pour laquelle il convient d'utiliser l'étanercept avec prudence chez les patients souffrant d'insuffisance cardiaque.
Réactions allergiques
Lors des essais cliniques, des réactions allergiques ont été fréquemment observées en relation avec l'administration d'étanercept. L'expérience montre que depuis l'introduction sur le marché, des cas de réactions allergiques, dont oedème de Quincke et urticaire, ainsi que des réactions graves, ont été rapportés.
En cas de réaction allergique grave ou de réaction anaphylactique, le traitement par Erelzi sera interrompu immédiatement et une thérapie appropriée sera instituée.
Immunosuppression
Il est possible que les traitements anti-TNF, y compris étanercept, altèrent les défenses immunitaires du patient à l'encontre des infections et des tumeurs malignes, vu que le TNF est un médiateur de l'inflammation et qu'il module la réponse immunitaire cellulaire. Divers cas de tumeurs malignes (y compris cancer du sein, du poumon, lymphome) ont été rapportés après commercialisation. Dans une étude englobant 49 patients atteints de polyarthrite rhumatoïde traités par étanercept, aucune diminution d'hypersensibilité retardée ou des taux d'immunoglobuline, et aucun changement dans la numération de la formule sanguine n'ont été observés. Deux patients atteints d'arthrite juvénile idiopathique ont développé une varicelle avec des signes et des symptômes de méningite aseptique suivie d'une guérison sans séquelle. Les patients exposés au virus de la varicelle doivent temporairement arrêter leur traitement par Erelzi et un traitement prophylactique par immunoglobulines spécifiques doit être envisagé. Dans le cadre d'études contrôlées, on a observé un nombre plus élevé de cas de lymphomes chez les patients recevant des antagonistes du TNF que chez les patients-contrôles. Cependant, l'apparition de lymphomes était rare, et la période de suivi des patients sous placebo était plus courte que celle des patients sous antagonistes du TNF. De plus, l'évaluation du risque est rendue plus difficile par la présence d'un risque de base accru de lymphome chez les patients atteints de longue date d'arthrite rhumatoïde et de maladie inflammatoire très active. Au stade actuel des connaissances, on ne peut pas exclure un risque potentiel de lymphome ou d'autre maladie maligne chez les patients traités aux antagonistes du TNF.
La sécurité et l'efficacité d'étanercept chez des patients immunodéprimés ou atteints d'infections chroniques n'ont pas été évaluées.
Maladies lymphoprolifératives malignes
Tumeurs solides (excepté cancers cutanés) et troubles hématopoïétiques malins, leucémie
Des cas de lymphomes ont été observés chez les patients traités avec des inhibiteurs du TNF-α (étanercept inclus). Lors des phases contrôlées d'études cliniques avec étanercept, on a observé 3 cas de lymphomes parmi les 4509 patients sous étanercept, alors qu'aucun cas n'était décelé chez les 2040 patients de contrôle (la durée de la période contrôlée allait de 3 à 24 mois). Lors des phases contrôlées et en ouvert d'études cliniques avec Erelzi, on a noté 9 cas de lymphomes parmi les 5723 patients totalisant 11'201 années-patients de traitement. Ceci correspond à 3 fois le nombre attendu dans la population en général. Les patients atteints de polyarthrite rhumatoïde ou de psoriasis pourraient être exposés à un plus grand risque (jusqu'au multiple) de lymphome, en particulier dans la phase très active de leur maladie.
Chez des enfants et des adolescents traités par des inhibiteurs du TNF (y compris l'étanercept), il a été fait état de tumeurs malignes (plus spécifiquement de lymphome hodgkinien et non-hodgkinien) qui ont eu dans certains cas une issue fatale. La plupart des patients concernés étaient traités simultanément par des immunosuppresseurs.
Dans l'état actuel des connaissances, il n'est pas possible d'exclure un risque de développement de lymphomes ou d'autres tumeurs malignes hématopoïétiques ou solides chez les patients traités par des inhibiteurs du TNF (voir section «Effets indésirables, Tumeurs malignes»).
Après la commercialisation, il a été fait état de cas de leucémie aiguë ou chronique en rapport avec l'utilisation d'inhibiteurs du TNF en cas de polyarthrite rhumatoïde ou d'autres indications. Même en absence de traitement par un inhibiteur du TNF, les patients atteints de polyarthrite rhumatoïde peuvent présenter un risque accru (environ 2 fois plus élevé que celui de la population générale) de développer une leucémie.
Cancer cutané
Des cas de cancer cutané mélanomateux et de cancer cutané non mélanomateux (non-melanoma skin cancer, NMSC) ont été rapportés chez les patients traités par des anti-TNF, parmi lesquels on trouve étanercept.
Le taux d'incidence standardisé («standardized incidence ratio») des mélanomes observés dans le cadre des études conduites avec étanercept (rapport entre le nombre de cas observés et le nombre de cas attendus dans la population générale) était de 1,6 chez les patients présentant une PR (IC: 0,5−3,8), de 3,2 chez les patients présentant un psoriasis (IC: 0,67−9,43) et de 2,1 pour l'ensemble des patients (IC: 0,95−3,9).
Chez 3306 patients rhumatologiques adultes (polyarthrite rhumatoïde (PR), arthrite psoriasique (Apso), spondylarthrite ankylosante (SA)) traités par étanercept lors des essais cliniques contrôlés, correspondant à environ 2669 années-patients sous traitement, le taux observé de NMSC était de 0,41 événement par 100 années-patients versus 0,37 événement par 100 années-patients chez les 1521 patients du groupe contrôle correspondant à 1077 années-patients. Chez 1245 patients psoriasiques adultes traités par étanercept dans le cadre d'essais cliniques contrôlés, correspondant à environ 283 années-patients sous traitement, le taux de NMSC était de 3,54 événements par 100 années-patients versus 1,28 événement par 100 années-patients chez les 720 patients du groupe contrôle correspondant à 156 années-patients.
Des cas de cancer à cellules de Merkel ont été rapportés au cours de la phase de post-marketing chez des patients traités par étanercept. Des contrôles réguliers de la peau sont donc recommandés sous étanercept. En combinant les résultats des essais cliniques contrôlés étanercept versus placebo et comparateur actif, un plus grand nombre de cas de cancers cutanés non mélanomateux a été observé chez les patients recevant étanercept par rapport au groupe contrôle, particulièrement chez les patients atteints de psoriasis.
Vaccins
Les vaccins vivants ne devraient pas être administrés à des patients traités par Erelzi. Aucune donnée n'est disponible sur la transmission infectieuse secondaire à l'administration de vaccins vivants chez des patients traités par étanercept.
Dans la mesure du possible avant de commencer le traitement par Erelzi, il est recommandé de mettre à jour les vaccinations des patients pédiatriques conformément au calendrier de vaccination actuellement en vigueur. Deux patients atteints d'arthrite juvénile idiopathique ont développé une varicelle avec des symptômes d'une méningite aseptique, suivie d'une guérison sans séquelles. Les patients largement exposés au virus varicella doivent interrompre provisoirement le traitement par Erelzi; dans ces cas, un traitement prophylactique par l'immunoglobuline varicella-zoster doit être envisagé.
Formation d'auto-anticorps/maladies auto-immunes
Erelzi est susceptible d'entraîner la formation d'anticorps auto-immuns (voir «Effets indésirables»).
Chez certains patients, notamment les patients avec polyarthrite rhumatoïde positifs pour le facteur rhumatoïde, les notifications de pharmacovigilance ont rapporté des cas rares d'apparition d'auto-anticorps associés à des éruptions se présentant sur le plan clinique ou à la biopsie comme un lupus sub-aigu ou comme un lupus discoïde. Des cas de syndrome type lupus ont aussi été rapportés.
Réactions hématologiques
De rares cas de pancytopénies et des cas isolés d'anémie aplasique, dont certaines d'évolution fatale, ont été rapportés chez des patients traités par étanercept. C'est pourquoi, une attention particulière doit être portée aux patients traités par Erelzi ayant des antécédents d'anomalie hématologique. Tous les patients et parents/entourage traités par Erelzi doivent être informés qu'en cas d'apparition de signes ou de symptômes évoquant une atteinte hématologique ou une infection (tels que fièvre persistante, douleurs pharyngées, ecchymoses, saignement, pâleur) chez le patient, ils doivent immédiatement consulter un médecin. Chez ces patients, des examens complémentaires, notamment une numération sanguine complète, doivent être pratiqués en urgence; si une atteinte hématologique est confirmée, le traitement par Erelzi doit être arrêté.
Troubles neurologiques
Dans de rares cas, des affections démyélinisantes du SNC ont été rapportés chez les patients adultes traités par étanercept. Des neuropathies périphériques démyélinisantes ont en outre été rapportées (syndrome de Guillain-Barré, polyneuropathies démyélinisantes, polyneuropathies chroniques inflammatoires démyélinisantes, neuropathies motrices multifocales et autres), de même que des myélites transverses et des névrites optiques (voir aussi «Effets indésirables»). La relation de cause à effet avec le traitement par étanercept demeure toutefois incertaine.
Il est de ce fait recommandé d'effectuer une évaluation soigneuse du rapport bénéfice/risque, y compris une évaluation neurologique, avant de prescrire Erelzi aux patients présentant des antécédents ou la survenue récente d'une maladie démyélinisante centrale ou périphérique ainsi qu'aux patients chez lesquels on considère que le risque de développer une maladie démyélinisante centrale ou périphérique est accru.
Hépatite alcoolique
Dans une étude de phase II randomisée, contrôlée versus placebo, portant sur 48 patients hospitalisés traités par étanercept ou placebo pour hépatite alcoolique modérée à sévère, étanercept n'a pas été efficace et le taux de mortalité des patients traités par étanercept était significativement plus élevé après 6 mois. Par conséquent, étanercept ne doit pas être utilisé pour traiter l'hépatite alcoolique. Les médecins doivent utiliser étanercept avec précaution chez les patients souffrant également d'hépatite alcoolique modérée à sévère.
Granulomatose de Wegener
Dans une étude contrôlée par placebo effectuée chez 89 patients adultes traités par étanercept en association avec une thérapie standard (y compris cyclophosphamide ou méthotrexate, et corticostéroïdes) pendant une durée de 25 mois, étanercept ne s'est pas avéré être un traitement efficace contre la granulomatose de Wegener. La fréquence de tumeurs malignes non cutanées de types divers était significativement plus élevée chez les patients traités par étanercept que chez les patients du groupe contrôle. étanercept n'est pas recommandé pour le traitement de la granulomatose de Wegener.
Hypoglycémies chez des patients traités pour un diabète
Des cas d'hypoglycémie ont été rapportés suite à l'initiation d'étanercept chez des patients qui recevaient un traitement antidiabétique. Ces hypoglycémies ont nécessité une diminution du traitement antidiabétique chez certains de ces patients.
Maladie inflammatoire chronique intestinale (inflammatory bowel disease, IBD) et uvéite chez les patients atteints de polyarthrite juvénile idiopathique (juvenile idiopathic arthritis, JIA) et maladie de Crohn chez les enfants atteints de psoriasis
Des cas de maladie chronique inflammatoire intestinale (y compris maladie de Crohn) et d'uvéite ont été rapportés chez les patients atteints d'une arthrite juvénile idiopathique (JIA) ainsi que des cas de maladie de Crohn chez les enfants atteints de psoriasis traités par étanercept. Des cas d'atteinte inflammatoire intestinale cliniquement manifeste ont également été signalés chez les patients présentant une JIA non traités.
Administration concomitante des TNF-α-inhibiteurs et de l'abatacept
L'administration concomitante de l'abatacept et d'étanercept au cours d'études cliniques a entraîné une augmentation de l'incidence des événements indésirables graves, des infections graves incluses. Cette association n'a pas démontré de bénéfice clinique supplémentaire; par conséquent cette association n'est pas recommandée.
InteractionsLe méthotrexate n'a pas d'effet sur la pharmacocinétique de l'étanercept. On ne peut pas exclure un effet d'étanercept sur la pharmacocinétique et la sécurité d'emploi du méthotrexate, bien que cela soit improbable. Dans les essais cliniques, aucune interaction n'a été observée lorsque étanercept était administré avec des glucocorticoïdes, des salicylés, des anti-inflammatoires non stéroïdiens (AINS), des analgésiques ou le méthotrexate.
Les interactions entre étanercept et d'autres principes actifs n'ont pas fait l'objet d'études cliniques particulières.
Administration concomitante d'Erelzi et de sulfasalazine
La leucopénie a été rapportée lors du traitement associé d'étanercept et de sulfasalazine.
Dans une étude clinique chez des patients adultes traités par des doses stables de sulfasalazine et chez lesquels étanercept était ajouté, les patients du groupe recevant cette association ont présenté une diminution significative du nombre moyen de globules blancs, par rapport aux groupes traités par étanercept ou la sulfasalazine seuls. La signification clinique de cette interaction est inconnue.
Interactions avec la digoxine et la warfarine
On a constaté lors d'une étude de pharmacocinétique (PK) que l'administration concomitante d'étanercept et de digoxine réduisait l'exposition à ces deux substances de façon minimale. Lors d'une étude de PK avec des doses uniques de warfarine et d'étanercept, il a été démontré qu'il n'y avait aucune influence réciproque de l'exposition à ces substances.
Administration concomitante d'Erelzi et de l'anakinra
Les patients adultes traités par étanercept et l'anakinra ont présenté un taux plus élevé d'infections graves par rapport aux patients traités soit par étanercept seul, soit par l'anakinra seul (données historiques).
De plus, dans un essai contrôlé, en double aveugle, versus placebo, chez des patients adultes recevant un traitement de fond par le méthotrexate, les patients traités par étanercept et l'anakinra ont présenté un taux plus élevé d'infections graves (7%) et de neutropénies que les patients traités par étanercept seul (voir section «Mises en garde et précautions»). L'association d'étanercept et de l'anakinra n'a pas démontré un bénéfice clinique supérieur et n'est par conséquent pas recommandée.
Grossesse/AllaitementAucune étude avec étanercept n'a été conduite chez la femme enceinte.
Grâce à un registre de grossesse élaboré pour étanercept, on a comparé les taux de malformations congénitales graves observées chez les nourrissons nés vivants de mères souffrant d'affections rhumatoïdes ou de psoriasis et ayant reçu étanercept au cours du premier trimestre (n=319) à celles observées chez les nourrissons de mères n'ayant pas reçu étanercept au cours de la grossesse (n=144). Le rapport de cotes global adapté pour les malformations congénitales graves s'élevait à 2,77 (IC 95% 1,04−7,35), et à 2,49 (IC 95% 0,92−6,68) si les dommages chromosomiques et connus d'origine génétique étaient exclus. Les résultats n'ont montré aucune hausse du taux pour les malformations légères et aucun modèle pour les malformations graves ou légères. De plus, on n'a observé aucune hausse du taux de troubles de la croissance intra-utérins ou postnataux, ni de retard du développement postnatal.
Des études de toxicité sur la reproduction réalisées chez le rat et le lapin n'ont pas mis en évidence de dommage pour le foetus ou pour le rat nouveau-né qui serait dû à étanercept. Il n'existe pas de données précliniques disponibles sur la toxicité péri- et postnatale de l'étanercept, ni sur les effets de l'étanercept sur la fertilité et la fonction reproductrice en général. Pendant la grossesse, Erelzi ne devrait être utilisé que dans les cas où cela est absolument nécessaire. Les femmes en âge de procréer doivent être averties qu'il faut éviter une grossesse pendant le traitement par Erelzi. Le passage d'étanercept dans le lait maternel a été rapporté après administration sous-cutanée. Du fait que de nombreux médicaments et d'immunoglobulines sont excrétés dans le lait maternel, il faut envisager soit d'interrompre l'allaitement soit de suspendre le traitement pendant l'allaitement.
Effet sur l’aptitude à la conduite et l’utilisation de machinesLes effets sur l'aptitude à conduire des véhicules et à utiliser des machines n'ont pas été étudiés.
Effets indésirablesÉtanercept a été étudié chez 2680 patients atteints de polyarthrite rhumatoïde lors d'essais en double aveugle et en ouvert. Cette expérience comprend deux études contrôlées contre placebo (349 patients sous étanercept et 152 patients sous placebo), un essai contrôlé contre traitement actif comparant étanercept au méthotrexate (415 patients sous étanercept et 217 patients sous méthotrexate) et un autre essai contrôlé versus traitement actif comparant étanercept (223 patients), méthotrexate (228 patients) et étanercept associé au méthotrexate (231 patients). La proportion de sorties d'essais dues à des événements indésirables était la même dans les groupes traités par étanercept et par le placebo; au cours du premier essai contrôlé contre traitement actif, le taux d'abandon était significativement plus élevé dans le groupe méthotrexate (10%) que dans le groupe étanercept (5%). Dans le second essai contrôlé versus traitement actif, le taux d'arrêt pour événements indésirables après 2 ans de traitement était similaire parmi les trois groupes de traitement, étanercept (16%), méthotrexate (21%) et étanercept associé au méthotrexate (17%). De plus, étanercept a été étudié chez 240 patients atteints de rhumatisme psoriasique dans deux études en double aveugle contrôlées contre placebo suivies d'une étude d'extension en ouvert.
Cinq cent huit (508) patients atteints de spondylarthrite ankylosante ont été traités par étanercept dans 4 études contrôlées versus placebo en double aveugle.
L'utilisation d'étanercept a également été étudiée pendant une durée maximale de 6 mois dans 5 études contrôlées en double aveugle versus placebo chez 1'492 patients atteints de psoriasis en plaques. Parmi les patients atteints de psoriasis en plaques et traités dans les essais contrôlés versus placebo, la fréquence des événements indésirables graves était d'environ 1,4% des 1341 patients traités par étanercept comparé à 1,4% des 766 patients traités par placebo.
Les effets indésirables mentionnés ci-dessous proviennent des observations faites dans les essais cliniques chez l'adulte et des données rapportées depuis la mise sur le marché.
Les effets indésirables sont listés ci-dessous selon le système de classification par organe et par ordre de fréquence (nombre de patients susceptibles de présenter un effet), en utilisant les catégories suivantes:
«Très fréquents»: (≥1/10), «fréquents»: (<1/10, ≥1/100), «occasionnels»: (<1/100, ≥1/1000), «rares»: (<1/1000, ≥1/10'000), «très rares»: (<1/10'000), «indéterminées»: La fréquence n'a pas pu être estimée précisément au cours des études cliniques. * renvoie à «Informations complémentaires» ci-dessous.
Infections et infestations
Très fréquents: Infections (29%) (y compris infections des voies respiratoires supérieures, bronchite, cystite, infections cutanées)*.
Occasionnels: Infections graves (y compris pneumonie, cellulite phlegmoneuse, arthrite septique, septicémie et infections parasitaires)*.
Rares: Tuberculose, infections opportunistes (incluant infections fongiques, à protozoaires, bactériennes, mycobactériennes atypiques et par virus, invasives et Legionella).
Indéterminées: Listeria, réactivation de l'hépatite B.
Tumeurs bénignes, malignes et non précisées (y compris kystes et polypes)
Occasionnels: Cancer cutané non mélanomateux*.
Rares: Lymphome, cancer cutané*.
Indéterminées: Leucémie, carcinome à cellules de Merkel* (voir «Mises en garde et précautions»).
Affections hématologiques et du système lymphatique
Occasionnels: Thrombocytopénie.
Rares: Anémie, leucopénie, neutropénie, pancytopénie*.
Très rares: Aplasie médullaire*.
Certains cas de pancytopénie et d'aplasie médullaire ont eu une issue fatale (voir «Mises en garde et précautions»).
Affections du système immunitaire
Fréquents: Réactions allergiques (voir «Troubles de la peau et du tissu sous-cutané»), formation d'auto-anticorps*.
Occasionnels: Vascularite systémique (y compris vascularite positive aux anticorps anticytoplasmiques de neutrophiles).
Rares: Réactions allergiques/anaphylactiques graves (y compris angioedème, bronchospasme), sarcoïdose.
Indéterminées: Syndrome d'activation macrophagique*, aggravation des symptômes d'une dermatomyosite.
Troubles du métabolisme et de la nutrition
Indéterminée: Hypoglycémie chez des patients qui recevaient un traitement antidiabétique (voir aussi «Mises en garde et précautions»).
Affections du système nerveux
Rares: Convulsions; épisodes de démyélinisation du SNC pouvant év
oquer une sclérose en plaques ou un tableau de démyélinisation localisée telle qu'une névrite optique ou une myélite transverse.
Très rares: Maladies démyélinisantes périphériques, y compris syndrome de Guillain-Barré, polyneuropathie chronique démyélinisante inflammatoire, polyneuropathie et neuropathie motrice multifocale (voir «Mises en garde et précautions»).
Affections oculaires
Occasionnels: Uvéite, sclérite.
Affections respiratoires, thoraciques et médiastinales
Occasionnels: Maladies pulmonaires interstitielles (incluant la fibrose pulmonaire et la pneumopathie)*.
Affections hépatobiliaires
Rares: Elévation des enzymes hépatiques, hépatite auto-immune.
Affections de la peau et du tissu sous-cutané
Fréquents: Prurit.
Occasionnels: Angio-œdème, urticaire, éruption cutanée, éruption psoriasiforme, psoriasis (y compris une première poussée ou aggravation et de type pustuleux, principalement palmo-plantaires).
Rares: Vascularite cutanée (y compris vascularite leucocytoclastique), syndrome de Stevens-Johnson, érythème polymorphe.
Très rares: Syndrome de Lyell.
Affections musculo-squelettiques et systémiques
Rares: Lupus érythémateux cutané subaigu, lupus érythémateux discoïde, syndrome lupique.
Troubles généraux et anomalies au site d'administration
Très fréquents: Réactions au site d'injection (37%) (y compris saignement, contusion, érythème, démangeaison, douleur, gonflement)*.
Fréquents: Fièvre*.
Affections cardiaques
Des cas d'aggravation de l'insuffisance cardiaque congestive (voir «Mises en garde et précautions»).
* Voir «Informations complémentaires» ci-dessous.
Informations complémentaires
Réactions au site d'injection
L'incidence des réactions au site d'injection a été significativement plus élevée chez les patients atteints d'affections rhumatismales traités par étanercept comparativement au placebo (36% vs 9%). Toutes les réactions au site d'injection (érythème et/ou démangeaisons, douleur ou tuméfaction) sont survenues généralement au cours du premier mois de traitement, pour devenir ensuite moins fréquentes. Leur durée moyenne était 4 jours. La majorité des réactions au site d'injection dans les groupes traités par étanercept n'a nécessité aucun traitement correcteur. La majorité des patients ayant reçu un traitement correcteur ont reçu des préparations topiques telles que des corticostéroïdes ou des antihistaminiques oraux. Par ailleurs, certains patients ont développé des réactions «de rappel» caractérisées par l'apparition d'une réaction cutanée au site d'injection le plus récent, accompagnée de réactions cutanées aux sites d'injections précédents. Ces réactions étaient généralement transitoires et ne sont pas réapparues lors de la poursuite du traitement.
Dans les essais contrôlés chez les patients atteints de psoriasis en plaques, approximativement 13,6% des patients traités par étanercept ont développé des réactions au site d'injection au cours des 12 premières semaines de traitement, comparé à 3,4% des patients traités par placebo.
Infections
Au cours des essais cliniques, les infections les plus fréquemment rapportées chez les patients traités par étanercept comme chez les patients traités par placebo étaient des infections des voies respiratoires supérieures («rhumes») et des sinusites. Dans des essais contrôlés contre placebo, l'incidence des infections des voies respiratoires supérieures était de 17% dans le groupe placebo contre 22% dans le groupe étanercept. Chez les patients atteints de polyarthrite rhumatoïde participant aux essais contrôlés contre placebo, ceci correspondait à 0,68 infection par année-patient dans le groupe placebo contre 0,82 dans le groupe étanercept, en prenant en considération la durée d'observation plus longue avec étanercept. Dans les essais contre placebo, aucune augmentation de l'incidence des infections graves n'a été observée avec étanercept (1,3% pour le placebo, 0,9% pour étanercept). Des infections graves sont survenues chez 6,3% des patients atteints de polyarthrite rhumatoïde traités par étanercept jusqu'à 48 mois. Ces infections incluaient des abcès (diverses localisations), bactériémie, bronchite, bursite, cellulite infectieuse, cholécystite, diarrhée, diverticulite, endocardite (suspectée), gastro-entérite, hépatite B, herpès, ulcère de la jambe, infection buccale, ostéomyélite, otite, péritonite, pneumonie, pyélonéphrite, septicémie, arthrite septique, sinusite, infection cutanée, ulcère de la peau, infection urinaire, vascularite et plaie infectée. Dans l'étude contrôlée versus traitement actif d'une durée de 2 ans, dans laquelle les patients étaient traités soit par étanercept seul, soit par le méthotrexate seul, soit par étanercept associé au méthotrexate, les taux d'infections graves étaient similaires parmi les groupes de traitement. Cependant, il ne peut être exclu que l'association d'étanercept au méthotrexate puisse être associée à une augmentation du taux d'infections.
Au cours des essais contrôlés contre placebo dans le rhumatisme psoriasique, il n'y a pas eu de différence dans les taux d'infection entre les patients traités avec étanercept et ceux traités avec le placebo. Aucune infection grave n'a été rapportée chez les patients traités par étanercept au cours de ces essais.
Au cours des essais contrôlés contre placebo dans la spondylarthrite ankylosante, le rhumatisme psoriasique, et le psoriasis en plaques, il n'y a pas eu de différence dans les taux d'infection entre les patients traités avec étanercept et ceux traités avec le placebo.
Au cours des essais en double aveugle et en ouvert dans le rhumatisme psoriasique, un cas d'infection grave (pneumonie) a été rapporté.
Au cours des essais réalisés dans le psoriasis en plaques en double-aveugle et en ouvert sur une durée maximale de 15 mois, des infections graves ont été rapportées chez les patients traités par étanercept, telles que cellulite, gastro-entérite, pneumonie, cholecystite, ostéomyélite et abcès.
Des effets secondaires graves, dont septicémies et décès, ont aussi été rapportés depuis la commercialisation d'étanercept. Certains sont apparus quelques semaines après le début du traitement par étanercept chez des patients présentant des maladies sous-jacentes (p.ex. diabète, insuffisance cardiaque congestive, antécédents infectieux aigus ou chroniques) en plus de leur polyarthrite rhumatoïde (voir «Mises en garde et précautions»). Des données provenant d'un essai clinique réalisé dans la septicémie chez des patients tout venant, indiquent qu'étanercept peut augmenter la mortalité chez les patients atteints de septicémie avérée.
Des infections opportunistes ont été rapportées en association avec étanercept y compris des infections fongiques invasives, à protozoaires, à virus (y compris l'herpès), bactériennes (incluant Listeria et Legionella), et mycobactériennes atypiques. Selon des données combinées des essais cliniques, l'incidence globale des infections opportunistes a été de 0,09% chez les 15'402 sujets ayant reçu étanercept. Le taux d'évènements rapporté à l'exposition a été de 0,06 évènement pour 100 patients-année.
Environ la moitié des cas d'infections opportunistes rapportés dans le monde après commercialisation étaient des infections fongiques invasives. Les infections fongiques invasives les plus fréquemment rapportées étaient dues à Candida, Pneumocystis, Aspergillus et Histoplasma. Plus de la moitié des décès liés à des infections opportunistes était due à des infections fongiques invasives. La majorité des cas de décès concernait des patients atteints de pneumonie à Pneumocystis, d'infection fongique systémique non spécifiée, ou d'aspergillose (voir «Mises en garde et précautions»).
Réactivation de l'hépatite B: comme c'est le cas avec d'autres immunosuppresseurs, une réactivation du virus de l'hépatite B (VHB) a été signalée chez des patients porteurs chroniques de ce virus (p.ex. positifs à l'antigène de surface) et traités par des substances anti-TNF (y compris étanercept). Une relation directe de cause à effet avec étanercept n'a pas été constatée. Les patients avec suspicion d'infection au VHB doivent être évalués pour détecter d'éventuels signes d'infection au VHB dans leurs antécédents avant de commencer un traitement anti-TNF. Les patients identifiés comme porteurs chroniques (p.ex. positifs à l'antigène de surface) devraient être surveillés quant aux signes et symptômes d'une infection évolutive au VHB durant toute la durée du traitement et plusieurs mois après la fin de la thérapie.
Tumeurs malignes
L'apparition de 129 nouvelles tumeurs malignes de différents types a été observée sur un total de 4114 patients atteints de polyarthrite rhumatoïde traités par étanercept dans des essais cliniques jusqu'à 6 ans environ, incluant 231 patients traités par étanercept associé au méthotrexate dans l'étude contrôlée versus traitement actif d'une durée de 2 ans. Les taux et incidences observés dans ces essais cliniques étaient similaires à ceux attendus dans la population étudiée. Un total de 2 tumeurs malignes a été rapporté au cours des études cliniques incluant 240 patients atteints de rhumatisme psoriasique traités par étanercept sur une durée de 2 ans environ.
Dans les études cliniques conduites pendant plus de 2 ans chez 351 patients atteints de spondylarthrite ankylosante, 6 tumeurs malignes ont été rapportées chez des patients traités par étanercept. Dans un groupe de 2711 patients atteints de psoriasis en plaques et traités par étanercept sur une durée maximale de 2,5 ans dans les études en double-aveugle et en ouvert, 30 tumeurs malignes et 43 cancers cutanés non mélanomateux ont été rapportés.
Dans un groupe de 7416 patients traités par étanercept au cours des essais cliniques dans la polyarthrite rhumatoïde, le rhumatisme psoriasique, la spondylarthrite ankylosante et le psoriasis, 18 lymphomes ont été rapportés.
Divers cas de tumeurs malignes, en particulier des lymphomes, ont été rapportés après commercialisation (voir «Mises en garde et précautions»).
Auto-anticorps
Des analyses sanguines à la recherche d'auto-anticorps ont été réalisées à différents moments. Parmi les patients atteints de polyarthrite rhumatoïde pour lesquels le taux d'anticorps anti-nucléaires (AAN) a été mesuré, le pourcentage de patients ayant développé des nouveaux AAN positifs (≥1:40) était plus élevé chez les patients traités par étanercept (11%) que chez les patients traités par placebo (5%). Il a aussi été constaté un pourcentage plus élevé de patients ayant développé des nouveaux anticorps anti-ADN natif, par dosage radio-immunologique (15% des patients traités par étanercept contre 4% des patients traités par placebo) et par recherche sur Crithidia lucilliae (3% des patients traités par étanercept contre 0% des patients traités par placebo). La proportion de patients ayant développé des anticorps anticardiolipines était augmentée de façon similaire dans les deux groupes.
L'impact à long terme d'un traitement par étanercept sur le développement de maladies auto-immunes est inconnu.
Chez certains patients, notamment les patients atteints de PR positifs pour le facteur rhumatoïde, les notifications de pharmacovigilance ont rapporté des cas rares d'apparition d'auto-anticorps associés à des éruptions se présentant sur le plan clinique ou à la biopsie comme un lupus sub-aigu ou comme un lupus discoïde. Des cas de syndrome type lupus ont aussi été rapportés.
Anticorps dirigés contre étanercept
Des anticorps ont été détectés dans le sérum de quelques patients traités par étanercept. Ces anticorps ont tous été non-neutralisants et ont généralement été transitoires. Il semble qu'il n'y ait aucune corrélation entre le développement d'anticorps et l'effet clinique ou des effets indésirables.
Chez les patients traités par des doses autorisées d'étanercept dans des études cliniques d'une durée jusqu'à 12 mois, les taux cumulés d'anticorps anti-étanercept ont été approximativement de 6% chez les sujets ayant une polyarthrite rhumatoïde, de 7,5% chez les patients ayant un rhumatisme psoriasique, de 2% chez les patients ayant une spondylarthrite ankylosante de 7% chez les patients atteints de psoriasis, (9,7% chez les enfants et les adolescents), et de 4,8% chez les patients ayant une arthrite juvénile idiopathique.
La proportion de patients qui ont développés des anticorps contre étanercept dans des essais à long terme (d'une durée jusqu'à 3,5 ans) a augmenté avec le temps, comme attendu. Cependant, du fait de leur nature transitoire, l'incidence des anticorps détectés lors de chaque évaluation a été habituellement inférieure à 7% chez les patients ayant une polyarthrite rhumatoïde et chez ceux atteints de psoriasis.
Dans une étude à long terme dans le psoriasis où des patients ont reçu une dose de 50 mg d'étanercept deux fois par semaine pendant un laps de temps plus long, c'est-à-dire de 96 semaines, l'incidence des anticorps observée lors de chaque contrôle a été jusqu'à environ 9% des patients.
Dans l'étude clinique d'Erelzi avec la préparation de comparaison étanercept chez des patients présentant un psoriasis modéré à sévère, une immunogénicité similairement faible a été observée pour les deux préparations.
Maladie pulmonaire interstitielle
Après commercialisation, des cas de maladie interstitielle du poumon (incluant la pneumopathie et la fibrose pulmonaire) ont été rapportés, dont certains ont eu une issue fatale.
Surveillance biologique
Sur la base des résultats des études cliniques, aucun examen de laboratoire n'est normalement nécessaire en complément de la surveillance médicale attentive des patients.
Parmi les patients atteints de PR traités dans les essais cliniques contrôlés, des effets indésirables graves sont apparus chez 4% des 349 patients traités par étanercept, contre 5% des 152 patients sous placebo. Dans l'essai contrôlé contre traitement actif, les effets indésirables graves sont survenus à la fréquence de 6% parmi les 415 patients traités par étanercept, contre 8% des 217 patients traités par le méthotrexate. Dans le second essai contrôlé versus traitement actif, le taux d'arrêt pour événements indésirables après 2 ans de traitement était similaire parmi les trois groupes de traitement, étanercept (16%), méthotrexate (15%) et étanercept associé au méthotrexate (17%).
Parmi les patients atteints de psoriasis en plaques traités dans les essais cliniques contrôlés par placebo, la fréquence des effets indésirables était de 1% chez les 933 patients traités par étanercept, contre 1% chez les 414 patients sous placebo.
Administration concomitante d'étanercept et de l'anakinra
Dans les études où les patients adultes ont reçu un traitement concomitant par étanercept et l'anakinra, un taux plus élevé d'infections graves a été observé par rapport à étanercept seul; 2% des patients (3/139) ont présenté une neutropénie (polynucléaires neutrophiles <1000/mm³). Tandis qu'il présentait une neutropénie, un patient a développé une cellulite qui a guéri après hospitalisation (voir «Mises en garde et précautions»).
Effets indésirables chez l'enfant atteint d'arthrite juvénile idiopathique
En général, les événements indésirables chez les enfants ont été similaires en fréquence et en nature à ceux observés chez les adultes. Les différences par rapport aux adultes et d'autres particularités sont décrites dans les paragraphes suivants.
Les effets indésirables sévères rapportés dans un essai clinique chez 69 patients atteints d'arthrite juvénile idiopathique âgés de 2 à 18 ans ont été: varicelle avec des symptômes de méningite aseptique, suivie d'une guérison sans séquelle (voir «Mises en garde et précautions»), gastro-entérite, dépression/trouble de la personnalité, ulcère cutané et oesophagite/gastrite, choc septique à streptocoque du groupe A, diabète de type I, infection d'une plaie post-opératoire et infection du tissu mou.
43 sur 69 enfants (62%) atteints d'arthrite juvénile idiopathique ont présenté une infection sous étanercept pendant les 3 mois de l'étude (phase 1, étude en ouvert). La fréquence ainsi que la sévérité des infections étaient similaires chez les 58 patients achevant 12 mois de thérapie prolongée en ouvert. Les infections rapportées chez les patients atteints d'arthrite juvénile idiopathique étaient généralement légères et similaires aux infections normalement observées parmi la population de patients pédiatriques ambulatoires. Le type et la fréquence des autres réactions indésirables chez les patients atteints d'arthrite juvénile idiopathique étaient similaires à ceux observés dans les essais cliniques d'étanercept chez les adultes atteints de polyarthrite rhumatoïde et étaient en général légers. Plusieurs effets indésirables ont été rapportés plus fréquemment chez les 69 patients atteints d'arthrite juvénile idiopathique ayant reçu étanercept pendant 3 mois en comparaison aux 349 patients adultes atteints de polyarthrite rhumatoïde. Il s'agissait de céphalées (19% des patients, 1,7 événements par année-patient), nausée (9%, 1,0 événement par année-patient), douleurs abdominales (19%, 0,74 événement par année-patient), et vomissements (13%, 0,74 événement par année-patient).
Quatre cas de syndrome d'activation macrophagique ont été rapportés au cours des essais cliniques dans l'arthrite juvénile idiopathique.
Au cours de la phase de post-marketing, certaines sources ont rapporté de cas de maladie chronique inflammatoire intestinale (y compris maladie de Crohn) et d'uvéite chez les patients atteints d'arthrite juvénile idiopathique (JIA) traités par étanercept, y compris des cas avec réexposition positive (voir «Mises en garde et précautions»).
Effets indésirables chez l'enfant et l'adolescent atteint de psoriasis en plaques
Dans une étude sur 48 semaines réalisée chez 211 enfants et adolescents atteints de psoriasis en plaques et âgés de 4 à 17 ans, les effets indésirables rapportés ont été similaires à ceux observés dans les études antérieures chez des adultes atteints de psoriasis en plaques.
La maladie de Crohn a été observée aussi bien dans les études cliniques chez les patients d'âge pédiatrique traités par étanercept (ayant tous des antécédents de rhumatisme psoriasique) que chez les patients atteints d'AJI avec un psoriasis manifeste selon les sources de la phase post-marketing.
SurdosageL'étanercept n'a pas induit de mortalité ou de signe notable de toxicité chez la souris ou le rat, à la dose de 2000 mg/kg en administration unique en s.c. ou à la dose de 1000 mg/kg en i.v. Aucune dose limite toxique d'étanercept ni aucune toxicité vis-à-vis d'un organe cible chez le singe cynomolgus n'ont été mises en évidence après administration sous-cutanée d'une dose de 15 mg/kg deux fois par semaine pendant 4 à 26 semaines consécutives. Cette dose, rapportée à l'aire sous la courbe (AUC), a entraîné des concentrations plasmatiques plus de 27 fois supérieures à celles obtenues chez des patients atteints de polyarthrite rhumatoïde et traités à la dose recommandée chez l'homme de 25 mg. Aucune dose limite toxique n'a été observée non plus durant les essais cliniques chez les patients atteints de PR. La posologie la plus élevée ayant été évaluée était une dose d'attaque i.v. de 32 mg/m², suivie de doses s.c. de 16 mg/m² administrées deux fois par semaine. Un patient atteint de PR s'est auto-administré par erreur 62 mg d'étanercept en s.c. deux fois par semaine pendant trois semaines sans présenter d'effets indésirables inattendus. Il n'existe aucun antidote connu d'étanercept.
Propriétés/EffetsCode ATC: L04AB01
Erelzi est un biosimilaire d'étanercept. La biosimilarité à la préparation de comparaison étanercept a été analysée dans des études de comparabilité de la qualité pharmaceutique et de l'activité biologique, ainsi que dans des études de comparabilité précliniques et cliniques.
L'étude clinique avec Erelzi est présentée à la fin du chapitre sur l'efficacité clinique.
L'étanercept est une protéine (humaine) de fusion du récepteur p75 Fc du facteur nécrosant des tumeurs (TNF); il est produit par la méthode des recombinants d'ADN (génie génétique) et exprimé dans des cellules ovariennes de hamster chinois (CHO). L'étanercept est un dimère d'une protéine chimère qui a été obtenue génétiquement en fusionnant le domaine de liaison extracellulaire du récepteur 2 humain du facteur nécrosant des tumeurs (TNFR2/p75) au domaine Fc de l'IgG1 humaine. Ce fragment Fc contient les régions charnière, CH2 et CH3, mais non la région CH1 de l'IgG1. L'étanercept est constitué de 934 acides aminés et son poids moléculaire apparent est d'environ 150 kilodaltons. L'activité de l'étanercept est déterminée en mesurant sa capacité à neutraliser l'inhibition de la croissance des cellules A375 médiée par le TNFα. L'activité spécifique de l'étanercept est de 1,7× 106 unités/mg.
Le facteur nécrosant des tumeurs (TNF) est une cytokine dominante dans le processus inflammatoire de la polyarthrite rhumatoïde (PR). Des taux élevés de TNF sont également retrouvés dans les membranes synoviales et les plaques de psoriasis des patients atteints de rhumatisme psoriasique, et dans le sérum et le tissu synovial des patients atteints de spondylarthrite ankylosante.
Dans le psoriasis en plaques, la migration des cellules de l'inflammation, entre autres les lymphocytes T, induit une concentration accrue du taux de TNF dans les lésions psoriasiques en comparaison avec les régions de la peau non touchées.
L'étanercept est un inhibiteur compétitif de la liaison du TNF à ses récepteurs de surface, inhibant ainsi l'activité biologique du TNF.
Le TNF et la lymphotoxine sont des cytokines pro-inflammatoires qui lient deux récepteurs distincts à la surface des cellules: les récepteurs du facteur nécrosant des tumeurs (TNFR) de 55 kilodaltons (p55) et de 75 kilodaltons (p75). Ces deux TNFR existent naturellement sous des formes membranaires et solubles. On pense que les TNFR solubles régulent l'activité biologique du TNF.
Le TNF et la lymphotoxine existent principalement sous forme d'homotrimères, leur activité biologique étant dépendante de la réticulation des TNFR à la surface des cellules. Les récepteurs dimères solubles tels que l'étanercept présentent une affinité plus marquée pour le TNF que les récepteurs monomères et sont ainsi des inhibiteurs compétitifs considérablement plus puissants de la liaison du TNF à ses récepteurs cellulaires. De plus, l'utilisation d'une région Fc d'immunoglobuline en tant qu'élément de fusion dans la construction d'un récepteur dimère confère à la molécule une demi-vie sérique plus longue.
L'étanercept peut également moduler les réponses biologiques contrôlées par d'autres molécules agissant en aval (par ex. cytokines, adhésines ou protéinases) dont l'activité est induite ou régulée par le TNF.
Efficacité clinique
Cette rubrique présente les données issues de quatre études contrôlées randomisées et de deux études supplémentaires en ouvert (V et VI) chez l'adulte atteint de polyarthrite rhumatoïde, de trois études dans l'arthrite juvénile idiopathique, d'une étude chez l'adulte atteint de rhumatisme psoriasique, de quatre études chez l'adulte atteint de spondylarthrite ankylosante, d'une étude chez l'enfant atteint de psoriasis en plaques et de quatre études en ouvert chez l'adulte atteint de psoriasis en plaques.
Polyarthrite rhumatoïde de l'adulte
La sécurité et l'efficacité d'étanercept ont été évaluées chez 2680 patients atteints de polyarthrite rhumatoïde active (PR).
La sécurité et l'efficacité d'étanercept ont été évaluées dans quatre études randomisées, en double aveugle, contrôlées contre placebo et deux études supplémentaires (V et VI).
L'étude I a évalué 234 patients, âgés de ≥18 ans, ayant une polyarthrite rhumatoïde active, qui ne répondaient pas au moins à un, et au plus à quatre traitements de fond (DMARD, p.ex.: hydroxychloroquine, sels d'or injectables ou per os, méthotrexate, azathioprine, D-pénicillamine, sulfasalazine). Ces patients avaient une polyarthrite rhumatoïde active définie par ≥12 articulations douloureuses, ≥10 articulations gonflées, et l'un des critères suivants: VS ≥28 mm/h, CRP >2,0 mg/dl, ou raideur matinale ≥45 minutes. Des doses de 10 mg ou 25 mg d'étanercept ou un placebo ont été administrés par voie sous-cutanée deux fois par semaine pendant 6 mois consécutifs.
Les résultats des études contrôlées ont été exprimés en pourcentage d'amélioration de la PR, en utilisant les critères de réponse de l'American College of Rheumatology (ACR). Le critère principal d'évaluation de l'étude I était l'obtention d'une réponse ACR 20 à 3 mois. Dans l'étude II, le critère principal était l'obtention d'une réponse ACR 20 à 6 mois. Par définition, une réponse ACR 20 est obtenue si le patient a une amélioration de 20% du nombre d'articulations gonflées et du nombre d'articulations douloureuses, associée à ≥20% d'amélioration d'au moins trois des cinq critères suivants: (1) évaluation de la douleur par le patient, (2) évaluation globale de la maladie par le patient, (3) évaluation globale de la maladie par le médecin, (4) évaluation de la limitation fonctionnelle par le patient, et (5) marqueurs de l'inflammation (VS ou CRP). Les réponses ACR 50 et 70 sont définies selon les mêmes critères, avec respectivement une amélioration de 50% et de 70%.
Les réponses ACR 20 et ACR 50 étaient supérieures chez les patients traités par étanercept par rapport au placebo à 3 et 6 mois (ACR 20: étanercept 62% et 59%, placebo 23% et 11% respectivement à 3 et 6 mois; ACR 50: étanercept 41% et 40%, placebo 8% et 5% respectivement à 3 et 6 mois; p <0,01 étanercept vs placebo à tous les temps de mesure pour les réponses ACR 20 et ACR 50).
Environ 15% des patients recevant étanercept ont obtenu une réponse ACR 70 à 3 mois et à 6 mois, comparativement à moins de 5% des patients sous placebo.
Parmi les patients recevant étanercept, les réponses cliniques ont généralement débuté 1 à 2 semaines après l'initiation du traitement, et ont été quasiment toujours obtenues dans les 3 mois. Une réponse dose-dépendante a été observée; les résultats avec 10 mg étaient intermédiaires entre le placebo et 25 mg. étanercept était significativement supérieur au placebo sur tous les items des critères ACR, ainsi que sur les autres mesures d'activité de la polyarthrite rhumatoïde non compris dans ces critères de réponse ACR, comme la durée de la raideur matinale. L'échelle HAQ (Health Assessment Questionnaire), incluant le handicap, l'activité, l'état mental, l'état général, l'état des fonctions articulaires, a été évaluée tous les 3 mois pendant l'étude. Tous les domaines de l'échelle HAQ ont été améliorés chez les patients traités par étanercept comparés aux patients sous placebo à 3 et 6 mois.
Après l'arrêt d'étanercept, les symptômes d'arthrite sont généralement réapparus au cours du mois suivant. Selon les résultats des études en ouvert, la reprise du traitement par étanercept après des arrêts allant jusqu'à 24 mois, a entrainé la même amplitude de réponse que chez les patients recevant étanercept sans interruption de traitement. Des réponses stables et durables ont été observées chez des patients recevant étanercept sans interruption jusqu'à 10 ans dans les études en ouvert (phase d'extension des études thérapeutiques).
L'efficacité d'étanercept a été comparée avec le méthotrexate dans une étude randomisée, contrôlée contre traitement actif avec des examens radiographiques réalisés en aveugle comme critère principal d'évaluation, chez 632 patients adultes ayant une polyarthrite rhumatoïde active (de durée <3 ans) qui n'avaient jamais reçu de traitement par méthotrexate. Les patients devaient avoir >12 articulations sensibles à la pression, >10 articulations gonflées, et soit une vitesse de sédimentation (VS) >28 mm/h, soit une concentration sérique de CRP >2,0 mg/dl, soit une raideur matinale >45 minutes. Des doses de 10 mg ou de 25 mg d'étanercept ont été administrées par voie sous-cutanée deux fois par semaine jusqu'à 24 mois. Les doses de méthotrexate ont été augmentées de 7,5 mg/semaine à 20 mg/semaine maximum au cours des 8 premières semaines de l'essai et maintenues jusqu'à 24 mois. Avec étanercept 25 mg l'amélioration clinique, y compris le délai d'action sous deux semaines, a été similaire à celle observée lors des essais précédents, et s'est maintenue jusqu'à 24 mois. Le temps de latence a été plus court avec la dose de 25 mg d'étanercept qu'avec le méthotrexate. A l'inclusion, les patients avaient un degré d'invalidité modéré, avec des scores moyens de HAQ de 1,4 à 1,5. Le traitement par étanercept à 25 mg a entraîné une amélioration importante à 12 mois, avec environ 44% de patients obtenant un score de HAQ normal (moins de 0,5). Ce bénéfice a été maintenu la deuxième année de cette étude.
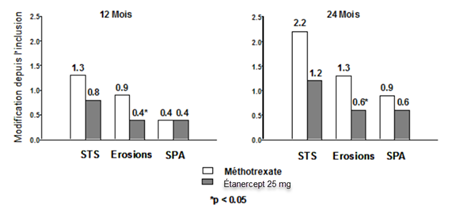
Dans cette étude, les dommages structuraux articulaires ont été évalués radiographiquement et exprimés en modification du Score Total de Sharp (STS) et de ses composants; le «score d'érosion» et le «Score de Pincement Articulaire (SPA)». Les radiographies des mains/poignets et pieds ont été lues à l'inclusion puis à 6, 12 et 24 mois. La dose de 10 mg d'étanercept a eu constamment moins d'effet sur les dommages structuraux que la dose de 25 mg. Étanercept à 25 mg a été significativement supérieur au méthotrexate pour les scores d'érosion, à la fois à 12 et 24 mois. Les différences entre le groupe méthotrexate et le groupe étanercept à 25 mg pour le STS et le SPA n'étaient pas statistiquement significatives. Les résultats sont présentés dans la figure ci-dessous.
Progression radiographique: comparaison d'étanercept vs méthotrexate chez des patients ayant une polyarthrite rhumatoïde d'ancienneté inférieure à 3 ans
Dans une autre étude contrôlée versus traitement actif, randomisée, en double aveugle, l'efficacité clinique, la tolérance, et l'évolution radiographique chez des patients atteints de PR traités par étanercept seul (25 mg deux fois par semaine), ou méthotrexate seul (7,5 à 20 mg par semaine, dose médiane 20 mg) ou étanercept associé au méthotrexate débutés simultanément, ont été comparées chez 682 patients adultes ayant une polyarthrite rhumatoïde active d'ancienneté de 6 mois à 20 ans (médiane 5 ans) et qui avaient eu une réponse insuffisante à au moins un traitement de fond autre que le méthotrexate.
Les patients traités par étanercept associé au méthotrexate avaient des réponses ACR 20, ACR 50 et ACR 70 ainsi qu'une amélioration des scores DAS et HAQ significativement plus élevées à la fois à 24 et 52 semaines, comparativement aux patients de chacun des groupes en monothérapie (résultats présentés dans le tableau ci-dessous). Des avantages significatifs avec étanercept associé au méthotrexate comparé à étanercept en monothérapie et au méthotrexate en monothérapie ont aussi été observés après 24 mois.
Résultats d'efficacité clinique à 12 mois: comparaison d'étanercept vs méthotrexate vs étanercept associé au méthotrexate chez des patients ayant une PR d'ancienneté de 6 mois à 20 ans
|
Critère
|
Méthotrexate
(n=228)
|
Étanercept
(n=223)
|
Étanercept + Méthotrexate
(n=231)
| |
Réponses ACRa
| |
ACR 20
|
58,8%
|
65,5%
|
74,5%†,φ
| |
ACR 50
|
36,4%
|
43,0%
|
63,2%†,φ
| |
ACR 70
|
16,7%
|
22,0%
|
39,8%†,φ
| |
DAS
| |
Score à l'inclusionb
|
5,5
|
5,7
|
5,5
| |
Score semaine 52b
|
3,0
|
3,0
|
2,3†,φ
| |
Rémissionc
|
14%
|
18%
|
37%†,φ
| |
HAQ
| |
Inclusion
|
1,7
|
1,7
|
1,8
| |
Semaine 52
|
1,1
|
1,0
|
0,8†,φ
|
a: les patients qui n'avaient pas terminé les 12 mois de l'étude ont été considérés comme non-répondeurs.
b: les valeurs du Disease Activity Score (DAS) sont des moyennes.
c: la rémission est définie par un DAS <1,6.
Valeur du p lors des comparaisons deux à deux:
†: p <0,05 pour les comparaisons des groupes étanercept + méthotrexate vs méthotrexate.
φ: p <0,05 pour les comparaisons des groupes étanercept + méthotrexate vs étanercept.
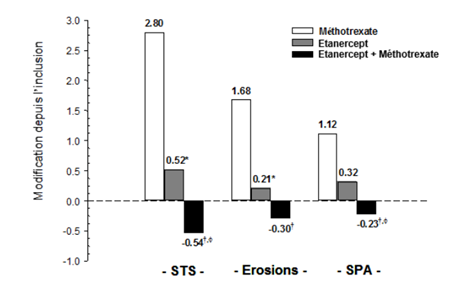
L'évolution radiographique à 12 mois était significativement moins importante dans le groupe étanercept que dans le groupe méthotrexate, alors que l'association était significativement meilleure que chacune des monothérapies pour ralentir l'évolution radiographique (voir figure ci-dessous).
Evolution radiographique: comparaison d'étanercept vs méthotrexate vs étanercept associé au méthotrexate chez des patients ayant une PR d'ancienneté de 6 mois à 20 ans (résultats à 12 mois)
Valeur du p lors des comparaisons deux à deux:
*: p<0,05 pour les comparaisons d'étanercept vs méthotrexate.
†: p <0,05 pour les comparaisons d'étanercept + méthotrexate vs méthotrexate.
φ: p <0,05 pour les comparaisons d'étanercept + méthotrexate vs étanercept.
Des avantages significatifs avec étanercept associé au méthotrexate comparativement à étanercept en monothérapie et au méthotrexate en monothérapie ont aussi été observés après 24 mois. De même, des avantages significatifs avec étanercept en monothérapie comparativement au méthotrexate en monothérapie ont aussi été observés après 24 mois.
Dans une analyse où tous les patients sortis prématurément de l'étude quelle qu'en soit la raison étaient considérés comme s'étant aggravés, le pourcentage de patients sans aggravation (variation du STS ≤0,5) à 24 mois était plus élevé dans le groupe étanercept associé au méthotrexate, comparativement à étanercept seul et au méthotrexate seul (respectivement 62%, 50% et 36%; p <0,05). La différence entre étanercept seul et méthotrexate seul a aussi été significative (p <0,05). Parmi les patients ayant terminé la totalité des 24 mois de traitement dans l'étude, les taux de patients sans aggravation étaient respectivement de 78%, 70% et 61%.
La tolérance et l'efficacité d'étanercept à la dose de 50 mg (deux injections de 25 mg en sous-cutanée) ont été évaluées dans une étude en double aveugle, contrôlée versus placebo chez 420 patients atteints de PR active. Dans cette étude, 53 patients ont reçu du placebo, 214 patients ont reçu 50 mg d'étanercept une fois par semaine et 153 patients ont reçu 25 mg d'étanercept deux fois par semaine. Les profils d'efficacité et de tolérance des deux schémas posologiques d'étanercept ont été similaires à la 8ème semaine sur les signes et symptômes de la PR.
A la 16ème semaine cependant, les deux schémas posologiques n'étaient plus équivalents, avec une tendance non significative en faveur de l'administration plus fréquente d'étanercept.
La biodisponibilité d'une injection unique de 50 mg d'étanercept s'est avérée semblable à celle de 2 injections simultanées de 25 mg.
L'étude V a évalué 89 patients présentant des critères d'inclusion similaires à ceux de l'étude I, en dehors du fait que les patients de l'étude II avaient reçu, en plus, du méthotrexate pendant au moins 6 mois à une dose stable (12,5 à 25 mg/semaine) pendant au moins 4 semaines, et avaient au moins 6 articulations douloureuses. Les patients de l'étude II ont reçu en plus de leur dose stable de méthotrexate, une dose de 25 mg d'étanercept ou un placebo, par voie sous-cutanée, deux fois par semaine pendant 6 mois.
L'étude VI enfin, a évalué 559 patients remplissant des critères d'inclusion similaires à ceux de l'étude I. Les patients ont été traités par étanercept pendant une période allant jusqu'à 6 mois, selon un des quatre schémas thérapeutiques suivants: 10 mg une fois par semaine, 10 mg deux fois par semaine, 25 mg une fois par semaine ou 25 mg deux fois par semaine.
Les résultats des études contrôlées ont été exprimés en pourcentage d'amélioration de la PR, en utilisant les critères de réponse de l'American College of Rheumatology (ACR). Le critère principal d'évaluation de l'étude V était l'obtention d'une réponse ACR 20 à 6 mois. Par définition, une réponse ACR 20 est obtenue si le patient a une amélioration de 20% du nombre d'articulations douloureuses et du nombre d'articulations gonflées, associée à ≥20% d'amélioration d'au moins trois des cinq critères suivants: (1) évaluation de la douleur par le patient, (2) évaluation globale de la maladie par le patient, (3) évaluation globale de la maladie par le médecin, (4) évaluation de la limitation fonctionnelle par le patient, et (5) marqueurs de l'inflammation (VS ou CRP). Les réponses ACR 50 et 70 sont définies selon les mêmes critères, avec respectivement une amélioration de 50% et de 70%. Dans l'étude VI, le critère principal était le pourcentage d'amélioration des articulations douloureuses et gonflées à 3 mois.
Dans les études V et VI, les réponses ont été supérieures chez les patients traités par étanercept, à 3 et à 6 mois.
Dans l'étude V; environ 15% des patients recevant étanercept ont obtenu une réponse ACR 70 à 3 mois et à 6 mois, comparativement à moins de 5% des patients sous placebo. Parmi les patients recevant étanercept, les réponses cliniques ont généralement début 1 à 2 semaines après l'initiation du traitement, et ont été quasiment toujours obtenues dans les 3 mois.
Enfants et adolescents atteints d'arthrite juvénile idiopathique
La sécurité et l'efficacité d'étanercept ont été évaluées dans une étude en 2 phases, chez 69 enfants atteints d'arthrite juvénile idiopathique polyarticulaire ayant présenté différentes formes de début de la maladie (polyarthrite, oligoarthrite, origine systémique). Les patients inclus dans l'étude étaient âgés de 4 à 17 ans, présentaient une arthrite juvénile idiopathique polyarticulaire d'intensité modérée à sévère et étaient réfractaires ou intolérants au méthotrexate. Une dose stable d'un seul anti-inflammatoire non stéroïdien et/ou de prednisone (<0,2 mg/kg/jour ou 10 mg maximum) a été maintenue chez les patients. Dans la première phase de l'étude, tous les patients ont reçu 0,4 mg/kg (maximum 25 mg par injection) d'étanercept administré en sous-cutané deux fois par semaine. Dans la deuxième phase, les patients présentant une réponse clinique au 90e jour, ont été randomisés soit pour rester sous étanercept, soit pour recevoir le placebo pendant 4 mois et ont été surveillés pour détecter toute flambée de la maladie. La réponse a été mesurée en utilisant le score ACR-Pedi 30 (score pédiatrique de l'American College of Rheumatology), à savoir une amélioration ≥30% d'au moins trois des six critères-clés de l'ACJ et une aggravation ≥30% d'au plus 1 des 6 critères. Ces critères incluent le nombre d'articulations atteintes, la limitation des mouvements, l'évaluation globale de la maladie par le médecin et le patient/parent, le handicap fonctionnel et la vitesse de sédimentation (VS). Une flambée de la maladie était définie comme une aggravation ≥30% de trois des six critères-clés de l'ACJ et une amélioration ≥30% d'au plus un des six critères, ainsi qu'un minimum de 2 articulations atteintes.
Dans la première phase de l'étude, 51 des 69 patients (74%) ont bénéficié d'une réponse clinique et ont été inclus dans la deuxième phase de l'étude. Dans la deuxième phase de l'étude, 6 patients sur 25 (24%) maintenus sous étanercept ont eu une flambée de la maladie, en comparaison à 20 patients sur 26 (77%) sous placebo (p=0,007). A partir du début de la deuxième phase de l'étude, la médiane du délai d'apparition de la flambée a été supérieure ou égale à 116 jours pour les patients ayant reçu étanercept et de 26 jours pour les patients sous placebo. Chaque item des critères de l'ACJ s'est aggravé dans le groupe placebo et est resté stable ou s'est même amélioré dans le groupe étanercept. Les données suggèrent la possibilité d'un taux plus élevé de flambée chez les patients présentant une VS plus accélérée. Parmi les patients qui ont bénéficié d'une réponse clinique à 90 jours et qui ont été inclus dans la deuxième phase de l'étude, certains des patients maintenus sous étanercept ont continué à s'améliorer entre le troisième mois et le septième mois alors que ceux sous placebo ne se sont pas améliorés.
Chez 58 patients d'âge pédiatrique de l'étude mentionnée ci-dessus (âgés d'au moins 4 ans au moment de l'inclusion), le traitement par étanercept a été poursuivi sur une période allant jusqu'à 10 ans dans une étude à long terme ouverte destinée à examiner la sécurité. La fréquence des effets indésirables graves et des infections graves n'a pas augmenté avec l'utilisation à long terme.
La sécurité à long terme d'étanercept en monothérapie (n=103), d'étanercept en association avec le méthotrexate (n=294) ou du méthotrexate en monothérapie (n=197) a été évaluée dans une étude de registre réalisée pendant 3 ans chez 594 enfants âgés de 2 à 18 ans atteints d'arthrite juvénile idiopathique. 39 de ces enfants étaient âgés de 2 à 3 ans. Globalement, des infections ont été rapportées plus fréquemment chez les patients traités par l'étanercept que chez les patients traités par le méthotrexate seul (3,8% vs 2%) et les infections associées à l'utilisation d'étanercept ont été plus graves.
Dans une autre étude ouverte à un bras, 60 patients atteints d'une oligoarthrite extensive (extended) (15 patients âgés de 2 à 4 ans, 23 patients âgés de 5 à 11 ans et 22 patients âgés de 12 à 17 ans), 38 patients atteints d'arthrite associée à une enthésite (âgés de 12 à 17 ans) et 29 patients atteints de rhumatisme psoriasique (âgés de 12 à 17 ans) ont reçu une dose hebdomadaire de 0,8 mg/kg de PC d'étanercept (et au maximum 50 mg par injection) pendant 12 semaines. Dans chaque sous-type d'AJI, la majorité des patients a rempli les critères ACR Pedi 30 et a montré des améliorations cliniques dans les critères secondaires d'évaluation tels que le nombre d'articulations douloureuses et l'évaluation globale de la maladie par le médecin. Le profil de sécurité a été comparable à celui observé dans les autres études menées sur l'AJI.
Aucune étude n'a été menée chez les patients atteints d'arthrite juvénile idiopathique dans le but d'évaluer l'influence de la poursuite d'un traitement par étanercept chez les patients qui n'avaient pas répondu 3 mois après le début du traitement par étanercept. En outre, aucune étude n'a été menée chez les patients atteints d'AJI afin d'examiner les effets de l'arrêt ou de la diminution de la dose recommandée d'étanercept après une utilisation à long terme.
Patients adultes atteints de rhumatisme psoriasique
L'efficacité d'étanercept a été évaluée au cours d'un essai clinique randomisé, en double aveugle, contrôlé contre placebo, chez 205 patients atteints de rhumatisme psoriasique. Les patients étaient âgés de 18 à 70 ans et souffraient d'un rhumatisme psoriasique actif (≥3 articulations gonflées et ≥3 articulations douloureuses) dans au moins l'une de ces formes: (1) atteinte interphalangienne distale (AID); (2) polyarthrite (absence de nodules rhumatoïdes et présence de psoriasis); (3) arthropathie destructrice; (4) rhumatisme psoriasique asymétrique; ou (5) ankylose vertébrale de type inflammatoire. Les patients avaient également un psoriasis en plaques avec une lésion caractéristique présentant un diamètre de ≥2 cm. Les patients étaient préalablement traités avec des AINS (86%), des traitements de fond (80%), et des corticoïdes (24%). Les patients également traités par méthotrexate MTX (stable depuis ≥2 mois) pouvaient continuer le méthotrexate à une dose constante ≤25 mg/semaine. Des doses de 25 mg d'étanercept (basé sur les études de recherche de dose chez les patients atteints de polyarthrite rhumatoïde) ou du placebo étaient administrées par voie s.c. deux fois par semaine pendant 6 mois. A la fin de l'étude en double aveugle, les patients pouvaient entrer dans une étude d'extension en ouvert au long cours pour une durée totale allant jusqu' à 2 ans.
La réponse clinique a été exprimée en pourcentages de patients atteignant une réponse ACR 20, 50 et 70 et en pourcentages de patients avec une amélioration des critères de réponse du rhumatisme psoriasique (Psoriatic Arthritis Response Criteria ou PsARC). Les résultats sont résumés dans le tableau ci-après.
Réponses des patients atteints de rhumatisme psoriasique dans l'essai contrôlé contre placebo
|
|
Pourcentage de patients
| |
Placebo
|
Étanercepta
| |
Réponse du rhumatisme psoriasique
|
n=104
|
n=101
| |
ACR 20
| |
Mois 3
|
15
|
59b
| |
Mois 6
|
13
|
50b
| |
ACR 50
| |
Monat 3
|
4
|
38b
| |
Monat 6
|
4
|
37b
| |
ACR 70
| |
Mois 3
|
0
|
11b
| |
Mois 6
|
1
|
9c
| |
PsARC
| |
Mois 3
|
31
|
72b
| |
Mois 6
|
23
|
70b
|
a: Étanercept 25 mg s.c. deux fois par semaine
b: p <0,001, comparé au vs placebo
c: p <0,01, comparé au vs placebo
Parmi les patients atteints de rhumatisme psoriasique qui ont reçu étanercept, les réponses cliniques étaient visibles dès la première visite (à 4 semaines) et se maintenaient pendant les 6 mois de traitement. étanercept a été significativement meilleur que le placebo sur tous les paramètres de l'activité de la maladie (p<0,001), et les réponses étaient similaires avec et sans traitement concomitant par le méthotrexate. La qualité de vie des patients atteints de rhumatisme psoriasique a été mesurée à plusieurs temps d'évaluation à l'aide de l'indice de handicap du questionnaire HAQ. L'indice de handicap était significativement amélioré à tous les temps d'évaluation chez les patients atteints de rhumatisme psoriasique traités par étanercept par rapport au groupe placebo (p<0,001).
Les modifications radiographiques ont été évaluées dans l'étude sur le rhumatisme psoriasique. Des radiographies des mains et des poignets ont été réalisées à l'inclusion et à 6, 12 et 24 mois. Le STS modifié à 12 mois est présenté dans le tableau ci-dessous.
Différence moyenne annualisée du score total de Sharp comparé à l'inclusion
|
|
Placebo
(n=104)
|
Étanercept
(n=101)
| |
Mois 12
|
1,00 (0,29)
|
-0,03 (0,09)a
|
a: p=0,0001, comparé au placebo.
Les capacités fonctionnelles ont été améliorées avec le traitement par étanercept pendant la période en double aveugle, et ce bénéfice a été maintenu au cours de l'exposition à long terme jusqu'à 2 ans.
Dans la forme axiale du rhumatisme psoriasique, proche de la spondylarthrite ankylosante, les preuves d'efficacité d'étanercept sont insuffisantes en raison du nombre trop faible de patients étudiés.
Aucune étude n'a été effectuée chez des patients atteints de rhumatisme psoriasique avec le schéma posologique de 50 mg une fois par semaine. Les preuves de l'efficacité de ce schéma posologique dans cette population de patients reposent sur des données provenant d'une étude chez des patients atteints de spondylarthrite ankylosante.
Patients adultes atteints de spondylarthrite ankylosante
L'efficacité d'étanercept dans la spondylarthrite ankylosante a été évaluée dans 3 études contrôlées, randomisées, en double aveugle, comparant l'administration à deux fois par semaine d'étanercept 25 mg versus placebo. Un total de 401 patients a été inclus dont 203 étaient traités par étanercept. La plus importante de ces études (n=277) a inclus des patients âgés de 18 à 70 ans et qui avaient une spondylarthrite ankylosante active. Celle-ci était définie par des scores d'échelle visuelle analogique (VAS) ≥30 pour la durée et l'intensité moyennes de la raideur matinale, associée à des scores VAS ≥30 pour au moins 2 des 3 paramètres suivants: évaluation globale par le patient; moyenne des valeurs VAS pour la douleur dorsale nocturne et la douleur dorsale totale; moyenne des 10 questions de l'indice fonctionnel de la spondylarthrite ankylosante de Bath (Bath Ankylosing Spondylitis Functional Index ou BASFI). Les patients recevant des traitements de fond, des AINS ou des corticoïdes pouvaient continuer ces traitements à des doses constantes. Les patients présentant une ankylose complète de la colonne vertébrale n'ont pas été inclus dans l'étude. Des doses de 25 mg d'étanercept (déterminées lors des études de recherche de dose chez les patients atteints de polyarthrite rhumatoïde) ou du placebo ont été administrées par voie sous-cutanée deux fois par semaine pendant 6 mois.
Le critère principal d'efficacité était une amélioration du critère de réponse ASAS (Assessment in Ankylosing Spondylitis, ou évaluation de la spondylarthrite ankylosante) de 20% (ASAS 20). Comparativement au placebo, le traitement avec étanercept a montré des améliorations significatives des réponses ASAS 20, ASAS 50 et ASAS 70 dès la deuxième semaine après l'initiation du traitement (voir tableau ci-après).
Réponses des patients atteints de spondylarthrite ankylosante dans un essai contrôlé contre placebo
|
|
Pourcentage de patients
| |
Réponse de la spondylarthrite ankylosante
|
Placebo
n=139
|
Étanercept
n=138
| |
ASAS 20
| |
2 semaines
|
22
|
46a
| |
3 mois
|
27
|
60a
| |
6 mois
|
23
|
58a
| |
ASAS 50
| |
2 semaines
|
7
|
24a
| |
3 mois
|
13
|
45a
| |
6 mois
|
10
|
42a
| |
ASAS 70
| |
2 semaines
|
2
|
12b
| |
3 mois
|
7
|
29b
| |
6 mois
|
5
|
28b
|
a: p <0,001, comparé au vs placebo.
b: p=0,002, comparé au vs placebo.
De plus, des améliorations significatives ont été observées pour les autres mesures d'activité de la maladie chez les patients atteints de spondylarthrite ankylosante. Comparativement au placebo, étanercept a montré des améliorations significatives de tous les paramètres du critère ASAS (évaluations globales par le patient, douleur nocturne et dorsale, BASFI et inflammation), des marqueurs biologiques de l'inflammation (CRP et VS), de l'évaluation globale par le médecin, et de la mobilité du rachis (test de Schober, ampliation thoracique et mesure de la distance occipit-mur).
Parmi les patients atteints de spondylarthrite ankylosante ayant reçu étanercept, les réponses cliniques sont apparues dès la première visite (2 semaines) et se sont maintenues au cours des 6 mois de traitement. Les réponses étaient similaires chez les patients qui initialement recevaient ou non des traitements concomitants.
Des résultats similaires ont été obtenus au cours des deux essais d'effectifs moins importants réalisés dans la spondylarthrite ankylosante.
Dans une quatrième étude, effectuée en double aveugle, contrôlée versus placebo chez 356 patients atteints de spondylarthrite ankylosante, on a évalué la tolérance et l'efficacité d'étanercept 50 mg (deux injections sous-cutanées de 25 mg) administré une fois par semaine versus étanercept 25 mg administré deux fois par semaine. Les profils de tolérance et d'efficacité des 2 schémas posologiques (50 mg une fois par semaine et 25 mg deux fois par semaine) ont été similaires.
Patients adultes atteints de psoriasis en plaques
La sécurité et l'efficacité d'étanercept ont été évaluées dans quatre études randomisées, contrôlées en double aveugle par placebo.
Les patients «en échec» dans la population cible sont définis comme présentant une réponse insuffisante (PASI <50 ou PGA insatisfaisant), ou une aggravation de la maladie au cours du traitement avec au moins chacun des trois traitements systémiques majeurs disponibles utilisés à une posologie adéquate pendant une durée suffisamment longue pour évaluer la réponse au traitement.
L'efficacité d'étanercept versus les autres traitements systémiques chez les patients avec un psoriasis modéré à sévère (répondeurs aux autres traitements systémiques) n'a pas été évaluée dans des études comparant directement étanercept aux autres traitements systémiques. A la place, l'efficacité et la tolérance d'étanercept ont été évaluées dans quatre études randomisées, contrôlées en double aveugle contre placebo. Le critère primaire d'efficacité dans les quatre études était la proportion de patients dans chaque groupe de traitement qui atteignait le PASI 75 (c'est-à-dire une amélioration par rapport à l'inclusion d'au moins 75% du score Psoriasis Area and Severity Index) à 12 semaines.
L'étude 1 était une étude de phase II chez des patients âgés d'au moins 18 ans et présentant un psoriasis en plaques actif mais cliniquement stable atteignant au moins 10% de la surface corporelle. Cent douze (112) patients ont été randomisés pour recevoir une dose de 25 mg d'étanercept (n=57) ou du placebo (n=55) deux fois par semaine pendant 24 semaines.
L'étude 2 a évalué 652 patients atteints de psoriasis chronique en plaques avec les mêmes critères d'inclusion que dans l'étude 1 et un PASI ≥10 au moment du screening. Erelzi a été administré à des doses de 25 mg une fois par semaine, 25 mg deux fois par semaine ou 50 mg deux fois par semaine pendant 6 mois consécutifs. Au cours des 12 premières semaines de la période de traitement en double aveugle, les patients ont reçu du placebo ou l'une des trois doses d'étanercept décrites ci-dessus. Après 12 semaines de traitement, les patients du groupe placebo ont commencé le traitement en aveugle par étanercept (25 mg deux fois par semaine); les patients dans les groupes de traitement actif ont continué jusqu'à la semaine 24, à la dose à laquelle ils avaient été initialement randomisés.
L'étude 3 a évalué 583 patients et les critères d'inclusion étaient les mêmes que dans l'étude 2. Dans cette étude, les patients ont reçu une dose de 25 mg ou 50 mg d'étanercept, ou du placebo, deux fois par semaine pendant 12 semaines; puis tous les patients ont reçu 25 mg d'étanercept deux fois par semaine en ouvert pendant 24 semaines supplémentaires.
L'étude 4 a évalué 142 patients et les critères d'inclusion étaient similaires à ceux des études 2 et 3. Dans cette étude, les patients ont reçu une dose de 50 mg d'étanercept ou du placebo une fois par semaine pendant 12 semaines; puis tous les patients ont reçu 50 mg d'étanercept une fois par semaine en ouvert pendant 12 semaines supplémentaires.
Dans l'étude 1, le groupe traité par étanercept avait une proportion significativement plus élevée de patients présentant une réponse PASI 75 à la semaine 12 (30%) comparativement au groupe traité par placebo (2%) (p <0,0001). A 24 semaines, 56% des patients dans le groupe traité par étanercept avaient atteint le PASI 75 comparativement à 5% des patients traités par placebo. Les résultats principaux des études 2, 3 et 4 sont présentés ci-dessous.
Réponses des patients atteints de psoriasis dans les études 2, 3 et 4
|
|
Etude 2
|
Etude 3
|
Etude 4
| |
Placebo
|
Étanercept
|
Placebo
|
Étanercept
|
Placebo
|
Étanercept
| |
25 mg
2 fois/sem
|
50 mg
2 fois/sem
|
25 mg
2 fois/sem
|
50 mg
2 fois/sem
|
50 mg
1 fois/sem
|
50 mg
1 fois/sem
| |
n=166
|
n=162
|
n=162
|
n=164
|
n=164
|
n=193
|
n=196
|
n=196
|
n=46
|
n=96
|
n=90
| |
Réponse
|
sem 12
|
sem 12
|
sem 24a
|
sem 12
|
sem 24a
|
sem 12
|
sem 12
|
sem 12
|
sem 12
|
sem 12
|
sem 24a
| |
PASI 50 [%]
|
14
|
58*
|
70
|
74*
|
77
|
9
|
64*
|
77*
|
9
|
69*
|
83
| |
PASI 75 [%]
|
4
|
34*
|
44
|
49*
|
59
|
3
|
34*
|
49*
|
2
|
38*
|
71
| |
DSGAb, pas de lésions apparentes ou presque pas de lésions apparentes [%]
|
5
|
34*
|
39
|
49*
|
55
|
4
|
39*
|
57*
|
4
|
39*
|
64
|
*: p ≤0,0001 comparé au placebo.
a: Aucune comparaison statistique versus placebo n'a été faite à la semaine 24 dans les études 2 et 4 étant donné que le groupe initialement sous placebo a commencé à recevoir étanercept 25 mg deux fois/sem ou 50 mg une fois/sem à partir de la semaine 13 jusqu'à la semaine 24.
b: Dermatologist Static Global Assessment. Pas de lésions apparentes ou presque pas de lésions apparentes définies par 0 ou 1 sur une échelle de 0 à 5.
Parmi les patients atteints de psoriasis en plaques qui recevaient étanercept, des réponses significatives comparativement au placebo sont apparues à la première visite (2 semaines) quant à l'amélioration moyenne du PASI, l'évaluation globale de l'activité de la maladie par le dermatologue, l'amélioration du Dermatology Life Quality Index, ainsi que l'évaluation globale de l'activité de la maladie par le patient. Ces améliorations ont été maintenues durant les 24 semaines de traitement.
L'étude 2 comprenait également une période d'arrêt du traitement au cours de laquelle les patients qui avaient atteint une amélioration du PASI d'au moins 50% à la semaine 24 arrêtaient le traitement. L'apparition d'un rebond (PASI ≥150% de la valeur à l'inclusion) et le délai de rechute (définie par la perte d'au moins la moitié de l'amélioration obtenue entre l'inclusion et la semaine 24) ont été évalués chez les patients qui n'étaient plus sous traitement. Au cours de la période sans traitement, les symptômes du psoriasis sont progressivement réapparus avec un délai médian de rechute de 3 mois. Aucun effet rebond de la maladie et aucun événement indésirable grave lié au psoriasis n'ont été observés. Il existe des données montrant le bénéfice de la reprise du traitement par étanercept chez les patients qui répondaient initialement au traitement.
Dans l'étude 3, la majorité des patients (77%) qui étaient initialement randomisés à la dose de 50 mg deux fois par semaine et avaient leur dose d'étanercept abaissée à 25 mg deux fois par semaine à la semaine 12, ont eu une réponse PASI 75 maintenue jusqu'à la semaine 36. Pour les patients qui recevaient 25 mg deux fois par semaine tout au long de l'étude, la réponse PASI 75 continuait de s'améliorer entre les semaines 12 et 36.
Dans l'étude 4, le groupe traité par étanercept avait une proportion plus élevée de patients avec une réponse PASI 75 à la semaine 12 (38%) comparativement au groupe traité par placebo (2%) (p <0,0001). Pour les patients qui recevaient 50 mg une fois par semaine tout au long de l'étude, les réponses d'efficacité ont continué à s'améliorer avec un PASI 75 à la semaine 24 atteignant 71%.
Dans les études en ouvert à long terme (jusqu'à 34 mois) au cours desquelles étanercept a été administré sans interruption, les réponses cliniques étaient maintenues et la sécurité était comparable aux études à court terme.
Une analyse des données cliniques n'a révélé aucune caractéristique de la maladie à l'inclusion qui pourrait conduire les cliniciens à sélectionner le type de posologie le plus approprié (intermittent ou continu). En conséquence, le choix d'un traitement intermittent ou continu doit être basé sur l'expérience thérapeutique individuelle du patient.
Enfants et adolescents atteints de psoriasis en plaques
L'efficacité d'étanercept a été évaluée dans une étude randomisée, en double aveugle, contrôlée contre placebo, chez 211 enfants et adolescents âgés de 4 à 17 ans, atteints de psoriasis en plaques modéré à sévère (défini par un score sPGA ≥3, une surface cutanée atteinte ≥10% (BSA) et un PASI ≥12). Les patients inclus avaient déjà reçu une photothérapie ou un traitement systémique ou avaient présenté une réponse insuffisante à un traitement topique.
Pendant 12 semaines, les patients ont reçu soit 0,8 mg d'étanercept/kg de poids corporel une fois par semaine (jusqu'à 50 mg) soit un placebo. À la semaine 12, davantage de patients étaient répondeurs en ce qui concerne l'efficacité (p.ex. PASI 75) dans le groupe étanercept que dans le groupe placebo.
Résultats à 12 semaines chez des enfants et adolescents atteints de psoriasis en plaques
|
|
Étanercept
0,8 mg/kg
une fois par semaine
(n=106)
|
Placebo
(n=105)
| |
PASI 75, n (%)
|
60 (57%)a
|
12 (11%)
| |
PASI 50, n (%)
|
79 (75%)a
|
24 (23%)
| |
sPGA pas de lésions apparentes ou minimal, n (%)
|
56 (53%)a
|
14 (13%)
|
Abréviation: sPGA-static Physician Global Assessment.
a p <0,0001, par rapport au placebo.
Après la phase de traitement en double aveugle de 12 semaines, tous les patients ont reçu 0,8 mg d'étanercept/kg de poids corporel (jusqu'à 50 mg) une fois par semaine pendant 24 semaines supplémentaires. Les taux de réponse observés pendant la phase ouverte de l'étude ont été comparables à ceux observés pendant la phase en double aveugle.
Par rapport aux patients à nouveau randomisés dans le groupe étanercept, un nombre significativement plus élevé de patients à nouveau randomisés dans le groupe placebo ont présenté une rechute de la maladie (perte de la réponse au PASI 75) pendant la phase randomisée d'arrêt. En cas de traitement continu, les taux de réponse se sont maintenus pendant une période allant jusqu'à 48 semaines.
La sécurité et l'efficacité continues d'étanercept 0,8 mg/kg de PC (jusqu'à une dose maximale de 50 mg) une fois par semaine observées au cours de l'étude de 48 semaines mentionnée ci-dessus, ont été évaluées au cours d'une étude d'extension ouverte allant jusqu'à 2 ans, qui incluait 181 patients pédiatriques atteints de psoriasis en plaques. L'utilisation d'étanercept sur une longue durée n'a révélé aucun nouvel aspect concernant la sécurité. Le rapport global bénéfice-risque est resté positif et comparable aux résultats de l'étude initiale de 48 semaines.
Étude clinique comparative avec Erelzi
La comparabilité d'Erelzi avec la préparation de comparaison étanercept a été montrée dans une étude multicentrique randomisée en double aveugle chez des patients présentant un psoriasis en plaques modéré à sévère. Les patients ont reçu deux fois par semaine soit 50 mg d'Erelzi (264 patients) soit la préparation de comparaison étanercept (267 patients). Le critère principal d'évaluation était le taux de réponse PASI 75 à la semaine 12. L'équivalence clinique d'Erelzi et de la préparation de comparaison étanercept a été montrée pour le critère principal d'évaluation PASI 75 à la semaine 12:
La différence de traitement entre Erelzi et la préparation de comparaison étanercept était de -2,3% (intervalle de confiance à 95% -9,85%, +5,30%). L'intervalle de confiance à 95% se trouvait dans les limites d'équivalence prédéfinies de -18%, +18%).
Pour résumer, l'étude clinique chez des patients présentant un psoriasis en plaques modéré à sévère confirme que l'efficacité thérapeutique d'Erelzi est comparable à la préparation de comparaison étanercept.
PharmacocinétiqueAbsorption
L'étanercept est absorbé lentement depuis le site d'injection sous-cutanée, atteignant une concentration maximale environ 48 h après administration unique. La biodisponibilité absolue est de 76%. Avec deux doses par semaine, on peut s'attendre à ce que les concentrations à l'état d'équilibre représentent environ deux fois celles que l'on mesure après administration unique. Après l'administration unique en s.c. de 25 mg d'étanercept, la concentration sérique maximale moyenne observée chez les volontaires sains était de 1,65 ± 0,66 µg/ml, l'aire sous la courbe étant de 235 ± 96,6 µg × h/ml. La recherche d'une proportionnalité par rapport à la dose administrée n'a pas fait l'objet d'une évaluation particulière, mais il n'y a aucun signe de saturation de la clairance dans l'intervalle des posologies proposées.
Distribution
La courbe de concentration d'étanercept en fonction du temps est biexponentielle. Le volume de distribution central d'étanercept est de 7,6 l, alors que le volume de distribution à l'état d'équilibre est de 10,4 l.
Les caractéristiques des concentrations sériques moyennes à l'équilibre chez les patients atteints de PR étaient une Cmax de 2,4 mg/l vs 2,6 mg/l, une Cmin de 1,2 mg/l vs 1,4 mg/l, et une aire sous la courbe partielle (AUC) de 297 mg × h/l vs 316 mg × h/l pour la dose de 50 mg d'étanercept une fois par semaine (n=21) vs 25 mg d'étanercept deux fois par semaine (n=16) respectivement. Dans une étude en ouvert, croisée, avec administration unique de deux posologies différentes chez des volontaires sains, il a été démontré que l'administration d'une injection unique de 50 mg/ml d'étanercept était bioéquivalente à deux injections simultanées de 25 mg/ml.
Dans une analyse pharmacocinétique de patients atteints de spondylarthrite ankylosante, les AUC de l'étanercept à l'équilibre ont été de 466 µg × h/ml et de 474 µg x h/ml respectivement pour étanercept 50 mg une fois par semaine (n=154) et étanercept 25 mg deux fois par semaine (n=148).
Elimination
L'étanercept est éliminé lentement par l'organisme. Sa demi-vie est longue, environ 70 h. Sa clairance est d'environ 0,066 l/h chez les patients atteints de polyarthrite rhumatoïde, soit un peu moins que celle observée chez les volontaires sains (0,11 l/h).
La pharmacocinétique d'étanercept chez les patients atteints de polyarthrite rhumatoïde, de spondylarthrite ankylosante, ou de psoriasis en plaques, est similaire.
Cinétique pour certains groupes de patients
Bien que l'on détecte de la radioactivité dans les urines après l'administration d'étanercept radiomarqué à des patients et à des volontaires sains, aucune augmentation des concentrations d'étanercept n'a été observée chez les patients présentant une insuffisance rénale ou hépatique aiguë. La présence d'une insuffisance rénale ou hépatique ne devrait pas nécessiter d'ajustement de la posologie. Il n'a pas été observé de différence pharmacocinétique entre les hommes et les femmes.
Association avec le méthotrexate
Le méthotrexate n'a pas d'effet sur la pharmacocinétique de l'étanercept. On ne peut pas exclure un effet d'étanercept sur la pharmacocinétique et la sécurité d'emploi du méthotrexate, bien que cela soit improbable.
Patients âgés
L'impact du grand âge sur les concentrations sériques d'étanercept a été étudié dans le cadre d'une étude pharmacocinétique de populations. La clairance et le volume estimés chez les patients âgés de 65 à 87 ans étaient comparables aux estimations obtenues chez les patients âgés de moins de 65 ans.
Enfants et adolescents atteints d'arthrite juvénile idiopathique
Dans un essai clinique sur étanercept dans l'arthrite juvénile idiopathique polyarticulaire, 69 patients âgés de 4 à 17 ans ont reçu 0,4 mg/kg d'étanercept deux fois par semaine pendant trois mois. Les concentrations sériques étaient similaires à celles que l'on observe chez les patients adultes atteints de PR.
Enfants et adolescents atteints de psoriasis en plaques
Des enfants et adolescents atteints de psoriasis en plaques (âgés de 4 à 17 ans) ont reçu 0,8 mg d'étanercept/kg de poids corporel (jusqu'à une dose maximale de 50 mg par semaine) une fois par semaine pendant une période allant jusqu'à 48 semaines. A l'état d'équilibre, les taux sériques en vallée moyens ont été compris entre 1,6 et 2,1 µg/ml aux semaines 12, 24 et 48. Ces concentrations moyennes chez les enfants et des adolescents atteints de psoriasis en plaques étaient comparables à celles observées chez les patients atteints d'arthrite juvénile idiopathique (ayant reçu 0,4 mg d'étanercept/kg de poids corporel deux fois par semaine, jusqu'à une dose maximale de 50 mg par semaine). Ces concentrations ont également été comparables à celles observées chez les patients adultes atteints de psoriasis en plaques ayant reçu 25 mg d'étanercept deux fois par semaine.
Données précliniquesLes études de toxicologie sur étanercept n'ont fait apparaître aucune dose limite toxique ni de toxicité vis-à-vis d'un organe cible. Sur la base des résultats d'une batterie de tests réalisés in vitro et in vivo, étanercept est considéré comme non génotoxique. Les études de carcinogénicité, et les évaluations standards de fertilité et de toxicité postnatales, n'ont pas pu être réalisées avec étanercept à cause du développement d'anticorps neutralisants chez les rongeurs.
Étanercept n'a pas induit de mortalité ou de signe notable de toxicité chez la souris ou le rat à la dose de 2000 mg/kg en administration unique sous-cutanée ou à la dose de 1000 mg/kg en injection unique par voie intraveineuse. Aucune dose limite toxique d'étanercept ni aucune toxicité vis-à-vis d'un organe cible chez le singe cynomolgus n'ont été mises en évidence après administration sous-cutanée d'une dose de 15 mg/kg deux fois par semaine pendant 4 à 26 semaines consécutives. Cette dose, rapportée à l'aire sous la courbe (AUC), a entraîné des concentrations plasmatiques plus de 27 fois supérieures à celles obtenues chez des patients atteints de polyarthrite rhumatoïde et traités à la dose recommandée chez l'homme de 25 mg.
Les études précliniques réalisées avec Erelzi n'ont pas fourni de résultats supplémentaires importants d'un point de vue de la sécurité.
Remarques particulièresIncompatibilités
En l'absence d'études d'incompatibilité, ce médicament ne doit pas être mélangé avec d'autres médicaments.
Stabilité
Erelzi ne peut être utilisé au-delà de la date imprimée sur le récipient avec la mention «EXP».
Remarques concernant le stockage
Conserver dans l'emballage original, au réfrigérateur (2–8 °C) et hors de la portée des enfants. Ne pas congeler.
La solution injectable d'Erelzi en seringue pré-remplie et en stylo pré-rempli peuvent être conservées à température ambiante (ne dépassant pas 25 °C) pendant une période maximale unique de 4 semaines. La solution injectable d'Erelzi en seringue pré-remplie et en stylo pré-rempli doivent être jetées et ne doivent plus être remises au réfrigérateur si elles n'ont pas été utilisées dans les quatre semaines suivant la sortie du réfrigérateur et conservées entre 15−25 °C.
Il faut recommander au patient/à la patiente de noter sur la boîte la date à laquelle il/elle a sorti Erelzi du réfrigérateur et la date après laquelle Erelzi ne doit plus être utilisé.
Solution injectable en seringue pré-remplie et en stylo pré-rempli
Conserver le médicament dans l'emballage d'origine pour protéger le contenu de la lumière.
Remarques concernant la manipulation
Solution injectable en seringue pré-remplie
La seringue pré-remplie devrait atteindre la température ambiante avant l'injection; c'est pourquoi il faut la sortir du réfrigérateur environ 15 à 30 minutes avant. Ne pas retirer le capuchon de l'aiguille de la seringue pendant ce temps. N'agitez pas la seringue pré-remplie.
La solution devrait être limpide à légèrement opalescente, incolore à légèrement jaunâtre. Elle peut contenir de petites particules protéiques blanches ou translucides. Si elle est colorée, le liquide présente un aspect trouble ou contient des grumeaux, des flocons ou d'autres particules que celles décrites, il ne faut pas l'utiliser.
Solution injectable en stylo pré-rempli
Avant de faire l'injection, le stylo pré-rempli SensoReady à usage unique d'Erelzi doit atteindre la température ambiante, c'est pourquoi il faut le sortir du réfrigérateur environ 15 à 30 minutes avant l'utilisation. Ne pas retirer le protège-aiguille pendant ce temps. Contrôlez la solution à travers la fenêtre d'inspection, elle doit être limpide à discrètement opalescente, incolore à légèrement jaunâtre. Elle peut contenir de petites particules protéiques blanches ou translucides. Si elle est colorée, si elle semble trouble ou contient des grumeaux, des flocons ou d'autres particules que celles décrites, il ne faut pas l'utiliser.
Tout produit non utilisé ou déchet doit être éliminé.
Numéro d’autorisation66175, 66176 (Swissmedic).
PrésentationSolution injectable en seringue pré-remplie
Erelzi 25 mg/0,5 ml: emballages de 1,2 et 4 seringues pré-remplies. [B]
Erelzi 25 mg/0,5ml: emballages multiples de 12 seringues pré-remplies (3 emballages de 12 seringues pré-remplies). [B]
Erelzi 50 mg/1,0 ml: emballages de 1, 2 et 4 seringues pré-remplies. [B]
Erelzi 50 mg/1.0 ml: emballages multiples de 12 seringues pré-remplies (3 emballages de 12 seringues pré-remplies). [B]
Solution injectable en stylo pré-rempli
Erelzi SensoReady 50 mg/1,0 ml: emballages de 1, 2 et 4 stylos pré-remplis. [B]
Erelzi SensoReady 50 mg/1,0 ml: emballages multiples de 12 stylos pré-remplis (3 emballages de 4 stylos pré-remplis). [B]
Titulaire de l’autorisationSandoz Pharmaceuticals SA, Risch; domicile: Rotkreuz.
Mise à jour de l’informationDécembre 2017.
|


