CompositionPrincipes actifs
Florbetaben (18F)
Excipients
Acide ascorbique: 4,4 mg/ml, éthanol: 118 mg/ml, macrogol 400: 200 mg/ml, ascorbate sodique: 28,8 mg/ml (équivalent à 3,34 mg de sodium/ml), eau pour préparations injectables: 677,5 mg/ml
Spécifications
•Radionucléide Fluor [18F]
•Pureté du radionucléide ≥ 99 %
•Pureté radiochimique ≥ 95 % T
Indications/Possibilités d’emploiCe médicament est un produit à usage diagnostique. Neuraceq est un produit radiopharmaceutique indiqué pour l’évaluation par tomographie par émission de positons (TEP) de la densité des plaques séniles β-amyloïdes dans le cerveau des patients adultes atteints de troubles cognitifs pour le diagnostic de la maladie d’Alzheimer (MA) ou d’autres causes de troubles cognitifs. Il doit être utilisé en association avec un examen clinique.
Un examen négatif montre l’absence de plaques ou la présence de plaques éparses, infirmant ainsi le diagnostic de MA. Pour les limites relatives à l’interprétation d’un examen positif, voir rubriques «Mises en garde et précautions» (Limitations d’utilisation) et «Propriétés/Effets».
Posologie/Mode d’emploiL’activité recommandée chez l’adulte est de 300 MBq de florbetaben (18F). La dose maximale à injecter est de 360 MBq et la dose injectée minimale ne doit pas être inférieure à 240 MBq. Le volume de Neuraceq à injecter peut varier de 0,5 à 10 ml de façon à délivrer l’activité cible de 300 MBq au moment de l’administration intraveineuse.
Populations particulières de patients
Patients âgés
Aucun ajustement posologique n’est recommandé en fonction de l’âge.
Troubles de la fonction rénale et hépatique
L’activité à administrer doit être évaluée soigneusement, une augmentation de l’exposition aux rayonnements étant possible chez ces patients. Voir rubrique «Mises en garde et précautions» (troubles de la fonction rénale et hépatique).
Aucune étude approfondie sur la marge thérapeutique et l’ajustement posologique n’a été menée avec ce médicament dans les populations normales et particulières. Aucune étude sur la pharmacocinétique du florbetaben (18F) n’a été menée chez les patients présentant des troubles de la fonction rénale ou hépatique.
Enfants et adolescents
Neuraceq ne s’applique pas aux enfants et aux adolescents.
Mode d’administration
Neuraceq est destiné à un usage multidose et par voie intraveineuse.
L’activité du florbetaben (18F) doit être mesurée avec un activimètre (calibrateur de dose) juste avant l’injection.
Le florbetaben (18F) ne doit pas être dilué.
La dose est administrée par injection intraveineuse lente en bolus (6 s/ml), suivie d’un rinçage avec environ 10 ml de solution injectable de chlorure de sodium isotonique afin de garantir l’administration de la dose entière. Si le volume d’injection est compris entre 0,5 et 1 ml, seules des seringues de taille appropriée (1 ml) doivent être utilisées et la seringue doit être rincée avec une solution de chlorure de sodium (voir rubrique «Autres remarques» [Instructions pour la préparation des produits radiopharmaceutiques]).
L’injection de florbetaben (18F) doit être strictement réalisée par voie intraveineuse, afin d’éviter une exposition aux rayonnements suite à une extravasation locale, ainsi que des artéfacts d’imagerie.
Acquisition des images
L’acquisition des images de TEP peut commencer environ 90 minutes après l’injection intraveineuse de florbetaben (18F) et dure environ 20 minutes.
Les patients doivent être en décubitus dorsal et leur tête doit être positionnée de sorte à centrer le cerveau, cervelet y compris, dans le champ de vue du scanner TEP. Il est possible d’utiliser de l’adhésif ou d’autres dispositifs de contention flexibles pour réduire les mouvements de la tête. La reconstruction doit comprendre la correction de l’atténuation permettant d’obtenir des coupes transaxiales avec des pixels de taille comprise entre 2,0 et 3,0 mm.
Exposition aux rayonnements
Le tableau 1 ci-dessous présente la dosimétrie telle que calculée à l’aide du logiciel OLINDA (Organ Level INternal Dose Assessment).
Les doses de rayonnements estimées absorbées par les organes sont énumérées dans le Tableau 1, d’après des données obtenues sur des témoins sains caucasiens (n = 17). Les calculs de dosimétrie ont été adaptés au modèle adulte (avec un poids corporel de 70 kg).
Tableau 1: Doses estimées absorbées par les organes dans le cadre d’une injection intraveineuse de Neuraceq à des sujets caucasiens
|
Organe
|
Dose absorbée par les organes par activité administrée [mGy/MBq]
| |
Surrénales
|
0,0130
| |
Cerveau
|
0,0125
| |
Seins
|
0,0074
| |
Paroi de la vésicule biliaire
|
0,137
| |
Tractus gastro-intestinal
| |
Côlon inférieur
|
0,0351
| |
Intestin grêle
|
0,0314
| |
Estomac
|
0,0116
| |
Côlon supérieur
|
0,0382
| |
Cœur
|
0,0139
| |
Reins
|
0,0238
| |
Foie
|
0,0386
| |
Poumons
|
0,0148
| |
Muscles
|
0,00948
| |
Ovaires
|
0,0156
| |
Pancréas
|
0,0139
| |
Moelle rouge
|
0,0122
| |
Cellules ostéogéniques
|
0,0148
| |
Peau
|
0,00689
| |
Rate
|
0,0102
| |
Testicules
|
0,00913
| |
Thymus
|
0,00892
| |
Thyroïde
|
0,00842
| |
Vessie
|
0,0695
| |
Utérus
|
0,0163
| |
Autres organes
|
0,0110
| |
Dose efficace (mSv/MBq)
|
0,0193
|
La dose efficace résultant de l’administration de l’activité recommandée maximale de 360 MBq chez un adulte pesant 70 kg est d’environ 7,0 mSv. Si un examen TDM est pratiqué simultanément dans le cadre de l’examen TEP, l’exposition aux rayonnements augmente en fonction des réglages utilisés pour l’examen TDM. Pour une activité administrée de 360 MBq, la dose de rayonnements habituelle absorbée par l’organe cible (cerveau) est de 4,5 mGy.
Pour une activité administrée de 360 MBq, la dose de rayonnements habituelle absorbée par les organes critiques est de 49,3 mGy pour la vésicule biliaire, de 25,0 mGy pour la vessie, de 13,8 mGy pour la paroi du côlon supérieur, de 12,6 mGy pour la paroi du côlon inférieur, de 11,3 mGy pour l’intestin grêle et de 13,9 mGy pour le foie.
Contre-indicationsHypersensibilité au principe actif ou à l’un des excipients.
Mises en garde et précautionsÉvaluation individuelle du rapport bénéfice-risque
Chez chaque patient, l’exposition aux rayonnements doit être justifiée par le bénéfice diagnostique attendu. L’activité administrée doit, dans tous les cas, être maintenue au niveau le plus bas possible et ne doit pas être supérieure à ce qui est nécessaire pour obtenir les informations diagnostiques.
Ce médicament contient 33,4 mg de sodium par 10 ml (dose maximale), ce qui équivaut à 1,6 % de l’apport alimentaire quotidien maximal recommandé par l’OMS de 2 g de sodium par adulte.
Ce médicament contient au maximum 118 mg/ml d’alcool (éthanol). Un patient reçoit au maximum 10 ml, soit au maximum 1180 mg d’alcool. La quantité en 10 ml de ce médicament est équivalente à 30 ml de bière ou 12 ml de vin. La quantité d’alcool contenue dans ce médicament n’est pas susceptible d’avoir un effet chez les adultes. L’alcool contenu dans ce médicament peut modifier les effets d’autres médicaments. Parlez-en à votre médecin ou à votre pharmacien si vous prenez d’autres médicaments. Si vous êtes enceinte ou que vous allaitez, parlez-en à votre médecin ou à votre pharmacien avant de prendre ce médicament.
Troubles de la fonction rénale et hépatique
Le rapport bénéfice-risque doit être évalué soigneusement, une augmentation de l’exposition aux rayonnements étant possible chez ces patients. Le florbetaben (18F) est principalement excrété par le système hépatobiliaire. Les patients présentant des troubles de la fonction hépatique sont potentiellement plus exposés aux rayonnements. Voir rubrique «Posologique/Mode d’emploi» (Populations particulières de patients).
Enfants et adolescents
Neuraceq ne s’applique pas aux enfants et aux adolescents.
Interprétation des images obtenues au Neuraceq
Les images obtenues avec Neuraceq doivent uniquement être interprétées par des évaluateurs formés à l’interprétation des images de TEP au florbetaben (18F). Un examen négatif montre une densité nulle ou faible des plaques β-amyloïdes du cerveau, un examen positif montre une densité modérée à élevée. Des erreurs d’interprétation des images dans l’évaluation de la densité des plaques séniles β-amyloïdes du cerveau, notamment des faux négatifs et des faux positifs, ont été observées.
Les images de TEP sont interprétées selon des coupes transaxiales à l’aide d’une échelle de gris. L’évaluateur doit comparer l’intensité du signal de la substance grise corticale à l’intensité maximale du signal de la substance blanche. Les images doivent être évaluées de façon méthodique (Figure 1) en commençant au niveau du cervelet, puis en remontant vers le lobe temporal latéral et le lobe frontal jusqu’à la zone du cortex cingulaire postérieur et du précunéus pour finalement atteindre le lobe pariétal.
L’interprétation des images se fait visuellement, en comparant l’activité dans la substance grise corticale avec l’activité dans la substance blanche corticale adjacente. Chacune de ces régions cérébrales (lobe temporal latéral et lobe frontal, cortex cingulaire postérieur, précunéus et lobe pariétal) doit être systématiquement évaluée visuellement et d’après le score RCTU (Regional Cortical Tracer Uptake [fixation corticale régionale du traceur]) (Tableau 2).
Tableau 2: Définitions de l’échelle d’évaluation RCTU (Regional Cortical Tracer Uptake [fixation corticale régionale du traceur])
Score RCTU Conditions d’évaluation
|
Score RCTU
|
Conditions d’évaluation
| |
1 (Absence de fixation du traceur)
|
La fixation du traceur (c.-à-d. l’intensité du signal) dans la substance grise est inférieure à celle observée dans la substance blanche.
| |
2 (Fixation modérée du traceur)
|
Zone(s) plus petite(s) de fixation du traceur dans la substance grise supérieures ou égales à celles observées dans la substance blanche, se prolongeant au-delà du bord de la substance blanche jusqu’au bord cortical externe et observées sur la majorité des coupes concernant la région en question.
| |
3 (Fixation prononcée du traceur)
|
Zone confluente importante de fixation du traceur dans la substance grise supérieure ou égale à celle observée dans la substance blanche, se prolongeant au-delà du bord de la substance blanche jusqu’au bord cortical externe et observée dans toute la région, y compris sur la majorité des coupes concernant la région en question.
|
Remarque: Pour l’attribution d’un score de fixation du traceur dans le cortex, l’observation doit avoir été faite sur la majorité des coupes concernant la région en question.
Figure 1: Cas de TEP avec Neuraceq montrant des exemples de TEP au florbetaben (18F) négatives (ligne du haut) et positives (ligne du bas)
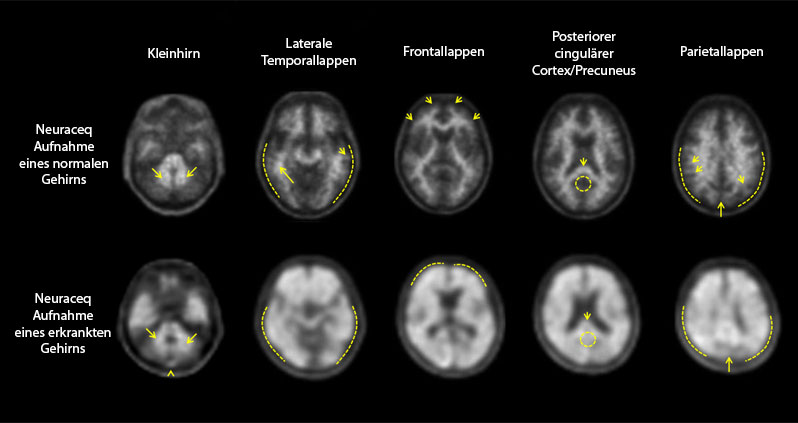
Le résultat global de l’évaluation visuelle de l’examen TEP est basé sur le patient et binaire, à savoir «positif» ou «négatif». Un patient est considéré comme «positif» ou «négatif» d’après le score BAPL (Brain Amyloid Plaque Load [étendue de la plaque amyloïde dans le cerveau]; Tableau 3) qui est dérivé des scores RCTU dans les quatre régions cérébrales (Tableau 2).
Tableau 3: Définitions du score BAPL (Brain Amyloid Plaque Load [étendue de la plaque amyloïde dans le cerveau])
|
Évaluation
|
Score BAPL
|
Conditions d’évaluation
|
| |
Examen négatif
|
1
|
Examen ne révélant aucun dépôt bêta-amyloïde
|
Score RCTU égal à 1 dans chacune des 4 régions cérébrales (lobe temporal latéral, lobe frontal, cortex cingulaire postérieur/précunéus, lobe pariétal)
| |
Examen positif
|
2
|
Examen révélant des dépôts bêta-amyloïdes modérés
|
Score RCTU égal à 2 dans au moins une des 4 régions cérébrales et aucun score égal à 3 dans ces 4 régions
| |
3
|
Examen révélant des dépôts bêta-amyloïdes prononcés
|
Score RCTU égal à 3 dans au moins une des 4 régions cérébrales
|
Limitations d’utilisation
L’injection de florbetaben (18F) doit être strictement réalisée par voie intraveineuse, afin d’éviter une exposition aux rayonnements suite à une extravasation locale, ainsi que des artéfacts d’imagerie.
Un examen positif seul ne permet pas de poser le diagnostic de MA ou d’autres troubles cognitifs, car des dépôts de plaques séniles dans la substance grise peuvent être observés chez des patients âgés asymptomatiques et dans certaines démences neurodégénératives (MA, maladie à corps de Lewy, maladie de Parkinson).
Pour les limites d’utilisation chez les patients atteints de trouble cognitif léger (MCI), voir rubrique «Propriétés/Effets».
L’efficacité du florbetaben (18F) dans la prédiction du développement de la MA ou dans le suivi de la réponse au traitement n’a pas été établie (voir rubrique 14).
Certains examens peuvent être difficiles à interpréter en raison du bruit de l’image, d’une atrophie avec un ruban cortical affiné ou du flou de l’image qui peuvent entraîner des erreurs d’interprétation. En cas d’incertitude sur la localisation de la substance grise et de la frontière substance grise/blanche sur l’image de TEP, et si une image récente de TDM ou d’IRM est disponible, l’évaluateur doit examiner l’image fusionnée TEP-TDM ou TEP-IRM pour clarifier la relation spatiale entre la radioactivité de la TEP et l’anatomie de la substance grise.
Dans certains cas, une augmentation de la fixation a été identifiée dans des structures extra-cérébrales telles que le visage, le cuir chevelu et l’os. Une activité résiduelle peut parfois être observée dans le sinus sagittal supérieur (voir rubrique «Pharmacocinétique»).
Après l’examen
Tout contact étroit avec des enfants en bas âge et des femmes enceintes doit être évité pendant les 24 heures suivant l’injection.
InteractionsAucune étude in vivo des interactions n’a été menée.
Dans des dosages de liaison au ligand radioactif avec un large panel de récepteurs, canaux ioniques et transporteurs animaux et humains, aucune liaison significative n’a été observée.
Les études in vitro utilisant des microsomes hépatiques humains n’ont révélé aucun potentiel d’inhibition du système enzymatique du cytochrome P450.
Grossesse, AllaitementFemmes en âge de procréer
Lorsqu’il est prévu d’administrer un produit radiopharmaceutique à une femme en âge de procréer, il est important de déterminer si elle est enceinte ou non. Toute femme n’ayant pas eu ses règles doit être considérée comme enceinte jusqu’à preuve du contraire. Dans le doute (si la femme a un retard de règles, si les règles sont très irrégulières, etc.), d’autres techniques n’impliquant pas l’emploi de rayonnements ionisants (le cas échéant) doivent être proposées à la patiente.
Grossesse
Les examens de médecine nucléaire chez la femme enceinte entraînent également l’exposition aux rayonnements du fœtus. Seuls les examens essentiels doivent par conséquent être pratiqués pendant la grossesse, dans les cas où le bénéfice prévu est largement supérieur au risque encouru par la mère et le fœtus.
Aucune étude n’a été menée chez les femmes enceintes. Aucune étude expérimentale animale n’a été menée sur la toxicité sur la reproduction du florbetaben (18F) (voir rubrique «Données précliniques»).
Allaitement
On ignore si le florbetaben (18F) est excrété dans le lait maternel. Avant d’administrer un produit radiopharmaceutique à une mère allaitante, il convient d’envisager la possibilité de repousser l’examen jusqu’à la fin de l’allaitement et de réfléchir au choix le plus approprié de produit radiopharmaceutique, en gardant à l’esprit que la radioactivité passe dans le lait maternel. Si l’administration s’avère nécessaire, l’allaitement doit être interrompu pendant 24 heures et le lait tiré doit être éliminé.
Tout contact étroit avec des enfants en bas âge doit être limité pendant les 24 heures suivant l’injection.
Fertilité
Aucune étude de fertilité n’a été menée.
Effet sur l’aptitude à la conduite et l’utilisation de machinesAucune étude correspondante n’a été menée.
Effets indésirablesRésumé du profil de sécurité
Le profil de sécurité global de Neuraceq repose sur des données obtenues sur 1090 administrations de Neuraceq à 872 patients et 12 patients ayant reçu un excipient. L’administration répétée à des intervalles d’un an n’a révélé aucune différence au niveau du profil de sécurité après la première, la deuxième ou la troisième administration.
Liste des effets indésirables
Les effets indésirables sont rangés par fréquence selon la convention suivante: très fréquents (≥ 1/10); fréquents (≥ 1/100, < 1/10); occasionnels (≥ 1/1000, < 1/100); rares (≥ 1/10'000, < 1/1000); très rares (< 1/10'000); fréquence inconnue (ne peut être estimée sur la base des données disponibles). Bien que les effets indésirables puissent survenir en réalité à une fréquence inférieure à celle mentionnée, la taille de la base de données ne permet pas de les classer dans un groupe de fréquence inférieur à «occasionnels» (≥ 1/1000, < 1/100).
|
Classe de système d’organes
|
Effets indésirables
|
Fréquence
| |
Affections gastro-intestinales
|
Diarrhée, nausées
|
Occasionnels
| |
Troubles généraux et anomalies au site d’administration
|
Irritation au site d’injection, douleur au site d’injection, érythème au site d’administration/injection
|
Fréquents
| |
Douleur au site du cathéter, gêne au site d’injection, hématome au site d’injection, chaleur au site d’injection, réaction au site de ponction, douleur au site de ponction vasculaire, fatigue, sensation de chaud, fièvre
|
Occasionnels
| |
Affections hépatobiliaires
|
Fonction hépatique anormale
|
Occasionnels
| |
Investigations
|
Créatinine sanguine augmentée
L’exposition aux rayonnements ionisants peut induire un cancer ou des modifications du matériel génétique. La dose efficace étant de 5,8 mSv environ après l’administration de l’activité recommandée maximale de 300 MBq de florbetaben (18F), la probabilité de survenue de tels effets indésirables est faible.
|
Occasionnels
| |
Affections musculosquelettiques et du tissu conjonctif
|
Extrémités douloureuses, gêne dans un membre
|
Occasionnels
| |
Affections du système nerveux
|
Sensation de brûlure, céphalées, névralgie, tremblements
|
Occasionnels
| |
Affections de la peau et du tissu sous-cutané
|
Hyperhidrose, rash, éruption cutanée toxique
|
Occasionnels
| |
Affections vasculaires
|
Bouffée congestive, hématome, hypotension
|
Occasionnels
|
L’annonce d’effets secondaires présumés après l’autorisation est d’une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d’effet secondaire nouveau ou grave via le portail d’annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageÉtant donné la faible quantité de florbetaben (18F) dans chaque dose, un surdosage n’est pas censé entraîner d’effets pharmacologiques. En cas de surdosage du produit radiopharmaceutique, la dose efficace attendue liée aux rayonnements doit, si possible, être réduite en augmentant l’élimination du radionucléide par des mictions et des défécations fréquentes. Il peut être utile d’estimer la dose efficace liée aux rayonnements.
Propriétés/EffetsCode ATC
V09AX06
Propriétés physiques
Le fluor (18F) se désintègre en oxygène stable (18O) avec une demi-vie d’environ 110 minutes par émission de positons d’une énergie de 634 keV, suivie d’une émission de deux photons d’annihilation d’une énergie de 511 keV.
Mécanisme d’action
Le florbetaben (18F) se lie aux plaques séniles β-amyloïdes dans le cerveau. In vitro, le florbetaben (18F) présente une affinité nanomolaire pour les fibrilles β-amyloïdes synthétiques et pour l’homogénat du cerveau de patients atteints de MA. En outre, la liaison du florbetaben (18F) aux plaques β-amyloïdes dans des sections du cerveau des patients atteints de MA post mortem a été démontrée par autoradiographie et étayée par immunohistochimie ou coloration de Bielschowsky.
Chez des patients en fin de vie, la corrélation quantitative in vivo entre la fixation du florbetaben (18F) dans la substance grise corticale et les dépôts dans les échantillons d’autopsie n’a pas été évaluée. Aucune étude sur la liaison in vivo du florbetaben (18F) aux autres structures β-amyloïdes, ou aux autres structures cérébrales ou récepteurs n’a été menée.
Pharmacodynamique
Aux concentrations chimiques faibles présentes dans Neuraceq, le florbetaben (18F) n’a pas d’activité pharmacodynamique détectable.
Dans les essais cliniques achevés, la fixation du florbetaben (18F) dans 7 zones corticales prédéfinies du cerveau (lobe frontal, pariétal, temporal latéral et médial, occipital, cortex et noyau caudé, gyrus cingulaire postérieur/précunéus et gyrus cingulaire antérieur) et dans le cervelet a été mesurée quantitativement à l’aide des valeurs de fixation normalisées (Standardized Uptake Values, SUV). Les ratios de SUV corticales (SUVR; par rapport au cortex cérébelleux) sont plus élevés chez les patients atteints de MA par rapport à ceux observés chez les témoins sains.
Efficacité clinique
Une étude pivot réalisée sur 31 patients en fin de vie avait pour objectif de déterminer la performance diagnostique du florbetaben (18F) lors de l’évaluation de la densité des plaques séniles β-amyloïdes corticales (nulle ou faible par rapport à modérée ou élevée), d’après les critères CERAD. Les résultats de TEP ont été comparés avec la densité maximale des plaques séniles mesurée sur des sections du gyrus frontal moyen, du gyrus temporal supérieur et moyen, du lobe pariétal inférieur, de l’hippocampe et d’autres régions cérébrales à l’autopsie du patient. Le statut cognitif des patients n’a pas pu être déterminé de manière fiable. Pour les 31 patients, une interprétation visuelle, spécifique au patient, en aveugle de la TEP par 3 évaluateurs en aveugle a généralement révélé une sensibilité de l’interprétation de 100 % (IC à 95 %: 80,5 à 100 %) et une spécificité de 85,7 % (IC à 95 %: 67,4 à 100 %). Dans une analyse post hoc, la sensibilité et la spécificité de l’interprétation visuelle des évaluations spécifiques au patient de la TEP par rapport à l’histopathologie dans une plus grande population (74 patients) étaient respectivement de 97,9 % (IC à 95 %: 93,8 à 100 %) et de 88,9 % (IC à 95 %: 77 à 100 %).
La sensibilité et la spécificité de la détermination des dépôts bêta-amyloïdes au florbetaben (18F) ont fait l’objet d’une étude supplémentaire dans laquelle un groupe différent de 5 évaluateurs en aveugle, formés sur support électronique, a interprété les images de 54 patients de l’étude pivot, étudiés jusqu’à l’autopsie comprise. Les critères d’histopathologie ne correspondaient pas aux critères CERAD. Les résultats étaient inférieurs à ceux obtenus dans l’étude pivot: une sensibilité comprise entre 77,5 et 90 % ainsi qu’une spécificité comprise entre 62,5 et 85,7 %. L’accord inter-évaluateurs d’après les valeurs de kappa selon Fleiss était compris entre 0,68 et 0,87. En comparant les résultats de TEP avec les prélèvements histopathologiques obtenus pour tous les patients (les mêmes utilisés dans l’étude pivot d’origine et son analyse post hoc), la sensibilité et la spécificité était généralement de 100 % (IC à 95 %: 89,4 à 100 %) et 71,4 % (IC à 95 %: 52,1 à 90,8 %), respectivement.
Dans une étude longitudinale, 45 patients (ayant reçu le diagnostic clinique de trouble cognitif léger [mild cognitive impairment, MCI]) ont subi des examens TEP initiaux au florbetaben (18F) et ont été suivis pendant 24 mois pour évaluer la relation entre l’imagerie au florbetaben (18F) et les modifications du statut diagnostique. Au total, 29 (64,4 %) patients atteints de MCI étaient positifs d’après l’examen TEP au florbetaben (18F). Lors de l’examen de suivi à 24 mois, 19 (42,2 %) étaient passés au diagnostic clinique de MA. Sur les 29 patients atteints de MCI ayant présenté un examen TEP positif, un diagnostic clinique de MA a été posé chez 19 (65,5 %) après 24 mois par rapport à 0 (0 %) des 16 patients ayant présenté un examen négatif. La sensibilité de la TEP au florbetaben (18F) pour démontrer la progression d’un MCI en MA chez 19 patients ayant développé une MA était de 100 %, la spécificité chez 26 patients sans progression était de 61,5 % (IC à 95 %: 42,8 à 80,2 %) et le rapport de vraisemblance était de 2,60 (1,60 à 4,23). La conception de l’étude ne permet pas d’estimer le risque de progression d’un MCI en MA clinique.
Enfants et adolescents
Neuraceq ne s’applique pas aux enfants et aux adolescents.
PharmacocinétiqueDistribution
Après injection intraveineuse en bolus, une activité de 2 à 3 % de la dose injectée/l est obtenue dans le plasma artériel 10 minutes après l’injection.
Le florbetaben (18F) est fortement lié aux protéines plasmatiques (> 98,5 %).
Fixation aux organes
La fixation de l’activité dans le cerveau est rapide, atteignant environ 6 % de l’activité injectée 10 minutes après l’injection.
Les témoins sains ont présenté une fixation relativement faible de florbetaben (18F) dans le cortex. Le taux de fixation le plus élevé est observé au niveau du pont et d’autres régions de la substance blanche. Chez les patients atteints de MA, le cortex et le striatum présentent une fixation significativement plus importante que chez les témoins. Chez les patients atteints de MA comme chez les témoins, une fixation importante est observée au niveau du pont et d’autres zones de la substance blanche.
Dans certains cas, une fixation a également été identifiée dans des structures extra-cérébrales telles que le visage, le cuir chevelu et l’os. La cause n’est pas connue, mais peut être due à la fixation du florbetaben (18F) ou de l’un de ses métabolites radioactifs, ou encore à la radioactivité dans le sang.
Une activité résiduelle peut parfois être observée dans le sinus sagittal supérieur, probablement due à la présence du traceur dans le sang.
La base biophysique de la fixation du florbetaben (18F) dans la substance blanche du cerveau de l’être humain ne peut pas être catégoriquement expliquée. L’hypothèse selon laquelle la liaison non spécifique du produit radiopharmaceutique à la gaine de myéline contenant les lipides pourrait contribuer à la fixation dans la substance blanche a été formulée.
Métabolisme
Le florbetaben (18F) est éliminé du plasma des patients atteints de MA avec une demi-vie biologique moyenne d’environ 1 heure. Aucune radioactivité n’a été mesurée dans le sang environ 4 heures après l’injection.
D’après les études in vitro, le florbetaben (18F) est principalement métabolisé par le CYP2J2 et le CYP4F2.
Élimination
12 heures après l’injection, jusqu’à environ 30 % de l’activité injectée sont excrétés dans les urines. Aucune autre activité n’a été détectée dans les urines à des moments ultérieurs.
Demi-vie
Le fluor (18F) a une demi-vie physique de 110 minutes. 98,93 % de l’activité sont désintégrés 12 heures après l’injection et 99,99 % 24 heures après l’injection.
Cinétique pour certains groupes de patients
Patients présentant des troubles de la fonction rénale et hépatique
Aucune étude de pharmacocinétique n’a été menée chez les patients présentant des troubles de la fonction rénale ou hépatique.
Données précliniquesLes données précliniques issues des études conventionnelles sur la pharmacologie de sécurité, la toxicité en administration unique et répétée, et la génotoxicité n’ont pas révélé de risque particulier pour l’homme. La toxicité potentielle de 28 jours d’injections intraveineuses répétées de florbetaben a été évaluée chez des rats et des chiens, et la dose sans effet nocif observable (NOAEL) s’est avérée au moins 20 fois supérieure à la dose maximale chez l’homme.
Aucune étude avec administration chronique et de cancérogénicité n’a été menée, le médicament n’étant pas destiné à être administré de façon régulière ou continue.
Aucune étude de toxicité sur la reproduction n’a été menée.
Autres remarques
Incompatibilités
Comme aucune étude de tolérance n’a été menée, ce médicament ne doit pas être mélangé avec d’autres médicaments.
Influence sur les méthodes de diagnostic
Voir rubrique «Mises en garde et précautions», paragraphe «Limitations d’utilisation».
Stabilité
Jusqu’à 10 heures à compter de la fin de la fabrication (fin de la synthèse). Le médicament ne doit pas être utilisé au-delà de l’heure du jour de fabrication figurant après la mention «EXP» sur l’emballage.
Remarques particulièresRemarques concernant le stockage
Conserver à température ambiante (15-25°C). Conserver dans l’emballage d’origine et le récipient en plomb.
Conseils d’utilisation
Instructions pour la préparation des produits radiopharmaceutiques
Préparation
Avant l’utilisation, le conditionnement doit être vérifié et l’activité mesurée avec un activimètre (calibrateur de dose). Le florbetaben (18F) ne doit pas être dilué.
Le contenu doit être prélevé dans des conditions aseptiques. Les flacons ne doivent pas être ouverts avant la désinfection du bouchon. La solution doit être prélevée à travers le bouchon à l’aide d’une seringue à usage unique munie d’une protection appropriée et d’une aiguille stérile à usage unique, ou d’un système d’administration automatique validé. Le médicament ne doit être utilisé si l’intégrité n’est pas garantie.
Contrôle qualité
Un contrôle visuel de la solution doit être effectué avant l’injection. Seules les solutions limpides et dépourvues de particules visibles peuvent être utilisées.
Prescriptions légales
L’utilisation de matières radioactives chez l’humain est règlementée par l’Ordonnance sur la radioprotection. La manipulation de matières radioactives est soumise à l’autorisation de l’Office fédéral de la santé publique. Les mesures de protection de l’ordonnance précitée doivent être observées lors de la manipulation de matières radioactives ainsi que l’élimination des déchets radioactifs produits afin d’éviter toute exposition aux radiations inutile pour les patients et le personnel. Les solutions radioactives non utilisées et les objets contaminés doivent être conservés dans des lieux de stockage pour décroissance prévus à cet effet jusqu’à la décroissance de l’activité au niveau de libération du radionucléide. L’Ordonnance sur la radioprotection (ORaP, RS 814.501) doit être observée.
Numéro d’autorisation66210
PrésentationLe médicament est fourni dans un flacon multidose, en verre de type 1, incolore, de 15 ml scellé par un bouchon en caoutchouc chlorobutyle et un opercule en aluminium.
Chaque flacon multidose contient de 1,0 à 10 ml de solution, ce qui correspond à 300 à 3000 MBq à l’heure de la calibration.
En raison de différences au niveau du processus de fabrication, il est possible que certains flacons soient distribués avec des bouchons en caoutchouc percés.
Conditionnement: flacon
Catégorie de remise: A
Titulaire de l’autorisationSWAN Isotopen AG, Berne
Mise à jour de l’informationNovembre 2022
|

