Mises en garde et précautionsÉvaluation individuelle du rapport bénéfice-risque
Chez chaque patient, l’exposition aux rayonnements doit être justifiée par le bénéfice diagnostique attendu. L’activité administrée doit, dans tous les cas, être maintenue au niveau le plus bas possible et ne doit pas être supérieure à ce qui est nécessaire pour obtenir les informations diagnostiques.
Ce médicament contient 33,4 mg de sodium par 10 ml (dose maximale), ce qui équivaut à 1,6 % de l’apport alimentaire quotidien maximal recommandé par l’OMS de 2 g de sodium par adulte.
Ce médicament contient au maximum 118 mg/ml d’alcool (éthanol). Un patient reçoit au maximum 10 ml, soit au maximum 1180 mg d’alcool. La quantité en 10 ml de ce médicament est équivalente à 30 ml de bière ou 12 ml de vin. La quantité d’alcool contenue dans ce médicament n’est pas susceptible d’avoir un effet chez les adultes. L’alcool contenu dans ce médicament peut modifier les effets d’autres médicaments. Parlez-en à votre médecin ou à votre pharmacien si vous prenez d’autres médicaments. Si vous êtes enceinte ou que vous allaitez, parlez-en à votre médecin ou à votre pharmacien avant de prendre ce médicament.
Troubles de la fonction rénale et hépatique
Le rapport bénéfice-risque doit être évalué soigneusement, une augmentation de l’exposition aux rayonnements étant possible chez ces patients. Le florbetaben (18F) est principalement excrété par le système hépatobiliaire. Les patients présentant des troubles de la fonction hépatique sont potentiellement plus exposés aux rayonnements. Voir rubrique «Posologique/Mode d’emploi» (Populations particulières de patients).
Enfants et adolescents
Neuraceq ne s’applique pas aux enfants et aux adolescents.
Interprétation des images obtenues au Neuraceq
Les images obtenues avec Neuraceq doivent uniquement être interprétées par des évaluateurs formés à l’interprétation des images de TEP au florbetaben (18F). Un examen négatif montre une densité nulle ou faible des plaques β-amyloïdes du cerveau, un examen positif montre une densité modérée à élevée. Des erreurs d’interprétation des images dans l’évaluation de la densité des plaques séniles β-amyloïdes du cerveau, notamment des faux négatifs et des faux positifs, ont été observées.
Les images de TEP sont interprétées selon des coupes transaxiales à l’aide d’une échelle de gris. L’évaluateur doit comparer l’intensité du signal de la substance grise corticale à l’intensité maximale du signal de la substance blanche. Les images doivent être évaluées de façon méthodique (Figure 1) en commençant au niveau du cervelet, puis en remontant vers le lobe temporal latéral et le lobe frontal jusqu’à la zone du cortex cingulaire postérieur et du précunéus pour finalement atteindre le lobe pariétal.
L’interprétation des images se fait visuellement, en comparant l’activité dans la substance grise corticale avec l’activité dans la substance blanche corticale adjacente. Chacune de ces régions cérébrales (lobe temporal latéral et lobe frontal, cortex cingulaire postérieur, précunéus et lobe pariétal) doit être systématiquement évaluée visuellement et d’après le score RCTU (Regional Cortical Tracer Uptake [fixation corticale régionale du traceur]) (Tableau 2).
Tableau 2: Définitions de l’échelle d’évaluation RCTU (Regional Cortical Tracer Uptake [fixation corticale régionale du traceur])
Score RCTU Conditions d’évaluation
|
Score RCTU
|
Conditions d’évaluation
| |
1 (Absence de fixation du traceur)
|
La fixation du traceur (c.-à-d. l’intensité du signal) dans la substance grise est inférieure à celle observée dans la substance blanche.
| |
2 (Fixation modérée du traceur)
|
Zone(s) plus petite(s) de fixation du traceur dans la substance grise supérieures ou égales à celles observées dans la substance blanche, se prolongeant au-delà du bord de la substance blanche jusqu’au bord cortical externe et observées sur la majorité des coupes concernant la région en question.
| |
3 (Fixation prononcée du traceur)
|
Zone confluente importante de fixation du traceur dans la substance grise supérieure ou égale à celle observée dans la substance blanche, se prolongeant au-delà du bord de la substance blanche jusqu’au bord cortical externe et observée dans toute la région, y compris sur la majorité des coupes concernant la région en question.
|
Remarque: Pour l’attribution d’un score de fixation du traceur dans le cortex, l’observation doit avoir été faite sur la majorité des coupes concernant la région en question.
Figure 1: Cas de TEP avec Neuraceq montrant des exemples de TEP au florbetaben (18F) négatives (ligne du haut) et positives (ligne du bas)
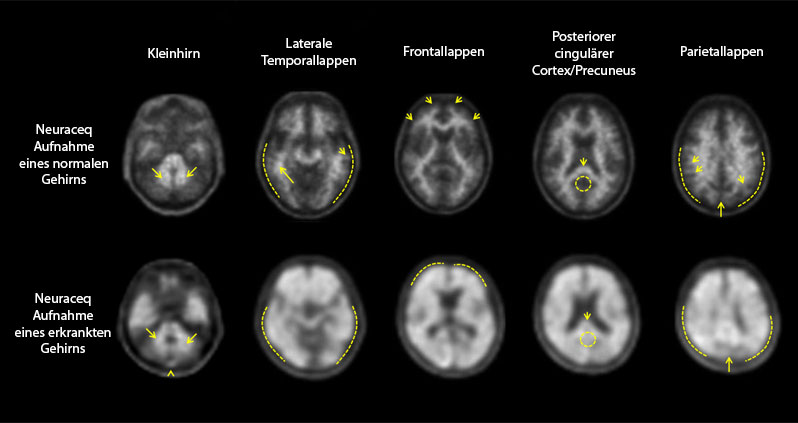
Le résultat global de l’évaluation visuelle de l’examen TEP est basé sur le patient et binaire, à savoir «positif» ou «négatif». Un patient est considéré comme «positif» ou «négatif» d’après le score BAPL (Brain Amyloid Plaque Load [étendue de la plaque amyloïde dans le cerveau]; Tableau 3) qui est dérivé des scores RCTU dans les quatre régions cérébrales (Tableau 2).
Tableau 3: Définitions du score BAPL (Brain Amyloid Plaque Load [étendue de la plaque amyloïde dans le cerveau])
|
Évaluation
|
Score BAPL
|
Conditions d’évaluation
|
| |
Examen négatif
|
1
|
Examen ne révélant aucun dépôt bêta-amyloïde
|
Score RCTU égal à 1 dans chacune des 4 régions cérébrales (lobe temporal latéral, lobe frontal, cortex cingulaire postérieur/précunéus, lobe pariétal)
| |
Examen positif
|
2
|
Examen révélant des dépôts bêta-amyloïdes modérés
|
Score RCTU égal à 2 dans au moins une des 4 régions cérébrales et aucun score égal à 3 dans ces 4 régions
| |
3
|
Examen révélant des dépôts bêta-amyloïdes prononcés
|
Score RCTU égal à 3 dans au moins une des 4 régions cérébrales
|
Limitations d’utilisation
L’injection de florbetaben (18F) doit être strictement réalisée par voie intraveineuse, afin d’éviter une exposition aux rayonnements suite à une extravasation locale, ainsi que des artéfacts d’imagerie.
Un examen positif seul ne permet pas de poser le diagnostic de MA ou d’autres troubles cognitifs, car des dépôts de plaques séniles dans la substance grise peuvent être observés chez des patients âgés asymptomatiques et dans certaines démences neurodégénératives (MA, maladie à corps de Lewy, maladie de Parkinson).
Pour les limites d’utilisation chez les patients atteints de trouble cognitif léger (MCI), voir rubrique «Propriétés/Effets».
L’efficacité du florbetaben (18F) dans la prédiction du développement de la MA ou dans le suivi de la réponse au traitement n’a pas été établie (voir rubrique 14).
Certains examens peuvent être difficiles à interpréter en raison du bruit de l’image, d’une atrophie avec un ruban cortical affiné ou du flou de l’image qui peuvent entraîner des erreurs d’interprétation. En cas d’incertitude sur la localisation de la substance grise et de la frontière substance grise/blanche sur l’image de TEP, et si une image récente de TDM ou d’IRM est disponible, l’évaluateur doit examiner l’image fusionnée TEP-TDM ou TEP-IRM pour clarifier la relation spatiale entre la radioactivité de la TEP et l’anatomie de la substance grise.
Dans certains cas, une augmentation de la fixation a été identifiée dans des structures extra-cérébrales telles que le visage, le cuir chevelu et l’os. Une activité résiduelle peut parfois être observée dans le sinus sagittal supérieur (voir rubrique «Pharmacocinétique»).
Après l’examen
Tout contact étroit avec des enfants en bas âge et des femmes enceintes doit être évité pendant les 24 heures suivant l’injection.
| 
