CompositionPrincipes actifs
·insulinum glarginum (humanum insulinum analogum) (21A-Gly-30Ba-L-Arg-30Bb-L-Arg-humanum insulinum), produite par la technique de l'ADN recombinant à l'aide de souches K12 d'Escherichia coli.
·lixisenatidum
Excipients
Glycerolum, Methioninum, Conserv.: Metacresolum 2,7 mg, Zinci chloridum, Acidum hydrochloridum (pour l'ajustement du pH), Natrii hydroxidum (pour l'ajustement du pH), Aqua ad iniectibilia qs ad solutionem pro 1 ml.
Indications/Possibilités d’emploiSuliqua est utilisé en association avec de la metformine dans le traitement du diabète de type 2 chez l'adulte, quand la metformine seule, le traitement combiné par metformine et sulfonylurée, la metformine en association avec un agoniste des récepteurs du GLP-1 ou le traitement combiné par metformine et insuline basale ne permet pas de garantir un contrôle glycémique adéquat.
Posologie/Mode d’emploiPosologie
Suliqua est disponible sous deux concentrations, offrant différentes options posologiques. La différence entre les deux concentrations/stylos pré-remplis repose sur la fourchette posologique proposée par chacun d'eux.
Suliqua 100/50 (Stylo pré-rempli SoloStar jaune 10-40)
Suliqua 100/50 permet d'administrer des doses quotidiennes de 10 à 40 doses unitaires (10 à 40 unités d'insuline glargine et 5 à 20 µg de lixisénatide).
Suliqua 100/33 (Stylo pré-rempli SoloStar vert 30-60)
Suliqua 100/33 permet d'administrer des doses quotidiennes de 30 à 60 doses unitaires (30 à 60 unités d'insuline glargine et 10 à 20 µg de lixisénatide).
Pour éviter toute erreur de traitement, le médecin doit s'assurer que l'ordonnance précise bien la concentration, le type de stylo pré-rempli à utiliser et la dose.
La dose quotidienne maximale de Suliqua est de 60 doses unitaires (60 unités d'insuline glargine et 20 µg de lixisénatide).
Suliqua est administré par voie sous-cutanée une fois par jour, dans l'heure qui précède n'importe quel repas de la journée.
Il est préférable que l'injection prandiale de Suliqua soit effectuée chaque jour à la même heure, d'où la nécessité pour le patient de choisir le repas le plus pratique pour lui et de préférence avant le petit-déjeuner. En cas d'oubli d'une injection, Suliqua doit être administré dans l'heure précédant le repas suivant.
La dose de Suliqua administrée est une dose individuelle basée sur la réponse clinique du patient. Elle est déterminée en fonction du besoin du patient en insuline. La dose de lixisénatide augmente ou diminue avec la dose d'insuline glargine et dépend également du stylo utilisé.
L'ajustement par le patient de la dose ou du moment de l'injection, doit se faire uniquement sous examen médical avec une surveillance appropriée de la glycémie (voir «Mises en garde et précautions»).
Dose initiale de Suliqua
La dose initiale de Suliqua sélectionnée est déterminée en fonction du traitement antidiabétique antérieur et de manière à ne pas dépasser la dose initiale de 10 µg recommandée pour le lixisénatide.
Tout traitement antérieur avec une insuline, un agoniste des GLP-1 ou un anti-diabétique oral autre que la metformine devrait être arrêté avant d'instaurer un traitement avec Suliqua.
·Après un traitement antérieur avec des antidiabétiques oraux, associés ou non à un agoniste des récepteurs du GLP-1, la posologie initiale recommandée est de 10 doses unitaires de Suliqua 100/50 par jour.
·Après un traitement antérieur avec une insuline basale administrée 1 fois par jour (excepté Toujeo), se référer au tableau ci-dessous pour la détermination de la dose initiale quotidienne de Suliqua.
·Après un traitement antérieur avec une insuline basale administrée 2 fois par jour ou avec Toujeo (insuline glargine 300 unités/ml), la dose quotidienne précédemment administrée doit être réduite de 20% avant de choisir la dose initiale de Suliqua selon le tableau ci-dessous.
|
Traitement antérieur: insuline basale
| |
Dose d'insuline quotidienne*
|
≥10 à <20 unités
|
≥20 à <30 unités
|
≥30 à ≤60 unités
| |
Dose initiale et stylo
|
Suliqua
100/50
|
10 doses unitaires/jour
(10 unités/5 µg)**
|
20 doses unitaires/jour
(20 unités/10 µg)**
|
| |
Suliqua
100/33
|
|
30 doses unitaires/jour
(30 unités/10 µg)**
|
* dose précédemment réduite de 20% si le patient était précédemment traité avec Toujeo (insuline glargine 300 unités/ml) ou avec une insuline administrée 2 fois/jour.
** unités d'insuline glargine (100 unités/ml)/ microgrammes de lixisénatide
La dose quotidienne maximale est de 60 unités d'insuline glargine et 20 µg de lixisénatide correspondant à 60 doses unitaires.
Ajustement posologique de Suliqua
La posologie de Suliqua doit être déterminée en fonction des besoins du patient en insuline. Il est recommandé d'optimiser le contrôle glycémique par un ajustement posologique en se basant sur le glucose plasmatique à jeun (voir «Propriétés pharmacodynamiques»). Une surveillance étroite de la glycémie est recommandée lors du passage à Suliqua et pendant les semaines suivantes.
·Si le patient commence avec Suliqua 100/50, la dose peut aller jusqu'à 40 doses unitaires.
·Pour des doses >40 doses unitaires/jour, opter pour Suliqua 100/33.
·Si le patient commence avec Suliqua 100/33, la dose peut aller jusqu'à 60 doses unitaires.
·La dose journalière maximale est de 60 doses unitaires. Ne pas utiliser Suliqua pour des doses supérieures à 60 doses unitaires/jour.
Mode d'administration
Suliqua est injecté par voie sous-cutanée dans l'abdomen, le muscle deltoïde, ou la cuisse.
Suliqua Solostar, stylo pré-rempli, convient uniquement aux injections sous-cutanées.
La vitesse d'absorption et par conséquent le début et la durée d'action du produit peuvent varier avec l'exercice physique et avec d'autres paramètres comme le stress, les maladies intercurrentes, les changements de traitements médicamenteux concomitants ou la prise des repas.
Une rotation des sites d'injection dans une même zone (abdomen, muscle deltoïde ou cuisse) est recommandée d'une injection à l'autre afin de réduire ou d'éviter des risques de lipodystrophie et d'amyloïdose cutanée (voir les sections «Mises en garde et précautions» et «Effets indésirables»). Suliqua ne doit pas être prélevé d'une cartouche de stylo pré-rempli Solostar à l'aide d'une seringue sous peine d'erreur de dose et potentiellement de surdosage.
Afin d'assurer la traçabilité des médicaments biotechnologiques, il convient de documenter pour chaque traitement le nom commercial et le numéro de lot.
Populations particulières
Patients âgés
Suliqua peut être administré chez le sujet âgé. La dose doit être ajustée en fonction du patient, en se basant sur la surveillance de la glycémie.
Patients présentant des troubles de la fonction rénale
Chez les patients insuffisants rénaux, les besoins en insuline peuvent être diminués en raison d'une réduction du métabolisme de l'insuline. L'administration de Suliqua peut impliquer une surveillance de la glycémie et un ajustement posologique fréquents chez les patients insuffisants rénaux. Il n'existe aucune expérience thérapeutique de l'utilisation du lixisénatide chez les patients avec une insuffisance rénale sévère (clairance de la créatinine inférieure à 30 ml/min) ou une insuffisance rénale terminale; l'administration de Suliqua chez ces populations n'est donc pas recommandée.
Patients présentant des troubles de la fonction hépatique
Le lixisénatide est éliminé principalement par les reins. Un dysfonctionnement hépatique n'est donc pas censé influer sur la pharmacocinétique du lixisénatide. Chez les patients insuffisants hépatiques, les besoins en insuline peuvent être diminués en raison d'une réduction de la capacité de néoglucogenèse et d'une réduction du métabolisme de l'insuline. L'administration de Suliqua peut impliquer une surveillance de la glycémie et un ajustement posologique fréquents chez les patients insuffisants hépatiques.
Enfants et adolescents
La sécurité et l'efficacité de Suliqua chez l'enfant et l'adolescent de moins de 18 ans n'ont pas été établies.
Contre-indicationsHypersensibilité à l'une des substances actives ou aux deux substances actives, ou à l'un des excipients.
Mises en garde et précautionsSuliqua ne doit pas être utilisé pour le traitement du diabète de type 1 ou le traitement de l'acidocétose diabétique.
En principe, l'insulinothérapie exige du patient qu'il soit capable de gérer son affection diabétique de manière indépendante, c'est-à-dire le contrôle de sa glycémie, l'apprentissage de la technique d'injection correcte et un comportement adéquat face aux situations métaboliques d'hypoglycémie et d'hyperglycémie. Les patients doivent suivre une formation afin de pouvoir appliquer les mesures nécessaires de manière indépendante. Par ailleurs, il convient d'expliquer aux patients le comportement à adopter dans les situations d'exception qui peuvent se produire lorsque les administrations d'insuline sont insuffisantes, lorsqu'elles ont été oubliées ou lorsque par inadvertance elles sont trop élevées ou encore en cas d'absorption insuffisante de nourriture ou de repas omis.
Avant d'utiliser le stylo pré-rempli, le mode d'emploi du stylo se trouvant avec la notice d'emballage doit être lu soigneusement. Le stylo pré-rempli doit être manipulé selon les indications décrites. Afin d'éviter la transmission de maladies, chaque stylo prêt à l'emploi ne doit être utilisé que par une seule personne.
Le traitement par l'insuline exige une attention constante en ce qui concerne les hyperglycémies ou les hypoglycémies éventuelles. Les patients et leurs proches doivent savoir quelles mesures correctrices ils doivent prendre lorsqu'une hyperglycémie ou une hypoglycémie se manifeste ou est supposée, et à quel moment il est opportun d'informer le médecin.
Si l'équilibre glycémique n'est pas optimal ou si le patient a tendance à présenter des épisodes hyperglycémiques ou hypoglycémiques, il faut d'abord vérifier le respect par le patient du traitement prescrit, les sites et les techniques d'injection, le maniement du stylo et l'ensemble des autres facteurs susceptibles d'augmenter la tendance à l'hyper- ou l'hypoglycémie, avant d'envisager l'ajustement de la dose d'insuline.
Le passage à une autre préparation insulinique ne devrait avoir lieu que sous contrôle médical strict et selon des instructions précises. De même, le schéma de traitement ne doit être modifié qu'après entretien avec le médecin ou selon ses indications.
Les patients doivent avoir pour instruction de varier constamment les sites d'injection à chaque administration afin de réduire le risque de développer une lipodystrophie et une amyloïdose cutanée. Il existe un risque potentiel de retard dans l'absorption de l'insuline et d'aggravation du contrôle de la glycémie après des injections d'insuline aux sites présentant ces réactions. Il a été signalé qu'un changement soudain du site d'injection vers une zone non touchée pouvait entraîner une hypoglycémie. Il est recommandé de surveiller la glycémie après le changement de site d'injection et d'envisager un ajustement de la dose des médicaments antidiabétiques.
Hypoglycémie
L'hypoglycémie est la réaction indésirable la plus souvent signalée pendant le traitement sous Suliqua. Une hypoglycémie peut se produire si la dose de Suliqua injectée est supérieure à la dose nécessaire. Pour le diabétique traité à l'insuline, il existe en principe un risque d'hypoglycémie plus ou moins sévère. Celle-ci peut entraîner une diminution de l'attention, particulièrement lors de la conduite d'un véhicule ou de l'utilisation de machines. Le risque d'hypoglycémie est généralement plus élevé en début de traitement, lors de changement de préparation, d'injections irrégulières, de repas irréguliers, ainsi que plus généralement lors de diabète mal ou non équilibré (fortes fluctuations de la glycémie). Le patient doit être informé de ce risque accru d'hypoglycémie.
Sont à considérer entre autres comme causes de l'hypoglycémie: repas omis, vomissements, diarrhées, effort physique inhabituel, surdosage d'insuline, maladies endocriniennes telles qu'insuffisance surrénalienne, hypothyroïdie, administration conjointe de certains autres médicaments, changement de zone d'injection, amélioration de la sensibilité à l'insuline (par exemple après élimination de facteurs de stress).
En outre, les patients ayant déjà été atteints d'hypoglycémie sévère présentent un risque élevé de récidive.
Afin de prévenir l'hypoglycémie, il y a lieu de recommander au patient de se munir constamment de sucre de raisin, de sucre en morceaux ou équivalents. Il doit aussi porter sur lui sa carte de diabétique.
Le moment de survenue d'une hypoglycémie dépend du profil d'action des insulines utilisées et peut donc changer après modification du schéma de traitement.
Il faut être particulièrement prudent et intensifier la surveillance de la glycémie chez les patients pour lesquels les épisodes hypoglycémiques risqueraient d'avoir des conséquences cliniques particulièrement graves, par exemple en cas de sténose serrée des artères coronaires ou carotidiennes (risque de complications cardiaques ou cérébrales de l'hypoglycémie), de même qu'en cas de rétinopathie proliférante, surtout si celle-ci n'est pas traitée par photocoagulation (risque d'amaurose transitoire après une hypoglycémie).
Si le taux d'hémoglobine glycosylée est normal ou abaissé, la possibilité d'épisodes hypoglycémiques récidivants passés inaperçus (surtout nocturnes) doit être évoquée.
Les symptômes d'une hypoglycémie sont:
Des signes neurovégétatifs: sueurs, sensation de faim, tremblements (dits symptômes d'alarme neurovégétatifs), pâleur, palpitations, céphalées.
Des signes neuroglycopéniques: troubles de la concentration, modification du comportement (entre autres agitation, nervosité, agressivité, état confusionnel), troubles de la conscience, de la coordination, de la vue et de la parole. Ceux-ci peuvent aller jusqu'à l'étourdissement, la somnolence et même la perte de connaissance. L'hypoglycémie peut aussi provoquer des crises épileptiques ou se manifester comme un ictus cérébral, accompagné p.ex. d'hémiparésie (en général passagère), d'aphasie et de réflexe de Babinski positif.
Signes d'alarme atténués/modifiés: les signes d'alarme de l'hypoglycémie peuvent être modifiés et les symptômes neurovégétatifs l'accompagnant peuvent être perçus de façon atténuée ou retardée, en particulier lors de traitement visant des taux de glycémie basse (p.ex. traitement selon le principe dose de basal-bolus par injections répétées), lors de diabète ancien (éventuellement accompagné de polynévrite), chez les personnes âgées ou lors de changement d'insuline.
Les β-bloquants peuvent réduire ou masquer les symptômes d'alerte courants de l'hypoglycémie.
Veuillez donc informer le diabétique traité à l'insuline et son entourage que l'hypoglycémie peut se déclarer de manière soudaine et d'abord par des signes neuroglycopéniques tels que troubles de la concentration, agitation, troubles du comportement et de la conscience avec le risque de négliger de prendre du sucre à temps.
La consommation d'alcool peut augmenter le risque d'hypoglycémie (inhibition de la néoglucogenèse hépatique). Il convient de prendre en compte que la teneur en hydrates de carbone des boissons alcoolisées pourrait aussi entraîner une augmentation de la glycémie.
Traitement de l'hypoglycémie (voir «Surdosage»):
Après chaque hypoglycémie sévère, il convient de rééquilibrer le diabète. Par conséquent, il faut recommander au patient d'informer le médecin de chaque hypoglycémie sévère subie.
Les facteurs qui augmentent la sensibilité à l'hypoglycémie imposent une surveillance particulièrement étroite et peuvent nécessiter un ajustement posologique. Parmi ces facteurs:
·changement de la zone d'injection
·meilleure sensibilité à l'insuline (par exemple par élimination des facteurs de stress)
·exercice physique inhabituel, plus intense ou prolongé
·maladies intercurrentes (par exemple vomissements, diarrhées)
·prise alimentaire inadaptée
·repas manqués
·consommation d'alcool
·certaines maladies endocriniennes non compensées (par exemple hypothyroïdie et insuffisance de l'hypophyse antérieure ou insuffisance corticosurrénalienne)
·traitement concomitant avec certains autres produits médicamenteux (voir «Interactions»).
·le lixisénatide et/ou l'insuline en association avec une sulfonylurée peut augmenter le risque d'hypoglycémie.
La dose de Suliqua administrée est une dose individuelle basée sur la réponse clinique du patient. Elle est déterminée en fonction du besoin du patient en insuline (voir «Posologie/Mode d'emploi»).
Dans une étude clinique concernant le lixisénatide et menée chez des patients âgés (≥70 ans), on a observé plus de cas d'hypoglycémies symptomatiques chez les patients positifs aux anticorps anti-lixisénatide que chez les patients anticorps-négatifs.
Hyperglycémie
Une élévation de la glycémie (hyperglycémie), une acidocétose et des états hyperosmolaires peuvent survenir par exemple si les doses d'insuline sont trop faibles par rapport aux apports glucidiques, si l'effet de l'insuline a diminué (p.ex. du fait de mauvaises conditions de conservation), si l'exercice physique a été réduit, si la sensibilité à l'insuline a diminué du fait d'un stress émotionnel ou physique (p.ex. à la suite d'un traumatisme, d'une intervention chirurgicale, d'infections fébriles ou d'autres pathologies) ou si des médicaments ayant un effet hyperglycémiant sont administrés conjointement (cf. «Interactions»).
Les signes et symptômes d'un déséquilibre métabolique hyperglycémique sont: soif, polyurie, glycosurie, acétonurie, fatigue, sécheresse cutanée, érythème facial, anorexie, hypotension artérielle et tachycardie. Une acidocétose doit toujours être évoquée, surtout en cas de symptômes tels que vomissements, douleurs abdominales, respiration rapide et profonde, somnolence et coma. Une hyperglycémie sévère ou une acidocétose peut devenir alarmante au point de menacer le pronostic vital. Selon la disponibilité de l'insuline, l'acidocétose peut se développer en quelques heures ou quelques jours. Dès l'identification des signes et symptômes potentiels d'une hyperglycémie ou acidocétose, la glycémie et l'acétonurie doivent être mesurées et si nécessaire, le traitement mis en route sans délai.
La consommation de marijuana est susceptible de réduire la tolérance au glucose. (D'autres substances illégales n'ont pas été testées; autres interactions voir «Interactions»).
Troubles aigus de la vésicule biliaire
Des troubles aigus de la vésicule biliaire ont été observés avec l'utilisation d'agonistes des récepteurs du GLP-1. Des évènements aigus de la vésicule biliaire, tels que la cholelithiase ou la cholécystite, ont été signalés chez des patients traités par lixisenatide bien qu'une relation de cause à effet n'ait pas été établie. Les patients doivent être informés des symptômes caractéristiques des troubles aigus de la vésicule biliaire: douleurs abdominales supérieures, fièvre, nausées, vomissements, et jaunisse. Si une cholelithiase est suspectée, des examens de la vésicule biliaire et un suivi sont prescrits.
Anaphylaxie et réactions sérieuses d'hypersensibilité
Dans les essais cliniques de lixisénatide (l'un des composants de Suliqua), des cas d'anaphylaxie ont été observés (fréquence de 0,1% ou 10 cas pour 10 000 années-patient) et d'autres réactions d'hypersensibilité graves, y compris l'angio-œdème. L'insuline glargine, autre composant de Suliqua, peut présenter des allergies sévères, généralisées, potentiellement mortelles, y compris une anaphylaxie, des réactions cutanées généralisées, un angio-œdème, un bronchospasme, une hypotension et un choc (voir «Effets indésirables»).
Informer et suivre de près les patients ayant des antécédents d'anaphylaxie ou d'angio-œdème avec un autre agoniste du récepteur GLP-1 pour les réactions allergiques, car on ne sait pas si ces patients seront prédisposés à l'anaphylaxie par le lixisénatide. Suliqua est contre-indiqué chez les patients présentant une hypersensibilité connue au lixisénatide ou à l'insuline glargine (voir «Contre-indications»). Si une réaction d'hypersensibilité survient, le patient doit arrêter Suliqua et consulter rapidement un médecin.
Pancréatite aiguë
L'utilisation d'agonistes du récepteur du glucagon-like peptide-1 (GLP-1) a été associée au risque de développer une pancréatite aiguë. Les patients doivent être informés des symptômes caractéristiques de la pancréatite aiguë, à savoir une douleur abdominale sévère et persistante. En cas de pancréatite suspectée, Suliqua doit être arrêté; si la pancréatite aiguë est confirmée, le traitement par Suliqua ne doit pas être réinstauré. L'administration de Suliqua doit faire l'objet d'une attention particulière chez les patients ayant des antécédents de pancréatite.
Maladies gastro-intestinales sévères
La prise d'agonistes du récepteur du GLP-1 peut être associée à des réactions indésirables gastro-intestinales. Suliqua n'ayant pas été étudié chez les patients atteints de maladies gastro-intestinales sévères, notamment gastroparésie sévère, l'administration de Suliqua n'est donc pas recommandée chez ces patients.
Insuffisance rénale
Il n'existe aucune expérience thérapeutique chez les patients avec insuffisance rénale sévère (clairance de la créatinine inférieure à 30 ml/min) ou insuffisance rénale terminale. L'administration de Suliqua chez les patients avec insuffisance rénale sévère ou insuffisance rénale terminale n'est donc pas recommandée (voir «Posologie/Mode d'emploi» et «Pharmacocinétique»).
Traitements médicamenteux concomitants
Le ralentissement de la vidange gastrique provoqué par le lixisénatide peut réduire la vitesse d'absorption de médicaments administrés par voie orale. Suliqua doit être administré avec prudence chez les patients recevant des médicaments administrés per os nécessitant une absorption gastro-intestinale rapide, une surveillance clinique étroite ou présentant une fenêtre thérapeutique étroite. Des recommandations particulières concernant la prise de ce type de médicaments sont indiquées à la rubrique «Interactions».
Maladie intercurrente
Toute maladie intercurrente nécessite un renforcement de la surveillance métabolique. Il est souvent indiqué de rechercher la présence de corps cétoniques dans les urines et souvent nécessaire d'ajuster les doses d'insuline. Les besoins en insuline sont souvent accrus.
Déshydratation
Les patients sous Suliqua doivent être informés du risque potentiel de déshydratation en lien avec les réactions indésirables gastro-intestinales et prendre les précautions nécessaires pour éviter toute déplétion hydrique.
Formation d'anticorps
L'administration de Suliqua peut entraîner la formation d'anticorps dirigés contre l'insuline glargine et/ou le lixisénatide. Dans de rares cas, la présence de ces anticorps peut nécessiter l'ajustement de la dose de Suliqua pour corriger une tendance à l'hyper- ou à l'hypoglycémie.
Par ailleurs, il y a une augmentation de l'incidence de réactions au site d'injection parmi les patients avec anticorps anti-lixisénatide (5,9% chez les patients positifs pour les anticorps par rapport à 2,9% chez les patients négatifs pour les anticorps pendant toute la période de traitement).
Hypokaliémie
Tous les produits contenant de l'insuline, y compris Suliqua, provoquent un déplacement du potassium de l'espace extracellulaire vers l'espace intracellulaire, conduisant éventuellement à une hypokaliémie. L'hypokaliémie non traitée peut provoquer une paralysie respiratoire, une arythmie ventriculaire et la mort. Surveiller les niveaux de potassium chez les patients à risque d'hypokaliémie, si indiqué (par exemple, les patients utilisant des médicaments hypokaliémiants, les patients prenant des médicaments sensibles aux concentrations sériques de potassium).
Résultats macrovasculaires
Il n'y a pas eu d'études cliniques établissant la réduction du risque macrovasculaire avec Suliqua ou tout autre antidiabétique (voir «Propriétés/Effets»).
Erreurs médicamenteuses
Les patients doivent être informés de la nécessité de vérifier systématiquement l'étiquette du stylo avant chaque injection, pour éviter toute erreur entre les 2 différents dosages de Suliqua ou encore toute erreur avec d'autres antidiabétiques injectables.
Pour éviter toute erreur de dosage et risque de surdosage, les patients ne doivent jamais prélever avec une seringue le produit contenu dans la cartouche du stylo prérempli.
Populations non étudiées
·Le passage d'un agoniste du récepteur du GLP-1 à Suliqua n'a pas fait l'objet d'étude.
·Suliqua n'a pas été étudié en association avec les inhibiteurs de la DPP-4, les sulfonylurées, les glinides, la pioglitazone et les inhibiteurs du SGLT-2.
·Le remplacement d'une insuline basale à une dose <10 unités ou >60 unités par Suliqua n'a pas été étudiée.
Excipients
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c.-à-d. qu'il est essentiellement «sans sodium».
Ce médicament contient du métacrésol (conservateur) qui peut être source de réactions allergiques.
InteractionsAucune étude sur les interactions avec Suliqua n'a été menée.
Un certain nombre de substances affectent le métabolisme du glucose et peuvent nécessiter un ajustement posologique de Suliqua.
Interactions pharmacodynamiques
Les substances susceptibles d'augmenter l'effet hypoglycémiant et la sensibilité à l'hypoglycémie sont, entre autres, les médicaments anti-hyperglycémiques, les inhibiteurs de l'enzyme de conversion (IEC), le disopyramide, les fibrates, la fluoxétine, les inhibiteurs de la monoamine oxydase (IMAO), la pentoxifylline, le propoxyphène, les salicylates et les antibiotiques de type sulfamides.
Les substances susceptibles de réduire l'effet hypoglycémiant sont, entre autres, les corticoïdes, le danazol, le diazoxide, les diurétiques, le glucagon, l'isoniazide, les œstrogènes et progestatifs, les dérivés de la phénothiazine, la somatotropine, les médicaments sympathomimétiques [par exemple épinéphrine (adrénaline), salbutamol, terbutaline], les hormones thyroïdiennes, les antipsychotiques atypiques (par exemple clozapine et olanzapine) et les inhibiteurs de protéases.
Les bêtabloquants, la clonidine, les sels de lithium et l'alcool peuvent augmenter ou réduire l'effet hypoglycémiant de l'insuline. La pentamidine peut provoquer une hypoglycémie, parfois suivie d'une hyperglycémie.
D'autre part, sous l'influence de médicaments sympatholytiques tels que les bêtabloquants, la clonidine, la guanéthidine et la réserpine, les signes d'une contre-régulation adrénergique peuvent être réduits ou absents.
Interactions pharmacocinétiques
Le lixisénatide est un peptide et n'est pas métabolisé par le cytochrome P450. Dans les études in vitro, le lixisénatide n'a pas eu d'effet sur l'activité des isoenzymes du cytochrome P450 ou des transporteurs humains testés.
Effet de la vidange gastrique sur les médicaments administrés par voie orale
Le lixisénatide ralentit la vidange gastrique ce qui peut réduire la vitesse d'absorption des médicaments administrés par voie orale. L'administration concomitante de médicaments administrés per os présentant une fenêtre thérapeutique étroite ou nécessitant une surveillance clinique importante doit être envisagée avec prudence. Si ces médicaments doivent être pris en même temps qu'une prise alimentaire, les patients doivent être informés de la nécessité de les prendre avec un repas ou un en-cas au cours duquel le lixisénatide n'est pas administré.
Les médicaments administrés par voie orale dont l'efficacité dépend particulièrement des seuils de concentration, tels que les antibiotiques, doivent être pris au moins 1 heure avant ou 11 heures après l'injection de Suliqua.
Les patients sous statines, comme l'atorvastatine, doivent être informés de la nécessité de les prendre de préférence au moins 1 heure avant ou 11 heures après l'injection de Suliqua.
Paracétamol
Le paracétamol a été utilisé comme modèle médicamenteux afin de déterminer l'effet du lixisénatide sur la vidange gastrique. Après administration d'une dose unique de 1 000 mg de paracétamol, l'AUC (aire sous la courbe) et la t1/2 du paracétamol sont restées identiques quel que soit le moment de l'administration (avant ou après l'injection de lixisénatide). Lorsque le paracétamol a été administré 1 heure ou 4 heures après 10 μg de lixisénatide, la Cmax du paracétamol a été baissée respectivement de 29% et 31%, et le tmax médian a été prolongé respectivement de 2,0 et 1,75 heures. Un délai supplémentaire du tmax et une réduction de la Cmax du paracétamol sont normalement attendues avec une dose d'entretien de 20 μg.
Aucun effet n'a été observé sur la Cmax et le tmax du paracétamol lorsque celui-ci est administré 1 heure avant le lixisénatide.
D'après ces résultats, aucun ajustement de la dose de paracétamol n'est nécessaire, mais le retard du tmax observé lorsque le paracétamol est administré 1h à 4 heures après le lixisénatide doit être pris en compte lorsqu'un effet rapide du paracétamol est recherché.
Contraceptifs oraux
L'administration d'une dose unique d'un contraceptif oral (0,03 mg d'éthinylestradiol/0,15 mg de lévonorgestrel) 1 heure avant ou 11 heures après l'injection de 10 μg de lixisénatide n'a pas modifié la Cmax, l'AUC, la t1/2 ni le tmax de l'éthinylestradiol et du lévonorgestrel.
L'administration du contraceptif oral 1 heure ou 4 heures après l'injection de lixisénatide n'a pas modifié l'AUC ni la t1/2 de l'éthinylestradiol ni du lévonorgestrel, mais a réduit la Cmax de l'éthinylestradiol de respectivement 52% et 39%, et la Cmax du lévonorgestrel respectivement de 46% et 20% et a retardé le tmax médian de 1 à 3 heures.
La réduction de la Cmax a une pertinence clinique limitée et aucun ajustement posologique des contraceptifs oraux n'est nécessaire.
Les patientes sous contraceptifs oraux doivent être informées de la nécessité de les prendre au moins 1 heure avant ou 11 heures après l'injection de Suliqua.
Atorvastatine
L'administration concomitante de 20 μg de lixisénatide et 40 mg d'atorvastatine le matin pendant 6 jours n'a pas affecté l'exposition à l'atorvastatine mais la Cmax a été réduite de 31% et le tmax prolongé de 3,25 heures.
Cette hausse du tmax n'a pas été observée lorsque l'atorvastatine était administrée le soir et le lixisénatide le matin, mais l'AUC et la Cmax de l'atorvastatine ont augmenté de 27% et 66%, respectivement.
Ces variations ne sont pas pertinentes du point de vue clinique et ne nécessitent donc pas d'ajustement posologique de l'atorvastatine en cas d'administration concomitante avec le lixisénatide.
Warfarine et autres dérivés de la coumarine
Après administration concomitante de 25 mg de warfarine et administration répétée de 20 μg de lixisénatide, aucun effet n'a été observé sur l'AUC ni sur l'INR («International Normalized Ratio») alors que la Cmax a été réduite de 19% et le tmax retardé de 7 heures.
D'après ces résultats, aucun ajustement posologique de la warfarine n'est nécessaire en cas d'administration concomitante avec le lixisénatide; cependant, une surveillance fréquente de l'INR chez les patients sous warfarine et/ou dérivés de la coumarine est recommandée au moment de l'instauration ou à l'arrêt du traitement par lixisénatide.
Digoxine
Après administration concomitante de 20 μg de lixisénatide et de 0,25 mg de digoxine à l'état d'équilibre, l'AUC de la digoxine n'a pas été modifiée. Le tmax de la digoxine a été retardé de 1,5 heure et la Cmax a été réduite de 26%.
D'après ces résultats, aucun ajustement posologique de la digoxine n'est nécessaire en cas d'administration concomitante avec le lixisénatide.
Ramipril
Après administration concomitante de 20 μg de lixisénatide et 5 mg de ramipril pendant 6 jours, l'AUC du ramipril a augmenté de 21% tandis que la Cmax a baissé de 63%. L'AUC et la Cmax du métabolite actif (ramiprilate) n'ont pas été modifiées. Le tmax du ramipril et du ramiprilate ont été retardés d'environ 2,5 heures.
D'après ces résultats, aucun ajustement posologique du ramipril n'est nécessaire en cas d'administration concomitante avec le lixisénatide.
Grossesse, allaitementFemmes en âge de procréer
Suliqua n'est pas recommandé chez les femmes en âge de procréer n'utilisant pas de contraception.
Grossesse
Il n'existe pas de données cliniques concernant l'utilisation de Suliqua, de l'insuline glargine ou du lixisénatide chez la femme enceinte.
Suliqua ne doit pas être utilisé pendant la grossesse, période durant laquelle il est recommandé d'utiliser de l'insuline. Si la patiente envisage une grossesse ou si une grossesse survient pendant le traitement sous Suliqua, celui-ci doit être arrêté.
Les nombreuses données sur les femmes enceintes (plus de 1 000 grossesses) avec l'insuline glargine ne montrent pas d'effets indésirables particuliers de l'insuline glargine sur la grossesse et aucune malformation particulière ou toxicité fœtale/néonatale de l'insuline glargine. Les données sur l'insuline glargine chez l'animal n'indiquent pas de toxicité pour la reproduction.
Les études sur le lixisénatide conduites chez l'animal ont montré une toxicité pour la reproduction (voir «Données précliniques»). Le risque éventuel chez l'homme n'est pas connu.
Allaitement
En l'absence de données concernant le passage de l'insuline glargine ou du lixisénatide dans le lait maternel, Suliqua ne doit pas être utilisé pendant l'allaitement.
L'ingestion d'insuline glargine par le nouveau-né/nourrisson lors de l'allaitement ne doit normalement produire aucun effet métabolique car l'insuline glargine, en tant que peptide, est digérée et transformée en acides aminés dans le tractus gastro-intestinal.
Fertilité
Les études sur le lixisénatide ou l'insuline glargine chez l'animal n'ont pas montré d'effets délétères directs sur la fertilité.
Effet sur l’aptitude à la conduite et l’utilisation de machinesLa capacité du patient à se concentrer et à réagir peut baisser sous l'effet d'une hypoglycémie ou d'une hyperglycémie ou, par exemple, à la suite de troubles visuels. Ceci peut représenter un risque dans des situations où ces aptitudes ont une importance toute particulière (par exemple conduire une voiture ou utiliser des machines).
Les patients doivent être informés de la nécessité de prendre des précautions pour éviter les hypoglycémies lors de la conduite de véhicules ou de l'utilisation de machines. Ceci est particulièrement important chez les patients dont les signes avant-coureurs de l'hypoglycémie sont peu ou pas du tout ressentis ou ceux chez qui les épisodes d'hypoglycémie sont fréquents. Il convient d'examiner s'il est recommandé de conduire ou d'utiliser des machines dans ces circonstances.
Effets indésirablesRésumé du profil de sécurité
Les essais de phase III ont inclus 834 patients recevant Suliqua.
Les hypoglycémies et les effets indésirables gastro-intestinaux ont été les événements les plus souvent signalés pendant le traitement sous Suliqua (voir la rubrique « Description de certains effets indésirables» ci-après).
Liste des effets indésirables
Les effets indésirables sont rangés par classe de système d'organes de la classification MedDRA et par fréquence selon la convention suivante: « très fréquents » (≥1/10), «fréquents» (≥1/100 à <1/10), «occasionnels» (≥1/1000 à <1/100), «rares» (≥1/10 000 à <1/1000), « très rares » (<1/10 000), « Fréquence inconnue » (ne peut être estimée sur la base des données disponibles)
|
SOC
|
Fréquence de l'occurrence
| |
|
Très fréquents
|
Fréquents
|
Occasionnels
|
Inconnue
| |
Infections et infestations
|
|
|
Rhinopharyngite
Infection des voies
respiratoires supérieures
|
| |
Affections du système immunitaire
|
|
|
Urticaire
|
| |
Troubles du métabolisme et de la nutrition
|
Hypoglycémie
|
|
|
| |
Affections du système nerveux
|
|
Etourdissements
|
Céphalées
|
| |
Affections gastro-intestinales
|
|
Nausées
Diarrhées
Vomissements
|
Dyspepsie
Douleurs abdominales
|
| |
Affections hépatobiliaires
|
|
|
Cholélithiase et cholécystite
|
| |
Troubles généraux et anomalies au site d'administration
|
|
|
Fatigue
Réactions au site d'injection
Lipodystrophie
|
Amyloïdose cutanée
|
Description de certains effets indésirables
Hypoglycémie
Les crises d'hypoglycémie sévère, surtout si elles sont récurrentes, peuvent conduire à une atteinte neurologique. Les épisodes d'hypoglycémie prolongée ou sévère peuvent mettre en danger la vie du patient.
Chez de nombreux patients, les signes et les symptômes d'une neuroglycopénie sont précédés de signes d'une contre-régulation adrénergique. En général, plus la baisse de la glycémie est forte et rapide, plus le phénomène de contre-régulation et ses symptômes sont marqués (voir «Mises en garde et précautions»).
Dans les études cliniques de phase III, chez les patients sous Suliqua, l'incidence des hypoglycémies symptomatiques (avec taux de glucose plasmatique ≤3,9 mmol/l) a été de 25,6% pour ceux n'ayant jamais reçu d'insuline (469 patients) et de 40,0% pour ceux précédemment traités par insuline basale (365 patients).
Concernant les hypoglycémies sévères (nécessitant l'intervention d'un tiers pour l'administration active d'hydrates de carbone, de glucagon ou pour toute autre mesure de réanimation), l'incidence a été nulle pour les patients n'ayant jamais reçu d'insuline et de 0,02% pour les patients précédemment sous insuline basale.
Affections gastro-intestinales
Les effets indésirables gastro-intestinaux (nausées, vomissements et diarrhées) ont été ceux les plus fréquemment signalés pendant la période de traitement. Chez les patients sous Suliqua, l'incidence des nausées, diarrhées et vomissements associés était respectivement de 8,4%, 2,2% et 2,2%. Les effets indésirables gastrointestinaux étaient le plus souvent légers et transitoires. Chez les patients sous lixisénatide, l'incidence des nausées, diarrhées et vomissements associés était respectivement de 22,3%, 3% et 3,9%.
Affections du système immunitaire
Des réactions allergiques (urticaire) éventuellement associées à Suliqua ont été signalées chez 0,3% des patients. Des cas de réaction allergique généralisée, y compris réaction anaphylactique et œdème de Quincke, ont été signalés après commercialisation de l'insuline glargine et du lixisénatide.
Les réactions d'hypersensibilité immédiates à l'insuline sont rares. Des réactions allergiques à des préparations à base d'insuline (y compris l'insuline glargine) ou à leurs excipients peuvent s'accompagner par exemple d'une éruption cutanée généralisée, d'un œdème de Quincke, de bronchospasmes, d'une hypotension ou d'un état de choc et prendre des formes potentiellement mortelles.
L'administration d'insuline peut entraîner la formation d'anticorps anti-insuline. Des réactions antigène-anticorps à l'insuline humaine et à l'insuline glargine se sont produites à une même fréquence dans des essais cliniques sur des groupes de patients traités par insuline humaine NPH et par insuline glargine. Dans des cas rares, la présence d'anticorps anti-insuline peut exiger l'adaptation de la dose d'insuline pour contrer la tendance à l'hyperglycémie ou à l'hypoglycémie.
Il y a une augmentation de l'incidence de réactions au site d'injection parmi les patients avec anticorps anti-lixisénatide (5,9% chez les patients positifs pour les anticorps par rapport à 2,9% chez les patients négatifs pour les anticorps pendant toute la période de traitement).
Chez les patients insulino-naïfs, une incidence plus élevée d'anticorps anti-insuline glargine a été observée avec Suliqua comparé à Lantus. Cependant, ce phénomène pourrait être due à la variabilité génétique dans la population étudiée et n'a pas été observé chez les patients précédemment traités avec de l'insuline.
Lipodystrophie et Amyloïdose cutanée
L'administration sous-cutanée de produits injectables contenant de l'insuline peut entraîner une lipoatrophie (dépression du tissu cutané), une lipohypertrophie (développement ou épaississement du tissu) ou une amyloïdose cutanée au site d'injection. Une rotation des sites d'injection dans une même zone (abdomen, cuisse ou deltoïde) est recommandée d'une injection à l'autre pour contribuer à réduire ou éviter ces réactions (voir les sections « Posologie/Mode d'emploi» et «Effets indésirables»).
Réactions au site d'injection
Certains patients recevant un traitement contenant de l'insuline, y compris Suliqua, ont eu un érythème, un œdème local et un prurit au site d'injection. Ces affections se sont généralement résolues spontanément.
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageLes données cliniques concernant un surdosage de Suliqua sont limitées.
Une hypoglycémie et des effets indésirables gastrointestinaux peuvent se produire si le patient a pris une dose de Suliqua supérieure à la dose nécessaire.
Les hydrates de carbone suffisent généralement à corriger les épisodes légers d'hypoglycémie. Un ajustement de la dose de Suliqua, de la prise des repas, ou de l'exercice physique peut être nécessaire.
Des épisodes d'hypoglycémie plus sévères avec coma, crise épileptique ou atteinte neurologique peuvent être traités avec du glucagon administré par voie intramusculaire/sous-cutanée ou du glucose concentré administré par voie intraveineuse. Il peut être nécessaire de poursuivre la prise des hydrates de carbone et l'observation du patient car l'hypoglycémie peut récidiver après le rétablissement clinique apparent.
En cas d'effets indésirables gastrointestinaux, un traitement approprié doit être instauré en fonction des symptômes et des signes cliniques du patient et la dose de Suliqua doit être réduite à la dose prescrite.
Propriétés/EffetsCode ATC
A10AE
Mécanisme d'action
Suliqua
Suliqua associe 2 agents anti-hyperglycémiques aux mécanismes d'action complémentaires: l'insuline glargine, analogue de l'insuline basale et le lixisénatide, agoniste du récepteur du GLP-1, qui ciblent respectivement le glucose plasmatique à jeun (FPG) et le glucose plasmatique postprandial (PPG) pour améliorer le contrôle de la glycémie chez les patients atteints du diabète de type 2, tout en réduisant au minimum la prise de poids et le risque d'hypoglycémie.
Insuline glargine
L'activité principale de l'insuline, y compris l'insuline glargine, consiste à réguler le métabolisme du glucose. L'insuline et ses analogues réduisent le glucose sanguin en stimulant l'absorption du glucose périphérique, en particulier par les muscles squelettiques et les graisses et en inhibant la production de glucose hépatique. L'insuline inhibe la lipolyse, la protéolyse et stimule la synthèse des protéines.
Lixisénatide
Le lixisénatide est un agoniste sélectif du récepteur du GLP-1. Le récepteur du GLP-1 est la cible du GLP-1 natif, hormone incrétine endogène qui renforce de façon glucose-dépendante la sécrétion d'insuline par les cellules bêta du pancréas.
L'action du lixisénatide résulte d'une interaction spécifique avec les récepteurs du GLP-1, entraînant une augmentation de la formation d'adénosine monophosphate cyclique (cAMP) intracellulaire. Le lixisénatide stimule la sécrétion d'insuline lorsque la glycémie augmente mais pas lorsqu'elle est normale, ce qui limite le risque d'hypoglycémie. En parallèle, la sécrétion du glucagon est inhibée. En cas d'hypoglycémie, le mécanisme de secours que constitue la sécrétion de glucagon est donc préservé.
Le lixisénatide ralentit la vidange gastrique, réduisant ainsi la vitesse à laquelle le glucose provenant des aliments apparaît dans la circulation sanguine. Cet effet sur la vidange gastrique pourrait aussi contribuer à la perte de poids.
Pharmacodynamique
Suliqua
L'association de l'insuline glargine et du lixisénatide n'a pas d'incidence sur la pharmacodynamie de l'insuline glargine. L'effet de l'association de l'insuline glargine et du lixisénatide sur la pharmacodynamie du lixisénatide n'a pas été étudié dans les études de phase I.
Conformément au profil de concentration de l'insuline glargine en fonction du temps, relativement constant sur 24 heures, sans pic prononcé lorsqu'elle est administrée seule, le profil du taux d'utilisation du glucose en fonction du temps était similaire, sans pic prononcé, après administration de l'association insuline glargine/lixisénatide.
Le temps d'absorption des insulines, y compris Suliqua, peut varier d'un individu à l'autre et également chez le même individu.
Insuline glargine
Les études cliniques sur l'insuline glargine (100 unités/ml) montrent que l'effet hypoglycémiant sur une base molaire (en d'autres termes lorsque le produit est administré aux mêmes doses) de l'insuline glargine intraveineuse est à peu près le même que celui de l'insuline humaine.
Lixisénatide
Une étude comparative versus placebo conduite sur 28 jours chez des diabétiques de type 2 a évalué les effets de 5 à 20 µg de lixisénatide administrés une fois par jour ou deux fois par jour, sur la glycémie induite par un repas d'épreuve standardisé pris au petit déjeuner. Les doses de 10 et 20 µg de lixisénatide, administrés une fois par jour ou deux fois par jour, ont amélioré le contrôle glycémique en réduisant les concentrations en glucose postprandiales et à jeun. Le lixisénatide administré dans cette étude le matin à la dose de 20 µg une fois par jour a maintenu des réductions statistiquement significatives de la glycémie postprandiale après le petit déjeuner, le déjeuner et le dîner.
Glucose postprandial
Une étude conduite sur 4 semaines chez des diabétiques de type 2 évaluant le lixisénatide en association avec la metformine et sur 8 semaines en association avec l'insuline glargine avec ou sans metformine, la dose de 20 µg de lixisénatide administrée une fois par jour avant le petit déjeuner, a démontré une réduction du glucose plasmatique postprandial (AUC 0:30-4:30h) après un repas test. Le nombre de patients chez qui le taux de glucose postprandial était inférieur à 7,77 mmol/l était de 69,3% après 28 jours et de 76,1% après 56 jours.
Sécrétion d'insuline
Une étude sur le lixisénatide administré en monothérapie a montré que le produit restaure à lui seul la première phase de sécrétion d'insuline chez les diabétiques de type 2 de manière glucose-dépendante par 2,8 fois (IC à 90%; 2,5-3,1) et augmente la sécrétion d'insuline de deuxième phase de 1,6 fois (IC à 90%; 1,4-1,7) par rapport au placebo d'après la mesure de l'AUC.
Vidange gastrique
Après un repas test standardisé, le lixisénatide ralentit la vidange gastrique et réduit ainsi la vitesse d'absorption du glucose postprandial. Après 28 jours de traitement sous lixisénatide administré en monothérapie, l'effet de ralentissement de la vidange gastrique est maintenu chez les diabétiques de type 2.
Sécrétion du glucagon
Le lixisénatide administré seul à raison de 20 µg une fois par jour a démontré une réduction des taux du glucagon postprandial par rapport aux taux de base après un repas test chez les diabétiques de type 2. Une étude de clamp hypoglycémique comparative versus placebo conduite chez des sujets sains évaluant l'effet d'une injection unique de 20 µg de lixisénatide sur la réponse du glucagon, a montré que la réponse du glucagon contre-régulatrice est préservée dans des conditions hypoglycémiques en présence de concentrations plasmatiques efficaces en lixisénatide.
Électrophysiologie cardiaque (QTc)
L'effet du lixisénatide sur la repolarisation cardiaque a été évalué dans une étude QTc (à 1,5 fois la dose d'entretien autorisée) qui n'a indiqué aucune conséquence pertinente du lixisénatide sur la repolarisation ventriculaire.
Fréquence cardiaque
Les études comparatives versus placebo de phase III sur Suliqua n'ont montré aucune augmentation de la fréquence cardiaque moyenne.
Efficacité clinique
La sécurité de Suliqua et son efficacité sur le contrôle de la glycémie ont été évaluées dans deux études cliniques randomisées conduites chez des diabétiques de type 2:
·Traitement d'appoint des antidiabétiques oraux (ADO) [patients n'ayant jamais reçu d'insuline]
·Patients précédemment sous insuline basale
Dans chacun des essais comparatifs avec substance active, le traitement sous Suliqua a produit des améliorations cliniquement et statistiquement significatives de l'hémoglobine A1c (HbA1c).
Par rapport à l'insuline glargine administrée seule, le traitement combiné a permis d'obtenir des taux d'HbA1c inférieurs et une réduction d'HbA1c plus importante sans augmenter les taux d'hypoglycémies (voir «Effets indésirables»).
Dans l'étude clinique du traitement d'appoint de la metformine, la dose initiale était de 10 doses unitaires. Dans l'étude clinique du traitement remplaçant l'insuline basale, la dose initiale était de 20 ou 30 doses unitaires, selon la dose antérieure d'insuline. Dans les deux études, la dose était ajustée une fois par semaine, selon les valeurs du glucose plasmatique à jeun mesurées par le patient.
·Traitement d'appoint des antidiabétiques oraux (ADO) [patients n'ayant jamais reçu d'insuline]
Étude clinique du diabète de type 2 insuffisamment équilibré sous ADO
Un total de 1 170 diabétiques de type 2 a été réparti de manière aléatoire dans une étude contrôlée versus traitement actif, conduite en ouvert sur 30 semaines en vue d'évaluer l'efficacité et la sécurité de Suliqua par rapport aux composants individuels, à savoir l'insuline glargine (100 unités/ml) et le lixisénatide.
Les diabétiques de type 2, recevant la metformine seule ou la metformine et un second ADO, c'est-à-dire une sulfonylurée ou un glinide ou un inhibiteur de SGLT-2 (sodium/glucose cotransporteur 2) ou un inhibiteur de la dipeptidyl peptidase-4 (DPP-4) et chez qui ce traitement ne permettait pas de contrôler correctement la glycémie (HbA1c de 7,5% à 10% chez les patients antérieurement sous metformine seule et 7,0% à 9% chez les patients antérieurement sous metformine et second antidiabétique oral) ont commencé une période de pré-inclusion de 4 semaines. Pendant cette phase de pré-inclusion, la metformine a été optimisée et les autres ADO ont été arrêtés. À la fin de la phase de pré-inclusion, les patients chez qui le contrôle glycémique restait insuffisant (HbA1c entre 7% et 10%) ont été répartis de manière aléatoire soit dans le groupe sous Suliqua, sous insuline glargine ou sous lixisénatide. Au total, 58% des patients recevaient un deuxième ADO au moment de la sélection.
Les diabétiques de type 2 présentaient les caractéristiques suivantes: l'âge moyen était de 58,4 ans, 50,6% des individus étaient des hommes, l'IMC moyen au départ était de 31,7 kg/m2 et le diabète remontait à environ 9 ans en moyenne.
Au bout de la 30ème semaine, Suliqua a produit une amélioration statistiquement significative du taux d'HbA1c (valeur p <0,0001) par rapport aux composants individuels. Dans une analyse préétablie de ce critère d'évaluation primaire, les différences observées ont été cohérentes au regard du taux d'HbA1c initial (<8% ou ≥8%) ou de l'utilisation d'ADO au départ (metformine seule ou metformine plus deuxième ADO).
Voir le tableau et la figure ci-dessous pour les autres critères d'évaluation de l'étude.
Résultats au bout de 30 semaines: étude clinique du traitement d'appoint de la metformine (population en mITT)
|
|
Suliqua
|
Insuline glargine
|
Lixisénatide
| |
Nombre de sujets (mITT)
|
468
|
466
|
233
| |
HbA1c (%)
| |
Valeur initiale (moyenne; après pré-inclusion)
|
8,1
|
8,1
|
8,1
| |
Fin d'étude (moyenne)
|
6,5
|
6,8
|
7,3
| |
Variation par les moindres carrés par rapport à la valeur initiale (moyenne)
|
- 1,6
|
-1,3
|
-0,9
| |
Différence par rapport à l'insuline glargine
|
-0,3
|
| |
[intervalle de confiance à 95%]
|
[-0,4; -0,2]
|
| |
(valeur de p)
|
(<0,0001)
|
| |
Différence par rapport au lixisénatide
|
|
|
-0,8
| |
[intervalle de confiance à 95%]
|
|
|
[-0,9; -0,7]
| |
(valeur de p)
|
|
|
(<0,0001)
| |
Nombre de patients (%) parvenant à un taux d'HbA1c <7% à la semaine 30
|
345 (74%)
|
277 (59%)
|
77 (33%)
| |
Glucose plasmatique à jeun (mmol/l)
| |
Valeur initiale (moyenne)
|
9,88
|
9,75
|
9,79
| |
Fin d'étude (moyenne)
|
6,32
|
6,53
|
8,27
| |
Variation par les moindres carrés par rapport à la valeur initiale (moyenne)
|
-3,46
|
-3,27
|
-1,50
| |
Variation par les moindres carrés par rapport à l'insuline glargine (moyenne)
|
-0,19
|
|
| |
[IC à 95%]
|
[-0,420 à 0,038]
|
|
| |
(valeur de p)
|
(0,1017)
|
|
| |
Variation par les moindres carrés par rapport au lixisénatide (moyenne)
|
-1,96
|
|
| |
[IC à 95%]
|
[-2,246 à -1,682]
|
|
| |
(valeur de p)
|
(<0,0001)
|
|
|
|
|
Suliqua
|
Insuline glargine
|
Lixisénatide
| |
Nombre de sujets (mITT)
|
468
|
466
|
233
| |
GPP 2 heures (mmol/l)
| |
[excursion glycémique 2 heures* (mmol/L)]
| |
Variation par les moindres carrés de la valeur initiale à la semaine 30
|
-5,68
|
-3,31
|
-4,58
| |
(moyenne)
|
[-2,31]
|
[-0,18]
|
[-3,23]
| |
Poids corporel moyen (kg)
| |
Valeur initiale (moyenne)
|
89,4
|
89,8
|
90,8
| |
Variation par les moindres carrés par rapport à la valeur initiale (moyenne)
|
-0,3
|
1,1
|
-2,3
| |
Comparaison versus insuline glargine
|
|
-1,4
|
| |
[intervalle de confiance à 95%]
|
|
[-1,9 à -0,9]
|
| |
(valeur de p)
|
|
(<0,0001)
|
| |
Comparaison versus lixisénatide [intervalle de confiance à 95%]
|
|
|
2,01
[1,4 à 2,6]
| |
Nombre de patients (%) parvenant à un taux d'HbA1c <7,0% sans prise de poids au bout de la semaine 30
|
202
(43,2%)
|
117
(25,1%)
|
65
(27,9%)
| |
Pourcentage de différence par rapport à l'insuline glargine
|
|
18,1
|
| |
[intervalle de confiance à 95%]
|
|
[12,2 à 24,0]
|
| |
(valeur de p)
|
|
(<0,0001)
|
| |
Pourcentage de différence par rapport au lixisénatide [intervalle de confiance à 95%]
|
|
|
15,2
[8,1 à 22,4]
| |
Prise quotidienne d'insuline glargine
| |
Variation par les moindres carrés de la dose d'insuline au bout de la semaine 30 (moyenne)
|
39,8
|
40,5
|
N/A
|
* PPG 2 heures moins la valeur du glucose avant le repas
Taux d'HbA1c (%) moyen au début de la sélection, au moment de la randomisation et à chaque point dans le temps (sujets allant au terme de l'étude) et à la semaine 30 (LOCF*) - population en mITT
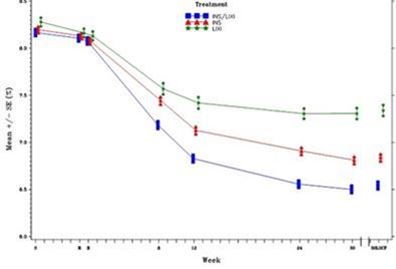
* LOCF = Last observation carried forward ou dernières observations disponibles
Les patients sous Suliqua ont montré une réduction statistiquement significative
du profil moyen du glucose plasmatique auto-mesurée (SMPG) à 7 points entre le début et la semaine 30 (-3,35 mmol/l) par rapport aux patients sous insuline glargine
(-2,66 mmol/l; différence -0,69 mmol/l) et par rapport aux patients sous lixisénatide
(-1,95 mmol/l; différence -1,40 mmol/l) (p <0,0001 pour les deux comparaisons).
À tous les points dans le temps, les valeurs moyennes du glucose plasmatique sur 30 semaines étaient plus faibles dans le groupe sous Suliqua que dans le groupe sous insuline glargine ou sous lixisénatide, sauf en ce qui concerne la valeur avant le petit déjeuner qui était semblable entre le groupe sous Suliqua et le groupe sous insuline glargine.
·Patients précédemment sous insuline basale
Études cliniques du diabète de type 2 insuffisamment équilibré sous insuline basale
Un total de 736 diabétiques de type 2 a participé à une étude multicentrique randomisée en groupes parallèles, à deux bras, contrôlée versus traitement actif, conduite en ouvert sur 30 semaines en vue d'évaluer l'efficacité et la sécurité de Suliqua par rapport à l'insuline glargine (100 unités/ml).
Les patients sélectionnés avaient un diabète de type 2 et recevaient de l'insuline basale depuis au moins 6 mois à une dose quotidienne stable comprise entre 15 et 40 U, seule ou associée à un ou deux ADO (metformine ou une sulfonylurée ou un glinide ou un inhibiteur de SGLT-2 ou un inhibiteur de DPP-4). Ils présentaient un taux d'HbA1c compris entre 7,5% et 10% et une glycémie à jeun inférieure ou égale à 10,0 mmol/l ou 11,1 mmol/l, selon le traitement antidiabétique antérieur.
Après la sélection, les patients éligibles (n = 1 018) ont entamé une phase de pré-inclusion de 6 semaines pendant laquelle ils sont restés ou sont passés à l'insuline glargine, lorsqu'ils prenaient une autre insuline basale, et leur dose d'insuline était ajustée/stabilisée tout en poursuivant la metformine (le cas échéant). Tout autre ADO était arrêté.
À la fin de la période de pré-inclusion, les patients avec un taux d'HbA1c compris entre 7 et 10%, une glycémie à jeun ≤7,77 mmol/l et une dose quotidienne d'insuline glargine de 20 à 50 unités, ont été randomisés dans le groupe sous Suliqua (n = 367) ou sous insuline glargine (n = 369).
Les diabétiques de type 2 présentaient les caractéristiques suivantes: l'âge moyen était de 60 ans, 46,7% des individus étaient des hommes, l'IMC moyen au moment de la sélection était d'environ 31 kg/m2 et le diabète remontait à environ 12 ans en moyenne.
Au bout de la 30ème semaine, Suliqua a produit une amélioration statistiquement significative du taux d'HbA1c (valeur p <0,0001) par rapport à l'insuline glargine.
Voir le tableau et la figure ci-dessous pour les autres critères d'évaluation de l'étude.
Résultats à 30 semaines: étude clinique du diabète de type 2 insuffisamment équilibré sous insuline basale (population en mITT)
|
|
Suliqua
|
Insuline glargine
| |
Nombre de sujets (mITT)
|
366
|
365
| |
HbA1c (%)
| |
Lors de la sélection (moyenne)
|
8,5
|
8,5
| |
Valeur initiale (moyenne; après pré-inclusion)
|
8,1
|
8,1
| |
Fin du traitement (moyenne)
|
6,9
|
7,5
| |
Variation par les moindres carrés par rapport à la valeur initiale (moyenne)
|
-1,1
|
-0,6
| |
Différence par rapport à l'insuline glargine
|
-0,5
| |
[intervalle de confiance à 95%]
|
[-0,6; -0,4]
| |
(valeur de p)
|
(<0,0001)
| |
Patients [n (%)] parvenant à un taux d'HbA1c <7% au bout de la semaine 30
|
201 (54,9%)
|
108 (29,6%)
| |
Glucose plasmatique à jeun (mmol/l)
| |
Valeur initiale (moyenne)
|
7,33
|
7,32
| |
Fin d'étude (moyenne)
|
6,78
|
6,69
| |
Variation par les moindres carrés par rapport à la valeur initiale (moyenne)
|
-0,35
|
-0,46
| |
GPP 2 heures (mmol/l) [excursion glycémique 2 heures* (mmol/L)]
| |
Variation par les moindres carrés de la valeur initiale à la semaine 30 (moyenne)
|
-4,72
[-3,90]
|
-1,39
[-0,47]
| |
Poids corporel moyen (kg)
| |
Valeur initiale (moyenne)
|
87,8
|
87,1
| |
Variation par les moindres carrés par rapport à la valeur initiale (moyenne)
|
-0,7
|
0,7
| |
Comparaison versus insuline glargine
|
-1,4
| |
[intervalle de confiance à 95%]
|
[-1,8 à -0,9]
| |
(valeur de p)
|
(<0,0001)
|
|
|
Suliqua
|
Insuline glargine
| |
Nombre de sujets (mITT)
|
366
|
365
| |
Nombre de patients (%) parvenant à un taux d'HbA1c <7,0% sans prise de poids à la semaine 30
|
125
(34,2%)
|
49
(13,4%)
| |
Pourcentage de différence par rapport à l'insuline glargine
|
20,8
| |
[intervalle de confiance à 95%]
|
[15,0 à 26,7]
| |
(valeur de p)
|
(<0,0001)
| |
Prise quotidienne d'insuline glargine
| |
Valeur initiale (moyenne)
|
35,0
|
35,2
| |
Critère d'évaluation (moyenne)
|
46,7
|
46,7
| |
Variation par les moindres carrés de la dose d'insuline à la semaine 30 (moyenne)
|
10,6
|
10,9
|
* PPG 2 heures moins la valeur du glucose avant le repas
Taux d'HbA1c (%) moyen au début de la sélection, à la randomisation et à chaque point dans le temps (sujets allant au terme de l'étude) et à la semaine 30 (LOCF*) - population en mITT
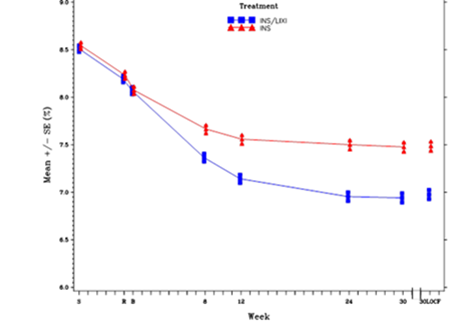
* LOCF = Last observation carried forward, ou dernières observations disponibles
Études sur l'évolution cardiovasculaire
La sécurité cardiovasculaire de l'insuline glargine et du lixisénatide a été établie respectivement dans les essais cliniques ORIGIN et ELIXA. Aucun essai sur l'évolution cardiovasculaire n'a été conduit avec Suliqua.
Insuline glargine
L'essai ORIGIN (Outcome Reduction with Initial Glargine Intervention) est une étude ouverte, randomisée, conduite chez 12 537 patients à haut risque cardiovasculaire (CV) et présentant une anomalie de la glycémie à jeun (AGJ), une intolérance au glucose ou un diabète de type 2 à un stade précoce, qui a comparé LANTUS au traitement standard au moment de la première occurrence d'un événement cardiovasculaire indésirable majeur (MACE). Le MACE se définissait comme un critère combiné associant décès d'origine cardiovasculaire, infarctus du myocarde non fatal et accident vasculaire cérébral non fatal. La durée médiane du suivi de l'étude était de 6,2 ans. L'incidence de MACE avec LANTUS et le traitement standard était similaire dans l'essai ORIGIN [hazard ratio (IC à 95%) pour MACE; 1,02 (0,94, 1,11)].
Lixisénatide
L'étude ELIXA multinationale, randomisée, en double aveugle, contrôlée versus placebo, a évalué les résultats cardiovasculaires (CV) pendant le traitement par lixisénatide chez des patients (n = 6068) diabétiques de type 2 ayant récemment présenté un syndrome coronarien aigu. Le critère combiné d'efficacité primaire était le temps écoulé avant la première apparition de l'un des événements suivants validés par le comité d'adjudication des événements cardiovasculaires: décès de cause cardiovasculaire, infarctus du myocarde non fatal, AVC non fatal ou hospitalisation pour angor instable. Parmi les critères secondaires d'évaluation CV figurait l'un des événements du critère d'évaluation principal, ou une hospitalisation pour insuffisance cardiaque ou pour revascularisation coronarienne. La durée médiane du suivi de l'étude était de 25,8 et 25,7 mois dans le groupe sous lixisénatide et le groupe sous placebo, respectivement.
L'incidence du critère d'évaluation primaire dans le groupe sous lixisénatide et le groupe sous placebo était similaire: le hazard ratio (HR) pour le lixisénatide contre placebo était de 1,017, avec un intervalle de confiance (IC) à 95% bilatéral associé de 0,886 à 1,168. Des pourcentages similaires entre les traitements ont aussi été observés pour les critères d'évaluation secondaires, et pour chacune des composantes individuelles des critères d'évaluation combinés. Les pourcentages de patients hospitalisés pour insuffisance cardiaque étaient de 4,0% et 4,2% dans le groupe sous lixisénatide et le groupe sous placebo, respectivement (HR [IC à 95%] = 0,96 [0,75 – 1,23]).
PharmacocinétiqueLe rapport insuline glargine/lixisénatide n'avait aucune conséquence pertinente sur la pharmacocinétique de l'insuline glargine et du lixisénatide sous la forme Suliqua.
Par rapport au lixisénatide administré seul, la Cmax est inférieure alors que l'AUC (Aire sous la courbe) est généralement comparable quand il est administré sous la forme Suliqua. Les différences pharmacocinétiques du lixisénatide observées, selon qu'il est administré sous la forme Suliqua ou seul, ne sont pas jugées cliniquement significatives.
Absorption
Après injection sous-cutanée d'associations insuline glargine/lixisénatide à des diabétiques de type 1, l'insuline glargine n'a montré aucun pic prononcé. L'exposition à l'insuline glargine allait de 86% à 101% par rapport à l'administration d'insuline glargine seule.
Après injection sous-cutanée d'associations insuline glargine/lixisénatide à des diabétiques de type 1, le tmax médian du lixisénatide était compris entre 2,5 et 3,0 heures. Une petite réduction de la Cmax du lixisénatide de 22 à 34% a été observée par rapport à l'administration simultanée séparée d'insuline glargine et du lixisénatide, ce qui n'est probablement pas cliniquement significatif. Il n'existe aucune différence cliniquement significative de la vitesse d'absorption lorsque le lixisénatide est administré par voie sous-cutanée dans l'abdomen, la cuisse ou le deltoïde.
Distribution
Le lixisénatide se lie peu (55%) aux protéines humaines.
Métabolisme
Une étude sur le métabolisme chez l'homme recevant de l'insuline glargine en monothérapie indique que l'insuline glargine est partiellement métabolisée au niveau de l'extrémité carboxyle de la chaîne B dans le dépôt sous-cutané pour former deux métabolites actifs ayant une activité in vitro similaire à celle de l'insuline humaine, M1 (21A-Gly-insuline) et M2 (21A-Gly-des-30B-Thr-insuline). Le médicament intact et ces produits de dégradation sont aussi présents dans la circulation.
Élimination
En tant que peptide, le lixisénatide est éliminé par filtration glomérulaire, réabsorption tubulaire et dégradation métabolique ce qui produit des peptides plus petits ainsi que des acides aminés qui sont réintroduits dans le métabolisme des protéines.
Cinétique pour certains groupes de patients
Troubles de la fonction rénale
Une étude ouverte à dose unique a évalué la pharmacocinétique du lixisénatide 5 µg chez des sujets ayant différents degrés d'insuffisance rénale (classement selon la formule de Cockcroft & Gault estimant la clairance de la créatinine (CLcr)) par rapport à des sujets sains.
Aucune différence pertinente de la Cmax moyenne et de l'AUC du lixisénatide n'était observée entre les sujets à fonction rénale normale et les sujets avec insuffisance rénale légère (CLcr 60 à 90 ml/min). Chez les sujets avec insuffisance rénale modérée (CLcr 30 à 60 ml/min), l'AUC a augmenté d'environ 51% et chez les sujets avec insuffisance rénale sévère (CLcr 15-30 ml/min), l'AUC a augmenté d'environ 87%.
Troubles de la fonction hépatique
Le lixisénatide étant éliminé principalement par les reins, aucune étude pharmacocinétique n'a été effectuée chez les patients avec insuffisance hépatique aiguë ou chronique. Un dysfonctionnement hépatique ne doit normalement pas influer sur la pharmacocinétique du lixisénatide.
Age, race, sexe et poids corporel
Insuline glargine
L'influence de l'âge, de la race et du sexe sur la pharmacocinétique de l'insuline glargine n'a pas été évaluée. Dans les essais cliniques comparatifs conduits chez l'adulte avec l'insuline glargine (100 unités/ml), les analyses de sous-groupes basées sur l'âge, la race et le sexe n'ont pas montré de différences en matière de sécurité et d'efficacité.
Lixisénatide
D'après l'analyse pharmacocinétique de la population, l'âge, le poids corporel, le sexe et la race n'ont pas montré d'effet cliniquement significatif sur la pharmacocinétique du lixisénatide.
Enfants et adolescents
Aucune étude sur Suliqua n'a été conduite chez l'enfant et l'adolescent de moins de 18 ans.
Données précliniquesAucune étude sur l'association insuline glargine et lixisénatide n'a été conduite chez l'animal pour évaluer la toxicité des doses répétées, la carcinogénicité, la génotoxicité ou la toxicité sur la reproduction.
Insuline glargine
Les données non cliniques sur l'insuline glargine issues des études conventionnelles de sécurité pharmacologique, de toxicité des doses répétées, de génotoxicité, de carcinogénicité, et de toxicité sur la reproduction n'ont pas révélé de risque particulier pour l'homme.
Lixisénatide
Les données non cliniques issues des études conventionnelles de pharmacologie de sécurité et de génotoxicité n'ont pas révélé de risque particulier pour l'homme.
Dans des études de carcinogénicité en administration sous-cutanée sur 2 ans, des carcinomes à cellules C de la thyroïde ont été observés chez le rat mais pas chez la souris. La dose sans effet toxique observable (NOAEL) pour les carcinomes à cellules C a été de 40 µg/kg deux fois par jour (BID) chez le rat, correspondant à une exposition systémique (AUC) 913 fois supérieure à l'exposition chez l'homme à la dose thérapeutique de 20 µg (QD). Des effets de prolifération sur les cellules C de la thyroïde (hyperplasies et adénomes) ont été observés chez le rat et la souris à des multiples d'exposition très élevés (respectivement ≥913 fois et ≥272 fois) comparativement à l'exposition humaine aux doses thérapeutiques. On estime que ces résultats sont dus à un mécanisme non génotoxique médié par le récepteur du GLP-1 auquel les rongeurs sont particulièrement sensibles. L'étude de carcinogénicité sur 2 ans a révélé en outre chez la souris une augmentation de l'incidence d'adénocarcinomes de l'endomètre à une dose correspondant à une exposition 97 fois supérieure à l'exposition clinique à la dose thérapeutique.
Les études sur l'animal n'ont pas montré d'effet délétère direct sur la fertilité mâle et femelle chez le rat. Des lésions testiculaires et épididymaires réversibles ont été observées chez le chien suite à un traitement par le lixisénatide. La dose sans effet toxique observable (NOAEL) a été de 2 µg/kg BID, correspondant à une exposition seulement 17 fois supérieure à l'exposition chez l'homme à la dose thérapeutique. Des effets similaires ont été observés à toutes les doses testées (NOAEL <5 µg/kg BID) dans une étude de toxicité sur des chiens juvéniles.
Au cours des études sur le développement embryofoetal, des malformations, des retards de croissance, des retards d'ossification et des effets sur le squelette ont été observés chez le rat et le lapin à toutes les posologies à partir de 2.5 µg/kg BID, correspondant chez le rat à une exposition systémique égale à 0.5 fois l'exposition chez l'homme à la dose thérapeutique et 3.8 fois chez le lapin. Dans les deux espèces, une légère toxicité maternelle s'est manifestée par une consommation alimentaire faible et une réduction du poids corporel. La croissance néo-natale a été réduite chez les rats exposés au lixisénatide en fin de gestation et pendant la lactation, et une légère augmentation de la mortalité des petits a été observée.
Remarques particulièresIncompatibilités
Ce médicament ne doit pas être mélangé avec d'autres médicaments.
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur l'emballage.
Après première utilisation du stylo
À utiliser dans les 28 jours après la première utilisation du stylo.
Remarques particulières concernant le stockage
Stylo pré-rempli SoloStar avant première utilisation
Conserver au réfrigérateur (2 °C-8 °C).
Ne pas congeler ou placer près du compartiment de congélation ou d'une poche de congélation. Conserver le stylo pré-rempli dans son emballage extérieur pour le protéger de la lumière. Tenir hors de portée des enfants.
Stylo pré-rempli SoloStar en cours d'utilisation
Ne pas conserver au-dessus de 25 °C, à utiliser dans les 28 jours maximum. Ne pas conserver au réfrigérateur. Ne pas congeler.
Ne pas conserver le stylo pré-rempli avec l'aiguille fixée dessus.
Conserver le stylo pré-rempli à l'abri de la chaleur directe ou de la lumière. Remettez le capuchon sur le stylo après chaque injection afin de le protéger de la lumière. Tenir hors de portée des enfants.
Remarques concernant la manipulation
Avant sa première utilisation, le stylo doit impérativement être conservé à température ambiante pendant 1 à 2 heures.
Examiner la cartouche avant de l'utiliser. Celle-ci ne doit être utilisée que si la solution est limpide, incolore, sans particules visibles et si la consistance ressemble à celle de l'eau. Suliqua est une solution, elle ne nécessite donc pas d'être mise en suspension avant d'être injectée.
La solution Suliqua ne doit pas être mélangée avec une autre insuline, ni être diluée. Le mélange ou la dilution peuvent modifier son profil d'action dans le temps et le mélange peut entraîner la précipitation.
Une aiguille neuve doit toujours être insérée avant chaque utilisation. Une aiguille ne doit jamais être réutilisée. Le patient doit jeter l'aiguille après chaque injection.
En cas d'aiguille obstruée, suivre les explications décrites dans les instructions d'utilisation du stylo accompagnant l'information Patient, présentes dans les boîtes de Suliqua.
Un stylo vide ne doit jamais être réutilisé et doit être jeté conformément aux règles d'usage.
Pour éviter toute transmission possible de maladie, chaque stylo doit être utilisé par un seul patient.
L'étiquette du stylo doit toujours être vérifiée avant chaque injection pour éviter toute confusion entre les deux dosages /stylos pré-remplis différents de Suliqua et/ou d'autres antidiabétiques injectables (voir «Mises en garde et précautions»).
Avant d'injecter Suliqua, lire attentivement les instructions d'utilisation du stylo.
Numéro d’autorisation66283 (Swissmedic).
PrésentationStylos pré-remplis SoloStar® de 3 ml de solution injectable.
Suliqua 100/50 (Stylo pré-rempli SoloStar® jaune pour 10 - 40 doses unitaires): boîtes de 3 stylos (B).
Suliqua 100/33 (Stylo pré-rempli SoloStar® vert pour 30 - 60 doses unitaires): boîtes de 3 stylos (B).
Titulaire de l’autorisationsanofi-aventis (suisse) sa, 1214 Vernier/GE.
Mise à jour de l’informationJuillet 2023
|


