CompositionPrincipes actifs
Phenylephrinum (ut Phenylephrini hydrochloridum).
Excipients
Natrii chloridum, acidum citricum monohydricum, natrii citras dihydricus, natrii hydroxidum, aqua ad injectabile.
1 seringue préremplie de 10 ml contient 36,8 mg de sodium.
Indications/Possibilités d’emploi·Traitement de l'hypotension au cours de l'anesthésie générale et de l'anesthésie rachidienne ou péridurale (y compris sectio caesarea);
·Traitement préventif de l'hypotension au cours de l'anesthésie rachidienne (y compris sectio caesaserea).
Posologie/Mode d’emploiPhenylephrin Aguettant est administré par voie intraveineuse (bolus).
La dose doit être adaptée à la réponse pressive sanguine.
La dose habituelle est de 0,05-0,1 mg (1-2 ml) en bolus, renouvelable jusqu'à l'obtention de l'effet recherché.
Les doses peuvent être augmentées en cas d'hypotension sévère, sans dépasser 0,1 mg (2 ml) en bolus.
Phenylephrin Aguettant doit être administré uniquement par des médecins ayant une formation et une expérience adéquate. La seringue préremplie ne convient pas pour une utilisation dans un pousse-seringue.
Instructions posologiques particulières
Patients présentant des troubles de la fonction rénale
Des doses plus faibles de phényléphrine peuvent être nécessaires chez les patients présentant une insuffisance rénale.
Patients présentant des troubles de la fonction hépatique
Des doses plus importantes de phényléphrine peuvent être nécessaires chez les patients présentant une cirrhose hépatique.
Enfants et adolescents:
L'utilisation et la sécurité d'emploi de Phenylephrin chez les enfants et les adolescents n'ont pas été étudiées à ce jour. Pour cette raison, l'utilisation chez les enfants et les adolescents n'est pas recommandée.
Contre-indicationsPhenylephrin Aguettant ne doit pas être utilisé:
·Chez les patients présentant une hypersensibilité au principe actif ou aux excipients selon la composition;
·Chez les patients présentant une hypertension grave, une tachycardie ventriculaire, un glaucome à angle fermé;
·En association avec les IMAO non sélectifs en raison du risque d'hypertension paroxystique et d'hyperthermie pouvant être fatale;
·Chez les patients souffrant d'hyperthyroïdie sévère.
Mises en garde et précautionsLa pression sanguine doit être surveillée pendant le traitement.
Phenylephrin doit être administré avec prudence chez les patients atteints de:
·diabète,
·hypertension artérielle,
·anévrisme,
·hyperthyroïdie incontrôlée
·pathologie myocardique
·maladie coronarienne et maladie cardiaque chronique
·bradycardie
·bloc cardiaque partiel
·tachycardie
·arythmie
·angine de poitrine, (phényléphrine peut précipiter ou aggraver l'angine de poitrine chez les patients souffrant d'une maladie coronarienne et d'une histoire d'angine de poitrine)
·insuffisance vasculaire périphérique non sévère
·artériosclérose grave
Phenylephrin peut induire une diminution du débit cardiaque. Par conséquent, il doit être administré avec une extrême prudence chez les patients souffrant d'athérosclérose, chez les sujets âgés et chez les patients avec dysfonction de la circulation cérébrale ou coronarienne.
Chez les patients atteints d'insuffisance cardiaque aigue ou de choc cardiogénique, Phenylephrin peut aggraver l'insuffisance cardiaque à la suite de la vasoconstriction induite (augmentation de la postcharge).
Les patients ayant des pathologies telles que le débit cardiaque diminué ou une maladie artérielle périphérique devraient avoir une surveillance fréquente des fonctions vitales du corps et la limite inférieure de la pression artérielle systolique devrait être considérée comme un critère de réduction de la dose ou de l'interruption de Phenylephrin.
Une attention particulière devrait être accordée lors de l'administration de l'injection de phényléphrine afin d'éviter l'extravasation, car cela pourrait provoquer la nécrose des tissus.
Des doses inférieures peuvent être nécessaires chez les patients présentant une insuffisance rénale.
Des doses supérieures peuvent être nécessaires chez les patients atteints de cirrhose du foie.
L'administration concomitante de Phenylephrin Aguettant et de médicaments suivants est déconseillée en raison du risque de vasoconstriction et/ou d'une crise hypertensive associée à son effet sympathomimétique indirect:
·alcaloïdes de l'ergot de seigle dopaminergiques (bromocriptine, cabergoline, lisuride, pergolide) ou vasoconstricteurs (dihydroergotamine, ergotamine ou méthysergide, méthylergométrine)
·en association avec le linézolide
A prendre en compte chez les patients suivant un régime hyposodé strict.
En cas d'administration concomitante de Phenylephrin Aguettant et de médicaments ocytociques (oxytocine, extraits neurohypophysaires, alcaloïdes de l'ergot de seigle, etc.), l'effet des sympathomimétiques est renforcé.
Sodium
Ce médicament contient 36,8 mg de sodium par seringue préremplie de 10 ml, ce qui équivaut à 1,8% de l'apport alimentaire quotidien maximal recommandé par l'OMS de 2 g de sodium par adulte.
InteractionsAssociations contre-indiquées
Inhibiteurs de la monoamine oxydase (IMAO), non sélectifs (iproniazide, nialamide)
Hypertension paroxystique, hyperthermie pouvant être fatale. Du fait de la longue durée d'action de l'IMAO, cette interaction est encore possible 15 jours après l'arrêt de l'IMAO.
Associations déconseillées
Alcaloïdes de l'ergot de seigle dopaminergiques (bromocriptine, cabergoline, lisuride, pergolide):
Risque de vasoconstriction et/ou de crise hypertensive.
Alcaloïdes de l'ergot de seigle vasoconstricteurs (dihydroergotamine, ergotamine, methylergometrine, methylsergide):
Risque de vasoconstriction et/ou de crise hypertensive.
Antidépresseurs tricycliques (ex. imipramine)
Hypertension paroxystique avec possibilité d'arythmies (inhibition de l'entrée de l'adrénaline ou de la noradrénaline dans les fibres sympathiques).
Antidépresseurs noradrénergiques et sérotoninergiques (minalcipran, venlafaxine)
Hypertension paroxystique avec possibilité d'arythmies (inhibition de l'entrée de l'adrénaline ou de la noradrénaline dans les fibres sympathiques).
Inhibiteurs sélectifs de la monoamine oxidase A (IMAO) (moclobemide, toloxatone)
Risque de vasoconstriction et/ou de crise hypertensive.
Linezolide
Risque de vasoconstriction et/ou de crise hypertensive.
Guanethidine et produits apparentés
Augmentation substantielle de la tension artérielle (hyperréactivité liée à la réduction du tonus sympathique et/ou à l'inhibition de l'entrée de l'adrénaline ou de la noradrénaline dans les fibres sympathiques).
Si l'association ne peut pas être évitée, utiliser avec prudence des doses plus faibles d'agents sympathomimétiques.
Glycosides cardiaques, quinidine
Risque accru d'arythmies.
Sibutramine
Hypertension paroxystique avec possibilité d'arythmies (inhibition de l'entrée de l'adrénaline ou de la noradrénaline dans les fibres sympathiques).
Anesthésiques volatils halogénés (desflurane, enflurane, halothane, isoflurane, methoxyflurane, sevoflurane)
Risque de poussée hypertensive peropératoire et d'arythmie.
Associations faisant l'objet de précautions d'emploi
Agents ocytociques
L'effet des amines sympathomimétiques presso-actives est potentialisé. Ainsi, certains agents ocytociques peuvent provoquer une hypertension persistante sévère et des accidents vasculaires cérébraux peuvent survenir pendant la période post-partum.
Grossesse, allaitementGrossesse
Aucune étude expérimentale réalisée sur l'animal n'est disponible concernant l'effet sur la grossesse, le développement embryonnaire, le développement du fœtus et/ou le développement post-natal. Le risque potentiel pour l'être humain n'est pas connu.
Ce médicament ne doit pas être utilisé pendant la grossesse, sauf dans le cas où le traitement est absolument nécessaire.
Allaitement
On ne sait pas si Phenylephrin passe dans le lait maternel. Phenylephrin Aguettant ne doit donc pas être utilisé pendant l'allaitement.
Effet sur l’aptitude à la conduite et l’utilisation de machinesAucune étude pertinente n'a été réalisée. Au cours de l'utilisation de la phényléphrine, des effets indésirables, tels que nausée et céphalées, ont été rapportés occasionnellement. Si un patient est concerné par ces effets, il ne doit conduire aucun véhicule ni utiliser de machines.
Effets indésirables«Très fréquents» (≥1/10), «fréquents» (<1/10, ≥1/100), «occasionnels» (<1/100, ≥1/1000), «rares» (<1/1000, ≥1/10'000), «très rares» (<1/10'000).
La plupart des effets indésirables de phényléphrine sont dose-dépendants et en conséquence du profil pharmacodynamique attendu.
Les effets indésirables les plus fréquents sont la bradycardie, des épisodes d'hypertension, des nausées et vomissements. L'hypertension est plus fréquente avec des doses élevées.
L'effet indésirable cardiovasculaire le plus fréquemment rapporté est la bradycardie, probablement due à une stimulation vagale médiée par un barorécepteur, en cohérence avec l'effet pharmacologique de la phényléphrine.
Les effets secondaires suivants peuvent survenir:
Affections du système immunitaire
Hypersensibilité.
Troubles du métabolisme et de la nutrition
Métabolisme du glucose anormal.
Affections psychiatriques
Euphorie, agitation, anxiété, états psychotiques, confusion mentale.
Affections du système nerveux
Occasionnels: Céphalées, picotements, lourdeurs dans la tête, nervosité, insomnie, paresthésie, tremblement.
Affections oculaires
Mydriase, aggravation d'un glaucome à angle fermé préexistant.
Affections cardiaques
Occasionnels: Bradycardie réflexe, arythmies, tachycardie, arrêt cardiaque, douleur angineuse, palpitations, ischémie myocardique.
Affections vasculaires
Hémorragie cérébrale, hypertension, hypotension avec une sensation vertigineuse, évanouissements, bouffée congestive, froideur de la peau, pâleur.
Affections respiratoires, thoraciques et médiastinales
Dyspnée, œdème pulmonaire.
Affections gastro-intestinales
Occasionnels: Nausées, hypersalivation, vomissements.
Affections de la peau et du tissu sous-cutané
Diaphorèse, horripilation, sécrétion de sueur, pâlissement de la peau.
Affections du rein et des voies urinaires
Difficulté à la miction, rétention urinaire.
Troubles généraux et anomalies au site d'administration
Extravasation nécrose au site d'injection.
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
SurdosageSignes et symptômes
En cas de surdosage, principalement par administration IV directe, des extrasystoles ventriculaires et même de petites crises de tachycardie ventriculaire peuvent être observées.
Traitement
En cas d'augmentation excessive de la pression sanguine, celle-ci peut être immédiatement réduite par un inhibiteur alpha-adrénergique, par exemple phentolamine.
Propriétés/EffetsCode ATC
C01CA06
Mécanisme d'action
La vasoconstriction provoquée par la phényléphrine dure 20 minutes après injection intraveineuse et jusqu'à 50 minutes après injection sous-cutanée. La phényléphrine ralentit la fréquence cardiaque et accroît le volume systolique sans influencer la fréquence cardiaque.
La phényléphrine est un agoniste des récepteurs alpha-adrénergiques post-synaptiques ayant un effet limité sur les récepteurs bêta du cœur. À des doses thérapeutiques, il n'entraîne pas de stimulation de la moelle épinière ni du cerveau, ou bien une stimulation modérée. Des injections répétées peuvent permettre l'obtention d'effets comparables.
Pharmacodynamique
La phényléphrine agit principalement sur le système cardio-vasculaire. L'administration parentérale produit chez l'homme et dans d'autres espèces une augmentation de la pression sanguine systolique et diastolique. La réponse pressive à la phényléphrine s'accompagne d'une bradycardie réflexe marquée qui peut être inhibée par l'atropine; après administration d'atropine, des doses élevées du médicament n'augmentent que de manière limitée la fréquence cardiaque.
Chez l'homme, le volume-minute du cœur est légèrement réduit et les résistances périphériques sont considérablement augmentées. Le temps de circulation est légèrement prolongé et la pression veineuse légèrement accrue; il n'y a pas de constriction veineuse marquée. La plupart des lits vasculaires sont rétrécis; l'irrigation rénale, splanchnique, cutanée et des extrémités est réduite; la circulation coronarienne est augmentée. Les vaisseaux pulmonaires sont rétrécis et la pression artérielle pulmonaire augmente.
Efficacité clinique
Aucune donnée disponible.
PharmacocinétiqueAbsorption
En cas d'absorption orale, la biodisponibilité est de 38%.
Distribution
La demi-vie de distribution est de 5 minutes et le volume de distribution est supérieur à 40 litres. Après administration i.v., le volume de distribution du compartiment central est comparable au volume extracellulaire (env. 40 litres), alors que le volume de distribution à l'état d'équilibre est de 340 litres.
Métabolisme
La phényléphrine est métabolisée en acide m-hydroxymandélique et en conjugués phénoliques. La dégradation en conjugués phénoliques est accrue en cas d'administration orale et réduite en cas d'administration intraveineuse. La métabolisation a lieu au niveau du foie et de la paroi intestinale.
Élimination
En cas d'administration i.v., la demi-vie d'élimination est de 2 à 3 heures, l'excrétion rénale est de 80 à 86%, et 16% de la substance active sont excrétés dans l'urine sous forme inchangée. La demi-vie d'élimination est de 2 à 3 heures.
Cinétique pour certains groupes de patients
Aucune donnée disponible
Données précliniquesAucune étude expérimentale réalisée sur l'animal n'est disponible concernant la toxicité de la phényléphrine pour la reproduction et le développement.
Les données expérimentales obtenues avec des rats et des souris n'indiquent aucun potentiel carcinogène ni génotoxique.
Remarques particulièresIncompatibilités
Les seringues préremplies sont prêtes à l'emploi et ne doivent pas être mélangées à d'autres médicaments.
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur l'emballage.
Stabilité après ouverture
La préparation ne contient pas de conservateur. Pour des raisons microbiologiques, la préparation prête à l'emploi doit être utilisée immédiatement après ouverture du blister.
Les quantités éventuellement restantes dans la seringue préremplie sont à jeter.
Remarques particulières concernant le stockage
Conserver à température ambiante (15–25 °C) et hors de la portée des enfants.
Conserver le blister dans l'emballage original, à l'abri de la lumière.
Remarques concernant la manipulation
La seringue préremplie est à usage unique, pour un patient donné.
Le contenu d'un blister non ouvert et non endommagé est stérile et il ne doit pas être ouvert avant utilisation.
La surface externe de la seringue est stérile jusqu'à l'ouverture du blister. Vérifier l'intégrité du blister avant utilisation.
1) Sortir la seringue préremplie du blister stérile.
2) Pousser le piston pour décoller le joint.
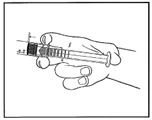
3) Tourner le capuchon protecteur pour rompre l'emballage de scellage.
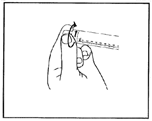
4) Vérifier que l'embout de scellage de la seringue a été complètement ôté.
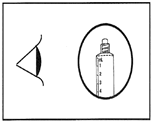
5) Purger l'air en poussant légèrement sur le piston.
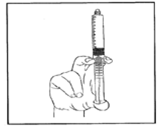
6) Connecter la seringue à la voie d'accès i.v.. Pousser lentement sur le piston pour injecter le volume souhaité.
Numéro d’autorisation66317 (Swissmedic).
PrésentationPhenylephrin Aguettant 0,05 mg/ml, seringue préremplie de 10 ml: 1 (B)
Phenylephrin Aguettant 0,05 mg/ml, seringue préremplie de 10 ml: 10 (B)
Titulaire de l’autorisationAguettant Suisse SA, Thônex
Mise à jour de l’informationAvril 2023
| 



